文档内容
第 20 讲 硫酸 硫酸盐
[复习目标] 1.掌握浓硫酸的三大特性及应用。2.熟知常见的硫酸盐,掌握SO的检验方法。
3.能依据信息,控制条件制取硫的复杂含氧酸盐并探究其性质。
考点一 硫酸及其工业制法
1.硫酸的物理性质
HSO 是无色液体,能与水以任意比互溶,稀释时放出大量的热,浓 HSO 稀释的方法是将
2 4 2 4
浓 H SO 沿烧杯内壁缓缓倒入水中并用玻璃棒不断搅拌。
2 4
2.浓硫酸的三大特性
3.硫酸的工业制法
(1)制备流程
完成相关反应的化学方程式:
①________________________________________________________________________,
________________________________________________________________________;
②________________________________________________________________________。
答案 ①4FeS+11O=====2Fe O+8SO S+O=====SO ②2SO +O2SO
2 2 2 3 2 2 2 2 2 3
(2)常考问题①SO 进入催化反应室前净化、干燥的目的是 混合气中除含有二氧化硫外,还含有多种杂质 。
2
这些杂质有的使催化剂中毒、失效,有的对反应设备有腐蚀作用,所以必须净化处理。
②工业生产SO 采用常压的原因: 常压下 SO 的转化率已经很大,高压下 SO 转化率提高不
2 2 2
多,但成本大大增加。
③用98.3%的浓硫酸吸收SO 而不用水的原因: 用水吸收 SO 会产生大量酸雾。
3 3
1.浓硫酸具有强氧化性,所以浓硫酸不可用于干燥H 和CO( )
2
2.少量胆矾加入浓硫酸中,蓝色晶体变白,体现浓硫酸的吸水性( )
3.用玻璃棒蘸取浓硫酸滴在滤纸上,滤纸变黑,体现浓硫酸的脱水性( )
4.将铜片加入盛有浓硫酸的试管中,加热铜片逐渐溶解,产生无色、有刺激性气味的气体,
体现浓硫酸的强氧化性、酸性( )
5.将少量铜加入浓硫酸中加热,很快能观察到溶液变为蓝色( )
6.一定量浓硫酸中加入足量锌粒加热,产生的气体为SO 和H 的混合气体( )
2 2
7.将铜片放入浓硫酸中,无明显现象是因为铜片发生了钝化( )
8.工业上可用稀硫酸洗去锅炉中的水垢( )
答案 1.× 2.√ 3.√ 4.√ 5.× 6.√ 7.× 8.×
一、浓HSO 的特性及应用
2 4
1.下列有关硫酸的实验或用途中利用了硫酸的哪些性质?
(1)用浓硫酸作干燥剂干燥CO、SO 、Cl 等气体:________________。
2 2
(2) 分 别 用 浓 硫 酸 与 NaCl(s) 、 NaNO (s) 反 应 制 取 HCl 、 HNO :
3 3
__________________________。
(3)用铝或铁制容器贮存或运输浓硫酸:____________________________________________。
(4)工业上用硫酸与磷酸钙反应制取磷酸:___________________________________________
________________________。
(5) 实 验 室 用 铜 与 浓 硫 酸 反 应 制 取 SO :
2
_______________________________________________
________________________。
(6) 实 验 室 用 甲 酸 与 浓 硫 酸 作 用 制 取 CO : HCOOH― ― ―CO→+ HO :
2
_____________________。
(7)浓硫酸与蔗糖制取“黑面包”的实验:___________________________________________
________________________。
答案 (1)浓硫酸的吸水性 (2)浓硫酸具有高沸点、难挥发性 (3)浓硫酸的强氧化性 (4)硫
酸的强酸性 (5)浓硫酸的酸性、强氧化性 (6)浓硫酸的脱水性 (7)浓硫酸的脱水性、强氧化性
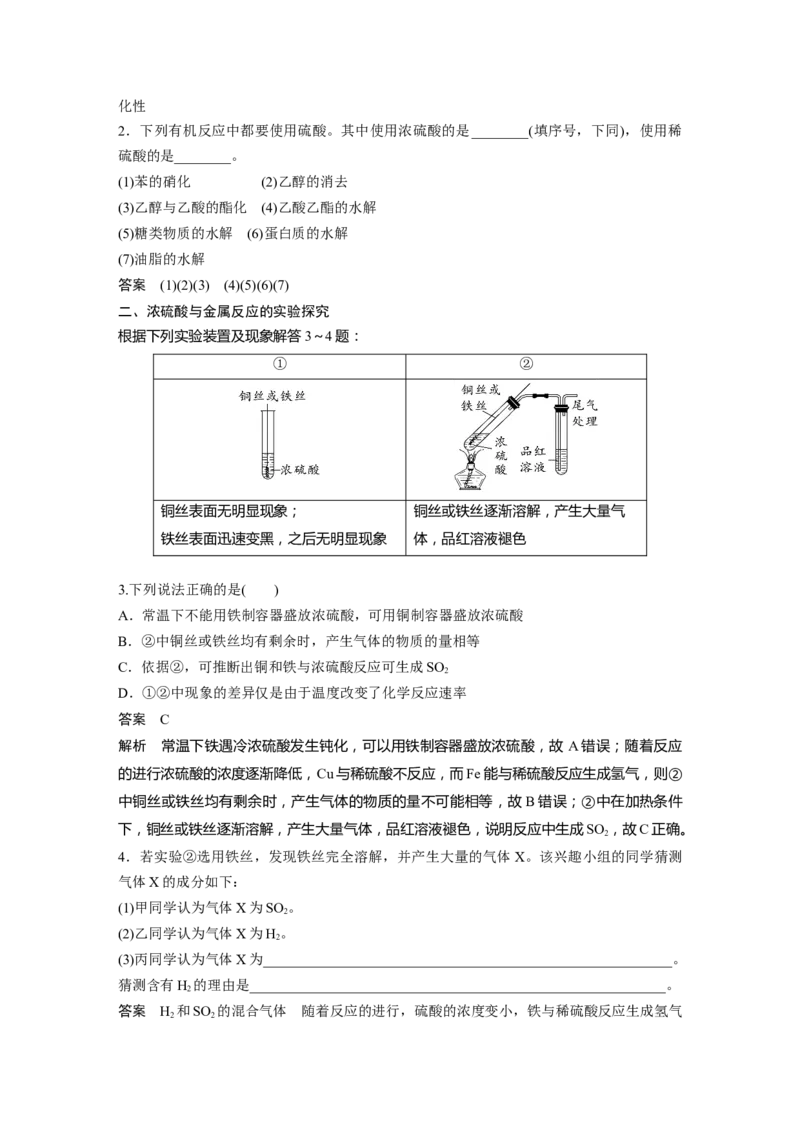
2.下列有机反应中都要使用硫酸。其中使用浓硫酸的是________(填序号,下同),使用稀
硫酸的是________。
(1)苯的硝化 (2)乙醇的消去
(3)乙醇与乙酸的酯化 (4)乙酸乙酯的水解
(5)糖类物质的水解 (6)蛋白质的水解
(7)油脂的水解
答案 (1)(2)(3) (4)(5)(6)(7)
二、浓硫酸与金属反应的实验探究
根据下列实验装置及现象解答3~4题:
① ②
铜丝表面无明显现象; 铜丝或铁丝逐渐溶解,产生大量气
铁丝表面迅速变黑,之后无明显现象 体,品红溶液褪色
3.下列说法正确的是( )
A.常温下不能用铁制容器盛放浓硫酸,可用铜制容器盛放浓硫酸
B.②中铜丝或铁丝均有剩余时,产生气体的物质的量相等
C.依据②,可推断出铜和铁与浓硫酸反应可生成SO
2
D.①②中现象的差异仅是由于温度改变了化学反应速率
答案 C
解析 常温下铁遇冷浓硫酸发生钝化,可以用铁制容器盛放浓硫酸,故 A错误;随着反应
的进行浓硫酸的浓度逐渐降低,Cu与稀硫酸不反应,而Fe能与稀硫酸反应生成氢气,则②
中铜丝或铁丝均有剩余时,产生气体的物质的量不可能相等,故B错误;②中在加热条件
下,铜丝或铁丝逐渐溶解,产生大量气体,品红溶液褪色,说明反应中生成SO ,故C正确。
2
4.若实验②选用铁丝,发现铁丝完全溶解,并产生大量的气体X。该兴趣小组的同学猜测
气体X的成分如下:
(1)甲同学认为气体X为SO 。
2
(2)乙同学认为气体X为H。
2
(3)丙同学认为气体X为__________________________________________________________。
猜测含有H 的理由是___________________________________________________________。
2
答案 H 和SO 的混合气体 随着反应的进行,硫酸的浓度变小,铁与稀硫酸反应生成氢气
2 2浓HSO 与金属反应时“量变”引起的“质变”规律
2 4
(1)较活泼金属(如Zn)反应开始产生SO ,硫酸浓度变小后产生H。
2 2
(2)不活泼金属(如Cu)反应开始产生SO (加热),硫酸浓度变小后,稀HSO 不再与不活泼金
2 2 4
属反应。
考点二 SO 的检验 硫的复杂含氧酸盐
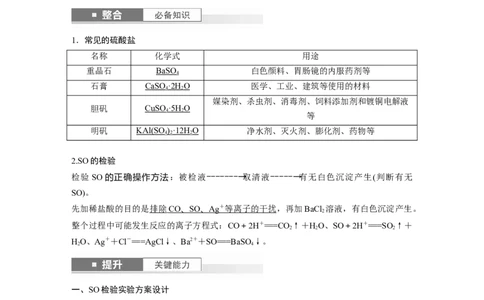
1.常见的硫酸盐
名称 化学式 用途
重晶石 BaSO 白色颜料、胃肠镜的内服药剂等
4
石膏 CaSO·2H O 医学、工业、建筑等使用的材料
4 2
媒染剂、杀虫剂、消毒剂、饲料添加剂和镀铜电解液
胆矾 CuSO ·5H O
4 2
等
明矾 KAl(SO )·12H O 净水剂、灭火剂、膨化剂、药物等
4 2 2
2.SO的检验
检验 SO的正确操作方法:被检液―――――――→取清液―――――→有无白色沉淀产生(判断有无
SO)。
先加稀盐酸的目的是 排除 CO 、 SO 、 Ag + 等离子的干扰 ,再加BaCl 溶液,有白色沉淀产生。
2
整个过程中可能发生反应的离子方程式:CO+2H+===CO↑+HO、SO+2H+===SO ↑+
2 2 2
HO、Ag++Cl-===AgCl↓、Ba2++SO===BaSO↓。
2 4
一、SO检验实验方案设计
1.下列过程中,最终的白色沉淀物不一定是BaSO 的是( )
4
A.Fe(NO ) 溶液―――――――――――――→白色沉淀
3 2
B.Ba(NO ) 溶液―――――――――――→白色沉淀
3 2
C.无色溶液――――――――→白色沉淀
D.无色溶液――――→无色溶液――――→白色沉淀
答案 C
解析 A项,二氧化硫被硝酸氧化为硫酸,加氯化钡一定生成硫酸钡沉淀;B项,亚硫酸根
离子被硝酸氧化为硫酸根离子,沉淀也是硫酸钡;C项,所得沉淀可能是氯化银;D项,先加过量盐酸无明显现象,再加氯化钡产生的白色沉淀一定是硫酸钡。
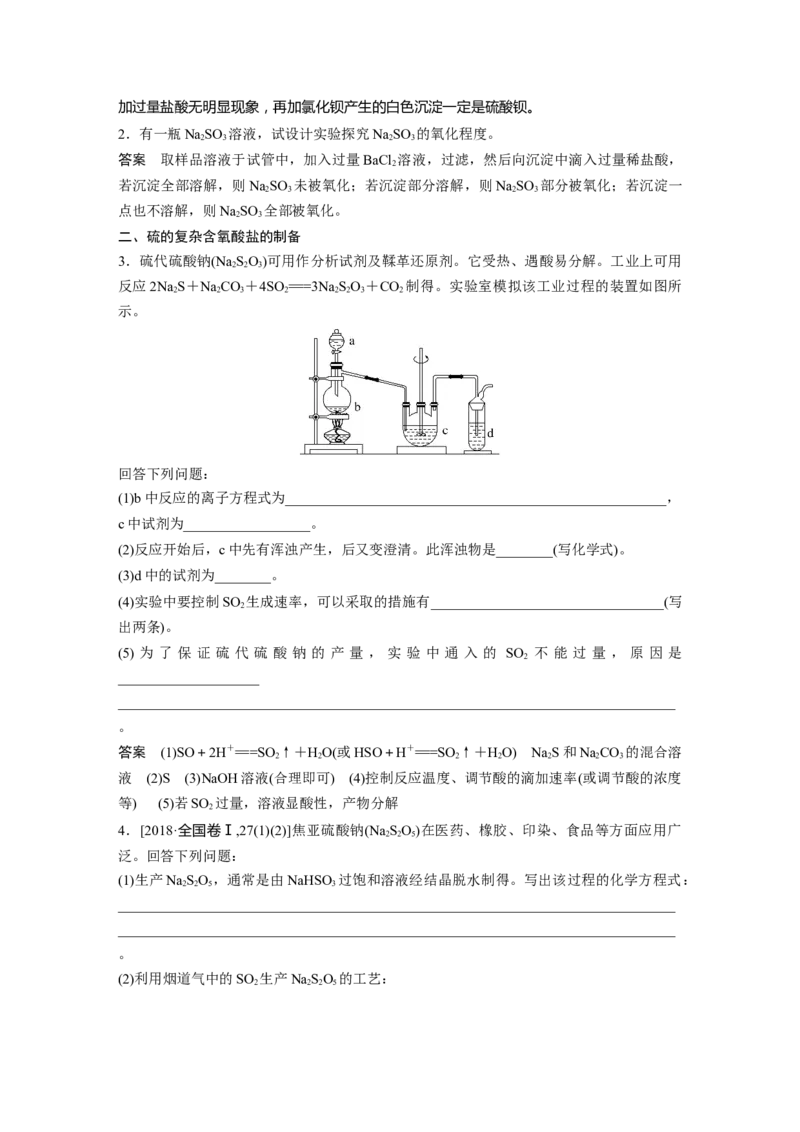
2.有一瓶NaSO 溶液,试设计实验探究NaSO 的氧化程度。
2 3 2 3
答案 取样品溶液于试管中,加入过量BaCl 溶液,过滤,然后向沉淀中滴入过量稀盐酸,
2
若沉淀全部溶解,则NaSO 未被氧化;若沉淀部分溶解,则NaSO 部分被氧化;若沉淀一
2 3 2 3
点也不溶解,则NaSO 全部被氧化。
2 3
二、硫的复杂含氧酸盐的制备
3.硫代硫酸钠(Na SO)可用作分析试剂及鞣革还原剂。它受热、遇酸易分解。工业上可用
2 2 3
反应2NaS+NaCO +4SO ===3NaSO +CO 制得。实验室模拟该工业过程的装置如图所
2 2 3 2 2 2 3 2
示。
回答下列问题:
(1)b中反应的离子方程式为______________________________________________________,
c中试剂为__________________。
(2)反应开始后,c中先有浑浊产生,后又变澄清。此浑浊物是________(写化学式)。
(3)d中的试剂为________。
(4)实验中要控制SO 生成速率,可以采取的措施有_________________________________(写
2
出两条)。
(5) 为 了 保 证 硫 代 硫 酸 钠 的 产 量 , 实 验 中 通 入 的 SO 不 能 过 量 , 原 因 是
2
____________________
_______________________________________________________________________________
。
答案 (1)SO+2H+===SO ↑+HO(或HSO+H+===SO ↑+HO) NaS和NaCO 的混合溶
2 2 2 2 2 2 3
液 (2)S (3)NaOH溶液(合理即可) (4)控制反应温度、调节酸的滴加速率(或调节酸的浓度
等) (5)若SO 过量,溶液显酸性,产物分解
2
4.[2018·全国卷Ⅰ,27(1)(2)]焦亚硫酸钠(Na SO)在医药、橡胶、印染、食品等方面应用广
2 2 5
泛。回答下列问题:
(1)生产NaSO ,通常是由NaHSO 过饱和溶液经结晶脱水制得。写出该过程的化学方程式:
2 2 5 3
_______________________________________________________________________________
_______________________________________________________________________________
。
(2)利用烟道气中的SO 生产NaSO 的工艺:
2 2 2 5①pH=4.1时,Ⅰ中为____________(写化学式)溶液。
②工艺中加入NaCO 固体,并再次充入SO 的目的是________________________________。
2 3 2
答案 (1)2NaHSO===NaSO+HO
3 2 2 5 2
(2)①NaHSO ②得到NaHSO 过饱和溶液
3 3
解析 (2)①酸性条件下,SO 与NaCO 溶液反应生成NaHSO。
2 2 3 3
5.连二亚硫酸钠(Na SO)俗称保险粉,可以用作染色工艺的还原剂,纸浆、肥皂等的漂白
2 2 4
剂。NaSO 易溶于水,不溶于乙醇,在碱性介质中较稳定,在空气中易被氧化。回答下列
2 2 4
问题:
(1)Na SO 在潮湿空气中被氧化,生成的两种常见酸式盐是________(填化学式)。
2 2 4
(2)锌粉法制备NaSO 的工艺流程如图所示:
2 2 4
①工业上常将锌块进行预处理得到锌粉-水悬浊液,其目的是___________________________。
②步骤Ⅰ中发生反应的化学方程式为________________________________________________
_______________________________________________________________________________
。
③在步骤Ⅲ中得到的NaSO 固体要用乙醇洗涤,其优点是____________________________,
2 2 4
“后续处理”最终要加入少量的NaCO 固体,其原因是_____________________________。
2 3
(3)目前,我国普遍采用甲酸钠法生产连二亚硫酸钠,其原理是先将 HCOONa和烧碱加入乙
醇水溶液中,然后通入SO 发生反应,有CO 气体放出,总反应的离子方程式是_________。
2 2
答案 (1)NaHSO 、NaHSO (2)① 增大锌的表面积,加快化学反应速率 ② Zn+
3 4
2SO ===ZnS O ③减少NaSO 的溶解损失,易于干燥 NaCO 为碱性物质,保险粉在碱
2 2 4 2 2 4 2 3
性介质中较稳定 (3)HCOO-+OH-+2SO ===SO+CO+HO
2 2 2 2
解析 (1)Na SO 中S显+3价,在潮湿空气中被氧化,S部分转化为+4价,部分转化为+
2 2 4
6价,则生成的两种常见酸式盐为NaHSO 和NaHSO 。(2)③NaSO 固体易溶于水,不溶于
3 4 2 2 4
乙醇,用乙醇洗涤,既可减少溶解损失,又易于干燥;NaSO 在碱性介质中较稳定,
2 2 4
NaCO 固体可提供碱性环境,增强保险粉的稳定性。
2 3
几种硫的复杂含氧酸盐
(1)硫代硫酸钠(Na SO) 俗名大苏打,它是无色透明的晶体,易溶于水,溶于水后溶液呈碱
2 2 3性。它受热、遇酸易分解,其与酸反应的离子方程式:SO+2H+===S↓+SO ↑+HO。它
2 2 2
具有较强的还原性,可用作分析试剂及鞣革还原剂。
(2)连二亚硫酸钠(Na SO)能溶于冷水,在热水中分解,不溶于乙醇。其水溶液有很强的还
2 2 4
原性,在碱性介质中较稳定,在空气中易被氧化。
(3)焦亚硫酸钠(Na SO) 具有还原性,温度高于150 ℃易分解,在食品加工中常作防腐剂、
2 2 5
漂白剂、疏松剂。
(4)过二硫酸钠(Na SO)中S元素的化合价是+6价,其阴离子SO结构中含有1个过氧键(—
2 2 8 2
O—O—),性质与过氧化氢相似,具有氧化性,是一种强氧化剂。
1.正误判断,正确的打“√”,错误的打“×”。
(1)工业上煅烧黄铁矿(FeS )生产SO (2023·浙江1月选考,5B)( )
2 2
(2)浓HSO 具有强吸水性,能吸收糖类化合物中的水分并使其炭化(2023·河北,10A)( )
2 4
(3)稀硫酸具有酸性,可用于除去铁锈(2019·江苏,3B)( )
(4)向盛有饱和硫代硫酸钠溶液的试管中滴加稀盐酸,有刺激性气味气体产生,溶液变浑浊
(2019·全国卷Ⅱ,10C)( )
(5)用烧碱溶液吸收蔗糖与浓硫酸反应产生的刺激性气体:SO +2OH-===SO+HO(2022·福
3 2
建,8C)( )
答案 (1)√ (2)× (3)√ (4)√ (5)×
2.(2019·上海等级考试,12)证明亚硫酸钠部分变质所需要的试剂是( )
A.硝酸钡,稀硫酸 B.稀盐酸,氯化钡
C.稀硫酸,氯化钡 D.稀硝酸,氯化钡
答案 B
3.(2022·广东,5)若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的
探究实验,下列分析正确的是( )
A.Cu与浓硫酸反应,只体现HSO 的酸性
2 4
B.a处变红,说明SO 是酸性氧化物
2
C.b或c处褪色,均说明SO 具有漂白性
2
D.试管底部出现白色固体,说明反应中无HO生成
2答案 B
解析 铜和浓硫酸反应生成CuSO ,体现浓硫酸的酸性,生成SO ,体现浓硫酸的强氧化性,
4 2
故A错误;a处的紫色石蕊变红,其原因是SO 溶于水生成了酸,可说明SO 是酸性氧化物,
2 2
故B正确;b处品红褪色,其原因是SO 具有漂白性,而c处酸性高锰酸钾褪色,其原因是
2
SO 和酸性KMnO 发生氧化还原反应,SO 体现还原性,故C错误;实验过程中试管底部出
2 4 2
现白色固体,其原因是浓硫酸具有吸水性,将反应生成的HO吸收,故D错误。
2
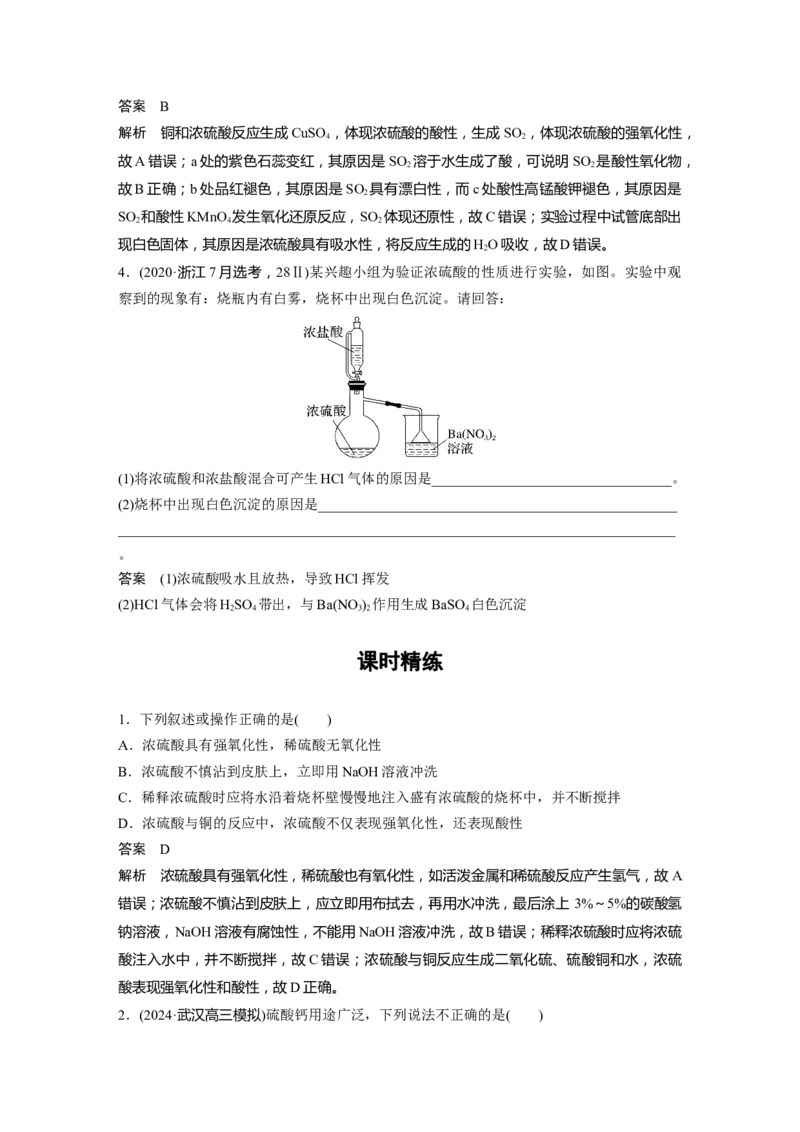
4.(2020·浙江7月选考,28Ⅱ)某兴趣小组为验证浓硫酸的性质进行实验,如图。实验中观
察到的现象有:烧瓶内有白雾,烧杯中出现白色沉淀。请回答:
(1)将浓硫酸和浓盐酸混合可产生HCl气体的原因是__________________________________。
(2)烧杯中出现白色沉淀的原因是___________________________________________________
_______________________________________________________________________________
。
答案 (1)浓硫酸吸水且放热,导致HCl挥发
(2)HCl气体会将HSO 带出,与Ba(NO ) 作用生成BaSO 白色沉淀
2 4 3 2 4
课时精练
1.下列叙述或操作正确的是( )
A.浓硫酸具有强氧化性,稀硫酸无氧化性
B.浓硫酸不慎沾到皮肤上,立即用NaOH溶液冲洗
C.稀释浓硫酸时应将水沿着烧杯壁慢慢地注入盛有浓硫酸的烧杯中,并不断搅拌
D.浓硫酸与铜的反应中,浓硫酸不仅表现强氧化性,还表现酸性
答案 D
解析 浓硫酸具有强氧化性,稀硫酸也有氧化性,如活泼金属和稀硫酸反应产生氢气,故A
错误;浓硫酸不慎沾到皮肤上,应立即用布拭去,再用水冲洗,最后涂上 3%~5%的碳酸氢
钠溶液,NaOH溶液有腐蚀性,不能用NaOH溶液冲洗,故B错误;稀释浓硫酸时应将浓硫
酸注入水中,并不断搅拌,故C错误;浓硫酸与铜反应生成二氧化硫、硫酸铜和水,浓硫
酸表现强氧化性和酸性,故D正确。
2.(2024·武汉高三模拟)硫酸钙用途广泛,下列说法不正确的是( )A.CaSO·2H O俗名:熟石膏
4 2
B.CaSO 属于强电解质
4
C.CaSO 中既含离子键又含共价键
4
D.石膏可用来调节水泥硬化速度
答案 A
解析 CaSO·2H O俗名:生石膏,A错误;CaSO 是盐,在水溶液中完全电离,属于强电
4 2 4
解质,B正确;水泥具有水硬性,石膏可用来调节水泥硬化速度,D正确。
3.下列关于鉴别1 mol·L-1稀硫酸和98%的浓硫酸的叙述正确的是( )
A.常温下测定两溶液的导电能力,导电能力强的是浓硫酸
B.常温下可以用铜片鉴别两种溶液
C.常温下不能用铝片鉴别两种溶液
D.两溶液敞口在空气中放置一段时间后质量明显增大的是浓硫酸
答案 D
解析 稀硫酸中硫酸完全电离,离子浓度较大,浓硫酸几乎没有电离,因此常温下测定两溶
液的导电能力,导电能力强的是稀硫酸,故 A错误;常温下,铜与稀硫酸和浓硫酸均不反
应,不能鉴别两种溶液,故B错误;常温下,铝片与稀硫酸反应能够产生气泡,铝遇浓硫
酸发生钝化,可以鉴别两种溶液,故C错误;浓硫酸具有吸水性,两溶液敞口在空气中放
置一段时间后质量明显增大的是浓硫酸,故D正确。
4.实验室用如图装置制备HCl气体。推压注射器活塞将浓盐酸慢慢注入浓硫酸中,可制备少
量干燥HCl气体,其原理分析不正确的是( )
A.混合时放热使HCl溶解度减小
B.浓硫酸具有吸水性,吸收了盐酸中水分
C.浓盐酸具有挥发性,利于HCl气体逸出
D.浓盐酸中HCl以分子形式存在,利于HCl气体逸出
答案 D
解析 浓硫酸与浓盐酸混合过程中放出大量的热,温度升高使HCl溶解度减小,有利于HCl
的逸出,故A正确;浓硫酸有吸水性,可以干燥氯化氢气体,故 B正确;氯化氢是强电解
质,浓盐酸中以H+、Cl-形式存在,故D错误。
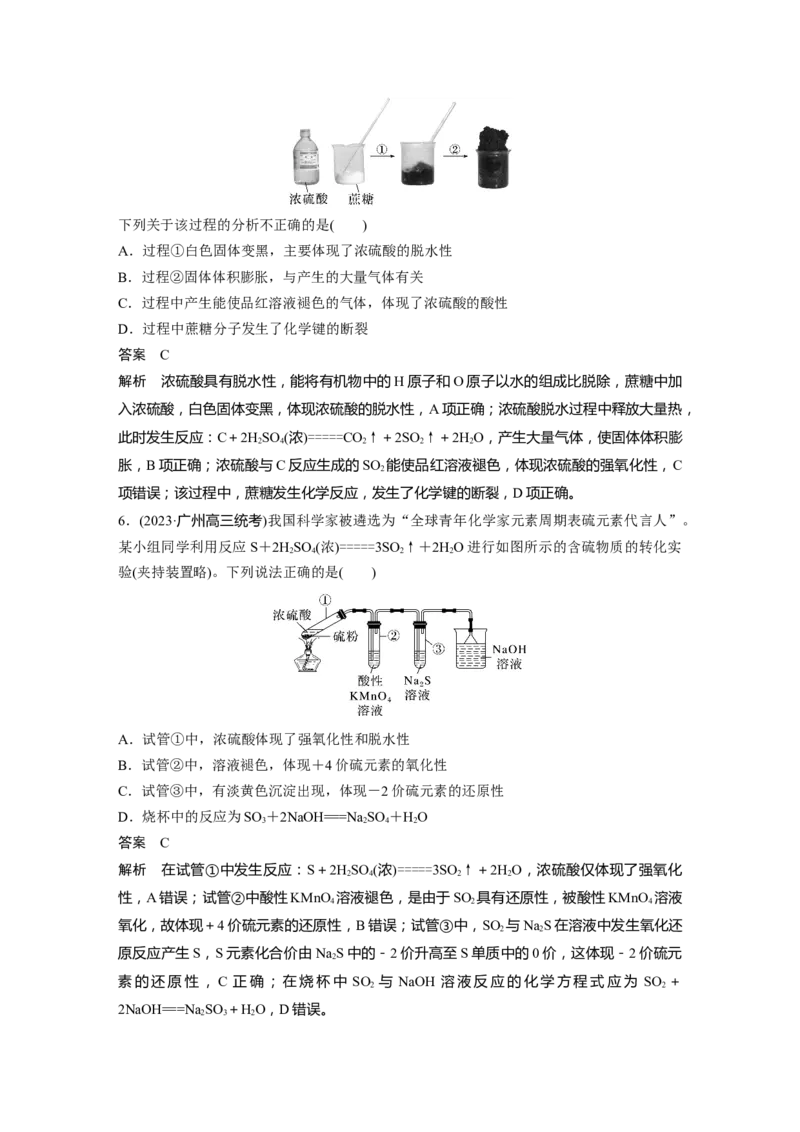
5.(2023·北京,7)蔗糖与浓硫酸发生作用的过程如图所示。下列关于该过程的分析不正确的是( )
A.过程①白色固体变黑,主要体现了浓硫酸的脱水性
B.过程②固体体积膨胀,与产生的大量气体有关
C.过程中产生能使品红溶液褪色的气体,体现了浓硫酸的酸性
D.过程中蔗糖分子发生了化学键的断裂
答案 C
解析 浓硫酸具有脱水性,能将有机物中的H原子和O原子以水的组成比脱除,蔗糖中加
入浓硫酸,白色固体变黑,体现浓硫酸的脱水性,A项正确;浓硫酸脱水过程中释放大量热,
此时发生反应:C+2HSO (浓)=====CO↑+2SO ↑+2HO,产生大量气体,使固体体积膨
2 4 2 2 2
胀,B项正确;浓硫酸与C反应生成的SO 能使品红溶液褪色,体现浓硫酸的强氧化性,C
2
项错误;该过程中,蔗糖发生化学反应,发生了化学键的断裂,D项正确。
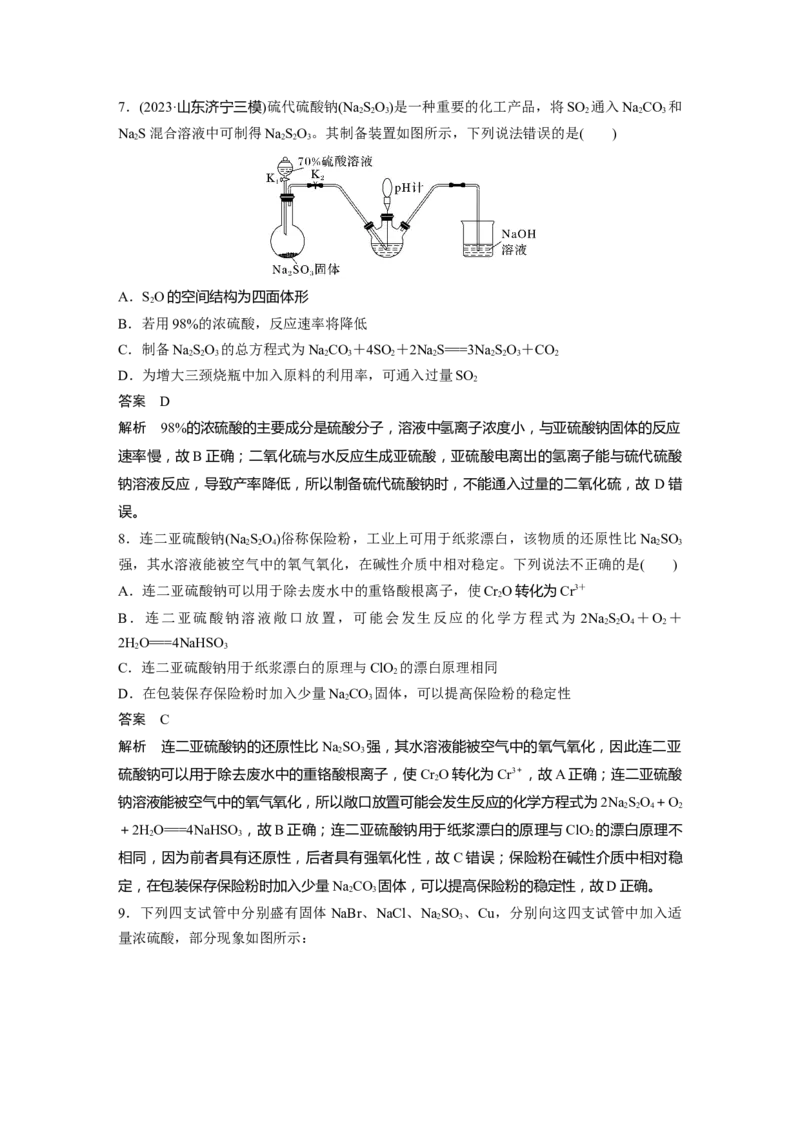
6.(2023·广州高三统考)我国科学家被遴选为“全球青年化学家元素周期表硫元素代言人”。
某小组同学利用反应S+2HSO (浓)=====3SO ↑+2HO进行如图所示的含硫物质的转化实
2 4 2 2
验(夹持装置略)。下列说法正确的是( )
A.试管①中,浓硫酸体现了强氧化性和脱水性
B.试管②中,溶液褪色,体现+4价硫元素的氧化性
C.试管③中,有淡黄色沉淀出现,体现-2价硫元素的还原性
D.烧杯中的反应为SO +2NaOH===NaSO +HO
3 2 4 2
答案 C
解析 在试管①中发生反应:S+2HSO (浓)=====3SO ↑+2HO,浓硫酸仅体现了强氧化
2 4 2 2
性,A错误;试管②中酸性KMnO 溶液褪色,是由于SO 具有还原性,被酸性KMnO 溶液
4 2 4
氧化,故体现+4价硫元素的还原性,B错误;试管③中,SO 与NaS在溶液中发生氧化还
2 2
原反应产生S,S元素化合价由NaS中的-2价升高至S单质中的0价,这体现-2价硫元
2
素的还原性,C 正确;在烧杯中 SO 与 NaOH 溶液反应的化学方程式应为 SO +
2 2
2NaOH===NaSO +HO,D错误。
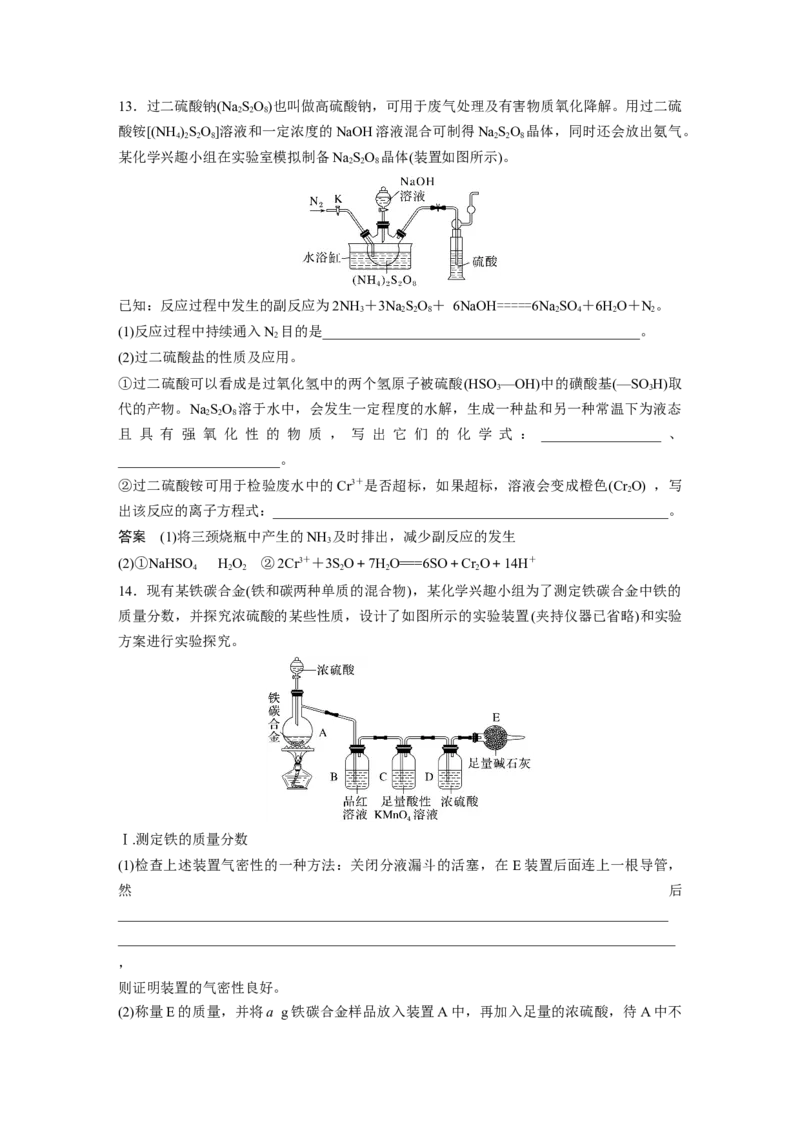
2 3 27.(2023·山东济宁三模)硫代硫酸钠(Na SO)是一种重要的化工产品,将SO 通入NaCO 和
2 2 3 2 2 3
NaS混合溶液中可制得NaSO。其制备装置如图所示,下列说法错误的是( )
2 2 2 3
A.SO的空间结构为四面体形
2
B.若用98%的浓硫酸,反应速率将降低
C.制备NaSO 的总方程式为NaCO+4SO +2NaS===3NaSO+CO
2 2 3 2 3 2 2 2 2 3 2
D.为增大三颈烧瓶中加入原料的利用率,可通入过量SO
2
答案 D
解析 98%的浓硫酸的主要成分是硫酸分子,溶液中氢离子浓度小,与亚硫酸钠固体的反应
速率慢,故B正确;二氧化硫与水反应生成亚硫酸,亚硫酸电离出的氢离子能与硫代硫酸
钠溶液反应,导致产率降低,所以制备硫代硫酸钠时,不能通入过量的二氧化硫,故 D错
误。
8.连二亚硫酸钠(Na SO)俗称保险粉,工业上可用于纸浆漂白,该物质的还原性比NaSO
2 2 4 2 3
强,其水溶液能被空气中的氧气氧化,在碱性介质中相对稳定。下列说法不正确的是( )
A.连二亚硫酸钠可以用于除去废水中的重铬酸根离子,使Cr O转化为Cr3+
2
B.连二亚硫酸钠溶液敞口放置,可能会发生反应的化学方程式为 2NaSO +O +
2 2 4 2
2HO===4NaHSO
2 3
C.连二亚硫酸钠用于纸浆漂白的原理与ClO 的漂白原理相同
2
D.在包装保存保险粉时加入少量NaCO 固体,可以提高保险粉的稳定性
2 3
答案 C
解析 连二亚硫酸钠的还原性比NaSO 强,其水溶液能被空气中的氧气氧化,因此连二亚
2 3
硫酸钠可以用于除去废水中的重铬酸根离子,使Cr O转化为Cr3+,故A正确;连二亚硫酸
2
钠溶液能被空气中的氧气氧化,所以敞口放置可能会发生反应的化学方程式为2NaSO+O
2 2 4 2
+2HO===4NaHSO ,故B正确;连二亚硫酸钠用于纸浆漂白的原理与ClO 的漂白原理不
2 3 2
相同,因为前者具有还原性,后者具有强氧化性,故C错误;保险粉在碱性介质中相对稳
定,在包装保存保险粉时加入少量NaCO 固体,可以提高保险粉的稳定性,故D正确。
2 3
9.下列四支试管中分别盛有固体NaBr、NaCl、NaSO 、Cu,分别向这四支试管中加入适
2 3
量浓硫酸,部分现象如图所示:下列判断正确的是( )
A.反应①和②的现象说明还原性:Br->Cl-
B.浓硫酸与NaCl不反应,白雾是浓硫酸吸水所致
C.反应③的现象说明氧化性:浓硫酸>Na SO
2 3
D.反应④的现象除产生刺激性气味的气体外,溶液中还析出蓝色晶体
答案 A
解析 ①中有红棕色气体产生,此气体为Br ,浓硫酸作氧化剂把Br-氧化成Br ,②中有白
2 2
雾,此白雾是浓硫酸与NaCl反应生成的HCl的小液滴,Cl-没有被氧化,说明Br-的还原性
强于Cl-,故A正确、B错误;③中发生的反应为NaSO +HSO (浓)===NaSO +SO ↑+
2 3 2 4 2 4 2
HO,此反应不是氧化还原反应,故C错误;Cu与浓硫酸反应生成CuSO 、SO 、HO,利
2 4 2 2
用浓硫酸的吸水性,溶液中应析出白色固体,故D错误。
10.NaSO 是常用的防腐剂和漂白剂,通常由NaHSO 过饱和溶液经结晶脱水制得。可利
2 2 5 3
用烟道气中的SO 生产NaSO,其流程如下:
2 2 2 5
下列说法正确的是( )
A.上述制备过程所涉及的物质中只有一种酸性氧化物
B.NaSO 作防腐剂和SO 作漂白剂时,均表现还原性
2 2 5 2
C.上述流程中的NaCO 饱和溶液和NaCO 固体不可互换
2 3 2 3
D.实验室模拟“结晶脱水”时用到的仪器只有蒸发皿、玻璃棒
答案 C
解析 题述制备过程所涉及的物质中有两种酸性氧化物——二氧化硫和二氧化碳,故A错
误;SO 用作漂白剂时,未发生氧化还原反应,故B错误;根据题给流程图分析,流程中的
2
NaCO 饱和溶液和NaCO 固体不可互换,否则得不到过饱和的NaHSO 溶液,故C正确。
2 3 2 3 3
11.某实验小组同学探究不同金属和浓硫酸的反应,向三等份浓硫酸中分别加入大小相同的
不同金属片,加热,用生成的气体进行下表实验操作并记录实验现象。
实验操作 实验现象铜 锌 铝
点燃 不燃烧 燃烧 燃烧
通入酸性KMnO 溶液 褪色 褪色 褪色
4
通入CuSO 溶液 无明显变化 无明显变化 出现黑色沉淀
4
通入品红溶液 褪色 褪色 不褪色
已知:HS+CuSO ===CuS↓+HSO (CuS为黑色固体);HS可燃。
2 4 2 4 2
下列说法不正确的是( )
A.加入铜片的实验中,使酸性KMnO 溶液褪色的气体是SO
4 2
B.加入铝片的实验中,燃烧现象能证明生成气体中一定含HS
2
C.加入锌片的实验中,生成的气体一定是混合气体
D.金属与浓硫酸反应的还原产物与金属活动性强弱有关
答案 B
解析 加入铜片的实验中,气体能使酸性KMnO 溶液和品红溶液褪色、不可燃,则气体具
4
有还原性、漂白性,则气体是SO ,A正确;加入铝片的实验中,气体能使酸性KMnO 溶
2 4
液褪色、能与CuSO 溶液反应产生黑色沉淀,则气体是HS,硫化氢具有可燃性,但具有可
4 2
燃性的气体不一定是硫化氢,B不正确;加入锌片的实验中,气体能使酸性KMnO 溶液、
4
品红溶液褪色,则气体含SO ,但SO 不可燃,而锌片与浓硫酸反应产生的气体具有可燃性,
2 2
则还含有另一种气体,C正确。
12.将一定量的锌放入200 mL 18.4 mol·L-1浓硫酸中加热,充分反应后锌完全溶解,同时
生成气体X 44.8 L(标准状况)。将反应后的溶液稀释至0.8 L,测得溶液c(H+)=0.2 mol·L-
1,下列判断错误的是( )
A.气体X为SO 和H 的混合物
2 2
B.反应中共转移4 mol电子
C.气体X中SO 与H 的体积比为1∶4
2 2
D.反应中共消耗Zn 130 g
答案 C
解析 稀释至0.8 L时,c(H+)=0.2 mol·L-1,说明硫酸过量,反应的硫酸的物质的量为
(0.2×18.4-0.8×0.1) mol=3.6 mol,假设只生成SO ,发生的反应是Zn+2HSO (浓)=====
2 2 4
ZnSO +SO ↑+2HO,SO 的体积为(×22.4) L=40.32 L<44.8 L,说明除生成SO 外,还有
4 2 2 2 2
氢气生成,A正确;设生成SO 的物质的量为x mol,则氢气的物质的量为(2-x) mol,生成
2
SO 消耗的硫酸的物质的量为2x mol,生成氢气消耗的硫酸的物质的量为(2-x) mol,则根
2
据A选项的分析,有2x+2-x=3.6,解得x=1.6,氢气的物质的量为0.4 mol,转移电子的
物质的量为(1.6×2+0.4×2) mol=4 mol,B正确;气体X中SO 与H 的体积比为4∶1,C
2 2
错误;根据得失电子守恒,消耗的锌的质量为2 mol×65 g·mol-1=130 g,D正确。13.过二硫酸钠(Na SO)也叫做高硫酸钠,可用于废气处理及有害物质氧化降解。用过二硫
2 2 8
酸铵[(NH )SO]溶液和一定浓度的NaOH溶液混合可制得NaSO 晶体,同时还会放出氨气。
4 2 2 8 2 2 8
某化学兴趣小组在实验室模拟制备NaSO 晶体(装置如图所示)。
2 2 8
已知:反应过程中发生的副反应为2NH +3NaSO+ 6NaOH=====6NaSO +6HO+N。
3 2 2 8 2 4 2 2
(1)反应过程中持续通入N 目的是_____________________________________________。
2
(2)过二硫酸盐的性质及应用。
①过二硫酸可以看成是过氧化氢中的两个氢原子被硫酸(HSO —OH)中的磺酸基(—SO H)取
3 3
代的产物。NaSO 溶于水中,会发生一定程度的水解,生成一种盐和另一种常温下为液态
2 2 8
且 具 有 强 氧 化 性 的 物 质 , 写 出 它 们 的 化 学 式 : _________________ 、
_______________________。
②过二硫酸铵可用于检验废水中的Cr3+是否超标,如果超标,溶液会变成橙色(CrO) ,写
2
出该反应的离子方程式:________________________________________________________。
答案 (1)将三颈烧瓶中产生的NH 及时排出,减少副反应的发生
3
(2)①NaHSO HO ②2Cr3++3SO+7HO===6SO+Cr O+14H+
4 2 2 2 2 2
14.现有某铁碳合金(铁和碳两种单质的混合物),某化学兴趣小组为了测定铁碳合金中铁的
质量分数,并探究浓硫酸的某些性质,设计了如图所示的实验装置(夹持仪器已省略)和实验
方案进行实验探究。
Ⅰ.测定铁的质量分数
(1)检查上述装置气密性的一种方法:关闭分液漏斗的活塞,在 E装置后面连上一根导管,
然 后
______________________________________________________________________________
_______________________________________________________________________________
,
则证明装置的气密性良好。
(2)称量E的质量,并将a g铁碳合金样品放入装置A中,再加入足量的浓硫酸,待A中不再逸出气体时,停止加热,拆下 E 并称重,E 增重 b g。铁碳合金中铁的质量分数为
_____________________________________________________________________(写表达式)。
(3)装置C的作用:_____________________________________________________________。
(4)甲同学认为,依据此实验测得的数据计算合金中铁的质量分数可能会偏低,原因是空气
中CO、水蒸气进入E使b增大。你认为改进的方法是
2
_______________________________________________________________________________
。
(5)乙同学认为,即使甲同学认为的偏差得到改进,依据此实验测得合金中铁的质量分数也
可 能 会 偏 高 。 你 认 为 其 中 的 原 因 是
____________________________________________________
_______________________________________________________________________________
。
Ⅱ.探究浓硫酸的某些性质
(6)往 A 中滴加足量的浓硫酸,未点燃酒精灯前,A、B 均无明显现象,其原因是
________________________________________________________________________________
_______________________________________________________________________________
。
(7)A中铁与足量浓硫酸发生反应的化学方程式是
_______________________________________________________________________________
_______________________________________________________________________________
。
答案 (1)把导管放入盛有水的水槽中,微热烧瓶,如果导管口有气泡产生,停止加热后导
管中产生一段水柱 (2)×100% (3)除去CO 中的SO 并检验SO 是否除尽 (4)在E的后边
2 2 2
再连接一个与E相同的装置 (5)反应产生的CO 气体未能完全排到E中,导致b偏低 (6)
2
常温下,Fe被浓HSO 钝化,碳与浓HSO 不反应 (7)2Fe + 6HSO (浓)=====Fe (SO )
2 4 2 4 2 4 2 4 3
+ 3SO ↑ + 6HO
2 2
解析 (2)铁、碳在加热条件下与浓硫酸反应产生 SO 和CO ,用品红溶液检验SO ,用足量
2 2 2
酸性高锰酸钾溶液除去SO ,酸性KMnO 溶液颜色变浅但未完全褪色说明SO 已除尽;浓
2 4 2
硫酸作干燥剂,碱石灰吸收产生的CO ,根据碳元素守恒,n(C)=n(CO)= mol,则铁的质
2 2
量为(a-b×) g= g,铁的质量分数为×100%。