文档内容
第 28 讲 常见气体的实验室制备、净化和收集
[复习目标] 1.了解常见气体的制备原理、装置及改进。2.能根据气体的性质及制备原理设
计实验流程。
1.气体制备实验的基本思路
2.重要气体的发生装置
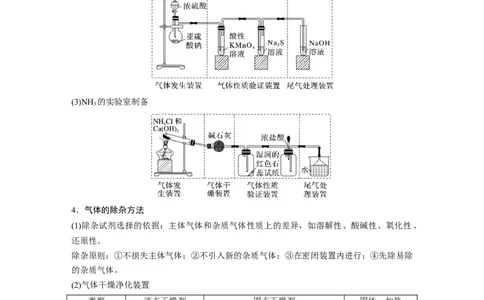
依据制备气体所需的反应物状态和反应条件,可将发生装置分为三类:
(1)固体+固体――→气体
制备气体:O、NH 、CH 等。
2 3 4
(2)固体+液体(或液体+液体)――→气体
制备气体:Cl、C H 等。
2 2 4
(3)固体+液体(不加热)―→气体
制备气体:选择合适的药品和装置能制取中学化学中常见的气体。
3.常见气体典型制备装置举例(1)Cl 的实验室制备
2
(2)SO 的实验室制备
2
(3)NH 的实验室制备
3
4.气体的除杂方法
(1)除杂试剂选择的依据:主体气体和杂质气体性质上的差异,如溶解性、酸碱性、氧化性、
还原性。
除杂原则:①不损失主体气体;②不引入新的杂质气体;③在密闭装置内进行;④先除易除
的杂质气体。
(2)气体干燥净化装置
类型 液态干燥剂 固态干燥剂 固体,加热
装
置
图
Ⅰ Ⅱ Ⅲ Ⅳ
常见 浓HSO (酸性、强 Cu、CuO、Mg
2 4
无水氯化钙(中性)、碱石灰(碱性)
试剂 氧化性) 等
当CO 中混有O 杂质时,应选用上述Ⅰ~Ⅳ中的装置Ⅳ除O,除杂试剂是 Cu 粉 。
2 2 25.气体的收集方法
收集方法 收集气体的类型 收集装置 可收集的气体(举例)
难溶于水或微溶于水,且不
排水法 O、H、NO、CO等
2 2
与水反应的气体
向上排 密度大于空气且不与空气中
排 Cl、SO 、NO 、CO
2 2 2 2
空气法 的成分反应
空
气
向下排 密度小于空气且不与空气中
法 H、NH
2 3
空气法 的成分反应
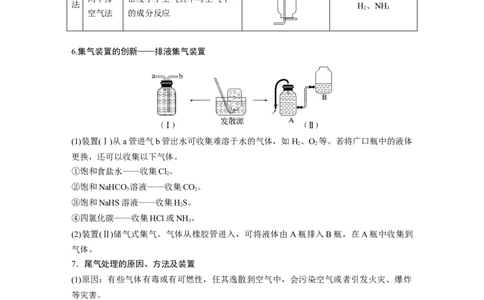
6.集气装置的创新——排液集气装置
(1)装置(Ⅰ)从a管进气b管出水可收集难溶于水的气体,如H、O 等。若将广口瓶中的液体
2 2
更换,还可以收集以下气体。
①饱和食盐水——收集Cl。
2
②饱和NaHCO 溶液——收集CO。
3 2
③饱和NaHS溶液——收集HS。
2
④四氯化碳——收集HCl或NH 。
3
(2)装置(Ⅱ)储气式集气。气体从橡胶管进入,可将液体由A瓶排入B瓶,在A瓶中收集到
气体。
7.尾气处理的原因、方法及装置
(1)原因:有些气体有毒或有可燃性,任其逸散到空气中,会污染空气或者引发火灾、爆炸
等灾害。
(2)处理方法:一般根据气体的相关性质,使其转化为非气态物质或无毒物质,如酸性有毒
气体用碱溶液吸收,可燃性气体用点燃等措施。
(3)尾气处理装置(见图a、b、c)
①实验室制取Cl 时,尾气的处理可采用b装置。
2②制取CO时,尾气的处理可采用a、c装置。
③制取H 时,尾气的处理可采用a、c装置。
2
8.防倒吸装置
肚容式 分液式
一、一种装置多种用途
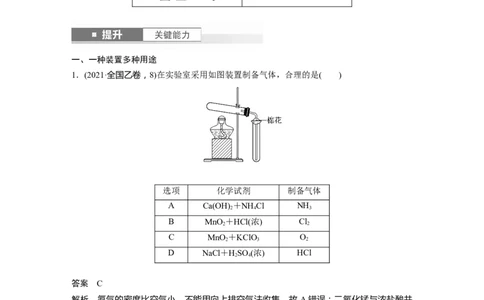
1.(2021·全国乙卷,8)在实验室采用如图装置制备气体,合理的是( )
选项 化学试剂 制备气体
A Ca(OH) +NH Cl NH
2 4 3
B MnO +HCl(浓) Cl
2 2
C MnO +KClO O
2 3 2
D NaCl+HSO (浓) HCl
2 4
答案 C
解析 氨气的密度比空气小,不能用向上排空气法收集,故 A错误;二氧化锰与浓盐酸共
热制备氯气为固液加热反应,不能选用固固加热装置,故B错误;二氧化锰和氯酸钾共热
制备氧气为固固加热的反应,氧气的密度大于空气,可选用向上排空气法收集,故C正确;
氯化钠与浓硫酸共热制备HCl为固液加热反应,不能选用固固加热装置,故D错误。
2.(2022·北京,10)利用如图所示装置(夹持装置略)进行实验,b中现象不能证明a中产物生
成的是( )a中反应 b中检测试剂及现象
A 浓HNO 分解生成NO 淀粉-KI溶液变蓝
3 2
B Cu与浓HSO 生成SO 品红溶液褪色
2 4 2
C 浓NaOH与NH Cl溶液生成NH 酚酞溶液变红
4 3
D CHCHBrCH 与NaOH乙醇溶液生成丙烯 溴水褪色
3 3
答案 A
解析 浓硝酸具有挥发性,挥发出的硝酸也能与碘化钾反应生成碘,则淀粉-KI溶液变蓝色
不能说明浓硝酸分解生成二氧化氮,故 A符合题意;铜与浓硫酸共热反应生成的二氧化硫
具有漂白性,使品红溶液褪色,故B不符合题意;浓氢氧化钠溶液与氯化铵溶液共热反应
生成氨气,使酚酞溶液变红,故C不符合题意;乙醇具有挥发性,挥发出的乙醇不能与溴
水反应,溴水褪色则说明2-溴丙烷与氢氧化钠乙醇溶液共热发生消去反应生成了丙烯,故D
不符合题意。
二、仪器装置的选择
3.(2021·北京,5)实验室制备下列气体所选试剂、制备装置及收集方法均正确的是( )
气体 试剂 制备装置 收集方法
A O KMnO a d
2 4
B H Zn+稀HSO b e
2 2 4
C NO Cu+稀HNO b c
3
D CO CaCO +稀HSO b c
2 3 2 4
答案 B
解析 KMnO 是固体物质,加热分解产生O ,由于O 难溶于水,因此可以用排水法或向上
4 2 2
排空气法收集,故不可以使用d装置收集O ,A错误;Zn与HSO 发生置换反应产生H ,
2 2 4 2
块状固体与液体反应制取气体,产生的 H 难溶于水且不与水反应,因此可以用排水法收集,
2故可以使用装置b、e制取和收集H ,B正确;Cu与稀HNO 反应产生NO气体,NO能够
2 3
与O 发生反应产生NO 气体,因此不能使用排空气法收集,C错误;CaCO 与稀硫酸反应
2 2 3
产生的CaSO 微溶于水,使制取CO 气体不能持续发生,因此不能使用该方法制取CO 气体,
4 2 2
D错误。
4.某化学研究性学习小组,按如图装置制备NaClO溶液(部分夹持装置省去)。
(1)图中A为实验室制备Cl 的发生装置,可以选用下列图中__________(填“甲”“乙”或
2
“丙”)装置,用该装置制备Cl 反应的化学方程式为__________________________________。
2
(2)B装置中仪器 a的名称是__________,B装置可除去氯气中的氯化氢杂质,此外还有
________________________________________________________________________________
_____________________________________________________________________________(写
出一点)的作用。
(3)反应一段时间后,经测定 C瓶溶液的 pH=12,预测其中溶质除 NaCl外,还可能有
__________(填化学式)。
答 案 (1) 甲 ( 或 乙 ) MnO + 4HCl( 浓 )=====MnCl + Cl↑ + 2HO[ 或 2KMnO +
2 2 2 2 4
16HCl(浓)===2KCl+2MnCl +5Cl↑+8HO] (2)长颈漏斗 贮存少量气体[或平衡气压(安
2 2 2
全瓶)或防倒吸] (3)NaClO、NaOH
5.某实验小组设计如图所示装置制备焦亚硫酸钠(Na SO),部分夹持装置省略。
2 2 5
已知:Ⅰ.Na SO +SO ===NaSO
2 3 2 2 2 5
Ⅱ.Na SO 易溶于水,微溶于乙醇。性质活泼,受潮易分解,露置空气中易被氧化成硫酸钠。
2 2 5
(1)仪器组装结束,检查装置气密性并加入实验药品,开始实验需进行的第一步操作是
_______________________________________________________________________________________________________________________________________________________________
。
(2)装置Ⅱ中的试剂最好选用______________________________________________________,
该装置的作用是_________________________________________________________________。
(3)装置Ⅳ用于处理尾气,可选用的合理装置为__________(填字母)。
答案 (1)打开装置Ⅰ的弹簧夹,通入N 排出装置中的空气,然后关闭弹簧夹 (2)饱和亚硫
2
酸氢钠溶液 通过观察气泡调控SO 的生成速率;作安全瓶 (3)bd
2
三、仪器的连接
6.根据实验目的设计的如图装置的连接正确的是( )
A.制备收集C H:连接a→c→g
2 4
B.制备收集NO:连接b→c→e→d
C.制备收集NH :连接b→d→e→c
3
D.制备收集Cl:连接a→f→c→e→d
2
答案 D
7.根据装置和下表内的物质(省略夹持、净化以及尾气处理装置,图1中虚线框内的装置是
图2),其中能完成相应实验目的的是( )
实验目的、试剂和操作
选项 a中的物质 b中的物质
实验目的 c中的物质 进气方向
A 稀硝酸 Cu 收集贮存NO 水 N→M
B 浓硝酸 NaSO 检验SO 的氧化性 品红溶液 M→N
2 3 2
饱和NH Cl
4
C 浓氨水 碱石灰 收集贮存氨气 N→M
溶液
D 浓盐酸 MnO 检验Cl 的氧化性 NaS溶液 M→N
2 2 2答案 A
解析 稀硝酸和Cu反应生成NO,NO不溶于水,不与水反应,用排水法收集 NO,进气方
向是N→M,故A符合题意;浓硝酸具有强氧化性,与NaSO 反应生成硫酸盐和NO 气体,
2 3 2
因此无法检验SO 的氧化性,故B不符合题意;由于氨气极易溶于水,因此氨气溶于饱和
2
NH Cl溶液,不能用排饱和NH Cl溶液的方法来收集氨气,故C不符合题意;二氧化锰和
4 4
浓盐酸在加热条件下反应,而该实验没有加热装置,因此不能产生氯气,故D不符合题意。
四、实验装置的改进与创新
8.(2023·湖南永州市第一中学高三联考)FeCl (易升华)是常见的化学试剂,可通过下列实验
3
制备FeCl ,下列说法错误的是( )
3
A.装置F的作用是尾气吸收,并防止空气中的水蒸气进入收集器
B.硬质玻璃管直接连接收集器的优点是不因FeCl 固体积聚而造成堵塞
3
C.实验室配制FeCl 溶液时应先将FeCl 固体溶于少量盐酸,再加水稀释
3 3
D.实验开始时,应先点燃D处酒精灯,后点燃A处酒精灯
答案 D
解析 A装置是氯气发生装置,B为除去氯气中的氯化氢,C为干燥装置,D为氯气与铁的
反应装置,E为氯化铁的收集装置,氯化铁易水解,故F装置是尾气吸收装置并防止空气中
的水蒸气进入收集器,A正确;FeCl 蒸气遇冷变为固体,若导管较细,容易堵塞,所以硬
3
质玻璃管直接连接收集器,B正确;FeCl 固体溶于水发生水解,配制FeCl 溶液时应先将
3 3
FeCl 固体溶于少量盐酸,抑制水解,再加水稀释,C正确;实验开始时,应先点燃A处酒
3
精灯,至装置中充满氯气后,再点燃D处酒精灯,D错误。
9.[2021·天津,15(1)(2)(3)(4)]某化学小组同学利用一定浓度的HO 溶液制备O。
2 2 2
该小组同学设计了如下气体发生装置(夹持装置省略)。(1)甲装置中主要仪器的名称为____________________________。
(2)乙装置中,用粘合剂将MnO 制成团,放在多孔塑料片上,连接好装置,气密性良好后打
2
开活塞K,经长颈漏斗向试管中缓慢加入3% H O 溶液至_____________________________。
1 2 2
欲使反应停止,关闭活塞K 即可,此时装置中的现象是______________________________
1
_______________________________________________________________________________
。
(3)丙装置可用于制备较多O ,催化剂铂丝可上下移动。制备过程中如果体系内压强过大,
2
安全管中的现象是______________________,此时可以将铂丝抽离HO 溶液,还可以采取
2 2
的 安 全 措 施 是
_____________________________________________________________________。
(4)丙装置的特点是______________(填序号)。
a.可以控制制备反应的开始和结束
b.可通过调节催化剂与液体接触的面积来控制反应的速率
c.与乙装置相比,产物中的O 含量高、杂质种类少
2
答案 (1)分液漏斗、锥形瓶
(2)刚好没过MnO 固体 试管内的HO 溶液被压入长颈漏斗中,与MnO 分离
2 2 2 2
(3)液面上升 打开弹簧夹K (4)ab
2
解析 (2)乙装置是启普发生器的简易装置,可以随时控制反应的发生和停止。用粘合剂将
MnO 制成团,放在多孔塑料片上,连接好装置,气密性良好后打开活塞 K ,经长颈漏斗向
2 1
试管中缓慢加入3% H O 溶液至刚好没过MnO 固体,此时可以产生氧气,氧气通过导管导
2 2 2
出。欲使反应停止,关闭活塞K ,此时由于气体还在产生,使容器内压强增大,可观察到
1
试管内的HO 溶液被压入长颈漏斗中,与MnO 分离。(3)丙装置用圆底烧瓶盛装HO 溶液,
2 2 2 2 2
可用于制备较多O ,催化剂铂丝可上下移动,可以控制反应速率。制备过程中如果体系内
2
压强过大,HO 溶液会被压入安全管中,可观察到安全管中液面上升,圆底烧瓶中液面下
2 2
降。此时可以将铂丝抽离HO 溶液,使反应速率减慢,还可以打开弹簧夹K ,使烧瓶内压
2 2 2
强降低。(4)催化剂铂丝可上下移动,可以控制制备反应的开始和结束,a正确;催化剂与液
体接触的面积越大,反应速率越快,可通过调节催化剂与液体接触的面积来控制反应的速率,
b正确;丙装置用圆底烧瓶盛装HO 溶液,与乙装置相比,可用于制备较多O ,但产物中
2 2 2
的O 含量和杂质种类和乙中没有区别,c错误。
2
10.某同学设计利用如图装置制备硫酸锰。(1) 盛 放 70%H SO 的 仪 器 名 称 是 ________ , 其 中 导 管 a 的 作 用 是
2 4
_________________________
_______________________________________________________________________________
。
(2)单向阀b的作用是____________________________________________________________。
(3)装置Ⅱ中反应的化学方程式:___________________________________________________,
其中“多孔球泡”的作用是_______________________________________________________。
(4)装置Ⅲ烧杯中的溶液是__________,倒扣漏斗的作用是____________。
答案 (1)恒压滴液漏斗 平衡气压,便于硫酸顺利滴下 (2)防止倒吸 (3)SO +
2
MnO ===MnSO 增大反应物的接触面积,加快反应速率,增大二氧化硫的吸收效率 (4)
2 4
氢氧化钠溶液 防止倒吸
课时精练
1.(2021·海南,3)用如图装置制取干燥的气体(a、b表示加入的试剂),能实现的是( )
选项 气体 a b
A HS 稀HSO FeS
2 2 4
B O HO 溶液 MnO
2 2 2 2
C NO 浓HNO 铁片
2 3
D NH 浓氨水 CaO
3
答案 B
解析 HS 与浓硫酸反应,故不能用浓硫酸干燥 HS,故 A 错误;发生反应:
2 2
2HO=====2HO+O↑,浓硫酸可以干燥氧气,故B正确;常温下,铁片遇浓硝酸发生钝
2 2 2 2化,故不能制取二氧化氮气体,故C错误;氨气与浓硫酸反应,故不能用浓硫酸干燥氨气,
故D错误。
2.(2023·广东肇庆高要一中模拟)下列实验装置正确的是( )
答案 A
解析 实验室可以用MnO 和浓盐酸在加热条件下制备Cl,故A正确;实验室可以用MnO
2 2 2
催化HO 分解制备O,用浓硫酸干燥O,O 的密度大于空气,可以用向上排空气法收集,
2 2 2 2 2
应该长管进、短管出,故B错误;收集NH 时,导管应伸入试管底部,故C错误;铜和浓
3
硫酸在加热的条件下反应生成二氧化硫,二氧化硫可以使石蕊溶液变红,但不能用浸有稀硫
酸的棉花团吸收过量的二氧化硫,应该用浸有NaOH溶液的棉花团,故D错误。
3.(2023·广州高三二模)将Cl 通入冷的NaOH溶液中可制得漂白液。下列装置(箭头表示Cl
2 2
的气流方向)能达到相应目的的是( )
A.制备Cl B.除去Cl 中的HCl C.制备漂白液 D.尾气处理
2 2
答案 C
解析 二氧化锰和浓盐酸反应需要加热,故A错误;用饱和食盐水除去Cl 中的HCl,气体
2
应该“长进短出”,故B错误;氯气和氢氧化钠在较低温度下反应生成氯化钠、次氯酸钠
和水,故C正确;石灰水的浓度太小,应该用氢氧化钠溶液吸收氯气,故D错误。
4.利用图示装置进行实验,反应进行足够长时间后装置Ⅱ中实验现象正确的是( )选项 ① ② ③ 装置Ⅱ中实验现象
A 稀盐酸 MnO 饱和NaCl溶液 有细小的白色晶体析出
2
B 浓氨水 氧化钙 硫酸亚铁溶液 产生大量白色沉淀
溶液分层,上层为油状液
C 冰醋酸 乙醇和浓硫酸 饱和碳酸钠溶液
体
D 浓盐酸 碳酸钙 滴有酚酞的稀碳酸钠溶液 溶液由红色变为无色
答案 D
解析 稀盐酸和二氧化锰不反应,装置Ⅱ中无明显现象,故A错误;浓氨水和氧化钙反应
生成氨气,氨气与硫酸亚铁溶液反应生成 Fe(OH) 白色沉淀,然后变为灰绿色,最终变为
2
Fe(OH) 红褐色沉淀,故B错误;酯化反应需要加热,但图中没有加热装置,不能生成乙酸
3
乙酯,故C错误;浓盐酸与碳酸钙反应生成CO 气体,且浓盐酸易挥发,CO 、HCl均与
2 2
NaCO 反应使溶液碱性减弱,观察到装置Ⅱ中溶液由红色最终变为无色,故D正确。
2 3
5.某学生想利用如图装置(烧瓶不能移动)收集下列气体:①H ;②Cl ;③SO ;④HCl;
2 2 2
⑤NH ;⑥NO;⑦NO 。下列说法正确的是( )
3 2
A.若烧瓶是干燥的,由b进气,可收集②③④⑥⑦
B.若烧瓶是干燥的,由a进气,可收集①⑤
C.若烧瓶中充满水,由a进气,可收集①⑤⑦
D.若烧瓶中充满水,由b进气,可收集⑥
答案 B
解析 NO不能用排空气法收集,A错误;由a进气可以收集比空气密度小且与空气中的成
分不反应的气体,B正确;NH 、NO 不能用排水法收集,C错误;用排水法集气不能由b
3 2
进气,D错误。
6.NaH是有机合成中用途很广泛的物质。已知NaH遇水蒸气剧烈反应,某小组设计如图实
验装置制备NaH。下列说法不正确的是( )A.安全漏斗的作用是液封
B.装置A中的试剂是稀硝酸和粗锌
C.装置B中的试剂是浓硫酸
D.实验开始后先启动A中反应,再点燃C处酒精灯
答案 B
解析 加入液体后,部分液体存于漏斗上部弯管中起液封作用,避免氢气从漏斗中逸出,A
正确;硝酸具有强氧化性,与 Zn反应不生成氢气,B错误;B是干燥氢气的装置,B中试
剂为浓硫酸,C正确;先启动A中反应,利用生成的氢气将装置中的空气排出,防止钠与氧
气反应,后点燃C处酒精灯,D正确。
7.(2023·南京二模)用如图所示装置制备氨并验证氨的还原性,其中不能达到实验目的的是(
)
A.用装置甲生成氨
B.用装置乙干燥氨
C.用装置丙验证氨的还原性
D.用装置丁和戊分别收集氨和氮气
答案 D
解析 反应2NH Cl+Ca(OH) =====CaCl +2NH ↑+2HO可用于制备氨,A正确;NH 是
4 2 2 3 2 3
碱性气体,可用碱石灰进行干燥,B正确;装置丙发生反应3CuO+2NH =====3Cu+N +
3 2
3HO,可验证氨的还原性,C正确;氨的密度比空气小,收集时应从短管进长管出,D错
2
误。
8.(2023·河南信阳质检)实验室常利用难挥发性酸制备易挥发性酸,用浓硫酸与硝石(NaNO )
3
反应可制备少量HNO,反应装置如图所示,下列说法不正确的是( )
3A.反应的化学方程式为NaNO +HSO (浓)=====NaHSO+HNO↑
3 2 4 4 3
B.反应温度如果过高,制得的HNO 可能会呈现黄色
3
C.曲颈甑是一种原始的蒸馏烧瓶,为了增强冷凝效果可以在长颈上再接一根长玻璃管
D.可从实验室中选无色、透明、洁净的试剂瓶盛装制得的浓硝酸
答案 D
解析 反应温度如果过高,HNO 分解生成NO ,NO 溶于HNO 使制得的HNO 呈现黄色,
3 2 2 3 3
B正确;实验室中浓硝酸应保存在棕色瓶内,防止其见光分解,D错误。
9.实验室用H 还原WO 制备金属W的装置如图所示(Zn粒中往往含有硫等杂质,焦性没
2 3
食子酸溶液用于吸收少量氧气)。下列说法正确的是( )
A.①②③中依次盛装KMnO 溶液、浓HSO 、焦性没食子酸溶液
4 2 4
B.管式炉加热前,用试管在④处收集气体并点燃,通过声音判断气体纯度
C.结束反应时,先关闭活塞K,再停止加热
D.装置Q(启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气
答案 B
解析 A项,气体从溶液中逸出易带出水蒸气,所以浓硫酸应放在③中,错误;B项,先通
H 以排出空气,加热前应先检验H 的纯度,正确;C项,若先停止通H ,空气中的氧气有
2 2 2
可能重新将W氧化,应先停止加热,待装置冷却后再关闭活塞K,错误;D项,MnO 和浓
2
盐酸反应制氯气需要加热,不能用启普发生器制备,错误。
10.某实验小组拟利用如图装置制取干燥的氮气。下列说法错误的是( )
A.装置Ⅰ中发生反应的化学方程式为NaNO +NH Cl=====NaCl+N↑+2HO
2 4 2 2
B.加热片刻后需要将酒精灯移开,说明该反应是放热反应C.装置Ⅱ的作用是冷凝水蒸气
D.在装置Ⅲ末端收集纯净干燥的N 只能用向下排空气法
2
答案 D
解析 因移开酒精灯后反应仍能进行,说明该反应是放热反应,B项正确;根据化学方程式
可知产物中有水蒸气,为便于干燥,可用装置Ⅱ冷凝大部分水蒸气,再用装置Ⅲ进行干燥,
C项正确。
11.(2023·天津和平区统考模拟)氯化锌易潮解、易升华。从市售的氯化锌[含Zn(OH)Cl]中制
备无水氯化锌,装置如图所示,管式炉有升温和降温的调节功能。下列说法错误的是( )
A.恒压滴液漏斗、倒置漏斗的作用分别是平衡气压、防止倒吸
B.通入装置中的N 必须是干燥的
2
C.在尾气吸收装置前应增加一个盛有浓硫酸的洗气瓶
D.管式炉Ⅰ采取阶段式升温,实验结束时先撤去管式炉Ⅰ,再撤去管式炉Ⅱ
答案 D
解析 氯化锌易吸水,所以需要通入干燥的N ,B项正确;尾气吸收装置中含水会使ZnCl
2 2
潮解,所以尾气吸收装置前应增加一个盛有浓硫酸的洗气瓶,C项正确。
12.实验室常见气体制备装置及收集方法如图:
(1) 实 验 室 中 可 用 装 置 a 制 取 O 或 NH , 反 应 的 化 学 方 程 式 分 别 为
2 3
________________________
_______________________________________________________________________________
,
_______________________________________________________________________________
。
(2)实验室中可用装置b制取O、NH 、Cl、CO、SO 、NO 等气体,则制取Cl 的化学方程
2 3 2 2 2 2 2
式为________________________________________________________________________
_______________________________________________________________________________
,制取NO 的化学方程式为________________________________________________________。
2
若利用该装置用浓氨水和NaOH固体制取NH ,其原理是______________________________
3
_______________________________________________________________________________
。
(3)实验室用过氧化氢溶液及少量MnO 制取O,可选用________(填字母)装置收集O。
2 2 2
答案 (1)2KMnO=====KMnO +MnO +O↑(或2KClO=====2KCl+3O↑)
4 2 4 2 2 3 2
Ca(OH) +2NH Cl=====CaCl +2NH ↑+2HO
2 4 2 3 2
(2)2KMnO +16HCl(浓)===2KCl+2MnCl +5Cl↑+8HO Cu+4HNO(浓)===Cu(NO ) +
4 2 2 2 3 3 2
2NO ↑+2HO 把氨水滴加到NaOH固体上,NaOH溶于水放出热量可促进NH ·H O的分
2 2 3 2
解;NaOH溶于水电离产生的OH-促使平衡NH +HONH ·H ONH+OH-逆向移动,
3 2 3 2
导致放出NH (3)c或e
3
13.氧钒(Ⅳ)碱式碳酸铵晶体难溶于水,是制备热敏材料 VO 的原料,其化学式为
2
(NH )[(VO) (CO)(OH) ]·10H O。实验室以VOCl 和NH HCO 为原料制备氧钒(Ⅳ)碱式碳酸
4 5 6 3 4 9 2 2 4 3
铵晶体的装置如图所示。
已知:+4价钒的化合物易被氧化。
回答下列问题:
(1)制备过程中,上述装置依次连接的合理顺序为e→________(按气流方向,用小写字母表
示 ) 。 装 置 A 中 饱 和 NaHCO 溶 液 的 作 用 是
3
_______________________________________________。
(2)连接好装置,检查气密性良好后,加入试剂,开始实验,先________________(填实验操
作),当装置B中溶液变浑浊时,关闭K,打开K,进行实验。
1 2
(3)装置D中生成氧钒(Ⅳ)碱式碳酸铵晶体的化学方程式为_____________________________。
答案 (1)a→b→f→g→c 除去二氧化碳中的HCl杂质 (2)关闭K,打开K
2 1
(3)6VOCl +6HO+17NH HCO ===(NH )[(VO) (CO)(OH) ]·10H O↓+13CO↑+12NH Cl
2 2 4 3 4 5 6 3 4 9 2 2 4
解析 (1)由于+4价钒的化合物易被氧化,因此装置D反应前需要用装置C产生的CO 排
2
出装置内的空气,而装置C中产生的CO 中会混入HCl杂质,用装置A中的饱和NaHCO
2 3
溶液除去,用装置B检验CO 是否充满整个实验装置,故上述装置依次连接的合理顺序为
2e→a→b→f→g→c。