文档内容
第 57 讲 难溶电解质的沉淀溶解平衡
[复习目标] 1.了解难溶电解质的沉淀溶解平衡。2.理解溶度积(K )的含义,并能进行相关计
sp
算。3.了解沉淀的生成、溶解与转化,并能应用化学平衡原理解释。
考点一 沉淀溶解平衡 溶度积
1.物质的溶解性与溶解度的关系
20 ℃时,电解质在水中的溶解度与溶解性存在如下关系:
2.沉淀溶解平衡
(1)沉淀溶解平衡的建立
溶质溶解的过程是一个可逆过程:
固体溶质溶液中的溶质
(2)特点(同其他化学平衡):逆、等、定、动、变(适用平衡移动原理)。
(3)沉淀溶解平衡的影响因素
①内因:难溶电解质本身的性质,即难溶电解质的溶解能力。
②外因:难溶电解质在水溶液中会建立动态平衡,改变温度和某离子浓度,会使沉淀溶解平
衡发生移动。
以AgCl为例:AgCl(s)Ag+(aq)+Cl-(aq)
ΔH>0,完成下表:
外界条件 移动方向 c(Ag+)
升高温度 右移 增大
加水(固体有剩余) 右移 不变
加入少量AgNO(s) 左移 增大
3
加入NaS(s) 右移 减小
2
通入HCl 左移 减小
通入NH 右移 减小
3
[应用举例]
将足量BaCO 固体分别加入:①30 mL水;②10 mL 0.2 mol·L-1NaCO 溶液;③50 mL
3 2 3
0.01 mol·L-1 BaCl 溶液;④100 mL 0.01 mol·L-1盐酸中溶解至溶液饱和。
2所得溶液中c(Ba2+)由大到小的顺序为____________________________。
答案 ③>④>①>②
3.溶度积常数
(1)溶度积常数和离子积比较
以A B (s)mAn+(aq)+nBm-(aq)为例:
m n
溶度积(K ) 离子积(Q)
sp
含义 沉淀溶解平衡的平衡常数 溶液中有关离子浓度幂的乘积
K (A B )= c m (A n + )· c n (B m - ) ,式中的浓度 Q(A B )= c m (A n + )· c n (B m - ) ,式
sp m n m n
表达式
是平衡浓度 中的浓度是任意浓度
判断在一定条件下沉淀能否生成或溶解:
①Q>K :溶液过饱和,有沉淀析出;
sp
应用
②Q=K :溶液饱和,处于平衡状态;
sp
③Q<K :溶液未饱和,无沉淀析出
sp
(2)K 的影响因素
sp
①内因:溶度积与难溶电解质溶解能力的关系:阴、阳离子个数比相同的难溶电解质,溶度
积越小,其溶解能力越小;不同类型的难溶电解质,应通过计算才能进行比较溶解能力。
②外因:仅与温度有关,与浓度、压强、催化剂等无关。
[应用举例]
已知几种难溶电解质在25 ℃时的溶度积。
化学式 K
sp
AgCl 1.8×10-10
AgBr 5.4×10-13
AgI 8.5×10-17
Ag S 6.3×10-50
2
Mg(OH) 5.6×10-12
2
请思考并回答下列问题。
(1)25 ℃时,AgCl(s)、AgBr(s)、AgI(s)溶于水形成的饱和溶液中c(Ag+)大小关系能否直接判
断?三种物质的溶解能力由大到小如何排序?
(2)AgCl和Mg(OH) 相比,哪种物质更难溶?通过简单的计算阐述判断的依据。
2
答案 (1)能。溶解能力由大到小:AgCl>AgBr>AgI。
(2)K (AgCl)=c(Ag+)·c(Cl-)=c2(Ag+)=1.8×10-10,c(Ag+)≈1.34×10-5 mol·L-1,即AgCl
sp
的溶解浓度为1.34×10-5 mol·L-1;K [Mg(OH) ]=c(Mg2+)·c2(OH-)=4c3(Mg2+)=5.6×10-
sp 2
12,c(Mg2+)≈1.12×10-4 mol·L-1,即Mg(OH) 的溶解浓度为1.12×10-4 mol·L-1,则AgCl
2
更难溶。一、沉淀溶解平衡移动
1.已知溶液中存在平衡:Ca(OH) (s)Ca2+(aq)+2OH-(aq) ΔH<0,下列有关该平衡体
2
系的说法不正确的是______________(填序号)。
①升高温度,平衡逆向移动
②向溶液中加入少量碳酸钠粉末能增大钙离子的浓度
③除去氯化钠溶液中混有的少量钙离子,可以向溶液中加入适量的NaOH溶液
④恒温下,向溶液中加入CaO,溶液的pH升高
⑤给溶液加热,溶液的pH升高
⑥向溶液中加入NaCO 溶液,其中固体质量增加
2 3
⑦向溶液中加入少量NaOH固体,Ca(OH) 固体质量不变
2
答案 ②③④⑤⑦
解析 加入碳酸钠粉末会生成CaCO 沉淀,使Ca2+浓度减小,②错;加入氢氧化钠溶液会
3
使平衡左移,有Ca(OH) 沉淀生成,但Ca(OH) 的溶度积较大,要除去Ca2+,应把Ca2+转化
2 2
为更难溶的CaCO ,③错;恒温下K 不变,加入CaO后,溶液仍为Ca(OH) 的饱和溶液,
3 sp 2
pH不变,④错;加热,Ca(OH) 的溶解度减小,溶液的pH降低,⑤错;加入NaCO 溶液,
2 2 3
沉淀溶解平衡向右移动,Ca(OH) 固体转化为CaCO 固体,固体质量增加,⑥正确;加入
2 3
NaOH固体,沉淀溶解平衡向左移动,Ca(OH) 固体质量增加,⑦错。
2
2.(2023·青海海东统考模拟)将足量AgCl(s)溶解在水中,形成悬浊液。已知:AgCl(s)Ag
+(aq)+Cl-(aq) ΔH>0,下列叙述错误的是( )
A.加热悬浊液,使其温度升高,则K (AgCl)增大
sp
B.加少量水稀释,上述平衡正向移动,c(Ag+)不变
C.向悬浊液中通入少量氨气,Q(AgCl)K ,所以有AgCl沉淀生成。
sp4.(沉淀的pH)常温下,K [Cu(OH) ]=2×10-20,计算有关Cu2+沉淀的pH。
sp 2
(1)某CuSO 溶液中c(Cu2+)=0.02 mol·L-1,如果生成Cu(OH) 沉淀,应调整溶液的pH,使
4 2
之大于__________。
(2)要使0.2 mol·L-1 CuSO 溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则
4
应向溶液中加入NaOH溶液,使溶液的pH为________。
答案 (1)5 (2)6
解析 (1)根据题给信息,当 c(Cu2+)·c2(OH-)=2×10-20时开始出现沉淀,则 c(OH-)=
mol·L-1=10-9 mol·L-1,c(H+)=10-5 mol·L-1,pH=5,所以要生成Cu(OH) 沉淀,应调整
2
pH>5。
(2)要使Cu2+浓度降至=2×10-4 mol·L-1,c(OH-)= mol·L-1=10-8 mol·L-1,c(H+)=10-6
mol·L-1,此时溶液的pH=6。
5.(沉淀的顺序)已知K (AgCl)=1.56×10-10,K (AgBr)=7.7×10-13,K (AgCrO)=9.0×10
sp sp sp 2 4
-12。某溶液中含有 Cl-、Br-和CrO,浓度均为 0.01 mol·L-1,向该溶液中逐滴加入 0.01
mol·L-1的AgNO 溶液时,计算三种阴离子沉淀的先后顺序。
3
答案 三种阴离子浓度均为0.01 mol·L-1时,分别产生AgCl、AgBr和Ag CrO 沉淀,所需
2 4
要Ag+浓度依次为
c(Ag+)== mol·L-1=1.56×10-8 mol·L-1,
1
c(Ag+)== mol·L-1=7.7×10-11 mol·L-1,
2
c(Ag+)== mol·L-1=3×10-5 mol·L-1,沉淀时Ag+浓度最小的优先沉淀,因而沉淀的顺
3
序为Br-、Cl-、CrO。
考点二 沉淀溶解平衡的应用
1.沉淀的生成
(1)沉淀生成的实际应用
在无机物的制备和提纯、废水处理等领域,常利用生成沉淀来达到分离或除去某些离子的目
的。
(2)使溶液中的离子转化为沉淀的条件:溶液中离子积Q>K 。
sp
(3)常用的方法
方法 举例 解释
除去CuCl 溶液中的FeCl ,可向溶液中
2 3
CuO 与 H + 反应,促进 Fe 3 + 水
调节pH法 加入 CuO[ 或 Cu(OH) 或 CuCO 或
2 3
解生成 Fe(OH ) 沉淀
3
Cu (OH) CO]
2 2 3除去NH Cl溶液中的FeCl 杂质,可加入 Fe 3 + 与 NH ·H O 反应生成
4 3 3 2
氨水调节pH Fe(OH) 沉淀
3
以NaS 等沉淀污水中的Hg2+、Cu2+等重 Na S 与 Cu 2 + 、 Hg 2 + 反应生成
2 2
沉淀剂法
金属离子 沉淀
2.沉淀的溶解
(1)原理:不断减少沉淀溶解平衡体系中的相应离子,使QK (AgI)。
3 sp sp
②一定条件下溶解度小的沉淀也可以转化成溶解度相对较大的沉淀。
重晶石[BaSO(s)]―――――――→BaCO (s),但K (BaSO)②,C错误;b点为试管①加入蒸馏水稀释促进PbI 溶解,平衡正向移动,此时离子积小于溶度积,
2
则Q=c(Pb2+)·c2(I-)1.0×10-5 mol·L-1,所以误饮
4
c(Ba2+)=1.0×10-5 mol·L-1的溶液时,不会引起钡离子中毒,D错误。
三、沉淀转化反应平衡常数的相关计算
5.在湿法炼锌的电解循环溶液中,较高浓度的Cl-会腐蚀阳极而增大电解能耗。可向溶液
中同时加入Cu和CuSO ,生成CuCl沉淀从而除去Cl-。已知:Cu+Cu2+2Cu+ K=
4
7.6×
10-7;K (CuCl)=2.0×10-6。
sp
(1)通过计算说明上述除Cl-的反应能完全进行的原因为________________________。
(2)若用Zn替换Cu可加快除Cl-的速率,但需控制溶液的pH。若pH过低,除Cl-效果下降
的原因是____________________________。
答案 (1)已知:①Cu+Cu2+2Cu+ K=7.6×10-7;②CuCl(s)Cl-(aq)+Cu+(aq)
K =2.0×10-6;则①-2×②得:Cu+Cu2++2Cl-2CuCl,此反应的平衡常数为==
sp
1.9×105,说明此反应进行程度很大,能够完全进行
(2)若pH过低,锌会与溶液中的氢离子反应1.下列判断错误的是________(填字母)。
A.向AgCl、AgBr的饱和溶液中加入少量AgNO,溶液中增加(2016·全国卷Ⅲ,13D)
3
B.向2支盛有2 mL相同浓度银氨溶液的试管中分别加入2滴相同浓度的NaCl和NaI,一
支试管中产生黄色沉淀,另一支中无明显现象,说明 K (AgI)”或“<”)K (Ag S)。
sp sp 2
答案 >
解析 “浸锰”过程中,矿石中的银以Ag S的形式残留于浸锰渣中,MnS发生反应:MnS
2
+2H+===Mn2++HS↑,硫化锰溶于强酸而硫化银不溶于强酸,则可推断:
2
K (MnS)>K (Ag S)。
sp sp 2
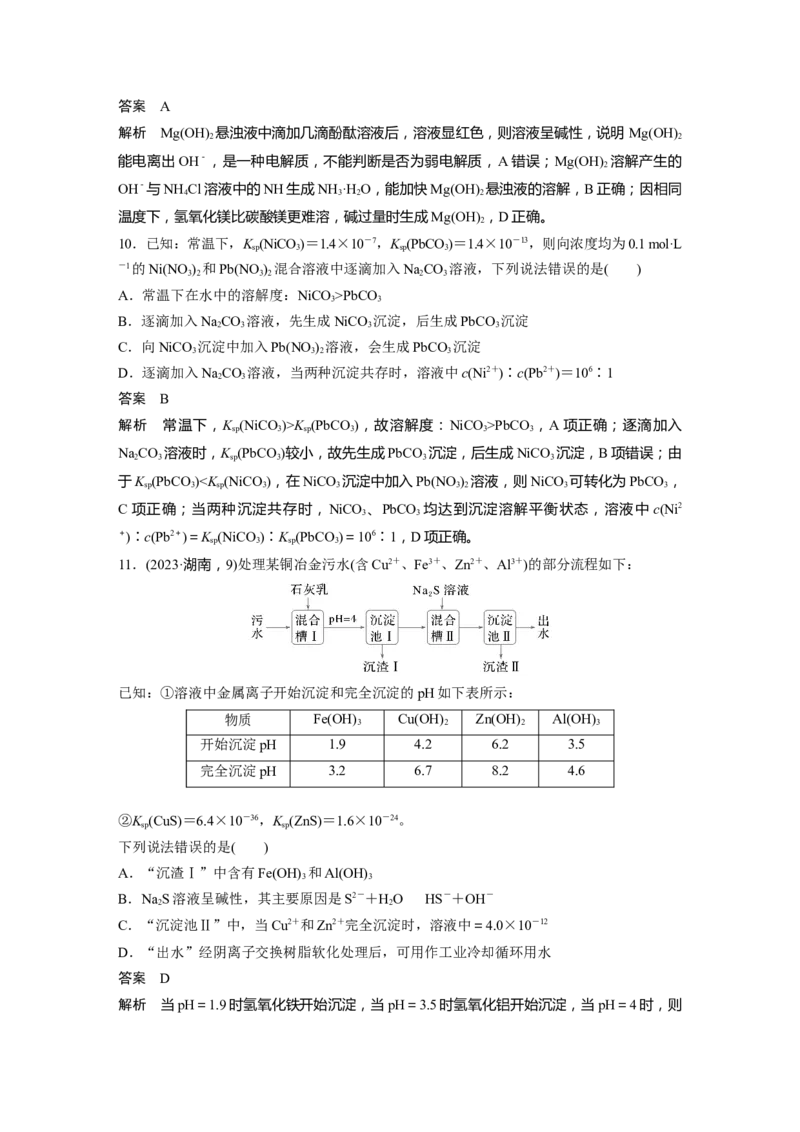
3.[2022·重庆,15(2)]25 ℃时相关的溶度积见表。
化学式 Fe(OH) Cu(OH)
3 2
溶度积 4×10-38 2.5×10-20
①在某滤液中Fe3+和Cu2+的浓度相近,加入NaOH溶液,先得到的沉淀是__________。
②25 ℃时,为了使Cu2+沉淀完全,需调节溶液H+浓度不大于__________ mol·L-1。
答案 ①Fe(OH) ②2×10-7
3
解析 ①由溶度积可知,向某滤液中加入氢氧化钠溶液,氢氧化铁先沉淀。②由溶度积可知,
25 ℃时,铜离子沉淀完全时,溶液中的氢氧根离子浓度为 mol·L-1=5×10-8 mol·L-1,则
溶液中的氢离子浓度不大于2×10-7 mol·L-1。
4.[2022·全国乙卷,26(1)(2)]废旧铅蓄电池的铅膏中主要含有PbSO 、PbO 、PbO和Pb,还
4 2
有少量Ba、Fe、Al的盐或氧化物等,为了保护环境、充分利用铅资源,通过下图流程实现
铅的回收。一些难溶电解质的溶度积常数如下表:
难溶电解质 PbSO PbCO BaSO BaCO
4 3 4 3
K 2.5×10-8 7.4×10-14 1.1×10-10 2.6×10-9
sp
(1)在“脱硫”中PbSO 转化反应的离子方程式为________________________,用沉淀溶解
4
平衡原理解释选择NaCO 的原因:___________________________________________
2 3
________________________________________________________________________。
(2)在“脱硫”中,加入NaCO 不能使铅膏中BaSO 完全转化,原因是_________
2 3 4
________________________________________________________________________。
答案 (1)PbSO (s)+CO(aq)PbCO (s)+SO(aq) 反应 PbSO (s)+CO(aq)PbCO (s)+
4 3 4 3
SO(aq)的平衡常数K===≈3.4×105>105,PbSO 可以比较彻底的转化为PbCO
4 3
(2)反应BaSO(s)+CO(aq)BaCO (s)+SO(aq)的平衡常数K===≈0.04≪105,反应正
4 3
向进行的程度有限
课时精练
1.(2020·全国卷Ⅱ,9)二氧化碳的过量排放可对海洋生物的生存环境造成很大影响,其原理
如下图所示。下列叙述错误的是( )
A.海水酸化能引起HCO浓度增大、CO浓度减小
B.海水酸化能促进CaCO 的溶解,导致珊瑚礁减少
3
C.CO 能引起海水酸化,其原理为HCOH++CO
2
D.使用太阳能、氢能等新能源可改善珊瑚的生存环境
答案 C
解析 二氧化碳能引起海水酸化,其原理为CO+HOHCOH++HCO,C错误。
2 2 2 3
2.(2018·海南,6)某温度下向含AgCl固体的AgCl饱和溶液中加少量稀盐酸,下列说法正确的是( )
A.AgCl的溶解度、K 均减小
sp
B.AgCl的溶解度、K 均不变
sp
C.AgCl的溶解度减小、K 不变
sp
D.AgCl的溶解度不变,K 减小
sp
答案 C
解析 向AgCl饱和溶液中加少量稀盐酸,c(Cl-)增大,导致沉淀溶解平衡AgCl(s)Ag+
(aq)+Cl-(aq)逆向移动,则AgCl的溶解度减小,但温度不变,K 不变。
sp
3.往锅炉注入NaCO 溶液浸泡,将水垢中的CaSO 转化为CaCO ,再用盐酸去除,下列叙
2 3 4 3
述正确的是( )
A.温度升高,NaCO 溶液的K 增大,c(OH-)减小
2 3 w
B.CaSO 能转化为CaCO ,说明K (CaCO)>K (CaSO)
4 3 sp 3 sp 4
C.CaCO 溶于盐酸而CaSO 不溶,是因为硫酸酸性强于盐酸
3 4
D.沉淀转化的离子方程式为CO(aq)+CaSO(s)CaCO (s)+SO(aq)
4 3
答案 D
解析 温度升高,水的电离平衡正向移动,K 增大;温度升高,NaCO 的水解平衡正向移
w 2 3
动,c(OH-)增大,A项错误;K (CaCO)<K (CaSO),B项错误;CaCO 与盐酸反应生成可
sp 3 sp 4 3
溶性的氯化钙、水和二氧化碳,CaSO 与盐酸不满足复分解反应发生的条件,与酸性强弱无
4
关,C项错误。
4.向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成。经查资
料得知:Ag++2NH ·H O[Ag(NH)]++2HO。下列分析不正确的是( )
3 2 3 2 2
A.浊液中存在沉淀溶解平衡:AgCl (s)Ag+(aq)+Cl-(aq)
B.实验可以证明NH 结合Ag+能力比Cl-强
3
C.实验表明实验室可用氨水洗涤银镜反应后的试管
D.由资料信息可推知:加浓硝酸后生成的沉淀为AgCl
答案 C
解析 Ag+与氨分子结合生成二氨合银离子,导致银离子浓度减小,促使 AgCl (s)Ag+
(aq)+Cl-(aq)正向移动,说明NH 结合Ag+能力比Cl-强,B正确;银镜反应后的试管壁上
3
是银单质,银离子能够与氨水反应,银单质不能,C错误;浓硝酸能够中和一水合氨,使
Ag++2NH ·H O[Ag(NH)]++2HO逆向移动,银离子与溶液中的氯离子结合生成沉淀,
3 2 3 2 2
所以加浓硝酸后生成的沉淀为AgCl,D正确。
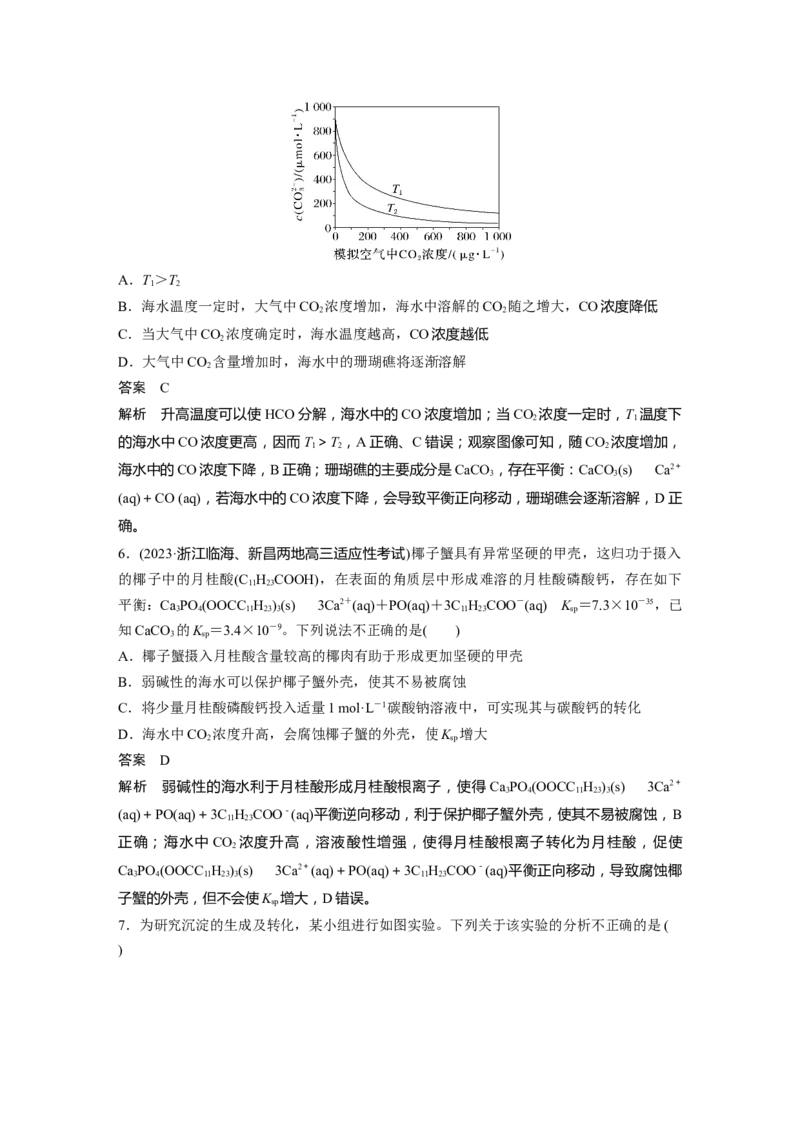
5.大气中CO 含量的增多除了导致地球表面温度升高外,还会影响海洋生态环境。某研究
2
小组在实验室测得不同温度下(T ,T)海水中CO浓度与模拟空气中CO 浓度的关系曲线。
1 2 2
已知:海水中存在以下平衡:CO(aq)+CO(aq)+HO(aq)2HCO(aq),下列说法不正确的
2 2
是( )A.T>T
1 2
B.海水温度一定时,大气中CO 浓度增加,海水中溶解的CO 随之增大,CO浓度降低
2 2
C.当大气中CO 浓度确定时,海水温度越高,CO浓度越低
2
D.大气中CO 含量增加时,海水中的珊瑚礁将逐渐溶解
2
答案 C
解析 升高温度可以使HCO分解,海水中的CO浓度增加;当CO 浓度一定时,T 温度下
2 1
的海水中CO浓度更高,因而T >T ,A正确、C错误;观察图像可知,随CO 浓度增加,
1 2 2
海水中的CO浓度下降,B正确;珊瑚礁的主要成分是CaCO ,存在平衡:CaCO (s)Ca2+
3 3
(aq)+CO (aq),若海水中的CO浓度下降,会导致平衡正向移动,珊瑚礁会逐渐溶解,D正
确。
6.(2023·浙江临海、新昌两地高三适应性考试)椰子蟹具有异常坚硬的甲壳,这归功于摄入
的椰子中的月桂酸(C H COOH),在表面的角质层中形成难溶的月桂酸磷酸钙,存在如下
11 23
平衡:Ca PO (OOCC H )(s)3Ca2+(aq)+PO(aq)+3C H COO-(aq) K =7.3×10-35,已
3 4 11 23 3 11 23 sp
知CaCO 的K =3.4×10-9。下列说法不正确的是( )
3 sp
A.椰子蟹摄入月桂酸含量较高的椰肉有助于形成更加坚硬的甲壳
B.弱碱性的海水可以保护椰子蟹外壳,使其不易被腐蚀
C.将少量月桂酸磷酸钙投入适量1 mol·L-1碳酸钠溶液中,可实现其与碳酸钙的转化
D.海水中CO 浓度升高,会腐蚀椰子蟹的外壳,使K 增大
2 sp
答案 D
解析 弱碱性的海水利于月桂酸形成月桂酸根离子,使得 Ca PO (OOCC H )(s)3Ca2+
3 4 11 23 3
(aq)+PO(aq)+3C H COO-(aq)平衡逆向移动,利于保护椰子蟹外壳,使其不易被腐蚀,B
11 23
正确;海水中 CO 浓度升高,溶液酸性增强,使得月桂酸根离子转化为月桂酸,促使
2
Ca PO (OOCC H )(s)3Ca2+(aq)+PO(aq)+3C H COO-(aq)平衡正向移动,导致腐蚀椰
3 4 11 23 3 11 23
子蟹的外壳,但不会使K 增大,D错误。
sp
7.为研究沉淀的生成及转化,某小组进行如图实验。下列关于该实验的分析不正确的是(
)A.①浊液中存在平衡:AgSCN(s)Ag+(aq)+SCN-(aq)
B.②中颜色变化说明上层清液中含有SCN-
C.③中颜色变化说明有AgI生成
D.该实验可以证明AgI比AgSCN更难溶
答案 D
解析 根据信息,上层清液中存在 SCN-,白色沉淀是 AgSCN,存在沉淀溶解平衡:
AgSCN(s)Ag+(aq)+SCN-(aq),A、B正确;在①中Ag+有剩余,可能是c(I-)·c(Ag+)>
K (AgI),出现沉淀,D错误。
sp
8.牙齿表面存在如下平衡:Ca (PO )OH(s)5Ca2+(aq)+3PO(aq)+OH-(aq) K =6.8×10
5 4 3 sp
-37,Ca (PO )F的K =2.8×10-61。下列说法错误的是( )
5 4 3 sp
A.在牙膏中添加适量的磷酸盐,能起到保护牙齿的作用
B.口腔中的食物残渣能产生有机酸,容易导致龋齿,使K 增大
sp
C.正常口腔的pH接近中性,有利于牙齿健康
D.使用含氟牙膏,当Ca (PO )OH(s)与Ca (PO )F(s)共存时,≈2.4×1024
5 4 3 5 4 3
答案 B
解析 在牙膏中添加适量的磷酸盐,使平衡逆向移动,生成Ca (PO )OH(s)覆盖在牙齿表面,
5 4 3
能起到保护牙齿的作用,A正确;K 只与温度有关,与溶液的酸碱性无关,B错误;==
sp
=≈2.4×1024,D正确。
9.探究Mg(OH) 的沉淀溶解平衡时,利用下表三种试剂进行实验,下列说法不正确的是(
2
)
编号 ① ② ③
分散质 Mg(OH) HCl NH Cl
2 4
备注 悬浊液 1 mol·L-1 1 mol·L-1
A.向①中滴加几滴酚酞溶液后,溶液显红色,说明Mg(OH) 是一种弱电解质
2
B.为了使Mg(OH) 悬浊液溶解得更快,加入过量NH Cl浓溶液并充分振荡,效果更好
2 4
C.①③混合后发生反应:Mg(OH) (s)+2NH(aq)Mg2+(aq)+2NH ·H O(aq)
2 3 2
D.向少量Mg(HCO ) 溶液中加入足量NaOH溶液,反应的离子方程式是Mg2++2HCO+
3 2
4OH-===Mg(OH) ↓+2CO+2HO
2 2答案 A
解析 Mg(OH) 悬浊液中滴加几滴酚酞溶液后,溶液显红色,则溶液呈碱性,说明 Mg(OH)
2 2
能电离出OH-,是一种电解质,不能判断是否为弱电解质,A错误;Mg(OH) 溶解产生的
2
OH-与NH Cl溶液中的NH生成NH ·H O,能加快Mg(OH) 悬浊液的溶解,B正确;因相同
4 3 2 2
温度下,氢氧化镁比碳酸镁更难溶,碱过量时生成Mg(OH) ,D正确。
2
10.已知:常温下,K (NiCO)=1.4×10-7,K (PbCO )=1.4×10-13,则向浓度均为0.1 mol·L
sp 3 sp 3
-1的Ni(NO ) 和Pb(NO ) 混合溶液中逐滴加入NaCO 溶液,下列说法错误的是( )
3 2 3 2 2 3
A.常温下在水中的溶解度:NiCO>PbCO
3 3
B.逐滴加入NaCO 溶液,先生成NiCO 沉淀,后生成PbCO 沉淀
2 3 3 3
C.向NiCO 沉淀中加入Pb(NO ) 溶液,会生成PbCO 沉淀
3 3 2 3
D.逐滴加入NaCO 溶液,当两种沉淀共存时,溶液中c(Ni2+)∶c(Pb2+)=106∶1
2 3
答案 B
解析 常温下,K (NiCO)>K (PbCO ),故溶解度:NiCO>PbCO ,A项正确;逐滴加入
sp 3 sp 3 3 3
NaCO 溶液时,K (PbCO )较小,故先生成PbCO 沉淀,后生成NiCO 沉淀,B项错误;由
2 3 sp 3 3 3
于K (PbCO )