文档内容
太原师院附中师苑中学 2022~2023 学年高三第一次月考
化学试题(理)
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 S-32 Cl-35.5 K-39 Mn-55
Fe-56 Ba-137
一、选择题(每小题只有一个选项符合题意。14-20每小题2分,15-20每小题3分,共46分)
1. 化学与生活密切相关。下列说法错误的是
A. 华为首款5G手机搭载了麒麟980芯片,此芯片主要成分是二氧化硅
的
B. 医用外科口罩 核心功能层聚丙烯熔喷布属于有机高分子材料
C. 将84消毒液和医用酒精混合使用,会降低杀死新冠病毒效果
D. 疫苗必须冷藏存放,其目的是避免疫苗蛋白质变性
2. 下列关于有机物的正确说法是
A. 聚乙烯可发生加成反应
B. 石油干馏可得到汽油、煤油等
C. 淀粉、纤维素互为同分异构体
D. 乙酸乙酯、油脂与NaOH溶液反应均有醇生成。
3. 我国古代四大发明是古代劳动人民智慧的结晶。下列说法错误的是
A. 黑火药爆炸反应为2KNO+3C+S=KS+N↑+3CO ↑,其中氧化剂是KNO 和S
3 2 2 2 3
B. 活字印刷使用的胶泥由Al O、SiO、CaO等组成,它们都属于氧化物
2 3 2
C. 宣纸的主要成分是纤维素,纤维素属于天然高分子化合物
D. 指南针由天然磁石制成,磁石的主要成分是Fe O
2 3
4. 常温下,下列各组离子在指定溶液中能大量共存的是
A. 无色透明的溶液中: 、 、 、
B. 的溶液中:
C. 的溶液中:
D. 能使甲基橙变红的溶液中:
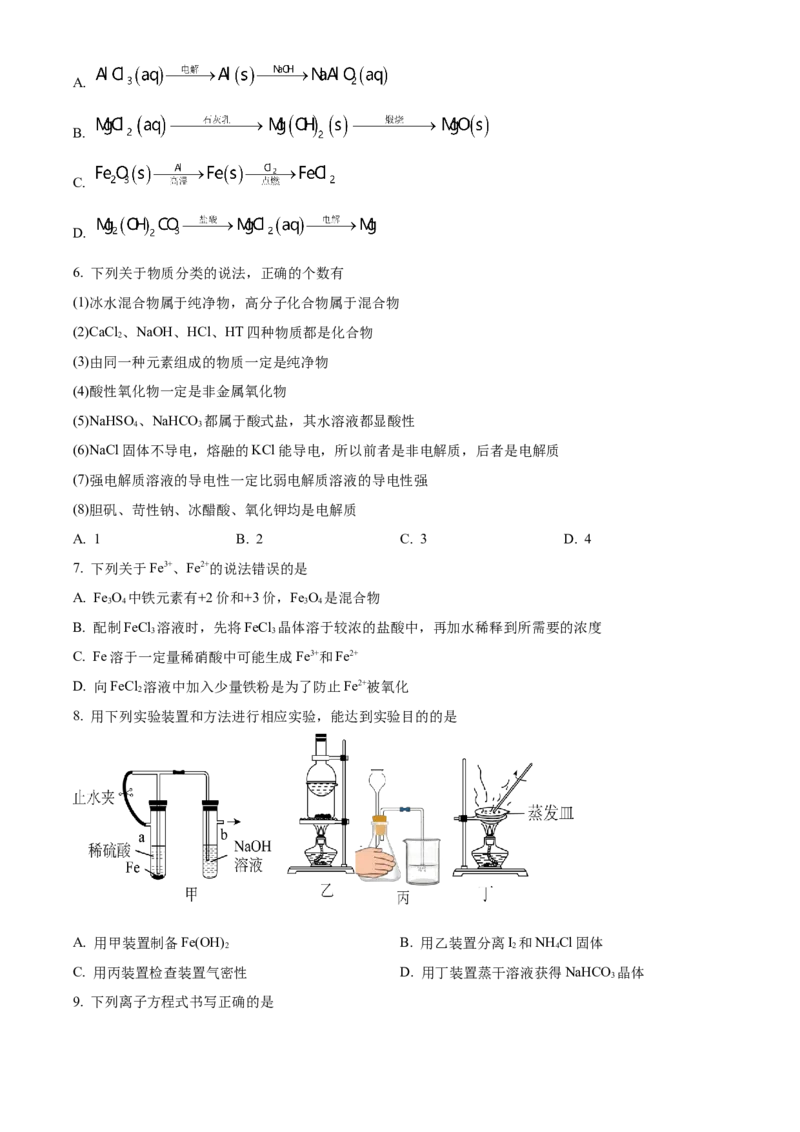
5. 在给定条件下,下列选项所示的物质间转化均能实现的是
下载最新免费模拟卷,到公众号:一枚试卷君A.
B.
C.
D.
6. 下列关于物质分类的说法,正确的个数有
(1)冰水混合物属于纯净物,高分子化合物属于混合物
(2)CaCl 、NaOH、HCl、HT四种物质都是化合物
2
(3)由同一种元素组成的物质一定是纯净物
(4)酸性氧化物一定是非金属氧化物
(5)NaHSO、NaHCO 都属于酸式盐,其水溶液都显酸性
4 3
(6)NaCl固体不导电,熔融的KCl能导电,所以前者是非电解质,后者是电解质
(7)强电解质溶液的导电性一定比弱电解质溶液的导电性强
(8)胆矾、苛性钠、冰醋酸、氧化钾均是电解质
A. 1 B. 2 C. 3 D. 4
7. 下列关于Fe3+、Fe2+的说法错误的是
A. Fe O 中铁元素有+2价和+3价,Fe O 是混合物
3 4 3 4
B. 配制FeCl 溶液时,先将FeCl 晶体溶于较浓的盐酸中,再加水稀释到所需要的浓度
3 3
C. Fe溶于一定量稀硝酸中可能生成Fe3+和Fe2+
D. 向FeCl 溶液中加入少量铁粉是为了防止Fe2+被氧化
2
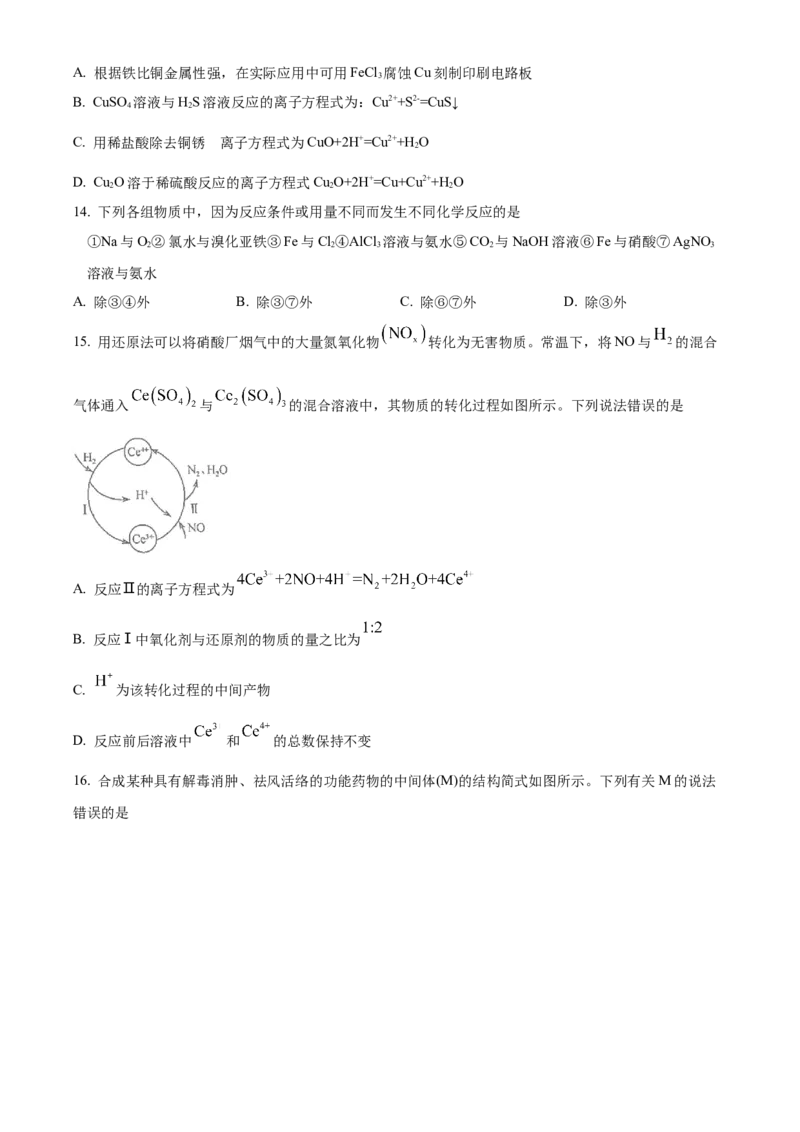
8. 用下列实验装置和方法进行相应实验,能达到实验目的的是
A. 用甲装置制备Fe(OH) B. 用乙装置分离I 和NH Cl固体
2 2 4
C. 用丙装置检查装置气密性 D. 用丁装置蒸干溶液获得NaHCO 晶体
3
9. 下列离子方程式书写正确的是A. 明矾溶液与足量氨水反应:
B. FeI 溶液与足量的Cl 反应:
2 2
C. NaOH和NaCO 等物质的量浓度混合溶液中加足量的盐酸:
2 3
D. 向硫酸铝铵溶液中滴加少量Ba(OH) 溶液:
2
10. 下列实验描述正确的是
A. 向淀粉在稀硫酸作用下的水解液中加入新制Cu(OH) 悬浊液并加热无砖红色沉淀生成,则淀粉未水解
2
B. 将铝锭加入浓硝酸中无明显现象,常温下铝和浓硝酸不反应,可以用铝槽车运输浓硝酸
C. 将金属钠加入CuSO 溶液中有大量红色固体产生,说明金属性钠强于铜
4
D. 草酸溶液和酸性KMnO 溶液混合,KMnO 溶液紫红色褪去,则HC O 还原性强于Mn2+
4 4 2 2 4
11. N 代表阿伏加德罗常数,下列说法中正确的是
A
的
A. 0.1mol/L 溶液中, 数目一定小于0.1N
A
B. 6.6g 分子中含的共用电子对数为0.6N
A
C. 标准状况下,22.4LNO和11.2L 混合后气体的分子总数为N
A
D. 1mol 与足量的 充分反应,转移的电子数为N
A
12. 化学在生产和日常生活中有着重要的应用,下表中用途与其性质或原理对应关系错误的是
选
用途 性质或原理
项
A 葡萄酒中添加适量的SO 起到保质作用 SO 具有杀菌、抗氧化作用
2 2
B 明矾可用作自来水净水剂 Al(OH) 胶体具有吸附性
3
在食品包装袋中放入装有硅胶、铁粉的透气小袋,可防止食物受 硅胶具有吸水性,铁粉具有氧
C
潮、氧化变质 化性
D 用小苏打治疗胃酸过多 NaHCO 可与胃液中的酸反应
3
A. A B. B C. C D. D
13. 下列有关铜的化合物说法正确的是A. 根据铁比铜金属性强,在实际应用中可用FeCl 腐蚀Cu刻制印刷电路板
3
B. CuSO 溶液与HS溶液反应的离子方程式为:Cu2++S2-=CuS↓
4 2
的
C. 用稀盐酸除去铜锈 离子方程式为CuO+2H+=Cu2++H O
2
D. Cu O溶于稀硫酸反应的离子方程式Cu O+2H+=Cu+Cu2++H O
2 2 2
14. 下列各组物质中,因为反应条件或用量不同而发生不同化学反应的是
①Na与O②氯水与溴化亚铁③Fe与Cl④AlCl 溶液与氨水⑤CO 与NaOH溶液⑥Fe与硝酸⑦AgNO
2 2 3 2 3
溶液与氨水
A. 除③④外 B. 除③⑦外 C. 除⑥⑦外 D. 除③外
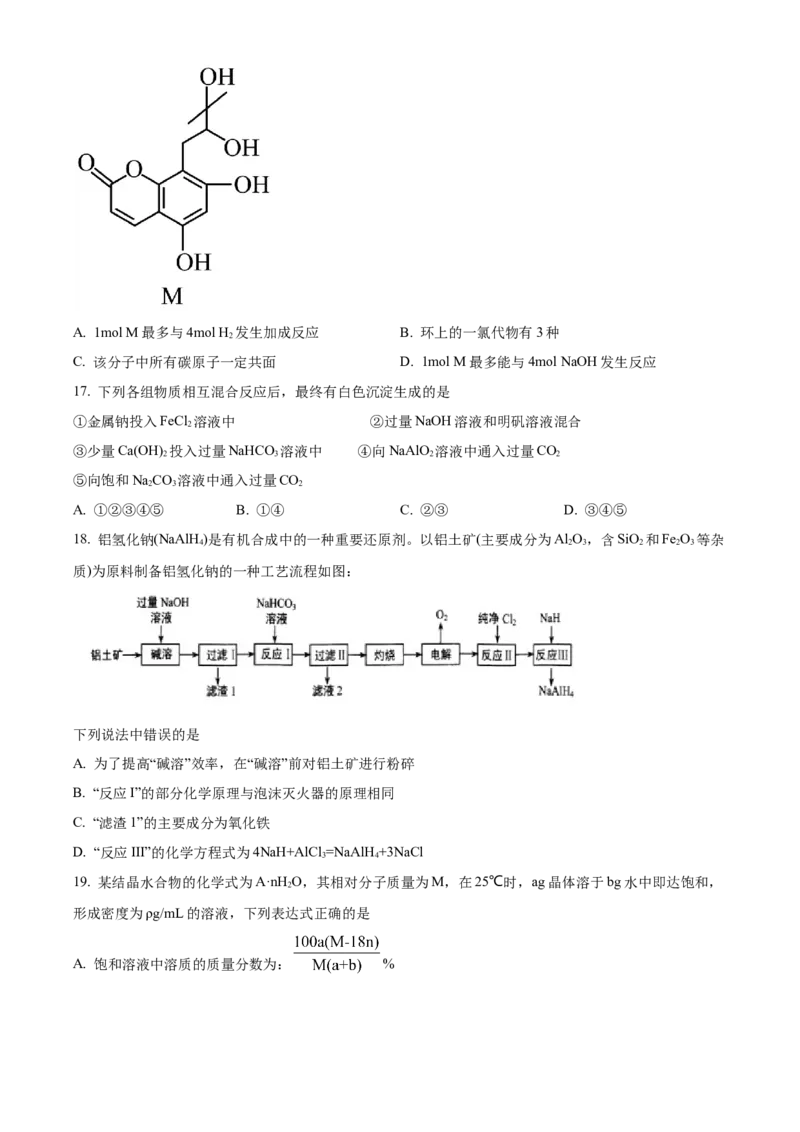
15. 用还原法可以将硝酸厂烟气中的大量氮氧化物 转化为无害物质。常温下,将NO与 的混合
气体通入 与 的混合溶液中,其物质的转化过程如图所示。下列说法错误的是
A. 反应Ⅱ的离子方程式为
B. 反应Ⅰ中氧化剂与还原剂的物质的量之比为
C. 为该转化过程的中间产物
D. 反应前后溶液中 和 的总数保持不变
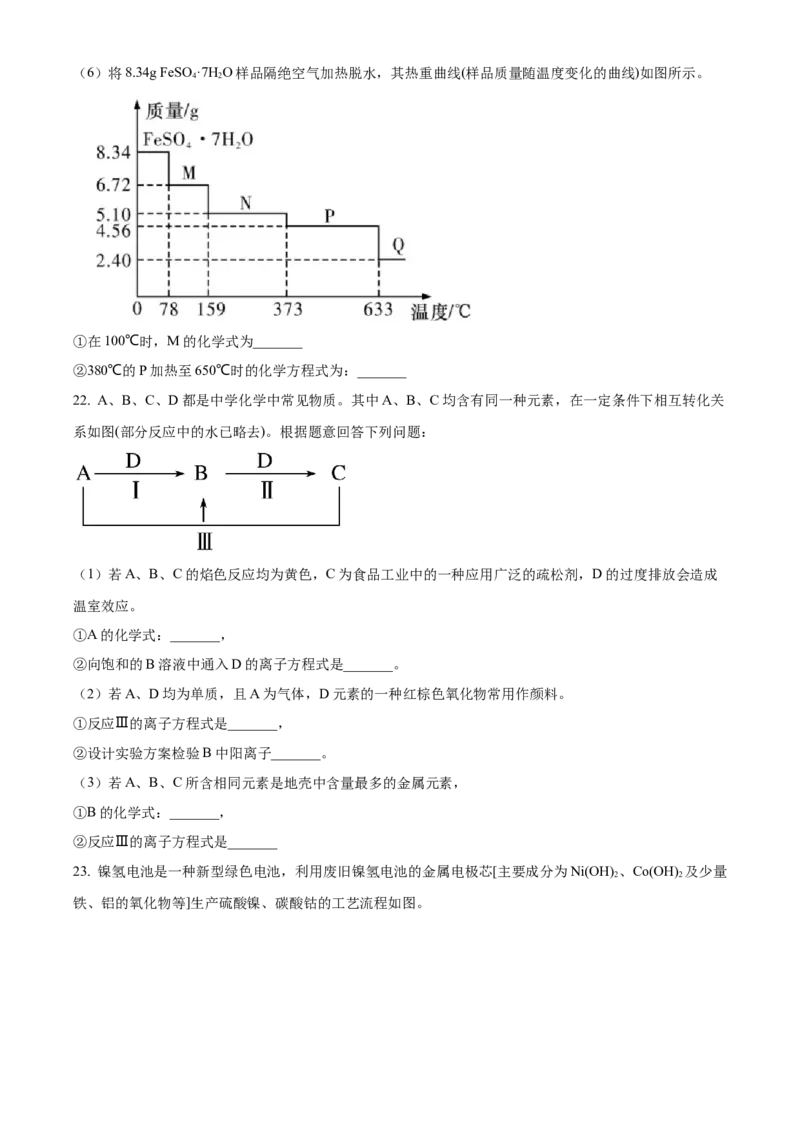
16. 合成某种具有解毒消肿、祛风活络的功能药物的中间体(M)的结构简式如图所示。下列有关M的说法
错误的是A. 1mol M最多与4mol H 发生加成反应 B. 环上的一氯代物有3种
2
C. 该分子中所有碳原子一定共面 D. 1mol M最多能与4mol NaOH发生反应
17. 下列各组物质相互混合反应后,最终有白色沉淀生成的是
①金属钠投入FeCl 溶液中 ②过量NaOH溶液和明矾溶液混合
2
③少量Ca(OH) 投入过量NaHCO 溶液中 ④向NaAlO 溶液中通入过量CO
2 3 2 2
⑤向饱和NaCO 溶液中通入过量CO
2 3 2
A. ①②③④⑤ B. ①④ C. ②③ D. ③④⑤
18. 铝氢化钠(NaAlH )是有机合成中的一种重要还原剂。以铝土矿(主要成分为Al O,含SiO 和Fe O 等杂
4 2 3 2 2 3
质)为原料制备铝氢化钠的一种工艺流程如图:
下列说法中错误的是
A. 为了提高“碱溶”效率,在“碱溶”前对铝土矿进行粉碎
B. “反应I”的部分化学原理与泡沫灭火器的原理相同
C. “滤渣1”的主要成分为氧化铁
D. “反应III”的化学方程式为4NaH+AlCl =NaAlH+3NaCl
3 4
19. 某结晶水合物的化学式为A·nH O,其相对分子质量为M,在25℃时,ag晶体溶于bg水中即达饱和,
2
形成密度为ρg/mL的溶液,下列表达式正确的是
A. 饱和溶液中溶质的质量分数为: %B. 饱和溶液的物质的量浓度为: mol/L
C. 饱和溶液的体积为: L
D. 25℃时,A的溶解度为: g
二、非选择题
20. 完成下列填空:
(1)3.01×1023个氯气分子的物质的量是_______,0.5mol的HO中含有的电子数为_______(用N 表示)。
2 A
(2)同温同压下,同体积的甲烷(CH)和CO 物质的量之比为_______,密度之比为_______。
4 2
的
(3)3.1g Na X含有Na+ 0.1mol,则NaX 摩尔质量为_______,X的相对原子质量为_______。
2 2
(4)在标准状况下,CO和CO 的混合气体共6.72L,质量为12g,则两种气体的物质的量之比为_______,
2
混合气体的平均摩尔质量为_______。
21. 高锰酸钾溶液常用于物质的定性检验与定量分析。
Ⅰ.实验室里欲用KMnO 固体来配制240mL 0.2mol/L的KMnO 溶液。
4 4
(1)计算所需KMnO 固体的质量为_______g。
4
(2)配制溶液时,必须用到的玻璃仪器有烧杯、玻璃棒、量筒、_______、_______。
(3)写出配制溶液时的正确操作顺序(用字母表示,每个字母只能用一次)_______。
A.洗涤 B.称量、溶解 C.转移 D.摇匀 E.定容
(4)配制过程中,下列操作导致溶液浓度偏小的是_______(填序号)。
A. 加水定容时俯视刻度线
B. 容量瓶未干燥处理
C. 定容加水时超过刻度线后,立即吸出多余的水
D. 溶液从烧杯转移到容量瓶中后没有洗涤烧杯
Ⅱ.为了增强高锰酸钾溶液的氧化性,需要加入2mol/L的稀硫酸溶液。现用其测定某补血剂片中亚铁的含
量:称取含FeSO ·7H O的补血剂片a克,充分研磨后溶于水,配成100mL溶液,取25.00mL的该溶液与c
4 2
mol/L的酸性高锰酸钾溶液反应,消耗酸性高锰酸钾溶液25.00mL。上述过程发生反应的化学方程式为
。
(5)则该补血剂中FeSO ·7H O的质量分数为_______(用含a、c的代数式表示)。
4 2(6)将8.34g FeSO ·7H O样品隔绝空气加热脱水,其热重曲线(样品质量随温度变化的曲线)如图所示。
4 2
①在100℃时,M的化学式为_______
②380℃的P加热至650℃时的化学方程式为:_______
22. A、B、C、D都是中学化学中常见物质。其中A、B、C均含有同一种元素,在一定条件下相互转化关
系如图(部分反应中的水已略去)。根据题意回答下列问题:
(1)若A、B、C的焰色反应均为黄色,C为食品工业中的一种应用广泛的疏松剂,D的过度排放会造成
温室效应。
①A的化学式:_______,
②向饱和的B溶液中通入D的离子方程式是_______。
(2)若A、D均为单质,且A为气体,D元素的一种红棕色氧化物常用作颜料。
①反应Ⅲ的离子方程式是_______,
②设计实验方案检验B中阳离子_______。
(3)若A、B、C所含相同元素是地壳中含量最多的金属元素,
①B的化学式:_______,
②反应Ⅲ的离子方程式是_______
23. 镍氢电池是一种新型绿色电池,利用废旧镍氢电池的金属电极芯[主要成分为Ni(OH) 、Co(OH) 及少量
2 2
铁、铝的氧化物等]生产硫酸镍、碳酸钴的工艺流程如图。已知:部分金属阳离子以氢氧化物的形式沉淀时溶液的pH见表:
金属阳离子 Fe2+ Fe3+ Al3+ Ni2+ Co2+
.
开始沉淀时pH 6.3 15 3.4 6.2 7.15
完全沉淀时pH(金属阳离子浓度<10-5mol/L) 9.0 3.2 4.7 9.2 9.15
回答下列问题:
(1)步骤①用稀硫酸浸取金属电极芯前,提高浸取率方法_______(写两种)。
(2)沉淀A的主要成分_______,步骤②调pH的范围为_______。
(3)将“母液1”的pH调至3~4,再加入NaClO,NaClO的作用是_______。
(4)步骤④离子方程式_______,若用盐酸代替HSO 和HO 的混合液也能达到目的,从环保角度分析不
2 4 2 2
采用盐酸的原因:_______。
(5)步骤⑤中“母液3”与NaHCO 溶液反应的离子方程式为_______。
3下载最新免费模拟卷,到公众号:一枚试卷君