文档内容
2022—2023 学年第一学期高三第四次练考化学试题
【本试卷分为选择题和非选择题两部分,共100分。考试时间90分钟】
可能用到的相对原子质量:H-1 C-12 B-11 O-16 P-31 S-32 Ce-140
第Ⅰ卷(选择题 共42分)
一、选择题(每小题3分,共42分。每小题只有一个正确选项,将正确答案填涂在答题卡
上)
1.化学是一门以实验为基础的学科,下列与实验相关的说法中,错误的是
A.滴定管的“0”刻度线在上端,量筒的“0”刻度线在下端
B.球形冷凝管用于冷凝回流时,应竖着使用
C.实验时,若不慎将浓碱沾到皮肤上,应立即用大量水冲洗,然后涂上1%的硼酸
D.应将未用完的钠、钾、白磷等放回原试剂瓶
2.下列物质不能通过化合反应制备的是
A.FeCl B. O C.H O D.Cu (OH) CO
2 3 2 3 2 2 3
3.下列叙述正确的是
NaHC Si
A.甲醇既可发生取代反应也可发生加成反应
B.仅根据碳原子数的多少,即可判断出烷烃的沸点高低
C.用饱和碳酸氢钠溶液可以鉴别乙酸和乙醇
D.戊二烯与环戊烷互为同分异构体
4.假设N 是阿伏伽德罗常数的值,下列说法一定正确的是
A
A.常温常压下,8g O 与O 的混合物中,含有4N 个电子
2 3 A
B.将1mol CH COONa溶于稀醋酸中使溶液呈中性,溶液中CH COO−数目小于N
3 3 A
C.33.6L氯化氢中含有氯原子的数目为1.5N ,则其处于标准状况下
A
D.1L pH=4的0.1mol/L K Cr O 溶液中Cr O2− 离子数为0.1N
2 2 7 2 7 A
5.某无色溶液含有下列离子中的若干种:H+、NH+ 、Fe3+、Ba2+、Al3+、CO2− 、Cl−、
4 3
OH−、NO−
,向该溶液中加入铝粉,只放出H ,则该溶液中能大量存在的离子最多有
3 2
A.4种 B.5种 C.6种 D.7种
6.离子方程式2Ca2++3HCO−+3OH−=2CaCO ↓+CO2−+3H O可以表示
3 3 3 2
A.Ca(HCO ) 与氨水溶液反应 B. O 与澄清石灰水反应
3 2 3
C.Ca(HCO ) 与澄清石灰水反应 D. H O 与澄清石灰水反应
3 2 NaH4C 3
7.已知:2FeSO +6Na O ≜2Na FeO +2Na O+2Na SO +O ↑,则该反应中被氧
4 2 2 2 4 N2 HC 2 4 2
化的Na O 与被FeSO 还原的Na O 的物质的量之比为
2 2 4 2 2A.2:3 B.1:4 C.5:1 D.1:5
8.对乙酰氨基酚paracetamol(扑热息痛),可用于缓解普通感冒或流行性感冒引起的高热以
及缓解轻至中度的疼痛症状。其结构如图所示,下列说法错误的是
A.paracetamol的分子式为C H NO
8 9 2
B.paracetamol的水溶液可与三氯化铁溶液反应,使溶液呈现出蓝紫色
C.paracetamol水溶液在酸、碱性条件下稳定性差,易水解,水解产物为对氨基酚和醋
酸
D.paracetamol是非处方药,其包装上有“OTC”标识,消费者可自行购买和使用
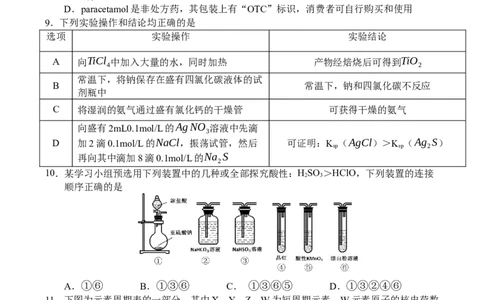
9.下列实验操作和结论均正确的是
选项 实验操作 实验结论
A 向TiCl 中加入大量的水,同时加热 产物经焙烧后可得到TiO
4 2
常温下,将钠保存在盛有四氯化碳液体的试
B 常温下,钠和四氯化碳不反应
剂瓶中
C 将湿润的氨气通过盛有氯化钙的干燥管 可获得干燥的氨气
向盛有2mL0.1mol/L的AgNO 溶液中先滴
3
D 加2滴0.1mol/L的NaCl,振荡试管,然后 可证明:K (AgCl)>K (Ag S)
sp sp 2
再向其中滴加8滴0.1mol/L的Na S
2
10.某学习小组预选用下列装置中的几种或全部探究酸性:HSO >HClO,下列装置的连接
2 3
顺序正确的是
A.①⑥ B.①③⑥ C. ①③⑥⑤ D.①③②④⑥
11.下图为元素周期表的一部分,其中X、Y、Z、W为短周期元素,W元素原子的核电荷数
为X元素的2倍。下列说法正确的是
X
Y Z W
T
A.X、W、Z元素的原子半径及它们的气态氢化物的热稳定性均依次递增
B.Y、Z、W元素在自然界中均不能以游离态存在,它们的最高价氧化物的水化物的酸
性依次递增
C.YX 晶体熔化、液态WX 气化均克服的是分子间作用力
2 3
D.根据元素周期律,可推测T元素的单质具有半导体特性,T X 具有氧化性和还原性
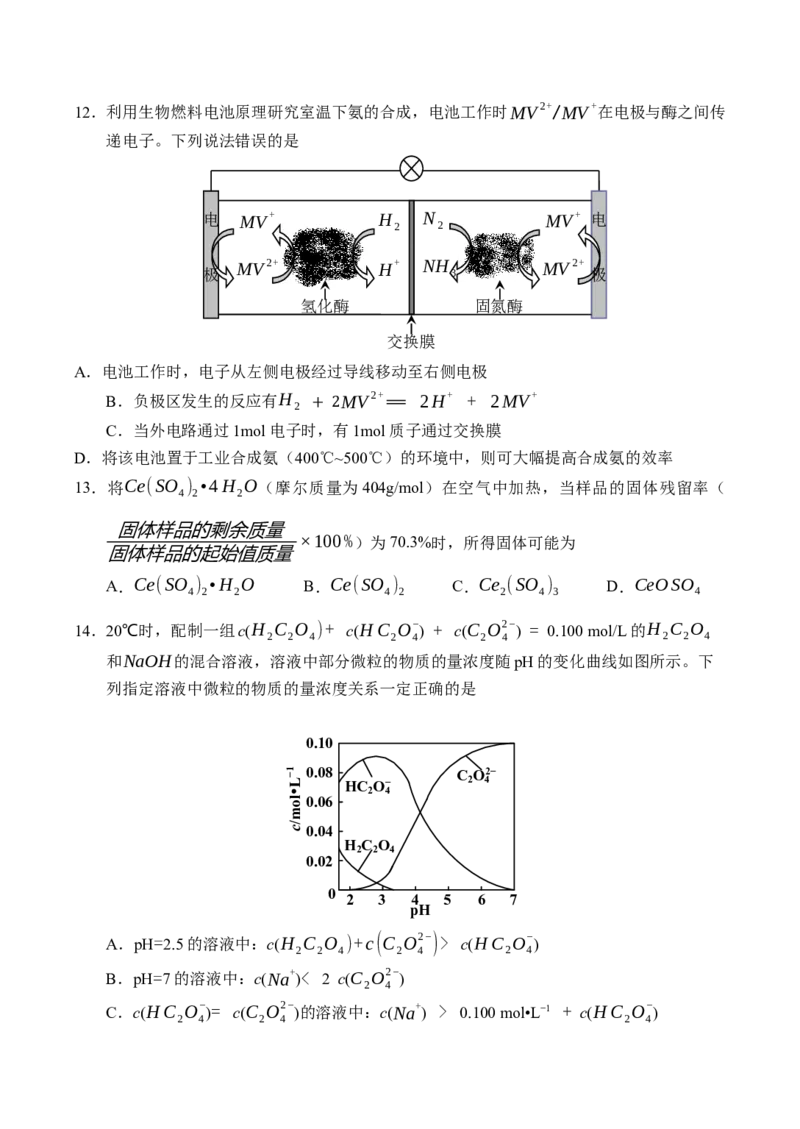
2 312.利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传
递电子。下列说法错误的是
A.电池工作时,电子从左侧电极经过导线移动至右侧电极
B.负极区发生的反应有H MV2+ 2H+ + 2MV+
2
C.当外电路通过1mol电子时,有1mol质子通过交换膜
+ 2 =
D.将该电池置于工业合成氨(400℃~500℃)的环境中,则可大幅提高合成氨的效率
13.将Ce(SO ) •4H O(摩尔质量为404g/mol)在空气中加热,当样品的固体残留率(
4 2 2
固体样品的剩余质量
×100%)为70.3%时,所得固体可能为
固体样品的起始值质量
A.Ce(SO ) •H O B.Ce(SO ) C.Ce (SO ) D.CeOSO
4 2 2 4 2 2 4 3 4
14.20℃时,配制一组c(H C O )+ c(HC O− ) + c(C O2− ) = 0.100 mol/L的H C O
2 2 4 2 4 2 4 2 2 4
和NaOH的混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下
列指定溶液中微粒的物质的量浓度关系一定正确的是
0.10
0.08
0.06
0.04
0.02
0
2 3 4 5 6 7
pH
1−L•lom/c
电 MV+ H N MV+ 电
2 2
MV2+ H+ NH MV2+
极 3 极
氢化酶 固氮酶
交换膜
C O2−
HC O− 2 4
2 4
H C O
2 2 4
A.pH=2.5的溶液中:c(H C O )+c(C O2−)> c(HC O− )
2 2 4 2 4 2 4
B.pH=7的溶液中:c(Na+ )< 2 c(C O2− )
2 4
C.c(HC O− )= c(C O2− )的溶液中:c(Na+ ) > 0.100 mol•L−1 + c(HC O− )
2 4 2 4 2 4D.c(Na+ )=0.100 mol/L的溶液中:c(H+ ) + c(H C O )=c(OH−) + c(C O2− )
2 2 4 2 4
第Ⅱ卷(非选择题 共58分)
二、非选择题
15.(14分)以硅藻土为载体的五氧化二钒(V O )是接触法生成硫酸的催化剂。从废钒催化
2 5
剂中回收V O 既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
2 5
物质 VO VO KSO SiO Fe O Al O
2 5 2 4 2 4 2 2 3 2 3
质量分数/% 2.2~2.9 2.8~3.1 22~28 60~65 1~2 <1
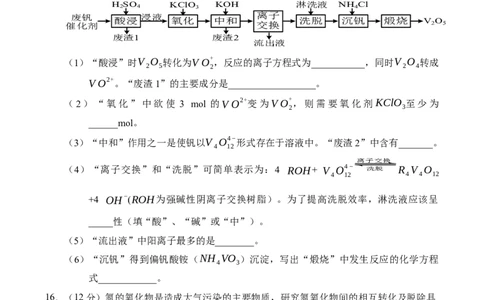
以下是一种废钒催化剂回收工艺路线:回答下列问题:
H 2 SO 4 KClO 3 KOH 淋洗液 NH 4 Cl
废钒 浸液 离子
酸浸 氧化 中和 洗脱 沉钒 煅烧 V O
催化剂 交换 2 5
废渣1 废渣2
流出液
(1)“酸浸”时V O 转化为V O+ ,反应的离子方程式为___________,同时V O 转成
2 5 2 2 4
V O2+。“废渣1”的主要成分是__________________。
(2)“氧化”中欲使 3 mol 的V O2+变为V O+ ,则需要氧化剂 KClO 至少为
2 3
______mol。
(3)“中和”作用之一是使钒以V O4−形式存在于溶液中。“废渣2”中含有_______。
4 12
离子交换
(4)“离子交换”和“洗脱”可简单表示为:4 ROH+ V O4− 洗脱 R V O
4 12 4 4 12
+4 OH−(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈
_____性(填“酸”、“碱”或“中”)。
(5)“流出液”中阳离子最多的是________。
(6)“沉钒”得到偏钒酸铵(NH VO )沉淀,写出“煅烧”中发生反应的化学方程
4 3
式____________。
16.(12分)氮的氧化物是造成大气污染的主要物质,研究氮氧化物间的相互转化及脱除具
有重要意义。
I.氮氧化物间的相互转化
(1)已知2NO(g)+O (g) 2NO (g)的反应历程分两步:
2 2
第一步 2NO(g) ⇌ ⇌N 2 O 2 (g) (快速平衡)
第二步 N
2
O
2
(g)+O
2
(g) ⇌2NO
2
(g) (慢反应)
①用O 表示的速率方程为v(O )=k c2(NO)·c(O );
2 2 1· 2NO 表示的速率方程为v(NO )=k c2(NO)·c(O ),k 与k 分别表示速率常数,则
2 2 2· 2 1 2
k/k =________。
1 2
②下列关于反应2NO(g)+O (g)=2NO (g)的说法正确的是_________(填序号)。
2 2
A.增大压强,反应速率常数一定增大
B.第一步反应的活化能小于第二步反应的活化能
C.反应的总活化能等于第一步和第二步反应的活化能之和
(2)2NO (g) N O (g)(△H<0),用分压(某组分的分压等于总压与其物质的量分数
2 2 4
的积)表⇌示的平衡常数K 与1/T (T为温度)的关系
P
lgKp
如图。 a
①能正确表示lgK 与1/T关系的曲线是________
P
b
(填“a”或“b”)。
1/T
②298K时,在体积固定的密闭容器中充入一定量
的NO ,平衡时NO 的分压为100kPa。已知K =2.7×10-3 kPa-1,则NO 的转
2 2 P 2
化率为__________。(取整数)
II.烟气中氮氧化物的脱除
(3)以NH 为还原剂在脱硝装置中消除烟气中的氮氧化物。
3
主反应:4NH (g)+4NO(g)+O (g) = 4N (g)+6H O(g) △H
3 2 2 2 1
副反应:4NH (g)+3O (g) = 2N (g)+6H O(g) △H =-1267.1kJ/mol
3 2 2 2 2
4NH (g)+5O (g)=4NO(g)+6H O(g) △H =-907.3 kJ/mol
3 2 2 3
请计算△H =____________。
1
(4)以连二亚硫酸盐(S O2-)为还原剂脱除烟气中的NO,并通过电解再生,装置如下图。
2 4阴极的电极反应式为 ,电解槽中的隔膜为_______(填“阳
离子”或“阴离子”)交换膜。
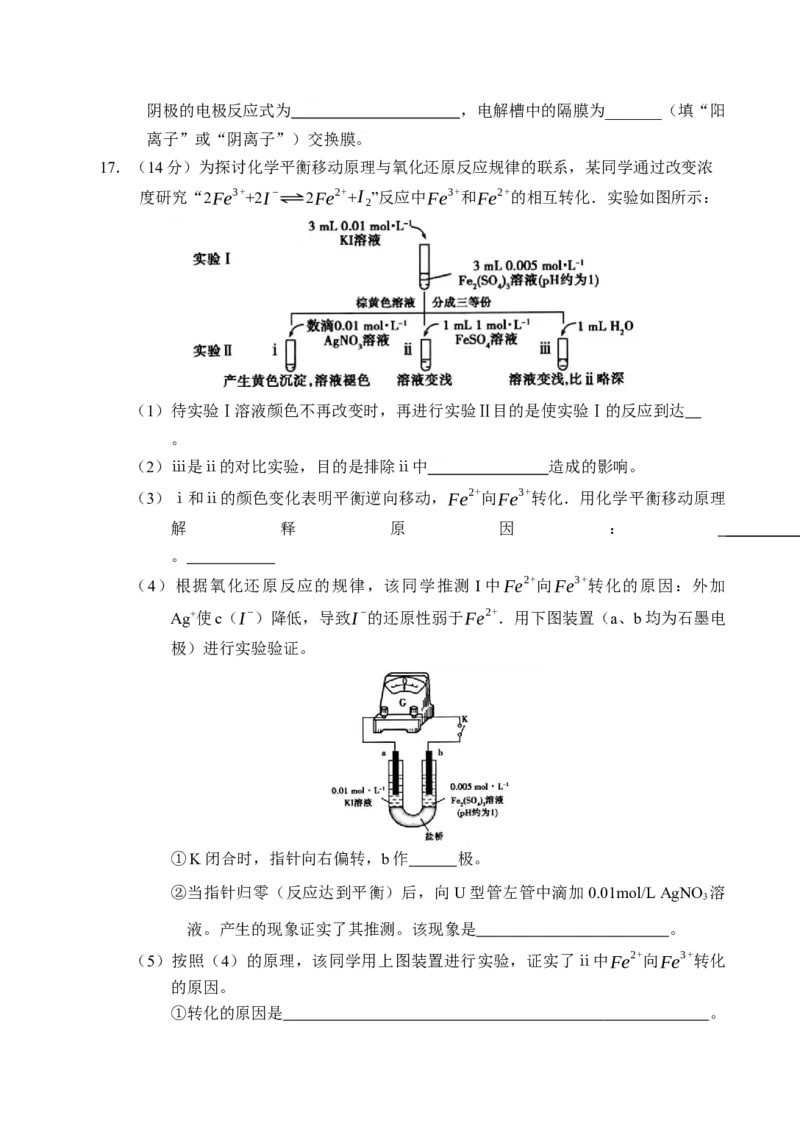
17.(14分)为探讨化学平衡移动原理与氧化还原反应规律的联系,某同学通过改变浓
度研究“2Fe3+ +2I− 2Fe2+ +I ”反应中Fe3+和Fe2+的相互转化.实验如图所示:
2
⇌
(1)待实验Ⅰ溶液颜色不再改变时,再进行实验Ⅱ目的是使实验Ⅰ的反应到达
。
(2)ⅲ是ⅱ的对比实验,目的是排除ⅱ中 造成的影响。
(3)ⅰ和ⅱ的颜色变化表明平衡逆向移动,Fe2+向Fe3+转化.用化学平衡移动原理
解 释 原 因 :
。
(4)根据氧化还原反应的规律,该同学推测 I中Fe2+向Fe3+转化的原因:外加
Ag+使c(I−)降低,导致I−的还原性弱于Fe2+.用下图装置(a、b均为石墨电
极)进行实验验证。
①K闭合时,指针向右偏转,b作 极。
②当指针归零(反应达到平衡)后,向U型管左管中滴加0.01mol/L AgNO 溶
3
液。产生的现象证实了其推测。该现象是 。
(5)按照(4)的原理,该同学用上图装置进行实验,证实了ⅱ中Fe2+向Fe3+转化
的原因。
①转化的原因是 。②与(4)实验对比,不同的操作是 。
(6)实验Ⅰ中,还原性:I−>Fe2+;而实验Ⅱ中,还原性Fe2+>I−.将(3)和
(4)、(5)作对比,得出的结论是 。
18.(8分)晶体的特殊性质是科学家不断研究和探索的新领域,根据你对晶体的认识,
回答下列问题。
(1)一种发光二极管的半导体材料为GaAs P ,该化合物中Ga、As、P的电负性从
x 1-x
大到小的顺序为 。
(2)下表列出了钠的卤化物和硅的卤化物的熔点:
NaX NaF NaCl NaBr NaI
熔点/℃ 995 801 775 651
SiX SiF SiCl SiBr SiI
4 4 4 4 4
熔点/℃ -90.2 -70.4 5.2 120.5
从表中可以看出,钠的卤化物的熔点比相应的硅的卤化物的熔点高很多,请用所
学知识简单解释: 。
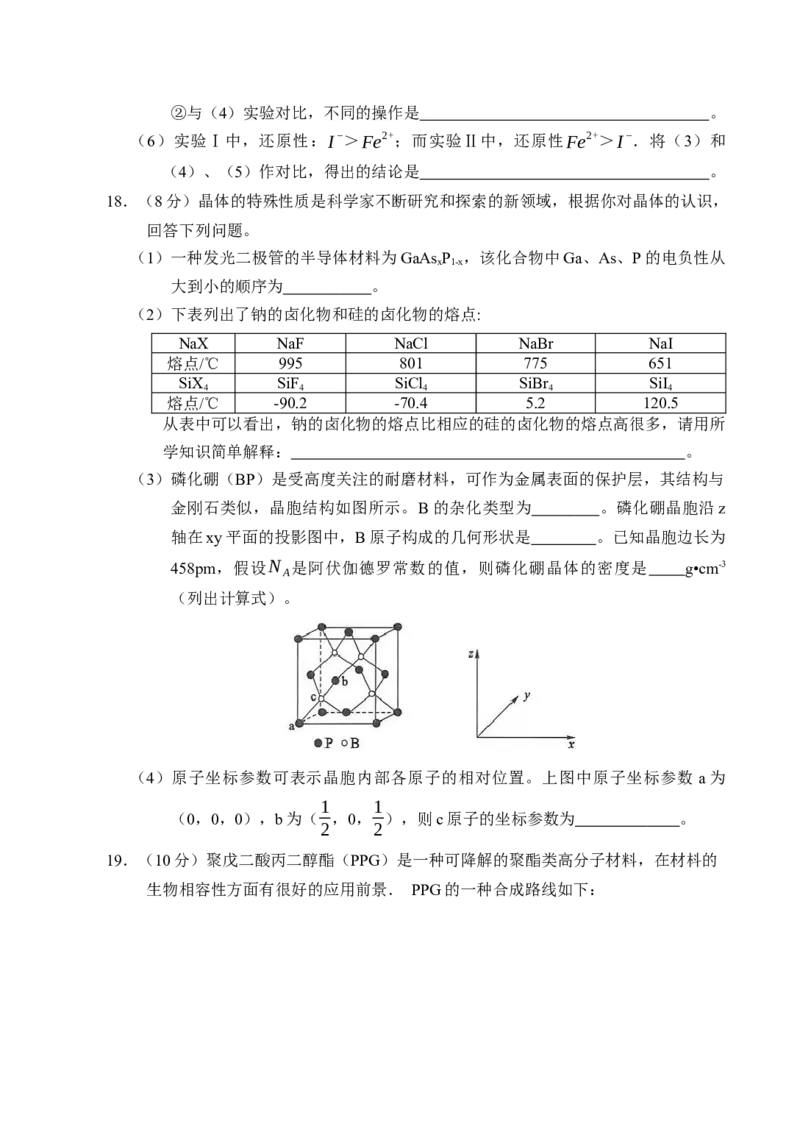
(3)磷化硼(BP)是受高度关注的耐磨材料,可作为金属表面的保护层,其结构与
金刚石类似,晶胞结构如图所示。B的杂化类型为 。磷化硼晶胞沿z
轴在xy平面的投影图中,B原子构成的几何形状是 。已知晶胞边长为
458pm,假设N 是阿伏伽德罗常数的值,则磷化硼晶体的密度是 g•cm-3
A
(列出计算式)。
(4)原子坐标参数可表示晶胞内部各原子的相对位置。上图中原子坐标参数 a为
1 1
(0,0,0),b为( ,0, ),则c原子的坐标参数为 。
2 2
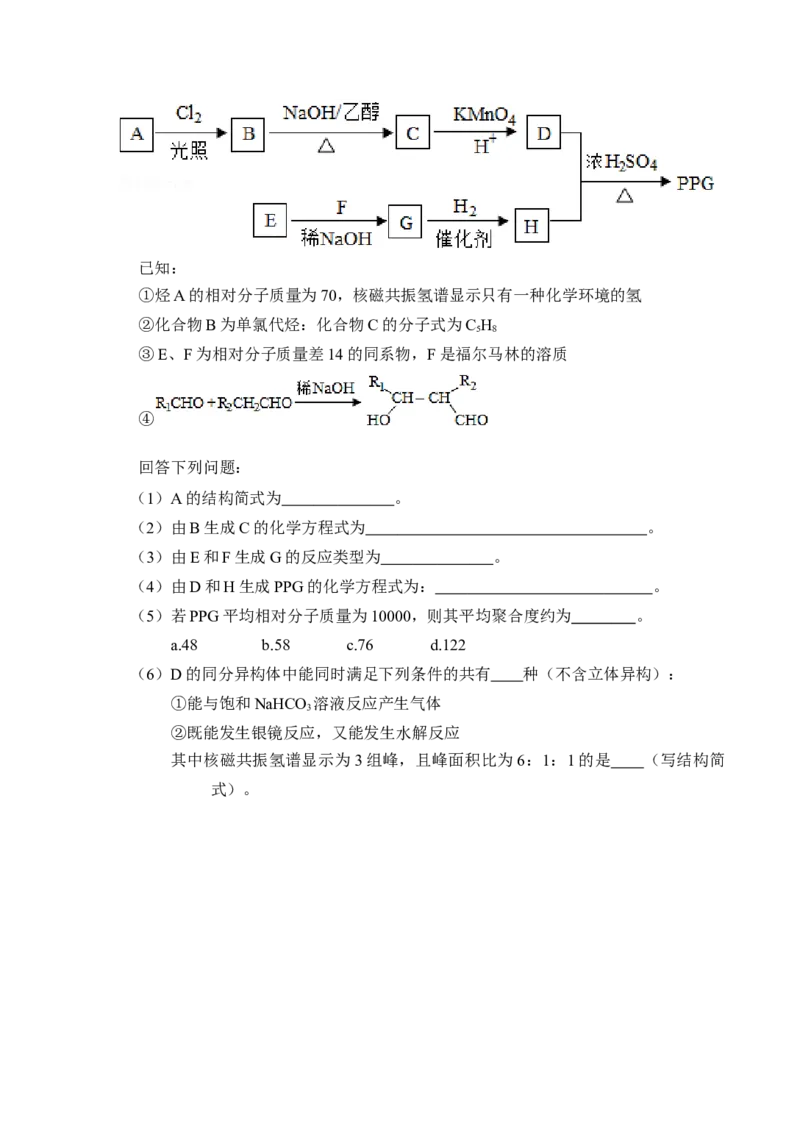
19.(10分)聚戊二酸丙二醇酯(PPG)是一种可降解的聚酯类高分子材料,在材枓的
生物相容性方面有很好的应用前景. PPG的一种合成路线如下:已知:
①烃A的相对分子质量为70,核磁共振氢谱显示只有一种化学环境的氢
②化合物B为单氯代烃:化合物C的分子式为C H
5 8
③E、F为相对分子质量差14的同系物,F是福尔马林的溶质
④
回答下列问题:
(1)A的结构简式为 。
(2)由B生成C的化学方程式为 。
(3)由E和F生成G的反应类型为 。
(4)由D和H生成PPG的化学方程式为: 。
(5)若PPG平均相对分子质量为10000,则其平均聚合度约为 。
a.48 b.58 c.76 d.122
(6)D的同分异构体中能同时满足下列条件的共有 种(不含立体异构):
①能与饱和NaHCO 溶液反应产生气体
3
②既能发生银镜反应,又能发生水解反应
其中核磁共振氢谱显示为3组峰,且峰面积比为6:1:1的是 (写结构简
式)。化学答案
一、选择题
1 2 3 4 5 6 7 8 9 10
A C C A B B B C A D
11 12 13 14
D D C D
二、非选择题
15.(14分,每空2分)
(1)VO+2H+=2VO ++H O SiO (2)0.5 (3)Fe(OH) 和Al(OH) (4)碱 (5)K+
2 5 2 2 2 3 3
△
(6)2NH VO VO+2NH↑+H O↑
4 3 2 5 3 2
16.(12分)
(1) ① 1/2 (2分) ② B(2分) (2) ① a(1分) ②35%(2分)
(3) -1626.9kJ/mol(2分) (4) 2SO2- + 2e- + 4H+ = S O2- + 2H O(2分) 阳离子(1分)
3 2 4 2
17.(14分)
(1)化学平衡状态; (1分) (2)溶液稀释对颜色变化; (1分)
(3)ⅰ中Ag+与I﹣生成AgI黄色沉淀,I﹣浓度降低,2Fe3++2I﹣ 2Fe2++I 平衡逆向移动;
2
ⅱ中加入FeSO ,Fe2+浓度增大,平衡逆移; (2分)
4 ⇌
(4)①正;(2分) ②左管出现黄色沉淀,指针向左偏转;(2分)
(5)Fe2+浓度增大,还原性增强,使Fe2+还原性强于I﹣;(2分)
向U型管右管中滴加1mol/L FeSO 溶液;(2分)
4
(6)该反应为可逆的氧化还原反应,在平衡时,通过改变物质的浓度,可以改变物质的氧化、
还原能力,并影响平衡移动。(2分)
18.(8分)
(1)P>As>Ga (1分)
(2)钠的卤化物是离子晶体,而硅的卤化物是分子晶体,离子键的强度比分子间的范德华力
更强,因此熔点更高。 (2分)
(3)sp3 (1分) 正方形(1分) 4x42 (2分)
(458x10−10))3xN
A
1 1 1
(4)( , , ) (1分)
4 4 4
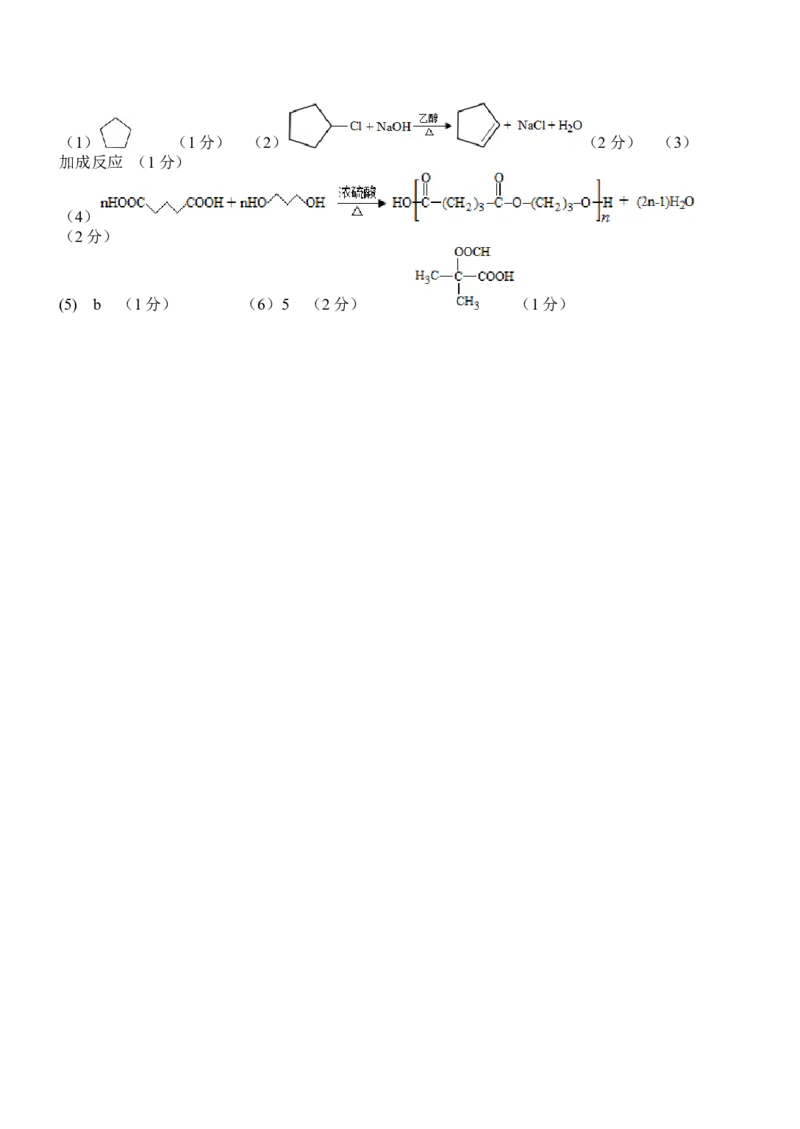
19.(10分)(1) (1分) (2) (2分) (3)
加成反应 (1分)
(4)
(2分)
(5) b (1分) (6)5 (2分) (1分)