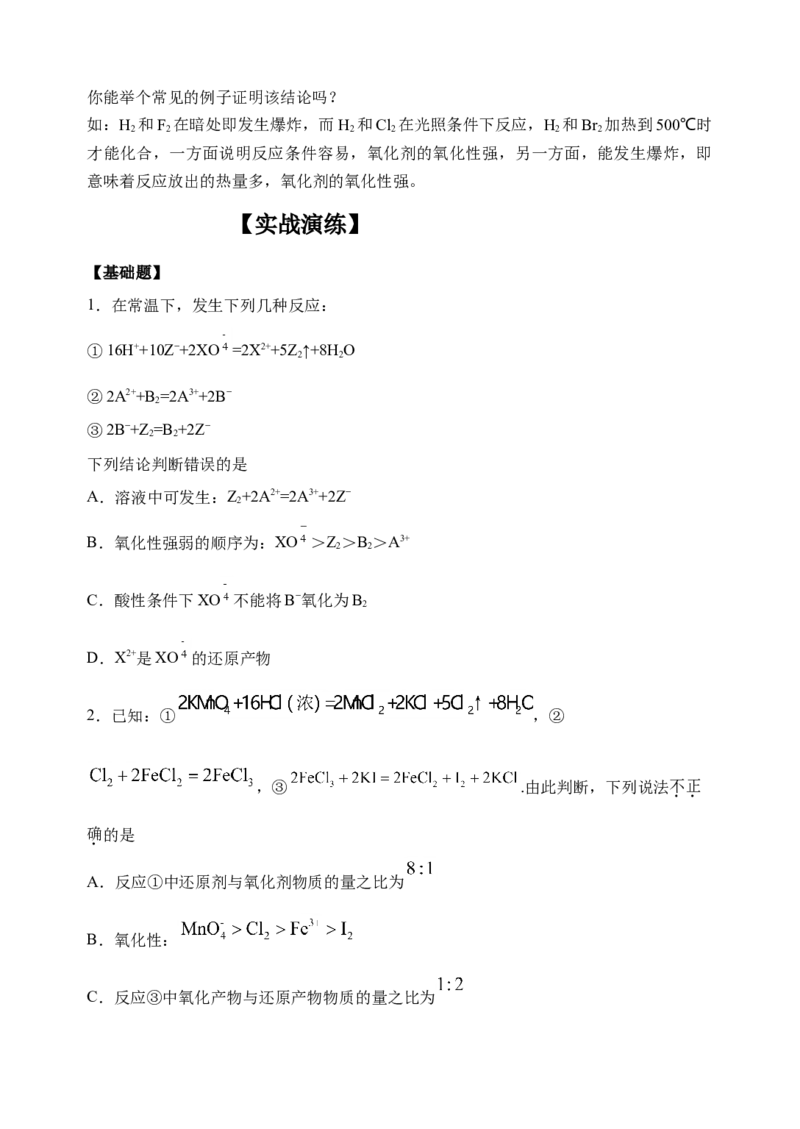文档内容
微专题 07 氧化性和还原性强弱的实验探究及应用
氧氧化化性性和和还还原原性性的的强强弱弱比比较较
方法一、依据反应原理判断
氧化还原反应总是遵循以下规律(简称强弱律):
氧化性:氧化剂>氧化产物,氧化剂>还原剂;
还原性:还原剂>还原产物,还原剂>氧化剂。
方法二、根据“三表”来判断
(1)根据元素在周期表中的相对位置判断
(2)依据金属活动性顺序表判断
(3)依据非金属活动性顺序表判断
方法三、依据“两池”判断
(1)两种不同的金属构成原电池的两极。负极金属是电子流出的极,正极金属是电子流
入的极。其还原性:负极>正极。(2)用惰性电极电解混合溶液时,在阴极先放电的阳离子的氧化性较强,在阳极先放电
的阴离子的还原性较强。在阳极阴离子放电顺序:S2−>I−>Br−>Cl−>OH−,即是还原性强弱
顺序。在阴极阳离子放电顺序:
Ag+>Hg2+>Fe3+>Cu2+>H+>Pb2+>Sn2+>Zn2+>Al3+>Mg2+>Na+>Ca2+>K+,即是氧化性强弱顺序。
方法四、依据与同一物质反应的情况(反应条件、剧烈程度等)判断。
当不同的氧化剂作用于同一还原剂时,若氧化产物价态相同,可根据反应条件高、低来
进行判断,反应条件越低,性质越强;若氧化产物价态不同,则价态越高,氧化剂的氧
化性越强。
方法五、根据物质中元素的化合价判断。
(1)一般来讲,同一种元素的化合价越高,氧化性越强,价态越低,还原性越强。如:
氧化性:浓HSO > H SO ;还原性:HS> SO 。又如氧化性:Fe3+> Fe2+> Fe,还原性反
2 4 2 3 2 2
之。
(2)在和同一种氧化剂(或还原剂)反应时,氧化剂(或还原剂)被还原(或氧化)的程度越大,
即是化合价降低(或升高)越多,还原剂(或氧化剂)的还原性(或氧化性)就越强。如Fe和
Cl 反应生成FeCl ,而Fe和S反应只生成FeS,则氧化性:Cl>S。
2 3 2
方法六、依据“三度”判断(“三度”即:温度、浓度、酸碱度)
(1)一般浓度越大,氧化性(或还原性)越强。如氧化性:浓HSO >稀HSO ,浓HNO>
2 4 2 4 3
稀HNO。
3
(2)一般温度越高,氧化性(或还原性)越强。如常温下浓HSO 和Cu反应放出缓慢,而
2 4
加热条件下浓HSO 氧化性增强,两者反应速率加快。
2 4
(3)一般是溶液的酸性越强,氧化性(或还原性)越强。如KMnO 是一种强氧化剂,而在
4
NO
酸、中、碱性溶液中,其氧化性强弱顺序是:酸性>中性>碱性。又如 3的氧化性也随
着H+浓度的增大而增强。
方法七、依据反应中能量变化判断
H+X===2HX ΔH<0
2 2 1
H+Y===2HY ΔH<0
2 2 2
若ΔH<ΔH,则X 的氧化性比Y 的氧化性强;X-的还原性比Y-的还原性弱。
1 2 2 2你能举个常见的例子证明该结论吗?
如:H 和F 在暗处即发生爆炸,而H 和Cl 在光照条件下反应,H 和Br 加热到500℃时
2 2 2 2 2 2
才能化合,一方面说明反应条件容易,氧化剂的氧化性强,另一方面,能发生爆炸,即
意味着反应放出的热量多,氧化剂的氧化性强。
【实战演练】
【基础题】
1.在常温下,发生下列几种反应:
①16H++10Z−+2XO =2X2++5Z↑+8H O
2 2
②2A2++B =2A3++2B−
2
③2B−+Z=B +2Z−
2 2
下列结论判断错误的是
A.溶液中可发生:Z+2A2+=2A3++2Z−
2
B.氧化性强弱的顺序为:XO >Z>B >A3+
2 2
C.酸性条件下XO 不能将B−氧化为B
2
D.X2+是XO 的还原产物
2.已知:① ,②
,③ .由此判断,下列说法不正
确的是
A.反应①中还原剂与氧化剂物质的量之比为
B.氧化性:
C.反应③中氧化产物与还原产物物质的量之比为D.反应 不能发生
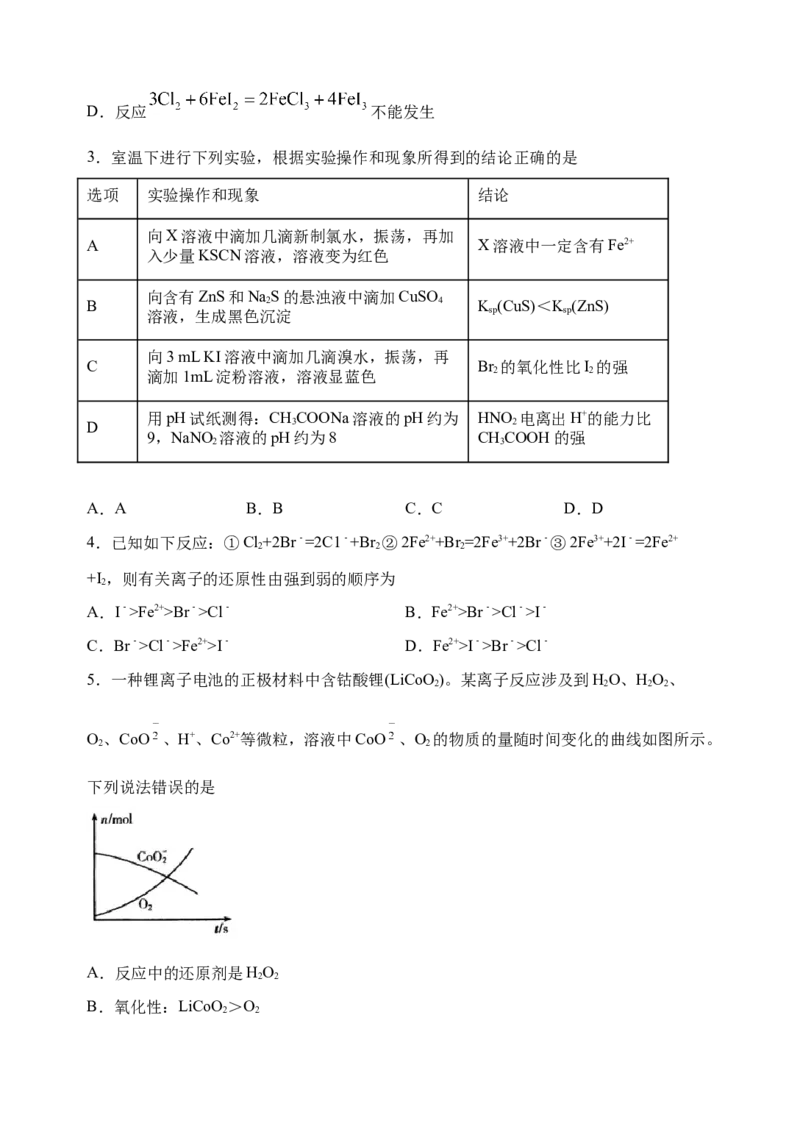
3.室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
选项 实验操作和现象 结论
向X溶液中滴加几滴新制氯水,振荡,再加
A X溶液中一定含有Fe2+
入少量KSCN溶液,溶液变为红色
向含有ZnS和NaS的悬浊液中滴加CuSO
B 2 4 K (CuS)<K (ZnS)
溶液,生成黑色沉淀 sp sp
向3 mL KI溶液中滴加几滴溴水,振荡,再
C Br 的氧化性比I 的强
滴加1mL淀粉溶液,溶液显蓝色 2 2
用pH试纸测得:CHCOONa溶液的pH约为 HNO 电离出H+的能力比
D 3 2
9,NaNO 溶液的pH约为8 CHCOOH的强
2 3
A.A B.B C.C D.D
4.已知如下反应:①Cl+2Br﹣=2C1﹣+Br ②2Fe2++Br =2Fe3++2Br﹣③2Fe3++2I﹣=2Fe2+
2 2 2
+I ,则有关离子的还原性由强到弱的顺序为
2
A.I﹣>Fe2+>Br﹣>Cl﹣ B.Fe2+>Br﹣>Cl﹣>I﹣
C.Br﹣>Cl﹣>Fe2+>I﹣ D.Fe2+>I﹣>Br﹣>Cl﹣
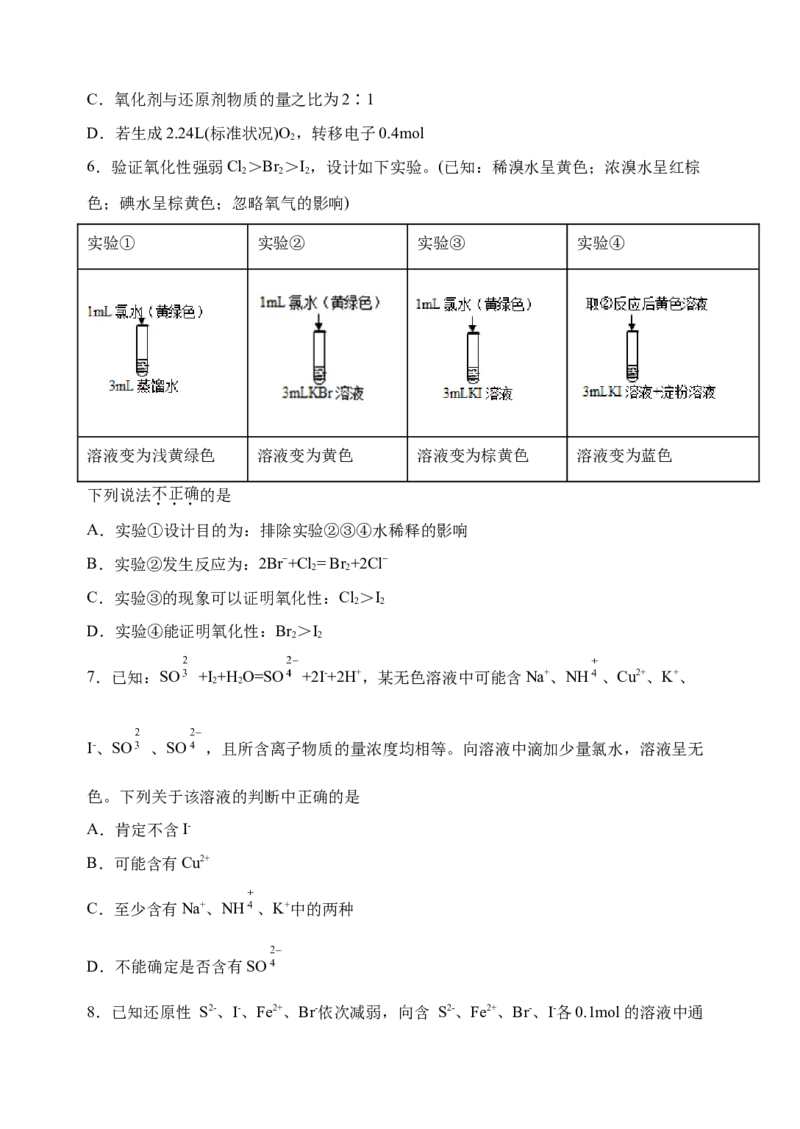
5.一种锂离子电池的正极材料中含钴酸锂(LiCoO )。某离子反应涉及到HO、HO、
2 2 2 2
O、CoO 、H+、Co2+等微粒,溶液中CoO 、O 的物质的量随时间变化的曲线如图所示。
2 2
下列说法错误的是
A.反应中的还原剂是HO
2 2
B.氧化性:LiCoO >O
2 2C.氧化剂与还原剂物质的量之比为2∶1
D.若生成2.24L(标准状况)O ,转移电子0.4mol
2
6.验证氧化性强弱Cl>Br >I,设计如下实验。(已知:稀溴水呈黄色;浓溴水呈红棕
2 2 2
色;碘水呈棕黄色;忽略氧气的影响)
实验① 实验② 实验③ 实验④
溶液变为浅黄绿色 溶液变为黄色 溶液变为棕黄色 溶液变为蓝色
下列说法不正确的是
A.实验①设计目的为:排除实验②③④水稀释的影响
B.实验②发生反应为:2Br−+Cl= Br+2Cl−
2 2
C.实验③的现象可以证明氧化性:Cl>I
2 2
D.实验④能证明氧化性:Br >I
2 2
7.已知:SO +I +H O=SO +2I-+2H+,某无色溶液中可能含Na+、NH 、Cu2+、K+、
2 2
I-、SO 、SO ,且所含离子物质的量浓度均相等。向溶液中滴加少量氯水,溶液呈无
色。下列关于该溶液的判断中正确的是
A.肯定不含I-
B.可能含有Cu2+
C.至少含有Na+、NH 、K+中的两种
D.不能确定是否含有SO
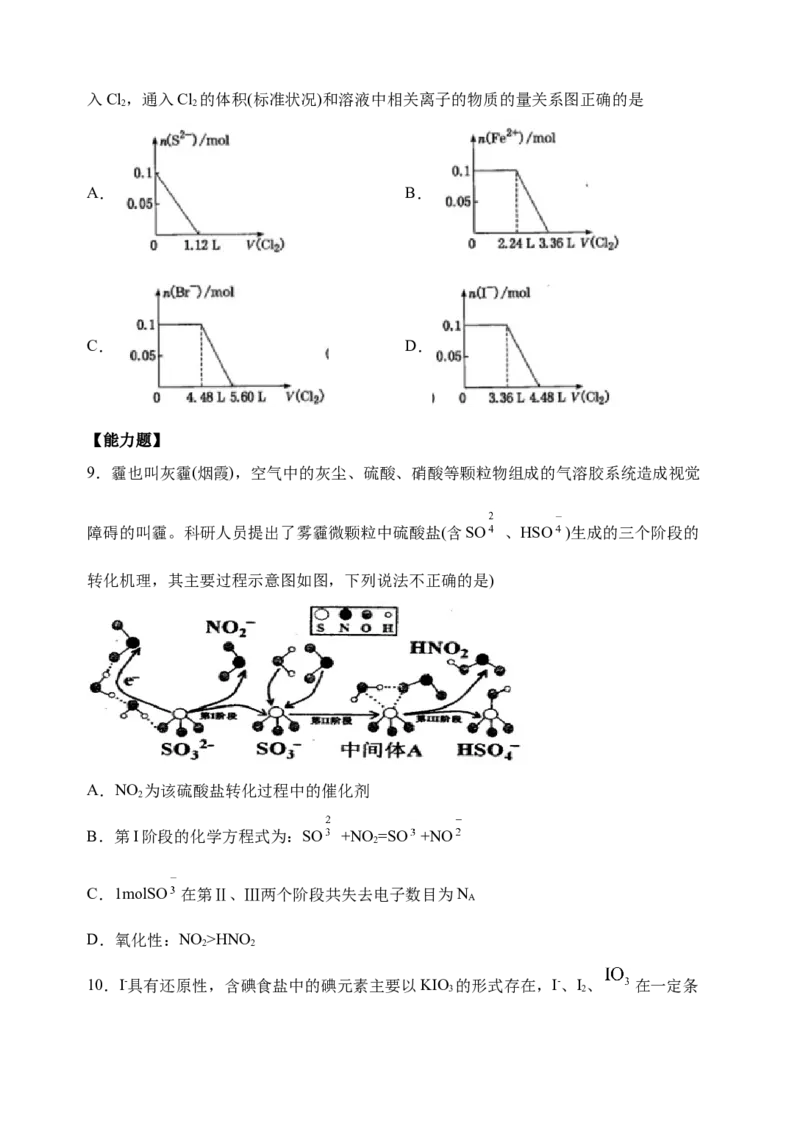
8.已知还原性 S2-、I-、Fe2+、Br-依次减弱,向含 S2-、Fe2+、Br-、I-各0.1mol的溶液中通入Cl,通入Cl 的体积(标准状况)和溶液中相关离子的物质的量关系图正确的是
2 2
A. B.
C. D.
【能力题】
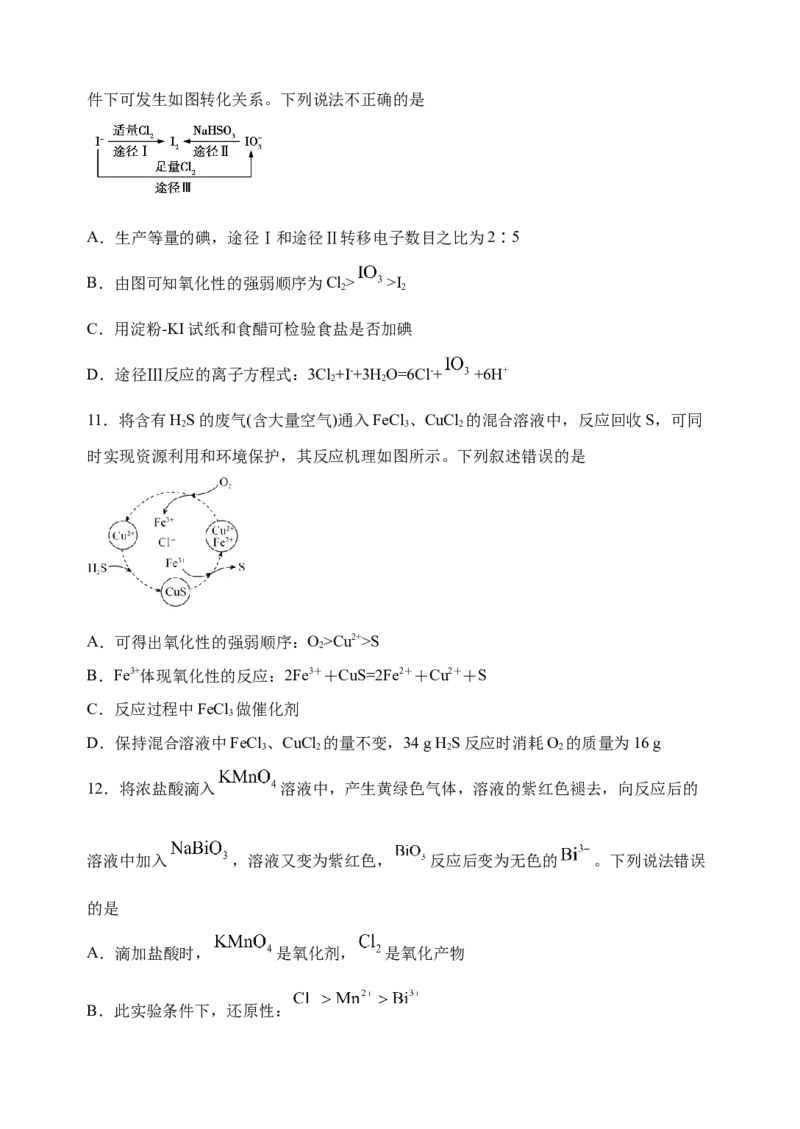
9.霾也叫灰霾(烟霞),空气中的灰尘、硫酸、硝酸等颗粒物组成的气溶胶系统造成视觉
障碍的叫霾。科研人员提出了雾霾微颗粒中硫酸盐(含SO 、HSO )生成的三个阶段的
转化机理,其主要过程示意图如图,下列说法不正确的是)
A.NO 为该硫酸盐转化过程中的催化剂
2
B.第I阶段的化学方程式为:SO +NO=SO +NO
2
C.1molSO 在第Ⅱ、Ⅲ两个阶段共失去电子数目为N
A
D.氧化性:NO >HNO
2 2
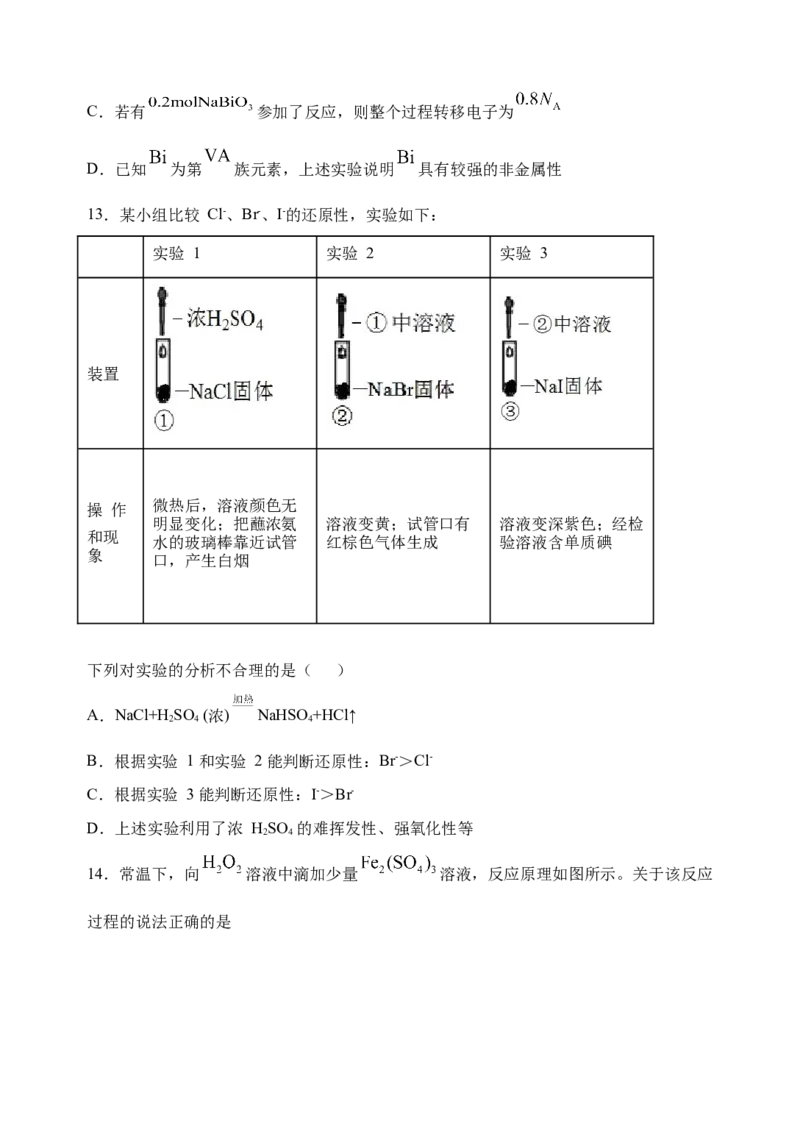
10.I-具有还原性,含碘食盐中的碘元素主要以KIO 的形式存在,I-、I、 在一定条
3 2件下可发生如图转化关系。下列说法不正确的是
A.生产等量的碘,途径Ⅰ和途径Ⅱ转移电子数目之比为2∶5
B.由图可知氧化性的强弱顺序为Cl> >I
2 2
C.用淀粉-KI试纸和食醋可检验食盐是否加碘
D.途径Ⅲ反应的离子方程式:3Cl+I-+3H O=6Cl-+ +6H+
2 2
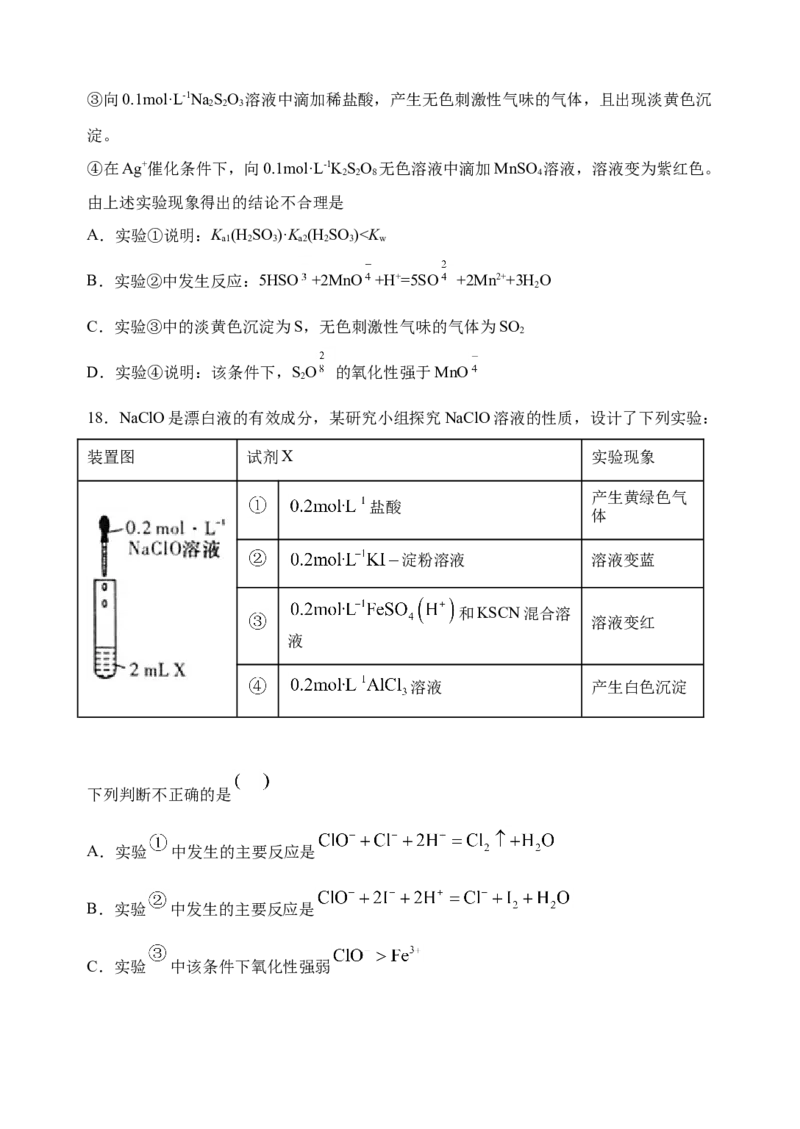
11.将含有HS的废气(含大量空气)通入FeCl 、CuCl 的混合溶液中,反应回收S,可同
2 3 2
时实现资源利用和环境保护,其反应机理如图所示。下列叙述错误的是
A.可得出氧化性的强弱顺序:O>Cu2+>S
2
B.Fe3+体现氧化性的反应:2Fe3++CuS=2Fe2++Cu2++S
C.反应过程中FeCl 做催化剂
3
D.保持混合溶液中FeCl 、CuCl 的量不变,34 g HS反应时消耗O 的质量为16 g
3 2 2 2
12.将浓盐酸滴入 溶液中,产生黄绿色气体,溶液的紫红色褪去,向反应后的
溶液中加入 ,溶液又变为紫红色, 反应后变为无色的 。下列说法错误
的是
A.滴加盐酸时, 是氧化剂, 是氧化产物
B.此实验条件下,还原性:C.若有 参加了反应,则整个过程转移电子为
D.已知 为第 族元素,上述实验说明 具有较强的非金属性
13.某小组比较 Cl-、Br-、I-的还原性,实验如下:
实验 1 实验 2 实验 3
装置
操 作 微热后,溶液颜色无
明显变化;把蘸浓氨 溶液变黄;试管口有 溶液变深紫色;经检
和现 水的玻璃棒靠近试管 红棕色气体生成 验溶液含单质碘
象 口,产生白烟
下列对实验的分析不合理的是( )
A.NaCl+H SO (浓) NaHSO+HCl↑
2 4 4
B.根据实验 1 和实验 2 能判断还原性:Br->Cl-
C.根据实验 3 能判断还原性:I->Br-
D.上述实验利用了浓 HSO 的难挥发性、强氧化性等
2 4
14.常温下,向 溶液中滴加少量 溶液,反应原理如图所示。关于该反应
过程的说法正确的是A.该反应过程中, 是 是 B.当有 生成时,转移 电子
C.在 分解过程中,溶液的 逐渐降低 D. 的氧化性比 强,还原性
比 弱
15.下列说法正确的是
A.根据反应 ,可推出 的还原性比 的强
B. ,每生成
共传移 电子
C.根据反应 可知氧化性:
D.因 的氧化性强于 ,所以置换反应 不能发生
16.将一定量的SO 通入Fe(NO ) 溶液中,再加入适量BaCl 溶液,一定会大量增加的是
2 3 3 2
A.H+ B.SO 2- C.Ba2+ D.Fe2+
4
【提升题】
17.为探究某些硫的含氧酸盐的部分性质,进行如下实验,并记录实验现象:
①测得0.01mol·L-1NaHSO 溶液的pH约为5。
3
②向0.01mol·L-1NaHSO 溶液中滴加少量酸性KMnO 溶液,溶液的紫红色褪去。
3 4③向0.1mol·L-1NaSO 溶液中滴加稀盐酸,产生无色刺激性气味的气体,且出现淡黄色沉
2 2 3
淀。
④在Ag+催化条件下,向0.1mol·L-1KSO 无色溶液中滴加MnSO 溶液,溶液变为紫红色。
2 2 8 4
由上述实验现象得出的结论不合理是
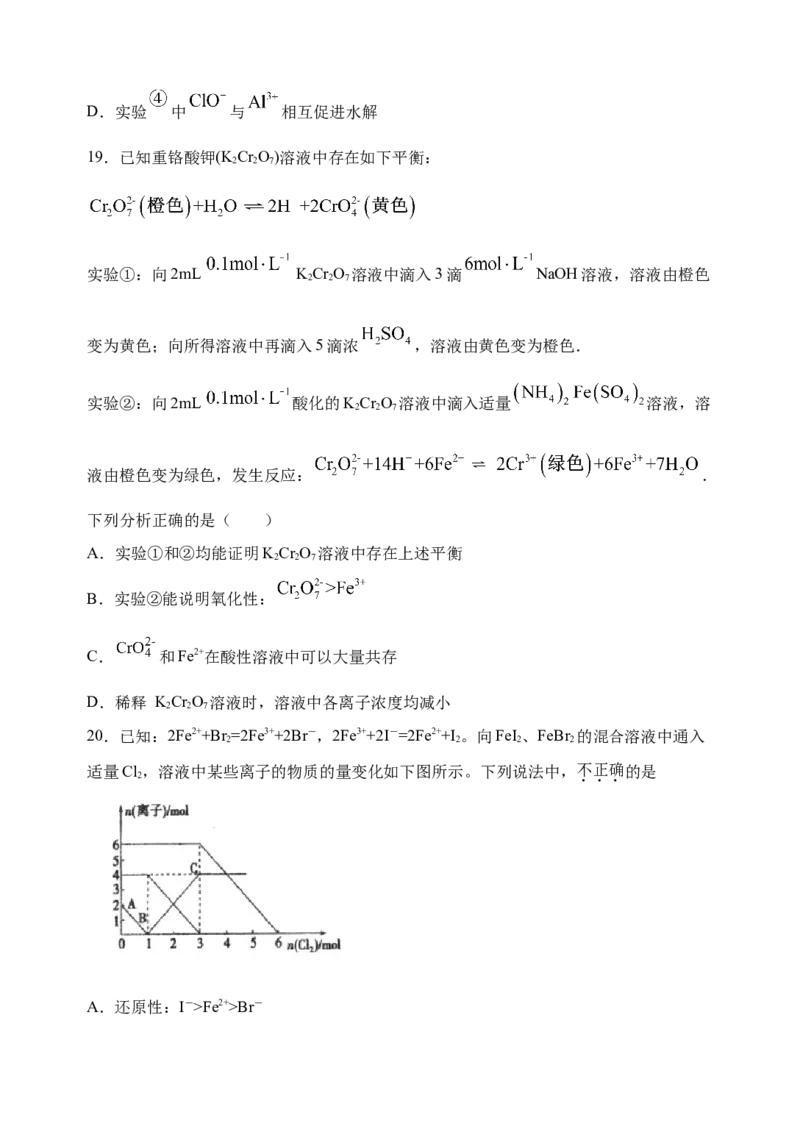
A.实验①说明:K (H SO )·K (H SO )Fe2+>Br-B.原混合溶液中FeBr 的物质的量为3mol
2
C.原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3
D.当通入3mol Cl 时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl=2Fe3++I +4Cl
2 2 2
-
21.下列有关实验操作、现象和结论均正确的是
操作 现象 结论
将硫酸酸化的HO 滴入Fe(NO ) 溶液
A 2 2 3 2 溶液变黄色 氧化性:HO 比Fe3+强
中 2 2
无色溶液滴加氯水和CCl ,振荡、静 下层溶液显紫
B 4 原溶液中有I-
置 色
原溶液一定含有某种钠
C 用洁净铂丝蘸取溶液进行焰色反应 火焰呈黄色
盐
D 将气体通过湿润的品红试纸 试纸褪色 该气体一定是SO
2
A.A B.B C.C D.D
22.下列说法正确的是
A.HClO中氯元素化合价比HClO 中氯元素化合价低,所以,HClO 的氧化性强
4 4
B.已知①Fe + Cu2+= Fe2++ Cu;② 2Fe3++ Cu = 2Fe2++ Cu2+,则氧化性强弱顺序为:Fe3+>
Cu2+> Fe2+
C.已知还原性:B-> C-> D-,反应 2C-+ D = 2D-+C 和反应 2C-+ B = 2B-+C 都能发
2 2 2 2
生
D.具有强氧化性和强还原性的物质放在一起就能发生氧化还原反应