文档内容
微专题 17 金属及其化合物制备流程(Li)
一、物质概况:
金属锂为一种银白色的轻金属;熔点为180.54°C,沸点1342°C,密度0.534克/厘米³,硬
度0.6。金属锂可溶于液氨。锂与其它碱金属不同,在室温下与水反应比较慢,但能与氮
气反应生成黑色的一氮化三锂晶体。锂的弱酸盐都难溶于水。在碱金属氯化物中,只有
氯化锂易溶于有机溶剂。锂的挥发性盐的火焰呈深红色,可用此来鉴定锂。锂很容易与
氧、氮、硫等化合,在冶金工业中可用做脱氧剂。锂也可以做铅基合金和铍、镁、铝等
轻质合金的成分。锂在原子能工业中有重要用途。
二、物理性质:
银白色金属。质较软,可用刀切割。是最轻的金属,密度比所有的油和液态烃都小,故
应存放于固体石蜡或者白凡士林中(在液体石蜡中锂也会浮起)。
锂的密度非常小,仅有0.534g/cm³,为非气态单质中最小的一个。
因为锂原子半径小,故其比起其他的碱金属,压缩性最小,硬度最大,熔点最高。
温度高于-117℃时,金属锂是典型的体心立方结构,但当温度降至-201℃时,开始转变为
面心立方结构,温度越低,转变程度越大,但是转变不完全。在20℃时,锂的晶格常数
为3.50Å,电导约为银的五分之一。*锂容易地与铁以外的任意一种金属熔合。
锂的焰色反应为紫红色。
三、化学性质:
锂(Lithium),是一种化学元素,是金属活动性较强的金属(金属性最强的金属是铯),它的
化学符号是Li,它的原子序数是3,三个电子其中两个分布在K层,另一个在L层。锂是
所有金属中最轻的。因为锂的电荷密度很大并且有稳定的氦型双电子层,使得锂容易极
化其他的分子或离子,自己本身却不容易极化。这一点就影响到它和它的化合物的稳定
性。
虽然锂的氢标电势是最负的,已经达到-3.045,但由于氢氧化锂溶解度不大而且锂与水反
应时放热不能使锂融化,所以锂与水反应还不如钠剧烈,反应在进行一段时间后,锂表
面的氮氧化物膜被溶解,从而使反应更加剧烈。在500℃左右容易与氢发生反应,产生氢
化锂,是唯一能生成稳定得足以熔融而不分解的氢化物的碱金属,电离能 5.392电子伏特,与氧、氮、硫等均能化合,是唯一的与氮在室温下反应,生成氮化锂(Li₃N)的碱金属。由
于易受氧化而变暗。如果将锂丢进浓硫酸,那么它将在硫酸上快速浮动,燃烧并爆炸。
如果将锂和氯酸钾混合(震荡或研磨),它也有可能发生爆炸式的反应。
锂的一些反应的化学反应方程式如下:
4 Li + O₂ = 2 Li₂O (反应条件:自发反应,或者加热,或者点燃)(燃烧猛烈)
6 Li + N₂ = 2 Li₃N(反应条件:自发反应,或者加热,或者点燃)
2 Li + S = Li₂S (该反应放出大量热,爆炸!)
2 Li + 2 H₂O = 2 LiOH + H₂↑(现象:锂浮动在水面上,迅速反应,放出无色气体)
2 Li + 2 CH₃CH₂OH(乙醇) = 2 CH₃CH₂OLi(乙醇锂) + H₂↑
4 Li + TiCl₄ = Ti + 4 LiCl
2 Li + 2 NH₃(l.) = 2 LiNH₂ + H₂↑
氢化锂遇水发生猛烈的化学反应,产生大量的氢气。两公斤氢化锂分解后,可以放出氢
气566千升。氢化锂的确是名不虚传的"制造氢气的工厂"。第二次世界大战期间,美国飞
行员备有轻便的氢气源--氢化锂丸作应急之用。飞机失事坠落在水面时,只要一碰到水,
氢化锂就立即与水发生反应,释放出大量的氢气,使救生设备(救生艇、救生衣、讯号气
球等)充气膨胀。
四、工业制备:
工业上可以用如下的方法制备锂单质:
将氯化锂在不超过其熔点(602℃)的温度下灼烧干燥1h。
使用经过氢氧化钾脱水干燥的、新蒸馏的吡啶溶解上述氯化锂,制成11.81%的氯化锂的
吡啶溶液作为电解液。用石墨板作阳极,光洁的铂片或铁片作阴极,无隔膜。电解时采
用的电压为1.4V,电流密度为0.2~0.3A/100c㎡。
五、工业用途:
锂主要以硬脂酸锂的形式用作润滑脂的增稠剂。这种润滑剂兼有高抗水性、耐高温和良
好的低温性能。锂化物用于陶瓷制品中,以起到助溶剂的作用。在冶金工业中也用来作
脱氧剂或脱氯剂,以及铅基轴承合金。锂也是铍、镁、铝轻质合金的重要成分。重要途
径之一就是发展向锂电池这样的新型电池。硼氢化锂和氢化铝锂,在有机化学反应中被广泛用做还原剂。
锂广泛应用于电池、陶瓷、玻璃、润滑剂、制冷液、核工业以及光电等行业。随着电脑、
数码相机、手机、移动电动工具等电子产品的不断发展,电池行业已经成为锂最大的消
费领域。此外,碳酸锂是陶瓷产业减能耗、环保的有效途径之一,对锂的需求量也将会
提高。与此同时,锂在玻璃中的各种新作用也在不断被发现,玻璃行业对锂的需求仍将
保持增长。因而,玻璃和陶瓷行业成为了锂的第二大消费领域。
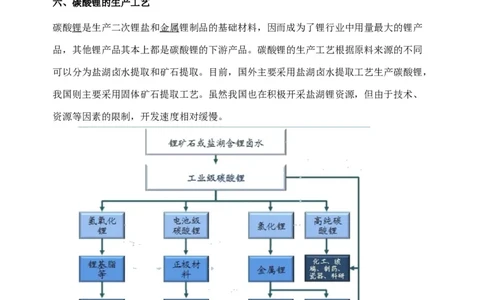
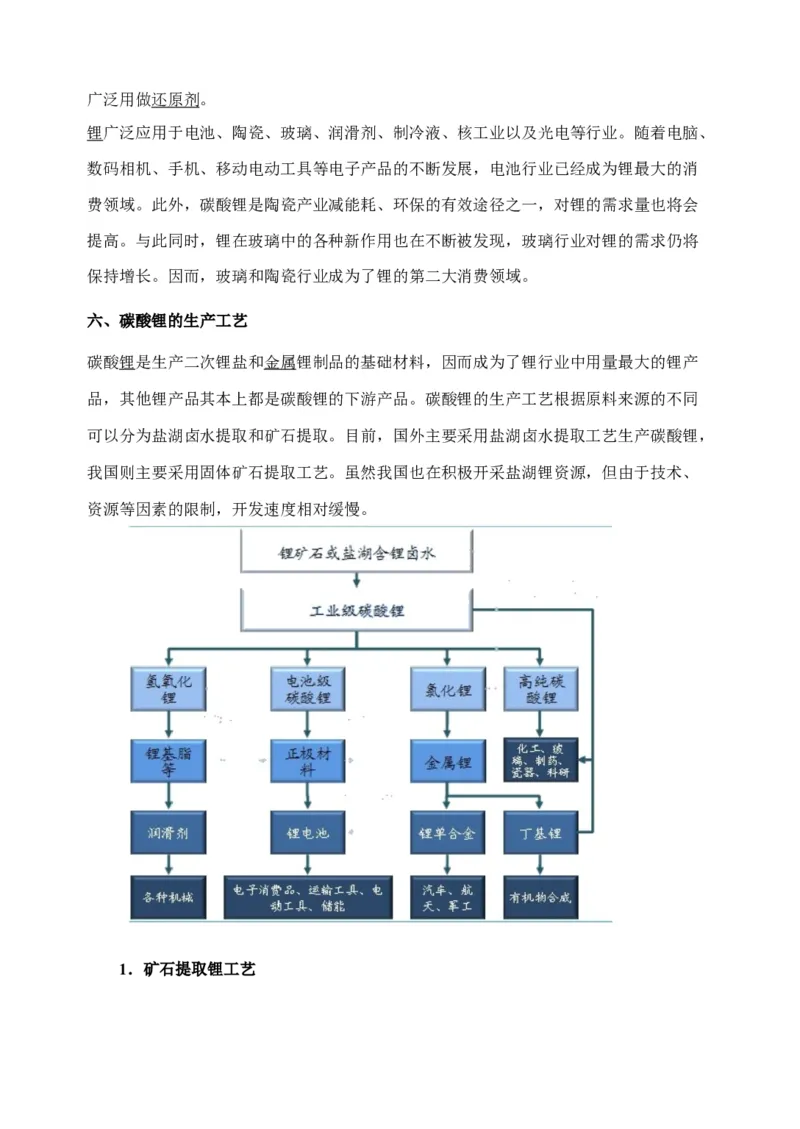
六、碳酸锂的生产工艺
碳酸锂是生产二次锂盐和金属锂制品的基础材料,因而成为了锂行业中用量最大的锂产
品,其他锂产品其本上都是碳酸锂的下游产品。碳酸锂的生产工艺根据原料来源的不同
可以分为盐湖卤水提取和矿石提取。目前,国外主要采用盐湖卤水提取工艺生产碳酸锂,
我国则主要采用固体矿石提取工艺。虽然我国也在积极开采盐湖锂资源,但由于技术、
资源等因素的限制,开发速度相对缓慢。
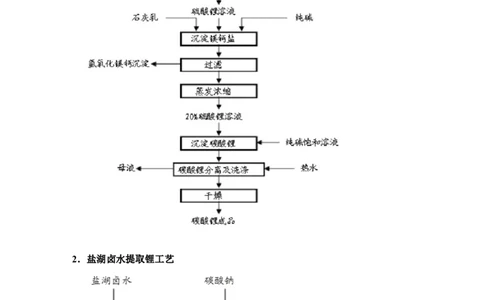
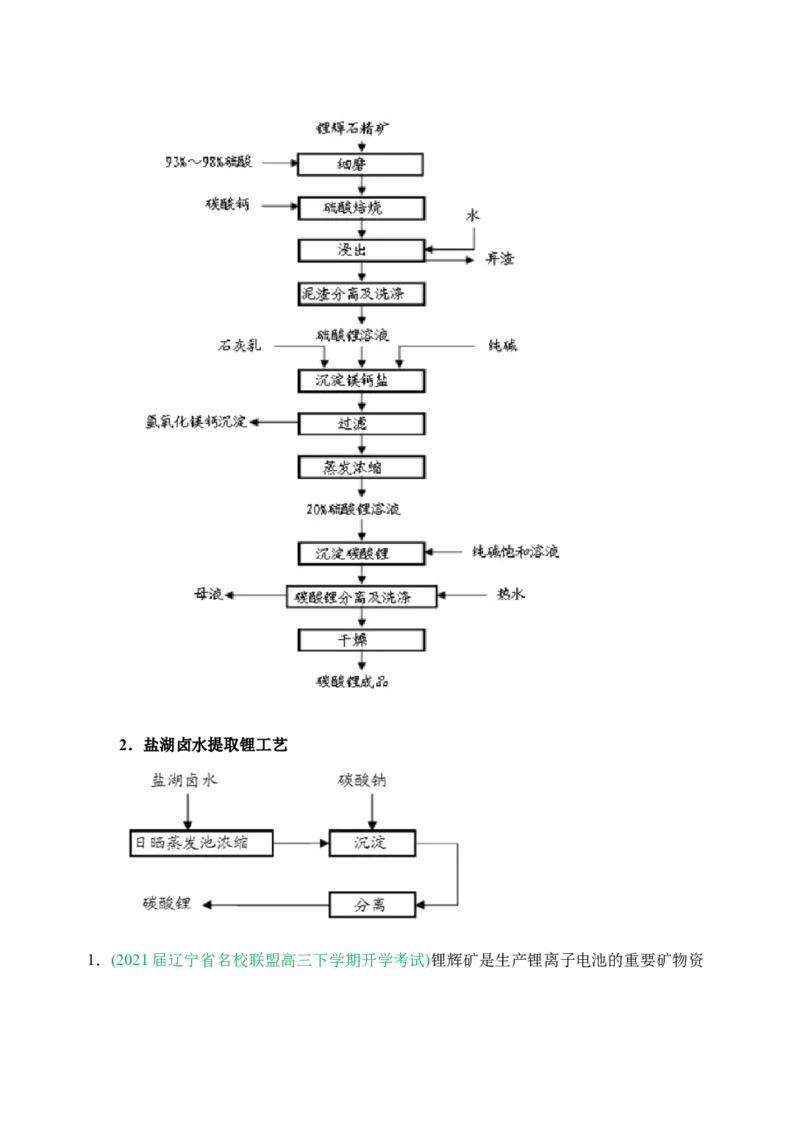
1.矿石提取锂工艺2.盐湖卤水提取锂工艺
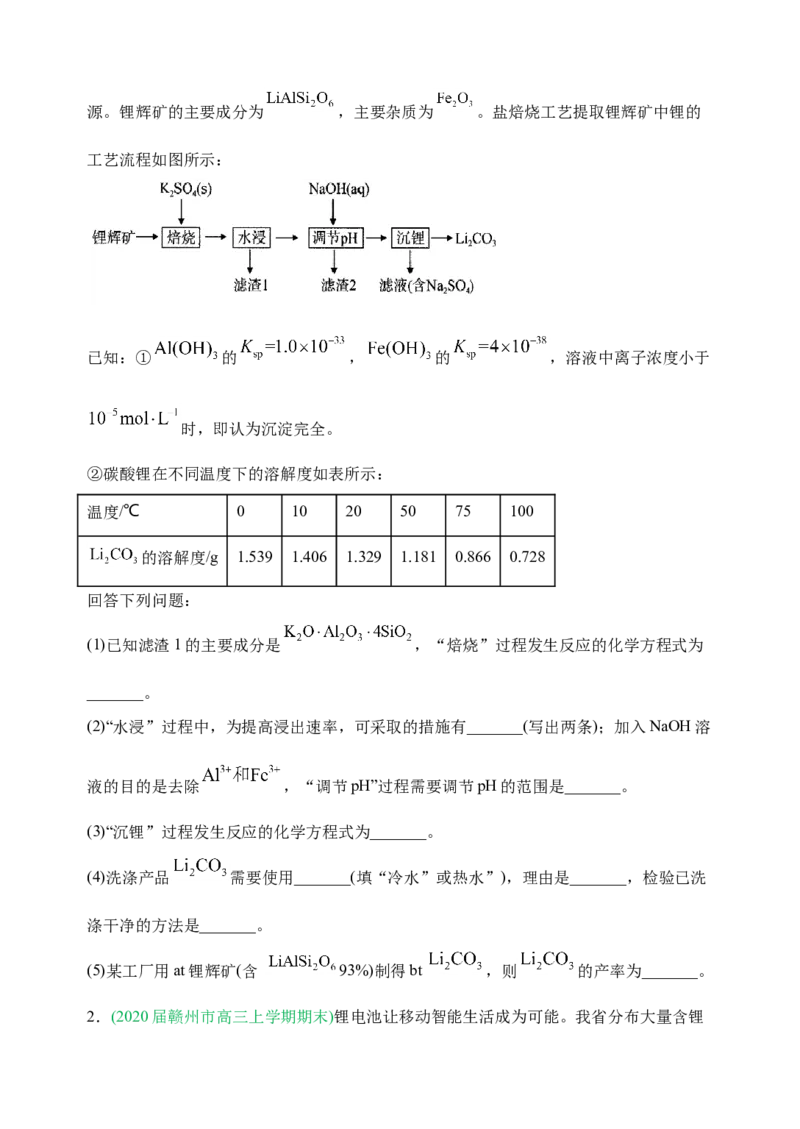
1.(2021届辽宁省名校联盟高三下学期开学考试)锂辉矿是生产锂离子电池的重要矿物资源。锂辉矿的主要成分为 ,主要杂质为 。盐焙烧工艺提取锂辉矿中锂的
工艺流程如图所示:
已知:① 的 , 的 ,溶液中离子浓度小于
时,即认为沉淀完全。
②碳酸锂在不同温度下的溶解度如表所示:
温度/℃ 0 10 20 50 75 100
的溶解度/g 1.539 1.406 1.329 1.181 0.866 0.728
回答下列问题:
(1)已知滤渣1的主要成分是 ,“焙烧”过程发生反应的化学方程式为
_______。
(2)“水浸”过程中,为提高浸出速率,可采取的措施有_______(写出两条);加入NaOH溶
液的目的是去除 ,“调节pH”过程需要调节pH的范围是_______。
(3)“沉锂”过程发生反应的化学方程式为_______。
(4)洗涤产品 需要使用_______(填“冷水”或热水”),理由是_______,检验已洗
涤干净的方法是_______。
(5)某工厂用at锂辉矿(含 93%)制得bt ,则 的产率为_______。
2.(2020届赣州市高三上学期期末)锂电池让移动智能生活成为可能。我省分布大量含锂云母的锂矿。锂云母主要成分为:KLi Al [AlSi O ](FOH) ,还含有铷、铯等稀有金属
1.5 1.5 3 10 2
及少量铁、镁等杂质。2019年,中国有色金属工业协会评估认为江西浩海锂能科技有限
公司开发完成的“锂云母全组分利用绿色工艺及关键技术”达到了国际领先水平。以下
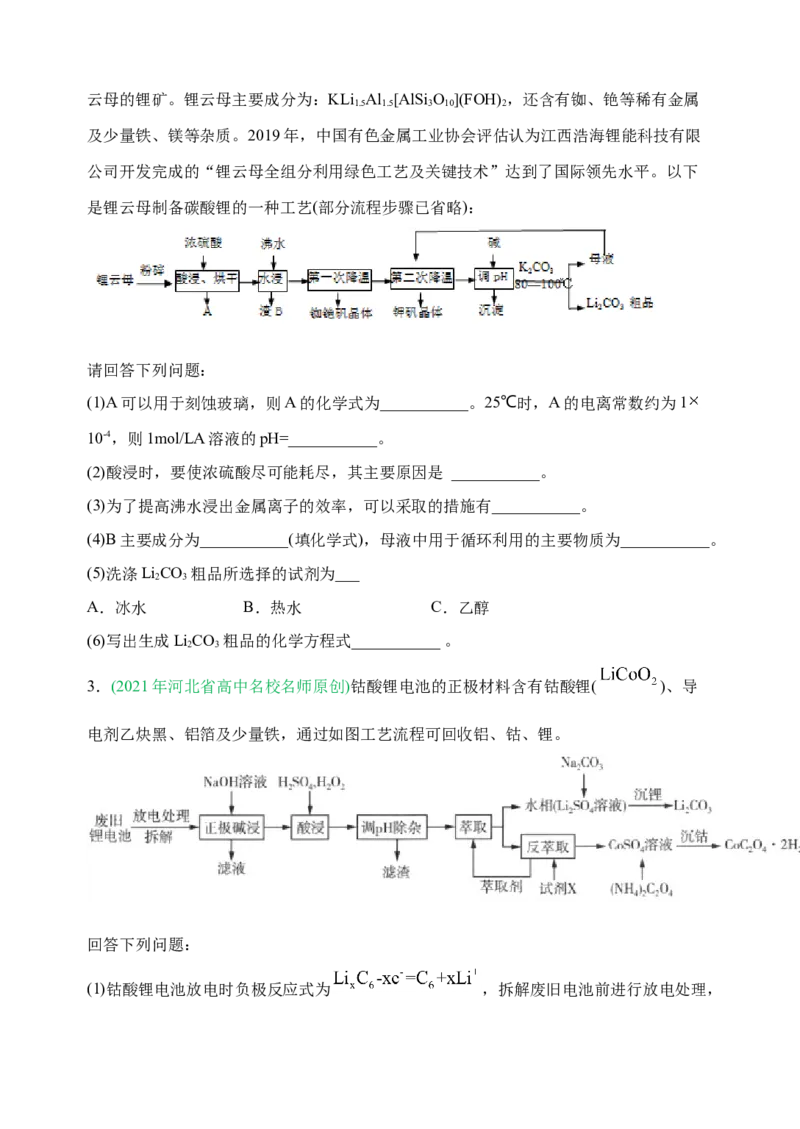
是锂云母制备碳酸锂的一种工艺(部分流程步骤已省略):
请回答下列问题:
(1)A可以用于刻蚀玻璃,则A的化学式为___________。25℃时,A的电离常数约为1
10-4,则1mol/LA溶液的pH=___________。
(2)酸浸时,要使浓硫酸尽可能耗尽,其主要原因是 ___________。
(3)为了提高沸水浸出金属离子的效率,可以采取的措施有___________。
(4)B主要成分为___________(填化学式),母液中用于循环利用的主要物质为___________。
(5)洗涤LiCO 粗品所选择的试剂为___
2 3
A.冰水 B.热水 C.乙醇
(6)写出生成LiCO 粗品的化学方程式___________ 。
2 3
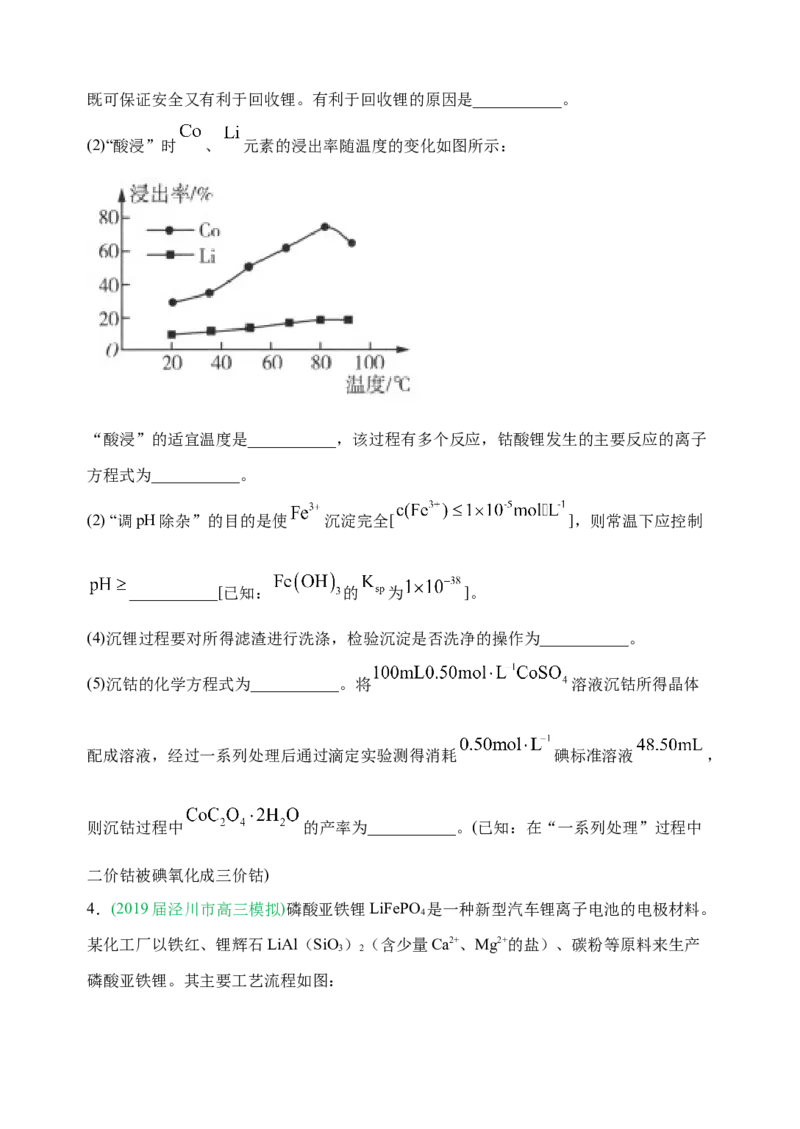
3.(2021年河北省高中名校名师原创)钴酸锂电池的正极材料含有钴酸锂( )、导
电剂乙炔黑、铝箔及少量铁,通过如图工艺流程可回收铝、钴、锂。
回答下列问题:
(1)钴酸锂电池放电时负极反应式为 ,拆解废旧电池前进行放电处理,既可保证安全又有利于回收锂。有利于回收锂的原因是___________。
(2)“酸浸”时 、 元素的浸出率随温度的变化如图所示:
“酸浸”的适宜温度是___________,该过程有多个反应,钴酸锂发生的主要反应的离子
方程式为___________。
(2) “调pH除杂”的目的是使 沉淀完全[ ],则常温下应控制
___________[已知: 的 为 ]。
(4)沉锂过程要对所得滤渣进行洗涤,检验沉淀是否洗净的操作为___________。
(5)沉钴的化学方程式为___________。将 溶液沉钴所得晶体
配成溶液,经过一系列处理后通过滴定实验测得消耗 碘标准溶液 ,
则沉钴过程中 的产率为___________。(已知:在“一系列处理”过程中
二价钴被碘氧化成三价钴)
4.(2019届泾川市高三模拟)磷酸亚铁锂LiFePO 是一种新型汽车锂离子电池的电极材料。
4
某化工厂以铁红、锂辉石LiAl(SiO)(含少量Ca2+、Mg2+的盐)、碳粉等原料来生产
3 2
磷酸亚铁锂。其主要工艺流程如图:已知:2LiAl(SiO)+H SO (浓) LiSO +AlO·4SiO·H O↓
3 2 2 4 2 4 2 3 2 2
温度/℃ 20 40 60 80
溶解度(Li CO)/g 1.33 1.17 1.01 0.85
2 3
溶解度(Li SO )/g 34.2 32.8 31.9 30.7
2 4
(1)从滤渣Ⅰ中可分离出Al O,如图所示。请写出生成沉淀的离子方程式___。
2 3
(2)滤渣Ⅱ的主要成分是:___(填化学式)。
(3)向滤液Ⅱ中加入饱和NaCO 溶液,过滤后,用“热水洗涤”的原因是___。
2 3
(4)写出在高温下生成磷酸亚铁锂的化学方程式:___。
(5)磷酸亚铁锂电池总反应为:FePO +Li LiFePO ,电池中的固体电解质可传导
4 4
Li+。试写出该电池放电时的正极反应:___。若用该电池电解饱和食盐水(电解池电极均
为惰性电极),当电解池两极共有4480mL气体(标准状况)产生时,该电池消耗锂的质
量为___。