文档内容
微专题29 无机反应图像题及综合应用
用图像来描述化学过程或者呈现化学背景知识是高中化学的基本表达方式之一,而高考
试题中通过图像把化学问题抽象为数学问题来考查考生从图像中获取、评价、整合和应
用信息的综合分析能力的做法已成常态。全国高考化学图像题在“证据推理与模型认
知”化学学科核心素养的考查颇具特色。试题的新颖度、难度和区分度在一定程度上都
借助于图像的创新得以体现。所以,我们以无机化学中化学图像试题出现较多的两部分
内容为例,体现出无机反应图像及综合应用在高考中对考生各项能力的考查。
一、CO 与盐溶液反应产物或现象的判断
2
1.一般从强酸制弱酸的角度去分析:
由于碳酸比硅酸、次氯酸、苯酚、Al(OH) (偏铝酸)的酸性强,因此可用CO 制取上述弱
3 2
酸,常涉及的变化如下:
CO +Na SiO +H O=Na CO +H SiO ↓ (或CO +Na SiO +2H O===H SiO ↓+Na
2 2 3 2 2 3 2 3 2 2 3 2 4 4
CO )
2 3
CO +Ca(ClO) +HO=CaCO ↓+2HClO
2 2 2 3
CO+C HONa+H O=C HOH+NaHCO
2 6 5 2 6 5 3
CO(过量)+NaAlO +2HO===Al(OH) ↓+NaHCO
2 2 2 3 3
CO(少量)+2NaAlO +3HO===2Al(OH) ↓+NaCO
2 2 2 3 2 3
【易错点】
把CO 通入到CaCl 和NaOH的混合溶液中或者通入到CaCl 和氨水的混合溶液中,则有
2 2 2
白色沉淀,因为CO 通入到CaCl 和NaOH的混合溶液中,先和碱反应生成碳酸钠和水,
2 2然后碳酸钠和氯化钙反应生成碳酸钙沉淀,若通入CaCl 和氨水的混合溶液中,则先和氨
2
水反应生成碳酸铵,然后碳酸铵与氯化钙反应生成碳酸钙白色沉淀。
二、CO 与碱反应产物的判断
2
(1)CO 与单一组分反应(如CO 通入NaOH 溶液)产物的分析
2 2
①反应原理
CO +2NaOH=Na CO +H O
2 2 3 2
CO +NaOH=NaHCO
2 3
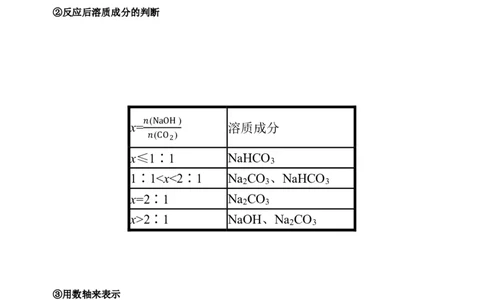
②反应后溶质成分的判断
( )
x= 溶质成分
( )
𝑛 NaOH
x≤𝑛1∶CO12 NaHCO
3
1∶12∶1 NaOH、Na CO
2 3
③用数轴来表示
(2)CO 与多组分[如CO 通入NaOH 、Ca(OH) 的混合溶液]反应的顺序:
2 2 2①Ca(OH) +CO =CaCO ↓+H O
2 2 3 2
②2NaOH +CO =Na CO +H O
2 2 3 2
③Na CO +CO +H O=2NaHCO
2 3 2 2 3
④CaCO +CO +H O=Ca(HCO )
3 2 2 3 2
二、铝及其化合物的相互转化
1.Al3+、Al(OH) 、AlO之间的转化关系
3
实现上述各步转化的离子方程式:
(1)①Al3++3NH ·H O===Al(OH) ↓+3NH
3 2 3
②Al3++3AlO+6HO===4Al(OH) ↓
2 3
③Al3++3OH-===Al(OH) ↓
3
(2)Al(OH) +3H+===Al3++3HO
3 2
(3)Al3++4OH-===AlO+2HO
2
(4)AlO+4H+===Al3++2HO
2
(5)①AlO+CO+2HO===Al(OH) ↓+HCO ②AlO+H++HO===Al(OH) ↓
2 2 3 2 3
(6)Al(OH) +OH-===AlO+2HO
3 2
2.与Al(OH) 沉淀生成有关的图象分析
3
(1)可溶性铝盐溶液与NaOH溶液反应的图象(从上述转化关系中选择符合图象变化的离子
方程式,下同)。
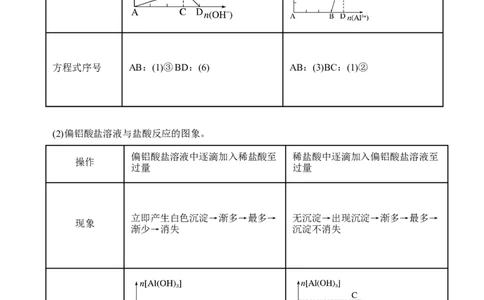
可溶性铝盐溶液中逐滴加入NaOH NaOH溶液中逐滴加入可溶性铝盐
操作
溶液至过量 溶液至过量立即产生白色沉淀→渐多→最多→ 无沉淀(有但即溶)→出现沉淀→渐
现象
渐少→消失 多→最多→沉淀不消失
图象
方程式序号 AB:(1)③BD:(6) AB:(3)BC:(1)②
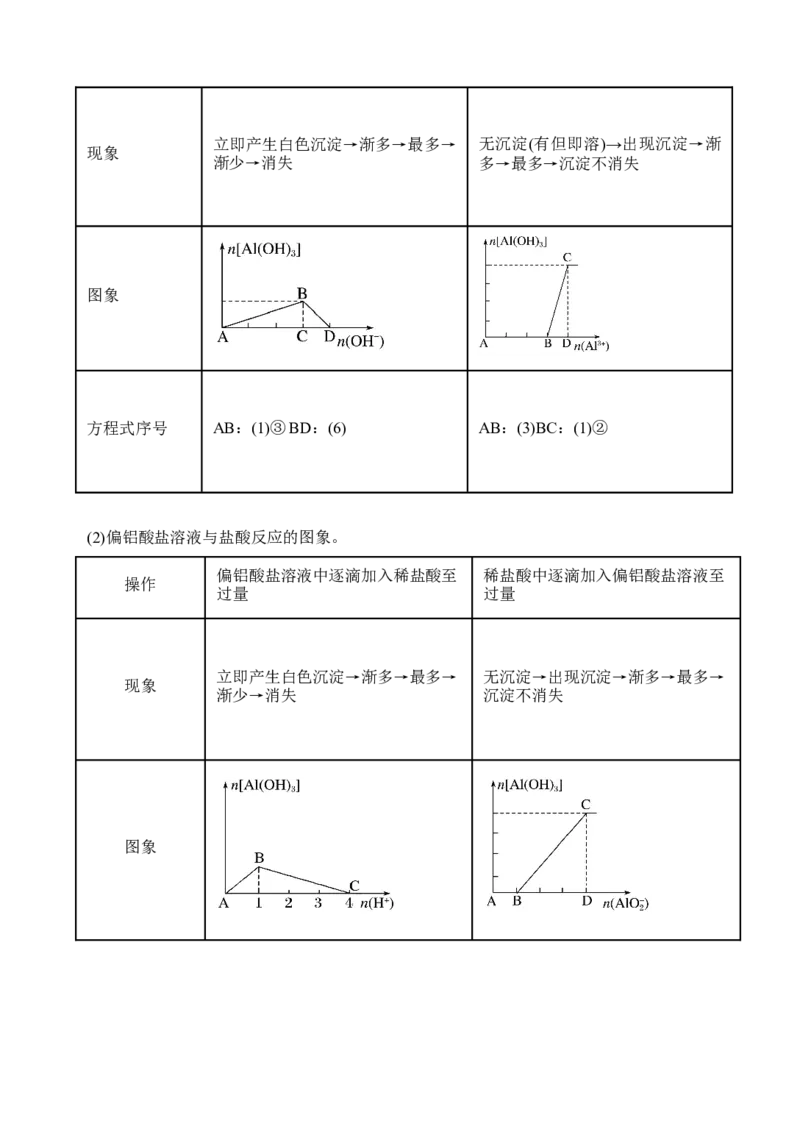
(2)偏铝酸盐溶液与盐酸反应的图象。
偏铝酸盐溶液中逐滴加入稀盐酸至 稀盐酸中逐滴加入偏铝酸盐溶液至
操作
过量 过量
立即产生白色沉淀→渐多→最多→ 无沉淀→出现沉淀→渐多→最多→
现象
渐少→消失 沉淀不消失
图象方程式 AB:(5)② AB:(4)
序号 BC:(2) BC:(1)②
3.可溶性铝盐与强碱反应的计算规律
(1)求产物Al(OH) 的量
3
①当n(OH-)≤3n(Al3+)时,n[Al(OH) ]=n(OH-);
3
②当3n(Al3+)<n(OH-)<4n(Al3+)时,n[Al(OH) ]=
3
4n(Al3+)-n(OH-);
③当n(OH-)≥4n(Al3+)时,n[Al(OH) ]=0,无沉淀。
3
(2)求反应物碱的量
①若碱不足(Al3+未完全沉淀),n(OH-)=3n[Al(OH) ];
3
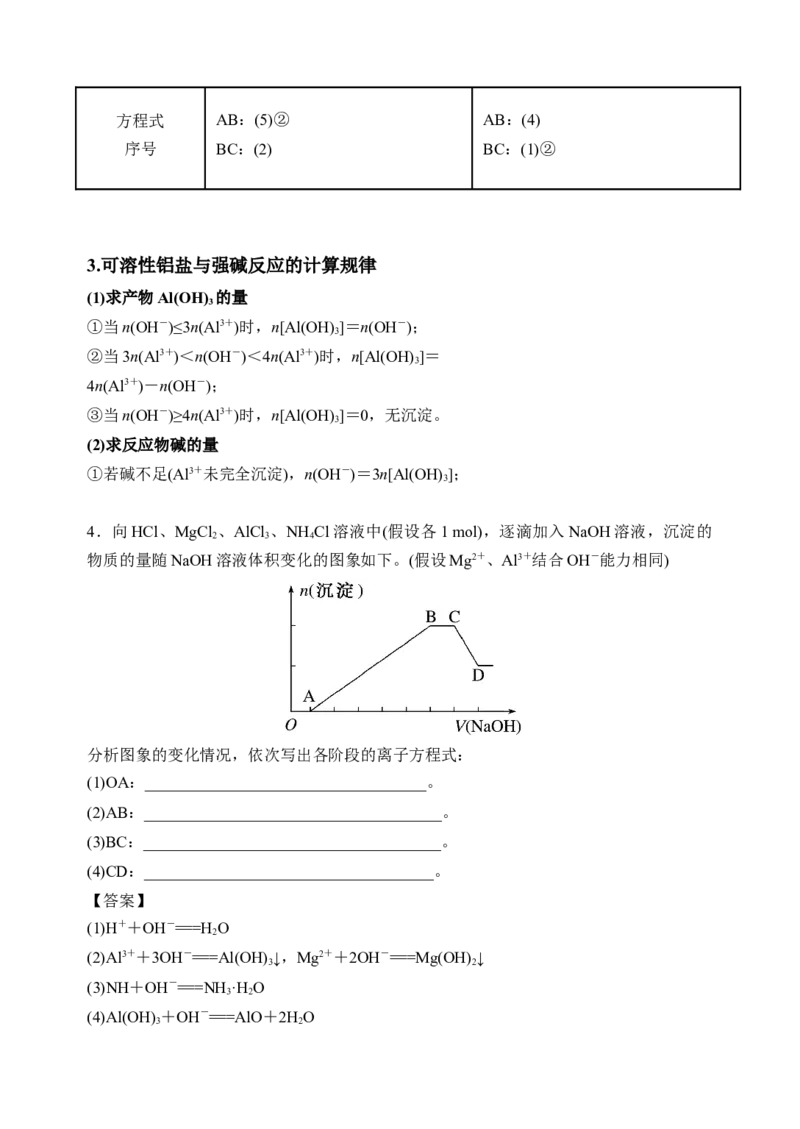
4.向HCl、MgCl 、AlCl 、NH Cl溶液中(假设各1 mol),逐滴加入NaOH溶液,沉淀的
2 3 4
物质的量随NaOH溶液体积变化的图象如下。(假设Mg2+、Al3+结合OH-能力相同)
分析图象的变化情况,依次写出各阶段的离子方程式:
(1)OA:___________________________________。
(2)AB:_____________________________________。
(3)BC:_____________________________________。
(4)CD:____________________________________。
【答案】
(1)H++OH-===H O
2
(2)Al3++3OH-===Al(OH) ↓,Mg2++2OH-===Mg(OH) ↓
3 2
(3)NH+OH-===NH·H O
3 2
(4)Al(OH) +OH-===AlO+2HO
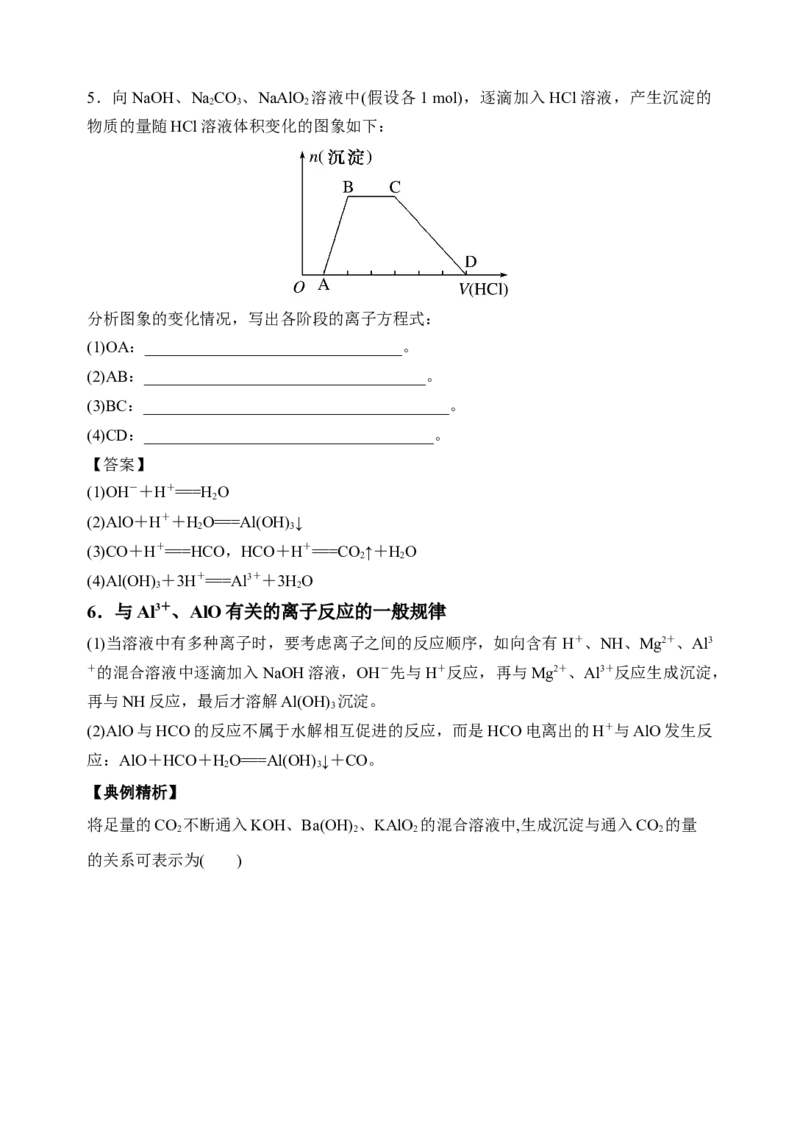
3 25.向NaOH、NaCO 、NaAlO 溶液中(假设各1 mol),逐滴加入HCl溶液,产生沉淀的
2 3 2
物质的量随HCl溶液体积变化的图象如下:
分析图象的变化情况,写出各阶段的离子方程式:
(1)OA:________________________________。
(2)AB:___________________________________。
(3)BC:______________________________________。
(4)CD:____________________________________。
【答案】
(1)OH-+H+===H O
2
(2)AlO+H++HO===Al(OH) ↓
2 3
(3)CO+H+===HCO,HCO+H+===CO ↑+HO
2 2
(4)Al(OH) +3H+===Al3++3HO
3 2
6.与Al3+、AlO有关的离子反应的一般规律
(1)当溶液中有多种离子时,要考虑离子之间的反应顺序,如向含有H+、NH、Mg2+、Al3
+的混合溶液中逐滴加入NaOH溶液,OH-先与H+反应,再与Mg2+、Al3+反应生成沉淀,
再与NH反应,最后才溶解Al(OH) 沉淀。
3
(2)AlO与HCO的反应不属于水解相互促进的反应,而是HCO电离出的H+与AlO发生反
应:AlO+HCO+HO===Al(OH) ↓+CO。
2 3
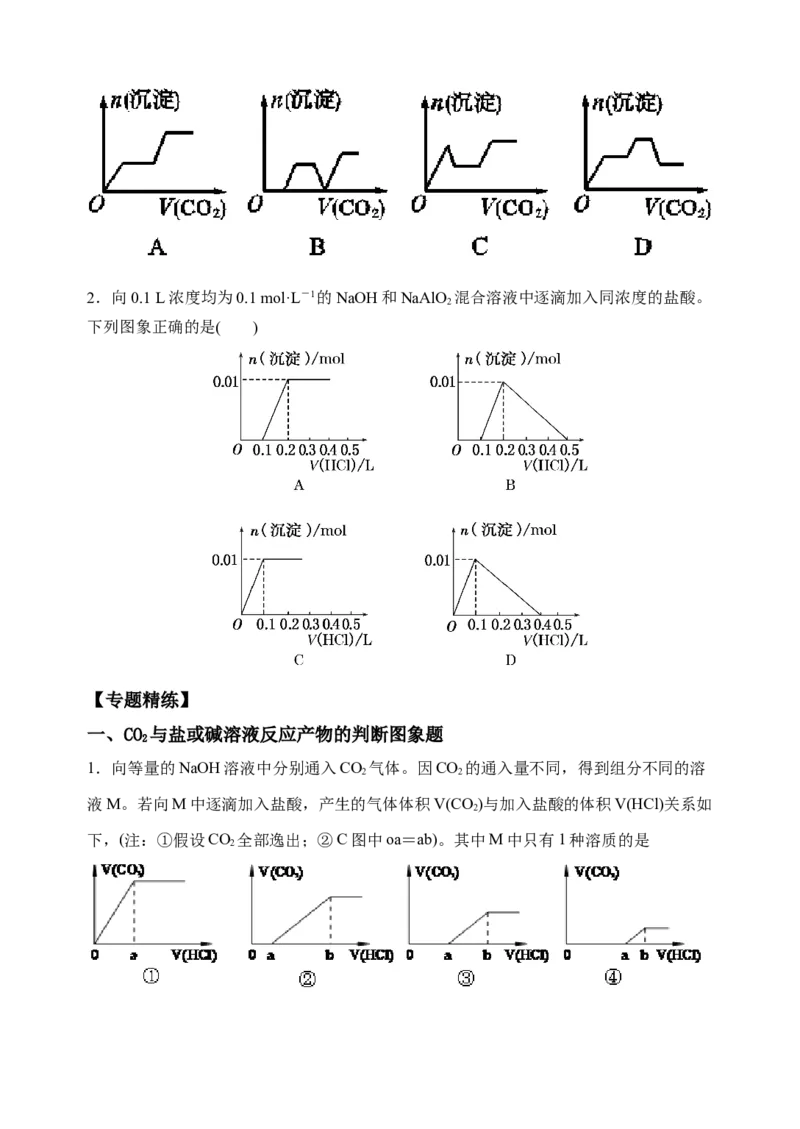
【典例精析】
将足量的CO 不断通入KOH、Ba(OH) 、KAlO 的混合溶液中,生成沉淀与通入CO 的量
2 2 2 2
的关系可表示为( )2.向0.1 L浓度均为0.1 mol·L-1的NaOH和NaAlO 混合溶液中逐滴加入同浓度的盐酸。
2
下列图象正确的是( )
【专题精练】
一、CO 与盐或碱溶液反应产物的判断图象题
2
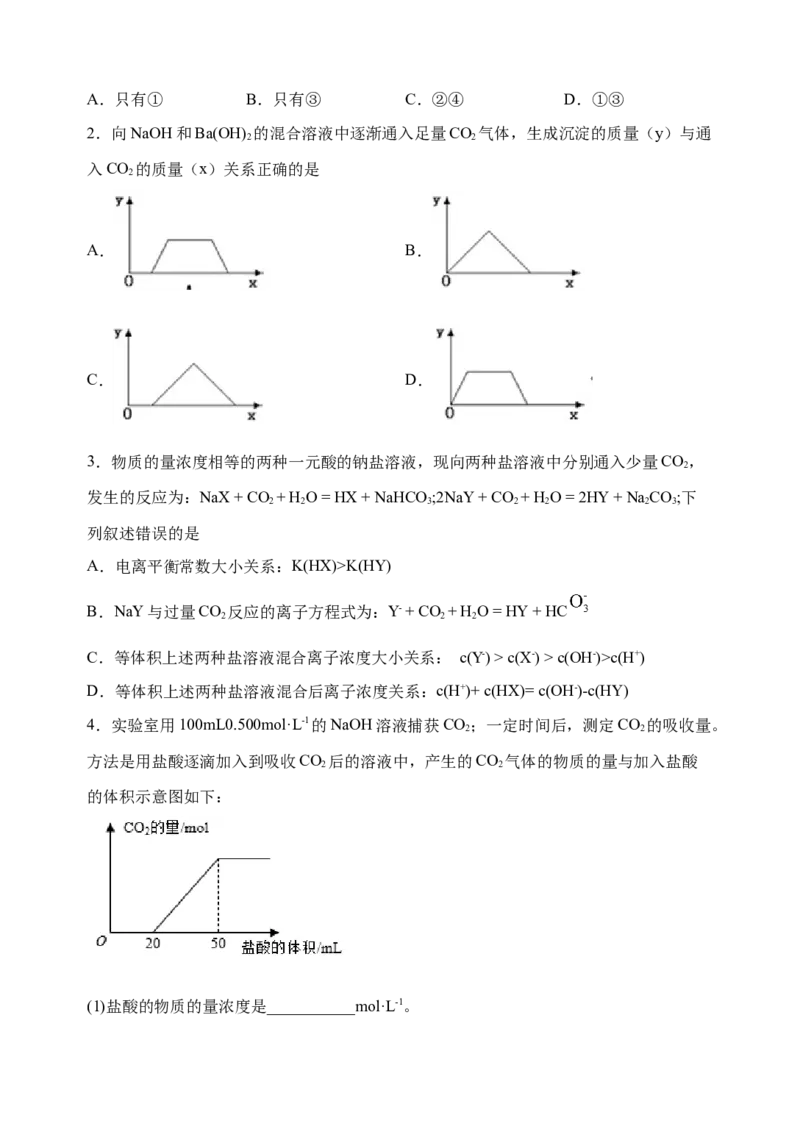
1.向等量的NaOH溶液中分别通入CO 气体。因CO 的通入量不同,得到组分不同的溶
2 2
液M。若向M中逐滴加入盐酸,产生的气体体积V(CO )与加入盐酸的体积V(HCl)关系如
2
下,(注:①假设CO 全部逸出;②C图中oa=ab)。其中M中只有1种溶质的是
2A.只有① B.只有③ C.②④ D.①③
2.向NaOH和Ba(OH) 的混合溶液中逐渐通入足量CO 气体,生成沉淀的质量(y)与通
2 2
入CO 的质量(x)关系正确的是
2
A. B.
C. D.
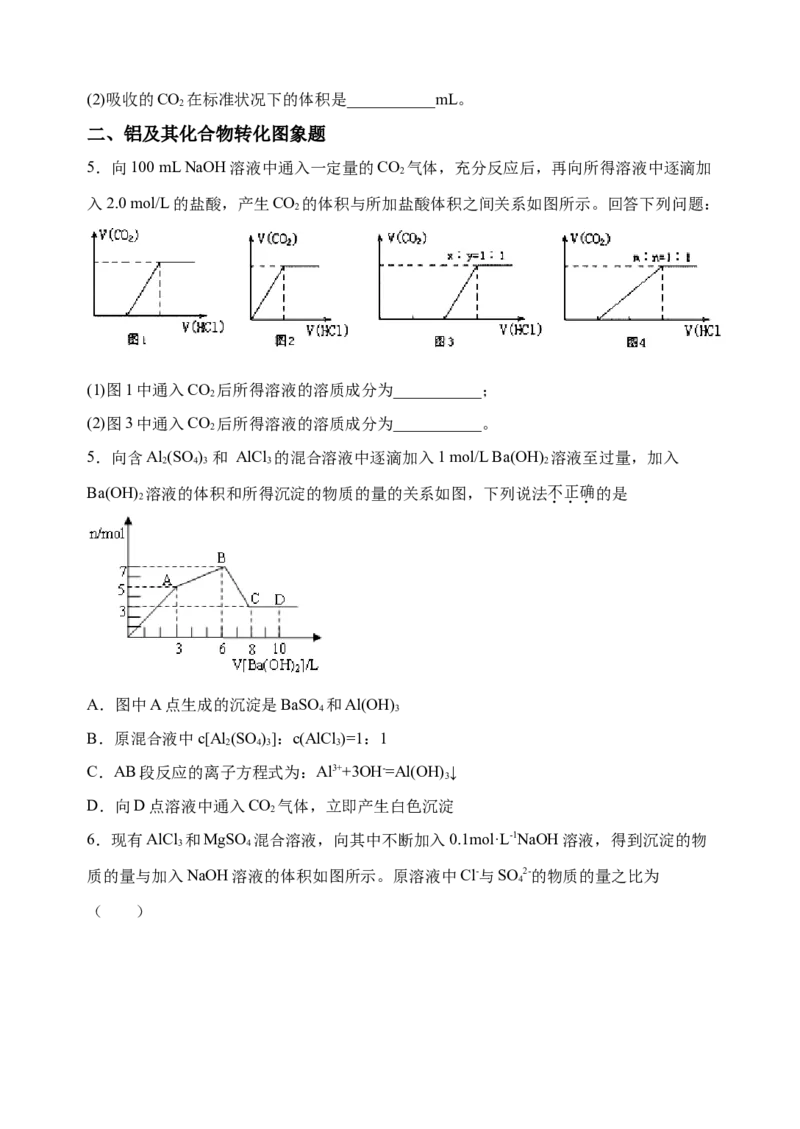
3.物质的量浓度相等的两种一元酸的钠盐溶液,现向两种盐溶液中分别通入少量CO,
2
发生的反应为:NaX + CO + H O = HX + NaHCO ;2NaY + CO + H O = 2HY + Na CO;下
2 2 3 2 2 2 3
列叙述错误的是
A.电离平衡常数大小关系:K(HX)>K(HY)
B.NaY与过量CO 反应的离子方程式为:Y- + CO + H O = HY + HC
2 2 2
C.等体积上述两种盐溶液混合离子浓度大小关系: c(Y-) > c(X-) > c(OH-)>c(H+)
D.等体积上述两种盐溶液混合后离子浓度关系:c(H+)+ c(HX)= c(OH-)-c(HY)
4.实验室用100mL0.500mol·L-1的NaOH溶液捕获CO;一定时间后,测定CO 的吸收量。
2 2
方法是用盐酸逐滴加入到吸收CO 后的溶液中,产生的CO 气体的物质的量与加入盐酸
2 2
的体积示意图如下:
(1)盐酸的物质的量浓度是___________mol·L-1。(2)吸收的CO 在标准状况下的体积是___________mL。
2
二、铝及其化合物转化图象题
5.向100 mL NaOH溶液中通入一定量的CO 气体,充分反应后,再向所得溶液中逐滴加
2
入2.0 mol/L的盐酸,产生CO 的体积与所加盐酸体积之间关系如图所示。回答下列问题:
2
(1)图1中通入CO 后所得溶液的溶质成分为___________;
2
(2)图3中通入CO 后所得溶液的溶质成分为___________。
2
5.向含Al (SO ) 和 AlCl 的混合溶液中逐滴加入1 mol/L Ba(OH) 溶液至过量,加入
2 4 3 3 2
Ba(OH) 溶液的体积和所得沉淀的物质的量的关系如图,下列说法不正确的是
2
A.图中A点生成的沉淀是BaSO 和Al(OH)
4 3
B.原混合液中c[Al (SO )]:c(AlCl )=1:1
2 4 3 3
C.AB段反应的离子方程式为:Al3++3OH-=Al(OH) ↓
3
D.向D点溶液中通入CO 气体,立即产生白色沉淀
2
6.现有AlCl 和MgSO 混合溶液,向其中不断加入0.1mol·L-1NaOH溶液,得到沉淀的物
3 4
质的量与加入NaOH溶液的体积如图所示。原溶液中Cl-与SO 2-的物质的量之比为
4
( )A.6:1 B.1:3 C.2:3 D.3:1
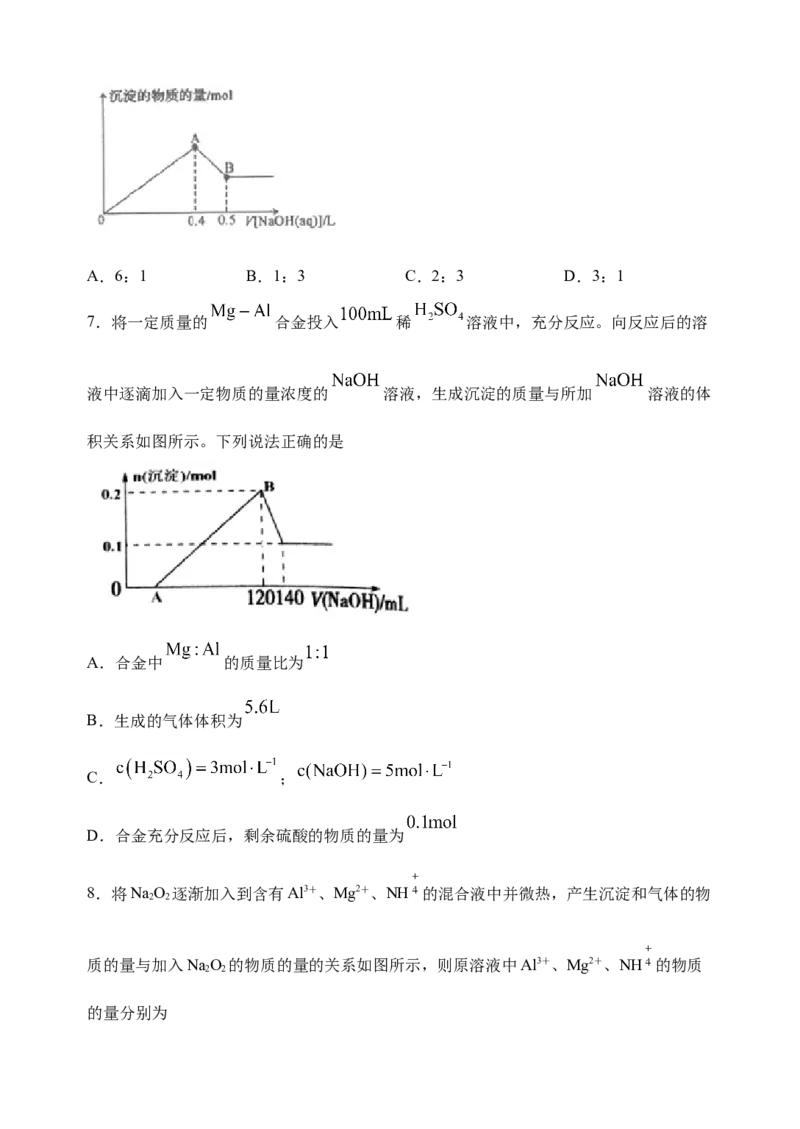
7.将一定质量的 合金投入 稀 溶液中,充分反应。向反应后的溶
液中逐滴加入一定物质的量浓度的 溶液,生成沉淀的质量与所加 溶液的体
积关系如图所示。下列说法正确的是
A.合金中 的质量比为
B.生成的气体体积为
C. ;
D.合金充分反应后,剩余硫酸的物质的量为
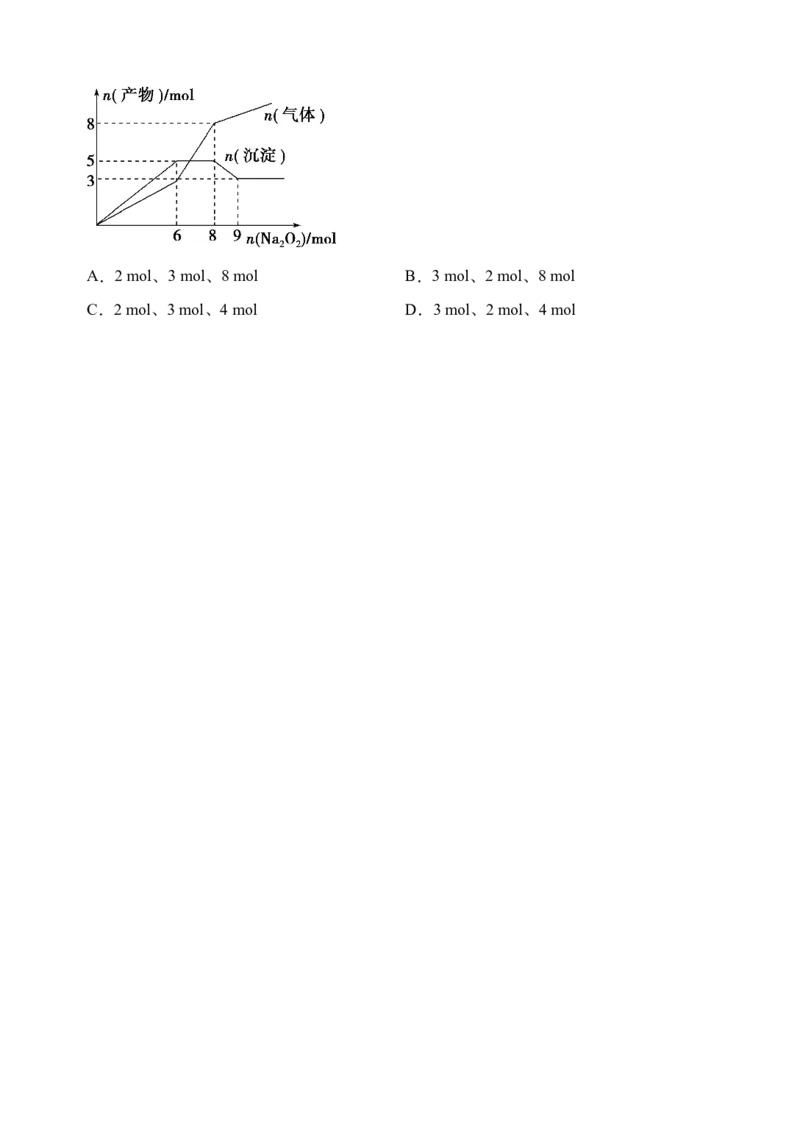
8.将NaO 逐渐加入到含有Al3+、Mg2+、NH 的混合液中并微热,产生沉淀和气体的物
2 2
质的量与加入NaO 的物质的量的关系如图所示,则原溶液中Al3+、Mg2+、NH 的物质
2 2
的量分别为A.2 mol、3 mol、8 mol B.3 mol、2 mol、8 mol
C.2 mol、3 mol、4 mol D.3 mol、2 mol、4 mol