文档内容
微专题突破2 氧化还原反应 离子反应二
一、选择题
1.(2024·徐州模拟)下列各组离子能大量共存的是
A.在c(H+)=1 mol·L-1的溶液中:NH、Al3+、OH-、SO 2-
4
B.在新制氯水中:Fe2+、Mg2+、NO -、Cl-
3
C.在加入NH HCO 产生气体的溶液中:Na+、Ba2+、Cl-、NO -
4 3 3
D.加入Al片能产生H 的溶液:NH、Ca2+、HCO -、NO -
2 3 3
2.(2023·盐城三模)周期表中第ⅦA族元素及其化合物应用广泛。氢氟酸可用作雕刻玻璃;
SOCl 可溶于苯、CCl 等有机溶剂,极易水解;卤素互化物(如ICl、IF )具有强氧化性;卤化银具有感光
2 4 3
性(HCO 的电离平衡常数分别为:K =4.3×10-7、K =5.6×10-11;HClO的电离平衡常数为 K =
2 3 a1 a2 a
3.0×10-8)。下列化学反应表示正确的是
A.Cl 溶于水:Cl+HO=2H++ClO-+Cl-
2 2 2
B.ICl溶于NaOH溶液:ICl+2OH-=Cl-+IO-+HO
2
C.SOCl 溶于水:SOCl +2HO=4H++SO+2Cl-
2 2 2
D.少量CO 通入NaClO溶液中:CO+2ClO-+HO=2HClO+CO
2 2 2
3.(2024·常州初测)下列实验对应的离子方程式不正确的是
A.将碳酸氢钙溶液与过量的澄清石灰水混合:HCO -+Ca2++OH-=CaCO ↓+HO
3 3 2
B.将少量SO 通入NaClO溶液:SO +HO+2ClO-=SO2-+2HClO
2 2 2 3
C.用过量氨水吸收工业尾气中的SO :2NH ·HO+SO =2NH+SO2-+HO
2 3 2 2 3 2
D.向氨水中滴入少量硝酸银溶液:Ag++2NH ·HO=[Ag(NH )]++2HO
3 2 3 2 2
4.(2024·北京卷)下列方程式与所给事实不相符的是
A.海水提溴过程中,用氯气氧化苦卤得到溴单质:2Br-+Cl=Br +2Cl-
2 2
B.用绿矾(FeSO ·7HO)将酸性工业废水中的Cr O2-转化为Cr3+:6Fe2++Cr O2-+14H+=6Fe3+
4 2 2 7 2 7
+2Cr3++7HO
2
C.用5% Na SO 溶液能有效除去误食的Ba2+:SO 2-+Ba2+=BaSO↓
2 4 4 4
D.用NaCO 溶液将水垢中的CaSO 转化为溶于酸的CaCO :Ca2++CO2-=CaCO ↓
2 3 4 3 3 3
5.(2024·镇江模拟)从废定影液[主要含有H+、Ag(SO)3-、HSO 、Br-等微粒]中回收Ag和
2 3 2 2 3
Br 的主要步骤:向该废定影液中加入NaOH调节pH在7.5~8.5之间,然后再加入稍过量NaS溶液沉银,
2 2
过滤、洗涤及干燥,灼烧Ag S制Ag;滤液中通入Cl 氧化Br-,用苯萃取分液。
2 2
下列化学反应表示正确的是
A.[Ag(NH )]OH废液用过量的硝酸处理:[Ag(NH )]++OH-+3H+=Ag++2NH+HO
3 2 3 2 2
B.用铜电极电解CuSO 溶液:2Cu2++2HO====2Cu+O↑+4H+
4 2 2
C.稀硝酸洗涤做过银镜反应的试管:Ag+2H++NO -=Ag++NO↑+HO
3 2
D.CuSO 溶液中加入小粒金属钠:Cu2++2Na=Cu+2Na+
4
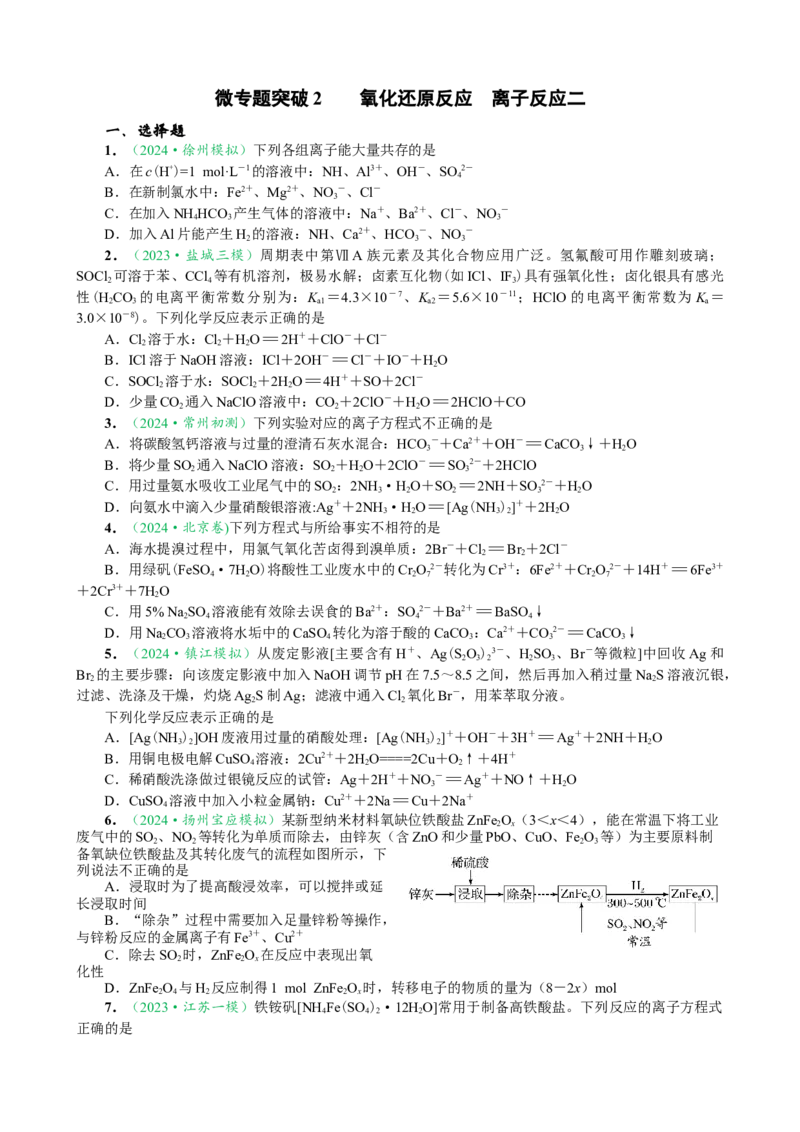
6.(2024·扬州宝应模拟)某新型纳米材料氧缺位铁酸盐ZnFe O(3<x<4),能在常温下将工业
2 x
废气中的SO 、NO 等转化为单质而除去,由锌灰(含ZnO和少量PbO、CuO、Fe O 等)为主要原料制
2 2 2 3
备氧缺位铁酸盐及其转化废气的流程如图所示,下
列说法不正确的是
A.浸取时为了提高酸浸效率,可以搅拌或延
长浸取时间
B.“除杂”过程中需要加入足量锌粉等操作,
与锌粉反应的金属离子有Fe3+、Cu2+
C.除去SO 时,ZnFe O 在反应中表现出氧
2 2 x
化性
D.ZnFe O 与H 反应制得1 mol ZnFe O 时,转移电子的物质的量为(8-2x)mol
2 4 2 2 x
7.(2023·江苏一模)铁铵矾[NH Fe(SO )·12HO]常用于制备高铁酸盐。下列反应的离子方程式
4 4 2 2
正确的是微专题突破2 氧化还原反应 离子反应二
A.铁铵矾溶液与氨水混合反应:Fe3++3OH-=Fe(OH)↓
3
B.向铁铵矾溶液中通入HS气体:2Fe3++HS=2Fe2++S↓+2H+
2 2
C.在强碱溶液中,铁铵矾与次氯酸钠反应生成NaFeO:3ClO-+2Fe3++6OH-=2FeO2-+3Cl-+HO+4H+
2 4 4 2
D.向铁铵矾溶液中加入过量 Ba(OH) 溶液:Fe3++2SO 2-+2Ba2++3OH-=Fe(OH)↓+
2 4 3
2BaSO↓
4
8.(2024·江苏预测卷改编)下列涉及SO 参与反应的离子方程式中,正确的是
2
A.过量SO 通入NaCO 溶液:CO2-+2SO +HO=2HSO -+CO
2 2 3 3 2 2 3 2
B.过量SO 通入NaS溶液:3SO +2NaS=3S↓+2NaSO
2 2 2 2 2 3
C.SO 通入碘水:SO +I+2HO=2H++S +2HI
2 2 2 2 O2−
4
D.少量SO 通入Ca(ClO) 溶液:SO +Ca2++2ClO-+HO=CaSO↓+2HClO
2 2 2 2 3
9.(2024·江苏押题卷)下列离子方程式,能正确解释沉淀产生原因的是
A.向FeCl 溶液中加入氨水,产生红褐色沉淀:Fe3++3OH-=Fe(OH)↓
3 3
B.向甲醛中加入足量新制Cu(OH) 悬浊液,加热,产生砖红色沉淀:HCHO+4Cu(OH) +2OH-
2 2
Δ—\s\up 4()CO2-+2Cu O↓+6HO
—→ 3 2 2
C.向饱和NaCO 溶液中通入CO,产生白色沉淀:Na++CO2-+CO+HO=NaHCO ↓
2 3 2 3 2 2 3
D.向Ba(NO ) 溶液中通入SO ,产生白色沉淀:Ba2++SO +HO=BaSO↓+2H+
3 2 2 2 2 3
10.(2024·南通二模)第四周期过渡元素形成的化合物具有重要作用。黄铜(CuFeS )用
2
Fe (SO ) 溶液浸泡后生成单质硫,所得CuSO 溶液可用于制取纳米Cu O,Cu O能与酸发生歧化反应。
2 4 3 4 2 2
CuO-TiO 可用于低温下催化氧化HCHO:HCHO(g)+O(g)============CO(g)+HO(l)。CoCl 具有
x 2 2 2 2 3
强氧化性,可与盐酸反应生成氯气。由 NaNO 、Co(NO )、HO 和 CHCOOH 反应制备的配合物
2 3 2 2 3
Na[Co(NO )]可应用于K+的鉴定。下列化学反应表示正确的是
3 2 6
A.Cu O与稀硫酸反应:Cu O+2H+=2Cu2++HO
2 2 2
B.Fe (SO ) 溶液和CuFeS 反应:CuFeS+4Fe3+=5Fe2++Cu2++2S
2 4 3 2 2
C.Co(OH) 与足量盐酸反应:Co(OH)+3HCl=CoCl +3HO
3 3 3 2
D.制备Na[Co(NO )]的反应:12NO2-+2Co2++HO+2H+=2[Co(NO )]3-+2HO
3 2 6 2 2 2 6 2
11.(2024·南外、金陵中学、海安中学三校模拟改编)下列反应表示正确的是
A.HClO在水中见光分解:HClO+HO=O↑+H++Cl-
2 2
B.惰性电极电解氯化镁溶液:2Cl-+2HO====2OH-+Cl↑+H↑
2 2 2
C.NaClO碱性溶液与Fe(OH) 制NaFeO:3ClO-+4OH-+2Fe(OH)=2FeO2-+3Cl-+5HO
3 2 4 3 4 2
D.用硫代硫酸钠溶液脱氯:SO2-+2Cl+3HO=2SO2-+4Cl-+6H+
2 3 2 2 3
12.(2024·南京玄武高级中学二模)[Cu(NH )]SO ·HO可用作杀虫剂,其制备步骤如下。
3 4 4 2
步骤1:向足量铜粉与一定量稀硫酸的混合物中通入热空气,当铜粉不再溶解时,过滤得滤液。
步骤2:向步骤1所得滤液中边搅拌边滴加氨水,沉淀先增加后减少。当沉淀完全溶解时,停止滴加氨水。
步骤3:向步骤2所得溶液中加入95%乙醇,析出深蓝色[Cu(NH )]SO ·HO晶体。
3 4 4 2
下列说法正确的是
A.步骤1发生反应的离子方程式为Cu+O+4H+====Cu2++2HO
2 2
B.步骤2所得溶液中大量存在的离子有Cu2+、NH、SO 2-、OH-
4
C.步骤3加入95%乙醇的目的是降低[Cu(NH )]SO ·HO的溶解量
3 4 4 2
D.[Cu(NH )]2+中有12个配位键
3 4
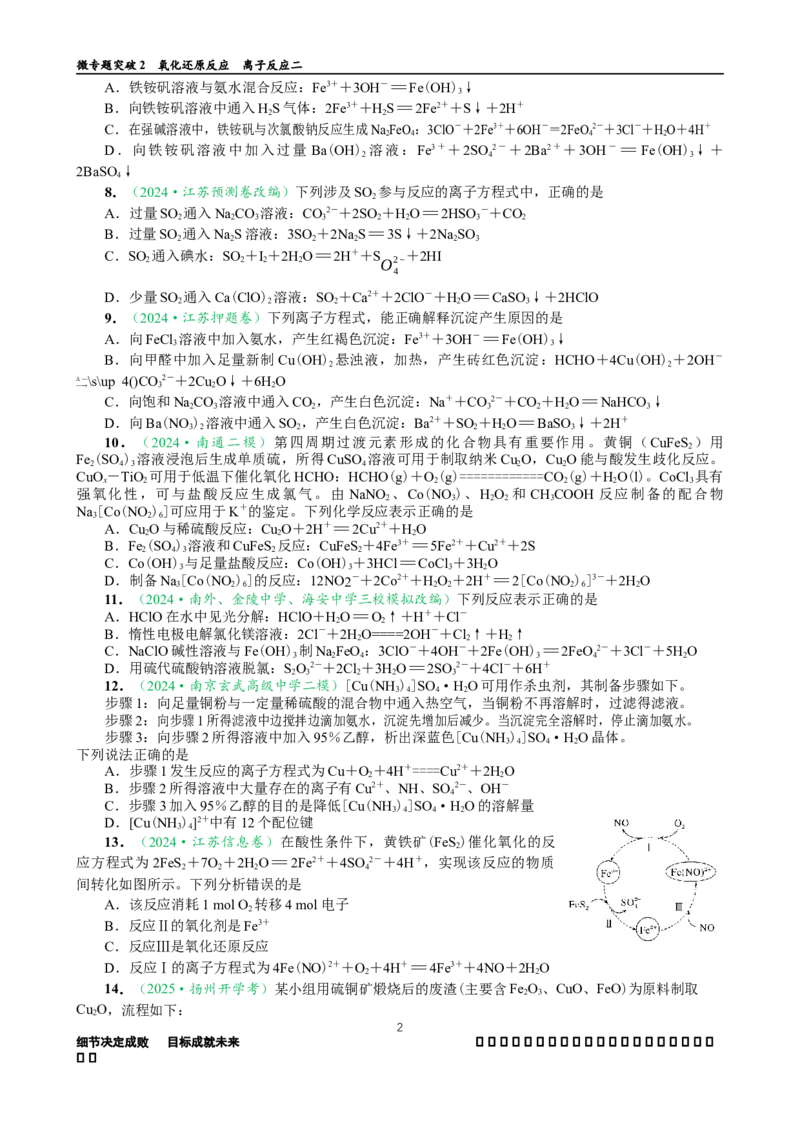
13.(2024·江苏信息卷)在酸性条件下,黄铁矿(FeS)催化氧化的反
2
应方程式为2FeS +7O +2HO=2Fe2++4SO 2-+4H+,实现该反应的物质
2 2 2 4
间转化如图所示。下列分析错误的是
A.该反应消耗1 mol O 转移4 mol电子
2
B.反应Ⅱ的氧化剂是Fe3+
C.反应Ⅲ是氧化还原反应
D.反应Ⅰ的离子方程式为4Fe(NO)2++O+4H+=4Fe3++4NO+2HO
2 2
14.(2025·扬州开学考)某小组用硫铜矿煅烧后的废渣(主要含Fe O、CuO、FeO)为原料制取
2 3
Cu O,流程如下:
2
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找下列说法正确的是
A.“酸浸”时使用98%的浓硫酸代替稀硫酸有利于提高原料利用率
B.“氧化”后溶液中存在的阳离子有:H+、Fe3+、Fe2+、Cu2+
C.“调节pH”时可以选择CuO或Cu(OH)
2
D.“还原”过程中消耗的CuSO 、NH 的物质的量之比为1∶4
4 2 4
15.(2023·江苏百校联考)室温下进行下列实验,根据实验操作和现象所得到的结论不正确的是
选项 实验操作和现象 实验目的或结论
A 向PbO 中滴加浓盐酸,出现黄绿色气体 PbO 具有氧化性
2 2
B 向溶有SO 的BaCl 溶液中通入气体X,出现白色沉淀 气体X一定具有强氧化性
2 2
向FeSO 溶液中先加入KSCN溶液,无现象,再加入HO 溶
C 4 2 2 Fe2+具有还原性
液,溶液变成血红色
D 向KI溶液中滴加几滴NaNO 溶液,再滴加淀粉溶液后变蓝色 NO的氧化性比I 的强
2 2
二、填空题
16.(2024·江苏省南通市三模)碲(Te)是元素周期表中第ⅥA元素,广泛应用于半导体材料、特
殊合金等领域。从碲铜渣中(含Cu Te及少量CuTeO 、Pb等化合物)可提取单质碲。
2 4
Ⅰ.干法炼碲
(1)将碲铜渣加热熔化后,向其中分批加入一定量还原碳粉,控制反应温度400~500℃,发生反应
2CuTeO+4C==========Cu Te+Te+4CO↑。每消耗1 mol CuTeO,反应中转移电子的物质的量为
4 2 2 4
_______mol。
(2)已知:常温下硫磺、单质碲的沸点分别为445℃、1 390℃。将还原后的碲铜渣与稍过量硫磺混
合加热,得到Cu S、Te和硫磺混合物。将混合物置于真空炉中,控制蒸馏温度1050℃,可收集得到较纯
2
净的Te.在真空炉中进行蒸馏的原因是______________________________________________。
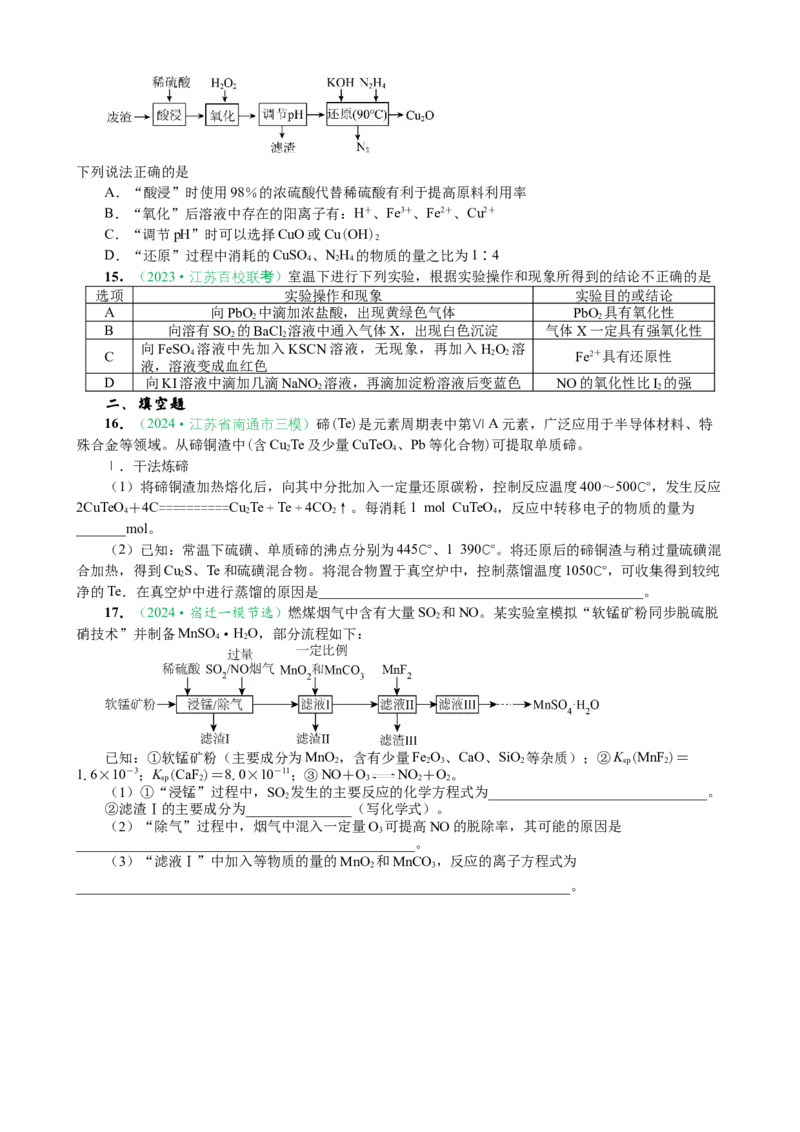
17.(2024·宿迁一模节选)燃煤烟气中含有大量SO 和NO。某实验室模拟“软锰矿粉同步脱硫脱
2
硝技术”并制备MnSO ·HO,部分流程如下:
4 2
已知:①软锰矿粉(主要成分为MnO ,含有少量Fe O、CaO、SiO 等杂质);②K (MnF )=
2 2 3 2 sp 2
1.6×10-3;K (CaF )=8.0×10-11;③NO+O NO +O。
sp 2 3 2 2
(1)①“浸锰”过程中,SO 发生的主要反应的化学方程式为_______________________________。
2
②滤渣Ⅰ的主要成分为_______________(写化学式)。
(2)“除气”过程中,烟气中混入一定量O 可提高NO的脱除率,其可能的原因是
3
________________________________________________。
(3)“滤液Ⅰ”中加入等物质的量的MnO 和MnCO ,反应的离子方程式为
2 3
______________________________________________________________________。