文档内容
第14讲 物质制备与实验方案设计考点透视二
1.(2024·江苏盐城市高三期中)铬和钒具有广泛用途。从含高价钒(Ⅴ)、铬(Ⅵ)废水中提取铬和
钒的一种流程如下图所示:
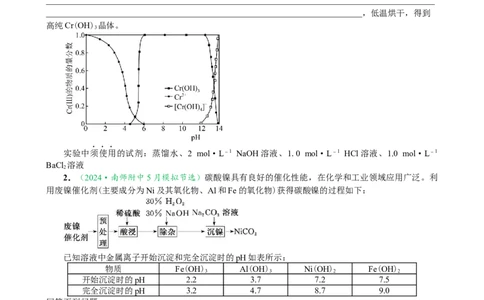
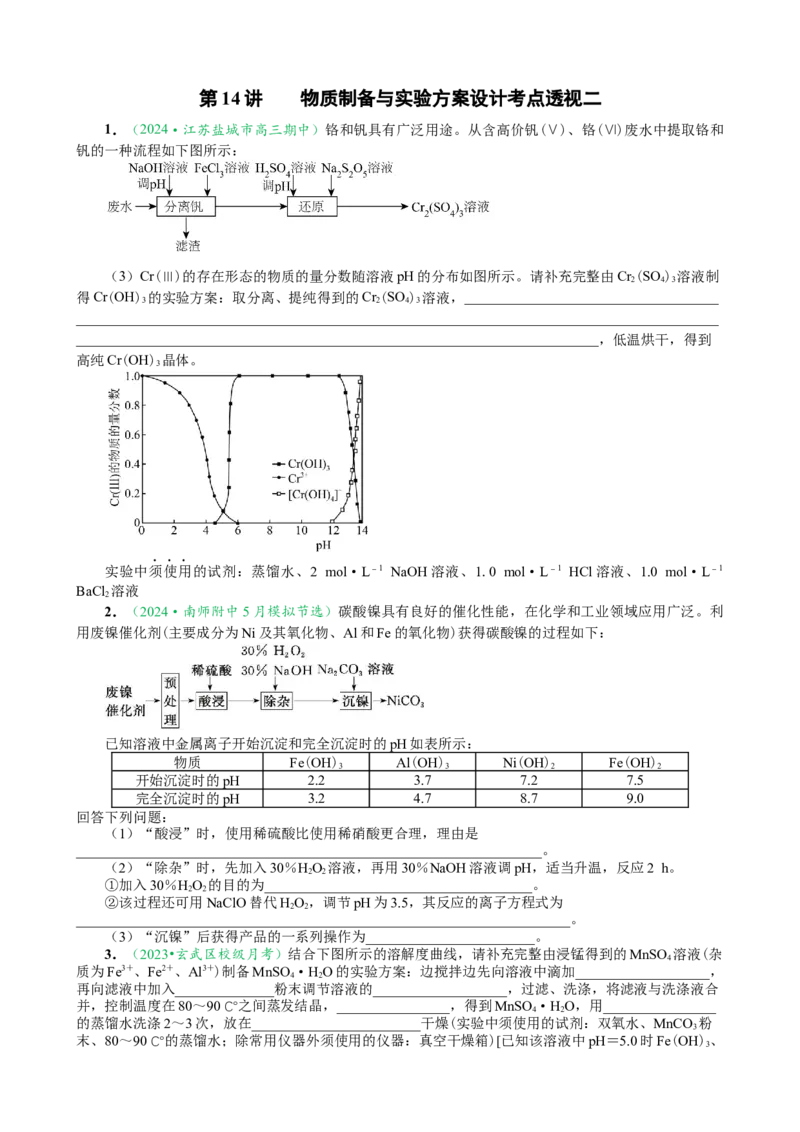
(3)Cr(Ⅲ)的存在形态的物质的量分数随溶液pH的分布如图所示。请补充完整由Cr (SO ) 溶液制
2 4 3
得Cr(OH) 的实验方案:取分离、提纯得到的Cr (SO ) 溶液,____________________________________
3 2 4 3
___________________________________________________________________________________________
__________________________________________________________________________,低温烘干,得到
高纯Cr(OH) 晶体。
3
实验中须使用的试剂:蒸馏水、2 mol·L-1 NaOH溶液、1.0 mol·L-1 HCl溶液、1.0 mol·L-1
BaCl 溶液
2
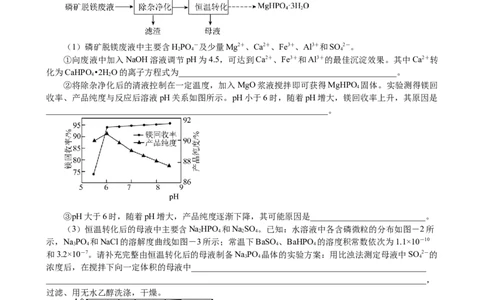
2.(2024·南师附中5月模拟节选)碳酸镍具有良好的催化性能,在化学和工业领域应用广泛。利
用废镍催化剂(主要成分为Ni及其氧化物、Al和Fe的氧化物)获得碳酸镍的过程如下:
已知溶液中金属离子开始沉淀和完全沉淀时的pH如表所示:
物质 Fe(OH) Al(OH) Ni(OH) Fe(OH)
3 3 2 2
开始沉淀时的pH 2.2 3.7 7.2 7.5
完全沉淀时的pH 3.2 4.7 8.7 9.0
回答下列问题:
(1)“酸浸”时,使用稀硫酸比使用稀硝酸更合理,理由是
__________________________________________________________________。
(2)“除杂”时,先加入30%HO 溶液,再用30%NaOH溶液调pH,适当升温,反应2 h。
2 2
①加入30%HO 的目的为______________________________________。
2 2
②该过程还可用NaClO替代HO,调节pH为3.5,其反应的离子方程式为
2 2
______________________________________________________________________。
(3)“沉镍”后获得产品的一系列操作为________________________。
3.(2023•玄武区校级月考)结合下图所示的溶解度曲线,请补充完整由浸锰得到的MnSO 溶液(杂
4
质为Fe3+、Fe2+、Al3+)制备MnSO ·HO的实验方案:边搅拌边先向溶液中滴加___________________,
4 2
再向滤液中加入______________粉末调节溶液的___________________,过滤、洗涤,将滤液与洗涤液合
并,控制温度在80~90 ℃之间蒸发结晶,________________,得到MnSO ·HO,用________________
4 2
的蒸馏水洗涤2~3次,放在________________________干燥(实验中须使用的试剂:双氧水、MnCO 粉
3
末、80~90 ℃的蒸馏水;除常用仪器外须使用的仪器:真空干燥箱)[已知该溶液中pH=5.0时Fe(OH)、
3微专题突破14 物质制备与实验方案设计考点透视二
Al(OH) 沉淀完全;pH=7.8时Mn(OH) 开始沉淀;pH=8.8时Fe(OH) 沉淀完全]。
3 2 2
的
4.(2024·苏锡常镇二模)实验室用磷矿脱镁废液制备MgHPO•3HO 实验过程可表示为:
4 2
(1)磷矿脱镁废液中主要含HPO -及少量Mg2+、Ca2+、Fe3+、Al3+和SO 2-。
2 4 4
①向废液中加入NaOH溶液调节pH为4.5,可达到Ca2+、Fe3+和Al3+的最佳沉淀效果。其中Ca2+转
化为CaHPO •2HO的离子方程式为___________________________________________________。
4 2
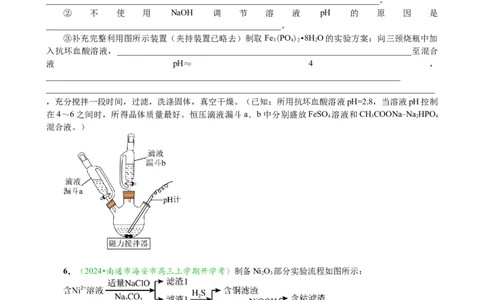
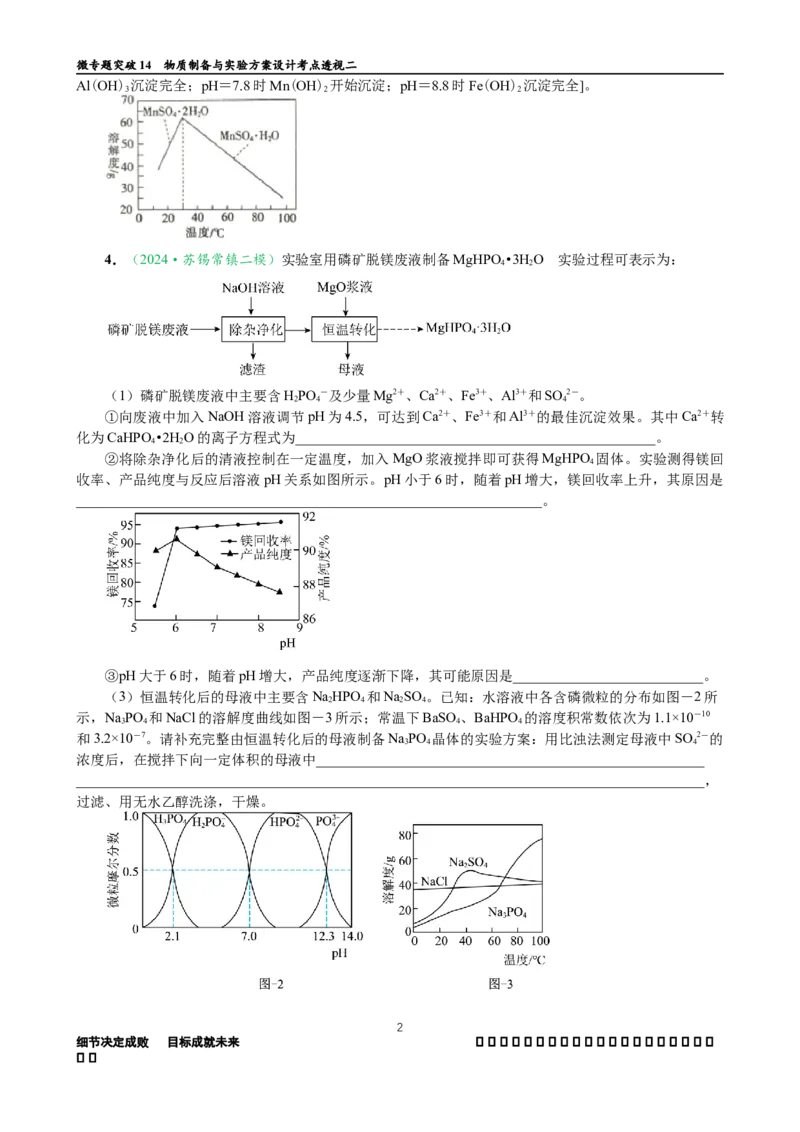
②将除杂净化后的清液控制在一定温度,加入MgO浆液搅拌即可获得MgHPO 固体。实验测得镁回
4
收率、产品纯度与反应后溶液pH关系如图所示。pH小于6时,随着pH增大,镁回收率上升,其原因是
__________________________________________________________________。
③pH大于6时,随着pH增大,产品纯度逐渐下降,其可能原因是___________________________。
(3)恒温转化后的母液中主要含NaHPO 和NaSO 。已知:水溶液中各含磷微粒的分布如图-2所
2 4 2 4
示,NaPO 和NaCl的溶解度曲线如图-3所示;常温下BaSO、BaHPO 的溶度积常数依次为1.1×10-10
3 4 4 4
和3.2×10-7。请补充完整由恒温转化后的母液制备NaPO 晶体的实验方案:用比浊法测定母液中SO 2-的
3 4 4
浓度后,在搅拌下向一定体积的母液中_______________________________________________________
_________________________________________________________________________________________,
过滤、用无水乙醇洗涤,干燥。
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找5.(2024·南通市二模)实验室以FeS 为原料制备磷酸亚铁晶体[Fe (PO )•8HO],其部分实验过
2 3 4 2 2
程如下:
(1)将一定体积98%的浓硫酸稀释为200 mL30%的硫酸,除量筒外,还必须使用的玻璃仪器有
____________________________。
(2)检验“还原”已完全的实验操作为_______________________________________________。
(3)向过滤后的滤液中加入NaHPO ,并用氨水或CHCOONa调节溶液pH,“共沉淀”生成
2 4 3
Fe (PO )•8HO。
3 4 2 2
①若使用CHCOONa调节溶液pH,“共沉淀”反应的离子方程式为
3
______________________________________________________________________________。
② 不 使 用 NaOH 调 节 溶 液 pH 的 原 因 是
_______________________________________________________。
③补充完整利用图所示装置(夹持装置已略去)制取Fe (PO )•8HO的实验方案:向三颈烧瓶中加
3 4 2 2
入抗坏血酸溶液,_____________________________________________________________________至混合
液 pH≈ 4 ,
___________________________________________________________________________________
___________________________________________________________________________________________
,充分搅拌一段时间,过滤,洗涤固体,真空干燥。(已知:所用抗坏血酸溶液pH=2.8,当溶液pH控制
在4~6之间时,所得晶体质量最好。恒压滴液漏斗a.b中分别盛放FeSO 溶液和CHCOONa-NaHPO
4 3 2 4
混合液。)
6.(2024•南通市海安市高三上学期开学考)制备Ni O 部分实验流程如图所示:
2 3
(5)含Ni2+溶液中含有硫酸,加NaCO 之前,NaClO和Fe2+反应离子方程式是
2 3
_________________________________________________________________________。
(6)已知:在空气中煅烧NiCO,其热重曲线如图所示(镍的相对原子质量为59)。补充完整以滤液
3
3(NiSO 溶液)制取Ni O 的实验方案:_________________________________________________________
4 2 3
___________________________________________________________________________________________
_________________________________________。(需使用的试剂:1 mol·L-1 NaCO 溶液、1 mol·L-1
2 3
HCl溶液、1 mol·L-1 BaCl 溶液)
2微专题突破14 物质制备与实验方案设计考点透视二
7.(2024·泰州市期中)连二亚硫酸钠(NaSO)广泛应用于造纸等行业。NaSO 易被氧化,129℃
2 2 4 2 2 4
时分解,在碱性条件下较稳定,易溶于水,不溶于乙醇。实验室用NaBH 碱性溶液和NaHSO 酸性溶液
4 3
制取NaSO,实验室制备装置如题图所示。
2 2 4
(1)实验前需打开K通入一段时间氮气,其目的是__________________________________。
(2)在10℃~35℃下,向盛有一定浓度的NaHSO 溶液容器中滴加NaBH 溶液,生成NaSO 和
3 4 2 2 4
NaBO ,制备NaSO 的化学方程式为________________________________________________________。
2 2 2 4
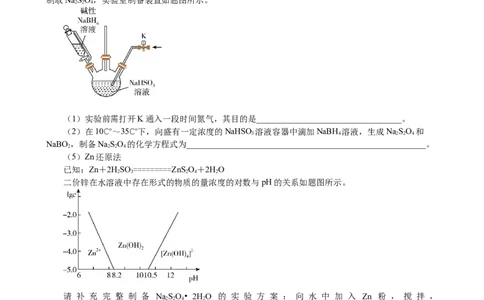
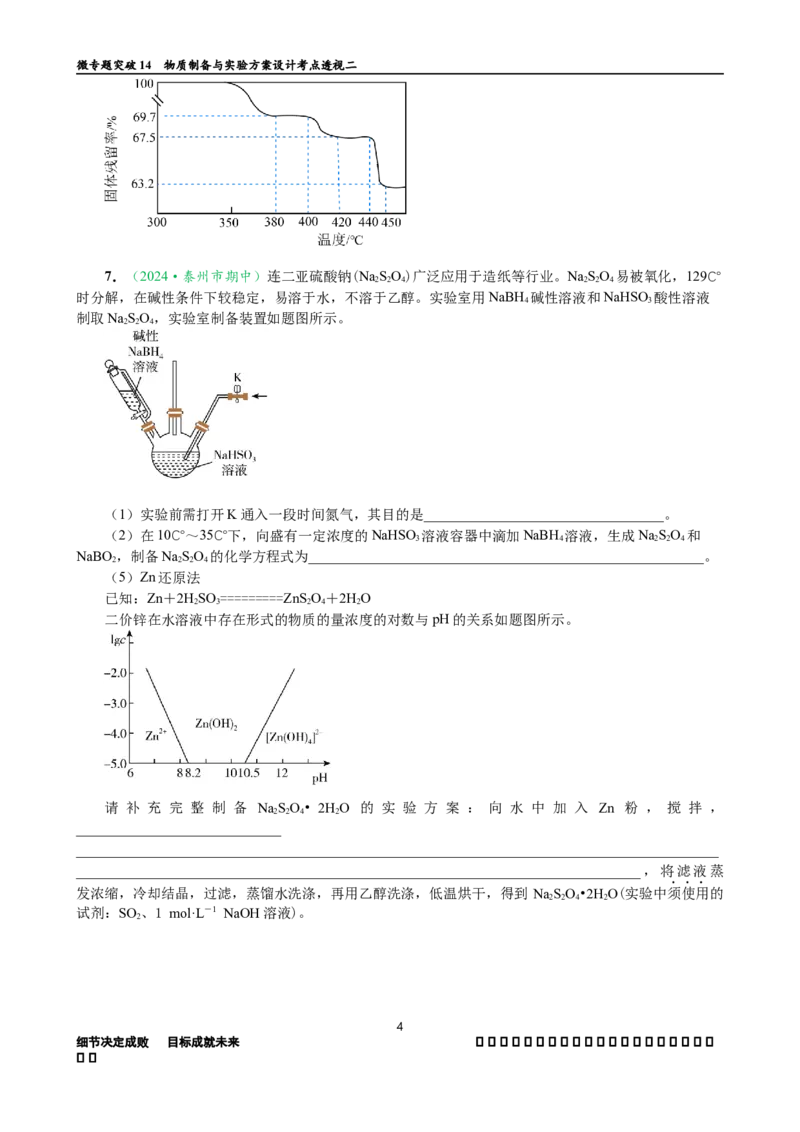
(5)Zn还原法
已知:Zn+2HSO=========ZnS O+2HO
2 3 2 4 2
二价锌在水溶液中存在形式的物质的量浓度的对数与pH的关系如题图所示。
请 补 充 完 整 制 备 NaSO• 2HO 的 实 验 方 案 : 向 水 中 加 入 Zn 粉 , 搅 拌 ,
2 2 4 2
_____________________________
___________________________________________________________________________________________
________________________________________________________________________________,将滤液蒸
发浓缩,冷却结晶,过滤,蒸馏水洗涤,再用乙醇洗涤,低温烘干,得到 NaSO•2HO(实验中须使用的
2 2 4 2
试剂:SO 、1 mol·L-1 NaOH溶液)。
2
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找