文档内容
微专题突破14 物质制备与实验方案设计考点透视
1.(2023·连云港高级中学高三下学期5月模拟)K[Fe(C O)]·3HO(三草酸合铁酸钾)为亮绿色
3 2 4 3 2
晶体,难溶于乙醇,受热易分解,110 ℃时可失去结晶水,230 ℃时发生分解,可用于晒制蓝图。
(1)K[Fe(C O)]·3HO的制备。取一定量的草酸钾加水溶解,加热溶液至微沸后,在搅拌下向其
3 2 4 3 2
中加入FeCl 溶液,充分反应后得到亮绿色透明溶液,经过一系列操作得到K[Fe(C O)]·3HO。
3 3 2 4 3 2
①制取K[Fe(C O)]·3HO的化学方程式为:
3 2 4 3 2
______________________________________________________________________________。
②若加热温度过高,会导致K[Fe(C O)]·3HO的产率偏低,其原因是:
3 2 4 3 2
____________________________________________________________________________。
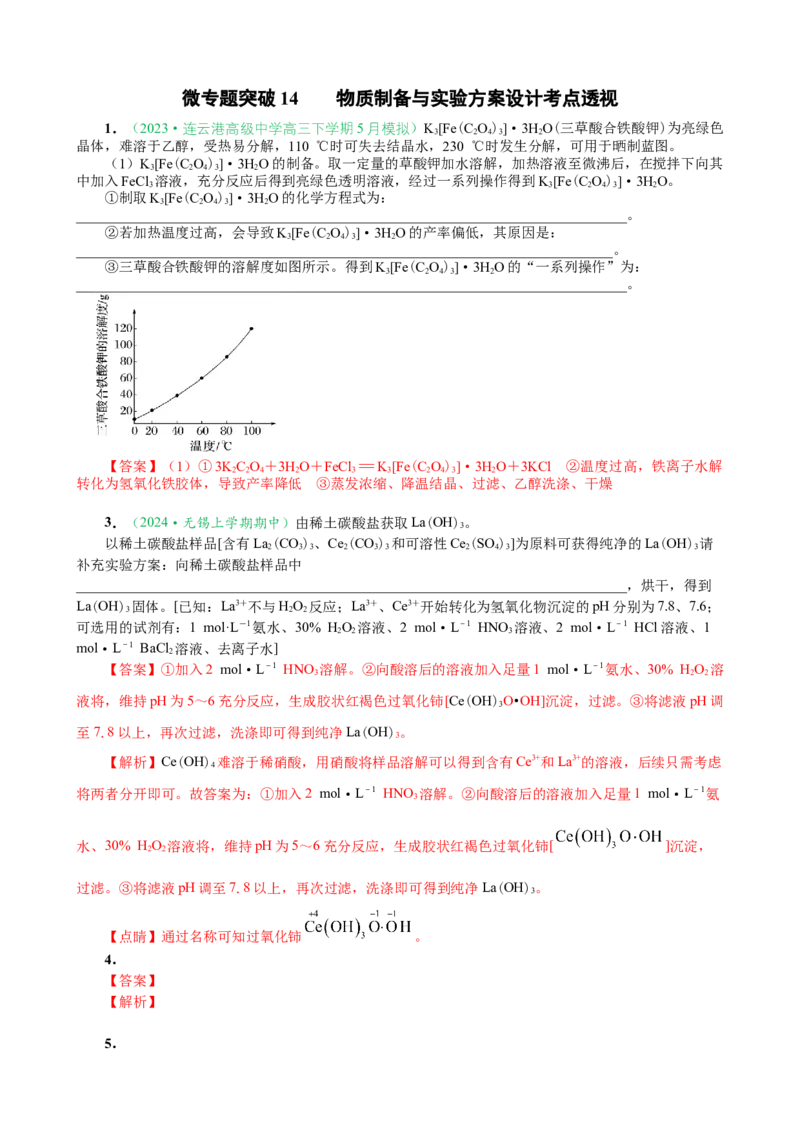
③三草酸合铁酸钾的溶解度如图所示。得到K[Fe(C O)]·3HO的“一系列操作”为:
3 2 4 3 2
______________________________________________________________________________。
【答案】(1)①3KC O +3HO+FeCl =K[Fe(C O)]·3HO+3KCl ②温度过高,铁离子水解
2 2 4 2 3 3 2 4 3 2
转化为氢氧化铁胶体,导致产率降低 ③蒸发浓缩、降温结晶、过滤、乙醇洗涤、干燥
3.(2024·无锡上学期期中)由稀土碳酸盐获取La(OH)。
3
以稀土碳酸盐样品[含有La(CO)、Ce (CO) 和可溶性Ce (SO )]为原料可获得纯净的La(OH) 请
2 3 3 2 3 3 2 4 3 3
补充实验方案:向稀土碳酸盐样品中
______________________________________________________________________________,烘干,得到
La(OH) 固体。[已知:La3+不与HO 反应;La3+、Ce3+开始转化为氢氧化物沉淀的pH分别为7.8、7.6;
3 2 2
可选用的试剂有:1 mol·L-1氨水、30% HO 溶液、2 mol·L-1 HNO 溶液、2 mol·L-1 HCl溶液、1
2 2 3
mol·L-1 BaCl 溶液、去离子水]
2
【答案】①加入2 mol·L-1 HNO 溶解。②向酸溶后的溶液加入足量1 mol·L-1氨水、30% HO 溶
3 2 2
液将,维持pH为5~6充分反应,生成胶状红褐色过氧化铈[Ce(OH)O•OH]沉淀,过滤。③将滤液pH调
3
至7.8以上,再次过滤,洗涤即可得到纯净La(OH)。
3
【解析】Ce(OH) 难溶于稀硝酸,用硝酸将样品溶解可以得到含有Ce3+和La3+的溶液,后续只需考虑
4
将两者分开即可。故答案为:①加入2 mol·L-1 HNO 溶解。②向酸溶后的溶液加入足量1 mol·L-1氨
3
水、30% HO 溶液将,维持pH为5~6充分反应,生成胶状红褐色过氧化铈[ ]沉淀,
2 2
过滤。③将滤液pH调至7.8以上,再次过滤,洗涤即可得到纯净La(OH)。
3
【点睛】通过名称可知过氧化铈 。
4.
【答案】
【解析】
5.微专题突破1 氧化还原反应
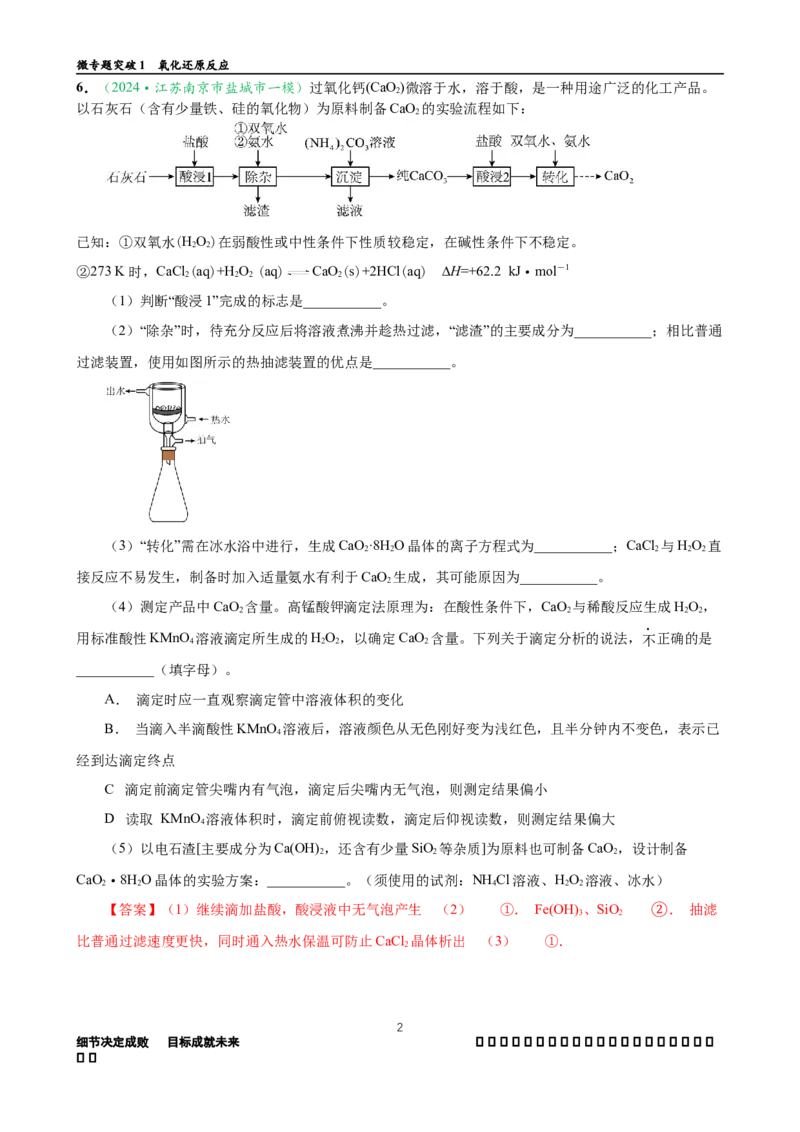
6.(2024·江苏南京市盐城市一模)过氧化钙(CaO)微溶于水,溶于酸,是一种用途广泛的化工产品。
2
以石灰石(含有少量铁、硅的氧化物)为原料制备CaO 的实验流程如下:
2
已知:①双氧水(HO)在弱酸性或中性条件下性质较稳定,在碱性条件下不稳定。
2 2
②273 K时,CaCl (aq)+H O (aq) CaO(s)+2HCl(aq) ∆H=+62.2 kJ·mol-1
2 2 2 2
(1)判断“酸浸1”完成的标志是___________。
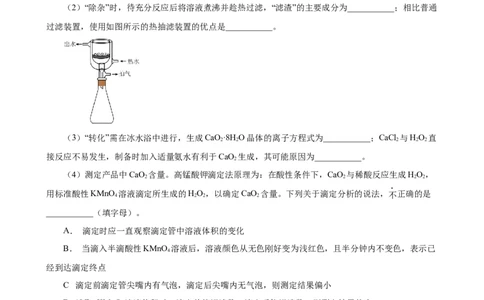
(2)“除杂”时,待充分反应后将溶液煮沸并趁热过滤,“滤渣”的主要成分为___________;相比普通
过滤装置,使用如图所示的热抽滤装置的优点是___________。
(3)“转化”需在冰水浴中进行,生成CaO·8H O晶体的离子方程式为___________;CaCl 与HO 直
2 2 2 2 2
接反应不易发生,制备时加入适量氨水有利于CaO 生成,其可能原因为___________。
2
(4)测定产品中CaO 含量。高锰酸钾滴定法原理为:在酸性条件下,CaO 与稀酸反应生成HO,
2 2 2 2
用标准酸性KMnO 溶液滴定所生成的HO,以确定CaO 含量。下列关于滴定分析的说法,不正确的是
4 2 2 2
___________(填字母)。
A. 滴定时应一直观察滴定管中溶液体积的变化
B. 当滴入半滴酸性KMnO 溶液后,溶液颜色从无色刚好变为浅红色,且半分钟内不变色,表示已
4
经到达滴定终点
.
C 滴定前滴定管尖嘴内有气泡,滴定后尖嘴内无气泡,则测定结果偏小
.
D 读取 KMnO 溶液体积时,滴定前俯视读数,滴定后仰视读数,则测定结果偏大
4
(5)以电石渣[主要成分为Ca(OH) ,还含有少量SiO 等杂质]为原料也可制备CaO,设计制备
2 2 2
CaO·8HO晶体的实验方案:___________。(须使用的试剂:NH Cl溶液、HO 溶液、冰水)
2 2 4 2 2
【答案】(1)继续滴加盐酸,酸浸液中无气泡产生 (2) ①. Fe(OH) 、SiO . 抽滤
3 2
比普通过滤速度更快,同时通入热水保温可防止CaCl 晶体析出 (3) ①. ②
2
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找②. 氨水与反应生成的HCl中和,
使H+浓度降低以及放出热量,均促进反应向生成CaO 的方向进行 (4)AC (5)在搅拌下,向
2
NH Cl溶液中分批加入电石渣,置于冰水浴中反应一段时间后,过滤;在冰水浴中,边搅拌边向HO 溶
4 2 2
液中缓慢滴加所得滤液,待有大量晶体生成,过滤,用少量冰水洗涤2--3次,干燥
【解析】
【分析】石灰石矿渣经过“酸浸”后产生的溶液中溶质主要为剩余的氯化氢、生成的氯化钙和氯化亚铁、氯
化铁,SiO 不能与酸反应,经过滤除去,然后经加入HO 溶液将氯化亚铁氧化为氯化铁,加入氨水,
2 2 2
HCl与氨水反应产生NH4Cl,氯化铁与氨水反应形成Fe(OH) 沉淀,过滤除去,所得溶液中的溶质主要为
3
氯化钙和新生成的氯化铵,通入碳酸铵溶液时,氯化钙与碳酸铵会反应生成碳酸钙沉淀和氯化铵,所以
过滤后,所得滤液中的溶质主要为NH Cl,纯CaCO 用盐酸酸浸,反应产生CaCl ,向其中加入双氧水及
4 3 2
氨水,反应产生CaO。
2
【小问1详解】
石灰石主要成分是CaCO ,在“酸浸1”时,会发生反应:CaCO +2HCl=CaCl +H O+CO↑,若“酸浸1”完成,
3 3 2 2 2
再滴加稀盐酸时,不能再与CaCO 发生反应产生CO 气体,就无气泡产生;
3 2
【小问2详解】
石灰石主要成分是CaCO ,还含有杂质Fe O、FeO、SiO,加入酸浸时,Fe O、FeO反应产生FeCl 、
3 2 3 2 2 3 3
FeCl ,加入双氧水,FeCl 被氧化变为FeCl ,加入的氨水与FeCl 反应产生Fe(OH) 沉淀,经过滤除去,
2 2 3 3 3
SiO 与HCl不能发生反应,也以沉淀的形式存在,故“除杂”时,待充分反应后将溶液煮沸并趁热过滤,
2
“滤渣”的主要成分为Fe(OH) 、SiO;
3 2
相比普通过滤装置,使用如图所示的热抽滤装置的优点是抽滤比普通过滤速度更快,同时通入热水保温
可防止CaCl 晶体析出;
2
【小问3详解】
“转化”需在冰水浴中进行,CaCl 与氨水、HO 在溶液中反应生成CaO 8HO晶体,同时反应产生
2 2 2 2 2
⋅
NH Cl,该反应的离子方程式为 ;
4
CaCl 与HO 直接反应不易发生,制备时加入适量氨水有利于CaO 生成,其可能原因为氨水与反应生成
2 2 2 2
的HCl中和,使H+浓度降低以及放出热量,均促进反应向生成CaO 的方向进行;
2
【小问4详解】
A.CaO 与稀酸反应生成HO,用标准酸性KMnO 溶液滴定所生成的HO,HO 被KMnO 氧化为O,
2 2 2 4 2 2 2 2 4 2微专题突破1 氧化还原反应
KMnO 被还原为无色Mn2+,因此滴加标准酸性KMnO 溶液时,若无气泡产生,溶于由无色变为浅红色,
4 4
则证明滴定达到终点,而不能一直观察滴定管中溶液体积的变化,A错误;
B.用标准酸性KMnO 溶液滴定HO 溶液时,滴定终点判断方法是:滴入最后半滴酸性KMnO 溶液后,
4 2 2 4
溶液颜色从无色刚好变为浅红色,且半分钟内不变色,表示已经到达滴定终点,B正确;
C.在滴定前滴定管尖嘴内有气泡,滴定后尖嘴内无气泡,则滴定消耗标准酸性KMnO 溶液体积偏大,
4
HO 的质量偏大,因而会导致测定结果偏大,C错误;
2 2
D.读取KMnO 溶液体积时,滴定前俯视读数,V 偏小,滴定后仰视读数,V 偏大,则消耗标准溶液体
4 1 2
积(V -V )就会偏大,最终导致测定结果偏大,D正确;
2 1
故合理选项是AC;(5)电石渣[主要成分为Ca(OH) ,还含有少量SiO 等杂质],以电石渣为原料液
2 2
可以制备CaO ,要求必须使用NH Cl溶液、HO 溶液、冰水,由于NH Cl是强酸弱碱盐,水解使溶液显
2 4 2 2 4
酸性,其水溶液溶解Ca(OH) ,反应产生CaCl 溶液,过滤除去酸性氧化物SiO 等固体杂质,CaCl 溶液
2 2 2 2
与HO 溶液在冰水浴反应,就可得到CaO·8H O晶体。故制备CaO·8H O晶体的实验方案是:在搅拌下,
2 2 2 2 2 2
向NH Cl溶液中分批加入电石渣,置于冰水浴中反应一段时间后,过滤;在冰水浴中,边搅拌边向HO
4 2 2
溶液中缓慢滴加所得滤液,待有大量晶体生成,过滤,用少量冰水洗涤2--3次,干燥。
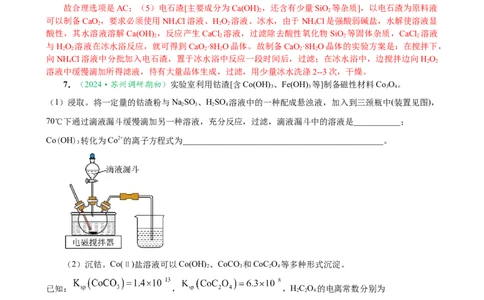
7.(2024·苏州调研期初)实验室利用钴渣[含Co(OH) 、Fe(OH) 等]制备磁性材料Co O。
3 3 3 4
(1)浸取。将一定量的钴渣粉与NaSO 、HSO 溶液中的一种配成悬浊液,加入到三颈瓶中(装置见图),
2 3 2 4
70℃下通过滴液漏斗缓慢滴加另一种溶液,充分反应,过滤,滴液漏斗中的溶液是___________;
Co(OH) 转化为Co2+的离子方程式为_______________________________________________。
3
(2)沉钴。Co(Ⅱ)盐溶液可以Co(OH) 、CoCO 和CoC O 等多种形式沉淀。
2 3 2 4
已知: , ,HC O 的电离常数分别为
2 2 4
、 ,NH ·H O的电离常数为K =1.8×10-5。
3 2 b
①向除杂后含0.100mol·L-1CoSO 溶液中滴加NaOH溶液调节pH,pH=7时开始出现Co(OH) 沉淀,
4 2
继续滴加NaOH溶液至pH=___________时,Co2+沉淀完全[c(Co2+)≤10-5mol·L-1]。
②向除杂后CoSO 溶液中加入HC O 溶液或(NH )C O 溶液作沉淀剂,可得到CoC O 反应
4 2 2 4 4 2 2 4 2 4.
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找的平衡常数K的数值为___________;不能用同浓度的NaC O 溶液
2 2 4
代替(NH )C O 溶液的原因是____________________________________________。
4 2 2 4
为
(3)制备Co O。以CoCl 原料先制得CoCO;然后再制备Co O。
3 4 2 3 3 4
已知:①尿素水溶液呈弱碱性,70℃以上能缓慢水解产生 ,pH为1~3时水解速率对生成
CoCO 沉淀较为适宜。
3
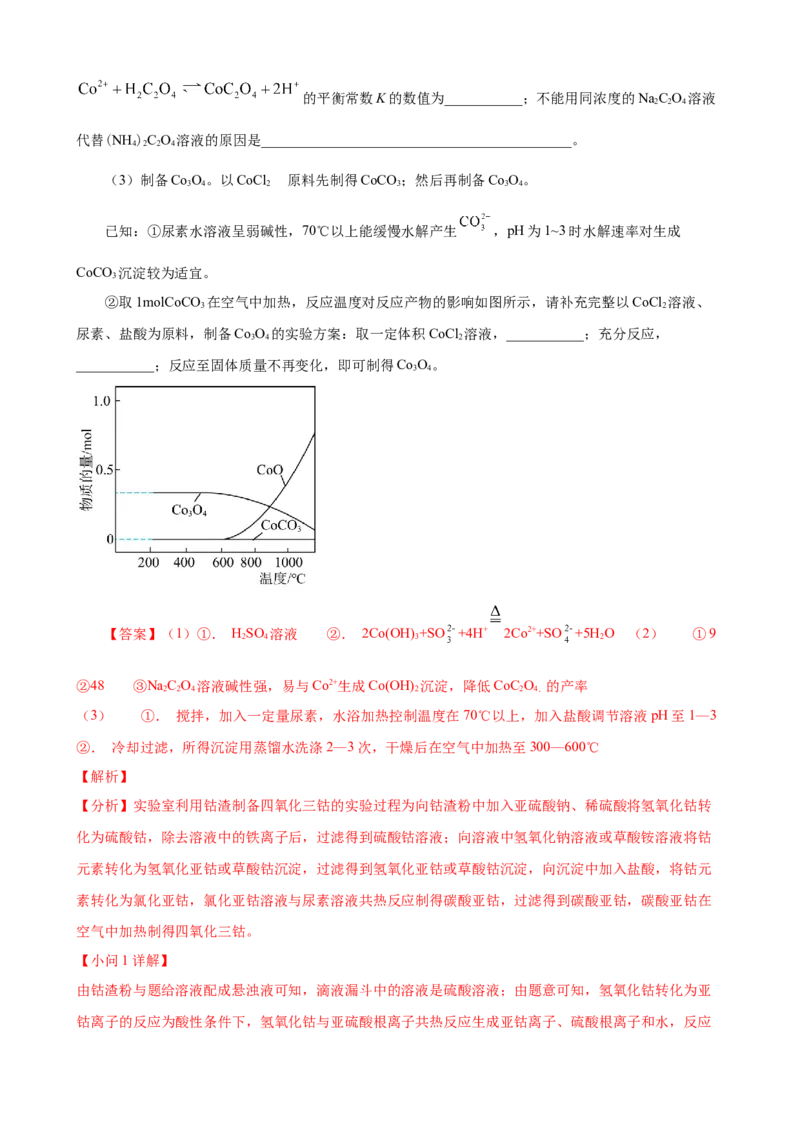
②取1molCoCO 在空气中加热,反应温度对反应产物的影响如图所示,请补充完整以CoCl 溶液、
3 2
尿素、盐酸为原料,制备Co O 的实验方案:取一定体积CoCl 溶液,___________;充分反应,
3 4 2
___________;反应至固体质量不再变化,即可制得Co O。
3 4
【答案】(1)①. HSO 溶液 ②. 2Co(OH) +SO +4H+ 2Co2++SO +5H O (2) ①9
2 4 3 2
②48 ③NaC O 溶液碱性强,易与Co2+生成Co(OH) 沉淀,降低CoC O 的产率
2 2 4 2 2 4.
(3) ①. 搅拌,加入一定量尿素,水浴加热控制温度在70℃以上,加入盐酸调节溶液pH至1—3
②. 冷却过滤,所得沉淀用蒸馏水洗涤2—3次,干燥后在空气中加热至300—600℃
【解析】
【分析】实验室利用钴渣制备四氧化三钴的实验过程为向钴渣粉中加入亚硫酸钠、稀硫酸将氢氧化钴转
化为硫酸钴,除去溶液中的铁离子后,过滤得到硫酸钴溶液;向溶液中氢氧化钠溶液或草酸铵溶液将钴
元素转化为氢氧化亚钴或草酸钴沉淀,过滤得到氢氧化亚钴或草酸钴沉淀,向沉淀中加入盐酸,将钴元
素转化为氯化亚钴,氯化亚钴溶液与尿素溶液共热反应制得碳酸亚钴,过滤得到碳酸亚钴,碳酸亚钴在
空气中加热制得四氧化三钴。
【小问1详解】
由钴渣粉与题给溶液配成悬浊液可知,滴液漏斗中的溶液是硫酸溶液;由题意可知,氢氧化钴转化为亚
钴离子的反应为酸性条件下,氢氧化钴与亚硫酸根离子共热反应生成亚钴离子、硫酸根离子和水,反应微专题突破1 氧化还原反应
的离子方程式为2Co(OH) +SO +4H+ 2Co2++SO +5H O,故答案为:HSO 溶液;2Co(OH) +SO +4H+
3 2 2 4 3
2Co2++SO +5H O;
2
【小问2详解】
①由溶液pH为7时生成氢氧化亚钴沉淀可知,氢氧化亚钴的溶度积K =0.1×(10—7)2=10—15,当溶液中
sp
亚钴离子完全沉淀时,溶液中氢氧根离子浓度为 =10—5mol/L,则溶液的pH为9,故答案为:
9;
②由方程式可知,反应的平衡常数K= = =
=48;草酸钠是强碱弱酸盐,草酸铵是弱酸弱碱盐,草酸钠溶液的碱性强于草酸铵溶液,若用草酸钠溶液
替换草酸铵溶液,会有氢氧化亚钴沉淀生成,导致草酸亚钴的产率降低,所以不能用草酸钠溶液替换草
酸铵溶液,故答案为:48;NaC O 溶液碱性强,易与Co2+生成Co(OH) 沉淀,降低CoC O 的产率;
2 2 4 2 2 4.
【小问3详解】
由题给信息可知,制备四氧化三钴的实验方案取一定体积氯化亚钴溶液,搅拌;充分反应,加入一
定量尿素,水浴加热控制温度在70℃以上,加入盐酸调节溶液pH至1—3,冷却过滤,所得沉淀用蒸馏
水洗涤2—3次,干燥后在空气中加热至300—600℃,反应至固体质量不再变化,即可制得四氧化三钴,
故答案为:搅拌,加入一定量尿素,水浴加热控制温度在70℃以上,加入盐酸调节溶液pH至1—3;冷
却过滤,所得沉淀用蒸馏水洗涤2—3次,干燥后在空气中加热至300—600℃。
8.
9.(2020·江苏高考19题节选)实验室由炼钢污泥(简称铁泥,主要成分为铁的氧化物)制备软磁
性材料α-Fe O。其主要实验流程如下:
2 3
(1)除杂。向“还原”后的滤液中加入NH F溶液,使Ca2+转化为CaF 沉淀除去。若溶液的pH偏低,
4 2
将会导致CaF 沉淀不完全,其原因是______________________________________________________
2
___________________________________________________________________[K (CaF )=5.3×10-9,
sp 2
K(HF)=6.3×10-4]。
a
(2)沉铁。将提纯后的FeSO 溶液与氨水-NH HCO 混合溶液反应,生成FeCO 沉淀。
4 4 3 3
①生成FeCO 沉淀的离子方程式为_________________________________________________________。
3
②设计以FeSO 溶液、氨水-NH HCO 混合溶液为原料,制备FeCO 的实验方案:________________
4 4 3 3
___________________________________________________________________________________________
___________________________________________________________________________________________
__________________________________[FeCO 沉淀需“洗涤完全”,Fe(OH) 开始沉淀的pH=6.5]。
3 2
【答案】(1)pH偏低时,H+与F-结合形成HF,导致溶液中F-浓度减小,CaF 沉淀不完全
2
6
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找(2)①Fe2++HCO -+NH ·HO=FeCO↓+NH+HO或Fe2++HCO -+NH =FeCO↓+NH ②在
3 3 2 3 2 3 3 3
搅拌下向FeSO 溶液中缓慢加入氨水-NH HCO 混合溶液,控制溶液pH不大于6.5;静置后过滤,所得
4 4 3
沉淀用蒸馏水洗涤2~3次;取最后一次洗涤后的滤液,滴加盐酸酸化的BaCl 溶液,不出现白色沉淀
2
【解析】(1)当c(Ca2+)·c2(F-)<K (CaF )时,CaF 不会沉淀出来,HF为弱酸,当pH过低时,
sp 2 2
H+与F-结合成弱电解质HF,则c(F-)减小,导致CaF 沉淀不完全;(2)①Fe2+与HCO -反应生成
2 3
FeCO 沉淀HCO -电离出的H+与NH ·HO结合生成NH,则生成FeCO 沉淀的离子方程式可以写成:Fe2
3 3 3 2 3
++HCO -+NH ·HO=FeCO↓+NH+HO或Fe2++HCO -+NH =FeCO↓+NH;②用FeSO 溶液
3 3 2 3 2 3 3 3 4
和氨水-NH HCO 混合溶液反应生成FeCO,若pH大于6.5,则会生成Fe(OH) 沉淀,故需要控制pH不
4 3 3 2
大于6.5;对生成的FeCO 用蒸馏水洗涤2~3次;因FeCO 表面会附着有SO 2-,若用盐酸酸化的BaCl
3 3 4 2
溶液检验不出SO 2-,则说明FeCO 已洗涤干净。
4 3