文档内容
微专题突破5 无机物的性质、转化与应用
千里之行,始于足下。——老子(学习注意积累)
目标定位
1.知道常见无机物的用途与物质之间的关系。
2.根据物质的性质判断给定的转化能否实现。
3.根据信息结合已有知识判断方程式是否正确。
4.根据化工微流程判断有关说法是否正确。
教学重点难点
1.物质转化能否实现的判断。
2.方程式书写的正误判断。
教学方法
讨论、归纳
教学过程
【规律点和易错点】
孙猴子七十二般变化,都逃不出你的手心
1.常见金属及其化合物的性质与应用
重要性质 应用
(1)钠具有较强的还原性 可用于冶炼钛、锆、铌等金属
(2)Na O 与HO、CO 反应均生成O 用作供氧剂
2 2 2 2 2
(3)Na CO 水解使溶液显碱性 用热的纯碱溶液洗去油污
2 3
(4)NaHCO 受热分解生成CO、能与酸反应 用作焙制糕点的膨松剂、胃酸中和剂
3 2
(5)肥皂水显碱性 肥皂水作蚊虫叮咬处的清洗剂
(6)锂密度小、比能量大 可用作电池负极材料
(7)Al具有良好的延展性和抗腐蚀性 常用铝箔包装物品
(8)常温下,铝、铁遇浓硫酸、浓硝酸钝化 用铝制或铁制容器盛装、运输浓硫酸、浓硝酸
(9)铝与氧化铁反应放出大量的热 用于焊接铁轨
(10)MgO、Al O 熔点高 用作耐高温材料
2 3
(11)小苏打溶液和硫酸铝溶液反应生成CO 用于泡沫灭火器
2
(12)明矾溶液显酸性 用于清除铜器表面的铜锈
(13)Al(OH) 有弱碱性 用于中和胃酸
3
(14)Fe具有还原性 防止食品氧化变质
(15)Fe O 是红棕色粉末 用作红色颜料
2 3
(16)FeCl 溶液具有较强氧化性 腐蚀Cu刻制印刷电路板
3
(17)CuSO 能使蛋白质变性 配制成波尔多液用于树木杀虫
4
(18)BaSO 不溶于水,不与胃酸反应 在医疗上进行胃部造影前,用作患者服用的“钡餐”
4
2.常见非金属及其化合物的性质与应用
重要性质 应用
(1)浓硫酸具有吸水性 用作干燥剂(不能干燥NH 、HS、HI)
3 2
(2)生石灰、无水氯化钙能与水反应 用作(食品)干燥剂
(3)P O 能与水反应 用作干燥剂(不可干燥食品)
2 5
(4)硅具有半导体性能 制作芯片和太阳能电池
(5)SiO 存在光的全反射,且有硬度和柔韧度 制作光导纤维
2
(6)2C+SiO=====Si+2CO↑ 碳还原二氧化硅制备粗硅
2
(7)4HF+SiO=2HO+SiF↑ 用氢氟酸刻蚀玻璃
2 2 4
(8)ClO 具有较强的氧化性 用于自来水的杀菌消毒
2微专题突破5 无机物的性质、转化与应用 问题的态度:问则少;辩则明
(9)次氯酸盐具有强氧化性 用作杀菌消毒剂、漂白剂
(10)碘酸钾在常温下稳定 食盐中的加碘物质
(11)氮气的化学性质稳定 作保护气
(12)氦气化学性质稳定、密度小 可用于填充飞艇、气球
(13)草木灰和硫酸铵反应生成氨气 草木灰和硫酸铵不能混合施用
(14)NH HCO 、NH NO 是可溶的含氮化合物 用作氮肥
4 3 4 3
(15)浓氨水具有挥发性和还原性 检验输送Cl 的管道是否漏气
2
(16)SO 具有漂白性 用来漂白纸浆、毛、丝等
2
(17)硅酸钠的水溶液黏结力强、不易燃烧 用作黏合剂、防火剂
(18)干冰升华吸收大量的热 用于人工降雨
(19)液氨汽化吸收大量的热 用作制冷剂
3.常考原料预处理阶段各操作的目的
研磨、粉碎等 增大反应物的接触面积,增大反应速率,提高原料转化率、利用率、浸取率
灼烧(煅烧、焙烧) 除去有机物;使无机物分解为金属氧化物等,便于后续浸取、溶解
水浸 分离水溶性和非水溶性的物质
浸取 酸浸 溶解金属、金属氧化物、调节pH促进某离子的水解而转化为沉淀
碱浸 除去油污、溶解酸性氧化物、溶解铝及其化合物、调节pH等
考考位位位
1.(2024·江苏卷)下列化学反应表示正确的是
A.汽车尾气处理:2NO+4CO=====N+4CO
2 2
B.NO -电催化为N 的阳极反应:2NO -+12H++10e—=N↑+6HO
3 2 3 2 2
C.硝酸工业中NH 的氧化反应:4NH +3O=====2N+6HO
3 3 2 2 2
D.CO 和H 催化制二甲醚:2CO+6H催化剂高温、CHOCH +3HO
2 2 2 2———高压 3 3 2
【答案】D
【解析】A项,该反应方程式配平错误,汽车尾气处理:2NO+2CO=====N +2CO ,错误;B项,NO -
2 2 3
电催化为N ,N元素化合价降低,发生还原反应,应是在阴极发生反应,反应方程式是:2NO -+12H++10e—
2 3
=N↑+6HO,错误;C项,硝酸工业中NH 发生催化氧化生成NO,NO进一步反应得到NO 后再与水反应
2 2 3 2
制得硝酸,该氧化反应为4NH +5O=====4NO+6HO,错误;D项,CO 和H 催化制二甲醚的反应式为2CO
3 2 2 2 2 2
+6H 催化剂高温、CHOCH +3HO,正确。
2———高压 3 3 2
2.(2024·江苏卷)在给定条件下,下列制备过程涉及的物质转化均可实现的是
A.HCl制备:NaCl溶液电解—\s\up 4()H 和Cl 点燃—\s\up 4()HCl
—→ 2 2 —→
B.金属Mg制备:Mg(OH) 盐酸—\s\up 4()MgCl 溶液电解—\s\up 4()Mg
2 —→ 2 —→
C.纯碱工业:NaCl溶液C —— O → 2\s\up 4()NaHCO 3Δ — — → \s\up 4()Na 2 CO 3
D.硫酸工业:FeS O2—高 SO H2O\s\up 4()HSO
2—→ 温 2——→ 2 4
【答案】A
【解析】A项,电解氯化钠溶液可以得到H 和Cl ,H 和Cl 点燃反应生成HCl,转化可以实现,符合题意;
2 2 2 2
B项,氢氧化镁和盐酸反应可以得到氯化镁溶液,但是电解氯化镁溶液不能得到 Mg,电解熔融MgCl 才能得到
2
金属镁单质,转化不能实现,不符合题意;C 项,纯碱工业是在饱和食盐水中,先通入 NH 和CO 得到
3 2
NaHCO ,然后加热NaHCO 分解为NaCO ,转化不能实现,不符合题意;D项,工业制备硫酸,首先黄铁矿
3 3 2 3
和氧气反应生成SO ,但是SO 和水反应生成HSO ,不能得到HSO ,转化不能实现,不符合题意。
2 2 2 3 2 4
【问题解决1】
(2023·江苏卷)下列物质结构与性质或物质性质与用途具有对应关系的是
A.H 具有还原性,可作为氢氧燃料电池的燃料
2
B.氨极易溶于水,液氨可用作制冷剂
C.HO分子之间形成氢键,HO(g)的热稳定性比HS(g)的高
2 2 2
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找D.NH 中的N原子与H+形成配位键,NH 具有还原性
2 4 2 4
【答案】A
【解析】A项,H 具有还原性,可与氧气反应,作为氢氧燃料电池的燃料,正确;B项,液氨可用作制冷
2
剂主要原因是液氨汽化吸热,和氨极易溶于水无关,错误;C项,HO(g)的热稳定性比HS(g)的高主要原因为
2 2
氧氢键的键能高于硫氢键,和HO分子之间形成氢键无关,错误;D项,NH 具有还原性因为N本身可以失电
2 2 4
子,与NH 与H+能否形成配位键无关,错误。
2 4
物质的性质与应用
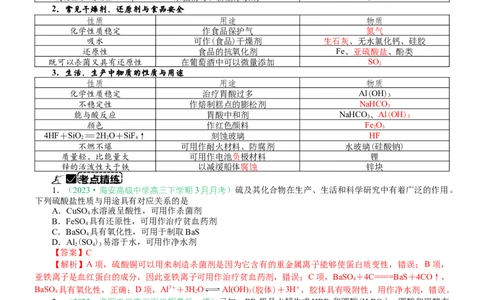
1.常见杀菌剂、消毒剂、净水剂的性质及用途
性质 用途 物质
吸附性 作净水剂(混凝剂) 明矾、铁盐(水解生成胶体)
杀菌消毒 次氯酸钠、漂白粉、二氧化氯
氧化性
漂白剂 漂白粉、过氧化钠
氧化性、吸附性 杀菌消毒、新型净水剂 KFeO
2 4
2.常见干燥剂、还原剂与食品安全
性质 用途 物质
化学性质稳定 作食品保护气 氮气
吸水 可作(食品)干燥剂 生石灰、无水氯化钙、硅胶
还原性 食品的抗氧化剂 Fe、亚硫酸盐、酚类
既可以杀菌又具有还原性 在葡萄酒中可以微量添加 SO
2
3.生活、生产中物质的性质与用途
性质 用途 物质
化学性质稳定 治疗胃酸过多 Al(OH)
3
不稳定性 作焙制糕点的膨松剂 NaHCO
3
能与酸反应 胃酸中和剂 NaHCO 、Al(OH)
3 3
颜色 作红色颜料 Fe O
2 3
4HF+SiO=2HO+SiF↑ 刻蚀玻璃 HF
2 2 4
不燃不爆 可用作耐火材料、防腐剂 水玻璃(硅酸钠)
质量轻、比能量大 可用作电池负极材料 锂
锌的活泼性大于铁 以减缓船体腐蚀 锌块
考点精练
1.(2023·海安高级中学高三下学期3月月考)硫及其化合物在生产、生活和科学研究中有着广泛的作用。
下列硫酸盐性质与用途具有对应关系的是
A.CuSO 水溶液呈酸性,可用作杀菌剂
4
B.FeSO 具有还原性,可用作治疗贫血药剂
4
C.BaSO 具有氧化性,可用于制取BaS
4
D.Al (SO ) 易溶于水,可用作净水剂
2 4 3
【答案】C
【解析】A项,硫酸铜可以用来制造杀菌剂是因为它含有的重金属离子能够使蛋白质变性,错误;B项,
亚铁离子是血红蛋白的成分,因此亚铁离子可用作治疗贫血药剂,错误;C项,BaSO+4C====BaS+4CO↑,
4
BaSO 具有氧化性,正确;D项,Al3++3HO Al(OH) (胶体)+3H+,胶体具有吸附性,用作净水剂,错误。
4 2 3
2.(2023·淮阴中学高三下学期最后一模)已知:BF 极易水解生成HBF 和硼酸(HBO);硼酸和甲醇在
3 4 3 3
浓硫酸存在下生成挥发性的硼酸甲酯[B(OCH )],硼酸甲酯主要用作热稳定剂、木材防腐剂等;GaN的结构与
3 3
晶体硅类似,是第三代半导体研究的热点。下列物质性质与用途具有对应关系的是
A.BF 极易水解,可用作催化剂
3
B.硼酸甲酯具有挥发性,可用作木材防腐剂
C.GaN硬度大,可用作半导体材料
D.Al O 熔点高,可用作耐火材料
2 3
【答案】D
【解析】A项,BF 极易水解生成HBF 和硼酸,与可用作催化剂无关,不符合题意;B项,硼酸甲酯可用
3 4
作木材防腐剂应该与杀菌、稳定等性质有关,与具有挥发性无关,不符合题意;C项,GaN的结构与晶体硅类
似,可用作半导体材料,GaN硬度大不是导电性的体现,与可用作半导体材料无关,不符合题意;D项,Al O
2 3
熔点高耐高温,可用作耐火材料,与性质有关,符合题意。
3.(2024·泰州市下学期一模)下列物质的结构、性质、用途具有对应关系的是
A.浓硫酸具有脱水性,可用于干燥Cl
2微专题突破5 无机物的性质、转化与应用 问题的态度:问则少;辩则明
B.ClF 具有强氧化性,可用作火箭助燃剂
3
C.冰晶石微溶于水,可用作电解铝工业的助熔剂
D.HF分子之间形成氢键,HF(g)的热稳定性比HCl(g)的高
【答案】B
【解析】A项,浓硫酸可用于干燥Cl ,是因为具有吸水性,错误;B项,ClF 具有强氧化性,可氧化燃料,
2 3
可用作火箭助燃剂,正确;C项,冰晶石可用作电解铝工业的助熔剂是因为可以降低氧化铝的熔点,与其微溶
于水的性质无关,错误;D项,HF(g)的热稳定性比HCl(g)的高,是因为H-F键能大于H-Cl键,与HF分子
之间形成氢键的性质无关,错误。
【问题解决2】
(2023·江苏南通市模拟)在给定条件下,下列选项所示的物质间转化能实现的是
A.MnO ――→Cl B.FeCl (aq)――→FeCl (s)
2 2 3 3
C.KFeO――→O D.MgCl (aq)――→Mg
2 4 2 2
【答案】C
【解析】A项,MnO 和浓盐酸需要在加热条件下才能生成Cl ,不符合题意;B项,FeCl (aq)中铁离子水
2 2 3
解,蒸干FeCl (aq)不能得到FeCl (s),不符合题意;C项,KFeO 能与水反应生成Fe(OH) 胶体和O ,所以
3 3 2 4 3 2
KFeO――→O 能实现,符合题意;D项,电解MgCl 溶液得到的是Mg(OH)、H 和Cl,不符合题意。
2 4 2 2 2 2 2
无机物的性质与转化
1.课本中金属与非金属及其化合物的转化
①金属——钠的、镁、铝、铁、铜及其化合物
②非金属——氯、硫、氮、碳与硅及其化合物
③化工生产——以海水为资源:候氏制碱法、氯碱工业、溴水提溴、提碘;以空气为资源:硝酸制备;以
矿石为资源:硫酸制备、铝、硅制备、硅酸盐工业(玻璃生产)
2.关注以下转化中的易错点
①反应原理——反应产物是否符合事实:如S与O 产物不是SO ,N 与O 不是NO ,I 与铁是FeI 而Cl、
2 3 2 2 2 2 2 2
Br 与Fe则是FeCl 、FeBr ;Al O、SiO 等与HO不反应;SO 、CO 与BaCl 溶液不反应。
2 3 3 2 3 2 2 2 2 2
②反应条件:如N 与O 是放电而不是加热,MnO 只与浓的盐酸反应且需加热。
2 2 2
③某些易水解的挥发酸盐或结晶水合物:如 FeCl (aq)加热得不到FeCl ,MgCl •6HO直接加热得不到
3 3 2 2
MgCl (应HCl气流中加热)。
2
考点精练
1.(2023·海安高级中学高三下学期3月月考)硫及其化合物在生产、生活和科学研究中有着广泛的作用。
可以用CuSO 溶液除去HS气体,生成黑色CuS沉淀。在给定条件下,下列物质间所示的转化可以实现的是
4 2
A.CaS(s)――――→HS(g) B.CuS(s)――――→HS(g)
2 2
C.SO (g)―――→HSO (aq) D.Cu(s)―――→SO (g)
2 2 4 2
【答案】D
【解析】A项,硝酸具有强氧化性,会将CaS中硫元素氧化,则硝酸与CaS反应得不到HS,不符合题意;
2
B项,由题意可知HS+CuSO =CuS↓+HSO ,则CuS与硫酸不反应,不符合题意;C项,SO 与HO反应
2 4 2 4 2 2
生成HSO ,不能得到HSO ,不符合题意;D项,浓硫酸具有强氧化性,可将铜氧化生成CuSO ,自身被还原
2 3 2 4 4
为SO ,符合题意。
2
2.(2024·江苏徐州模拟预测)在给定条件下,下列选项所示的物质间转化能实现的是
A.MgCl (aq)石灰乳\s\up 4()Mg(OH) 煅烧—\s\up 4()MgO B.Ca(OH) Cl2\s\up 4()Ca(ClO) 过量S\s\up
2 ——— 2 —→ 2——→ 2O2—
4()HClO
C.Fe
2
O
3
盐
—
酸
→
—\s\up 4()FeCl
3
(aq)蒸
—
发
→
—\s\up 4()FeCl
3
(s) D.CuSO
4
N
H
a
(
O
a
\s\up 4()Cu(OH)
2
悬浊液蔗
—
糖
→
—Δ
Cu O
2
【答案】A
【解析】A项,氯化镁溶液可以与石灰乳反应得到氢氧化镁沉淀,煅烧氢氧化镁可以分解生成氧化镁,符
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找合题意;B项,氯气与氢氧化钙反应生成次氯酸钙,次氯酸钙与过量SO 发生氧化还原反应,生成硫酸根和氯
2
离子,不符合题意;C项,铁与稀盐酸反应只能生成氯化亚铁,且氯化铁溶液蒸发过程中彻底水解得不到氯化
铁固体,不符合题意;D项,硫酸铜与氢氧化钠反应生成新制氢氧化铜,但是蔗糖中不含醛基是非还原糖,与
新制氢氧化铜不发生反应,不符合题意。
【问题解决3】
(2023·江苏)下列化学反应表示正确的是
A.水煤气法制氢:C(s)+HO(g)=H(g)+CO(g) ΔH=-131.3 kJ·mol-1
2 2
B.HCO催化加氢生成HCOO-的反应:HCO+H=====HCOO-+HO
2 2
C.电解水制氢的阳极反应:2HO-2e-=H↑+2OH-
2 2
D.CaH 与水反应:CaH+2HO=Ca(OH)+H↑
2 2 2 2 2
【答案】B
【解析】A项,水煤气法制氢的反应为吸热反应,其热化学方程式为 C(s)+HO(g)=H(g)+CO(g)
2 2
ΔH=131.3 kJ·mol-1,错误;B项,题意可知HCO在催化剂作用下与H 反应可得到HCOO-,根据原子守恒可
2
得离子方程式为HCO+H=====HCOO-+HO,正确;C项,电解水制氢的阳极反应为2HO-4e-=O↑+
2 2 2 2
4H+,错误;D项,CaH 与水反应的化学方程式为CaH+2HO=Ca(OH)+2H↑,错误。
2 2 2 2 2
化学反应表达式
1.熟记课本上的方程式。
2.据题中所给的信息结合有关原理,判断方程式正确否。
考点精练
1.(2024·江苏南通二模)下列化学反应表示正确的是
A.电解饱和食盐水制备Cl 的离子方程式:2Cl-+2H+====Cl↑+H↑
2 2 2
B.将氯水在强光下照射的化学方程式:2HClO====Cl↑+2HO
2 2
C.氨气检验Cl 泄露的化学方程式:3Cl+8NH =N+6NH Cl
2 2 3 2 4
D.Cl 处理含氰碱性废水的离子方程式:5Cl+2CN-+4HO=10Cl-+N↑+2CO↑+8H+
2 2 2 2 2
【答案】C
【解析】A项,电解饱和食盐水制备Cl 的离子方程式为2Cl-+2HO====Cl↑+H↑+2OH-,错误;B
2 2 2 2
项,将氯水在强光下照射的化学方程式为2HClO====O↑+2HCl,错误;C项,氨气检验Cl 泄露的化学方程
2 2
式为3Cl+8NH =N+6NH Cl,正确;D项,Cl 处理含氰碱性废水的离子方程式为5Cl+2CN-+8OH-=
2 3 2 4 2 2
10Cl-+N↑+2CO↑+4HO,错误。
2 2 2
2.(2024·南通市海门市第一次调研)周期表中VIA族元素及其化合物应用广泛。 O、 O、 O是氧元素
186 187 188
的3种核素,可以形成多种重要的化合物。亚硫酰氯(SOCl )为黄色液体,其结构式为( ),遇水发生
2
水解。工业上可电解HSO 与(NH )SO 混合溶液制备过二硫酸铵[(NH )SO],过二硫酸铵与双氧水中都含有
2 4 4 2 4 4 2 2 8
过氧键(-O-O-)。硝化法制硫酸的主要反应为:NO (g)+SO (g)=SO (g)+NO(g) ∆H=+41.8 kJ·mol-
2 2 3
1。SO 和SO 都是酸性氧化物,是制备硫酸的中间产物。下列化学反应表示正确的是
2 3
A.HO 氧化酸性废水中的Fe2+离子方程式:2Fe2++HO=2Fe3++2OH-
2 2 2 2
B.氢氧化钠吸收足量二氧化硫的离子方程式:2OH-+SO =SO2-+HO
2 3 2
C.亚硫酰氯水解的反应方程式:SOCl +2HO=HSO +2HCl
2 2 2 4
D.电解法制备(NH )SO 时的阳极反应:2SO 2--2e—=SO2-
4 2 2 8 4 2 8
【答案】D
【解析】A项,HO 氧化酸性废水中的Fe2+离子方程式为2Fe2++HO+2H+=2Fe3++2HO,错误;B项,
2 2 2 2 2
氢氧化钠吸收足量二氧化硫的离子方程式为OH-+SO =HSO -,错误;C项,亚硫酰氯水解的反应方程式为
2 3
SOCl +2HO=HSO +2HCl,错误;D项,电解法制备(NH )SO 时的阳极反应为2SO 2--2e—=SO2-,
2 2 2 3 4 2 2 8 4 2 8
正确。
3.(2024•南通市海安市高三上学期开学考)B、Al、Ga位于元素周期表中ⅢA族。BF 为无色气体,主
3
要用作有机合成中的催化剂,极易水解生成HBF (HBF 在水中完全电离为H+和BF-)和硼酸(HBO)。硼酸是
4 4 4 3 3微专题突破5 无机物的性质、转化与应用 问题的态度:问则少;辩则明
一元弱酸,能溶于水,硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯[B(OCH )],硼酸甲酯主要用作热稳
3 3
定剂、木材防腐剂等。高温下Al O 和焦炭在氯气的氛围中获得AlCl 。GaN的结构与晶体硅类似,是第三代半
2 3 3
导体研究的热点。下列化学反应表示不正确的是
A.制备B(OCH ):HBO+3CHOH========B(OCH )↑+3HO
3 3 3 3 3 3 3 2
B.BF 和NaOH溶液反应:4BF+6OH-=3BF-+BO3-+3HO
3 3 4 3 2
C.高温下Al O、焦炭在氯气中反应:2Al O+3C+3Cl====2AlCl +3CO
2 3 2 3 2 3
D.电解Al O(熔融)制备Al的阳极反应:2O2--4e—=O↑
2 3 2
【答案】B
【解析】A项,根据硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯[B(OCH )],则制备B(OCH ) 为
3 3 3 3
HBO +3CHOH========B(OCH )↑+3HO,正确;B项,BF 为无色气体,主要用作有机合成中的催化剂,
3 3 3 3 3 2 3
极易水解生成HBF (HBF 在水中完全电离为H+和BF -)和硼酸(HBO),硼酸是一元弱酸,则BF 和NaOH溶
4 4 4 3 3 3
液反应为4BF +4OH-=3BF -+HBO -+HO,错误;C 项,高温下 Al O 和焦炭在氯气的氛围中获得
3 4 2 3 2 2 3
AlCl ,则高温下Al O 、焦炭在氯气中反应为2Al O +3C+3Cl====2AlCl +3CO,正确;D项,电解Al O(熔
3 2 3 2 3 2 3 2 3
融)制备Al的阳极反应为2O2--4e—=O↑,正确。
2
【问题解决4】
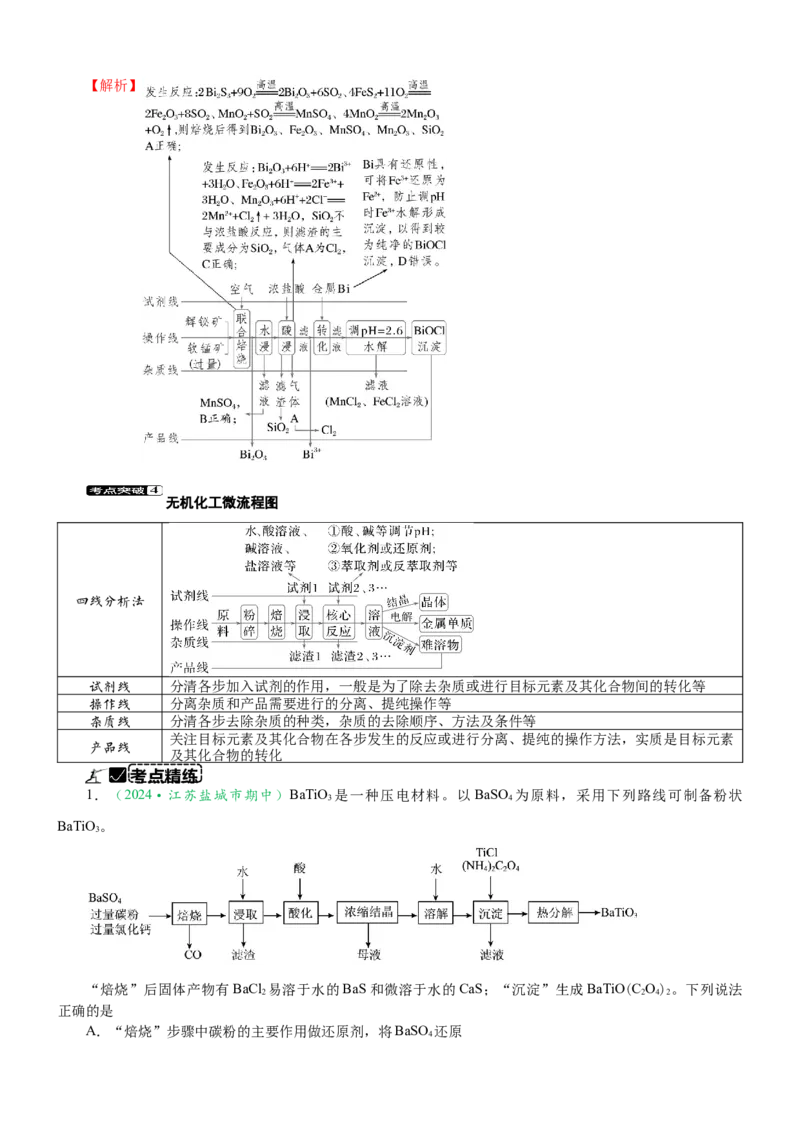
某工厂采用辉铋矿(主要成分为BiS ,含有FeS 、SiO 杂质)与软锰矿(主要成分为MnO )联合焙烧法制备
2 3 2 2 2
BiOCl,工艺流程如图所示。焙烧时过量的MnO 分解为MnO ,金属活动性:Fe>(H)>Bi>Cu。下列说法错
2 2 3
误的是
A.通过“联合焙烧”BiS 和FeS 分别转化为BiO、Fe O
2 3 2 2 3 2 3
B.“水浸”所得滤液的主要溶质是MnSO
4
C.“酸浸”所得滤渣的主要成分是SiO,气体A为Cl
2 2
D.向“酸浸”所得滤液中加入金属Bi的目的是消耗H+,促进Bi3+水解
【答案】D
6
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找【解析】
无机化工微流程图
四线分析法
试剂线 分清各步加入试剂的作用,一般是为了除去杂质或进行目标元素及其化合物间的转化等
操作线 分离杂质和产品需要进行的分离、提纯操作等
杂质线 分清各步去除杂质的种类,杂质的去除顺序、方法及条件等
关注目标元素及其化合物在各步发生的反应或进行分离、提纯的操作方法,实质是目标元素
产品线
及其化合物的转化
考点精练
1.(2024·江苏盐城市期中)BaTiO 是一种压电材料。以BaSO 为原料,采用下列路线可制备粉状
3 4
BaTiO 。
3
“焙烧”后固体产物有BaCl 易溶于水的BaS和微溶于水的CaS;“沉淀”生成BaTiO(C O) 。下列说法
2 2 4 2
正确的是
A.“焙烧”步骤中碳粉的主要作用做还原剂,将BaSO 还原
4微专题突破5 无机物的性质、转化与应用 问题的态度:问则少;辩则明
B.焙烧后的产物可以直接用酸浸取
C.“酸化”步骤选用的酸可以是稀硫酸
D.“热分解”生成粉状钛酸钡,产生的n(CO)∶n(CO)=1∶2
2
【答案】A
【解析】由流程和题中信息可知,BaSO 与过量的碳粉及过量的氯化钙在高温下焙烧得到CO、BaCl 、易
4 2
溶于水的BaS和微溶于水的CaS;烧渣经水浸取后过滤,滤渣中碳粉和CaS,滤液中有BaS和BaCl ;滤液经酸
2
化后浓缩结晶得到 BaCl 晶体;BaCl 晶体溶于水后,加入 TiCl 和(NH )C O 将 Ba2+充分沉淀得到
2 2 4 4 2 2 4
BaTiO(C O);BaTiO(C O) 经热分解得到BaTiO 。
2 4 2 2 4 2 3
A项,“焙烧”步骤中BaSO 与过量的碳粉及过量的氯化钙在高温下焙烧得到CO、BaCl 、易溶于水的
4 2
BaS和微溶于水的CaS,C的化合价从0价到+2价,即碳粉的主要作用是做还原剂,正确;B项,焙烧产物中
Ca2+、S2-均为杂质离子,需要进行除杂和分离提纯,将大部Ca2+、S2-除去,若直接酸浸,CaS会与盐酸反应
生成CaCl 而无法除去Ca2+,错误;C项,“浸取”步骤中的滤渣为CaS和碳粉;“酸化”步骤中的酸可用盐
2
酸,稀硫酸会引入杂质离子不可用,错误;D项,BaTiO(C O) 经热分解得到BaTiO ,对应的化学方程式为:
2 4 2 3
BaTiO(C O)====BaTiO +2CO↑+CO↑,CO和CO 的物质的量之比为1∶1,错误。
2 4 2 3 2 2
2.(2024·扬州市高三下学期开学考)某经预处理的含砷废水中砷元素主要以NaAsO 和NaAsO 形式存
3 3 3 4
在。以其为原料制备粗As O 的部分流程如下:
2 3
已知:①“沉砷”时发生反应:3NaAsO+5Ca(OH)=Ca (AsO )(OH)+9NaOH
3 4 2 5 4 3
②“酸化”时发生反应:Ca (AsO )(OH)+5HSO =3HAsO+HO
5 4 3 2 4 3 4 2
下列说法正确的是
A.“氧化”时每1 mol NaAsO 被氧化,会消耗11.2 L O
3 3 2
B.“沉砷”和“酸化”可提高溶液中砷元素浓度,实现砷元素的富集
C.“酸化”时可用HNO 溶液代替HSO 溶液
3 2 4
D.“还原”过程溶液的pH不断增大
【答案】B
【解析】A项,未指明标准状态,无法计算氧气的体积,错误;B项,通过“沉砷”和“酸化”后,废水
中的砷元素转变为HAsO ,砷元素浓度增大,可以达到富集砷元素的目的,正确;C项,若用“酸化”时可用
3 4
HNO 溶液代替HSO 溶液,后续‘还原’步骤中需要通入大量的SO ,且会产生污染性气体NO,错误;D项,
3 2 4 2
在“还原”过程中会发生反应:2HAsO +2SO =As O+2SO 2-+HO+4H+,使溶液的pH不断减小,错误。
3 4 2 2 3 4 2
成功体验
1.(2024·南通市二模)在指定条件下,下列含氯物质间转化不能实现的是
A.NaCl(熔融)通 — 电 → —\s\up 4()Cl 2 B.HCl(浓)M 2— n — OΔ Cl 2
C.MgCl 2 •6H 2 OH (g C — lΔ MgCl 2 (g) D.ClO-(aq)S —— O → 2\s\up 4()ClO 2 (g)
【答案】D
【解析】A项,电解熔融氯化钠反应生成钠和氯气,物质间转化能实现,不符合题意;B项,实验室是利
用浓盐酸和二氧化锰固体加热反应生成氯化锰、氯气和水,物质间转化能实现,不符合题意;C项,氯化镁结
晶水合物在氯化氢气流中加热失去结晶水得到固体氯化镁,氯化氢抑制氯化镁的水解,物质间转化能实现,不
符合题意;D项,ClO-具有强氧化性,二氧化硫具有强还原性,二者发生氧化还原反应,氯元素化合价降低,
二氧化硫中硫元素化合价升高,ClO-(aq)S —— O → 2\s\up 4()ClO 2 (g)不能实现,符合题意。
8
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找2.(2024·江苏一模)铁及其化合物的转化具有重要应用。下列说法正确的是
A.工业制硫酸涉及的物质转化:FeS 2O —— 2— — 高 温 SO 3H —— 2 → O\s\up 4()H 2 SO 4
B.实验室制溴苯涉及的物质转化:FeB —— r → 2\s\up 4()FeBr 2 ,C 6 H 6B —— r → 2F r e 2 BC 6 H 5 Br
C.利用高温水蒸气处理铁器的化学方程式:3Fe+4HO====Fe O+4H
2 3 4 2
D.利用铁粉从AgCl中获取Ag的离子方程式:Fe+2Ag+=Fe2++2Ag
【答案】C
【解析】A项,FeS 2 高温下与氧气反应生成SO 2 ,不能一步生成SO 3 ,转化错误,错误;B项,FeB —— r → 2\s\up
4()FeBr ,错误;C项,高温水蒸气与铁反应的化学方程式为3Fe+4HO====Fe O+4H,正确;D项,利用铁
3 2 3 4 2
粉从AgCl中获取Ag的离子方程式为Fe+2AgCl=Fe2++2Ag+2Cl-,错误。
3.(2024·江苏盐城市期中)碳元素及其化合物在自然界广泛存在且具有重要应用。 C、 C、 C是碳元
162 163 164
素的3种核素,碳元素不仅可以形成金刚石等单质,还能形成CO 、CH 、CHOH、CHCHOH、HCOONa、
2 4 3 3 2
NaHCO 重要化合物。CH 具有较大的燃烧热(890.3 kJ·mol-1),是常见燃料。用NaOH溶液吸收CO 生成
3 4 2
NaHCO 溶液是CO“固定”再利用的方法之一、电解NaHCO 溶液可获得CH ;向NaHCO 溶液中加入铁粉,
3 2 3 4 3
反应初期产生H 并生成FeCO ,FeCO 迅速转化为活性Fe O ,活性Fe O 催化HCO -加氢生成HCOO
2 3 3 3 4-x 3 4-x、 3
-。“侯氏制碱法”是以CO 、NH 、NaCl为原料制备NaCO 。下列物质结构与性质或物质性质与用途具有对
2 3 2 3
应关系的是
A.CO 不能燃烧也不助燃,可用于金属钠着火的灭火
2
B.刚石中碳原子形成立体空间网状结构,因此有很大的硬度
C.HCOO-离子间能形成氢键,所以HCOONa熔点比CHOH高
3
D.CHCHOH有氧化性,可用于杀菌消毒
3 2
【答案】B
【解析】A项,金属钠着火时生成过氧化钠,CO 能与过氧化钠反应生成氧气能助燃,因此CO 不可用于
2 2
金属钠着火的灭火,错误;B项,金刚石只有非极性共价键,碳原子间以极性键形成空间网状结构,有很大的
硬度,正确;C项,氢键是H原子与N、O、F等原子之间形成的分子间作用力,HCOO-离子间不能形成氢键,
错误;D项,细菌是一种蛋白质,酒精CHCHOH能使蛋白质变性失活从而起到杀菌消毒作用,与氧化性无关,
3 2
错误。
4.(2024·南京市二模)下列物质结构与性质或性质与用途不具有对应关系的是
A.MgCl 易溶于水,可用于制作豆腐的凝固剂
2
B.MgO是碱性氧化物,可用于吸收燃煤烟气中的SO
2
C.NaCl晶体中离子间存在较强的离子键,NaCl晶体的硬度较大
D.HCO -通过氢键缔合成较大的酸根,NaHCO 的溶解度小于NaCO
3 3 2 3
【答案】A
【解析】A项,氯化镁用作豆腐制作过程中的凝固剂是利用蛋白质在盐溶液中发生聚沉的性质,与其易溶
于水无关,符合题意;B 项,MgO 是碱性氧化物,SO 是酸性氧化物,二者能发生反应:MgO+SO =
2 2
MgSO ,故MgO可用于吸收燃煤烟气中的SO ,有对应关系,不合题意;C项,Na+和Cl-间存在正负电荷的强
3 2
烈作用,具有较强的离子键,具有较高的熔点,硬度较大,有对应关系,不合题意;D项,HCO -中含有O-H
3
键,故HCO -能形成分子间氢键,通过氢键缔合成较大的酸根,一般微粒越大越难溶于水,故 NaHCO 的溶解
3 3
度小于NaCO,有对应关系,不合题意。
2 3
5.(2024·南通市海安市)从砷化镓废料(主要成分为GaAs、Fe O、SiO 和CaCO)中回收镓和砷的工艺
2 3 2 3
流程如下图所示。下列说法不正确的是
A.“碱浸”前,废料先浆化为悬浊液的目的是提高Ga、As元素浸出率微专题突破5 无机物的性质、转化与应用 问题的态度:问则少;辩则明
B.“碱浸”后,溶液中主要离子有Ga3+、Na+、SiO2-、AsO3-
3 4
C.滤渣Ⅱ的成分为Ga(OH) 和HSiO
3 2 3
D.电解后的尾液中溶质主要成分为HSO ,可以循环利用
2 4
【答案】B
【解析】向砷化镓废料(主要成分为GaAs、Fe O,SiO 和CaCO )中加入NaOH、HO 溶液,主要发生反
2 3 2 3 2 2
应GaAs+4NaOH+4HO=NaGaO +NaAsO+6HO、SiO +2NaOH=NaSiO+HO,NaGaO 、NaAsO、
2 2 2 3 4 2 2 2 3 2 2 3 4
NaSiO 进入浸出液中,Fe O、CaCO 难溶于氢氧化钠溶液形成滤渣Ⅰ;浸出液中加硫酸中和,过滤所得滤液中
2 3 2 3 3
含NaAsO,滤液经蒸发浓缩、冷却结晶得到NaAsO•12HO;滤渣Ⅱ中含Ga(OH)、NaSiO 沉淀,向滤渣Ⅱ
3 4 3 4 2 3 2 3
中加入硫酸,Ga(OH) 转化为可溶于水的Ga(SO ),分离出滤渣Ⅲ(NaSiO),电解Ga(SO ) 溶液生成Ga、
3 2 4 3 2 3 2 4 3
氧气和硫酸。
A项,通过将废料先浆化为悬浊液,可以增大接触面积,提高Ga、As元素浸出率,正确;B项,通过分析
可知,“碱浸”后,NaGaO 、NaAsO 、NaSiO 进入浸出液中,则溶液中主要离子有Na+、SiO2-、AsO3-,
2 3 4 2 3 3 4
错误;C项,通过分析可知,滤渣Ⅱ的成分为Ga(OH) 和HSiO ,正确;D项,由分析可知,电解Ga(SO )
3 2 3 2 4 3
溶液生成Ga、氧气、硫酸,尾液中含有HSO ,可以循环利用,正确。
2 4
10
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找