文档内容
第一篇 化学基本概念
微练 10 物质转化“环式”历程与机理
“环式”反应历程题一般取材于真实的科研成果的情境素材,充分体现了化学反应和物质转化的本质,
进行类比迁移以考查考生的学科素养。反应历程是指化学反应中的反应物转化为最终产物通过的途径,因
为化学变化从根本上来说,就是旧键的破裂和新键的生成。反应的历程能够反映出物质结构和反应能力之
间的关系,从而可以加深我们对于物质运动形态的认识。反应机理是化学中用来描述某一化学变化所经由
的全部基元反应,机理详细描述了每一步转化的过程,包括过渡态的形成,键的断裂和生成,以及各步的
相对速率大小等。完整的反应机理需要考虑到反应物、催化剂、反应的立体化学、产物以及各物质的用量。
通过反应历程或机理可以帮助我们了解物质结构的知识。此类题以图示的形式来描述某一化学变化所经由
的全部反应,就是把一个复杂反应分解成若干个反应,然后按照一定规律组合起来,从而达到阐述复杂反
应的内在联系的目的。高考中常以此为载体考查催化剂、中间产物的判断、化学反应方程式的书写及反应
过程的化学键断裂与形成情况。解答时难点在于从陌生转化图中提取有效信息,注意题干信息的理解应用,
通过分析化学反应过程,明确反应过程中催化剂的作用和能量变化、化学键的变化。
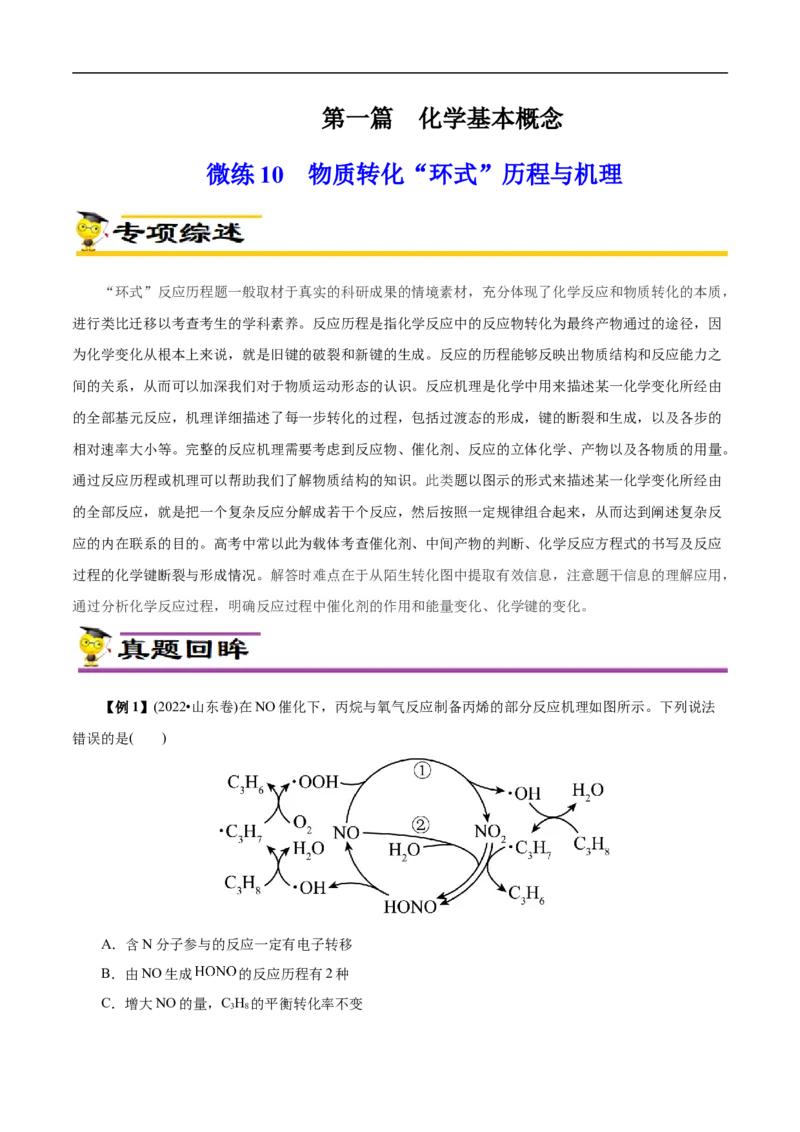
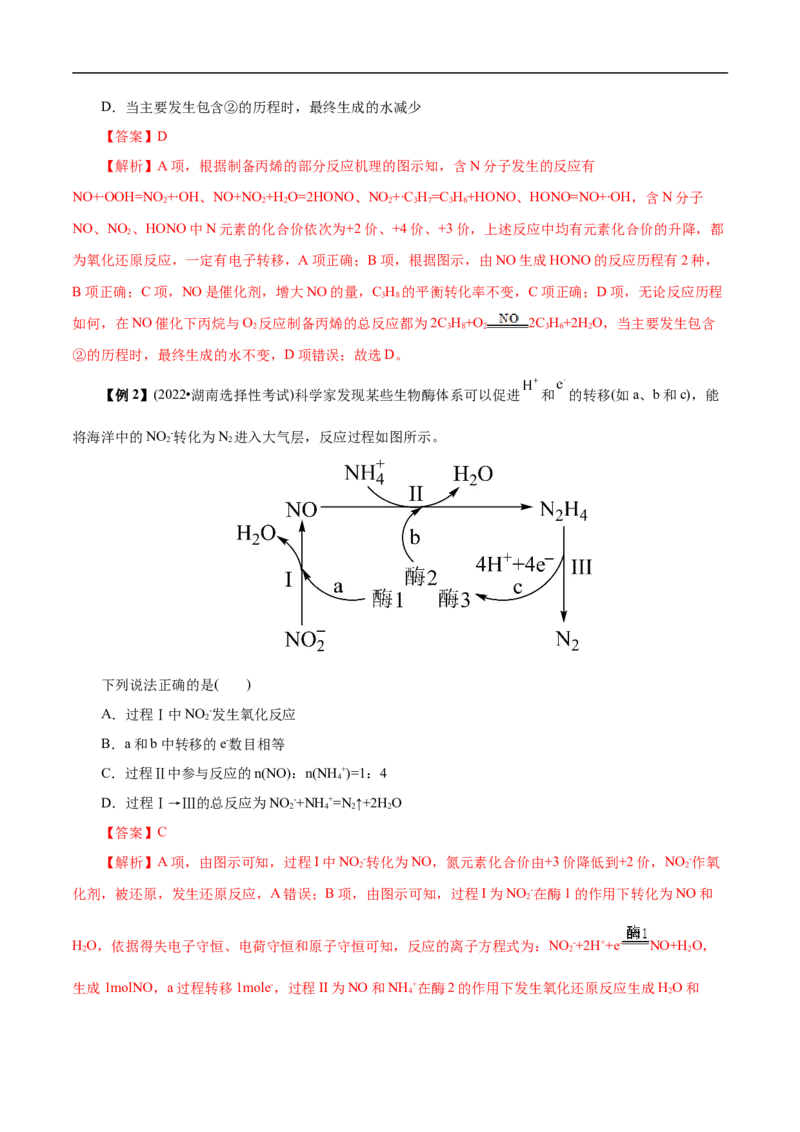
【例1】(2022•山东卷)在NO催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法
错误的是( )
A.含N分子参与的反应一定有电子转移
B.由NO生成 的反应历程有2种
C.增大NO的量,C H 的平衡转化率不变
3 8D.当主要发生包含②的历程时,最终生成的水减少
【答案】D
【解析】A项,根据制备丙烯的部分反应机理的图示知,含N分子发生的反应有
NO+∙OOH=NO+∙OH、NO+NO +H O=2HONO、NO +∙C H=C H+HONO、HONO=NO+∙OH,含N分子
2 2 2 2 3 7 3 6
NO、NO 、HONO中N元素的化合价依次为+2价、+4价、+3价,上述反应中均有元素化合价的升降,都
2
为氧化还原反应,一定有电子转移,A项正确;B项,根据图示,由NO生成HONO的反应历程有2种,
B项正确;C项,NO是催化剂,增大NO的量,C H 的平衡转化率不变,C项正确;D项,无论反应历程
3 8
如何,在NO催化下丙烷与O 反应制备丙烯的总反应都为2C H+O 2C H+2H O,当主要发生包含
2 3 8 2 3 6 2
②的历程时,最终生成的水不变,D项错误;故选D。
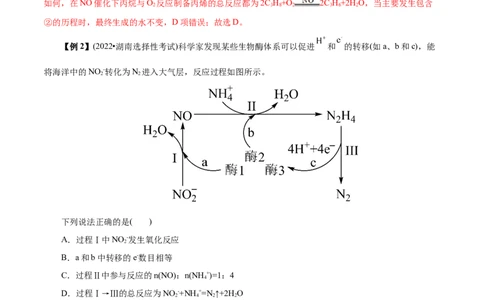
【例2】(2022•湖南选择性考试)科学家发现某些生物酶体系可以促进 和 的转移(如a、b和c),能
将海洋中的NO -转化为N 进入大气层,反应过程如图所示。
2 2
下列说法正确的是( )
A.过程Ⅰ中NO -发生氧化反应
2
B.a和b中转移的e-数目相等
C.过程Ⅱ中参与反应的n(NO):n(NH +)=1:4
4
D.过程Ⅰ→Ⅲ的总反应为NO -+NH+=N ↑+2H O
2 4 2 2
【答案】C
【解析】A项,由图示可知,过程I中NO -转化为NO,氮元素化合价由+3价降低到+2价,NO -作氧
2 2
化剂,被还原,发生还原反应,A错误;B项,由图示可知,过程I为NO -在酶1的作用下转化为NO和
2
HO,依据得失电子守恒、电荷守恒和原子守恒可知,反应的离子方程式为:NO -+2H++e- NO+H O,
2 2 2
生成1molNO,a过程转移1mole-,过程II为NO和NH +在酶2的作用下发生氧化还原反应生成HO和
4 2NH,依据得失电子守恒、电荷守恒和原子守恒可知,反应的离子方程式为:2NO+8NH +
2 4 4
2HO+5NH+8H+,消耗1molNO,b过程转移4mol e-,转移电子数目不相等,B错误;C项,由图示可知,
2 2 4
过程II发生反应的参与反应的离子方程式为:2NO+8NH + 2HO+5NH+8H+,n(NO):n(NH +)=1:4,
4 2 2 4 4
C正确;D项,由图示可知,过程III为NH 转化为N 和4H+、4e-,反应的离子方程式为:NH= N +4H+
2 4 2 2 4 2
+4e-,过程I-III的总反应为:2NO -+8NH+=5N ↑+4H O+24H++18e-,D错误;故选C。
2 4 2 2
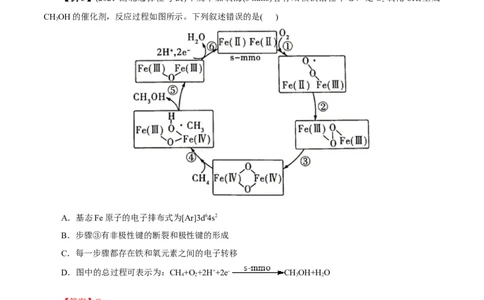
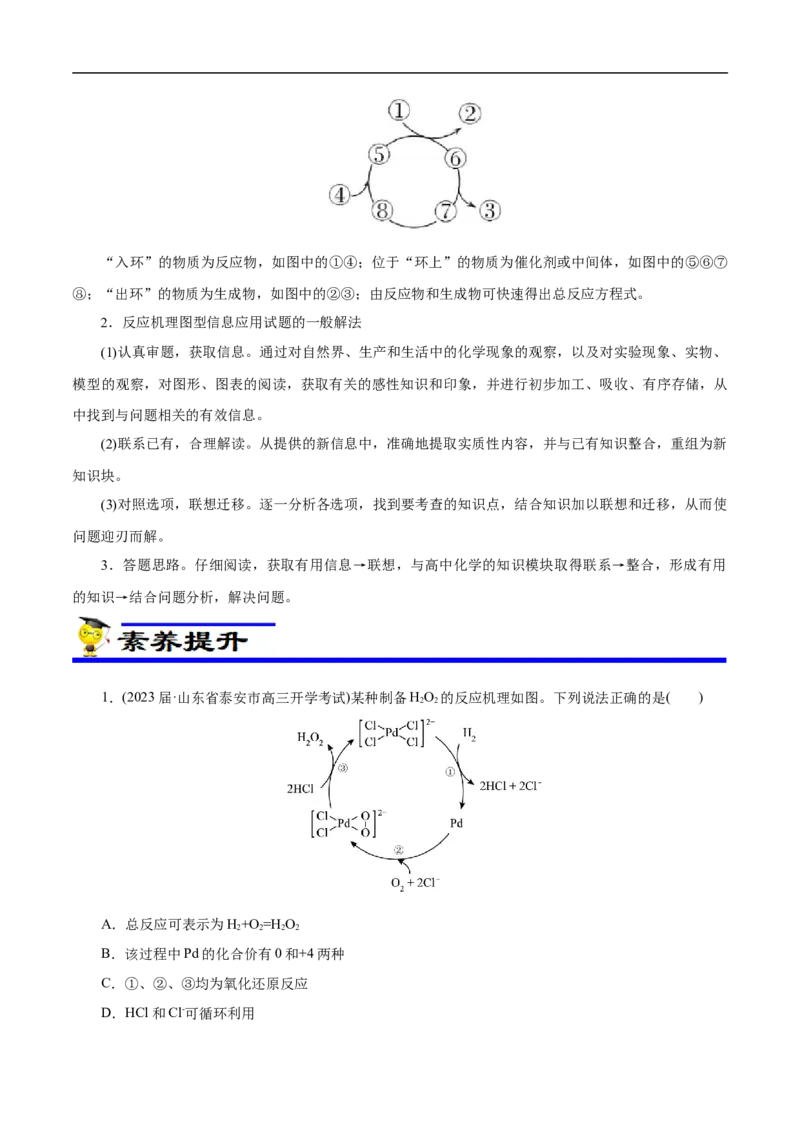
【例3】(2021•湖北选择性考试)甲烷单加氧酶(s-mmo)含有双核铁活性中心,是 O 氧化CH 生成
2 4
CHOH的催化剂,反应过程如图所示。下列叙述错误的是( )
3
A.基态Fe原子的电子排布式为[Ar]3d64s2
B.步骤③有非极性键的断裂和极性键的形成
C.每一步骤都存在铁和氧元素之间的电子转移
D.图中的总过程可表示为:CH+O +2H++2e- CHOH+H O
4 2 3 2
【答案】C
【解析】基态Fe原子核外有26个电子,其核外电子排布式为[Ar]3d64s2,A项正确;步骤③中断裂O
—O非极性键,形成O—Fe(Ⅳ)极性键,B项正确;步骤④中电子转移发生在Fe和C元素之间,C项错误;
根据图示,总过程的反应物为CH、O、H、e,产物为CHOH、HO,D项正确。
4 2 3 2
【例4】(2020•新课标Ⅰ卷)铑的配合物离子[Rh(CO) I]-可催化甲醇羰基化,反应过程如图所示。
2 2下列叙述错误的是( )
A.CHCOI是反应中间体
3
B.甲醇羰基化反应为CHOH+CO=CH COH
3 3 2
C.反应过程中Rh的成键数目保持不变
D.存在反应CHOH+HI=CH I+H O
3 3 2
【答案】C
【解析】题干中明确指出,铑配合物[Rh(CO) I]-充当催化剂的作用,用于催化甲醇羰基化。由题干中
2 2
提供的反应机理图可知,铑配合物在整个反应历程中成键数目,配体种类等均发生了变化;并且也可以观
察出,甲醇羰基化反应所需的反应物除甲醇外还需要CO,最终产物是乙酸;因此,凡是出现在历程中的,
既非反应物又非产物的物种如CHCOI以及各种配离子等,都可视作中间物种。A项,通过分析可知,
3
CHCOI属于甲醇羰基化反应的反应中间体;其可与水作用,生成最终产物乙酸的同时,也可以生成使甲
3
醇转化为CHI的HI,A项正确;B项,通过分析可知,甲醇羰基化反应,反应物为甲醇以及CO,产物为
3
乙酸,方程式可写成:CHOH+CO CHCOOH,B项正确;C项,通过分析可知,铑配合物在
3
整个反应历程中,成键数目,配体种类等均发生了变化,C项不正确;D项,通过分析可知,反应中间体
CHCOI与水作用生成的HI可以使甲醇转化为CHI,方程式可写成:CHOH+ HI→CH I+H O,D项正确;
3 3 3 3 2
故选C。
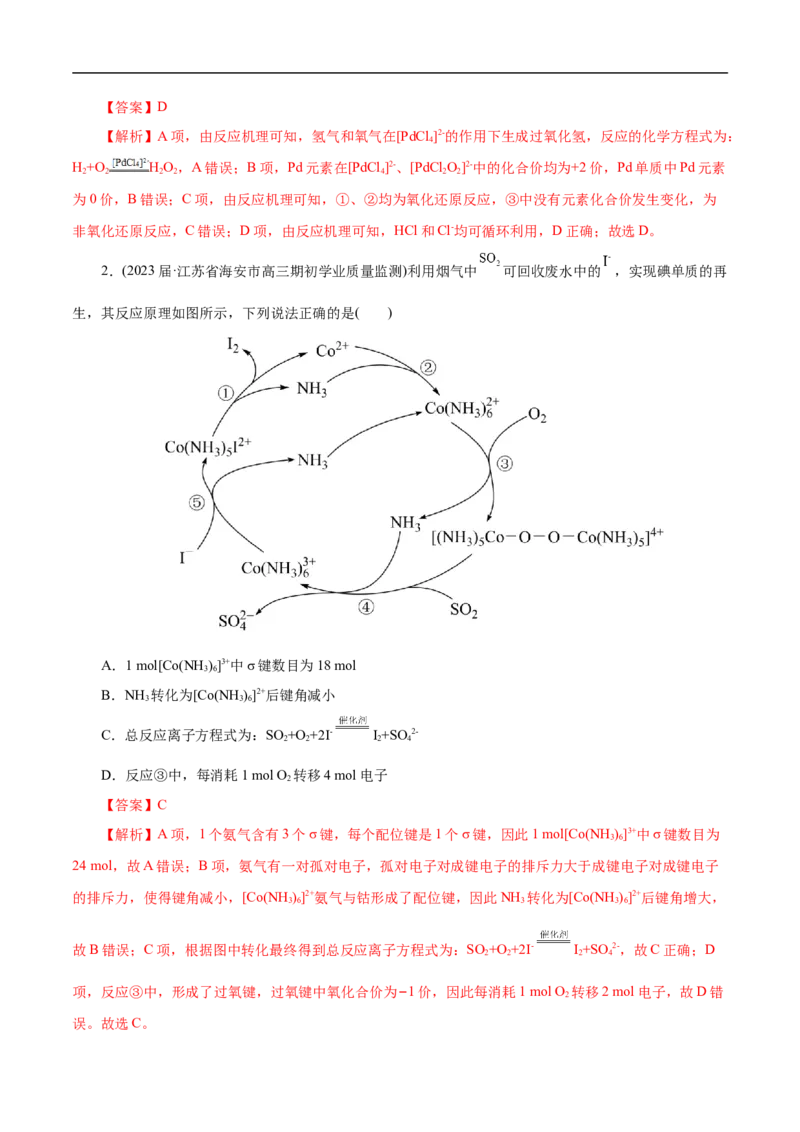
1.“环式”反应过程图如下:“入环”的物质为反应物,如图中的①④;位于“环上”的物质为催化剂或中间体,如图中的⑤⑥⑦
⑧;“出环”的物质为生成物,如图中的②③;由反应物和生成物可快速得出总反应方程式。
2.反应机理图型信息应用试题的一般解法
(1)认真审题,获取信息。通过对自然界、生产和生活中的化学现象的观察,以及对实验现象、实物、
模型的观察,对图形、图表的阅读,获取有关的感性知识和印象,并进行初步加工、吸收、有序存储,从
中找到与问题相关的有效信息。
(2)联系已有,合理解读。从提供的新信息中,准确地提取实质性内容,并与已有知识整合,重组为新
知识块。
(3)对照选项,联想迁移。逐一分析各选项,找到要考查的知识点,结合知识加以联想和迁移,从而使
问题迎刃而解。
3.答题思路。仔细阅读,获取有用信息→联想,与高中化学的知识模块取得联系→整合,形成有用
的知识→结合问题分析,解决问题。
1.(2023届·山东省泰安市高三开学考试)某种制备HO 的反应机理如图。下列说法正确的是( )
2 2
A.总反应可表示为H+O =H O
2 2 2 2
B.该过程中Pd的化合价有0和+4两种
C.①、②、③均为氧化还原反应
D.HCl和Cl-可循环利用【答案】D
【解析】A项,由反应机理可知,氢气和氧气在[PdCl ]2-的作用下生成过氧化氢,反应的化学方程式为:
4
H+O HO,A错误;B项,Pd元素在[PdCl ]2-、[PdCl O]2-中的化合价均为+2价,Pd单质中Pd元素
2 2 2 2 4 2 2
为0价,B错误;C项,由反应机理可知,①、②均为氧化还原反应,③中没有元素化合价发生变化,为
非氧化还原反应,C错误;D项,由反应机理可知,HCl和Cl-均可循环利用,D正确;故选D。
2.(2023届·江苏省海安市高三期初学业质量监测)利用烟气中 可回收废水中的 ,实现碘单质的再
生,其反应原理如图所示,下列说法正确的是( )
A.1 mol[Co(NH )]3+中σ键数目为18 mol
3 6
B.NH 转化为[Co(NH )]2+后键角减小
3 3 6
C.总反应离子方程式为:SO +O +2I- I+SO2-
2 2 2 4
D.反应③中,每消耗1 mol O 转移4 mol电子
2
【答案】C
【解析】A项,1个氨气含有3个σ键,每个配位键是1个σ键,因此1 mol[Co(NH )]3+中σ键数目为
3 6
24 mol,故A错误;B项,氨气有一对孤对电子,孤对电子对成键电子的排斥力大于成键电子对成键电子
的排斥力,使得键角减小,[Co(NH )]2+氨气与钴形成了配位键,因此NH 转化为[Co(NH )]2+后键角增大,
3 6 3 3 6
故B错误;C项,根据图中转化最终得到总反应离子方程式为:SO +O +2I- I+SO2-,故C正确;D
2 2 2 4
项,反应③中,形成了过氧键,过氧键中氧化合价为−1价,因此每消耗1 mol O 转移2 mol电子,故D错
2
误。故选C。3.(2023届·山东省青岛市高三期初测试)钴 使某析氧反应催化剂中流失 的原位自修复机理如图。
下列说法错误的是( )
A.催化析氧反应和自修复反应中的催化剂分别为 和
B.维持相对稳定的 有助于催化析氧和自修复的进行
C.自修复反应的方程式为:
D.图中所示物质之间的转化只有 和 的化合价发生了变化
【答案】D
【解析】根据图示可知,Co(OH) 转化成CoOOH,Co失电子化合价从+2变为+3价,OH-生成HO,
2 2
CoOOH再与Fe(OH) 反应,Fe失电子生成FeOOH,CoOOH得电子生成Co(OH) ,FeOOH失电子生成
2 2
FeO2-,Fe从+3价变为+6价,FeO2-得电子与OH-反应生成FeOOH,O 和HO。A项,从图中可知,催化
4 4 2 2
析氧反应最终生成氧气和水,FeO2-为催化剂,自修复反应中Fe(OH) 与CoOOH反应生成Co(OH) 和
4 2 2
FeOOH,Co(OH) 又生成了CoOOH,因此CoOOH为催化剂,A正确;B项,催化析氧有OH-参与,自修
2
复中Fe(OH) 、Co(OH) 也为碱性物质,维持相对稳定的pH有助于催化析氧和自修复的进行,B正确;C
2 2
项,根据图示可知,自修复反应中Fe(OH) 和CoOOH反应生成FeOOH和Co(OH) ,其方程式为
2 2
CoOOH+Fe(OH) =FeOOH+Co(OH) ,C正确;D项,从图中可知,OH-和FeO2-反应生成了氧气,此反应中
2 2 4
氧元素的化合价发生了变化,D错误;故选D。
4.(2023届·安徽省蚌埠市高三第一次教学质量检测)氨催化还原脱除NO的一种催化机理示意图如图,
下列有关说法不正确的是( )A. (即MnO )是反应的催化剂
2
B.该过程存在非极性键的断裂和形成
C.MnO 能结合NH 的原因是Mn原子有空轨道能接受孤电子对,形成配位键
2 3
D.该催化过程的总反应的化学方程式:4NH +6NO 5N+6H O
3 2 2
【答案】D
【解析】A项,根据反应过程,反应前后MnO 没变,可知MnO 是反应的催化剂,故A正确;B项,
2 2
反应物有O、生成物有N,所以存在非极性键的断裂和形成,故B正确;C项,氨分子中氮原子具有孤对
2 2
电子,二氧化锰中锰原子具有空轨道,氮原子和锰原子通过形成配位键使二氧化锰和氨分子相互结合,故
C正确;D项,根据图示,该催化过程的总反应的化学方程式为4NH +4NO+O 4N+6H O,故D错误;
3 2 2 2
故选D。
5.(2023届·河南省十所名校高中毕业班尖子生高三第一次考试)由 簇介导的光辅助水蒸气重
整甲烷的两个连续催化循环机理如图所示(“UV”代表紫外线)。下列说法错误的是( )
A. 在循环中起催化作用
B.该反应可用于制取合成气CO、H
2
C.过程中包含反应
D.反应过程中金属元素 、V的价态均不变
【答案】D
【解析】A项,由催化循环Ⅰ、Ⅱ及催化剂性质知,A项正确;B项,图中循环Ⅰ、Ⅱ反应都为HO
2
重整CH (CH+H O=CO+3H),得到合成气:CO和H,B项正确;C项,由图示可知,循环Ⅰ中,在UV
4 4 2 2 2
的作用下, ,C项正确;D项, 、 、 中
钒的化合价一定不同,D项错误;故选D。
6.(2023届·河南省安阳市高三TOP二十名校调研摸底考试)Sonogashira偶联反应是合成取代炔烃和共
轭快烃最重要的方法,钯/铜混合催化剂催化的Sonogashira偶联通常通过两个催化循环协同进行,较短的
波长( )主要驱动自偶联反应,而较长的波长( )显著增加了交叉偶联产物的合成。已
知R1-和R2-代表烃基,下列说法错误的是( )A.反应过程中,Cu和Pd的化合价发生变化
B.较短波长下存在反应
C.若以 和 为原料,在较长波长下可制得
D.该催化剂通过“可控波长开关”来切换反应途径,可提高产物选择性
【答案】C
【解析】A项,反应过程中,铜和钯都有单质和化合物,化合价均发生了变化,故A正确;B项,从
图中可以看出,较短波长下,R1-C C-Pd发生自偶连生成了R1C≡C-C≡CR1,故B正确;C项,从图中可
以看出,若以 和 为原料,在较长波长下发生交叉偶联可制得
,故C错误;D项,较短的波长( 400~500nm )主要驱动自偶联反应,而较长的
波长( 500-940nm )显著增加了交叉偶联产物的合成,所以该催化剂通过“可控波长开关”来切换反应途径,
可提高产物选择性,故D正确;故选C。
7.(2023届·广西桂林市联盟校高三统一检测)2021 年9月,我国科学家团队在实验室中利用二氧化碳
人工合成淀粉获得成功。如图是合成过程的相关反应路径(部分反应条件、产物等均已略去)。下列有关说
法正确的是( )A.人工合成淀粉的化学式可表示为(C H O)
6 12 6 n
B.反应①、②、③的原子利用率均为100%
C.CO→CHOH→ HCHO的转化过程中碳元素均被还原
2 3
D.过氧化氢酶使HO 及时分解,防止其氧化其它酶,同时增大O 的利用率
2 2 2
【答案】D
【解析】A项,根据人工合成淀粉的键线式可知,其化学式可表示为(C H O),A错误;B项,反应
6 10 5 n
①除了合成有机物以外,还有水生成,反应②除了合成甲醛以外,也还有过氧化氢生成,所以原子利用率
均未达到100%,B错误;C项,CO→CHOH过程中C的化合价由+4降低到-2价,被还原,CHOH→
2 3 3
HCHO过程中C元素化合价由-2价升高到0价,被氧化,C错误;D项,过氧化氢酶可使反应②产生的
HO 及时分解,使反应②正向进行程度增大,增大了O 的利用率,D正确;故选D。
2 2 2
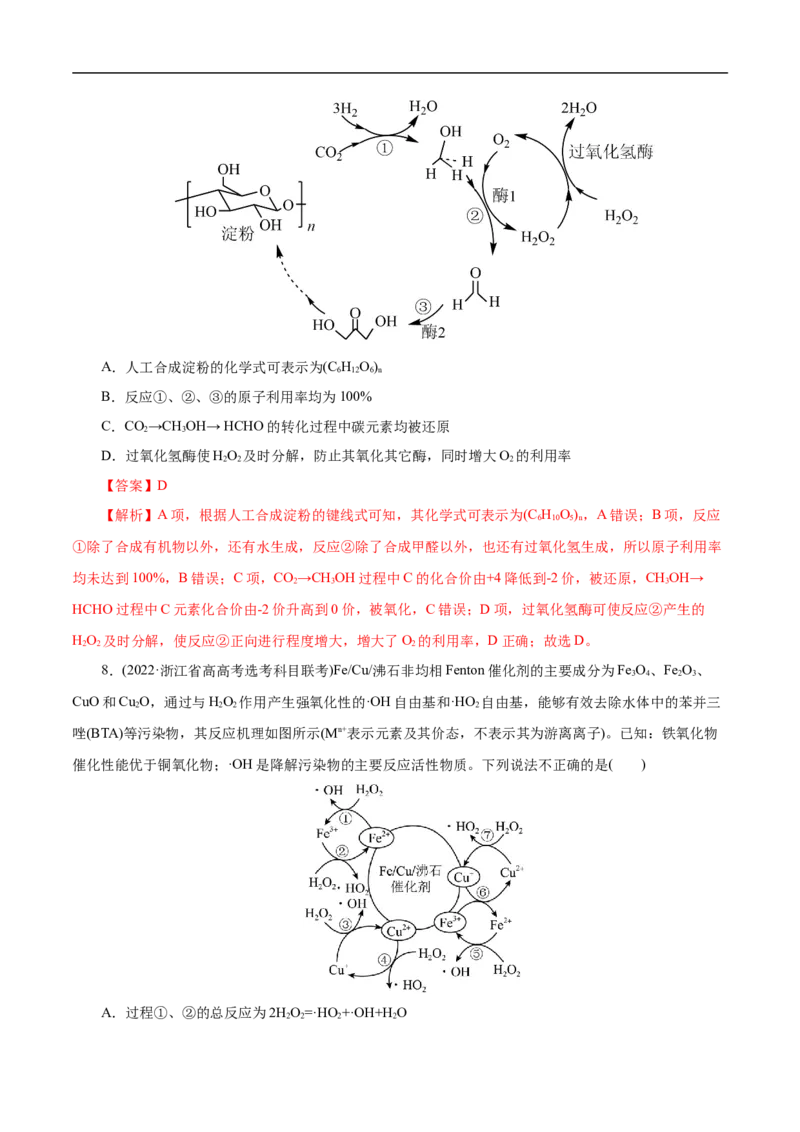
8.(2022·浙江省高高考选考科目联考)Fe/Cu/沸石非均相Fenton催化剂的主要成分为Fe O、Fe O、
3 4 2 3
CuO和Cu O,通过与HO 作用产生强氧化性的·OH自由基和·HO 自由基,能够有效去除水体中的苯并三
2 2 2 2
唑(BTA)等污染物,其反应机理如图所示(Mn+表示元素及其价态,不表示其为游离离子)。已知:铁氧化物
催化性能优于铜氧化物;·OH是降解污染物的主要反应活性物质。下列说法不正确的是( )
A.过程①、②的总反应为2HO=·HO+·OH+HO
2 2 2 2B.过程③、④中Cu2+和Cu+均可看作是催化剂
C.过程⑤中有OH-生成,过程⑦中有H+生成
D.过程⑥必然会导致反应生成的自由基减少
【答案】D
【解析】A项,由反应机理图可知过程①为HO+Fe2+=·OH+ Fe3+ +OH-,过程②为HO+Fe3+= Fe2+
2 2 2 2
+·HO+ H+,总反应为2HO=·HO+·OH+HO,故A正确;B项,过程③为HO+ Cu+=·OH+ Cu2++OH-,过
2 2 2 2 2 2 2
程④为HO+ Cu2+= Cu++·HO+ H+,总反应为2HO=·HO+·OH+HO,Cu2+和Cu+均可看作是催化剂,故B
2 2 2 2 2 2 2
正确;C项,过程⑤为HO+Fe2+=·OH+ Fe3+ +OH-,过程⑦HO+ Cu2+= Cu++·HO+ H+,故C正确;D项,
2 2 2 2 2
过程⑥Fe3+ + Cu+= Fe2++ Cu2+,而由以上过程反应可知Cu2+、Fe2+均有利于HO 转化成自由基,因此过程
2 2
⑥的发生导致自由基增加,故D错误;故选D。
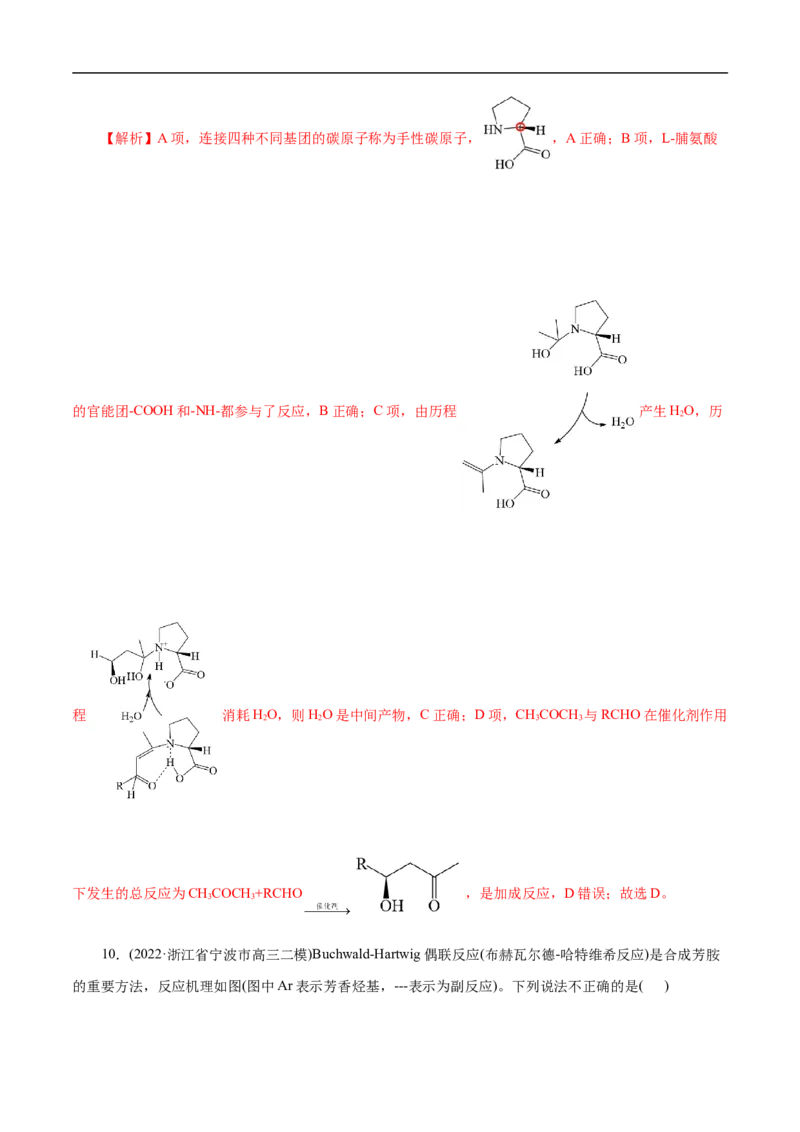
9.(2022·山东省淄博市高三教学质量摸底检测)2021 年诺贝尔化学奖授予对有机小分子不对称催化作
出重大贡献的科学家,其研究成果中L-脯氨酸催化CHCOCH 与RCHO反应的机理如图所示。下列叙述错
3 3
误的是( )
A.L-脯氨酸分子有一个手性碳原子
B.L-脯氨酸的官能团都参与了反应
C.HO是中间产物
2
D.CHCOCH 与RCHO在催化作用下发生的反应是取代反应
3 3
【答案】D【解析】A项,连接四种不同基团的碳原子称为手性碳原子, ,A正确;B项,L-脯氨酸
的官能团-COOH和-NH-都参与了反应,B正确;C项,由历程 产生HO,历
2
程 消耗HO,则HO是中间产物,C正确;D项,CHCOCH 与RCHO在催化剂作用
2 2 3 3
下发生的总反应为CHCOCH +RCHO ,是加成反应,D错误;故选D。
3 3
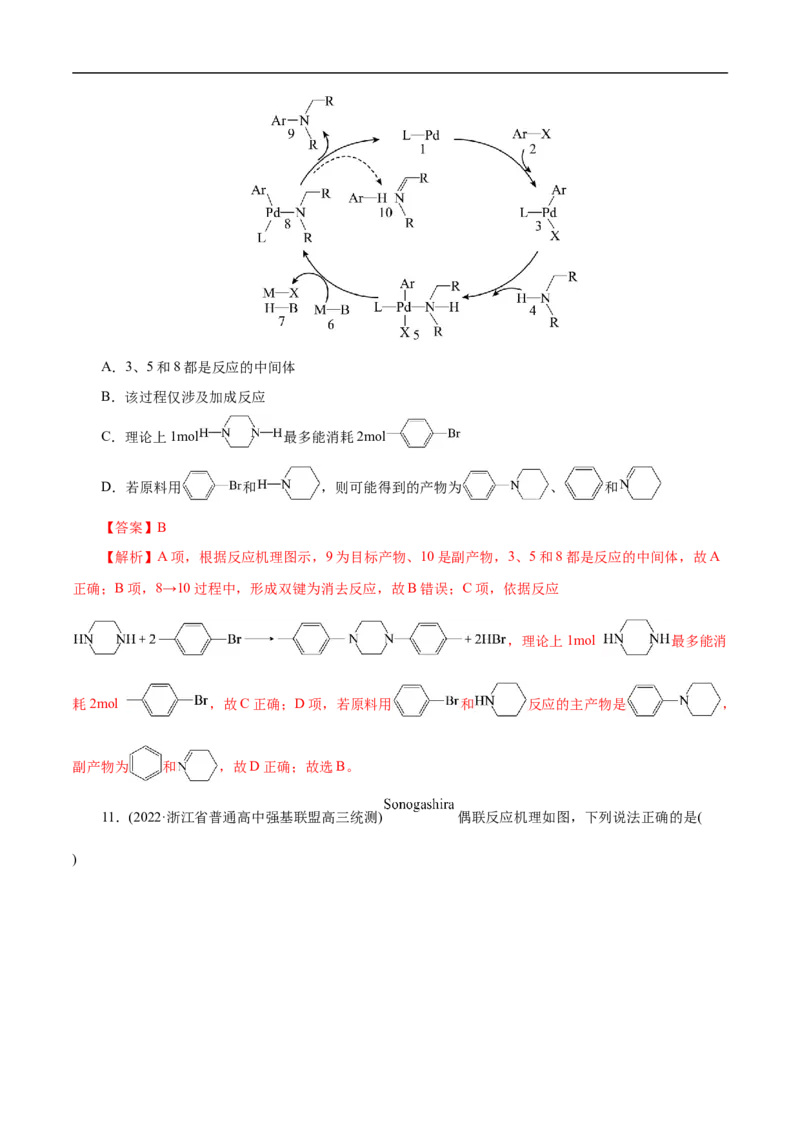
10.(2022·浙江省宁波市高三二模)Buchwald-Hartwig偶联反应(布赫瓦尔德-哈特维希反应)是合成芳胺
的重要方法,反应机理如图(图中Ar表示芳香烃基,---表示为副反应)。下列说法不正确的是( )A.3、5和8都是反应的中间体
B.该过程仅涉及加成反应
C.理论上1mol 最多能消耗2mol
D.若原料用 和 ,则可能得到的产物为 、 和
【答案】B
【解析】A项,根据反应机理图示,9为目标产物、10是副产物,3、5和8都是反应的中间体,故A
正确;B项,8→10过程中,形成双键为消去反应,故B错误;C项,依据反应
,理论上1mol 最多能消
耗2mol ,故C正确;D项,若原料用 和 反应的主产物是 ,
副产物为 和 ,故D正确;故选B。
11.(2022·浙江省普通高中强基联盟高三统测) 偶联反应机理如图,下列说法正确的是(
)A.若原料用苯乙炔和CH=CHBr,则产物是
2
B.R X变为 发生了氧化反应
1
C.该反应只用了一种催化剂LnPd
D.适量添加NaCO 有利于提高产率
2 3
【答案】D
【解析】由图知,在催化剂作用下, 。A项,苯环应和碳碳三键相
连,碳碳三键和碳碳双键应换一个位置,A错误;B项,LnPd中元素化合价升高、发生氧化反应,有机物
发生了还原反应,B错误;C项,由图知,CuX也参与循环、CuX也是催化剂,C错误;D项,由图知,
在催化剂作用下, , 能吸收HX,有利于反应向右进行、利
于提高产率,D正确;故选D。
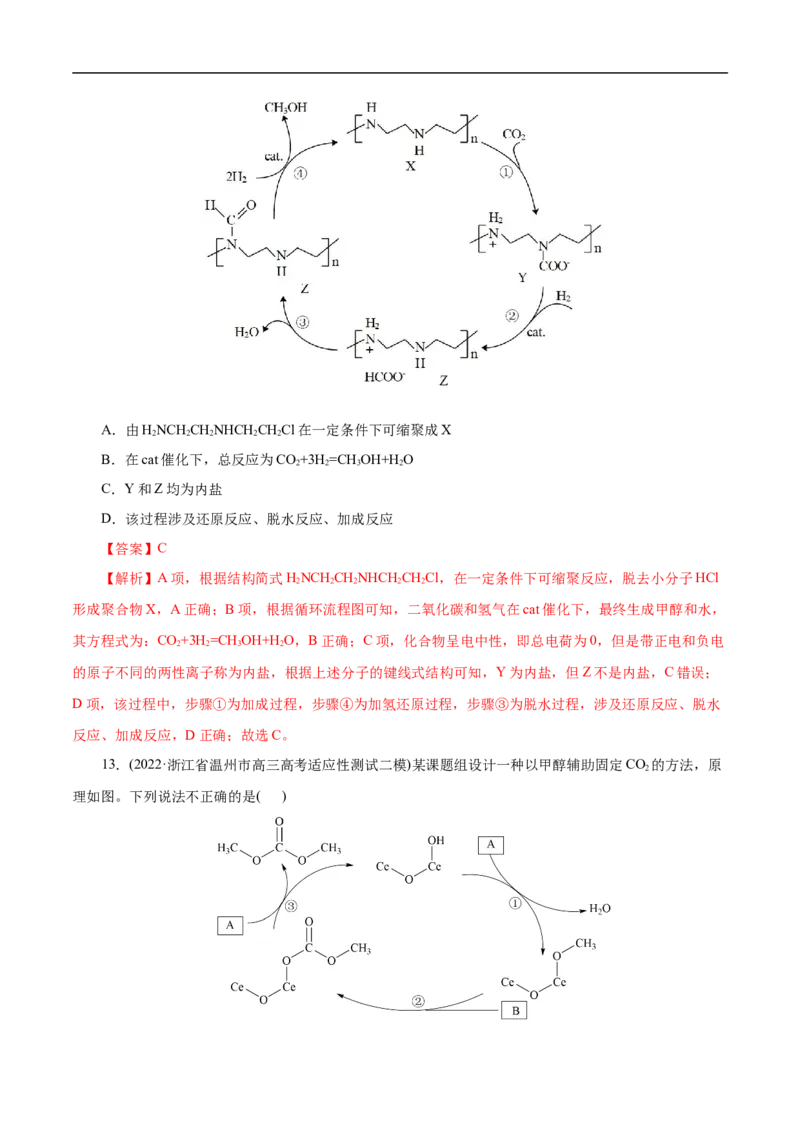
12.(2022·浙江省绍兴市高三选考科目适应性考试二模)某实验小组设计一种固定CO 的方法,下列说
2
法不正确的是( )A.由HNCH CHNHCH CHCl在一定条件下可缩聚成X
2 2 2 2 2
B.在cat催化下,总反应为CO+3H =CH OH+H O
2 2 3 2
C.Y和Z均为内盐
D.该过程涉及还原反应、脱水反应、加成反应
【答案】C
【解析】A项,根据结构简式HNCH CHNHCH CHCl,在一定条件下可缩聚反应,脱去小分子HCl
2 2 2 2 2
形成聚合物X,A正确;B项,根据循环流程图可知,二氧化碳和氢气在cat催化下,最终生成甲醇和水,
其方程式为:CO+3H =CH OH+H O,B正确;C项,化合物呈电中性,即总电荷为0,但是带正电和负电
2 2 3 2
的原子不同的两性离子称为内盐,根据上述分子的键线式结构可知,Y为内盐,但Z不是内盐,C错误;
D项,该过程中,步骤①为加成过程,步骤④为加氢还原过程,步骤③为脱水过程,涉及还原反应、脱水
反应、加成反应,D正确;故选C。
13.(2022·浙江省温州市高三高考适应性测试二模)某课题组设计一种以甲醇辅助固定CO 的方法,原
2
理如图。下列说法不正确的是( )A.化合物A为CHOH
3
B.若用HOCH CHOH辅助固定,则产物可能为
2 2
C.反应原料中的原子100%转化为产物
D.反应②的类型为加成反应
【答案】C
【解析】根据题意和原子守恒,① +CHOH→HO+ ②
3 2
+CO → ③ +CH OH→ +
2 3
,总反应为2CHOH+CO →HO+ 。A项,① + →HO+
3 2 2 2
,化合物A为CHOH,故A正确;B项,根据总反应,若用HOCH CHOH辅助固定,
3 2 2
HOCH CHOH+CO →H2O+ ,则产物可能为 ,故B正确;C项,根据总反应,
2 2 2
产物中有水生成,反应原料中的原子利用率小于100%,故C错误;D项,反应②中二氧化碳分子中有碳
氧双键断裂,反应②的类型为加成反应,故D正确;故选C。
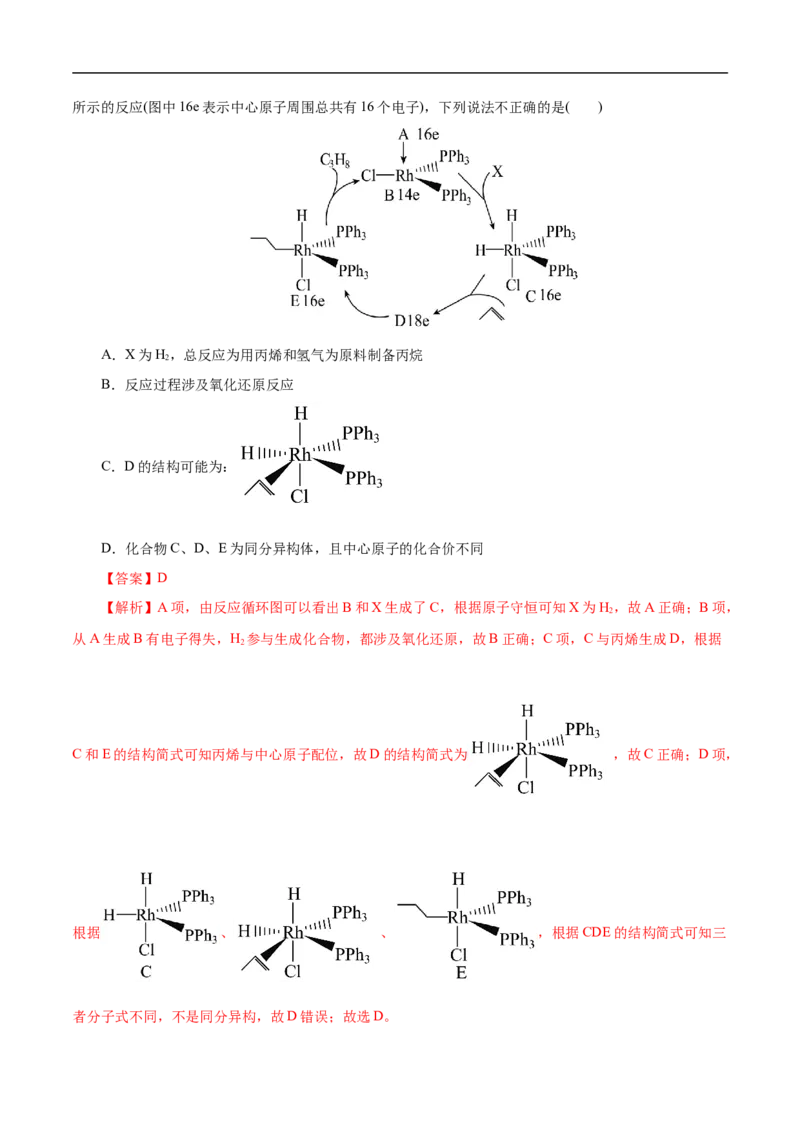
14.(2022·浙江省名校协作体高三下学期化学模拟联考)化合物A( )进行如下图所示的反应(图中16e表示中心原子周围总共有16个电子),下列说法不正确的是( )
A.X为H,总反应为用丙烯和氢气为原料制备丙烷
2
B.反应过程涉及氧化还原反应
C.D的结构可能为:
D.化合物C、D、E为同分异构体,且中心原子的化合价不同
【答案】D
【解析】A项,由反应循环图可以看出B和X生成了C,根据原子守恒可知X为H,故A正确;B项,
2
从A生成B有电子得失,H 参与生成化合物,都涉及氧化还原,故B正确;C项,C与丙烯生成D,根据
2
C和E的结构简式可知丙烯与中心原子配位,故D的结构简式为 ,故C正确;D项,
根据 、 、 ,根据CDE的结构简式可知三
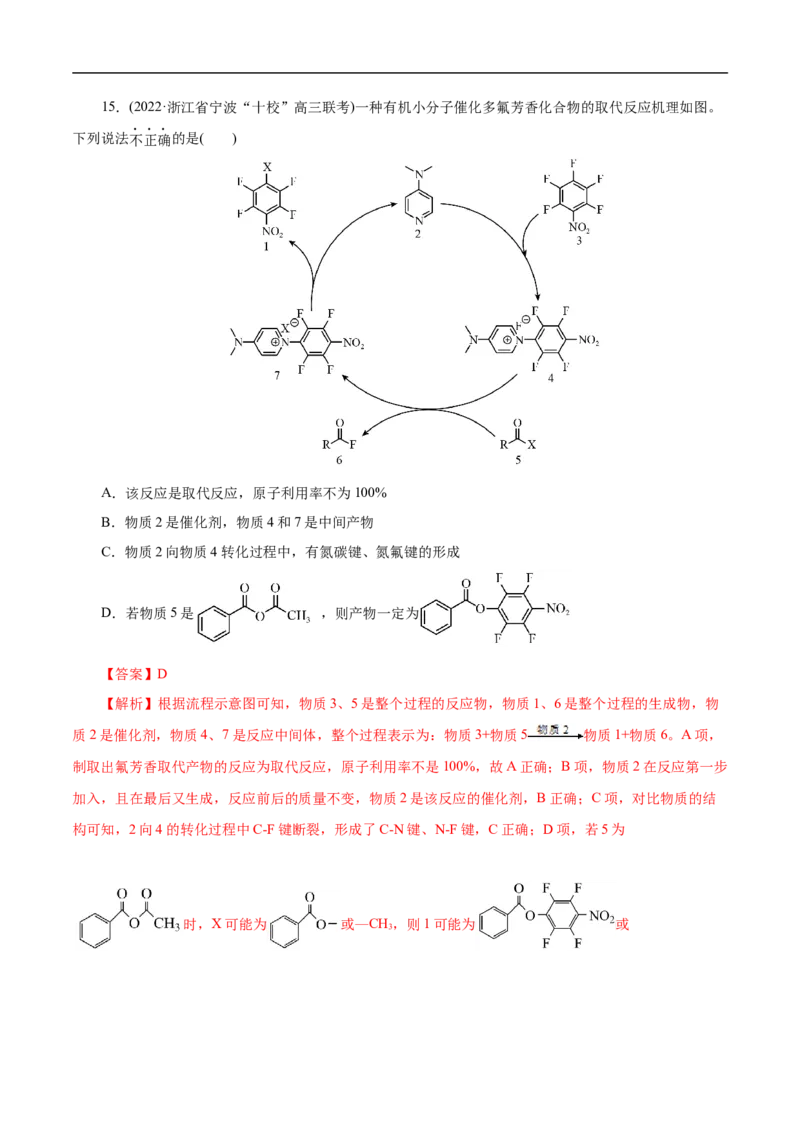
者分子式不同,不是同分异构,故D错误;故选D。15.(2022·浙江省宁波“十校”高三联考)一种有机小分子催化多氟芳香化合物的取代反应机理如图。
下列说法不正确的是( )
A.该反应是取代反应,原子利用率不为100%
B.物质2是催化剂,物质4和7是中间产物
C.物质2向物质4转化过程中,有氮碳键、氮氟键的形成
D.若物质5是 ,则产物一定为
【答案】D
【解析】根据流程示意图可知,物质3、5是整个过程的反应物,物质1、6是整个过程的生成物,物
质2是催化剂,物质4、7是反应中间体,整个过程表示为:物质3+物质5 物质1+物质6。A项,
制取出氟芳香取代产物的反应为取代反应,原子利用率不是100%,故A正确;B项,物质2在反应第一步
加入,且在最后又生成,反应前后的质量不变,物质2是该反应的催化剂,B正确;C项,对比物质的结
构可知,2向4的转化过程中C-F键断裂,形成了C-N键、N-F键,C正确;D项,若5为
时,X可能为 或—CH,则1可能为 或
3,故D错误。故选D。
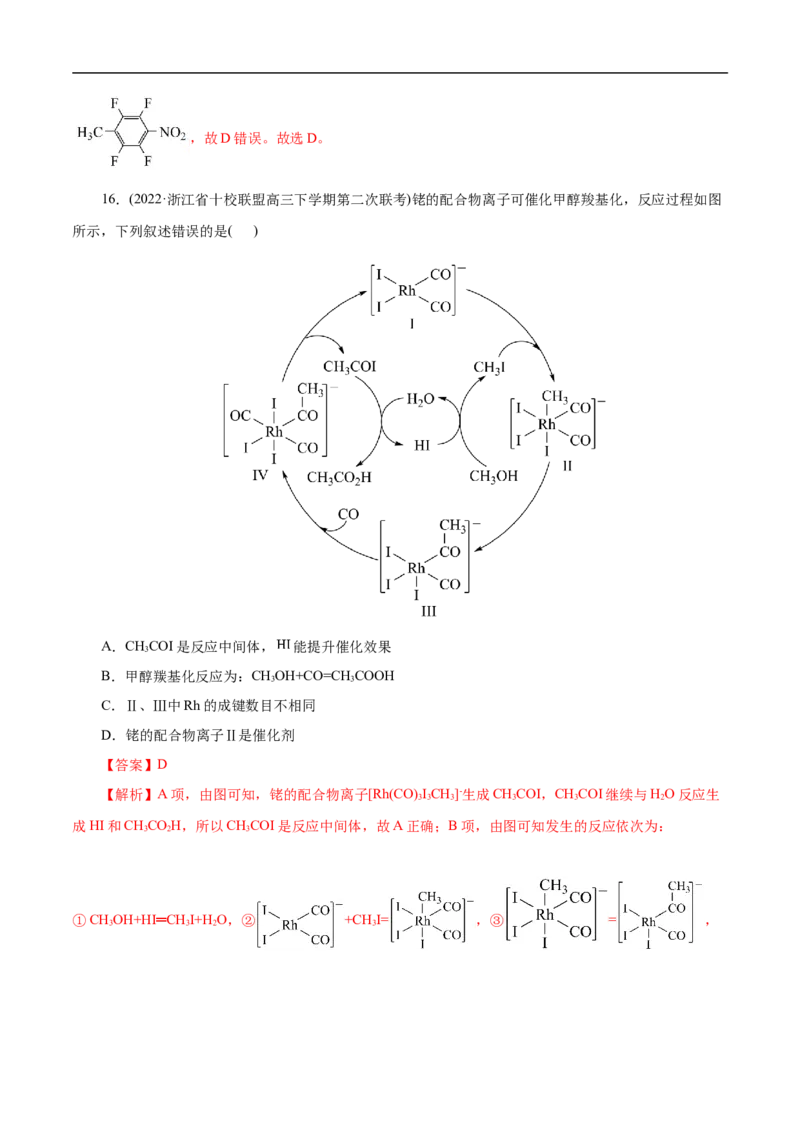
16.(2022·浙江省十校联盟高三下学期第二次联考)铑的配合物离子可催化甲醇羧基化,反应过程如图
所示,下列叙述错误的是( )
A.CHCOI是反应中间体, 能提升催化效果
3
B.甲醇羰基化反应为:CHOH+CO=CH COOH
3 3
C.Ⅱ、Ⅲ中Rh的成键数目不相同
D.铑的配合物离子Ⅱ是催化剂
【答案】D
【解析】A项,由图可知,铑的配合物离子[Rh(CO) ICH]-生成CHCOI,CHCOI继续与HO反应生
3 3 3 3 3 2
成HI和CHCOH,所以CHCOI是反应中间体,故A正确;B项,由图可知发生的反应依次为:
3 2 3
①CHOH+HI═CH I+H O,② +CH I= ,③ = ,
3 3 2 3④ +CO= ,⑤ =CH COI+ ,
3
⑥CHCOI+HO=HI+CHCOH,6个反应依次发生,6个反应方程式相加和,消去中间产物得出总反应:
3 2 3 2
CHOH+CO═CH COOH,故B正确;C项,由图可以看出Rh的成键数目由4变为6再变为5再变为6再变
3 3
为4,依次循环,故C正确;D项,铑的配合物离子Ⅱ先生成后消耗,是中间产物,故D错误;故选D。
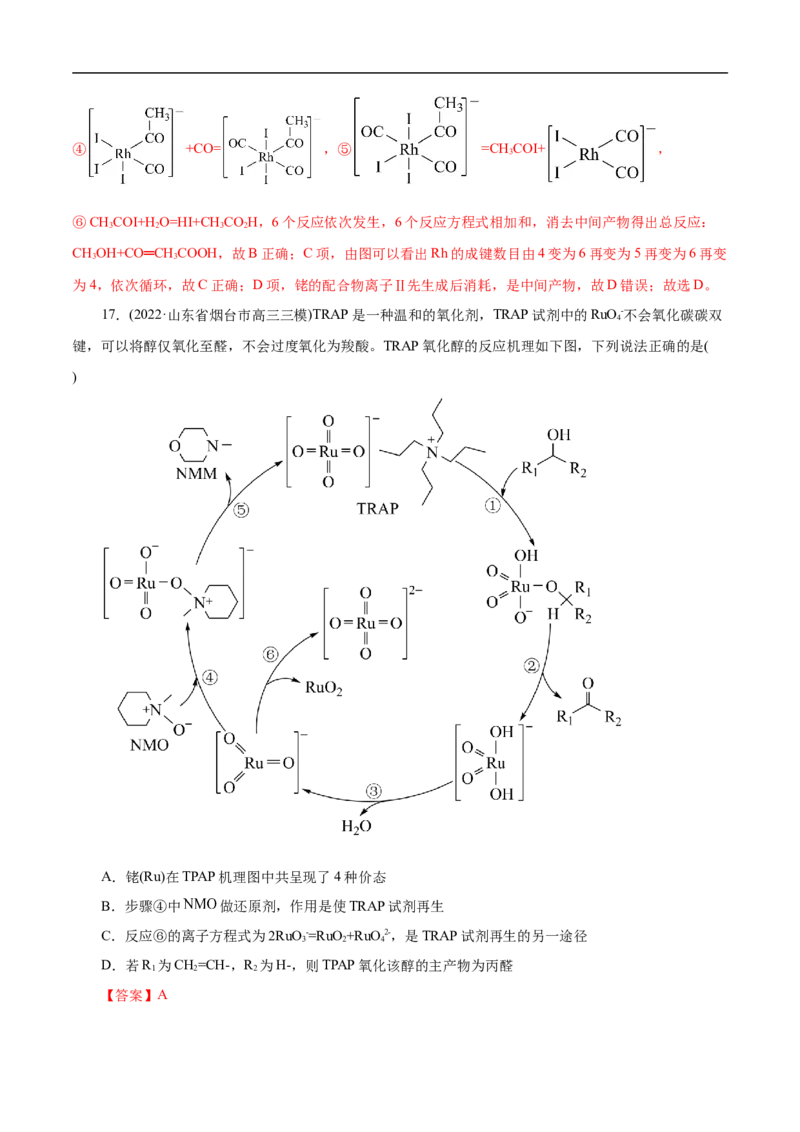
17.(2022·山东省烟台市高三三模)TRAP是一种温和的氧化剂,TRAP试剂中的RuO-不会氧化碳碳双
4
键,可以将醇仅氧化至醛,不会过度氧化为羧酸。TRAP氧化醇的反应机理如下图,下列说法正确的是(
)
A.铑(Ru)在TPAP机理图中共呈现了4种价态
B.步骤④中 做还原剂,作用是使TRAP试剂再生
C.反应⑥的离子方程式为2RuO-=RuO+RuO2-,是TRAP试剂再生的另一途径
3 2 4
D.若R 为CH=CH-,R 为H-,则TPAP氧化该醇的主产物为丙醛
1 2 2
【答案】A【解析】根据题中的反应机理图,TRAP试剂中的RuO-,经历过程①和②将 氧化为
4
,本身被还原为HRuO-,HRuO-经历过程③脱水,得到RuO-;RuO-与NMO反应,经历过
2 4 2 4 3 3
程④和⑤得到RuO-和NMM;RuO-自身发生歧化反应⑥,得到RuO2-和RuO。A项,铑(Ru)在TPAP机理
4 3 4 2
图中共呈现了4种价态,分别是+4价、+5价、+6价、+7价,A项正确;B项,RuO-与NMO反应,经过
3
过程④和⑤得到RuO-和NMM,其中Ru元素从+5价升至+7价,则RuO-做还原剂,NMO做氧化剂,B项
4 3
错误;C项,RuO-自身发生歧化反应⑥,离子方程式为2RuO-=RuO+RuO2-,产物不是RuO-,则不是
3 3 2 4 4
TRAP试剂再生的另一途径,C项错误;D项,TRAP试剂中的RuO-不会氧化碳碳双键,可以将醇仅氧化
4
至醛,若R 为CH=CH-,R 为H-,则RuO-经过过程①和②将 氧化为 ,
1 2 2 4
D项错误;故选A。
18.(2023届·浙江省Z20名校新高考研究联盟高三第一次联考)某催化剂催化烯烃醛基化的过程如图。
下列说法不正确的是( )
A.配合物HCo(CO) 的配体CO中提供孤对电子的是C原子
3
B.烯制备醛的总反应:RCH=CH+H +CO RCHCHCHO
2 2 2 2
C.如图循环转化过程中既存在π、σ及配位键的断裂,也存在π、σ及配位键的形成
D.可以用溴的四氯化碳溶液鉴别制得的产物RCHCHCHO中是否含有未完全转化RCH=CH
2 2 2
【答案】C【解析】A项,CO形成碳氧叁键后,两原子均有孤对电子,其中C原子半径更大,更易提供电子,
故配合物HCo(CO) 的配体CO中提供孤对电子的是C原子,A正确;B项,根据图示催化过程可知,烯制
3
备醛的总反应:RCH=CH+H +CO RCHCHCHO,B正确;C项,过程①碳碳双键变为单键、Co-
2 2 2 2
H键断裂生成Co-CO,有σ及配位键的断裂及形成,过程②碳氧叁键变为碳氧双键,断裂σ键,过程
③+④则Co-C键变为Co-H键和C-H键,有配位键的断裂和形成,整个过程没有π键断裂或形成,C不正
确;D项,RCHCHCHO没有碳碳双键,与溴的四氯化碳溶液不反应,而RCH=CH 含有碳碳双键可与溴
2 2 2
单质发生加成反应使溴的四氯化碳溶液褪色,D正确;故选C。
19.(2023届·浙江省名校协作体高三开学考试)某种制备HO 的反应机理如图。下列说法不正确的是(
2 2
)
A.总反应可表示为H+O HO B.HO 分子中,最多有3个原子共平面
2 2 2 2 2 2
C.HCl和 可循环利用 D.①②③均为氧化还原反应
【答案】D
【解析】A项,由反应机理可知,氢气和氧气在[PdCl ]2-的作用下生成过氧化氢,反应的化学方程式为:
4
H+O HO,A项正确;B项,HO 的分子结构为: ,最多有3个原子共平面,B项正
2 2 2 2 2 2
确;C项,依据过程图可知,HCl和Cl-可循环利用,C项正确;D项,①、②均为氧化还原反应,③不是
氧化还原反应,D项错误;故选D。
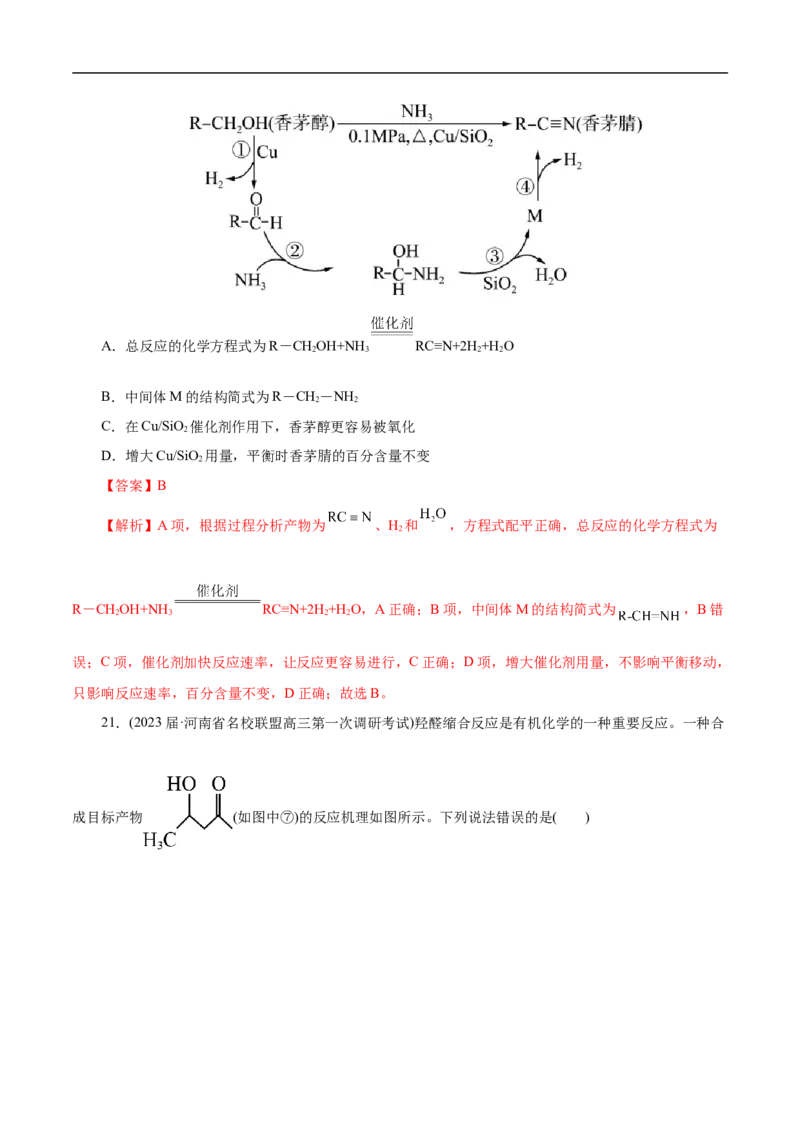
20.(2023届·山东省部分学校高三摸底考试)用Cu/SiO 催化香茅醇制取香料香茅腈反应及机理如图所
2
示。下列说法错误的是( )A.总反应的化学方程式为R-CHOH+NH RC≡N+2H +H O
2 3 2 2
B.中间体M的结构简式为R-CH-NH
2 2
C.在Cu/SiO 催化剂作用下,香茅醇更容易被氧化
2
D.增大Cu/SiO 用量,平衡时香茅腈的百分含量不变
2
【答案】B
【解析】A项,根据过程分析产物为 、H 和 ,方程式配平正确,总反应的化学方程式为
2
R-CHOH+NH RC≡N+2H +H O,A正确;B项,中间体M的结构简式为 ,B错
2 3 2 2
误;C项,催化剂加快反应速率,让反应更容易进行,C正确;D项,增大催化剂用量,不影响平衡移动,
只影响反应速率,百分含量不变,D正确;故选B。
21.(2023届·河南省名校联盟高三第一次调研考试)羟醛缩合反应是有机化学的一种重要反应。一种合
成目标产物 (如图中⑦)的反应机理如图所示。下列说法错误的是( )A.①是该反应的催化剂
B.③到④的过程中,有极性键的断裂和非极性键的生成
C.③④⑥均是该反应的中间产物
D.合成⑦的总反应为
【答案】D
【解析】A项,①是第一个反应的反应物,也是最后一个反应的生成物,所以是该反应的催化剂,故
A正确;B项,③到④的过程中,有C—N极性键的断裂和C—C非极性键的生成,故B正确;C项,由图
可知,③④⑥均是先生成后消耗,都是该反应的中间产物,故C正确;D项,合成⑦的总反应为
,故D错误;故选D。
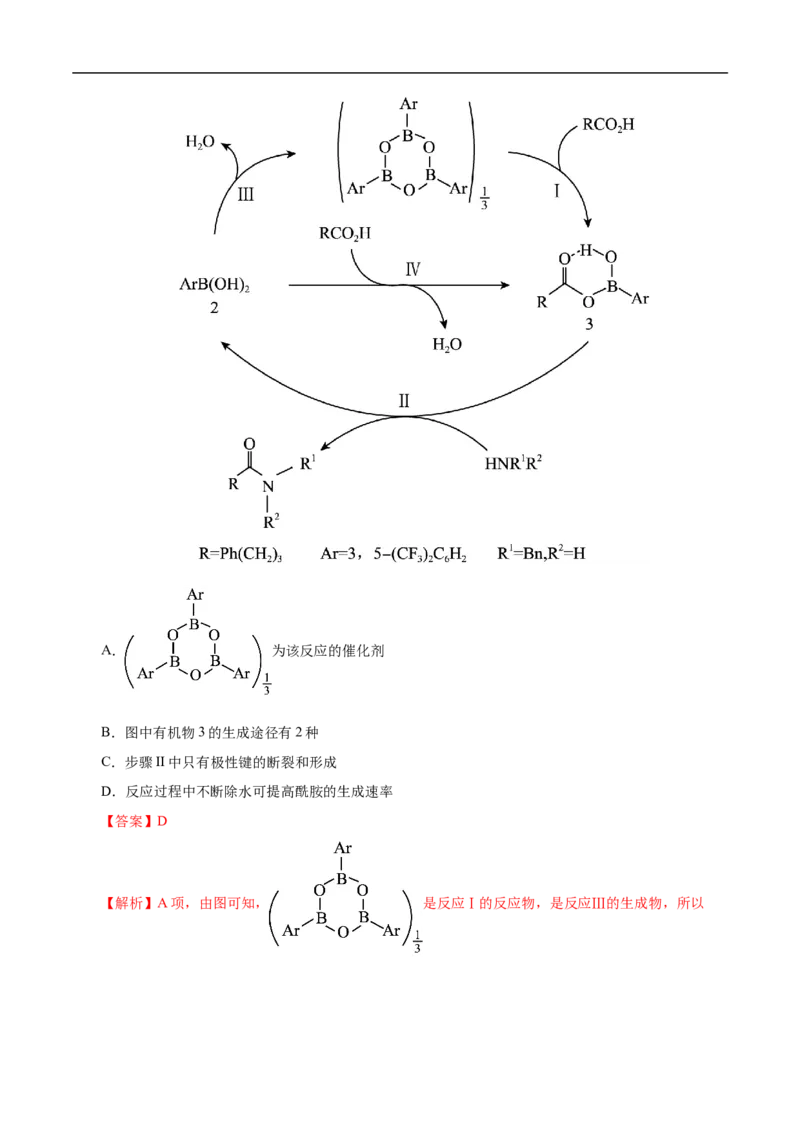
22.(2023届·河南省重点高中高三联考)在催化剂作用下,羧酸和胺脱水的反应机理如图所示。下列说
法错误的是( )A. 为该反应的催化剂
B.图中有机物3的生成途径有2种
C.步骤II中只有极性键的断裂和形成
D.反应过程中不断除水可提高酰胺的生成速率
【答案】D
【解析】A项,由图可知, 是反应Ⅰ的反应物,是反应Ⅲ的生成物,所以是反应的催化剂,故A正确;B项,由图可知,有机物3可以通过反应Ⅰ生成,也
能通过反应Ⅳ生成,所以生成途径有2种,故B正确;C项,由图可知,步骤II中,有机物3断裂了碳氧
键、胺断裂了氮氢键,产物中形成了碳氮键和氢氧键,反应中只有极性键的断裂和形成,故C正确;D项,
由图可知,羧酸和胺脱水时,水和酰胺是反应的生成物,反应过程中不断除水,可使平衡向正反应方向移
动,提高酰胺的产率,但生成速率减小,故D错误;故选D。
23.(2023届·河北省省级联测第一次联考)中国科学院化学研究所范青华和陈辉等,研究发现了首例非
贵金属锰—全氮大环配体催化烯丙醇的高效、高对映选择性氢胺化反应,反应机理如图(已知手性碳是指连
有四个不同原子或原子团的碳原子, 、 、 代表烃基或H)。下列说法正确的是( )
A.' 中含有手性碳原子
B.甲和乙中各元素化合价均相同
C.在烯丙醇氢胺化反应中,化合物乙是催化剂D.以 和 为原料,反应产物为
【答案】A
【解析】A项, 中含有手性碳原子,用“*”标出的碳原子连接H、-OH、R和乙烯基四
种不同原子或原子团,A正确;B项,根据甲、乙的结构简式可知,甲比乙少2个H原子,甲转化为乙为
还原,各元素化合价不可能全部相同,B错误;C项,根据转化图可知,在烯丙醇氢胺化反应中,化合物
甲是催化剂,化合物乙是中间产物,C错误;D项,参照流程,以 和 为原料,反应产物
为 ,D错误;故选A。