文档内容
第一篇 化学基本概念
微练 9 新情境的方程式书写
化学方程式是最具有化学学科特征的一种化学用语,陌生方程式的书写是高考题中常见的题型,往往
通过陌生情境下题干语言或化工流程,给出反应发生的环境,写出反应的化学方程式。这是“信息量大”
的一类题型,用于考查学生接受、整合化学信息和分析解决问题的能力,陌生方程式综合性强,能力要求
高,也是考生失分较多的题型之一。书写一些不曾熟悉的化学反应方程式的过程,实际是对信息的加工过
程,由于信息题大多数是由题干和若干问题两部分组成,其中题干给出一系列解题所要的条件、知识、启
发性提示等。这就要求通过阅读题干、发现本质、寻求规律,进而完成旧知识在新情景中的正确迁移。解
答陌生情境中的氧化还原反应方程式书写问题时,首先要根据材料中的信息写出反应物和生成物的化学式,
然后再根据得失电子(化合价升降法)配平,对于离子反应还要遵循电荷守恒规律。写化学方程式是一件非
常细致的工作,因此是学习化学的难点,总结许多成功者的经验归结为 “一角二平三条件,四要瞄准放
暗箭”,“一角”指写化学式要注意角码,“二平”指写化学方程式必须要配平,“三条件”强调的是要
在化学方程式的等号上下注明反应条件,“四要瞄准放暗箭”这种说法是一种为了加强记忆而采用的诙谐
语句,强调要在生成物的化学式右侧适当标出气体或沉淀的箭号,即↑或↓这是保证化学方程式完整性必
不可少的一步。
【例1】(2022•河北省选择性考试)以焙烧黄铁矿FeS(杂质为石英等)产生的红渣为原料制备铵铁蓝
2
Fe(NH )Fe(CN) 颜料。工艺流程如下:
4 6(3)还原工序中,不生成S单质的反应的化学方程式为_______。
(5)沉铁工序产生的白色沉淀Fe(NH )Fe(CN) 中 的化合价为_______,氧化工序发生反应的离子方程
4 2 6
式为_______。
【答案】(1)7Fe (SO )+FeS +8H O=15FeSO +8H SO
2 4 3 2 2 4 2 4
(2) +2 Fe(NH )Fe(CN) +ClO-+2H+=Fe(NH)Fe(CN) +H O+Cl-+NH+
4 2 6 4 6 2 4
【解析】(1)还原工序中,不产生S单质沉淀,则硫元素被氧化为SO 2-,反应原理为:14Fe3+
4
+FeS +8H O=15Fe2++2 SO 2-+16H+,故化学方程式为:7Fe (SO )+FeS +8H O=15FeSO +8H SO ;(2)沉铁工
2 2 4 2 4 3 2 2 4 2 4
序中产生的白色沉淀Fe(NH )Fe(CN) 中Fe的化合价为+2价和[Fe(CN) ]4-中的+3价,由分析可知,氧化工
4 2 6 6
序所发生的离子方程式为:6Fe(NH )Fe(CN) + ClO - +6H+=6Fe(NH)Fe(CN) +3H O+Cl-+6 NH +。
4 2 6 3 4 6 2 4
【例2】(2020•新课标Ⅲ卷)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的
NiOOH。写出该反应的离子方程式______________。
【答案】2Ni2++ClOˉ+4OHˉ=2NiOOH↓+Clˉ+H O
2
【解析】由题干信息,硫酸镍在强碱中被NaClO氧化得到NiOOH沉淀,即反应中Ni2+被氧化为
NiOOH沉淀,ClOˉ被还原为Clˉ,则根据氧化还原得失电子守恒可得离子方程式为2Ni2+
+ClOˉ+4OHˉ=2NiOOH↓+Clˉ+H O。书写步骤如下:
2
1.新情境下氧化还原反应方程式的书写流程
根据题目叙述,从文字信息或流程图信息中提炼反应物、生成物,进而分析反应中电子的得失情况,
其流程为:2.分步法书写方程式
陌生的非氧化还原反应主要为复分解反应,抓住复分解反应条件推断产物,结合盐类水解、酸碱强弱
综合分析。这类复杂的化学反应可以采用分步思考,例如,碳酸钠、氢氟酸和氢氧化铝混合物在高温下反
应 制 备 冰 晶 石 , 可 以 分 三 步 理 解 : Al(OH) +3HF=AlF +3H O , NaCO+2HF=2NaF+CO ↑+H O ,
3 3 2 2 3 2 2
AlF+3NaF=Na AlF 。加合得到总反应式为2Al(OH) +3Na CO+12HF=2Na AlF+3CO ↑+9H O。再如在碳酸
3 3 6 3 2 3 3 6 2 2
氢钠溶液中加入少量硫酸亚铁溶液制备碳酸亚铁:Fe2++HCO-=FeCO ↓+H+,H++ HCO -=CO ↑+H O,加合
3 3 3 2 2
得总反应式为Fe2++2 HCO -=FeCO ↓+CO ↑+H O。
3 3 2 2
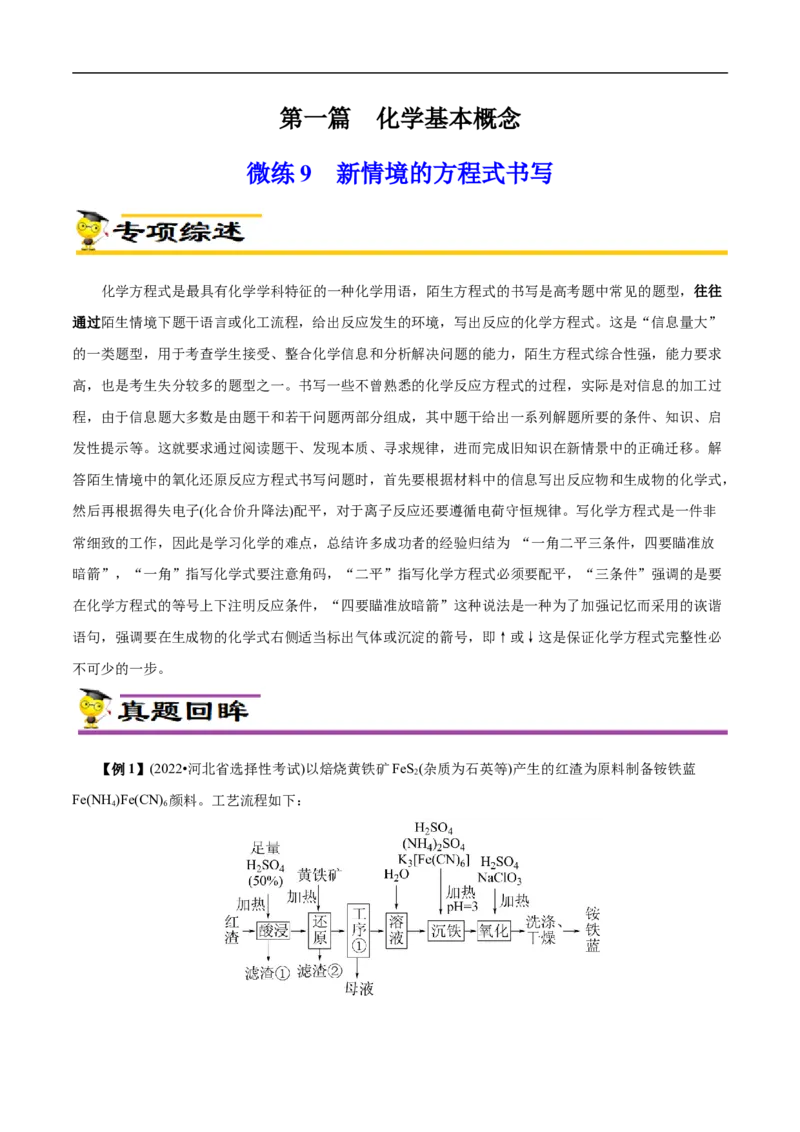
1.氯化亚铜是一种应用较广的催化剂,易水解,微溶于水,不溶于乙醇。以低品位铜矿砂(主要成分
)为原料制备氯化亚铜的路线如下:
(1)“酸溶1”步骤中发生反应的化学方程式为_______。
(2)“除锰”步骤中Mn2+转化为MnCO 沉淀,CuSO 转变为Cu(NH )CO 留在溶液中。则“除锰”步骤
3 4 3 4 3
中发生反应的离子方程式为_______。
(3)“合成”步骤加入NaSO 的速率不宜过快,否则会产生_______气体(写化学式),除可能与酸溶时硫
2 3
酸过量有关,还可能的原因是_______。(用离子方程式表示)。
2.常温下,二氧化氯(ClO )是一种黄绿色气体,具有强氧化性,已被联合国世界卫生组织(WHO)列为
2
AI级高效安全消毒剂。常温下,它可用氯酸钠固体与浓盐酸反应制备得到,该反应体系中的物质有NaCl
、HO、ClO 、NaClO、Cl、HCl。
2 2 3 2(1)写出并配平该反应的化学方程式 _____________________________________。
(2)二氧化氯可迅速氧化硫化物(其中还原产物中氯元素为负一价),以除去水中硫化物产生的臭味。取
适量ClO 通入到含有HS(二元弱酸)的水中,再向其中加入少量氯化钡溶液,发现有白色沉淀生成。写出
2 2
ClO 与HS水溶液反应的离子方程式_________________________________。
2 2
3.软锰矿的主要成分为MnO ,含少量Al O 和SiO 杂质。闪锌矿的主要成分为ZnS,含少量FeS、
2 2 3 2
CuS、CdS杂质。现以软锰矿和闪锌矿为原料制备MnO 和Zn,其简化流程如下(中间产物的固体部分已经
2
略去)。
①中发生多个反应,其中MnO 、FeS与硫酸共热时有淡黄色物质析出,溶液变为棕黄色,写出
2
MnO 、FeS与硫酸共热发生反应的化学方程式: 。
2
4.研究发现钼酸钠可减缓金属的腐蚀速率。工业上利用钼精矿(主要成分是不溶于水的MoS ,含少量
2
重金属化合物)制备钼酸钠晶体(Na MoO ·2H O)的途径如图所示:
2 4 2
途径①制备钼酸钠溶液,同时有SO 2-生成,该反应的离子方程式为 。
4
5.工业上用钛白渣[主要成分为FeSO ,还含有少量Fe (SO )、MgSO 及TiOSO ]为主要原料生产氧化
4 2 4 3 4 4
铁黄(FeOOH)的一种工艺流程如下:
(1)“溶解”时,TiOSO 发生水解生成难溶于水的HTiO,反应的化学方程式为
4 2 3
__________________________。
(2)“氧化”时,Fe2+生成FeOOH的离子方程式是______________________________________。
6.硼氢化锰[Mn(BH )]可以用作储氢材料,也能用于科学研究。以富锰渣(含60%MnO,还含有
4 2SiO、Al O、CaO、FeO)为原料制备硼氢化锰的工艺流程如下。
2 2 3
已知几种氢氧化物的K 的值如下表:
sp
(1)“氧化”中发生反应的离子方程式为__________________________,该反应中氧化性:Fe3+
__________(填“>”或“<”)MnO。
2
(2)Mn(BH ) 能与稀盐酸反应生成HBO,该反应的化学方程式为______________________________。
4 2 3 3
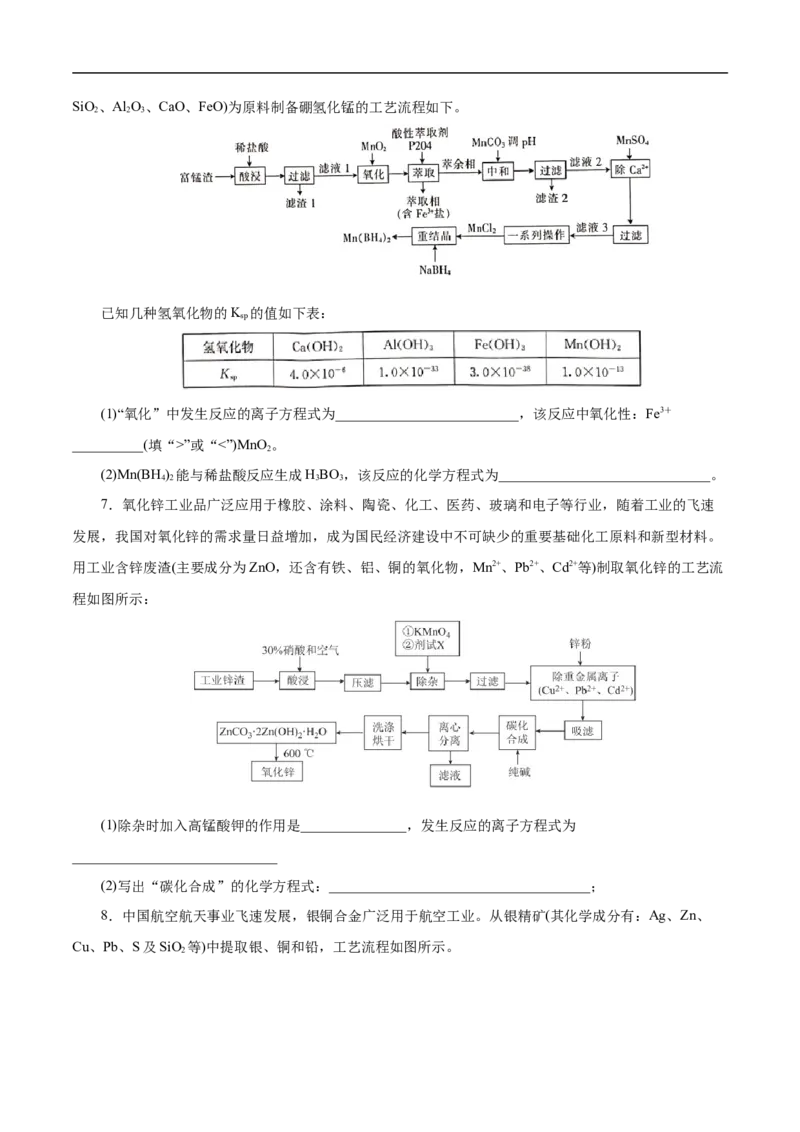
7.氧化锌工业品广泛应用于橡胶、涂料、陶瓷、化工、医药、玻璃和电子等行业,随着工业的飞速
发展,我国对氧化锌的需求量日益增加,成为国民经济建设中不可缺少的重要基础化工原料和新型材料。
用工业含锌废渣(主要成分为ZnO,还含有铁、铝、铜的氧化物,Mn2+、Pb2+、Cd2+等)制取氧化锌的工艺流
程如图所示:
(1)除杂时加入高锰酸钾的作用是_______________,发生反应的离子方程式为
_____________________________
(2)写出“碳化合成”的化学方程式:_____________________________________;
8.中国航空航天事业飞速发展,银铜合金广泛用于航空工业。从银精矿(其化学成分有:Ag、Zn、
Cu、Pb、S及SiO 等)中提取银、铜和铅,工艺流程如图所示。
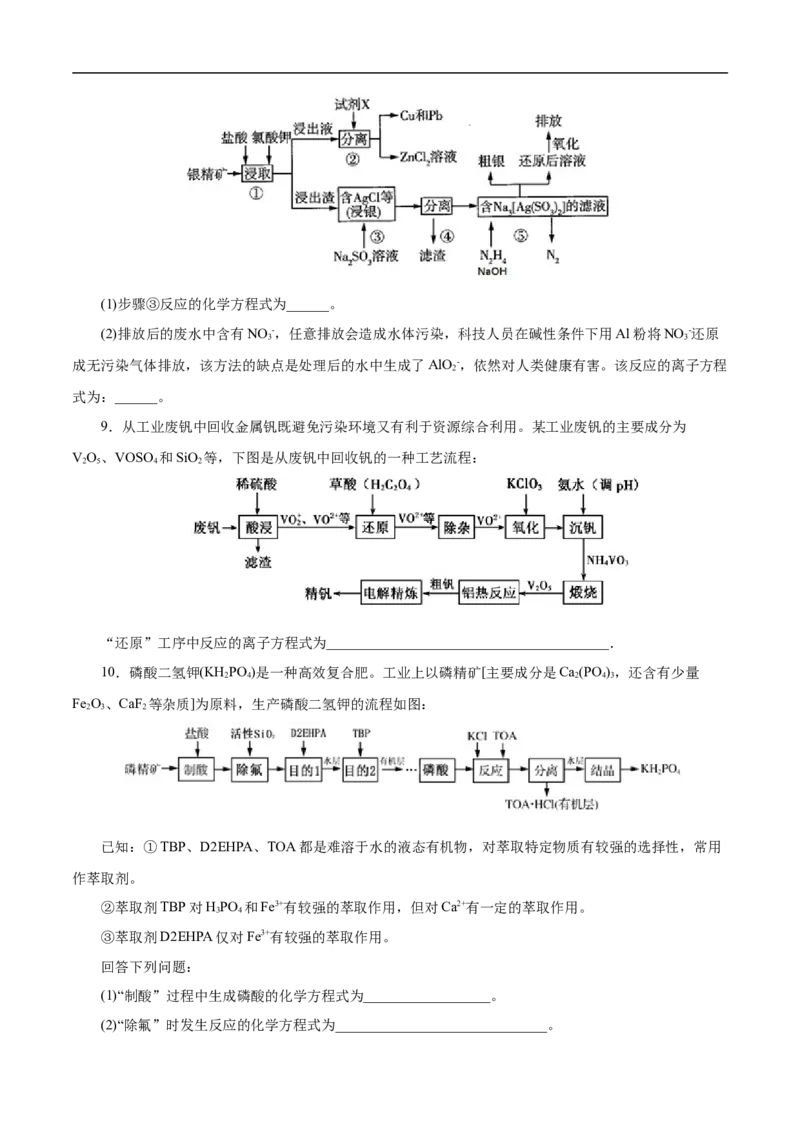
2(1)步骤③反应的化学方程式为______。
(2)排放后的废水中含有NO -,任意排放会造成水体污染,科技人员在碱性条件下用Al粉将NO -还原
3 3
成无污染气体排放,该方法的缺点是处理后的水中生成了AlO-,依然对人类健康有害。该反应的离子方程
2
式为:______。
9.从工业废钒中回收金属钒既避免污染环境又有利于资源综合利用。某工业废钒的主要成分为
VO、VOSO 和SiO 等,下图是从废钒中回收钒的一种工艺流程:
2 5 4 2
“还原”工序中反应的离子方程式为________________________________________.
10.磷酸二氢钾(KH PO )是一种高效复合肥。工业上以磷精矿[主要成分是Ca (PO ),还含有少量
2 4 2 4 3
Fe O、CaF 等杂质]为原料,生产磷酸二氢钾的流程如图:
2 3 2
已知:①TBP、D2EHPA、TOA都是难溶于水的液态有机物,对萃取特定物质有较强的选择性,常用
作萃取剂。
②萃取剂TBP对HPO 和Fe3+有较强的萃取作用,但对Ca2+有一定的萃取作用。
3 4
③萃取剂D2EHPA仅对Fe3+有较强的萃取作用。
回答下列问题:
(1)“制酸”过程中生成磷酸的化学方程式为__________________。
(2)“除氟”时发生反应的化学方程式为______________________________。(3)“目的2”分离出的有机层中除HPO 外,还有少量某金属阳离子。去除有机层中该阳离子的方法是
3 4
用含HSO 的磷酸洗涤,反应的离子方程式为______________________________。
2 4
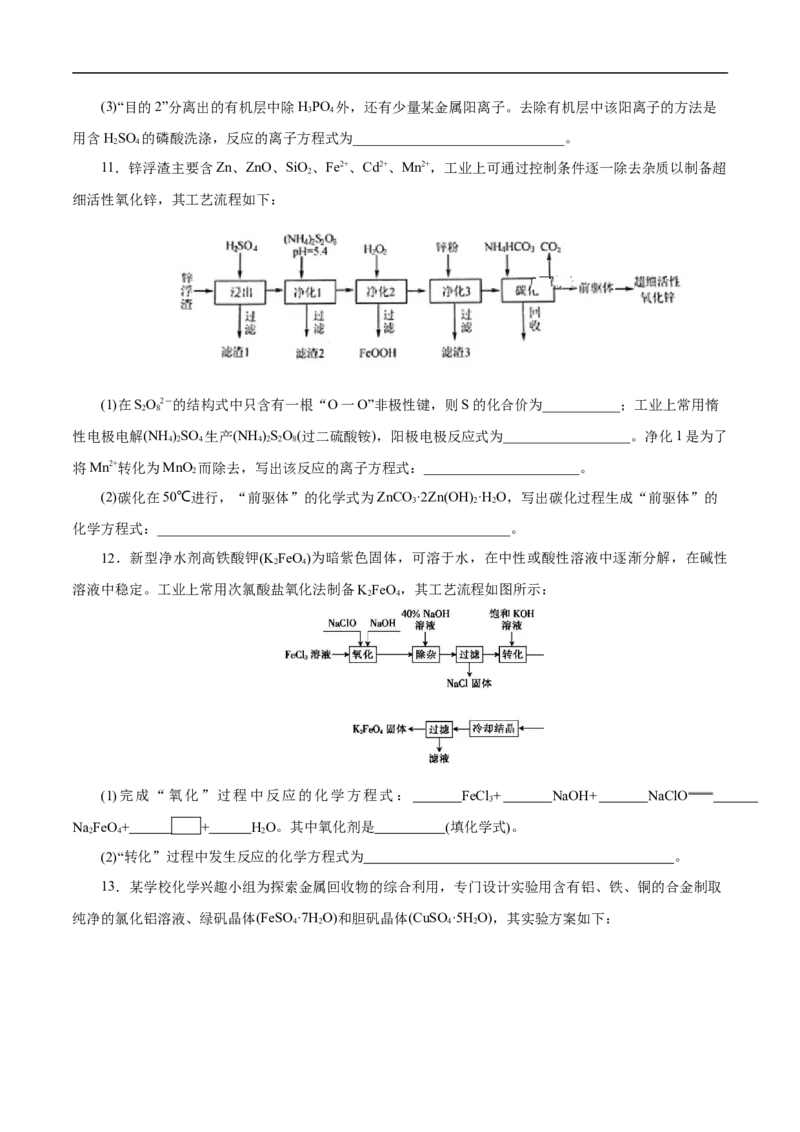
11.锌浮渣主要含Zn、ZnO、SiO、Fe2+、Cd2+、Mn2+,工业上可通过控制条件逐一除去杂质以制备超
2
细活性氧化锌,其工艺流程如下:
(1)在SO2-的结构式中只含有一根“O一O”非极性键,则S的化合价为___________;工业上常用惰
2 8
性电极电解(NH )SO 生产(NH )SO(过二硫酸铵),阳极电极反应式为__________________。净化1是为了
4 2 4 4 2 2 8
将Mn2+转化为MnO 而除去,写出该反应的离子方程式:______________________。
2
(2)碳化在50℃进行,“前驱体”的化学式为ZnCO ·2Zn(OH) ·H O,写出碳化过程生成“前驱体”的
3 2 2
化学方程式:__________________________________________________。
12.新型净水剂高铁酸钾(K FeO)为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性
2 4
溶液中稳定。工业上常用次氯酸盐氧化法制备KFeO,其工艺流程如图所示:
2 4
(1)完成“氧化”过程中反应的化学方程式: FeCl + NaOH+ NaClO
3
NaFeO+ + HO。其中氧化剂是 (填化学式)。
2 4 2
(2)“转化”过程中发生反应的化学方程式为 。
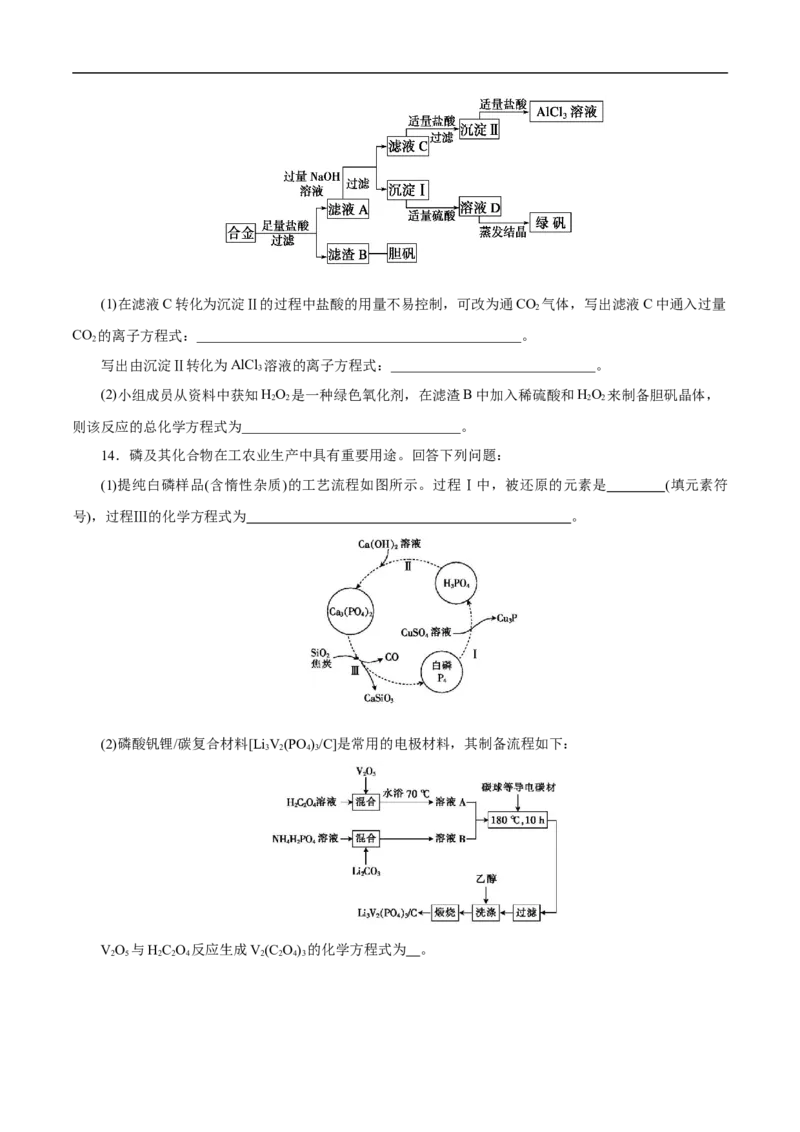
13.某学校化学兴趣小组为探索金属回收物的综合利用,专门设计实验用含有铝、铁、铜的合金制取
纯净的氯化铝溶液、绿矾晶体(FeSO ·7H O)和胆矾晶体(CuSO ·5H O),其实验方案如下:
4 2 4 2(1)在滤液C转化为沉淀Ⅱ的过程中盐酸的用量不易控制,可改为通CO 气体,写出滤液C中通入过量
2
CO 的离子方程式:______________________________________________。
2
写出由沉淀Ⅱ转化为AlCl 溶液的离子方程式:_____________________________。
3
(2)小组成员从资料中获知HO 是一种绿色氧化剂,在滤渣B中加入稀硫酸和HO 来制备胆矾晶体,
2 2 2 2
则该反应的总化学方程式为_______________________________。
14.磷及其化合物在工农业生产中具有重要用途。回答下列问题:
(1)提纯白磷样品(含惰性杂质)的工艺流程如图所示。过程Ⅰ中,被还原的元素是 (填元素符
号),过程Ⅲ的化学方程式为 。
(2)磷酸钒锂/碳复合材料[Li V(PO )/C]是常用的电极材料,其制备流程如下:
3 2 4 3
VO 与HC O 反应生成V(C O) 的化学方程式为 。
2 5 2 2 4 2 2 4 3