文档内容
第一篇 化学基本概念
微练 9 新情境的方程式书写
化学方程式是最具有化学学科特征的一种化学用语,陌生方程式的书写是高考题中常见的题型,往往
通过陌生情境下题干语言或化工流程,给出反应发生的环境,写出反应的化学方程式。这是“信息量大”
的一类题型,用于考查学生接受、整合化学信息和分析解决问题的能力,陌生方程式综合性强,能力要求
高,也是考生失分较多的题型之一。书写一些不曾熟悉的化学反应方程式的过程,实际是对信息的加工过
程,由于信息题大多数是由题干和若干问题两部分组成,其中题干给出一系列解题所要的条件、知识、启
发性提示等。这就要求通过阅读题干、发现本质、寻求规律,进而完成旧知识在新情景中的正确迁移。解
答陌生情境中的氧化还原反应方程式书写问题时,首先要根据材料中的信息写出反应物和生成物的化学式,
然后再根据得失电子(化合价升降法)配平,对于离子反应还要遵循电荷守恒规律。写化学方程式是一件非
常细致的工作,因此是学习化学的难点,总结许多成功者的经验归结为 “一角二平三条件,四要瞄准放
暗箭”,“一角”指写化学式要注意角码,“二平”指写化学方程式必须要配平,“三条件”强调的是要
在化学方程式的等号上下注明反应条件,“四要瞄准放暗箭”这种说法是一种为了加强记忆而采用的诙谐
语句,强调要在生成物的化学式右侧适当标出气体或沉淀的箭号,即↑或↓这是保证化学方程式完整性必
不可少的一步。
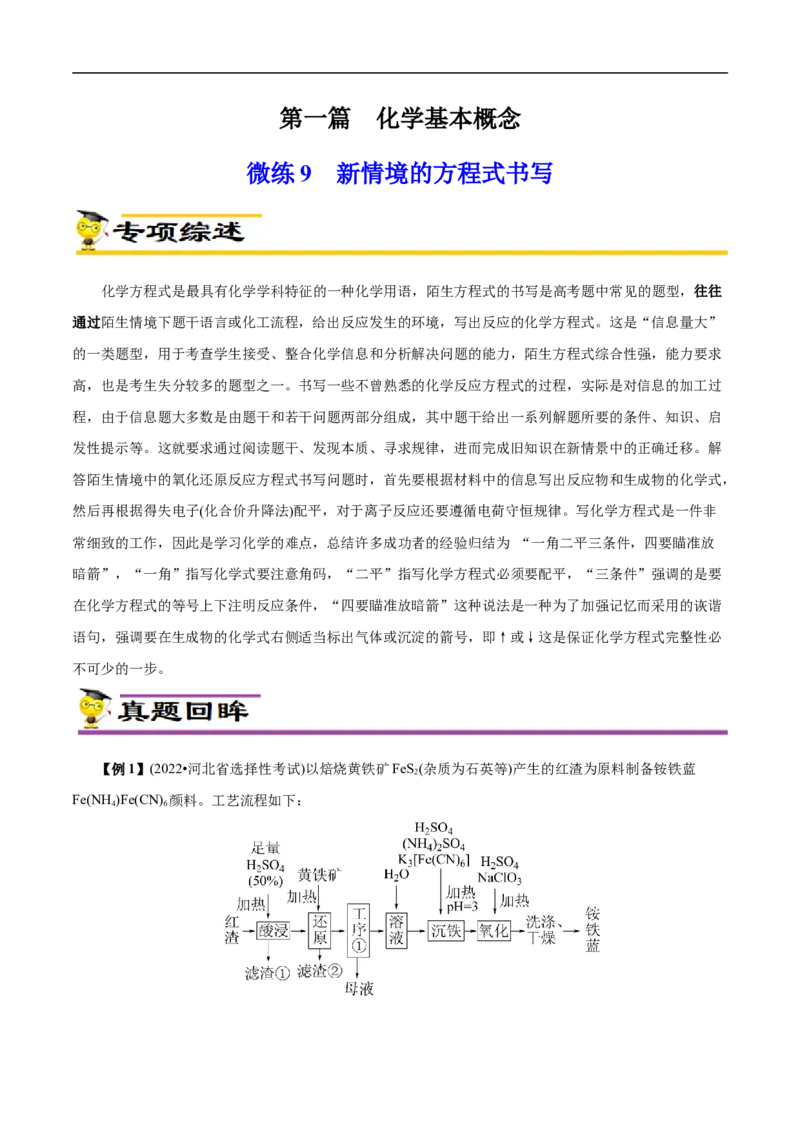
【例1】(2022•河北省选择性考试)以焙烧黄铁矿FeS(杂质为石英等)产生的红渣为原料制备铵铁蓝
2
Fe(NH )Fe(CN) 颜料。工艺流程如下:
4 6(3)还原工序中,不生成S单质的反应的化学方程式为_______。
(5)沉铁工序产生的白色沉淀Fe(NH )Fe(CN) 中 的化合价为_______,氧化工序发生反应的离子方程
4 2 6
式为_______。
【答案】(1)7Fe (SO )+FeS +8H O=15FeSO +8H SO
2 4 3 2 2 4 2 4
(2) +2 Fe(NH )Fe(CN) +ClO-+2H+=Fe(NH)Fe(CN) +H O+Cl-+NH+
4 2 6 4 6 2 4
【解析】(1)还原工序中,不产生S单质沉淀,则硫元素被氧化为SO 2-,反应原理为:14Fe3+
4
+FeS +8H O=15Fe2++2 SO 2-+16H+,故化学方程式为:7Fe (SO )+FeS +8H O=15FeSO +8H SO ;(2)沉铁工
2 2 4 2 4 3 2 2 4 2 4
序中产生的白色沉淀Fe(NH )Fe(CN) 中Fe的化合价为+2价和[Fe(CN) ]4-中的+3价,由分析可知,氧化工
4 2 6 6
序所发生的离子方程式为:6Fe(NH )Fe(CN) + ClO - +6H+=6Fe(NH)Fe(CN) +3H O+Cl-+6 NH +。
4 2 6 3 4 6 2 4
【例2】(2020•新课标Ⅲ卷)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的
NiOOH。写出该反应的离子方程式______________。
【答案】2Ni2++ClOˉ+4OHˉ=2NiOOH↓+Clˉ+H O
2
【解析】由题干信息,硫酸镍在强碱中被NaClO氧化得到NiOOH沉淀,即反应中Ni2+被氧化为
NiOOH沉淀,ClOˉ被还原为Clˉ,则根据氧化还原得失电子守恒可得离子方程式为2Ni2+
+ClOˉ+4OHˉ=2NiOOH↓+Clˉ+H O。书写步骤如下:
2
1.新情境下氧化还原反应方程式的书写流程
根据题目叙述,从文字信息或流程图信息中提炼反应物、生成物,进而分析反应中电子的得失情况,
其流程为:2.分步法书写方程式
陌生的非氧化还原反应主要为复分解反应,抓住复分解反应条件推断产物,结合盐类水解、酸碱强弱
综合分析。这类复杂的化学反应可以采用分步思考,例如,碳酸钠、氢氟酸和氢氧化铝混合物在高温下反
应 制 备 冰 晶 石 , 可 以 分 三 步 理 解 : Al(OH) +3HF=AlF +3H O , NaCO+2HF=2NaF+CO ↑+H O ,
3 3 2 2 3 2 2
AlF+3NaF=Na AlF 。加合得到总反应式为2Al(OH) +3Na CO+12HF=2Na AlF+3CO ↑+9H O。再如在碳酸
3 3 6 3 2 3 3 6 2 2
氢钠溶液中加入少量硫酸亚铁溶液制备碳酸亚铁:Fe2++HCO-=FeCO ↓+H+,H++ HCO -=CO ↑+H O,加合
3 3 3 2 2
得总反应式为Fe2++2 HCO -=FeCO ↓+CO ↑+H O。
3 3 2 2
1.氯化亚铜是一种应用较广的催化剂,易水解,微溶于水,不溶于乙醇。以低品位铜矿砂(主要成分
)为原料制备氯化亚铜的路线如下:
(1)“酸溶1”步骤中发生反应的化学方程式为_______。
(2)“除锰”步骤中Mn2+转化为MnCO 沉淀,CuSO 转变为Cu(NH )CO 留在溶液中。则“除锰”步骤
3 4 3 4 3
中发生反应的离子方程式为_______。
(3)“合成”步骤加入NaSO 的速率不宜过快,否则会产生_______气体(写化学式),除可能与酸溶时硫
2 3
酸过量有关,还可能的原因是_______。(用离子方程式表示)。
【答案】(1)CuS+MnO +2H SO =CuSO+MnSO +S+2H O
2 2 4 4 4 2
(2)Mn2++2HCO-=MnCO↓+CO ↑+H O
3 3 2 2
(3)SO 2Cu2++2Cl-+ SO 2-+H O=2CuCl↓+ SO 2-+2H+
2 3 2 4【解析】(1)酸溶1步骤中加入硫酸、MnO 得到S,除锰步骤Mn2+转化成MnCO 沉淀,可知二氧化锰
2 3
将CuS中-2价的S氧化为硫单质,则加入硫酸生成硫酸铜、硫酸锰以及S,反应的化学方程式为
CuS+MnO +2H SO =CuSO+MnSO +S+2H O。(2)“除锰”步骤中Mn2+转化为MnCO 沉淀,则“除锰”步骤
2 2 4 4 4 2 3
中发生反应的离子方程式为Mn2++2HCO-=MnCO↓+CO ↑+H O。(3)若加入NaSO 的速率过快,则NaSO
3 3 2 2 2 3 2 3
会与酸反应产生SO 气体,硫酸铜和氯化钠和亚硫酸钠和水反应生成氯化亚铜沉淀和硫酸钠和硫酸,若加
2
入较快会生成更多的酸,离子方程式为:Cu2++2Cl-+ SO 2-+H O=2CuCl↓+ SO 2-+2H+。
3 2 4
2.常温下,二氧化氯(ClO )是一种黄绿色气体,具有强氧化性,已被联合国世界卫生组织(WHO)列为
2
AI级高效安全消毒剂。常温下,它可用氯酸钠固体与浓盐酸反应制备得到,该反应体系中的物质有NaCl
、HO、ClO 、NaClO、Cl、HCl。
2 2 3 2
(1)写出并配平该反应的化学方程式 _____________________________________。
(2)二氧化氯可迅速氧化硫化物(其中还原产物中氯元素为负一价),以除去水中硫化物产生的臭味。取
适量ClO 通入到含有HS(二元弱酸)的水中,再向其中加入少量氯化钡溶液,发现有白色沉淀生成。写出
2 2
ClO 与HS水溶液反应的离子方程式_________________________________。
2 2
【答案】(1)2NaClO + 4HCl(浓)= 2ClO↑ + Cl ↑ + 2H O + 2NaCl
3 2 2 2
(2)5H S + 8ClO + 4H O = 5SO 2- + 8Cl- + 18H+
2 2 2 4
【解析】(1)氯酸钠具有强氧化性,浓盐酸具有还原性,氯酸钠固体与浓盐酸发生氧化还原反应生成二
氧化氯、氯气、氯化钠和水,反应的化学方程式为2NaClO + 4HCl(浓)= 2ClO↑ + Cl ↑ + 2H O + 2NaCl;(2)
3 2 2 2
由题意可知,ClO 与HS水溶液发生氧化还原反应生成盐酸和硫酸,根据得失电子守恒、原子守恒和电荷
2 2
守恒配平,反应的离子方程式为HS + 8ClO + 4H O = 5SO 2-+ 8Cl-+ 18H+。
2 2 2 4
3.软锰矿的主要成分为MnO ,含少量Al O 和SiO 杂质。闪锌矿的主要成分为ZnS,含少量FeS、
2 2 3 2
CuS、CdS杂质。现以软锰矿和闪锌矿为原料制备MnO 和Zn,其简化流程如下(中间产物的固体部分已经
2
略去)。
①中发生多个反应,其中MnO 、FeS与硫酸共热时有淡黄色物质析出,溶液变为棕黄色,写出
2
MnO 、FeS与硫酸共热发生反应的化学方程式: 。
2
【答案】3MnO +2FeS+6H SO Fe (SO )+3MnSO +2S+6H O
2 2 4 2 4 3 4 2
【解析】①中MnO 、FeS与硫酸共热时有淡黄色的S单质析出,溶液变为棕黄色,说明有Fe3+生成。
2
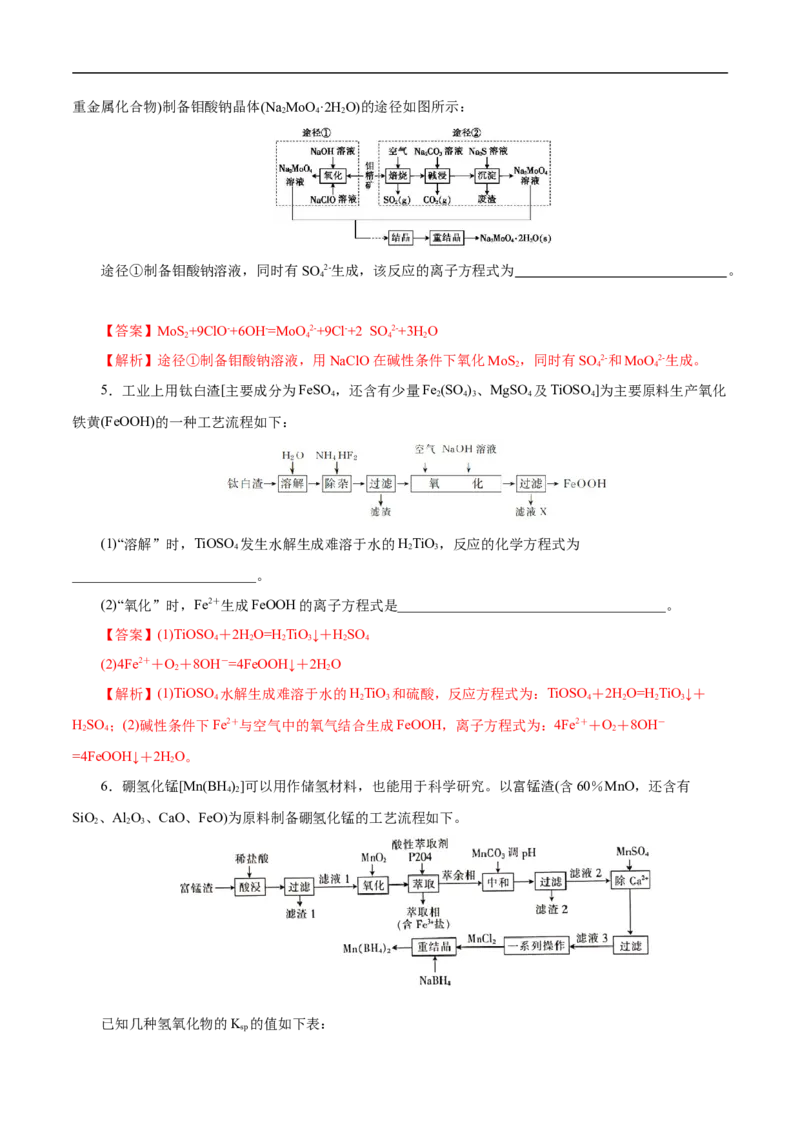
4.研究发现钼酸钠可减缓金属的腐蚀速率。工业上利用钼精矿(主要成分是不溶于水的MoS ,含少量
2重金属化合物)制备钼酸钠晶体(Na MoO ·2H O)的途径如图所示:
2 4 2
途径①制备钼酸钠溶液,同时有SO 2-生成,该反应的离子方程式为 。
4
【答案】MoS +9ClO-+6OH-=MoO 2-+9Cl-+2 SO 2-+3H O
2 4 4 2
【解析】途径①制备钼酸钠溶液,用NaClO在碱性条件下氧化MoS ,同时有SO 2-和MoO 2-生成。
2 4 4
5.工业上用钛白渣[主要成分为FeSO ,还含有少量Fe (SO )、MgSO 及TiOSO ]为主要原料生产氧化
4 2 4 3 4 4
铁黄(FeOOH)的一种工艺流程如下:
(1)“溶解”时,TiOSO 发生水解生成难溶于水的HTiO,反应的化学方程式为
4 2 3
__________________________。
(2)“氧化”时,Fe2+生成FeOOH的离子方程式是______________________________________。
【答案】(1)TiOSO +2HO=HTiO↓+HSO
4 2 2 3 2 4
(2)4Fe2++O+8OH-=4FeOOH↓+2HO
2 2
【解析】(1)TiOSO 水解生成难溶于水的HTiO 和硫酸,反应方程式为:TiOSO +2HO=HTiO↓+
4 2 3 4 2 2 3
HSO ;(2)碱性条件下Fe2+与空气中的氧气结合生成FeOOH,离子方程式为:4Fe2++O+8OH-
2 4 2
=4FeOOH↓+2HO。
2
6.硼氢化锰[Mn(BH )]可以用作储氢材料,也能用于科学研究。以富锰渣(含60%MnO,还含有
4 2
SiO、Al O、CaO、FeO)为原料制备硼氢化锰的工艺流程如下。
2 2 3
已知几种氢氧化物的K 的值如下表:
sp(1)“氧化”中发生反应的离子方程式为__________________________,该反应中氧化性:Fe3+
__________(填“>”或“<”)MnO。
2
(2)Mn(BH ) 能与稀盐酸反应生成HBO,该反应的化学方程式为______________________________。
4 2 3 3
【答案】(1)2Fe2++MnO+4H+=2Fe3++Mn2++2H O <
2 2
(2)Mn(BH )+2HCl+6H O= 2H BO+ MnCl +8H ↑
4 2 2 3 3 2 2
【解析】(1)“氧化”中是酸性溶液中二氧化锰将亚铁离子氧化生成铁离子,反应的离子方程式为2Fe2+
+MnO+4H+=2Fe3++Mn2++2H O,反应中二氧化锰是氧化剂,亚铁离子为还原剂,氧化性:Fe3+<MnO ;
2 2 2
(2)Mn(BH ) 能与稀盐酸反应生成HBO,Mn(BH ) 中H的化合价由-1价升高到0价,HCl和水中H由+1
4 2 3 3 4 2
价降低到0价形成氢气,同时生成氯化锰,反应的化学方程式为Mn(BH )+2HCl+6H O= 2H BO+
4 2 2 3 3
MnCl +8H ↑。
2 2
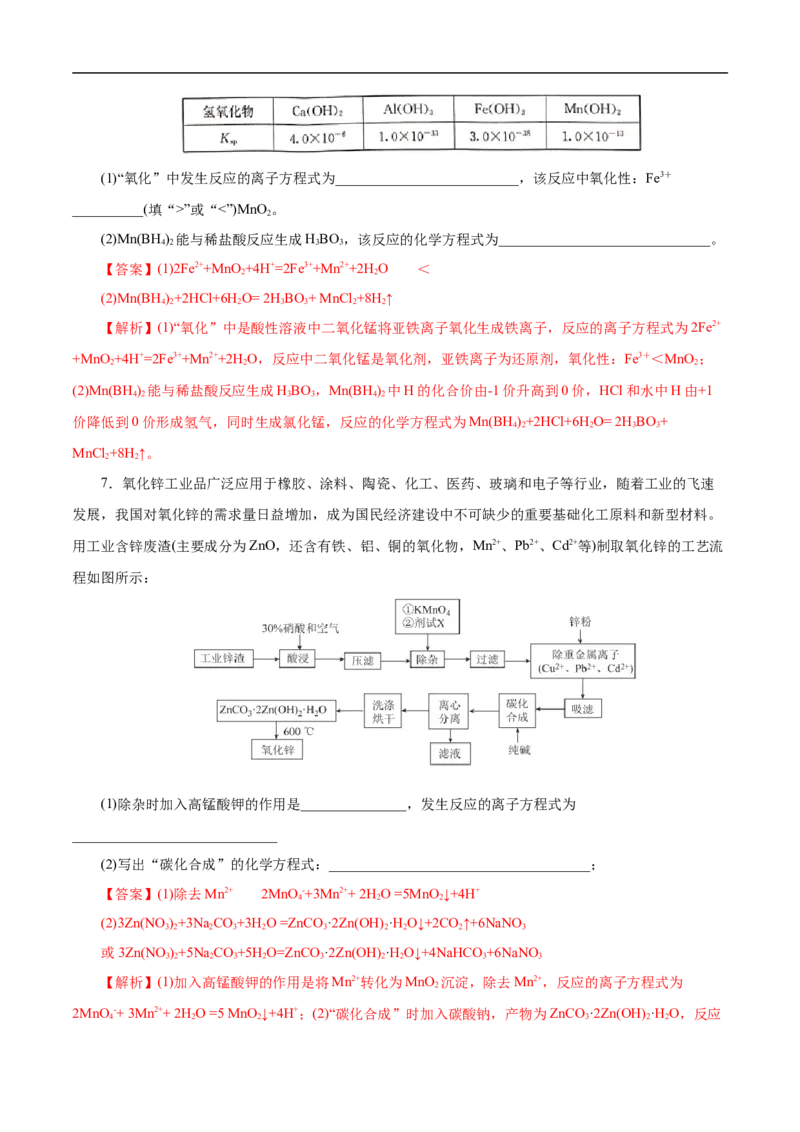
7.氧化锌工业品广泛应用于橡胶、涂料、陶瓷、化工、医药、玻璃和电子等行业,随着工业的飞速
发展,我国对氧化锌的需求量日益增加,成为国民经济建设中不可缺少的重要基础化工原料和新型材料。
用工业含锌废渣(主要成分为ZnO,还含有铁、铝、铜的氧化物,Mn2+、Pb2+、Cd2+等)制取氧化锌的工艺流
程如图所示:
(1)除杂时加入高锰酸钾的作用是_______________,发生反应的离子方程式为
_____________________________
(2)写出“碳化合成”的化学方程式:_____________________________________;
【答案】(1)除去Mn2+ 2MnO -+3Mn2++ 2H O =5MnO↓+4H+
4 2 2
(2)3Zn(NO )+3Na CO+3H O =ZnCO ·2Zn(OH) ·HO↓+2CO↑+6NaNO
3 2 2 3 2 3 2 2 2 3
或3Zn(NO )+5Na CO+5H O=ZnCO ·2Zn(OH) ·HO↓+4NaHCO +6NaNO
3 2 2 3 2 3 2 2 3 3
【解析】(1)加入高锰酸钾的作用是将Mn2+转化为MnO 沉淀,除去Mn2+,反应的离子方程式为
2
2MnO -+ 3Mn2++ 2H O =5 MnO ↓+4H+;(2)“碳化合成”时加入碳酸钠,产物为ZnCO ·2Zn(OH) ·HO,反应
4 2 2 3 2 2的化学方程式为:3Zn(NO )+3Na CO+3H O =ZnCO ·2Zn(OH) ·HO↓+2CO↑+6NaNO 或
3 2 2 3 2 3 2 2 2 3
3Zn(NO )+5Na CO+5H O=ZnCO ·2Zn(OH) ·HO↓+4NaHCO +6NaNO ;若碳酸钠过量,则沉淀后的溶液中
3 2 2 3 2 3 2 2 3 3
有碳酸根离子,检查碳酸根离子的方法是:静置,取上层清液少许于试管中,往试管中继续滴加碳酸钠溶
液,若无沉淀产生,则纯碱过量。
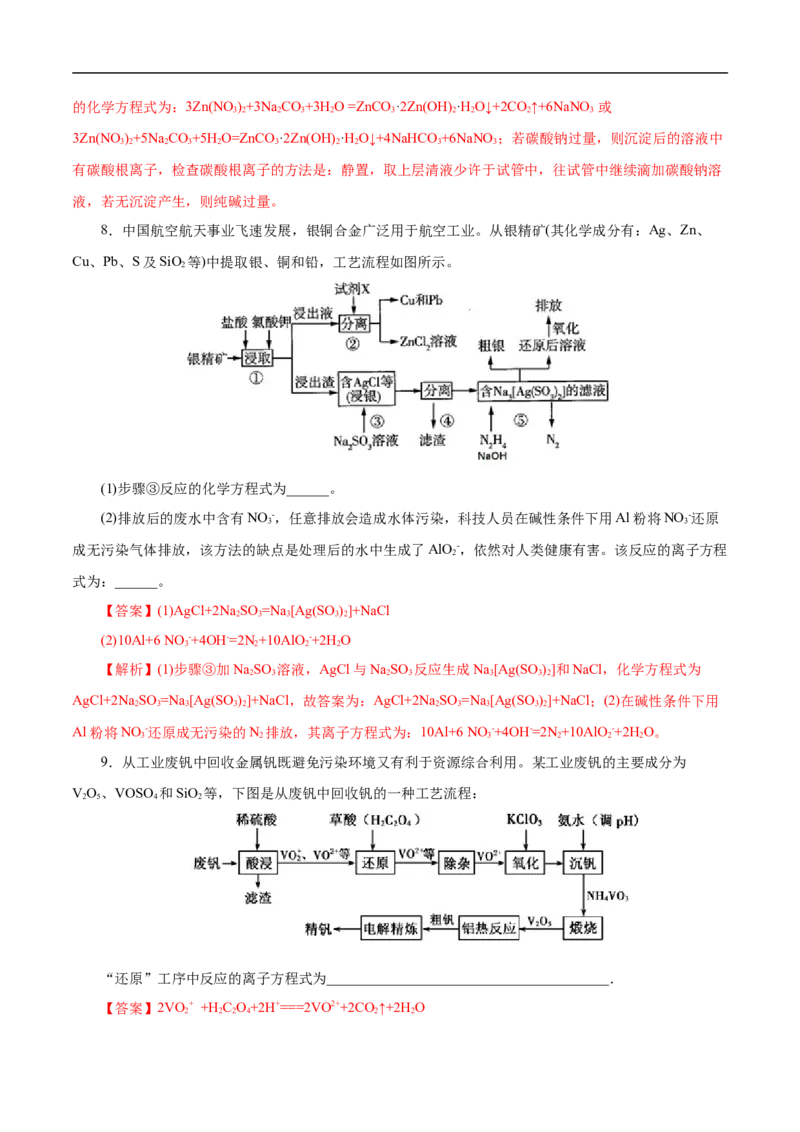
8.中国航空航天事业飞速发展,银铜合金广泛用于航空工业。从银精矿(其化学成分有:Ag、Zn、
Cu、Pb、S及SiO 等)中提取银、铜和铅,工艺流程如图所示。
2
(1)步骤③反应的化学方程式为______。
(2)排放后的废水中含有NO -,任意排放会造成水体污染,科技人员在碱性条件下用Al粉将NO -还原
3 3
成无污染气体排放,该方法的缺点是处理后的水中生成了AlO-,依然对人类健康有害。该反应的离子方程
2
式为:______。
【答案】(1)AgCl+2Na SO =Na [Ag(SO)]+NaCl
2 3 3 3 2
(2)10Al+6 NO -+4OH-=2N +10AlO -+2H O
3 2 2 2
【解析】(1)步骤③加NaSO 溶液,AgCl与NaSO 反应生成Na[Ag(SO)]和NaCl,化学方程式为
2 3 2 3 3 3 2
AgCl+2Na SO =Na [Ag(SO)]+NaCl,故答案为:AgCl+2Na SO =Na [Ag(SO)]+NaCl;(2)在碱性条件下用
2 3 3 3 2 2 3 3 3 2
Al粉将NO -还原成无污染的N 排放,其离子方程式为:10Al+6 NO -+4OH-=2N +10AlO -+2H O。
3 2 3 2 2 2
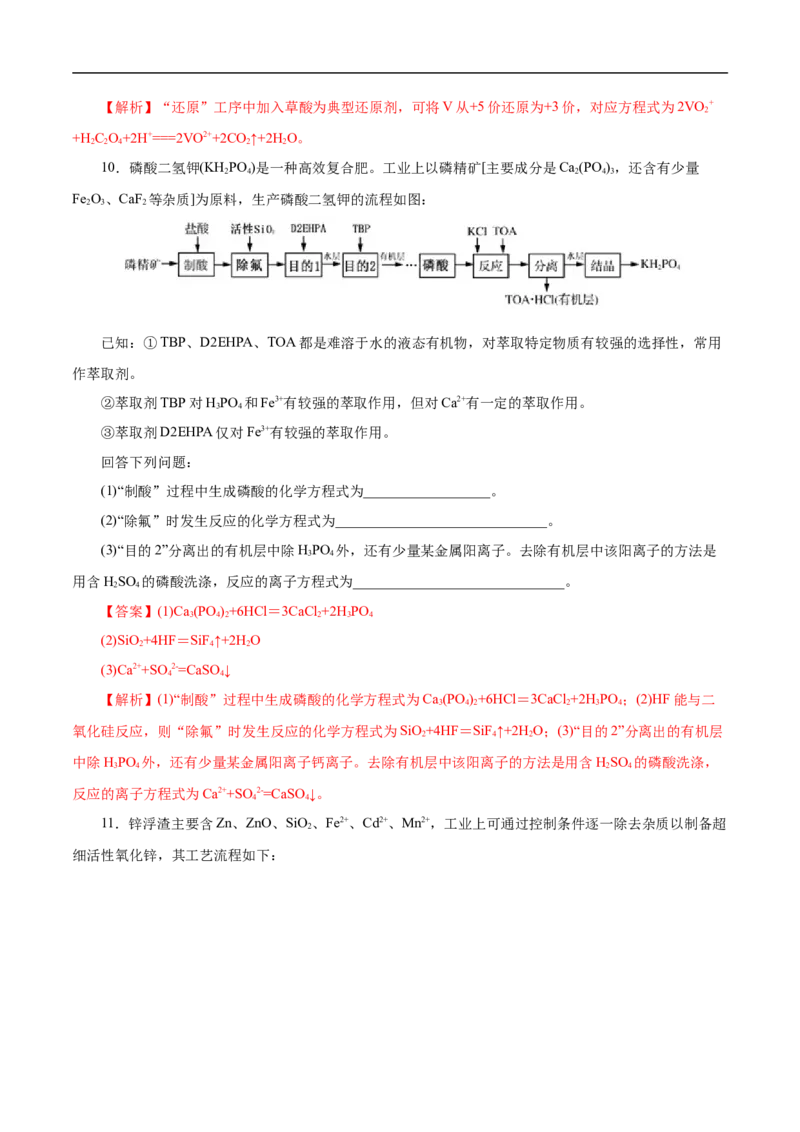
9.从工业废钒中回收金属钒既避免污染环境又有利于资源综合利用。某工业废钒的主要成分为
VO、VOSO 和SiO 等,下图是从废钒中回收钒的一种工艺流程:
2 5 4 2
“还原”工序中反应的离子方程式为________________________________________.
【答案】2VO + +H C O+2H+===2VO2++2CO ↑+2H O
2 2 2 4 2 2【解析】“还原”工序中加入草酸为典型还原剂,可将V从+5价还原为+3价,对应方程式为2VO +
2
+H C O+2H+===2VO2++2CO ↑+2H O。
2 2 4 2 2
10.磷酸二氢钾(KH PO )是一种高效复合肥。工业上以磷精矿[主要成分是Ca (PO ),还含有少量
2 4 2 4 3
Fe O、CaF 等杂质]为原料,生产磷酸二氢钾的流程如图:
2 3 2
已知:①TBP、D2EHPA、TOA都是难溶于水的液态有机物,对萃取特定物质有较强的选择性,常用
作萃取剂。
②萃取剂TBP对HPO 和Fe3+有较强的萃取作用,但对Ca2+有一定的萃取作用。
3 4
③萃取剂D2EHPA仅对Fe3+有较强的萃取作用。
回答下列问题:
(1)“制酸”过程中生成磷酸的化学方程式为__________________。
(2)“除氟”时发生反应的化学方程式为______________________________。
(3)“目的2”分离出的有机层中除HPO 外,还有少量某金属阳离子。去除有机层中该阳离子的方法是
3 4
用含HSO 的磷酸洗涤,反应的离子方程式为______________________________。
2 4
【答案】(1)Ca (PO )+6HCl=3CaCl +2H PO
3 4 2 2 3 4
(2)SiO+4HF=SiF↑+2H O
2 4 2
(3)Ca2++SO2-=CaSO ↓
4 4
【解析】(1)“制酸”过程中生成磷酸的化学方程式为Ca (PO )+6HCl=3CaCl +2H PO ;(2)HF能与二
3 4 2 2 3 4
氧化硅反应,则“除氟”时发生反应的化学方程式为SiO+4HF=SiF↑+2H O;(3)“目的2”分离出的有机层
2 4 2
中除HPO 外,还有少量某金属阳离子钙离子。去除有机层中该阳离子的方法是用含HSO 的磷酸洗涤,
3 4 2 4
反应的离子方程式为Ca2++SO2-=CaSO ↓。
4 4
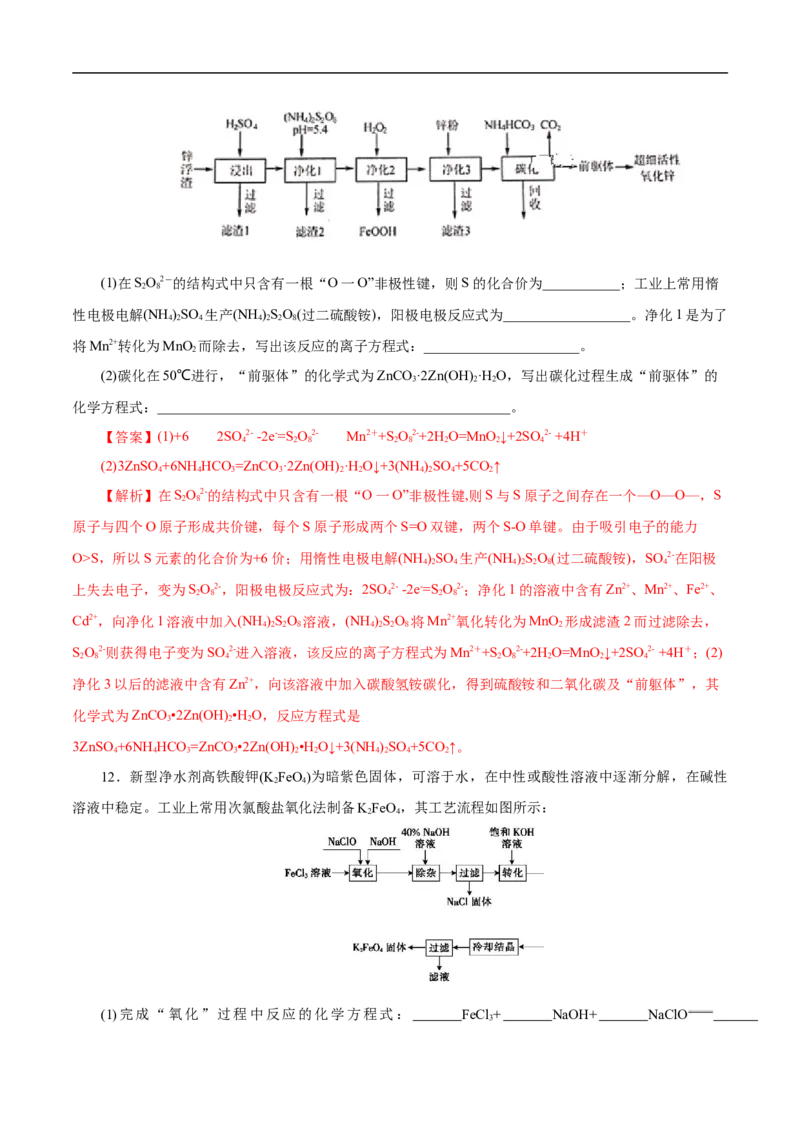
11.锌浮渣主要含Zn、ZnO、SiO、Fe2+、Cd2+、Mn2+,工业上可通过控制条件逐一除去杂质以制备超
2
细活性氧化锌,其工艺流程如下:(1)在SO2-的结构式中只含有一根“O一O”非极性键,则S的化合价为___________;工业上常用惰
2 8
性电极电解(NH )SO 生产(NH )SO(过二硫酸铵),阳极电极反应式为__________________。净化1是为了
4 2 4 4 2 2 8
将Mn2+转化为MnO 而除去,写出该反应的离子方程式:______________________。
2
(2)碳化在50℃进行,“前驱体”的化学式为ZnCO ·2Zn(OH) ·H O,写出碳化过程生成“前驱体”的
3 2 2
化学方程式:__________________________________________________。
【答案】(1)+6 2SO 2- -2e-=S O2- Mn2++S O2-+2H O=MnO ↓+2SO2- +4H+
4 2 8 2 8 2 2 4
(2)3ZnSO +6NHHCO =ZnCO ·2Zn(OH) ·H O↓+3(NH )SO +5CO ↑
4 4 3 3 2 2 4 2 4 2
【解析】在SO2-的结构式中只含有一根“O一O”非极性键,则S与S原子之间存在一个—O—O—,S
2 8
原子与四个O原子形成共价键,每个S原子形成两个S=O双键,两个S-O单键。由于吸引电子的能力
O>S,所以S元素的化合价为+6价;用惰性电极电解(NH )SO 生产(NH )SO(过二硫酸铵),SO 2-在阳极
4 2 4 4 2 2 8 4
上失去电子,变为SO2-,阳极电极反应式为:2SO 2- -2e-=S O2-;净化1的溶液中含有Zn2+、Mn2+、Fe2+、
2 8 4 2 8
Cd2+,向净化1溶液中加入(NH )SO 溶液,(NH )SO 将Mn2+氧化转化为MnO 形成滤渣2而过滤除去,
4 2 2 8 4 2 2 8 2
SO2-则获得电子变为SO 2-进入溶液,该反应的离子方程式为Mn2++S O2-+2H O=MnO ↓+2SO2- +4H+;(2)
2 8 4 2 8 2 2 4
净化3以后的滤液中含有Zn2+,向该溶液中加入碳酸氢铵碳化,得到硫酸铵和二氧化碳及“前躯体”,其
化学式为ZnCO •2Zn(OH)•H O,反应方程式是
3 2 2
3ZnSO+6NHHCO =ZnCO •2Zn(OH)•H O↓+3(NH )SO +5CO ↑。
4 4 3 3 2 2 4 2 4 2
12.新型净水剂高铁酸钾(K FeO)为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性
2 4
溶液中稳定。工业上常用次氯酸盐氧化法制备KFeO,其工艺流程如图所示:
2 4
(1)完成“氧化”过程中反应的化学方程式: FeCl + NaOH+ NaClO
3NaFeO+ + HO。其中氧化剂是 (填化学式)。
2 4 2
(2)“转化”过程中发生反应的化学方程式为 。
【答案】(1)2 10 3 2 9 NaCl 5 NaClO
(2)Na FeO+2KOH=K FeO+2NaOH
2 4 2 4
【解析】(1)Fe的化合价由+3→+6,化合价升高3价,Cl的化合价由+1→-1,化合价降低2价,最小公
倍 数 为 6 , 然 后 根 据 原 子 守 恒 配 平 其 他 即 可 , 即 反 应 的 化 学 方 程 式 为
2FeCl +10NaOH+3NaClO=2Na FeO+9NaCl+5HO,其中NaClO为氧化剂。(2)根据流程,过滤后滤液中含
3 2 4 2
有 NaFeO , 利 用 KFeO 的 溶 解 度 小 于 NaFeO 的 , 因 此 发 生 反 应 的 化 学 方 程 式 为
2 4 2 4 2 4
NaFeO+2KOH=K FeO+2NaOH。
2 4 2 4
13.某学校化学兴趣小组为探索金属回收物的综合利用,专门设计实验用含有铝、铁、铜的合金制取
纯净的氯化铝溶液、绿矾晶体(FeSO ·7H O)和胆矾晶体(CuSO ·5H O),其实验方案如下:
4 2 4 2
(1)在滤液C转化为沉淀Ⅱ的过程中盐酸的用量不易控制,可改为通CO 气体,写出滤液C中通入过量
2
CO 的离子方程式:______________________________________________。
2
写出由沉淀Ⅱ转化为AlCl 溶液的离子方程式:_____________________________。
3
(2)小组成员从资料中获知HO 是一种绿色氧化剂,在滤渣B中加入稀硫酸和HO 来制备胆矾晶体,
2 2 2 2
则该反应的总化学方程式为_______________________________。
【答案】(1)AlO -+CO+2HO=Al(OH) ↓+HCO - Al(OH) +3H+=Al3++3HO
2 2 2 3 3 3 2
(2)Cu+HO+HSO +3HO=CuSO ·5H O(或Cu+HO+HSO =CuSO+2HO)
2 2 2 4 2 4 2 2 2 2 4 4 2
【解析】(1)滤液C中含有偏铝酸钠,通入过量CO 生成氢氧化铝沉淀和碳酸氢钠,反应的离子方程式
2
为AlO-+CO +2H O=Al(OH) ↓+HCO-,沉淀Ⅱ为氢氧化铝,与盐酸反应转化为AlCl 溶液,反应的离子方
2 2 2 3 3 3
程式为Al(OH) +3H+═Al3++3H O;(2)铜与浓硫酸反应生成有毒有污染的二氧化硫气体,若铜先和氧气反应
3 2
生成氧化铜,然后氧化铜会和硫酸反应生成硫酸铜,不会产生污染大气的气体,该过程原料利用率高,所
以途径②最佳,Cu中加入稀硫酸和HO 可以制备胆矾晶体,反应方程式为:
2 2
Cu+H O+H SO +3H O═CuSO•5H O(或Cu+H O+H SO ═CuSO +2H O)。
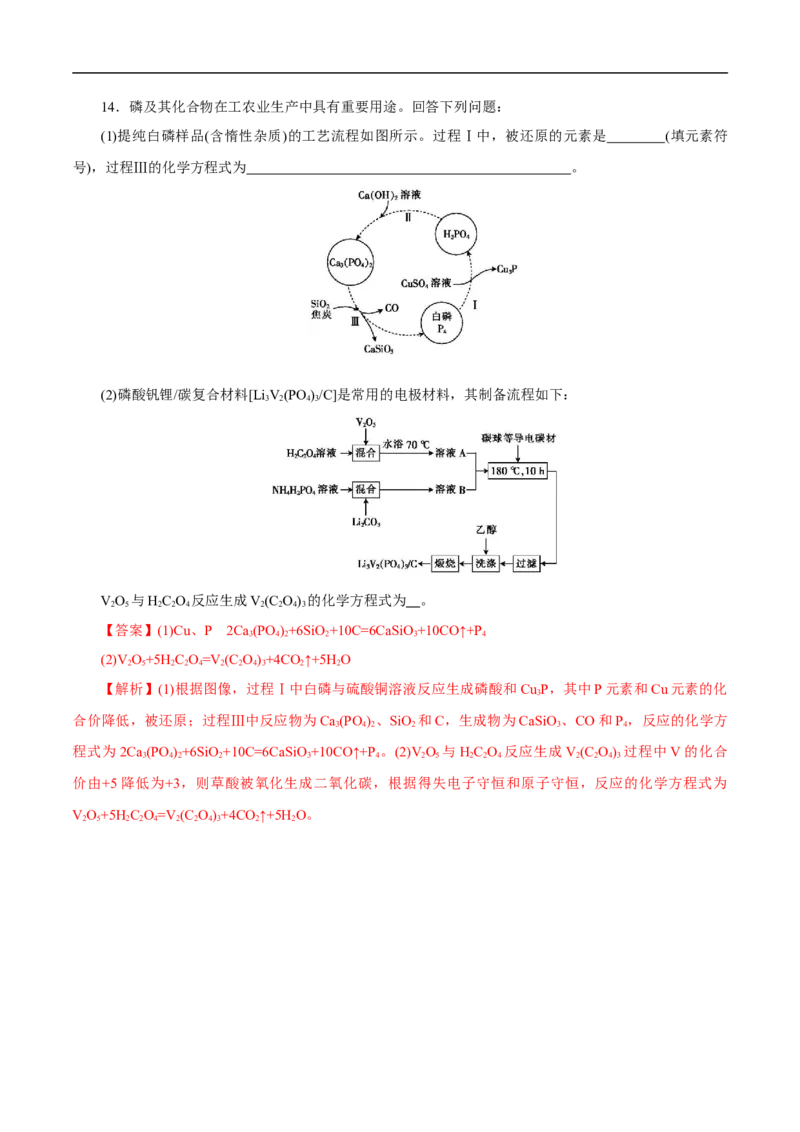
2 2 2 4 2 4 2 2 2 2 4 4 214.磷及其化合物在工农业生产中具有重要用途。回答下列问题:
(1)提纯白磷样品(含惰性杂质)的工艺流程如图所示。过程Ⅰ中,被还原的元素是 (填元素符
号),过程Ⅲ的化学方程式为 。
(2)磷酸钒锂/碳复合材料[Li V(PO )/C]是常用的电极材料,其制备流程如下:
3 2 4 3
VO 与HC O 反应生成V(C O) 的化学方程式为 。
2 5 2 2 4 2 2 4 3
【答案】(1)Cu、P 2Ca (PO )+6SiO +10C=6CaSiO +10CO↑+P
3 4 2 2 3 4
(2)V O+5H C O=V(C O)+4CO ↑+5H O
2 5 2 2 4 2 2 4 3 2 2
【解析】(1)根据图像,过程Ⅰ中白磷与硫酸铜溶液反应生成磷酸和Cu P,其中P元素和Cu元素的化
3
合价降低,被还原;过程Ⅲ中反应物为Ca (PO ) 、SiO 和C,生成物为CaSiO 、CO和P ,反应的化学方
3 4 2 2 3 4
程式为2Ca (PO )+6SiO +10C=6CaSiO +10CO↑+P 。(2)V O 与HC O 反应生成V(C O) 过程中V的化合
3 4 2 2 3 4 2 5 2 2 4 2 2 4 3
价由+5降低为+3,则草酸被氧化生成二氧化碳,根据得失电子守恒和原子守恒,反应的化学方程式为
VO+5H C O=V (C O)+4CO ↑+5H O。
2 5 2 2 4 2 2 4 3 2 2