文档内容
易错专题 20 化学工艺流程题解题策略
聚焦易错点:
一、物质制备型
1.原料处理阶段
(1)常见原料处理的方法:溶解、水(酸或碱)浸、浸出、灼(焙、煅)烧等。
(2)加快反应速率的方法:搅拌、加热、粉碎等。
2.分离提纯阶段
(1)调pH除杂:控制溶液的酸碱性,使其中的某些金属离子形成氢氧化物沉淀。
(2)加热:加快反应速率或促进平衡向某个反应方向移动。
(3)降温:防止某物质在高温时会溶解(或分解)或使化学平衡向着题目要求的方向移动。
(4)水(酸或碱)溶法:除去可溶性(碱性或酸性)杂质。
(5)氧化剂或还原剂法:除去还原性或氧化性杂质。
(6)分离方法:过滤、蒸发(冷却)结晶、萃取和分液、蒸馏(或分馏)等。
3.获得产品阶段
(1)洗涤:(冰水、热水)洗去晶体表面的杂质离子,并减少晶体在洗涤过程中溶解损耗。
(2)根据物质溶解度差异选择正确的方法,如蒸发浓缩、冷却结晶或蒸发结晶、趁热过滤。
二、物质分离提纯型
物质分离提纯型工艺流程题主要是针对混合物的除杂、分离和提纯。解题时找出要得到的主要物质是什么,
混有的杂质有哪些,分析加入某一试剂后,能与什么物质发生反应,生成了什么物质,要用什么样的方法才能
将杂质除去,将工艺流程转化为物质的转化流程,明确各步所加试剂或相关操作的目的。工艺流程题中文字
表述题答题方法如下:
1.“加过量试剂”:常考虑反应完全或增大转化率、产率等。
2.“控制pH”:常考虑防水解、促进生成沉淀或除去杂质等。
3.“能否加其他物质”:常考虑会不会引入杂质或是否影响产品的纯度。
4.“控制较低温度”:常考虑物质的挥发、物质的不稳定性和物质的转化等。
5.“判断沉淀是否洗净”:常取少量最后一次洗涤液于试管中,向其中滴加某试剂,以检验其中的某种离子。
6.“检验某物质的设计方案”:通常取少量某物质于试管中,加水溶解,再加入另一试剂产生某现象,然后得
出结论。
7.“用某些有机试剂清洗”:(1)降低物质溶解度有利于产品析出;(2)洗涤沉淀可减少损耗和提高利用率等。
8.“在空气中或在其他气体中”:主要考虑O 、HO、CO 或其他气体是否参与反应或达到防氧化、防水解、
2 2 2防潮解等目的。
考点精练
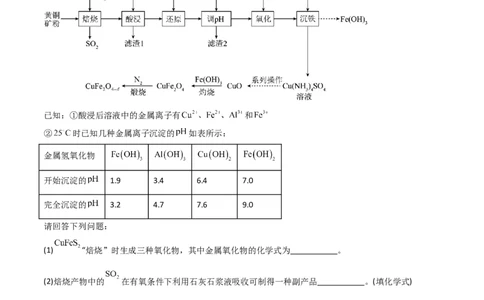
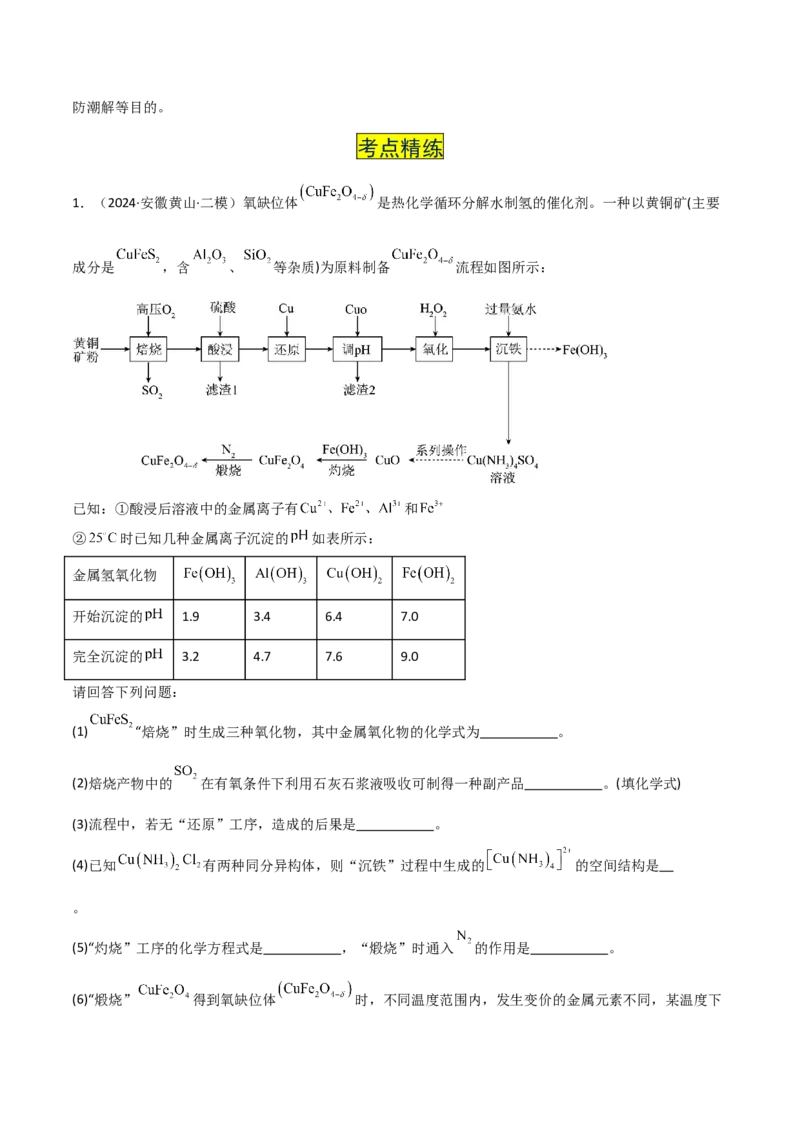
1.(2024·安徽黄山·二模)氧缺位体 是热化学循环分解水制氢的催化剂。一种以黄铜矿(主要
成分是 ,含 、 等杂质)为原料制备 流程如图所示:
已知:①酸浸后溶液中的金属离子有 和
② 时已知几种金属离子沉淀的 如表所示:
金属氢氧化物
开始沉淀的 1.9 3.4 6.4 7.0
完全沉淀的 3.2 4.7 7.6 9.0
请回答下列问题:
(1) “焙烧”时生成三种氧化物,其中金属氧化物的化学式为 。
(2)焙烧产物中的 在有氧条件下利用石灰石浆液吸收可制得一种副产品 。(填化学式)
(3)流程中,若无“还原”工序,造成的后果是 。
(4)已知 有两种同分异构体,则“沉铁”过程中生成的 的空间结构是
。
(5)“灼烧”工序的化学方程式是 ,“煅烧”时通入 的作用是 。
(6)“煅烧” 得到氧缺位体 时,不同温度范围内,发生变价的金属元素不同,某温度下制得的氧缺位体质量为原质量的 ,则 。
(7)氧缺位体催化分解水制氢可分为两步:
第一步: (完成方程式);
第二步: 。
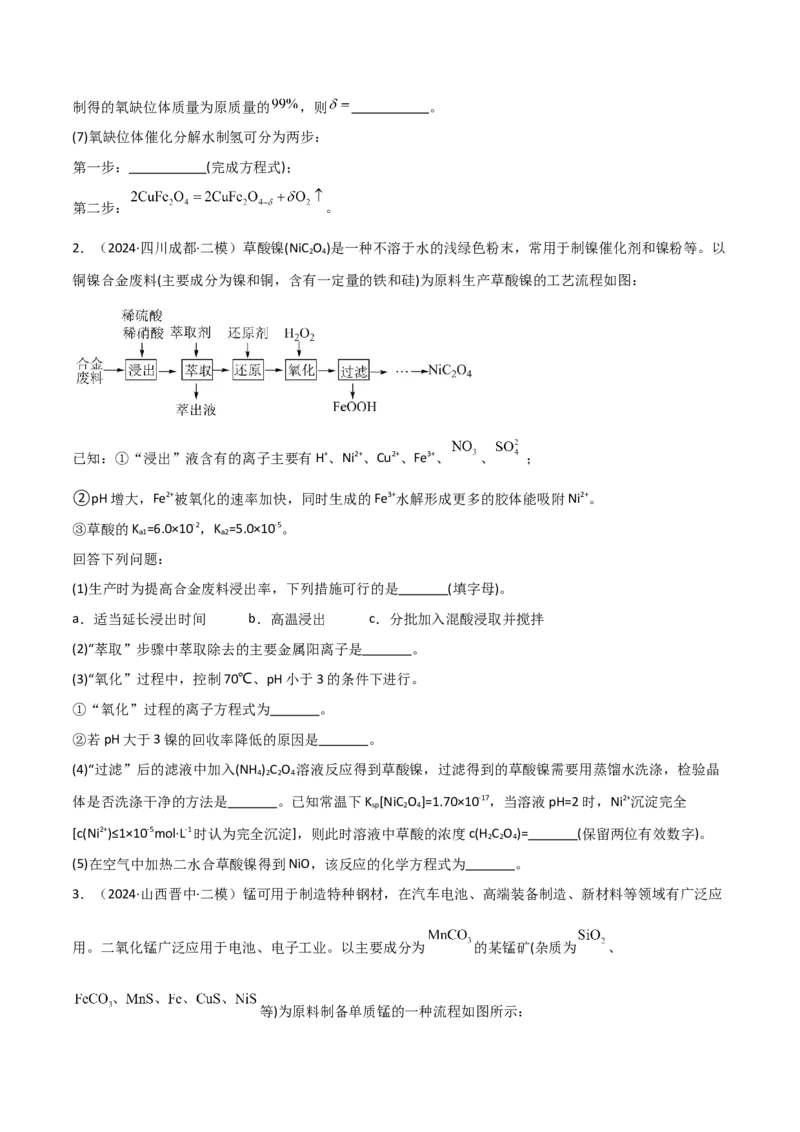
2.(2024·四川成都·二模)草酸镍(NiC O )是一种不溶于水的浅绿色粉末,常用于制镍催化剂和镍粉等。以
2 4
铜镍合金废料(主要成分为镍和铜,含有一定量的铁和硅)为原料生产草酸镍的工艺流程如图:
已知:①“浸出”液含有的离子主要有H+、Ni2+、Cu2+、Fe3+、 、 ;
②pH增大,Fe2+被氧化的速率加快,同时生成的Fe3+水解形成更多的胶体能吸附Ni2+。
③草酸的K =6.0×10-2,K =5.0×10-5。
a1 a2
回答下列问题:
(1)生产时为提高合金废料浸出率,下列措施可行的是 (填字母)。
a.适当延长浸出时间 b.高温浸出 c.分批加入混酸浸取并搅拌
(2)“萃取”步骤中萃取除去的主要金属阳离子是 。
(3)“氧化”过程中,控制70℃、pH小于3的条件下进行。
①“氧化”过程的离子方程式为 。
②若pH大于3镍的回收率降低的原因是 。
(4)“过滤”后的滤液中加入(NH ) C O 溶液反应得到草酸镍,过滤得到的草酸镍需要用蒸馏水洗涤,检验晶
4 2 2 4
体是否洗涤干净的方法是 。已知常温下K [NiC O ]=1.70×10-17,当溶液pH=2时,Ni2+沉淀完全
sp 2 4
[c(Ni2+)≤1×10-5mol·L-1时认为完全沉淀],则此时溶液中草酸的浓度c(H C O )= (保留两位有效数字)。
2 2 4
(5)在空气中加热二水合草酸镍得到NiO,该反应的化学方程式为 。
3.(2024·山西晋中·二模)锰可用于制造特种钢材,在汽车电池、高端装备制造、新材料等领域有广泛应
用。二氧化锰广泛应用于电池、电子工业。以主要成分为 的某锰矿(杂质为 、
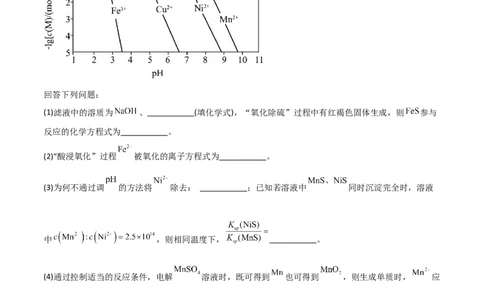
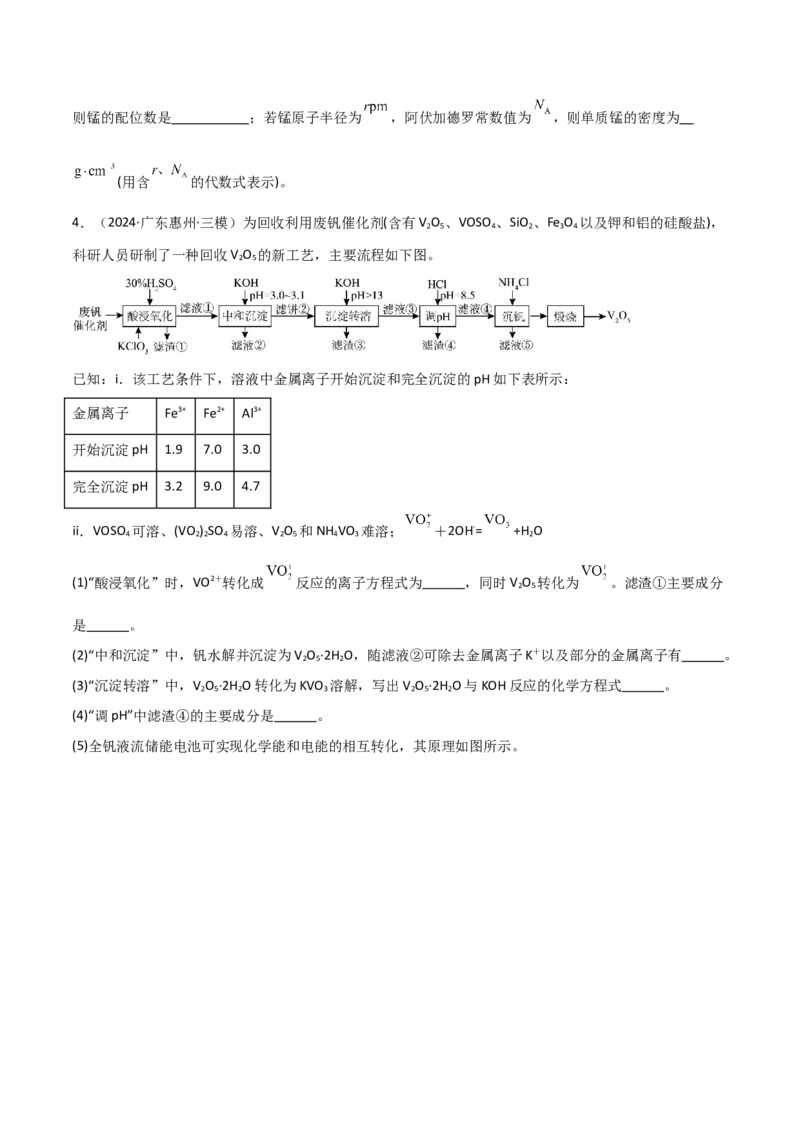
等)为原料制备单质锰的一种流程如图所示:已知:金属离子浓度的负对数 与溶液 的关系如图所示:
回答下列问题:
(1)滤液中的溶质为 、 (填化学式),“氧化除硫”过程中有红褐色固体生成,则 参与
反应的化学方程式为 。
(2)“酸浸氧化”过程 被氧化的离子方程式为 。
(3)为何不通过调 的方法将 除去: ;已知若溶液中 同时沉淀完全时,溶液
中 ,则相同温度下, 。
(4)通过控制适当的反应条件,电解 溶液时,既可得到 也可得到 ,则生成单质时, 应
在 (填“阳极”或“阴极”)上放电;写出生成 时的电极反应式: 。
(5)已知单质锰的立方晶胞结构如图所示:则锰的配位数是 ;若锰原子半径为 ,阿伏加德罗常数值为 ,则单质锰的密度为
(用含 的代数式表示)。
4.(2024·广东惠州·三模)为回收利用废钒催化剂(含有V O 、VOSO 、SiO 、Fe O 以及钾和铝的硅酸盐),
2 5 4 2 3 4
科研人员研制了一种回收V O 的新工艺,主要流程如下图。
2 5
已知:i.该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Fe3+ Fe2+ Al3+
开始沉淀pH 1.9 7.0 3.0
完全沉淀pH 3.2 9.0 4.7
ii.VOSO 可溶、(VO ) SO 易溶、V O 和NH VO 难溶; +2OH-= +H O
4 2 2 4 2 5 4 3 2
(1)“酸浸氧化”时,VO2+转化成 反应的离子方程式为 ,同时V O 转化为 。滤渣①主要成分
2 5
是 。
(2)“中和沉淀”中,钒水解并沉淀为V O ·2H O,随滤液②可除去金属离子K+以及部分的金属离子有 。
2 5 2
(3)“沉淀转溶”中,V O ·2H O转化为KVO 溶解,写出V O ·2H O与KOH反应的化学方程式 。
2 5 2 3 2 5 2
(4)“调pH”中滤渣④的主要成分是 。
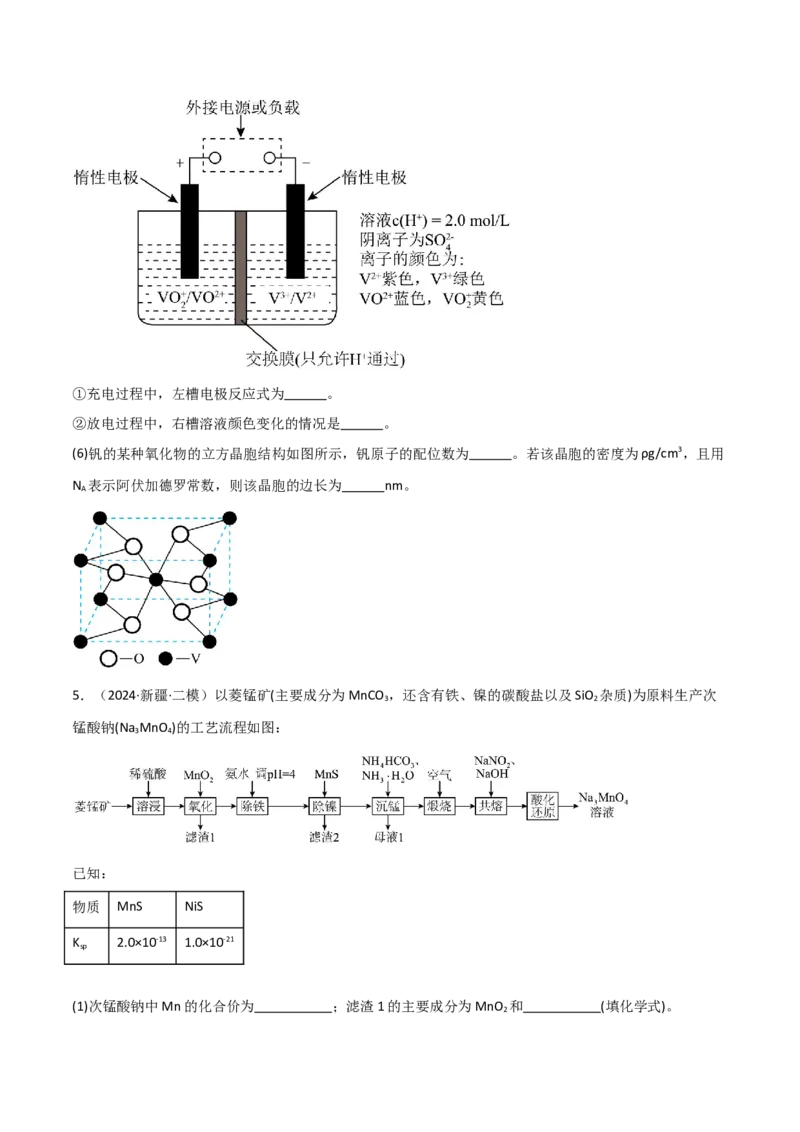
(5)全钒液流储能电池可实现化学能和电能的相互转化,其原理如图所示。①充电过程中,左槽电极反应式为 。
②放电过程中,右槽溶液颜色变化的情况是 。
(6)钒的某种氧化物的立方晶胞结构如图所示,钒原子的配位数为 。若该晶胞的密度为ρg/cm3,且用
N 表示阿伏加德罗常数,则该晶胞的边长为 nm。
A
5.(2024·新疆·二模)以菱锰矿(主要成分为MnCO ,还含有铁、镍的碳酸盐以及SiO 杂质)为原料生产次
3 2
锰酸钠(Na MnO )的工艺流程如图:
3 4
已知:
物质 MnS NiS
K 2.0×10-13 1.0×10-21
sp
(1)次锰酸钠中Mn的化合价为 ;滤渣1的主要成分为MnO 和 (填化学式)。
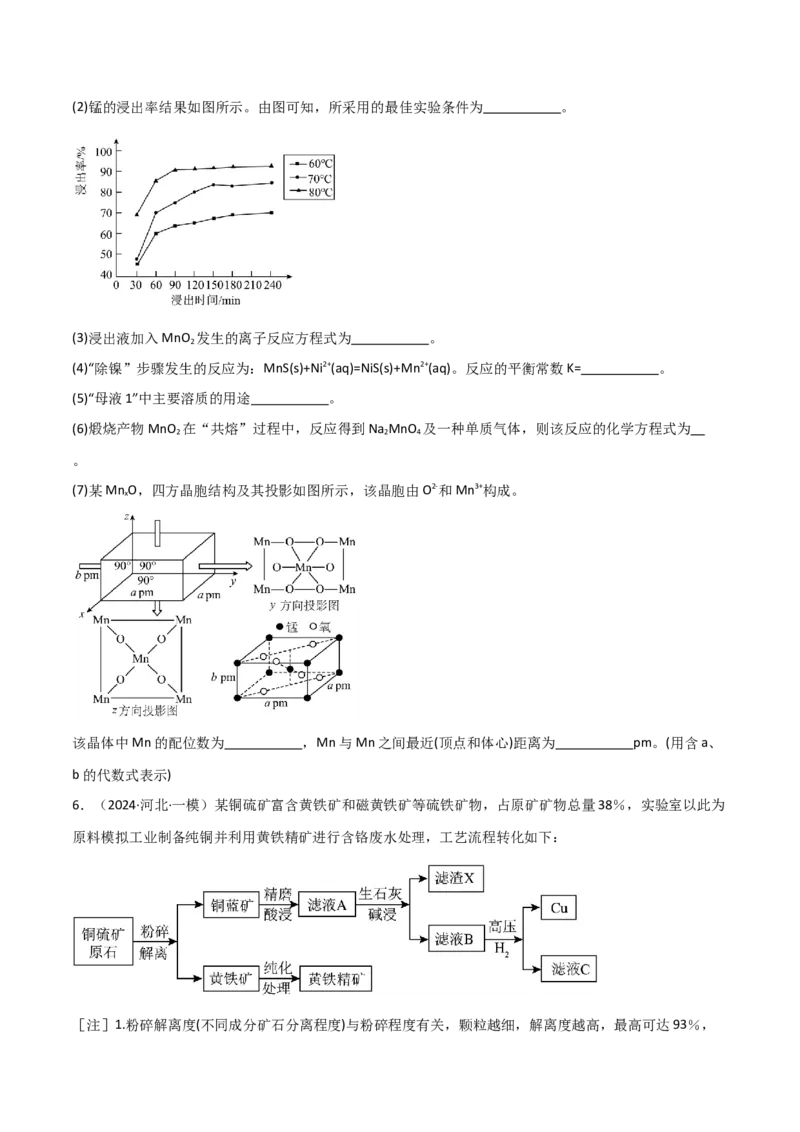
2(2)锰的浸出率结果如图所示。由图可知,所采用的最佳实验条件为 。
(3)浸出液加入MnO 发生的离子反应方程式为 。
2
(4)“除镍”步骤发生的反应为:MnS(s)+Ni2+(aq)=NiS(s)+Mn2+(aq)。反应的平衡常数K= 。
(5)“母液1”中主要溶质的用途 。
(6)煅烧产物MnO 在“共熔”过程中,反应得到Na MnO 及一种单质气体,则该反应的化学方程式为
2 2 4
。
(7)某MnO,四方晶胞结构及其投影如图所示,该晶胞由O2-和Mn3+构成。
x
该晶体中Mn的配位数为 ,Mn与Mn之间最近(顶点和体心)距离为 pm。(用含a、
b的代数式表示)
6.(2024·河北·一模)某铜硫矿富含黄铁矿和磁黄铁矿等硫铁矿物,占原矿矿物总量38%,实验室以此为
原料模拟工业制备纯铜并利用黄铁精矿进行含铬废水处理,工艺流程转化如下:
[注]1.粉碎解离度(不同成分矿石分离程度)与粉碎程度有关,颗粒越细,解离度越高,最高可达93%,但颗粒越细对设备要求越高。
2.铜蓝矿的主要成分为CuS,黄铁矿的主要成分为 。
3.可能用到的数据如下:
开始沉淀pH 1.9 4.2 6.2
沉淀完全pH 3.2 6.7 8.2
(1)基态铜原子的空间运动状态为 种。
(2)精磨酸浸过程中,精磨的作用是 ;酸浸一般选用硫酸溶液在纯氧环境中进行,酸浸的化学方程式
为 。
(3)已知增大氧气的浓度可以提高 的浸取率,请结合化学用语解释其原因 。
(4)生石灰碱浸时调节pH的范围为 。
(5)滤渣X的主要成分是 。
(6)向滤液B中通入高压 ,可成功制得单质铜的原因是 。
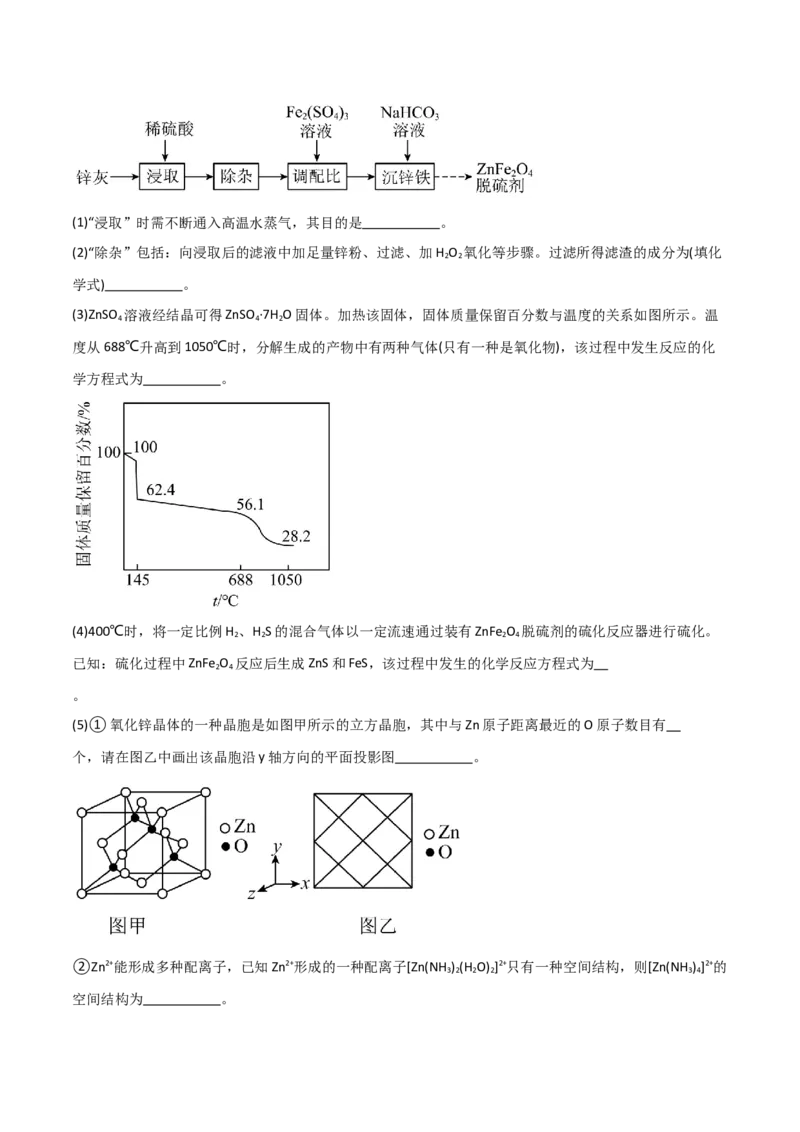
(7)黄铁精矿处理含铬废水的机理如图所示:
在溶液反应中,黄铁精矿会部分溶解与( )发生氧化还原反应,请结合信息写出此过程的离子反应方
程式: 。
7.(2024·福建龙岩·二模)以锌灰(含ZnO及少量PbO、CuO、Fe O 、SiO )和Fe (SO ) 为原料制备的ZnFe O
2 3 2 2 4 3 2 4
脱硫剂,可用于脱除煤气中的H S。脱硫剂的制备过程可表示为
2(1)“浸取”时需不断通入高温水蒸气,其目的是 。
(2)“除杂”包括:向浸取后的滤液中加足量锌粉、过滤、加H O 氧化等步骤。过滤所得滤渣的成分为(填化
2 2
学式) 。
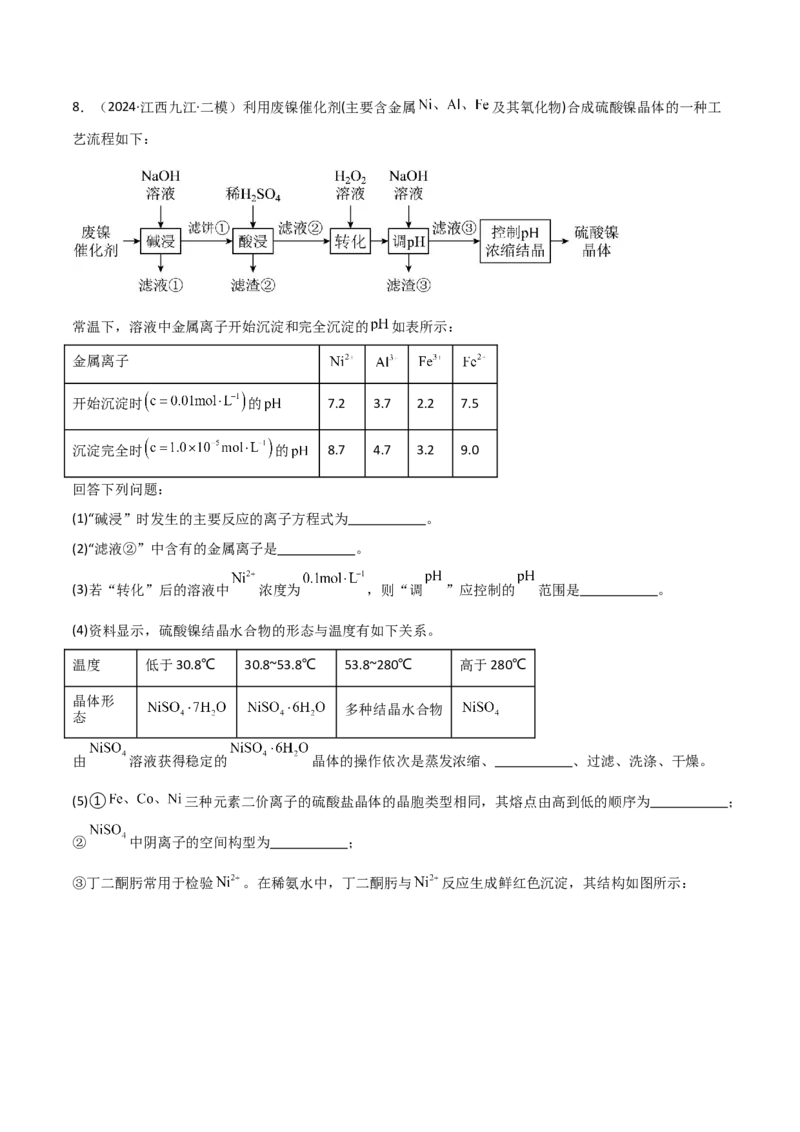
(3)ZnSO 溶液经结晶可得ZnSO ·7H O固体。加热该固体,固体质量保留百分数与温度的关系如图所示。温
4 4 2
度从688℃升高到1050℃时,分解生成的产物中有两种气体(只有一种是氧化物),该过程中发生反应的化
学方程式为 。
(4)400℃时,将一定比例H 、H S的混合气体以一定流速通过装有ZnFe O 脱硫剂的硫化反应器进行硫化。
2 2 2 4
已知:硫化过程中ZnFe O 反应后生成ZnS和FeS,该过程中发生的化学反应方程式为
2 4
。
(5)①氧化锌晶体的一种晶胞是如图甲所示的立方晶胞,其中与Zn原子距离最近的O原子数目有
个,请在图乙中画出该晶胞沿y轴方向的平面投影图 。
②Zn2+能形成多种配离子,已知Zn2+形成的一种配离子[Zn(NH ) (H O) ]2+只有一种空间结构,则[Zn(NH ) ]2+的
3 2 2 2 3 4
空间结构为 。8.(2024·江西九江·二模)利用废镍催化剂(主要含金属 及其氧化物)合成硫酸镍晶体的一种工
艺流程如下:
常温下,溶液中金属离子开始沉淀和完全沉淀的 如表所示:
金属离子
开始沉淀时 的 7.2 3.7 2.2 7.5
沉淀完全时 的 8.7 4.7 3.2 9.0
回答下列问题:
(1)“碱浸”时发生的主要反应的离子方程式为 。
(2)“滤液②”中含有的金属离子是 。
(3)若“转化”后的溶液中 浓度为 ,则“调 ”应控制的 范围是 。
(4)资料显示,硫酸镍结晶水合物的形态与温度有如下关系。
温度 低于30.8℃ 30.8~53.8℃ 53.8~280℃ 高于280℃
晶体形
多种结晶水合物
态
由 溶液获得稳定的 晶体的操作依次是蒸发浓缩、 、过滤、洗涤、干燥。
(5)① 三种元素二价离子的硫酸盐晶体的晶胞类型相同,其熔点由高到低的顺序为 ;
② 中阴离子的空间构型为 ;
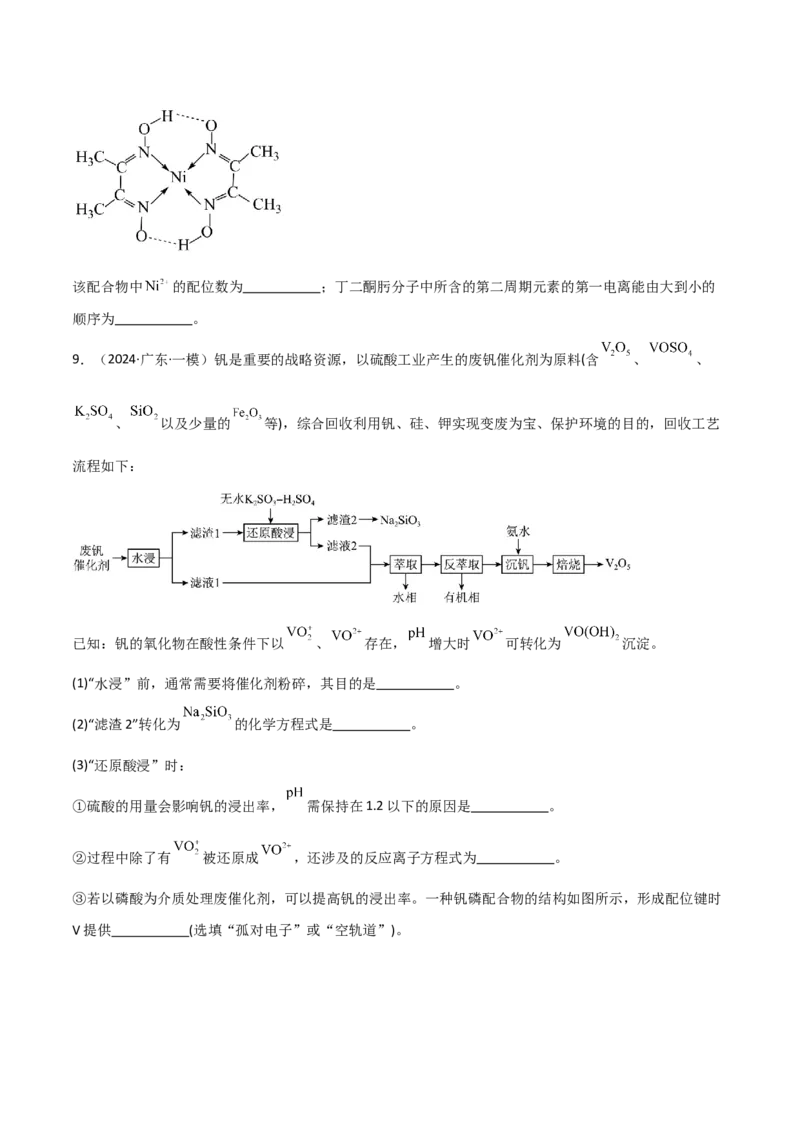
③丁二酮肟常用于检验 。在稀氨水中,丁二酮肟与 反应生成鲜红色沉淀,其结构如图所示:该配合物中 的配位数为 ;丁二酮肟分子中所含的第二周期元素的第一电离能由大到小的
顺序为 。
9.(2024·广东·一模)钒是重要的战略资源,以硫酸工业产生的废钒催化剂为原料(含 、 、
、 以及少量的 等),综合回收利用钒、硅、钾实现变废为宝、保护环境的目的,回收工艺
流程如下:
已知:钒的氧化物在酸性条件下以 、 存在, 增大时 可转化为 沉淀。
(1)“水浸”前,通常需要将催化剂粉碎,其目的是 。
(2)“滤渣2”转化为 的化学方程式是 。
(3)“还原酸浸”时:
①硫酸的用量会影响钒的浸出率, 需保持在1.2以下的原因是 。
②过程中除了有 被还原成 ,还涉及的反应离子方程式为 。
③若以磷酸为介质处理废催化剂,可以提高钒的浸出率。一种钒磷配合物的结构如图所示,形成配位键时
V提供 (选填“孤对电子”或“空轨道”)。(4)“萃取”时选择有机萃取剂,原理是: (有机层) (有机层),“反萃取”应选
择在 环境中进行(选填“酸性”、“中性”或“碱性”)。
(5)加氨水生成 沉淀,若经焙烧得到 产品,则消耗空气中 。
(6)近年来,研究人员发现含钒的锑化物在超导方面表现出潜在的应用前景。某含钒的锑化物晶胞如图1所
示,晶体中包含由V和 组成的二维平面如图2。
该含钒的锑化物化学式为 ,钒原子周围紧邻的锑原子数为 。
10.(2024·黑龙江哈尔滨·二模)钽(Ta)和铌(Nb)为高新技术产业的关键元素,其单质的性质相似。
一种以花岗伟晶岩型铌钽矿(主要成分为 、 、 和少量的FeO、CaO、MgO等)为原料制
取钽和铌的流程如图一:“浸取”后的浸出液中含有 、 两种二元强酸。
已知:①MIBK为甲基异丁基酮:
② , , 。
(1)加快“浸取”速率可采取的措施是 。
(2)“浸取”时得到的“浸渣”主要成分为 (填化学式),“浸取”时还会产生“废气”,“废气”
中除了挥发出的HF还可能有 (填化学式)。 与氢氟酸反应的离子方程式为 。
(3)“萃取”时,若萃取剂MIBK的量一定, (填“一次萃取”或“少量多次萃取”)的萃取效率更高。
(4)用金属钠还原 制取金属铌的化学方程式为 。
(5)钽形成的晶体TaAs在室温下拥有超高的空穴迁移率和较低的电子迁移率。TaAs的晶胞结构如图二所示。
诗写出As的配位数: 。晶体的密度为 (列出计算式,阿伏伽德罗常数的值为 )。
11.(2024·宁夏银川·一模)金属镓被称为“电子工业脊梁”,与铝同族,性质与铝相似。氮化镓是 5G技
术中广泛应用的新型半导体材料。利用粉煤灰(主要成分为Ga O 、Al O 、SiO ,还有少量Fe O 等杂质)制备
2 3 2 3 2 2 3
镓和氮化镓的流程如图:
常温下,相关元素可溶性组分的物质的量浓度的对数与pH的关系如图所示,当溶液中可溶性组分浓度
c≤10-5 mol·L-1时,可认为已除尽。
回答下列问题:(1)“焙烧”过程中Al O 变为NaAlO ,则Ga O 与纯碱反应的化学方程式为 。
2 3 2 2 3
(2)“碱浸”后滤渣的主要成分为 (写化学式)。用惰性电极电解含[Ga(OH) ]-的溶液可得到金属
4
Ga,阴极的电极反应式为 。
(3)常温下,反应[Ga(OH) ]-(aq) Ga(OH) (s)+OH-(aq)的平衡常数K= 。
4 3
(4)用石墨为电极电解熔融Ga O 得到Ga单质,电极材料需要定期补充的是 极(填“阴”或
2 3
“阳”)。
(5)高纯AlAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一种
氧化物,可阻止H O 刻蚀液与下层GaAs(砷化镓)反应。
2 2
①该氧化物为 。
②已知:Ga和Al同族,As和N同族。在H O 与上层GaAs的反应中,As元素的化合价变为+5价,则该反
2 2
应的氧化剂与还原剂物质的量之比为 。
(6)利用CVD(化学气相沉积)技术,将热分解得到的Ga O 与NH 在高温下反应可制得GaN,同时生成另一种
2 3 3
产物,该反应化学方程式为 。
12.(2024·河北·一模)天然锆英砂(主要成分为 )常含有 等氧化物杂质。工业上
以锆英砂为原科制备 的一种工艺流程如图所示。
已知:i.有机溶剂 (三辛胺与壬醇的混合溶液)与水互不相溶;ii.“萃取”过程中铁元素由 转化成有机配合物进入有机相。
(1)“碱熔”时,锆英砂转化为 ,该反应的化学方程式为 。
(2)“水浸”时,所得“滤液”中溶质的主要成分除 外,还有 (填化学式)。
(3)“酸浸”后,锆元素以 的形式存在于溶液中,此过程中 发生反应的离子方程式为
。
(4)“除铜”时,若测得剩余滤液中 ,通过计算判断溶液中 是否除尽 已知:
常温下, ,溶液中离子浓度低于 即可认为该离子被除尽)。
(5)“有机溶剂 ”中的壬醇 几乎与水互不相溶,解释其原因为 。
(6)已知氯氧化锆 的溶解度、铁的萃取率与盐酸浓度的关系如下图所示。
在“萃取”过程中,应选用盐酸的最适宜浓度为_______(填选项字母)。
A. B. C. D.
(7)“煅烧”时,需要在 条件下发生反应,所得两种气体的体积之比 。
13.(2024·山东·一模)以某种铁钴矿(主要成分为 ,还含有少量 等杂质)为原料制取
和黄钠铁矾的工艺流程如下图所示:回答下列问题:
(1)滤渣3的主要成分为 ;确定“滤液1”中的 已被完全氧化的方法是 。
(2)向“溶液A”中加入适量的 溶液,生成颗粒较大的黄钠铁矾[ ]沉淀的同时还
生成一种气体,这种气体的化学式是 。
(3)向“滤液3”中按物质的量之比为 加入 和 ,若“滤渣4”的成分为 ,总反应的
离子方程式是 。经检测,“滤渣4”是由 和 形成的混合物。隔绝空气灼烧
时, 发生反应的化学方程式是 ;如果控制温度不当, 会生成 杂质,
反应的化学方程式是 。
(4)向“滤液1”中加入的“ 溶液”须控制用量,请解释原因 。
14.(2024·四川南充·一模)锰废渣的硫酸浸出液含有大量 、 、 以及少量的 、 、
、 。通过沉淀-萃取法可以回收其中的锰、钴、镍,流程如图所示。已知:萃取剂a和b均为有机物,可用通式 表示,萃取金属离子时,发生反应:
( 代表被萃取的金属)。
(1) 的作用是 。
(2)该流程中涉及的实验操作有___________(填字母标号)。
A.过滤 B.蒸发结晶 C.分液 D.蒸馏
(3)加入 调 的目的是 。
(4)已知: , ,向除铁后的溶液中加入 ,当溶液中
时, 。(保留1位有效数字)
(5)写出反萃取出 的离子方程式 。
(6) 、 利用萃取剂b进行分离,二者萃取率随无机相 变化如图所示。无机相的 控制在
左右为宜。
(7)回收液中 浓度的测定:取 回收液,滴入几滴紫脲酸胺指示剂(遇 显橙黄色),用浓度为 的 溶液进行滴定( ),达到滴定终点时消耗 溶
液的体积 。 物质的量浓度为 。
15.(2023·山西太原·二模)MnCO 可用作电器元件材料,也可作为瓷釉、颜料的制作原料。工业上用酸
3
性含锰废水(主要含Mn2+、Cl-、H+、Fe2+、Cu2+)制备MnCO :
3
已知:几种金属离子沉淀的pH如表。
金属离子 Fe2+ Fe3+ Cu2+ Mn2+
开始沉淀的pH 7.5 3.2 5.2 8.8
完全沉淀的pH 9.7 3.7 6.4 10.4
回答下列问题:
(1)①中加入过量MnO 的作用是 。
2
(2)过程③中调pH的目的是 。
(3)过程④中有CO 生成,则生成MnCO 的离子方程是 。
2 3
(4)过程④中得到的副产品的化学式是 。
(5)MnCO 在空气中加热易转化为不同价态的锰的氧化物,其固体残留率随温度的变化如图所示。则300℃
3
时,剩余固体中n(Mn):n(O)为 ;图中点D对应固体的成分为 (填化学式)。
(6)NF 与NH 的立体构型相同,两者中心原子的轨道杂化类型均为 ,但NF 不易与Cu2+形成配离子,
3 3 3
其原因 。
(7)一种Hg-Ba-Cu-O高温超导材料的晶胞(长方体)如图所示。已知该晶胞中两个 Ba2+的间距为 cpm,则距离 Ba2+最近的 Hg+数目为 个,二者的最短距离为
pm。(列出计算式即可)。
参考答案
1.(1)CuO、Fe O
3 4
(2)CaSO
4
(3)还原工序是将Fe3+还原为Fe2+,若没有还原工序,会使Fe3+发生沉淀
(4)平面正方形
(5) CuO+2Fe(OH) CuFe O +3H O N 在煅烧时做保护气
3 2 4 2 2
(6)0.15
(7)
【分析】氧气具有氧化性,已知酸浸后的溶液中金属离子有Cu2+,Fe2+,Al3+和Fe3+,CuFeS 焙烧生成三种氧
2
化物,结合质量守恒可知,三种氧化物为SO 、CuO、Fe O ,加入硫酸金属氧化物转化为相应的硫酸盐,
2 3 4
滤渣1为SiO ,加入Cu还原Fe3+为Fe2+,加入CuO调节pH使Al3+沉淀,,而Cu2+和Fe2+不沉淀,滤渣2中有
2
Al(OH) 、CuO、Cu,加H O 将Fe2+氧化为Fe3+离子,加入过量的氨水反应生成Cu(NH ) SO ,Fe3+生成Fe(OH)
3 2 2 3 4 4 3
沉淀,Cu(NH ) SO 经过系列操作生成CuO,灼烧CuO和Fe(OH) 生成 CuFe O ,在N 做保护气下煅烧生成
3 4 4 3 2 4 2
。
【详解】(1)已知酸浸后的溶液中金属离子有Cu2+,Fe2+,Al3+和Fe3+,CuFeS 焙烧生成三种氧化物,结合
2
质量守恒可知,三种氧化物为SO 、CuO、Fe O ,其中金属氧化物的化学式为CuO、Fe O ;
2 3 4 3 4
(2)焙烧产物中的 在有氧条件下利用石灰石浆液Ca(OH) 吸收可制得一种副产品是CaSO ;
2 4
(3)加入Cu还原Fe3+为Fe2+,若没有还原工序,调节pH值时会使Fe3+发生沉淀;(4)已知 有两种同分异构体,则可知其结构不是四面体结构,而是平面四边形结构,故
的空间构型为平面正方形;
(5)灼烧CuO和Fe(OH) 生成 CuFe O ,反应的方程式为CuO+2Fe(OH) CuFe O +3H O;N 做保护气,
3 2 4 3 2 4 2 2
防止生成物被氧化;
(6)“煅烧” 得到氧缺位体 ,质量减少的是氧气质量,
,得出 =0.15
(7)制取氢气的总反应为:2 H O=2 H ↑+ O ↑,结合第二步反应 ,可
2 2 2
知第一步反应为 。
2.(1)ac
(2)Cu2+
(3) pH过高,Fe3+生成氢氧化铁胶体吸附大量Ni2+,导致镍
回收率降低
(4) 取最后一次的洗涤液少许于试管中,先加盐酸酸化,再加氯化钡溶液,若无沉淀生成,则证明洗
涤干净
(5)
【分析】由已知信息可知,合金废料中加入混酸浸取液浸取后,得到的溶液中含有的离子有H+、Ni2+、
Cu2+、Fe3+、 、 ,向溶液中加入萃取剂,用萃取剂除去溶液中的Cu2+,向萃取后的溶液中加入还原
剂,将Fe3+还原为Fe2+,然后加入H O ,将Fe2+氧化为FeOOH沉淀,除去溶液中的铁元素;过滤后,向滤
2 2
液中加入,(NH ) C O 溶液反应得到NiC O 。
4 2 2 4 2 4
【详解】(1)a.适当延长浸出时间可以使反应更充分,提高浸出率,a项选;b.高温条件下可以加快反应速率,但是在高温条件下硝酸会挥发,故不能用高温浸出,b项不选;
c.分批加入混酸浸取并搅拌能使反应物混合更均匀,更充分,提高浸出率,c项选;
答案选ac;
(2)由流程分析可知,后续的操作不能除去Cu2+,故只能在萃取步骤中除去Cu2+;
(3)①由题意可知,氧化过程是在70℃、pH小于3的条件下进行,过氧化氢与亚铁离子发生氧化还原反
应生成FeOOH沉淀,反应的离子方程式为 ;
②由题给信息可知,溶液pH增大,Fe2+被氧化的速率加快,同时生成的Fe3+水解形成更多的胶体能吸附
Ni2+,导致镍回收率降低;
(4)由流程可知,草酸镍晶体表面附有可溶的硫酸铵和硝酸铵,检验晶体是否洗涤干净实际上就是检验
洗涤液中是否存在硫酸根,则检验方法为取最后一次的洗涤液少许于试管中,先加盐酸酸化,再加氯化钡
溶液,若无沉淀生成,则证明洗涤干净;常温下K [NiC O ]=1.70×10-17,当溶液pH=2时,Ni2+沉淀完全,假
sp 2 4
设Ni2+浓度为1×10-5mol·L-1,则 = = ,溶液pH=2,
,草酸的K = =5.0×10-5,则 = =
a2
,K = =6.0×10-2,则 = ,
a1
(5)在空气中加热二水合草酸镍得到NiO,该反应的化学方程式为
。
3.(1)
(2)
(3) 当 沉淀完全时, 也会形成 沉淀(4) 阴极
(5) 12
【分析】矿石中的 能与 溶液反应生成 ,“酸浸氧化”过程中,二价铁被氧化为 ,
被还原为 ,调 的方法将Fe3+、Cu2+除去,加入(NH ) S除Ni2+,最后电解得到锰或二氧化锰。
4 2
【详解】(1)矿石中的 能与 溶液反应生成 ,故滤液中的溶质为NaOH、Na SiO ;由图
2 3
可知,硫化物中硫元素转化为单质硫,红褐色固体是 ,相应反应的化学方程式为
。
(2)“酸浸氧化”过程中,二价铁被氧化为 , 被还原为 ,离子方程式为
。
(3)由已知图可知,当 沉淀完全时, 也会形成 沉淀,当同时形成 沉淀时,
溶液中存在 、 。
(4) 转化为 时发生还原反应,故 在阴极上放电; 转化为 时发生氧化反应,电极
反应式为 。
(5)由图可知锰的配位数是12;由于面心上的原子与顶点上的原子相切,故面对角线长度为 ,设晶
胞参数为 ,则 ,解得 ,晶胞体积为 ,由均摊法知,一个晶胞中含有4个锰原子,故晶胞的质量为 ,锰的密度为 。
4.(1) 6VO2++ +3H O=6 +Cl-+6H+ SiO H SiO
2 2、 2 3
(2)Fe3+、Al3+
(3)V O •2H O+2KOH=2KVO +3H O
2 5 2 3 2
(4)Al(OH)
3
(5) VO2++H O-e-= +2H+ 紫色变为绿色
2
(6) 6
【分析】废钒催化剂(含有V O 、VOSO 、SiO 、Fe O 以及钾和铝的硅酸盐)加入30%硫酸、氯酸钾进行酸浸
2 5 4 2 3 4
氧化,滤液中含有 、Fe3+、K+、Al3+,二氧化硅难溶于酸,硅酸盐与酸反应生成硅酸沉淀,二氧化硅和
硅酸则是滤渣①,往滤液中加入KOH调节pH=3.0~3.1,由表中数据知,Fe3+、Al3+只有部分转化为沉淀;过
滤后,Fe(OH) 、Al(OH) 、V O ·2H O成为滤饼;再加入KOH调节pH>13,此时Fe3+转化为Fe(OH) 沉淀,
3 3 2 5 2 3
Al(OH) 转化为K[Al(OH) ],V O ·2H O转化为KVO ;加入盐酸调节pH=8.5,此时K[Al(OH) ]转化为Al(OH) 沉
3 4 2 5 2 3 4 3
淀;过滤后往滤液加入NH Cl,生成NH VO 沉淀,煅烧后得到V O 。
4 4 3 2 5
【详解】(1)“酸浸氧化”时,VO2+被氯酸钾在酸性环境下氧化成 反应的离子方程式为6VO2++
+3H O=6 +Cl-+6H+,二氧化硅难溶于酸,硅酸盐与酸反应生成硅酸沉淀,滤渣①的主要成分是二氧化
2
硅和硅酸。
(2)“中和沉淀”中,加入KOH调节pH=3.0~3.1,由表中数据知,Fe3+、Al3+只有部分转化为沉淀,所以随
滤液②可除去金属离子K+以及部分的金属离子有Fe3+、Al3+。
(3)“沉淀转溶”中,加入KOH调节pH>13,V O ·2H O转化为KVO 溶解,方程式为
2 5 2 3
V O •2H O+2KOH=2KVO +3H O。
2 5 2 3 2
(4)加入盐酸“调pH”, 此时K[Al(OH) ]转化为Al(OH) 沉淀,所以滤渣④的主要成分是Al(OH) 。
4 3 3
(5)①充电过程,由图中装置可以看出,左槽电极连电源正极,是电解池阳极,所以电极反应式为:VO2++H O-e-= +2H+。
2
②放电过程中,右槽电极是负极,V2+失电子生成V3+,右槽溶液颜色变化的情况是紫色变为绿色。
(6)由晶胞结构可以看出钒原子最近的氧原子有6个,所以钒原子的配位数是6。
结合晶胞结构进行计算,钒原子的个数为 ,氧原子的个数为 ,晶胞密度为
,所以a= nm。
5.(1) +5 SiO
2
(2)温度80℃,浸出时间90min
(3)5Fe2++ +8H+=5Fe3++Mn2++4H O
2
(4)
(5)用作氮肥
(6)5MnO +2NaNO +8NaOH 5Na MnO +N +4H O
2 3 2 4 2 2
(7) 6
【分析】菱锰矿(主要成分为MnCO ,还含有铁、镍的碳酸盐以及SiO 杂质)中加入硫酸进行溶浸,可以发
3 2
生反应生成硫酸盐,向其中加入具有氧化性的MnO ,可以将Fe2+氧化为Fe3+,滤渣1为SiO 和过量的
2 2
MnO ;向滤液中加入氨水调节pH=4将Fe3+以Fe(OH) 沉淀下来,过滤后向滤液中加入MnS,可以将Ni2+、
2 3
Co2+形成CoS和NiS沉淀下来,滤渣2为过量的MnS、CoS和NiS;向MnSO 溶液中加入NH HCO 溶液和氨
4 4 3
水,使Mn2+形成MnCO 沉淀,MnCO 经过煅烧后和NaNO 、NaOH共溶,再酸化还原得到锰酸钠(Na MnO )
3 3 3 3 4
溶液。
【详解】(1)由化合价代数和为零可知,Na MnO 中Mn的化合价为+5价,滤渣1的主要成分为MnO 和
3 4 2
SiO 。
2
(2)物质的浸出率越高,反应消耗的时间越短,反应要求的温度越低,反应条件越佳。根据图2可知,所
采用的最佳实验条件是温度80℃,浸出时间90min。(3)浸出液加入MnO 可以将Fe2+氧化为Fe3+,根据得失电子守恒和电荷守恒配平离子方程式为:5Fe2++
2
+8H+=5Fe3++Mn2++4H O。
2
(4)“除镍”步骤发生的反应为:MnS(s)+Ni2+(aq)=NiS(s)+Mn2+(aq),反应的平衡常数K=
。
(5)向MnSO 溶液中加入NH HCO 溶液和氨水,使Mn2+形成MnCO 沉淀,同时得到母液为(NH ) SO ,可
4 4 3 3 4 2 4
以用作氮肥。
(6)煅烧产物MnO 在“共熔”过程中,反应得到Na MnO 及一种单质气体,Mn元素由+4价上升到+6价,
2 2 4
由得失电子守恒可知,NaNO 中N元素化合价由+5价下降到0价生成N ,则该反应的化学方程式为:
3 2
5MnO +2NaNO +8NaOH 5Na MnO +N +4H O。
2 3 2 4 2 2
(7)根据晶胞投影图可知,在该晶体中与Mn原子距离相等且最近的O原子有6个,所以 Mn的配位数为
6。由晶胞结构可知,在该晶胞中距离最近的2个Mn之间的距离为晶胞体对角线长度的一半,晶胞的体对
角线长度为 pm,所以该晶体中Mn之间的最近距离为 pm。
6.(1)15
(2) 精磨可以使颗粒更细,提高酸浸效率
(3)CuS难溶于硫酸溶液,在溶液中存在沉淀溶解平衡 ,增大 的浓度,可以反
应消耗 ,使之转化为S,从而使沉淀溶解平衡正向移动,从而可促进 的浸取
(4)3.2≤pH<4.2
(5) 和
(6)向滤液中通入高压 , 被还原为Cu单质,通过过滤分离出来
(7)【分析】铜硫矿原石中经过粉碎解离得到主要成分为CuS的铜蓝矿和主要成分为FeS 的黄铁矿。 但解离度
2
达不到100%,即铜蓝矿含杂质FeS ,经过纯氧环境下的精磨酸浸,Cu生成Cu2+,S转变为单质和 ,杂
2
质二价铁被氧化成三价铁,碱浸时Fe3+生成Fe(OH) 沉淀,Ca2+结合 生成CaSO 沉淀,二者形成滤渣
3 4
X,滤液B中的Cu2+与H 反应得到Cu。
2
【详解】(1)基态原子的空间运动状态数即轨道数。Cu是29号元素,基态铜原子的电子排布式为
,共15个电子轨道,即铜原子的空间运动状态数为15。
(2)精磨可以使颗粒更细,增大反应物的接触面积,提高酸浸效率;“酸浸”时,S元素被O 氧化成单质
2
S和 ,杂质二价铁被氧化成三价铁,化学方程式为 。
(3)CuS难溶于硫酸溶液,在溶液中存在沉淀溶解平衡 ,增大 的浓度,可
以反应消耗 ,使之转化为S,从而使沉淀溶解平衡正向移动,从而可促进 的浸取。
(4)生石灰调pH值是为了除去杂质Fe3+,pH需要大于或等于3.2,但不能将Cu2+转化为沉淀,因此应调
pH小于4.2,即3.2≤pH<4.2。
(5)滤液A中含有CuSO 和Fe3+,加入CaO后,除了生成Fe(OH) 沉淀,还会有CaSO 生成,即滤渣X的主
4 3 4
要成分是Fe(OH) CaSO 。
3、 4
(6)向滤液中通入高压 , 被还原为Cu单质,通过过滤分离出来。
(7)黄铁精矿的 在反应时被氧化成Fe3+和 , 被还原为Cr3+,在酸性溶液中,反应方程式为:
。
7.(1)升高温度,加快反应速率
(2)Cu、Fe、Zn
(3)2ZnSO 2ZnO+2SO ↑+O ↑
4 2 2(4)ZnFe O +3H S+H ZnS+2FeS+4H O
2 4 2 2 2
(5) 4 正四面体
【分析】锌灰(含ZnO及少量PbO、CuO、Fe O 、SiO )中加入稀硫酸浸取,SiO 和硫酸不反应,PbSO 难溶于
2 3 2 2 4
水和稀硫酸,过滤后,滤渣为SiO 、PbSO ,滤液中含有硫酸锌、硫酸铜、硫酸铁、硫酸,加足量锌粉,硫
2 4
酸铜、硫酸铁、硫酸都能与锌反应,加H O 将未被还原的Fe2+氧化,再加入硫酸铁调节锌、铁的配比,加
2 2
入碳酸氢钠沉锌铁,制得脱硫剂ZnFe O 。
2 4
【详解】(1)“浸取”时不断通入高温水蒸气,可使溶液的温度升高,反应速率加快,则目的是:升高
温度,加快反应速率。
(2)向浸取后的滤液中加足量锌粉,Cu2+、Fe3+、H+都被还原,过滤、加H O ,将未被还原的Fe2+氧化为
2 2
Fe3+,过滤所得滤渣的成分为:Cu、Fe、Zn。
(3)设ZnSO ·7H O固体的质量是100g,物质的量为 mol,依据锌守恒的原则,可求出688℃时固体的
4 2
摩尔质量为 ≈161g/mol,其为ZnSO ;1050℃时所得固体的摩尔质量为 ≈81g/mol,其为
4
ZnO,分解产生的气体应为SO 、O 的混合气,该过程中发生反应的化学方程式为2ZnSO
2 2 4
2ZnO+2SO ↑+O ↑。
2 2
(4)硫化过程中ZnFe O 与H 、H S反应生成ZnS和FeS,铁元素化合价由+3降低为+2、氢气中H元素化合
2 4 2 2
价由0升高为+1,根据得失电子守恒,其化学方程式为ZnFe O +3H S+H ZnS+2FeS+4H O。
2 4 2 2 2
(5)①氧化锌晶胞中,含Zn原子个数为 =4,含O原子个数为4,则晶体的化学式为ZnO,从
图中可以看出,与O原子距离最近的Zn原子数目有4个,则与Zn原子距离最近的O原子数目也有4个,
该晶胞沿y轴方向的平面投影图中,Zn原子位于正方形的顶点、面心和棱心,4个O原子位于面内对角线离顶点 处,可表示为 。
②Zn2+形成的一种配离子[Zn(NH ) (H O) ]2+只有一种空间结构,则其为四面体结构,不是平面结构,所以
3 2 2 2
[Zn(NH ) ]2+的空间结构为正四面体。
3 4
【点睛】计算晶胞中含有的微粒个数时,可使用均摊法。
8.(1)2Al+2OH-+2H O=Al +3H
2 2
(2)Ni2+、Fe2+、Fe3+
(3)3.2≤pH<6.7
(4)冷却到30.8到53.8结晶
(5) NiSO >CoSO >FeSO 正四面体 4 N>O>C
4 4 4
【分析】本流程根据物质的相关物理性质、化学性质,设计一系列的分离提纯过程,除去杂质,获得所需
工业产品;通过碱洗除去Al元素,再通过酸洗除去不溶性杂质,Ni、Al、Fe及其氧化物和硫酸反应转化为
Ni2+、Fe2+、Fe3+。利用H O 氧化性将Fe元素存在形式均调整成Fe3+,利用Fe3+易水解,Fe3+、Ni2+水解pH环
2 2
境不一致的特点,通过调节溶液pH完成Fe元素的除去;再利用经典的蒸发结晶操作获得结晶水合物产品。
【详解】(1)“碱浸”时Al和NaOH溶液反应生成偏铝酸钠和氢气,离子方程式为:2Al+2OH-+2H O=Al
2
+3H 。
2
(2)由分析可知,“滤液②”中含有的金属离子是Ni2+、Fe2+、Fe3+。
(3)由上述表格可知,Ni2+完全沉淀时的pH=8.7,此时 c(Ni2+)=1.0×10-5mol·L-1,c(H+)=1.0×10-8.7mol·L-1,则
c(OH-)=10-5.3 mol/L,则Ni(OH) 的 K =c(Ni2+)⋅c2(OH-)=10-5×(10-5.3)2 =1.0×10-15.6,如果“转化”后的溶液中
2 sp
Ni2+浓度为0.1mol·L-1,此时,则 c(H+)= =10-6.7mol/L,即pH=6.7;为避免镍离子沉淀,溶液的pH
应小于6.7,Fe3+完全沉淀的pH 为3.2,因此“调节pH”应控制的pH范围是3.2≤pH<6.7。
(4)由 溶液获得稳定的 晶体的操作依次是蒸发浓缩、冷却到30.8到53.8结晶、过滤、洗涤、干燥。
(5)①Fe、Co、Ni三种元素二价离子的半径依次减小,硫酸盐晶体中品格能依次增大,所以其熔点出高
到低的顺序为NiSO >CoSO >FeSO ;
4 4 4
②NiSO 的阴离子为SO 中心原子价层电子对数为 =4,且没有孤电子对,空间构型为正四
4
面体;
③由图可知,Ni2+与4个N形成配位键,Ni2+的配位数为4;同周期元素,从左到右第一电离能呈增大趋势,
但氮原子的2p轨道为半充满稳定结构,第一电离能大于相邻元素,则C、N、O三种元素第一电离能从大
到小为:N>O>C。
9.(1)增大催化剂与水的接触面积,提高反应速率与浸出率
(2)SiO +2NaOH = Na SiO + H O或 SiO + Na CO Na SiO + CO ↑
2 2 3 2 2 2 3 2 3 2
(3) VO2+水解程度增加或生成VO(OH) ,影响钒的浸出率
2
空轨道
(4)酸性
(5)0.5
(6) CsV Sb 6
3 5
【分析】水浸废钒催化剂(含V O 、VOSO 、K SO 、SiO 以及少量的Fe O 等),VOSO 、K SO 进入滤液1,
2 5 4 2 4 2 2 3 4 2 4
V O 、SiO 以及Fe O 进入滤渣1,用无水K₂SO 和H₂SO 对滤渣1还原酸浸,V O 、Fe O₃和K SO 和H SO 反
2 5 2 2 3 3 4 2 5 2 2 3 2 4
应进入滤液2,SiO 进入滤渣2,用有机试剂对滤液1和滤液2中的 、VO2+进行萃取分离出亚铁离子和
2
钾离子,再反萃取出 和 VO2+,再加氨水沉钒,焙烧得到V O ,据此分析解答。
2 5
【详解】(1)“水浸”前,通常需要将催化剂粉碎,其目的是增大催化剂与水的接触面积,提高反应速
率与浸出率;
(2)“滤渣2”主要成分是SiO ,转化为 Na SiO 的化学方程式是:SiO +2NaOH = Na SiO + H O或 SiO +
2 2 3 2 2 3 2 2Na CO Na SiO + CO ↑;
2 3 2 3 2
(3)①“还原酸浸”时,硫酸的用量会影响钒的浸出率,pH超过1.2时,VO2+水解程度增加或生成
VO(OH) ,水解产物会进入滤渣中影响钒的浸出率;
2
②过程中除了有 ,被还原成VO2+,还涉及的反应离子方程式为
③由图2可知,和V形成配位键的P、O、Cl均含有孤电子对,故V提供的是空轨道;
(4)“萃取”时选择有机萃取剂,原理是:H R(有机层)+VO2+ 2H+ +VOR(有机层),“反萃取”应让平衡
2
逆向移动,使VO2+进入水层,故选择在酸性环境中进行;
(5)VO(OH) 沉淀经焙烧得到V O 的方程式为:4VO(OH) +O 2V O + 4H O,若经焙烧得到1molV O
2 2 5 2 2 2 5 2 2 5
产品,则消耗空气中O 的物质的量为: mol=0.5mol;
2
(6)由该化合物的晶胞可知,Cs位于顶点,含有 个,Sb位于棱上和晶胞内 个,V位于
面上和晶胞内,含有 个,所以锑化物M的化学式 CsV Sb ;晶胞中有4个面的面心由钒原子
3 5
占据,这些钒原子填充在锑原子构成的八面体空隙中,周围紧邻的锑原子数为6;
【点睛】本题考查物质准备工艺流程,涉及物质的分离提纯、条件的控制、原理的分析评价、陌生方程式
书写等,熟练掌握元素化合物性质,理解整个过程,题目难度中等。
10.(1)将铌钽矿粉碎、搅拌、升高温度等
(2) CaF 、MgF SiF
2 2 4
(3)少量多次萃取
(4)(5) 6
【分析】花岗伟晶岩型铌钽矿(主要成分为 、 、 和少量的FeO、CaO、MgO等)加入
HF、硫酸浸取,得到浸渣,主要成分为CaF 、MgF , 可与HF反应生成SiF 气体,得到浸出液加入
2 2 4
MIBK萃取,分为水相和有机相,有机相加入纯水进行反萃取,在水相中加入氨气沉钽,得到氢氧化钽,加
热分解得 ,电解制得Ta,水相加HF、KF沉铌,得到K NbF ,与Na反应得到铌粉。
2 7
【详解】(1)加快“浸取”速率可采取的措施是:将铌钽矿粉碎、搅拌、升高温度等;
(2)由CaF 和MgF 的K 可知,“浸取”时得到的“浸渣”主要成分为:CaF 、MgF ;“浸取”时还会产
2 2 sp 2 2
生“废气”,“废气”中除了挥发出的HF还可能有 可与HF反应生成的SiF ; 与氢氟酸反应生
4
成 ,离子方程式为: ;
(3)“萃取”时,若萃取剂MIBK的量一定,少量多次萃取接触更加充分,萃取效率更高;
(4)用金属钠还原 制取金属铌,根据氧化还原得失电子守恒的原子,可得到其化学方程式为:
;
(5)由图可知,As的配位数为6;由均摊法可知,一个晶胞中含有4个TaAs,晶胞质量为: ,
体积为 ,密度为 。
11.(1)Ga O +Na CO 2NaGaO +CO ↑
2 3 2 3 2 2
(2) Fe O [Ga(OH) ]-+3e-=Ga+4OH-
2 3 4
(3)100.4(4)阳
(5) Al O 4∶1
2 3
(6)Ga O +2NH 2GaN+3H O
2 3 3 2
【分析】
粉煤灰(主要成分为 Ga O 、Al O 、SiO ,还有少量 Fe O 等杂质)与纯碱焙烧得到 NaAlO 、NaGaO 、
2 3 2 3 2 2 3 2 2
Na SiO 、Fe O 等的混合物,“碱浸”所得滤渣中主要成分为 Fe O ,碱浸后滤液经“操作”得到含
2 3 2 3 2 3
[Ga(OH) ]-的溶液,向其中通入足量CO 得到Ga(OH) ,Ga(OH) 加热分解得到Ga O ,电解Ga O 得到Ga;电
4 2 3 3 2 3 2 3
解含[Ga(OH) ]-的溶液得到Ga,加入CH Br合成、再与NH 反应得到GaN。
4 3 3
【详解】(1)Ga的性质与铝相似,“焙烧”过程中Al O 变为NaAlO ,则Ga O 与纯碱反应的化学方程式
2 3 2 2 3
为Ga O +Na CO 2NaGaO +CO ↑。
2 3 2 3 2 2
(2)根据分析,“碱浸”后滤渣的主要成分为Fe O ;用惰性电极电解含[Ga(OH) ]-的溶液可得到金属Ga,
2 3 4
Ga元素的化合价由+3价降至0价,则阴极的电极反应式为[Ga(OH) ]-+3e-=Ga+4OH-。
4
(3)由图可知,当pH=9.4时lgc{[Ga(OH) ]-}=-5,则反应[Ga(OH) ]-(aq) Ga(OH) (s)+OH-(aq)的平衡常数K=
4 4 3
=100.4。
(4)用石墨为电极电解熔融Ga O 得到Ga单质,阴极得到Ga,阳极产生O ,O 消耗石墨产生CO 、CO气
2 3 2 2 2
体,故电极材料需要定期补充的是阳极。
(5)①图中所示致密保护膜为一种氧化物,可阻止H O 刻蚀液与下层GaAs(砷化镓)反应,说明H O 与
2 2 2 2
AlAs反应产生该致密的氧化物保护膜,该氧化物为Al O 。
2 3
②在H O 与上层GaAs的反应中,As元素的化合价变为+5价,As元素的化合价由-3价升至+5价,GaAs为
2 2
还原剂,1molGaAs失去8mol电子,H O 为氧化剂,1molH O 得到2mol电子,根据得失电子守恒,该反应
2 2 2 2
的氧化剂与还原剂的物质的量之比为8∶2=4∶1。
(6)将热分解得到的Ga O 与NH 在高温下反应可制得GaN,同时生成另一种产物,根据原子守恒,另一
2 3 3
种产物为H O,该反应的化学方程式为Ga O +2NH 2GaN+3H O。
2 2 3 3 212.(1)
(2)
(3)
(4)已除尽
(5)烃基是疏水基团,壬醇中烃基较大
(6)A
(7)2:7
【分析】锆英砂主要成分为 ,常含有 等氧化物杂质。加碳酸钠“碱熔”,锆英
砂转化为 、Al O 与转化为 ,水浸过滤,滤渣中含有 、Fe O 、CuO,滤
2 3 2 3
渣用盐酸“酸浸”,得ZrOCl 、氯化铁、氯化铜溶液,加NaCN生成Cu(CN) 沉淀除铜,滤液中加盐酸、萃
2 2
取剂 萃取,水层加浓盐酸析出 沉淀,煅烧 得ZrO 。
2
【详解】(1)“碱熔”时, 与碳酸钠反应生成 、二氧化碳,反应的化学方程式为
;
(2)碱熔时,Al O 与碳酸钠反应生成可溶性四羟基合铝酸钠、二氧化碳,“水浸”时,所得“滤液”中
2 3
溶质的主要成分除 外,还有 ;
(3)“酸浸”后,锆元素以 的形式存在于溶液中,此过程中 与盐酸发生反应生成
ZrOCl 、NaCl、H SiO ,反应的离子方程式为 。
2 2 3
(4)“除铜”时,若测得剩余滤液中 ,,可知 已经除尽。
(5)烃基是疏水基团,壬醇中烃基较大,所以“有机溶剂 ”中的壬醇 几乎与水互不相溶。
(6)盐酸的浓度越小氯氧化锆的溶解度越大,盐酸的浓度为2mol/L时铁的萃取率很高,所以在“萃取”
过程中,应选用盐酸的最适宜浓度为2mol/L,选A。
(7)“煅烧”时,需要在 条件下发生反应 ,所得两种气体的
体积之比 2:7。
13.(1) MgF 取适量滤液1于试管中,滴加几滴K [Fe(CN) ]溶液,无蓝色沉淀产生,说明Fe2+已
2 3 6
被完全氧化
(2)CO
2
(3)
(4)由于Fe2+的还原性强于Co2+,优先被NaClO溶液氧化为Fe3+,若NaClO溶液过量,则Co2+也会被氧化,所
以控制NaClO溶液有利于得到较纯的黄钠铁矾
【分析】铁钴矿焙烧时硫元素转化为二氧化硫,高温下碳元素转化为碳的氧化物,铁元素转化为铁单质,
钴元素转化为钴单质,然后用硫酸酸浸,二氧化硅不溶,滤液1中主要含有Co2+、Fe2+、Mg2+等,加入次氯
酸钠氧化溶液中的亚铁离子,加入碳酸钠调节pH沉淀铁离子,使其转化为黄钠铁矾,滤液2中加入氟化
钠沉淀镁离子,滤液3中加入次氯酸和碳酸钠,氧化Co2+,同时使其转化为滤渣4,滤渣4焙烧得到三氧化
二钴,据此解答。
【详解】(1)①滤液2中加入氟化钠沉淀镁离子,所以滤渣3的主要成分为MgF ;
2
②检验亚铁离子一般用K [Fe(CN) ]溶液,所以确定滤液1中的Fe2+已被氧化完全的方法为:取适量滤液1于
3 6
试管中,滴加几滴K [Fe(CN) ]溶液,无蓝色沉淀产生,说明Fe2+已被完全氧化;
3 6
(2)①在溶液A中加入适量的Na CO 调节pH为1.6∼2.0,生成黄钠铁矾[Na Fe (SO ) (OH) ]沉淀,根据原
2 3 2 6 4 4 12
子守恒可知生成气体的化学式为CO ;
2(3)①滤液3中加入次氯酸和碳酸钠,氧化Co2+钴离子,同时使其转化为Co(OH) ,根据添加比例及氧化
3
还原规律可得到总反应的离子方程式是 ;
②由流程可知,Co(OH)SO 隔绝空气灼烧时生成Co O ,根据原子守恒可知还有水和三氧化硫生成,则发生
4 2 3
的化学反应方程式为 ;
③如果控制温度不当,Co(OH) 会生成CoO杂质,发生氧化还原反应,根据氧化还原规律,可得反应方程
3
式为: ;
(4)由于Fe2+的还原性强于Co2+,优先被NaClO溶液氧化为Fe3+,若NaClO溶液过量,则Co2+也会被氧化,
所以控制NaClO溶液有利于得到较纯的黄钠铁矾。
14.(1)氧化
(2)AC
(3)使Fe3+转化成Fe(OH) 沉淀除去
3
(4)0.001
(5)
(6)5.4
(7)0.0250mol/L
【分析】锰废渣的硫酸浸出液首先用二氧化锰将二价铁氧化为三价铁,加入碳酸钙后调节pH使三价铁转
化为氢氧化铁除去三价铁离子,再用氟化锰除去钙离子、镁离子,随后再用萃取剂a萃取滤液中的 ,
所得有机相中加入反萃取剂得到含Mn2+的溶液,无机相用萃取剂b萃取 ,无机相中为含 的溶液,
有机相加入反萃取剂得到含Co2+的溶液,以此解题。【详解】(1)根据题意可知,浸出液中含有二价铁, 的作用是氧化 ;
(2)根据流程图可知,该流程涉及的实验过程有过滤,分液,故选AC;
(3)在用二氧化锰将二价铁氧化为三价铁后,加入碳酸钙调节pH使三价铁形成氢氧化铁沉淀,故目的是:
使Fe3+转化成Fe(OH) 沉淀除去;
3
(4)当溶液中 时, ,
;
(5)根据信息可知,反萃取剂为酸,则反萃取出 是加入适量的酸将锰离子反萃取出来,相应的方程
式为: ;
(6)根据图中信息可知,pH为5.4左右时, 、 的萃取率相差较大,故无机相的 控制在5.4左
右;
(7)根据滴定原理可知,Ni2+与H Y2-的物质的量之比为1∶1,则Ni2+的物质的量为0.1000mol/L×0.0125L
2
=0.00125mol,则Ni2+的物质的量浓度为 。
15.(1)将Fe2+全部氧化为Fe3+
(2)使Cu2+转化为Cu(OH) 除去
2
(3)Mn2++2HCO =MnCO ↓+CO ↑+H O
3 2 2
(4)NH Cl
4
(5) 1:2 Mn O 和MnO
3 4
(6) sp3 F的电负性比N大,N-F成键电子对向F偏移,导致NF 中N原子核对其孤对电子的吸引
3
能力增强,难以形成配位键,故NF 不易与Cu2+形成配离子
3
(7) 4
【分析】根据流程:酸性含锰废水(主要含Mn2+、Cl-、H+、Fe2+、Cu2+)加过量MnO ,将Fe2+氧化为Fe3+,加
2氨水调节pH=3.7,Fe3+转化为Fe(OH) 沉淀,过滤,滤渣为Fe(OH) 和过量的MnO ,滤液A含有Mn2+、Cl-、
3 3 2
H+、Cu2+,加氨水调节pH=6.4,则Cu2+转化为Cu(OH) 沉淀,过滤,滤渣Q为Cu(OH) 沉淀,滤液B含有
2 2
Mn2+、Cl-,加碳酸氢铵反应:Mn2++2 =MnCO ↓+CO ↑+H O,据此分析作答。
3 2 2
【详解】(1)MnO 在酸性条件下可将Fe2+氧化为Fe3+,反应的离子方程式为:MnO +2Fe2++4H+=Mn2++2Fe3+
2 2
+2H O;
2
(2)调pH=6.4,除去溶液中的铜离子,使Cu2+ 完全沉淀为Cu(OH) ;
2
(3)过程④中,反应会有CO 生成,故反应为Mn2++2 =MnCO ↓+CO ↑+H O;
2 3 2 2
(4)过程④中得到纯净MnCO 的操作方法是过滤、洗涤、干燥。根据元素守恒,流程中,氯离子未除去,
3
加入铵根离子,则副产品为NH Cl;
4
(5)MnCO 的物质的量为1 mol即质量为115 g,A点剩余固体质量为115 g×75.65%=87 g,减少的质量为
3
115 g-87 g=28 g,可知MnCO 失去的组成为CO,故剩余固体的成分为MnO ,n(Mn):n(O)为1:2;C点剩
3 2
余固体质量为115 g×61.74%=71 g,据锰元素守恒知m(Mn)=55 g,则m(O ) =71 g-55 g=16 g,则n(Mn):n(O)=
1
=1:1,故剩余固体的成分为MnO,同理,B点剩余固体质量为115 g×66.38%=76.337 g,因
m(Mn)=55 g,则m(O ) =76.337 g-55 g=21.337 g,则n(Mn):n(O)= =3:4,故剩余固体的成分为
2
Mn O ,因D点介于B、C之间,故D点对应固体的成分为Mn O 与MnO的混合物;故答案为:1:2;
3 4 3 4
Mn O 和MnO;
3 4
(6)NF 与NH 的空间构型相同,这两种分子中中心原子价层电子对个数都是4,根据价层电子对互斥理
3 3
论判断中心原子的轨道杂化类型为sp3;F 的电负性比N大,N-F 成键电子对向F偏移,导致NF 中N 原子
3
核对其孤对电子的吸引能力增强,难以形成配位键,故NF 不易与Cu2+形成配离子;
3
(7)该晶胞中两个Ba2+的间距为cpm,下边Ba原子距离底面中心的距离= pm,距离Ba2+最近的Hg+数
目为4个,二者的最短距离为 。