文档内容
易错专题 21 化学反应原理解题策略
聚焦易错点:
一、反应热的计算
1.反应热计算的方法:
(1)根据“两个”公式计算反应热:ΔH=E(生成物的总能量)-E(反应物的总能量);ΔH=E(反应物的键能
之和)-E(生成物的键能之和), 利用键能计算反应热,需算清物质中化学键的数目。常见物质中所含共价
键的数目:1 mol金刚石中含有2 mol C—C键,1 mol硅中含有2 mol Si—Si键,1 mol SiO 晶体中含有4
2
mol Si—O键; 1 mol P 中含有6 mol P—P键,1 mol P O (即五氧化二磷)中含有12 mol P—O键、4 mol
4 4 10
P===O键,1 mol CH CH 中含有6 mol C—H键和 1 mol C—C键。
3 3
(2)根据热化学方程式计算反应热:焓变与反应物的物质的量成正比。
(3)根据盖斯定律计算反应热:若一个热化学方程式可由另外几个热化学方程式相加减而得到,则该反应
的焓变可通过这几个化学反应焓变的加减而得到。表示方法: ,ΔH=ΔH+ΔH。
1 2
2.热化学方程式的书写:
(1)热化学方程式中化学计量数可以是整数,也可以是分数。
(2)物质的聚集状态:气体用“g”,液体用“l”,固体用“s”,溶液用“aq”。热化学方程式中不用
“↑”和“↓”。
(3)注意ΔH的单位、数值与符号。ΔH的单位为kJ·mol-1,如果化学计量数加倍,则ΔH也要加倍,逆
反应的反应热与正反应的反应热数值相等,但符号相反。
(4)对于具有同素异形体的物质,除了要注明聚集状态之外,还要注明物质的名称。如① S(s,单斜)+
O(g)===SO(g)ΔH=-297.16 kJ·mol-1;②S(s,正交)+O(g)===SO(g)ΔH=-296.83 kJ·mol-1;
2 2 1 2 2 2
③S(s,单斜)===S(s,正交) ΔH=-0.33 kJ·mol-1。
3
3. 根据盖斯定律计算反应热的方法:
(1)观察已知的热化学方程式与目标热化学方程式的差异,若目标热化学方程式中的某种反应物在某个已知
热化学方程式中作生成物,可把该热化学方程式的反应物和生成物颠倒,相应的ΔH改变符号。
(2)将每个已知热化学方程式两边同乘以某个合适的数,使已知热化学方程式中的化学计量数与目标热化学
方程式中的化学计量数一致,ΔH也同倍数变化。
(3)将已知热化学方程式相加或相减,热化学方程式中的ΔH同时相加或相减,得到目标方程式及反应热。
二、化学反应速率和化学平衡
1. 化学反应速率的计算:v(B)==
(1)浓度变化只适用于气体和溶液中的溶质,不适用于固体和纯液体。(2)化学反应速率是某段时间内的平均反应速率,而不是即时速率,且计算时取正值。
(3)同一反应用不同的物质表示反应速率时,数值可能不同,但意义相同。不同物质表示的反应速率之比
等于其化学计量数之比。
(4)计算反应速率时,若给出的是物质的量的变化值,要转化为物质的量浓度的变化值(计算时一定要除以
体积),再进行计算。
2. 外界条件对可逆反应的反应速率的影响:外界条件对可逆反应的正、逆反应速率的影响方向是一致的,
但影响程度不一定相同。
(1)当增大反应物浓度时,v正 增大,v逆 瞬间不变,随后也增大;
(2)增大压强,气体分子数减小方向的反应速率变化程度大;
(3)对于反应前后气体分子数不变的反应,改变压强可以同等程度地改变正、逆反应速率;
(4)升高温度,v正 和v逆 都增大,但吸热反应方向的反应速率增大的程度大;
(5)使用催化剂,能同等程度地改变正、逆反应速率。
3.平衡移动方向的判断:
(1)依勒夏特列原理判断。
(2)根据图像中正逆反应速率相对大小判断:若v >v ,则平衡向正反应方向移动;反之向逆反应方向移
正 逆
动。
(3)依变化过程中速率变化的性质判断:若平衡移动过程中,正反应速率增大(减小),则平衡向逆(正)反
应方向移动。
(4)依浓度熵(Q)规则判断:若某温度下Q<K,反应向正反应方向进行;Q>K,反应向逆反应方向进行。
c c c
4.化学平衡的计算:
(1)化学平衡常数:对于可逆化学反应mA(g)+nB(g) pC(g)+qD(g)在一定温度下达到化学平衡时,
K=。另可用压强平衡常数表示: K =[p(C)为平衡时气体C的分压]。反应体系中纯固体、纯液体以及稀
p
水溶液中水的浓度不写进平衡常数表达式,但非水溶液中,若有水参加或生成,则此时水的浓度不可视为
常数,应写进平衡常数表达式中;同一化学反应,化学反应方程式写法不同,其平衡常数表达式及数值亦
不同。书写平衡常数表达式及数值时,要与化学反应方程式相对应,否则就没有意义。
(2))依据化学方程式计算平衡常数:同一可逆反应中,K ·K =1;同一方程式中的化学计量数等倍扩
正 逆
大或缩小n倍,则新平衡常数K′与原平衡常K间的关系是:K′=Kn或K′=;几个可逆反应方程式相加,
得总方程式,则总反应的平衡常数等于分步反应平衡常数之积。
(3)转化率、产率及分压的计算:反应物转化率=×100%;产物的产率=×100%;分压=总压×物质的量
分数。
5.化学反应速率、化学平衡图像:(1))解题思路:
一看轴(即纵坐标与横坐标的意义),二看点(即起点、拐点、交点、终点),
三看线(即线的走向和变化趋势),四看辅助线(如等温线、等压线、平衡线
看图像
等),五看量的变化(如浓度变化、温度变化等)
想规律 看清图像后联想外界条件对化学反应速率和化学平衡的影响规律
作判断 通过对比分析,作出正确判断
(2)分析方法:认清坐标系,弄清纵、横坐标所代表的意义,并与有关原理相结合;看清起点,分清反
应物、生成物,浓度减小的是反应物,浓度增大的是生成物,一般生成物多数以原点为起点;看清曲线的
变化趋势,注意渐变和突变,分清正、逆反应,从而判断反应特点;注意终点。例如,在浓度时间图像上,
一定要看清终点时反应物的消耗量、生成物的增加量,并结合有关原理进行推理判断;先拐先平数值大。
例如,在转化率时间图像上,先出现拐点的曲线先达到平衡,此时逆向推理可得该曲线对应的温度高、浓
度大或压强大;定一议二。当图像中有三个量时,先确定一个量不变再讨论另外两个量的关系。
三、沉淀溶解平衡和K 的应用
sp
一般情况下,升高温度能促进沉淀的溶解,稀释使平衡向右移动;稀释后重新达到平衡时各离子浓度保持
不变。对于确定的物质来说,K 只与温度有关;温度相同时,组成形式相同的物质,K 较大者溶解度较大。
sp sp
1.沉淀的生成或溶解的判断:若体系内Q=K ,体系处于溶解平衡状态;Q>K ,体系内会有沉淀析出;
c sp c sp
QK 者先形成
c sp
沉淀。
3.沉淀的转化与K 大小间的关系:组成形式相同的难溶物质,K 较大的沉淀肯定可转化为K 较小的沉淀,
sp sp sp
但当二者K 相差不大时,反过来也可转化。
sp
四、电化学的常考点
1.电极名称的判断:总反应方程式中还原剂发生氧化反应做负极,与负极相连的电极为阴极,阴极发生还
原反应;总反应方程式中氧化剂发生还原反应做正极,与正极相连的电极为阳极,阳极发生氧化反应。
2.微粒的移动方向:原电池中,电子由负极移向正极,阳离子移向正极阴离子移向负极;电解池中,电子
由电源负极移向阴极、由阳极移向电源正极,阳离子移向阴极阴离子移向阳极。
3.充、放电的电化学原理:对于可充电电池,放电时为原电池,符合原电池工作原理,负极发生氧化反应,
正极发生还原反应;外电路中电子由负极流向正极,内电路中阳离子向正极移动,阴离子向负极移动。可
充电电池充电时为电解池,阳极发生氧化反应,阴极发生还原反应;充电时电池的“+”极与外接直流电
源的正极相连,电池的“-”极与外接直流电源的负极相连。
4. 不同“介质”与电极反应式的书写:酸性溶液中,电极反应式不可能出现OH—及与H+反应的微粒,如酸
性溶液中CHOH在负极上失去电子生成CO 气体,正极反应式为O +4e-+4H+=2HO;碱性溶液中,电极反
3 2 2 2
应式不可能出现H+及与OH—反应的微粒,如碱性溶液中CHOH在负极上失去电子生成CO,正极反应式为O
3 2
+4e-+2HO=4OH-;电解质为熔融盐或固体,电极反应式不可能出现OH—及H+。
2
5.隔膜的作用:离子交换膜是一种选择性透过膜,阳离子交换膜一般只允许阳离子通过,阴离子交换膜只允许阳离子通过,离子迁移方向遵循电池中离子迁移方向。
6.盐桥的作用:隔绝负极与正极电解质溶液发生化学反应,降低化学能转化为电能的效率;通过离子的定
向移动,构成原电池的闭合回路,并维持正极池和负极池中溶液的电性守恒。
7. 金属腐蚀快慢三个规律:
(1)金属腐蚀类型的差异:电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护腐蚀措施的
腐蚀。
(2)电解质溶液的影响:对同一金属来说,腐蚀的快慢(浓度相同):强电解质溶液>弱电解质溶液>非电解
质溶液;对同一种电解质溶液来说,电解质浓度越大,腐蚀越快。
(3)活泼性不同的两金属,活泼性差别越大,腐蚀越快。
考点精练
1.(2024·山东·二模)丙醛工业上主要用于制合成纤维、橡胶促进剂和防老剂等。在铑催化剂作用下与常
用乙烯羰基化合成丙醛,涉及的反应如下:
主反应Ⅰ:C H (g)+H (g)+CO(g) CH CH CHO(g) ΔH
2 4 2 3 2 1
副反应Ⅱ:C H (g)+H (g) CH CH (g) ΔH
2 4 2 3 3 2
已知:在一定条件下一氧化碳能与铑催化剂结合生成羰基铑络合物;丙醛选择性:x(CH CH CHO)=
3 2
×100%。
回答下列问题:
(1)反应Ⅰ、Ⅱ以气体分压表示的平衡常数Kp与温度T变化关系如图所示。
据图判断,CH CH (g)+CO(g) CH CH CHO(g) ΔH 0(填“>”、“<”或“=”), 的数值范围是
3 3 3 2
(填标号)。A.<-1 B.-1~0 C.0~1 D.>1
(2)在T ℃、压强为150kPa条件下,在密闭反应器中,按照投料n(C H ):n(CO):n(H )=1:1∶1,发生上述
1 2 4 2
反应,经tmin反应达到平衡,测得p(C H )=p(C H )=20kPa,则CH CH CHO(g)的选择性为 %(保留
2 4 2 6 3 2
小数点后一位),v(CO)= kPa/min(用含t的代数式表示),反应Ⅰ的逆反应的Kp= 。
(3)在恒压密闭容器中,在一定温度和铙催化剂作用下,发生上述反应,反应相同时间时,测得C H 的转化
2 4
率(α)和丙醛选择性随 变化关系如图所示。
①曲线a表示 (填“C H 的转化率”或“丙醛选择性”);
2 4
②当 小于1时,曲线b随 的降低而降低的可能原因是 。
2.(2024·内蒙古赤峰·三模)氢能新质生产力正加速发展。工业上利用天然气制备氢气,还能得到乙烯、
乙炔等化工产品,有关反应原理如下:
反应①:2CH (g) C H (g)+3H (g) ∆H=+376.3kJ/mol K ;
4 2 2 2 1 1
反应②:2CH (g) C H (g)+2H (g) ∆H=+202.0kJ/mol K ;
4 2 4 2 2 2
回答下列问题:
(1)反应③:C H (g)+2H (g) C H (g) ∆H= kJ/mol,K = (用含K 、K 的代数式表示)。
2 2 2 2 4 3 3 1 2
(2)若用 、 、 和 表示CH 、C H 、H 和固体催化剂,如图在催化剂表面进行反应①,
4 2 2 2
从吸附到解吸的过程中,能量状态最高的是 (填字母)。
(3)反应②的速率方程为(v =k ·c2(CH ),v =k ·c(C H )·c2(H )(k 、k 为正、逆反应速率常数)。其他条件相
正 正 4 逆 逆 2 4 2 正 逆同,T℃达到平衡时k =1.5k ,T℃达到平衡时k =3.0k 。由此推知,T T(填“>”“<”或“=”)。
1 正 逆 2 正 逆 1 2
(4)向恒温恒容密闭容器中充入适量CH ,同时发生上述反应①和反应②,在不同催化剂Cat1、Cat2作用下,
4
测得单位时间内H 的产率与温度的关系如图所示。在其他条件相同时,催化效率较高的是 (填
2
“Cat1”或“Cat2”)。在Cat2作用下,温度高于500℃时,H 的产率迅速降低的原因是 。
2
(5)在一定温度、102kPa下, 向反应器中充入1mol C H (g)发生反应:C H (g) C H (g)+H (g)制备氢气。
2 4 2 4 2 2 2
①实际操作中,往往向反应器中充入一定量的水蒸气,其目的是 。
②忽略其他副反应,若向反应器中充入5mol水蒸气,平衡时(C H 的转化率为75%,则该反应的Kp=
2 4
。
3.(2024·黑龙江哈尔滨·三模) 经催化加氢可以生成低碳有机物,实现 的综合利用和“碳达峰、
碳中和”的目标。 合成甲醇涉及以下三个反应:
①
②
③
已知:反应①、③是低温条件的自发反应。回答下列问题:
(1)上述三个反应的平衡常数 与温度关系如图1所示。图1中c线表示的反应是 (填“①”、
“②”或“③”), (填“>”、“=”或“<”)。(2) 加氢制甲醇反应机理如图2所示。
下列说法正确的是 (填字母)。
A.羧基物种 和甲酸盐物种 为两种中间体
B.该反应使用的催化剂既加快了反应速率,又提高了 的平衡转化率
C.反应过程中有极性键和非极性键的断裂和形成
(3)某温度下,向一恒容密闭容器中充入等物质的量的 和 ,在催化剂作用下发生反应③并达到平衡状
态。下列图像正确的是 (填字母)。(已知:C选项中t时刻再充入等物质的量的 和 )
(4)在密闭容器中,充入 和 合成 ,发生反应①和②。不同温度下达到平衡时 、
及 的体积分数如图3所示。
①已知曲线b代表 ,则曲线a代表 。
② 时, 的平衡转化率为 (保留两位有效数字,下同),此温度下反应②的
(用平衡物质的量分数代替平衡浓度计算)。
4.(2024·河北邢台·一模) 、 (主要指 和 )是大气主要污染物之一、有效去除大气中的 、
是环境保护的重要课题。
已知:
反应1:
反应2:反应3:
反应4:
回答下列问题:
(1)计算 ,已知反应3的 ,则该反应自发进行的最高温度为
(取整数)K。
(2)已知反应4在某催化剂作用下的反应历程如图。
① (填“ ”或“ ”)0.
②该反应历程的决速步骤为 。
③可提高该反应中 平衡转化率的措施有 (填两条)。
(3)向密闭容器中充入一定量的 和 ,保持总压为 ,发生反应4.当 时 的平
衡转化率随温度 以及 下NO的平衡转化率随投料比 的变化关系如图:①能表示此反应已经达到平衡状态的是 (填标号)。
A.气体的密度保持不变
B. 的浓度不变
C.
②表示 时 的平衡转化率随温度 的变化关系曲线是 (填“"或“II"),理由是 。
③a、d两点对应的平衡常数大小比较为 (填“>”“<”或“=”) 。
④b点对应条件下的压强平衡常数 ( 为用分压表示的平衡常数,分压=总压×物质的量分
数,列出计算式即可)。
5.(2024·天津·二模)二氧化碳利用技术已成为当今世界研究热点。回答下列问题:
(1)空气中CO 含量过高造成的环境问题是 。
2
(2)氢气还原二氧化碳是处理二氧化碳的方法之一,常见反应原理有
H (g)+CO (g) H O(g)+CO(g) H=+41.2kJ·mol-1
2 2 2 2
△
3H (g)+3CO(g) CH OCH (g)+CO (g) H=-245.5kJ·mol-1
2 3 3 2 2
△
①6H (g)+2CO (g) CH OCH (g)+3H O(g) H= kJ·mol-1
2 2 3 3 2 3
△
②在上述反应涉及的分子中,属于非极性分子的是 。甲醇的沸点(64.7℃)高于二甲醚的沸点
(-29.5℃),原因是 。
(3)在恒压密闭容器中通入CO 和H 的混合气体,制备甲醇:
2 2CO (g)+3H (g) CH OH(g)+H O(g) H=-94.3kJ·mol-1,反应过程中测得甲醇的时空收率(STY)(表示单位物质的
2 2 3 2
△
量催化剂表面甲醇的平均生成速率)随温度(T)变化如下表:
①该反应最适宜的温度是 ℃。
②随着温度升高,反应速率加快,甲醇的时空收率增大。继续升高温度,甲醇的时空收率反而降低的原因
可能是 。
(4)一种Li/CO 电池模拟装置如图所示。
2
①离子交换膜为 (填“阴”或“阳”)离子交换膜。
②充电时阳极的电极反应式为 。
6.(2024·天津河东·二模)氮是自然界重要元素之一,氮及其化合物的性质以及氮的循环利用对解决环境
和能源问题都具有重要意义。
已知:1 mol物质中的化学键断裂时所需能量如下表。
物质
能量/kJ·mol 945 498 631
(1)恒温下,将1 mol空气 和 的体积分数分别为0.78和0.21,其余为惰性组分)置于容积为V L的恒容
密闭容器中,假设体系中只存在如下两个反应:ⅰ.
ⅱ. kJmol
⋅
① kJmol 。
⋅
②以下操作可以降低上述平衡体系中NO浓度的有 (填标号)。
A.升高温度 B.移除 C.降低 浓度
③若上述平衡体系中 molL : molL ,则 molL 用含a、b、V
⋅ ⋅ ⋅
的计算式表示)。
(2) 也是造成水体富营养化的重要原因之一,用NaClO溶液氧化可除去氨气。其反应机理如图1(其中
和NaCl略去)。NaClO氧化 的化学反应程式为 。
(3)改变 对溶液中NaClO去除氨气效果与余氯(溶液中+1价氯元素的含量)的影响如图2所示,则
除氨气过程中最佳的 值约为 。
(4)室温下,用水稀释0.1 mol L 氨水,溶液中随着水量的增加而减小的是___________。
⋅A. B.
C. D.
(5)工业上以 和 为原料在一定温度和压强下合成尿素。反应分两步:
ⅰ. 和 生成 ;ⅱ. 分解生成尿素。
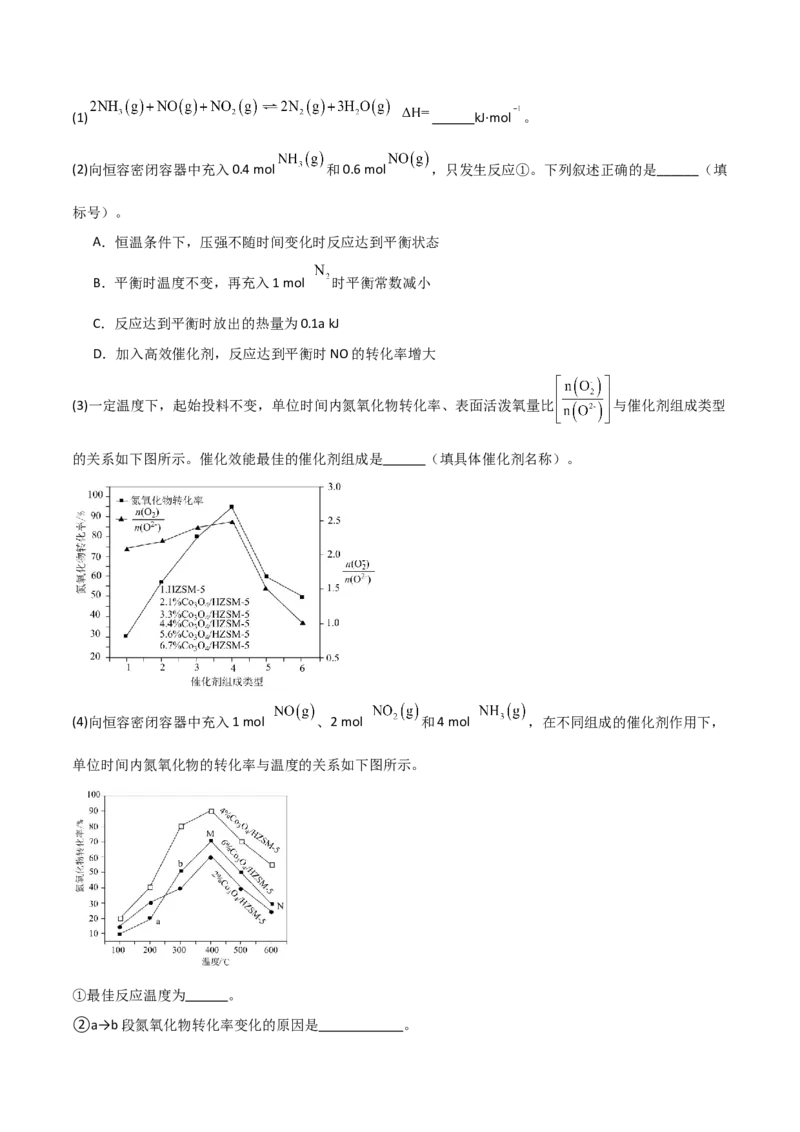
结合反应过程中能量变化图3,下列说法正确的是 。
a.活化能:反应ⅰ<反应ⅱ
b.ⅰ为放热反应,ⅱ为吸热反应
c.
7.(2024·辽宁抚顺·三模)我国科学家根据 在HZSM-5载体上的单层分散行为设计催化剂用于
选择性还原 。回答下列问题:
已知:① kJmol ( )
⋅
② kJmol ( )
⋅(1) kJmol 。
⋅
(2)向恒容密闭容器中充入0.4 mol 和0.6 mol ,只发生反应①。下列叙述正确的是______(填
标号)。
A.恒温条件下,压强不随时间变化时反应达到平衡状态
B.平衡时温度不变,再充入1 mol 时平衡常数减小
C.反应达到平衡时放出的热量为0.1a kJ
D.加入高效催化剂,反应达到平衡时NO的转化率增大
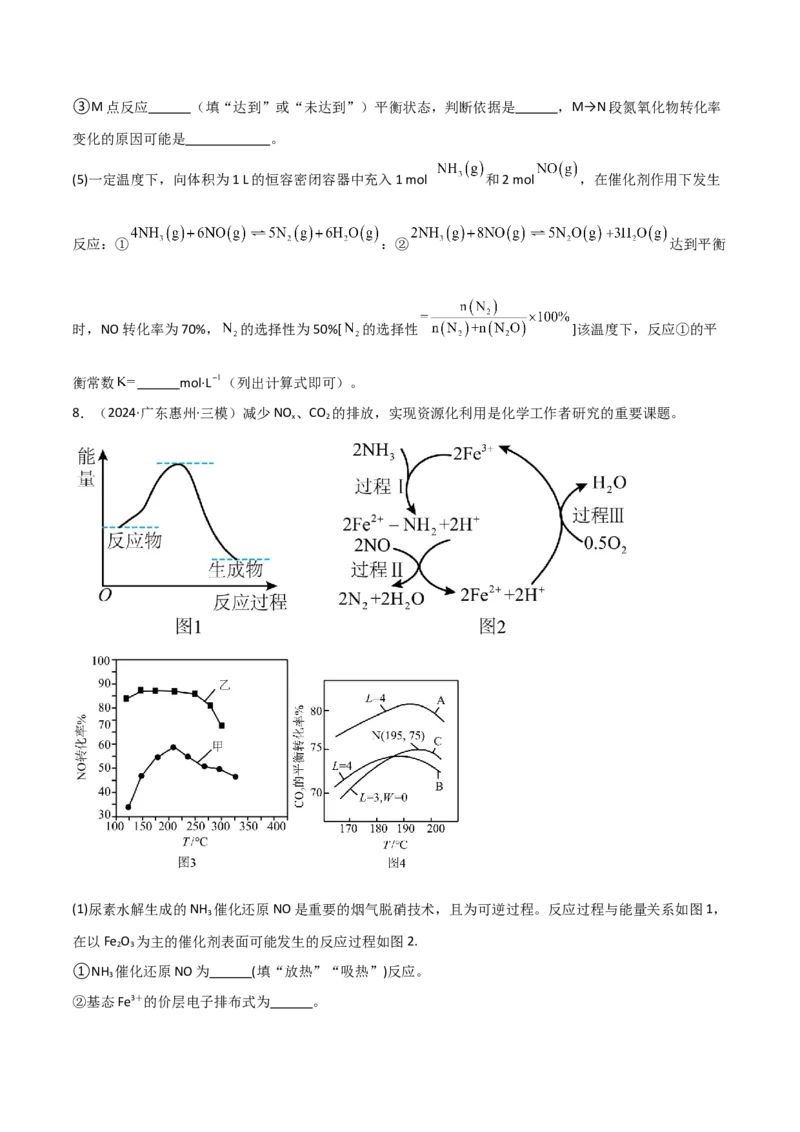
(3)一定温度下,起始投料不变,单位时间内氮氧化物转化率、表面活泼氧量比 与催化剂组成类型
的关系如下图所示。催化效能最佳的催化剂组成是 (填具体催化剂名称)。
(4)向恒容密闭容器中充入1 mol 、2 mol 和4 mol ,在不同组成的催化剂作用下,
单位时间内氮氧化物的转化率与温度的关系如下图所示。
①最佳反应温度为 。
②a→b段氮氧化物转化率变化的原因是 。③M点反应 (填“达到”或“未达到”)平衡状态,判断依据是 ,M→N段氮氧化物转化率
变化的原因可能是 。
(5)一定温度下,向体积为1 L的恒容密闭容器中充入1 mol 和2 mol ,在催化剂作用下发生
反应:① :② 达到平衡
时,NO转化率为70%, 的选择性为50%[ 的选择性 ]该温度下,反应①的平
衡常数 mol·L (列出计算式即可)。
8.(2024·广东惠州·三模)减少NO、CO 的排放,实现资源化利用是化学工作者研究的重要课题。
x 2
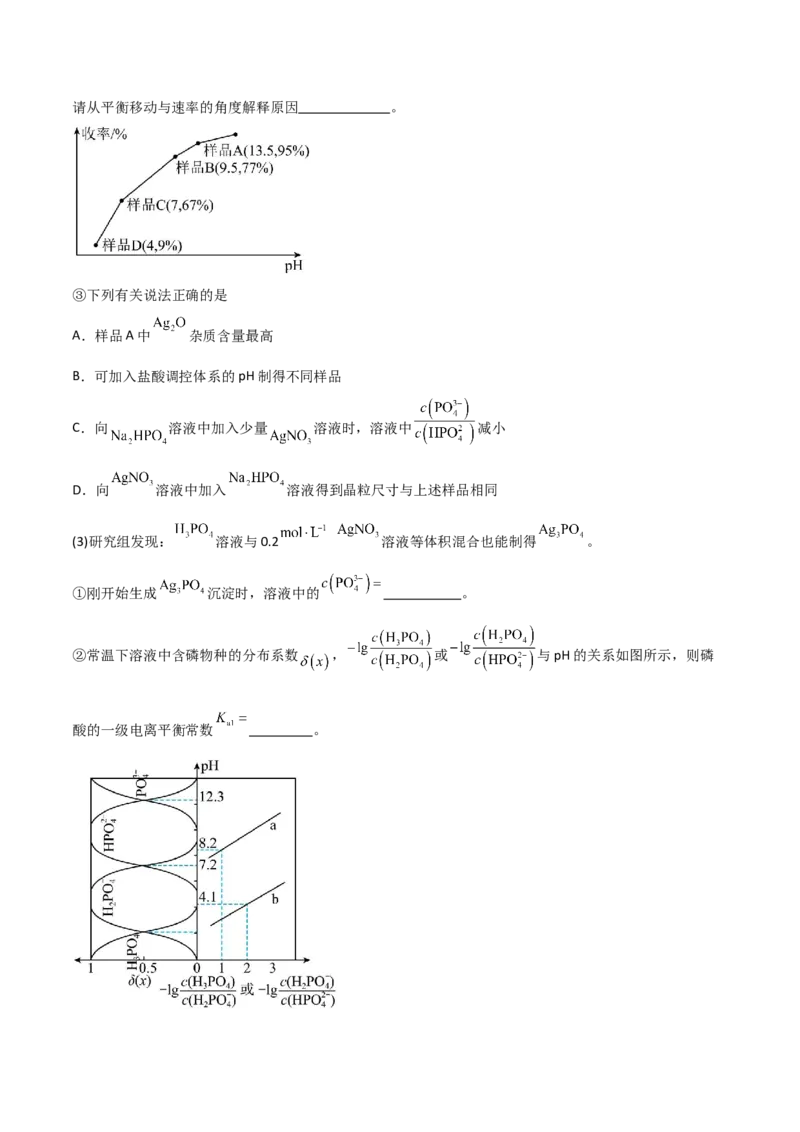
(1)尿素水解生成的NH 催化还原NO是重要的烟气脱硝技术,且为可逆过程。反应过程与能量关系如图1,
3
在以Fe O 为主的催化剂表面可能发生的反应过程如图2.
2 3
①NH 催化还原NO为 (填“放热”“吸热”)反应。
3
②基态Fe3+的价层电子排布式为 。③上述脱硝的总反应化学方程式为: 。
(2)电厂烟气脱氮的反应为:4NH
3
(g)+6NO(g)⇌5N
2
(g)+6H
2
O(g)ΔH<0,现向某2L密闭容器中分别投入一定量
的NH 和2.0×10-4molNO发生以上反应。其他条件相同时,在甲、乙两种催化剂的作用下,反应1min时NO
3
的转化率与温度的关系如图3.
①在催化剂甲的作用下,温度高于210℃小于300℃时,NO转化率降低的可能原因是 。
②100—300℃区间,0~1min内,使用甲催化剂时NO的最高平均速率为 。
(3)工业以NH 和CO 为原料合成尿素。液相中,合成尿素的热化学方程式为:2NH (l)+CO (l) H O(l)+
3 2 3 2 2
NH CONH (l) ΔH<0,在液相中,CO 的平衡转化率与温度、初始氨碳比(用L表示,L= )、初始水碳
2 2 2
比(用W表示,W= )关系如图4.
①曲线A、B中, (填“A”或“B”)的W较小。
②对于液相反应,常用某组分M达到平衡时的物质的量分数x(M)代替平衡浓度来计算平衡常数(记作K)。
x
195℃时,2NH (l)+CO (l) H O(l)+NH CONH (l)的K 的值为 。
3 2 2 2 2 x
9.(2024·广东·二模)催化剂形貌的优化会影响生产效率。 可做烟气脱硝工艺的固相催化剂。
已知:
ⅰ.常温下,AgOH极不稳定,易分解为难溶于水的 固体;
; 。
ⅱ.一般情况,析晶速率越快,晶粒尺寸越小。
(1)基态P原子的核外电子有 个空间运动状态,Ag、P、O元素的电负性由大到小的顺序为 。
(2)某研究组调控反应条件控制 晶体形貌。
①常温下,向银氨溶液逐滴加入 溶液制得 晶体,完善该反应的离子方程式 。
②在不同pH条件下,向 溶液中加入 溶液制得磷酸银收率如图所示。样品A的晶粒较小,请从平衡移动与速率的角度解释原因 。
③下列有关说法正确的是
A.样品A中 杂质含量最高
B.可加入盐酸调控体系的pH制得不同样品
C.向 溶液中加入少量 溶液时,溶液中 减小
D.向 溶液中加入 溶液得到晶粒尺寸与上述样品相同
(3)研究组发现: 溶液与0.2 溶液等体积混合也能制得 。
①刚开始生成 沉淀时,溶液中的 。
②常温下溶液中含磷物种的分布系数 , 或 与pH的关系如图所示,则磷
酸的一级电离平衡常数 。③体系中 由 第一步电离决定,可表示为 ,当生成 沉淀时,溶
液中 至少为 (写出计算过程)。
10.(2024·天津和平·二模)工业废气中H₂S的回收利用有重要意义。
I.利用H S 制CS 。
2 2
(1)热解H S和CH 的混合气体制H 和CS 。
2 4 2 2
①2H S(g) =2H (g)+S (g) ΔH =+170kJmol-1
2 2 2 1
②CH (g)+S (g)=CS (g)+2H (g) ΔH =+64kJmol-1
4 2 2 2 2
总反应:2H S(g)+CH (g) =CS (g)+4H (g),ΔH= 。
2 4 2 2
(2)CH 的电子式为 ,CS 分子的立体构型为 。
4 2
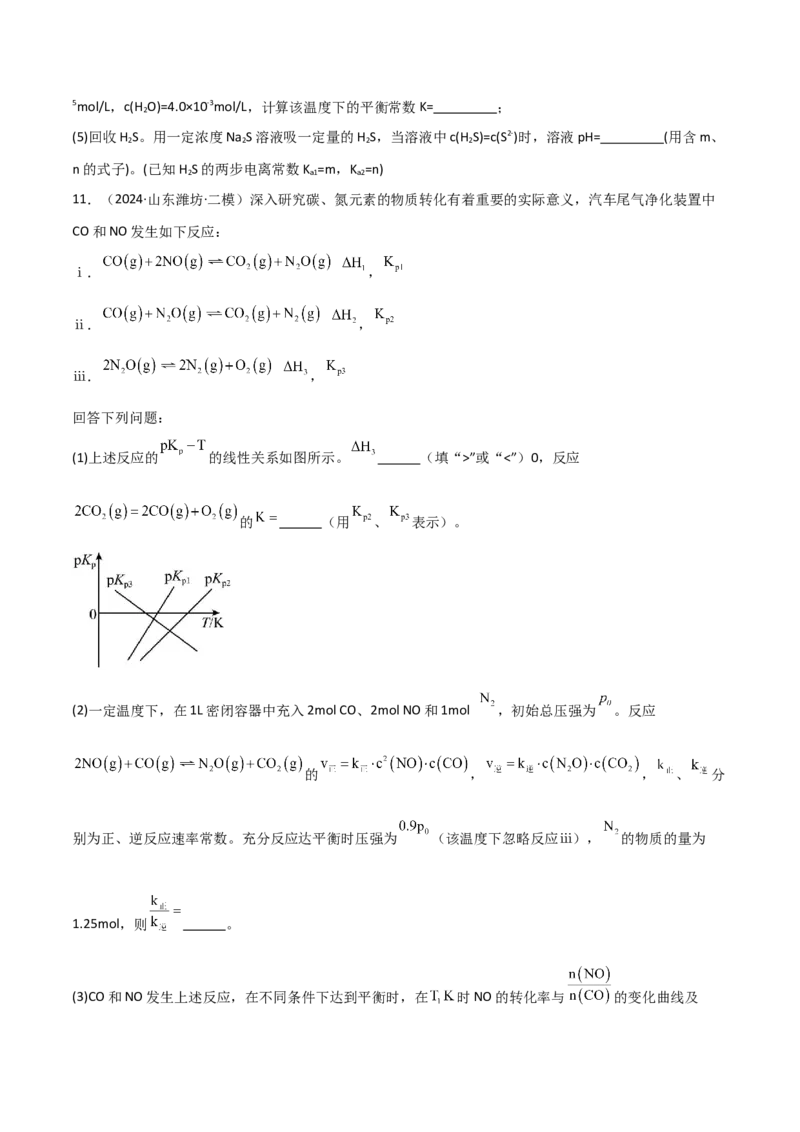
(3)工业上还可以利用硫(S ) 与CH 为原料制备 CS ,S8受热分解成气态 S , 发生反应 2S(g)+CH (g) =CS (g)
8 4 2 2 4 2
+2H S(g), 某温度下,若S 完全分解成气态S 。在恒温密闭容器中,S 与 CH 物质的量比为2:1时开始反
2 8 2 2 4
应。
①当CS 的体积分数为10%时,CH 的转化率为
2 4
②当以下数值不变时,能说明该反应达到平衡的是 (填序号)。
a.气体密度 b. 气体总压 c.CH 与S 体积比 d.CS 的体积分数
4 2 2
③一定条件下,CH 与 S 反应中 CH 的平衡转化率、S 分解产生 S 的体积分数随温度的变化由线如下图所
4 2 2 8 2
示,据图分析,生成 CS 的反应为 (填“放热”或“吸热”)反应。工业上通常采用在600~
2
650℃的条件下进行此反应,不采用低于600℃的原因是 。
Ⅱ.回收单质硫和回收H S。
2
(4)回收单质硫。将三分之一的H S燃烧。产生的SO 与其余H S混合反应:2H S(g)+SO (g) S (s)
2 2 2 2 2 8
+2H O(g)。在某温度下达到平衡,测得密闭系统中各组分浓度分别为c(H S)=2.0×10-5mol/L,c(SO )=5.0×10-
2 2 25mol/L,c(H O)=4.0×10-3mol/L,计算该温度下的平衡常数K= ;
2
(5)回收H S。用一定浓度Na S溶液吸一定量的H S,当溶液中c(H S)=c(S2-)时,溶液pH= (用含m、
2 2 2 2
n的式子)。(已知H S的两步电离常数K =m,K =n)
2 a1 a2
11.(2024·山东潍坊·二模)深入研究碳、氮元素的物质转化有着重要的实际意义,汽车尾气净化装置中
CO和NO发生如下反应:
ⅰ. ,
ⅱ. ,
ⅲ. ,
回答下列问题:
(1)上述反应的 的线性关系如图所示。 (填“>”或“<”)0,反应
的 (用 、 表示)。
(2)一定温度下,在1L密闭容器中充入2mol CO、2mol NO和1mol ,初始总压强为 。反应
的 , , 、 分
别为正、逆反应速率常数。充分反应达平衡时压强为 (该温度下忽略反应ⅲ), 的物质的量为
1.25mol,则 。
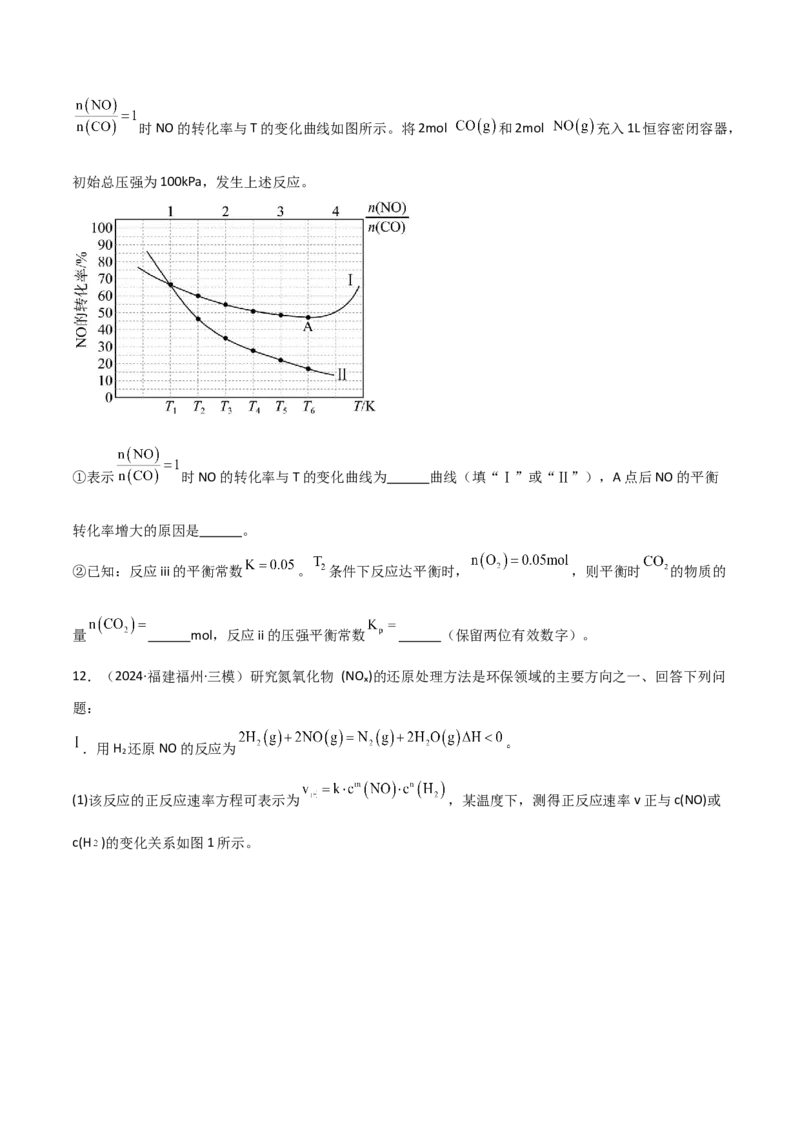
(3)CO和NO发生上述反应,在不同条件下达到平衡时,在 时NO的转化率与 的变化曲线及时NO的转化率与T的变化曲线如图所示。将2mol 和2mol 充入1L恒容密闭容器,
初始总压强为100kPa,发生上述反应。
①表示 时NO的转化率与T的变化曲线为 曲线(填“Ⅰ”或“Ⅱ”),A点后NO的平衡
转化率增大的原因是 。
②已知:反应iii的平衡常数 。 条件下反应达平衡时, ,则平衡时 的物质的
量 mol,反应ii的压强平衡常数 (保留两位有效数字)。
12.(2024·福建福州·三模)研究氮氧化物 (NOₓ)的还原处理方法是环保领域的主要方向之一、回答下列问
题:
.用H 还原NO的反应为
2
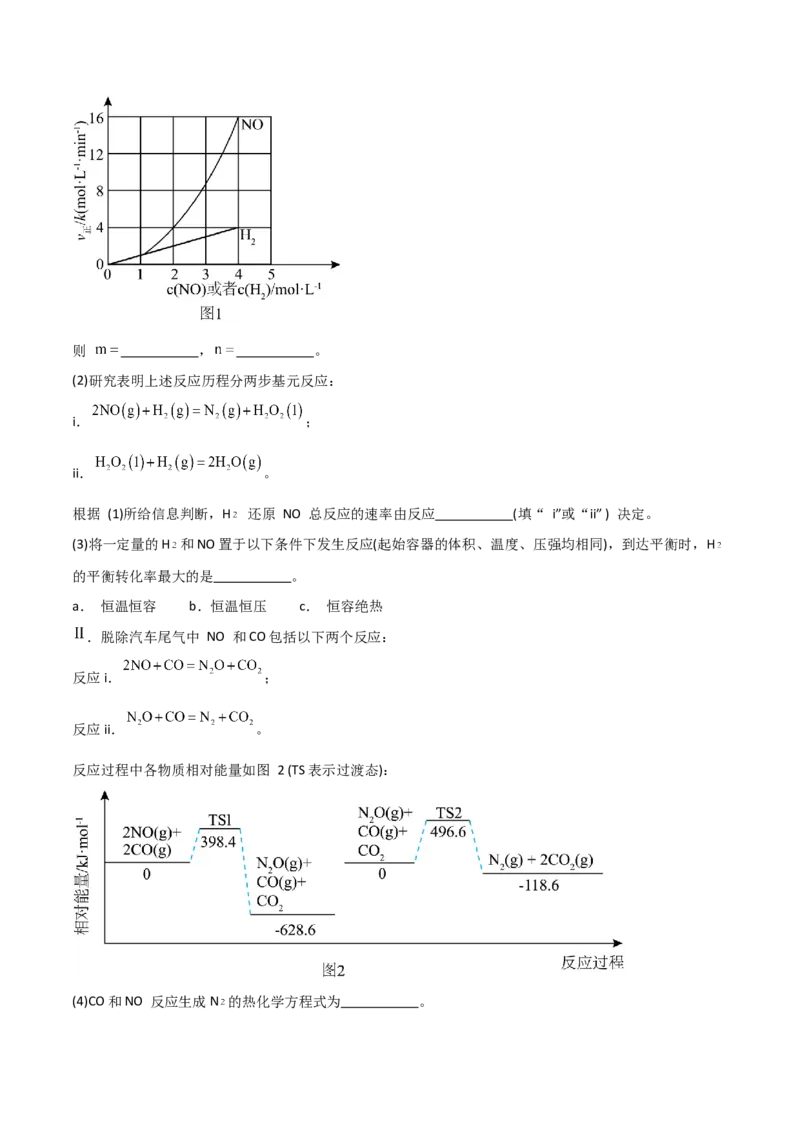
(1)该反应的正反应速率方程可表示为 ,某温度下,测得正反应速率v正与c(NO)或
c(H )的变化关系如图1所示。则 , 。
(2)研究表明上述反应历程分两步基元反应:
i. ;
ii. 。
根据 (1)所给信息判断,H 还原 NO 总反应的速率由反应 (填“ i”或“ii” ) 决定。
(3)将一定量的H 和NO置于以下条件下发生反应(起始容器的体积、温度、压强均相同),到达平衡时,H
的平衡转化率最大的是 。
a. 恒温恒容 b.恒温恒压 c. 恒容绝热
.脱除汽车尾气中 NO 和CO包括以下两个反应:
反应i. ;
反应ii. 。
反应过程中各物质相对能量如图 2 (TS表示过渡态):
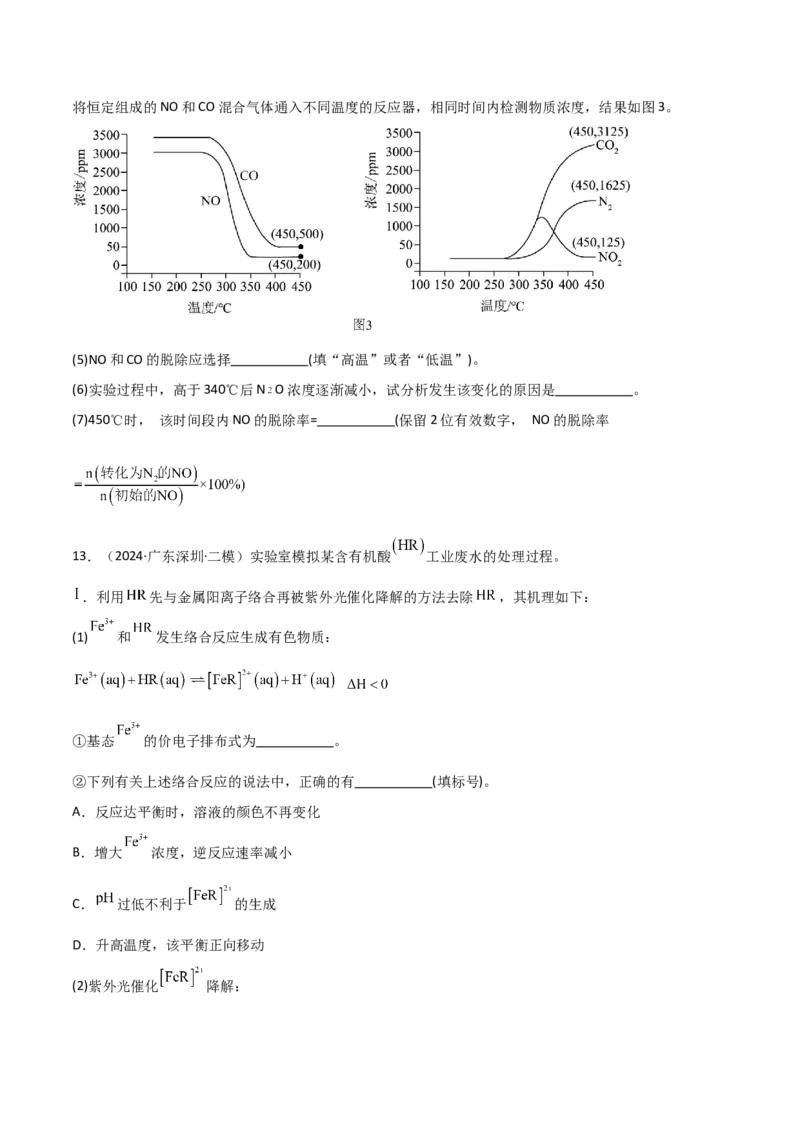
(4)CO和NO 反应生成N 的热化学方程式为 。将恒定组成的NO和CO混合气体通入不同温度的反应器,相同时间内检测物质浓度,结果如图3。
(5)NO和CO的脱除应选择 (填“高温”或者“低温”)。
(6)实验过程中,高于340℃后N O浓度逐渐减小,试分析发生该变化的原因是 。
(7)450℃时, 该时间段内NO的脱除率= (保留2位有效数字, NO的脱除率
13.(2024·广东深圳·二模)实验室模拟某含有机酸 工业废水的处理过程。
.利用 先与金属阳离子络合再被紫外光催化降解的方法去除 ,其机理如下:
(1) 和 发生络合反应生成有色物质:
①基态 的价电子排布式为 。
②下列有关上述络合反应的说法中,正确的有 (填标号)。
A.反应达平衡时,溶液的颜色不再变化
B.增大 浓度,逆反应速率减小
C. 过低不利于 的生成
D.升高温度,该平衡正向移动
(2)紫外光催化 降解:若有机酸为 ,则光催化降解反应的离子方程式为: 。
___________ ___________ ___________
___________
.利用有机溶剂从废水中萃取 的方法去除 。该过程涉及以下反应:
(i)
(ii)
(iii)
(3)根据盖斯定律,反应 (有机相)的 。
(4)水相的 以及体系温度 对 的平衡分配比 有影响。
已知: 。
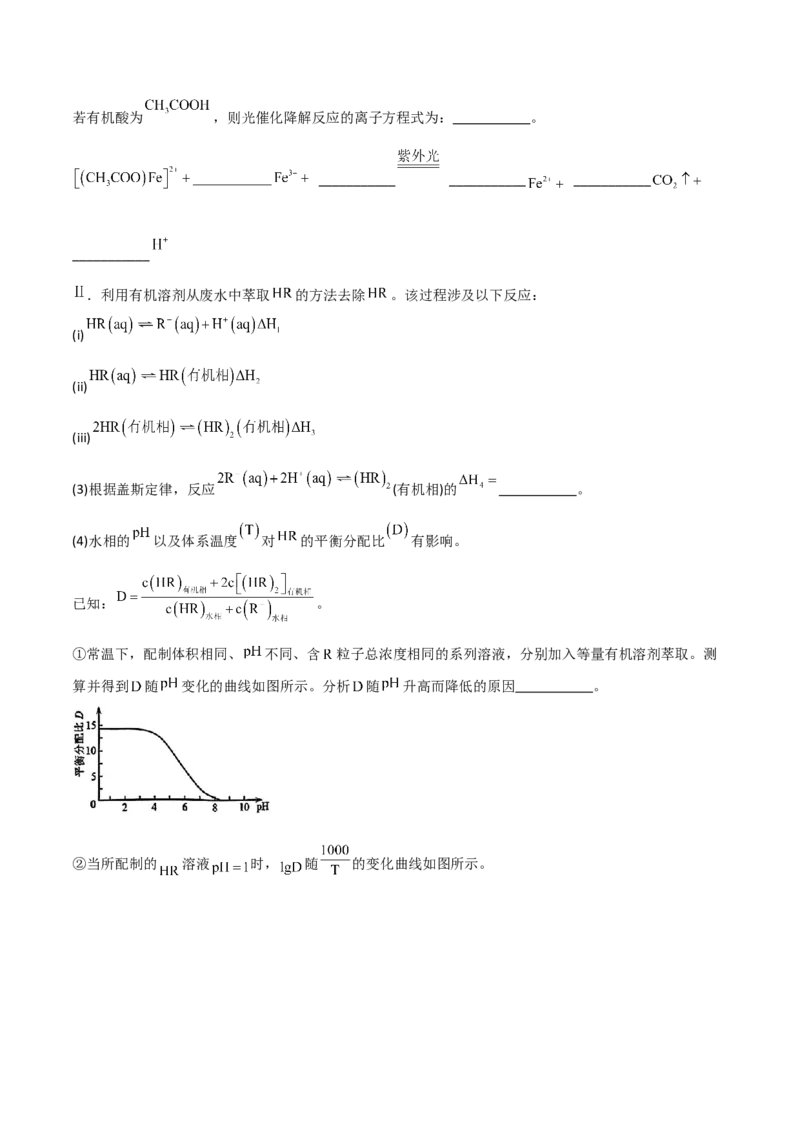
①常温下,配制体积相同、 不同、含 粒子总浓度相同的系列溶液,分别加入等量有机溶剂萃取。测
算并得到 随 变化的曲线如图所示。分析 随 升高而降低的原因 。
②当所配制的 溶液 时, 随 的变化曲线如图所示。萃取宜在 温度下进行(填“较高”或“较低”)。
经测定,在图中 点对应温度下,反应(ii)平衡常数 ,忽略水相中 的电
离,则有机相中 ;计算该温度下,反应(iii)的平衡常数 (写
出计算过程)。
14.(2024·重庆·模拟预测)回收、处理NO 是环境科学研究的重要课题,常用的处理方式有多孔材料吸
2
附法和CH 还原法等。
4
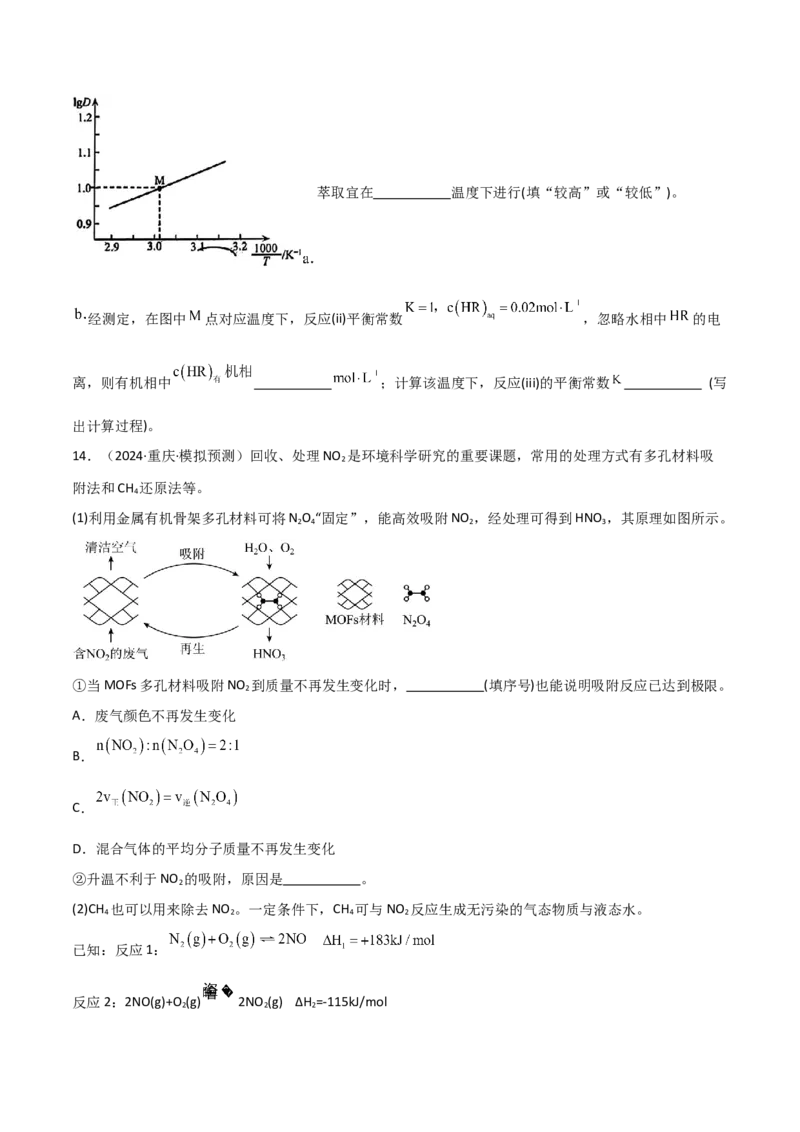
(1)利用金属有机骨架多孔材料可将N O “固定”,能高效吸附NO ,经处理可得到HNO ,其原理如图所示。
2 4 2 3
①当MOFs多孔材料吸附NO 到质量不再发生变化时, (填序号)也能说明吸附反应已达到极限。
2
A.废气颜色不再发生变化
B.
C.
D.混合气体的平均分子质量不再发生变化
②升温不利于NO 的吸附,原因是 。
2
(2)CH 也可以用来除去NO 。一定条件下,CH 可与NO 反应生成无污染的气态物质与液态水。
4 2 4 2
已知:反应1:
反应2:2NO(g)+O (g) 2NO (g) ∆H =-115kJ/mol
2 2 2①已知CH 的燃烧热为890.3kJ/mol,则 ∆H=
4
kJ/mol。
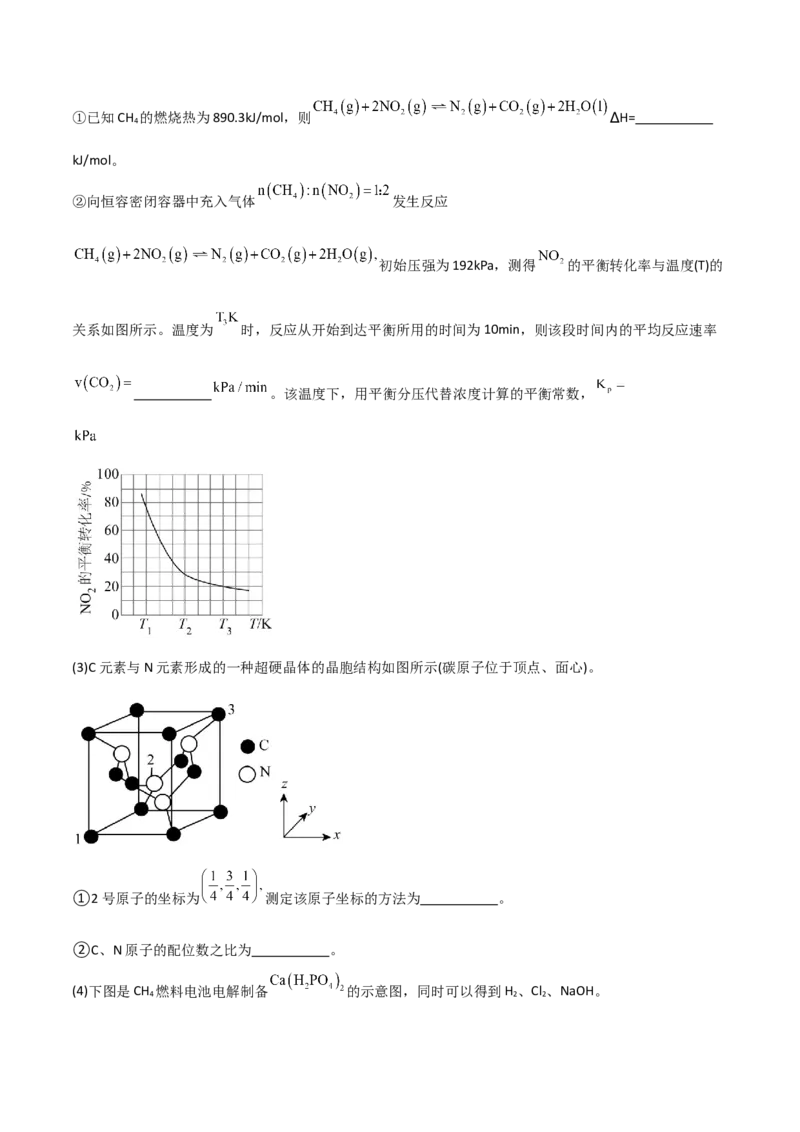
②向恒容密闭容器中充入气体 发生反应
初始压强为192kPa,测得 的平衡转化率与温度(T)的
关系如图所示。温度为 时,反应从开始到达平衡所用的时间为10min,则该段时间内的平均反应速率
。该温度下,用平衡分压代替浓度计算的平衡常数,
(3)C元素与N元素形成的一种超硬晶体的晶胞结构如图所示(碳原子位于顶点、面心)。
①2号原子的坐标为 测定该原子坐标的方法为 。
②C、N原子的配位数之比为 。
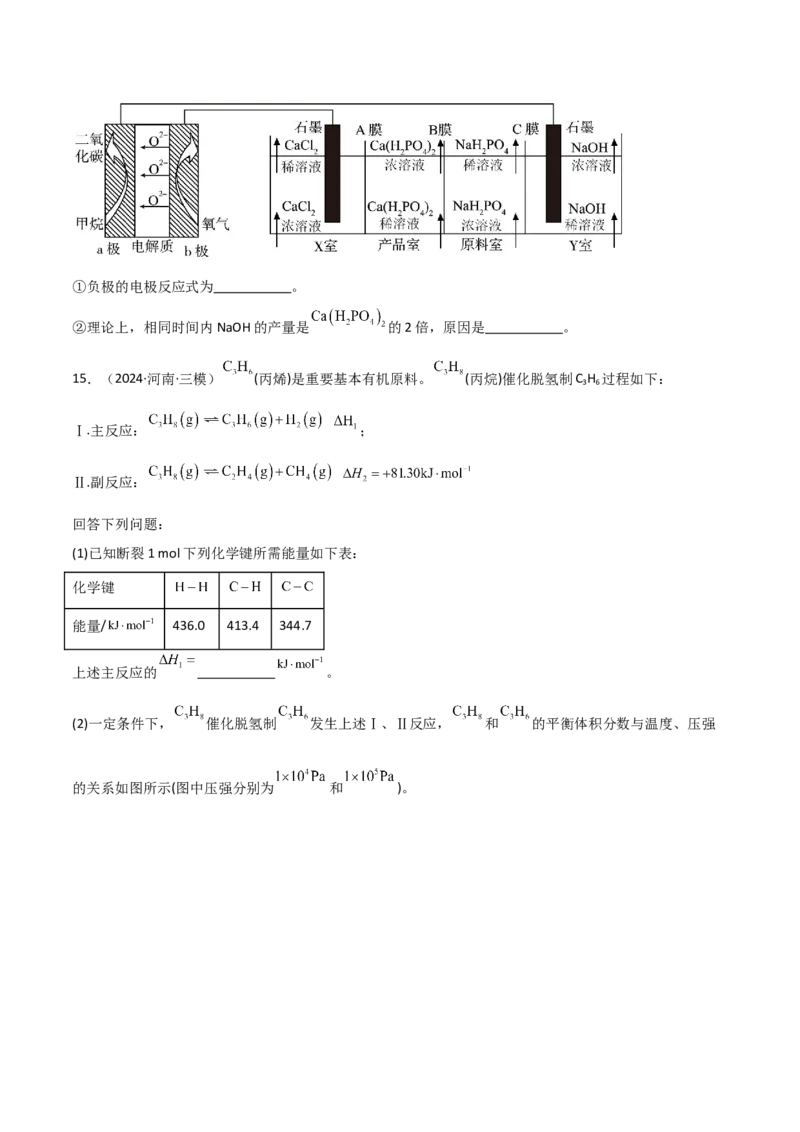
(4)下图是CH 燃料电池电解制备 的示意图,同时可以得到H 、Cl 、NaOH。
4 2 2①负极的电极反应式为 。
②理论上,相同时间内NaOH的产量是 的2倍,原因是 。
15.(2024·河南·三模) (丙烯)是重要基本有机原料。 (丙烷)催化脱氢制C H 过程如下:
3 6
Ⅰ.主反应: ;
Ⅱ.副反应:
回答下列问题:
(1)已知断裂1 mol下列化学键所需能量如下表:
化学键
能量/ 436.0 413.4 344.7
上述主反应的 。
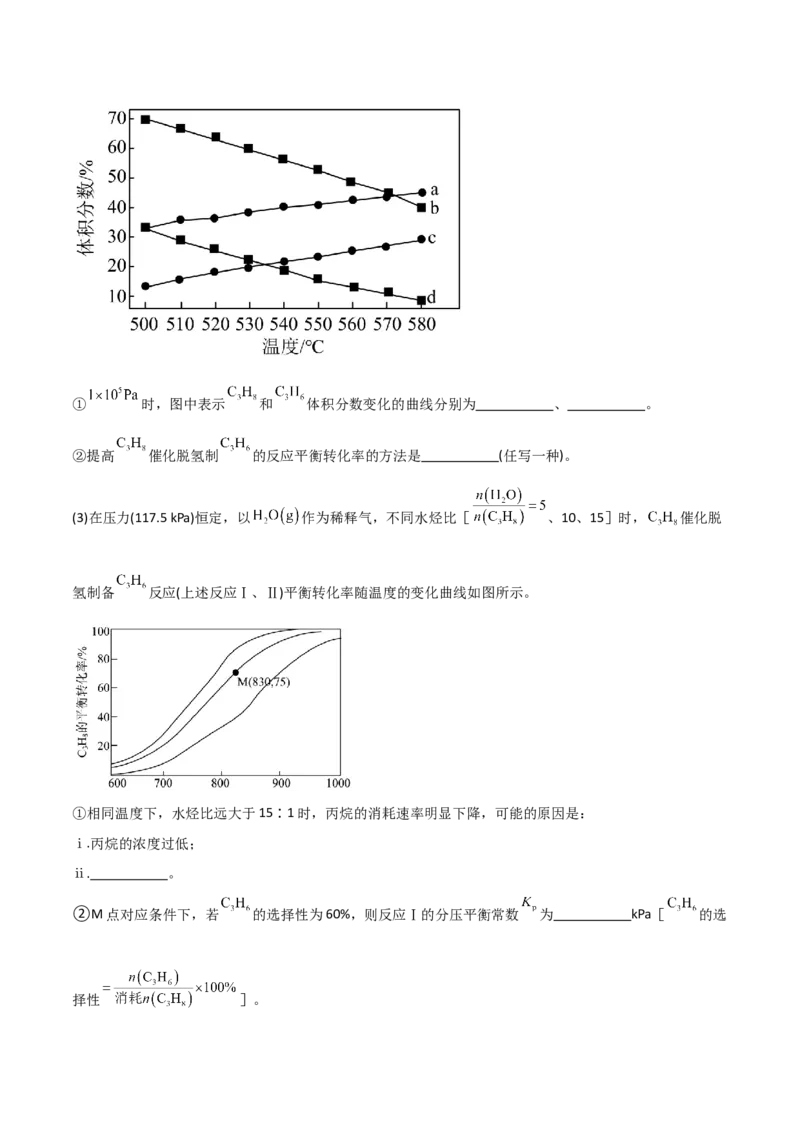
(2)一定条件下, 催化脱氢制 发生上述Ⅰ、Ⅱ反应, 和 的平衡体积分数与温度、压强
的关系如图所示(图中压强分别为 和 )。① 时,图中表示 和 体积分数变化的曲线分别为 、 。
②提高 催化脱氢制 的反应平衡转化率的方法是 (任写一种)。
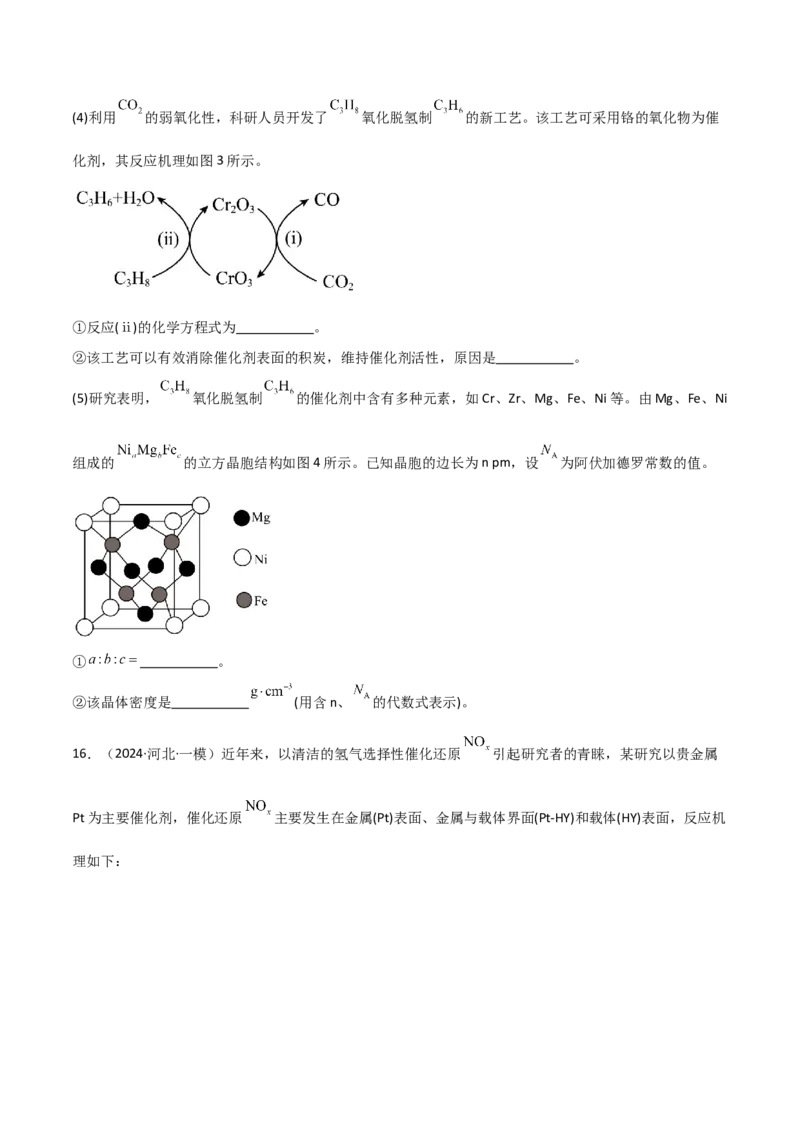
(3)在压力(117.5 kPa)恒定,以 作为稀释气,不同水烃比[ 、10、15]时, 催化脱
氢制备 反应(上述反应Ⅰ、Ⅱ)平衡转化率随温度的变化曲线如图所示。
①相同温度下,水烃比远大于15∶1时,丙烷的消耗速率明显下降,可能的原因是:
ⅰ.丙烷的浓度过低;
ⅱ. 。
②M点对应条件下,若 的选择性为60%,则反应Ⅰ的分压平衡常数 为 kPa[ 的选
择性 ]。(4)利用 的弱氧化性,科研人员开发了 氧化脱氢制 的新工艺。该工艺可采用铬的氧化物为催
化剂,其反应机理如图3所示。
①反应(ⅱ)的化学方程式为 。
②该工艺可以有效消除催化剂表面的积炭,维持催化剂活性,原因是 。
(5)研究表明, 氧化脱氢制 的催化剂中含有多种元素,如Cr、Zr、Mg、Fe、Ni等。由Mg、Fe、Ni
组成的 的立方晶胞结构如图4所示。已知晶胞的边长为n pm,设 为阿伏加德罗常数的值。
① 。
②该晶体密度是 (用含n、 的代数式表示)。
16.(2024·河北·一模)近年来,以清洁的氢气选择性催化还原 引起研究者的青睐,某研究以贵金属
Pt为主要催化剂,催化还原 主要发生在金属(Pt)表面、金属与载体界面(Pt-HY)和载体(HY)表面,反应机
理如下:(1)在金属Pt表面,NO被还原为 ,NO在空气中容易和氧气发生反应,结合下表数据,请写出NO
与 反应的热化学方程式: 。
物质
1mol物质中化学键断裂所需要的能量/kJ 631 498 937
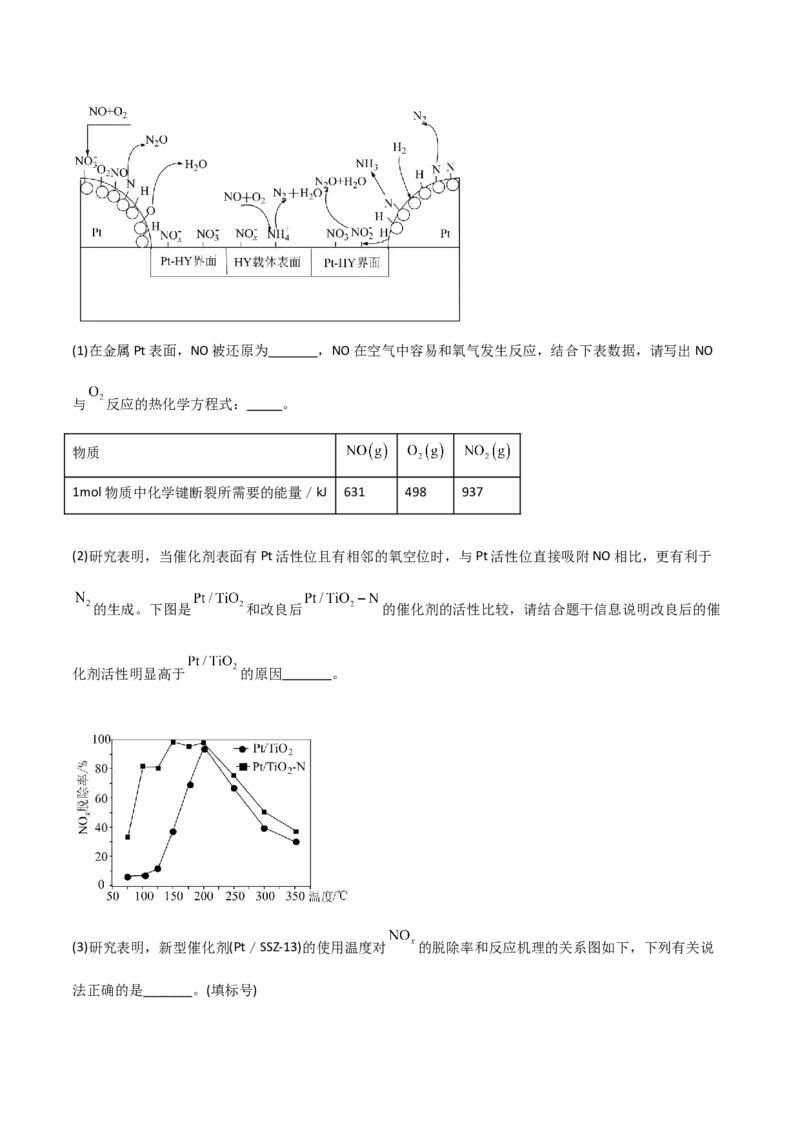
(2)研究表明,当催化剂表面有Pt活性位且有相邻的氧空位时,与Pt活性位直接吸附NO相比,更有利于
的生成。下图是 和改良后 的催化剂的活性比较,请结合题干信息说明改良后的催
化剂活性明显高于 的原因 。
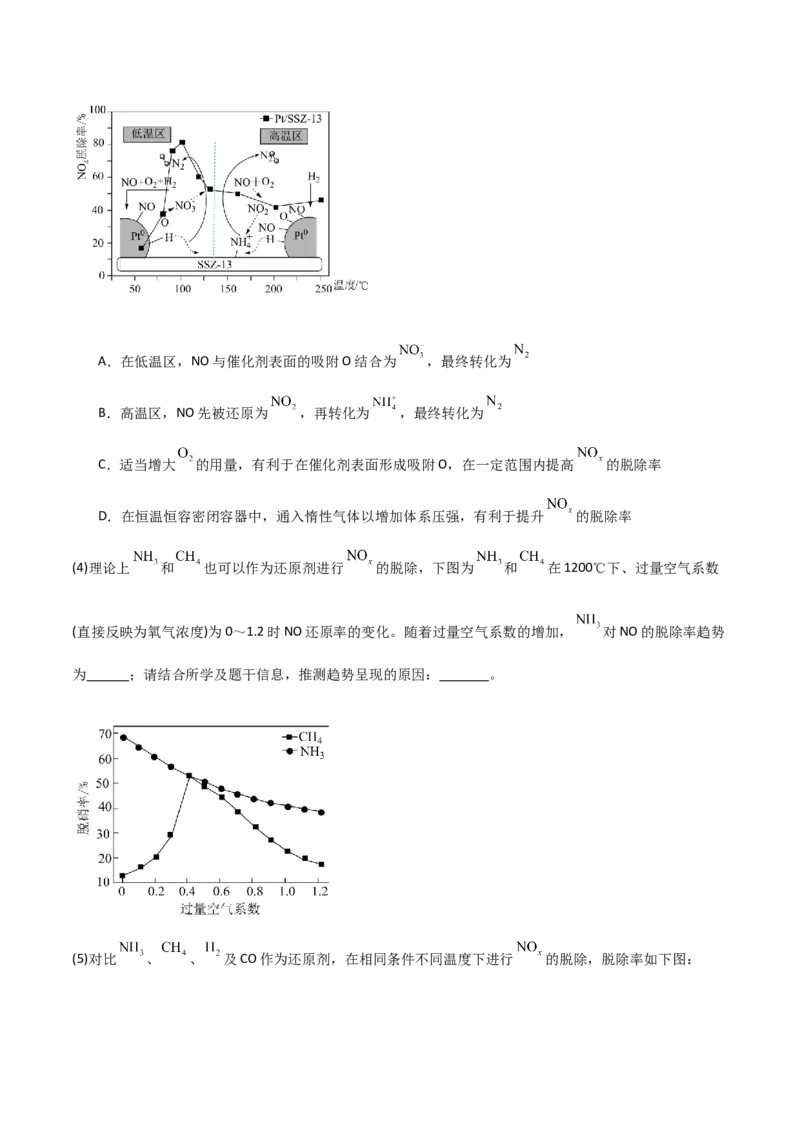
(3)研究表明,新型催化剂(Pt/SSZ-13)的使用温度对 的脱除率和反应机理的关系图如下,下列有关说
法正确的是_______。(填标号)A.在低温区,NO与催化剂表面的吸附O结合为 ,最终转化为
B.高温区,NO先被还原为 ,再转化为 ,最终转化为
C.适当增大 的用量,有利于在催化剂表面形成吸附O,在一定范围内提高 的脱除率
D.在恒温恒容密闭容器中,通入惰性气体以增加体系压强,有利于提升 的脱除率
(4)理论上 和 也可以作为还原剂进行 的脱除,下图为 和 在1200℃下、过量空气系数
(直接反映为氧气浓度)为0~1.2时NO还原率的变化。随着过量空气系数的增加, 对NO的脱除率趋势
为 ;请结合所学及题干信息,推测趋势呈现的原因: 。
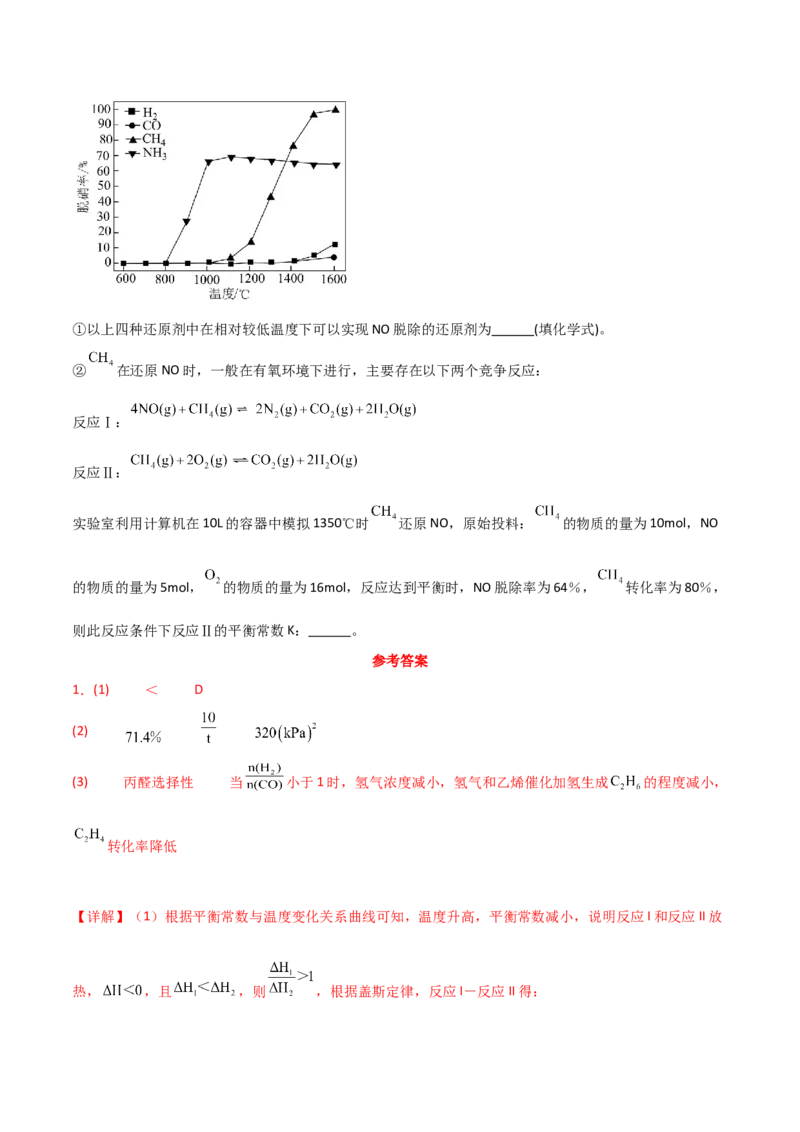
(5)对比 、 、 及CO作为还原剂,在相同条件不同温度下进行 的脱除,脱除率如下图:①以上四种还原剂中在相对较低温度下可以实现NO脱除的还原剂为 (填化学式)。
② 在还原NO时,一般在有氧环境下进行,主要存在以下两个竞争反应:
反应Ⅰ:
反应Ⅱ:
实验室利用计算机在10L的容器中模拟1350℃时 还原NO,原始投料: 的物质的量为10mol,NO
的物质的量为5mol, 的物质的量为16mol,反应达到平衡时,NO脱除率为64%, 转化率为80%,
则此反应条件下反应Ⅱ的平衡常数K: 。
参考答案
1.(1) < D
(2)
(3) 丙醛选择性 当 小于1时,氢气浓度减小,氢气和乙烯催化加氢生成 的程度减小,
转化率降低
【详解】(1)根据平衡常数与温度变化关系曲线可知,温度升高,平衡常数减小,说明反应I和反应II放
热, ,且 ,则 ,根据盖斯定律,反应I-反应II得:;
(2)设 物质的量均为1mol,初始气体总物质的量为3mol,初始总压强为
150kPa,平衡时p(C H )=p(C H )=20kPa,设平衡时 ,
2 4 2 6
,平衡时气体总的物质的量为(3a+1)mol,则
,a= ,平衡时气体总的物质的量为 mol,CH CH CHO(g)的选择性:
3 2
,初始气体总物质的量为3mol,初始总压强为150kPa,CO分压为50kPa,平衡时CO
分压为40kPa,反应速率: ;平衡时各物质分压为p(C H )=p(C H )=p(H )= 20kPa,n(CO)=40pkPa,
2 4 2 6 2
n(CH CH CHO)=50pkPa,反应Ⅰ的逆反应 ;
3 2
(3)根据反应I、II方程式,氢气比例增大,反应Ⅰ、Ⅱ中 的转化率均增大,所以曲线b表示 的
转化率,曲线a表示丙醛选择性;当 小于1时,氢气浓度减小,氢气和乙烯催化加氢生成 的程度减小, 转化率降低。
2.(1) -174.3 K /K
1 2
(2)B
(3)<
(4) Cat1 温度过高,催化剂失去活性
(5) 该反应为气体分子数增大的反应,恒压下通入水蒸气,容器体积增大,相当于减小压强,使平衡
正向移动,可提高乙烯转化率 34(或34kPa)
【详解】(1)根据盖斯定律反应③=反应②-反应①,所以:C H (g)+2H (g) C H (g) ∆H=∆H-
2 2 2 2 4 3 2
∆H=-174.3kJ/mol,而平衡常数K =K /K ;
1 3 2 1
(2)从吸附到解吸的过程中,甲烷的裂解为吸热反应,甲烷分子活化需要吸收能量,所以能量状态最高
的是B;
(3)反应②为吸热反应。根据平衡定义,平衡时正、逆反应速率相等,故v = v ,即k c2(CH ) = k
正 逆 正 4
·c(C H )·c2(H ), ,T 到T ℃时,K由1.5变成3,正反应为吸热反应,升高温度,平衡常数增大,故
逆 2 4 2 1 2
T 。④b点 , 的平衡转化率是80%,设开始投入氢气4mol,则 为1mol, 转化了0.8mol, ,平衡时气体总
物质的量为 , 。
5.(1)温室效应
(2) -121.9 H 、CO 甲醇分子间存在氢键
2 2
(3) 210 催化剂活性降低,反应平衡向逆向移动或有副反应发生等(合理答案均可)
(4) 阳 2Li CO +C-4e-=4Li++3CO
2 3 2
↑
【详解】(1)空气中CO 含量过高会导致全球变暖,两极冰川融化,海平面升高,则造成的环境问题是:
2
温室效应。
(2)(ⅰ)H (g)+CO (g) H O(g)+CO(g) H=+41.2kJ·mol-1
2 2 2 2
△
(ⅱ)3H (g)+3CO(g) CH OCH (g)+CO (g) H=-245.5kJmol-1
2 3 3 2 2
△ ∙
①利用盖斯定律,将反应ⅰ×3+ⅱ得:6H (g)+2CO (g) CH OCH (g)+3H O(g) H=(+41.2kJ·mol-1)×3+
2 2 3 3 2 3
△
(-245.5kJ·mol-1)= -121.9kJ·mol-1
②上述反应涉及的分子有H 、CO 、CO、H O、CH OCH ,H O、CH OCH 的中心O原子都存在孤电子对,都
2 2 2 3 3 2 3 3
为极性分子,则属于非极性分子的是H 、CO 。甲醇分子为含有-OH,能形成氢键,则甲醇的沸点(64.7℃)
2 2
高于二甲醚的沸点(-29.5℃),原因是:甲醇分子间存在氢键。
(3)①从图中可以看出,在210 时,甲醇的时空收率最高,则该反应最适宜的温度是210℃。
②随着温度升高,反应速率加快,℃甲醇的时空收率增大。210℃时,可能是催化剂的活性达到最佳,可能
是反应已达到平衡,则继续升高温度,甲醇的时空收率反而降低的原因可能是:催化剂活性降低,反应平
衡向逆向移动或有副反应发生等(合理答案均可)。
(4)Li/CO 电池放电时,a为负极,发生反应式4Li-4e-=4Li+,b电极为正极,电极反应式为3CO +4e-
2 2+4Li+=C+2Li CO 。
2 3
①由分析可知,放电时,a极生成Li+,b极消耗Li+,则Li+经过离子交换膜从左侧移向右侧,所以离子交换
膜为阳离子交换膜。
②充电时,b电极为阳极,C失电子产物与Li CO 反应生成CO 、Li+,电极反应式为2Li CO +C-4e-=4Li+
2 3 2 2 3
+3CO ↑。
2
【点睛】对于由两种元素组成的多原子分子,若中心原子存在孤电子对,则分子结构不对称,为极性分子。
6.(1) BC
(2)
(3)1.5
(4)BD
(5)ab
【详解】(1)①焓变=反应物总键能-生成物总键能,
;
②
A.升高温度,平衡向着吸热方向进行,反应i为吸热反应,则升温平衡正向进行,NO浓度增大,A错误;
B.移除NO ,平衡ii向正向进行,NO浓度降低,B正确;
2
C.降低N 浓度,平衡逆向进行,消耗NO,NO浓度降低,C正确;
2
③, ,
;
(2)根据始末状态判断反应物中氨气被氧化生成氮气,次氯酸被还原生成氯化钠,根据得失电子守恒,
化学方程式: ;
(3)当去除率较高时,余氯量较低,说明去除效果最佳,则除氨气过程中最佳 值约为1.5;
(4)A.加水稀释过程中,温度不变, 不变,A错误;
B.加水稀释过程中,温度不变, 不变,稀释过程中 减小,则 减
小,B正确;
C.加水稀释,氨水碱性减弱, 增大,C错误;
D.加水稀释,氨水碱性减弱, 增大, 减小, 减小,D正确;
(5)a.由反应历程图可知,活化能:反应ⅰ<反应ⅱ,正确;
b.由反应历程图可知,反应i正反应的反应物总能量高于生成物总能量,ⅰ为放热反应,反应ii正反应反
应物总能量低于生成物总能量,ⅱ为吸热反应,正确;
c.由反应历程图可知,反应i: ,反应ii: ,根据盖斯定律:i+ii得
,错误。7.(1)
(2)A
(3)4%
(4) 400℃ 其他条件不变,升温,活化分子百分数增大,反应速率增大 未达到 相同温
度时,不同催化剂下氮氧化物转化率还能增大 催化剂活性降低(或其他合理答案)
(5)
【详解】(1)① kJmol
⋅
② kJmol
⋅
根据盖斯定律(①+②)÷6得 kJmol 。
⋅
(2)A.反应前后气体系数和不同,恒温、恒容条件下,压强是变量,压强不随时间变化时反应达到平衡
状态,一定是平衡状态,故A正确;
B.平衡常数只与温度有关,平衡时温度不变,再充入1 mol 时平衡常数不变,故B错误;
C.该反应可逆,反应达到平衡时生成氮气的物质的量小于0.5mol,放出的热量小于0.1a kJ,故C错误;
D.催化剂不能使平衡移动,加入高效催化剂,反应达到平衡时NO的转化率不变,故D错误;
选A。
(3)根据图示,使用催化剂4% ,单位时间内氮氧化物转化率、表面活泼氧量比
最大,所以催化效能最佳的催化剂组成是4% 。
(4)①温度为400℃时,单位时间内氮氧化物的转化率最大,所以最佳反应温度为400℃。
②其他条件不变,升温,活化分子百分数增大,反应速率增大,所以a→b段氮氧化物转化率升高。
③相同温度时,M点氮氧化物的转化率不是最大,不同催化剂下氮氧化物转化率还能增大,所以M点反应
未达到平衡状态;温度升高,催化剂活性降低,所以M→N段氮氧化物转化率降低。
(5)设参加反应①的NO的物质的量为amol、参加反应②的NO的物质的量为bmol,则反应生成N 的物
2质的量为 、反应生成N O的物质的量为 , ,解得a=0.6、b=0.8;参加反应①的NH
2 3
的物质的量为0.4mol、参加反应②的NH 的物质的量为0.2mol,反应剩余氨气的物质的量为0.4mol、剩余
3
NO的物质的量为0.6mol;反应①生成的水的物质的量为0.6mol、反应②生成的水的物质的量为0.3mol,
容器中水的物质的量为0.9mol,反应①的平衡常数 mol·L 。
8.(1) 放热 3d5 4NH +4NO+O 4N +6H O
3 2 2 2
(2) 催化剂活性降低 6.0×10-5mol/(Lmin)
(3) A 3.25
【详解】(1)①由图可知反应物的总能量高于生成物的总能量,为放热反应;
②Fe的价电子排布式为3d64s2,而Fe3+失去3个电子,因此为3d5
③由图可知,反应物为氨气、一氧化氮、氧气、生成物为氮气和水,则脱硝的总反应为
;
(2)①催化剂的活性受温度的影响,温度升高催化剂的活性可能降低,因此转化率减小;
②由图可知100℃-300℃之间,NO的最高转化率为60%,故NO的变化量为2.0 10-4 60%=1.2 10-4mol,由
公式可知为 ;
(3)①当初始氨碳比相同,水碳比越大,二氧化碳的转化率越小,根据图中信息可知,曲线A二氧化碳
转化率大于B曲线,则W较小的曲线A。
②N点氨碳比为3,初始水碳比为0,二氧化碳的转化率为75%,设初始氨气物质的量为3a mol,平衡时总物质的量为3.25a mol,则
9.(1) 9 O>P>Ag
(2) pH越大,氢氧根离子浓度越大,
, ,磷酸根浓度越大,加入硝酸银生成 的速率越快,
根据已知ⅱ.一般情况,析晶速率越快,晶粒尺寸越小,故pH较大时,样品A的晶粒小; AC
(3) 体系中 由 第一步电离决定,则
故
由图可知, , ,
故 mol/L
【详解】(1)P为15号元素,其电子排布式为:1s22s22p63s23p3,则其核外电子的空间运动状态有
1+1+3+1+3=9;元素的非金属性越强,其电负性越大,由于非金属性O>P>Ag,故电负性:O>P>Ag;
(2)①根据银氨溶液的溶质为:Ag(NH ) OH以及元素守恒可知,该反应的离子方程式为:
3 2
;
②pH越大,氢氧根离子浓度越大, , ,磷酸根浓度越大,加入硝酸银生成 的速率越快,根据已知ⅱ.一般情况,析晶速率越快,晶粒尺寸越小,故pH较大
时,样品A的晶粒小;
③A.pH增大,氢氧根浓度增大,此时生成的氢氧化银不稳定生成Ag O,故样品A中 杂质含量最高,
2
A正确;
B.加入盐酸,含有氯离子,会生成氯化银沉淀,则不能用盐酸调控体系的pH,B错误;
C.由于 , ,加入硝酸银后会生成磷酸银,使电离平衡正向
移动,此时氢离子浓度增大,温度不变,K不变,则 减小,C正确;
D.向 溶液中加入少量 溶液时,此时银离子浓度增大,会生成 沉淀,此时溶液
pH和生成样品时相比较低,则晶体尺寸不同,D错误;
故选AC;
(3)① 溶液与0.2 溶液等体积混合中c(Ag+)=0.1mol/L,由于
,则刚开始生成 沉淀时,溶液中的
;
②由于 的一级电离常数大于二级电离常数,则当氢离子浓度相同时 较大,而 较
小,则 较大,故b代表 与pH的关系,根据图示可知,当pH=4.1时,,则 ;
③体系中 由 第一步电离决定,则
故
结合②的方法可知, , ,
故 mol/L。
10.(1)+234kJ/mol
(2) 直线型
(3) 30% d 放热 600℃时甲烷的平衡转化率高达99%,低于600℃时,S 的浓度明显偏小,
2
且反应速率慢
(4)8×188L/mol
(5)
【详解】(1)由盖斯定律,总反应=①+②,故ΔH=ΔH +ΔH =+170kJmol-1+64kJmol-1=+234kJ/mol;
1 2
(2)
CH 的电子式为 ;CS 分子中中心原子的杂化类型为sp杂化,立体构型为直线型;
4 2
(3)①在恒温密闭容器中,S 与CH 物质的量比为2∶1时开始反应,由三段式
2 4得,当CS 的体积分数为10%时,即 ,
2
,CH 的转化率为 ;②a.恒容容器,质量不变,故密度一直不变,故密度不变不
4
一定平衡,a错误;b.反应前后气体的物质的量不变,故压强也一直不变,故压强不变一定平衡,b错误;
c.CH 与S 体积比一直为1:2,故不一定平衡,c错误;d.CS 的体积分数说明反应已经达到了平衡,d正确;
4 2 2
③由图可知,随温度升高,甲烷的转化率降低,故反应为放热反应。工业上通常采用在600~650℃的条件
下进行此反应,不采用低于600℃的原因是;600℃时甲烷平衡转化率高达99%,低于600℃时,S 浓度明
2
显偏小,且反应速率慢;
(4)根据方程式可知,该温度下的平衡常数
;
(5)由 , ,则 ,
。
11.(1) >
(2)0.15
(3) Ⅰ 温度高于 时,随温度升高,反应iii正向反应程度变大,促进了反应ⅰ正向进行 0.8
0.67
【详解】(1)图像显示温度升高,pK 减小,即温度升高K 增大,所以升温反应iii正向移动,故 >
p3 p30;根据盖斯定律,反应iii-反应ii得反应 ,所以其K= ;
(2)该温度下忽略反应ⅲ,反应ⅱ. 左右两边气体化学计量数之和相
等,充分反应达平衡时压强为 ,所以平衡时n = ,即反应ⅰ.
总
的发生使得容器内气体物质的量减少(5-4.5)mol=0.5mol,由于反应ⅰ
左边的气体化学计量数比右边大1,所以反应ⅰ转化的n(CO)=n(CO )=n(N O)=0.5mol,转化的n(NO)=1mol,
2 2
三段式表示
,平衡时v =v ,又
正 逆
, ,所以 ,即
;
(3)① 越大,NO转化率越小,所以曲线Ⅱ表示NO的转化率与 的变化曲线,即曲线Ⅰ表
示 时NO的转化率与T的变化曲线;A点对应的温度为T ,A点后NO的平衡转化率增大的原因
6是反应iii为吸热反应,温度高于 时,随温度升高,反应iii正向反应程度变大,引起N O消耗,而N O为
2 2
反应ⅰ的生成物,所以反应iii正向反应程度变大后促进了反应ⅰ正向进行,从而使NO的平衡转化率增大;
②由图像可知, 、温度为T 时,NO的平衡转化率为60%,即NO的转化的物质的量为
2
2×60%=1.2mol,三段式表示 、
、
,反应iii的平衡常数 ,解得
x=0.2mol,则平衡时 的物质的量 (0.6+0.2)mol=0.8mol,反应ii的压强平衡常数
。
12.(1) 2 1
(2)i
(3)b
(4)2NO(g)+2CO(g)=N (g)+2CO (g) ΔH=-747.2 kJ·moL–1
2 2
(5)高温(6)反应i、ii速率随温度的升高而增大,高于 340℃后反应ii速率增加的程度超过反应i,所以 N O 浓度减
2
小
(7)88%
【详解】(1)由图可知 , ,所以 2, 1;
(2)因为 ,则反应速率主要由c(NO)决定,所以H 还原 NO 总反应的速率由反应i
决定;
(3)设恒温恒容时H 的平衡转化率为x,该反应是气体分子数减小的反应,恒温恒压时相对于恒温恒容
时,相当于增大压强,平衡正移,氢气转化率比x大,该反应是放热反应,恒容绝热时,混合气体温度升
高,相对于恒温恒容时,平衡逆移,氢气转化率小于x,所以氢气转化率最大的是恒温恒压时,选b;
(4)焓变等于生成物的能量与反应物的能量之差,所以 ΔH=-628.6 kJ·moL–1;
ΔH=-118.6kJ·moL–1;则根据盖斯定律知,CO和NO 反应生成N 的热化学方程式为:
2
2NO(g)+2CO(g)=N (g)+2CO (g) ΔH=-747.2 kJ·moL–1;
2 2
(5)由图知,NO和CO的浓度在高温时低,所以脱除应选择高温;
(6)因为反应i生成N O,反应ii消耗 N O,所以原因是:反应i、ii速率随温度的升高而增大,高于
2 2
340℃后反应ii速率增加的程度超过反应i,所以 N O 浓度减小
2
(7)根据氮元素守恒,NO的初始浓度为: ,转化为氮气的NO
的浓度为: ,NO的脱除率 。
13.(1)
(2) 8 2 7
(3)(4) 升高,反应(i)平衡正移,导致反应(ii)平衡逆移,平衡分配比下降 较低 图
中 点,lgD=1.0,则 ;反应(ii)平衡常数 ,则
, ,忽略水相中 的电离,则
,故 ,
,反应(iii)的平衡常数 为
【详解】(1)①铁原子失去3个电子形成铁离子,基态 的价电子排布式为 。
②A.反应达平衡时,各物质的浓度不再改变,溶液的颜色不再变化,正确;
B.增大 浓度,物质浓度增大,反应速率加快,则逆反应速率加快,错误;
C. 过低,使得平衡逆向移动,不利于 的生成,正确;
D.反应为放热反应,升高温度,该平衡逆向移动,错误;
故选AC;
(2)光催化降解反应中铁离子化合价由+3变为+2、碳元素化合价由0变为+4,结合电子守恒可知,反应
为: 8 2 7 ;
(3)由盖斯定律可知,2×(ii)+ (iii)-2×(i)得反应 (有机相),则;
(4)① 升高,促使反应(i)平衡正移,导致反应(ii)平衡逆移,使得有机相中HR减小,平衡分配比下降;
② 由图可知,萃取宜在较低温度下进行,此时 值较大,萃取效果较好。
图中 点,lgD=1.0,则 ;反应(ii)平衡常数 ,
则 , ,忽略水相中 的电离,则
,故 ,
,反应(iii)的平衡常数 为 。
14.(1) A、D ﹤0,该反应是放热反应,升温,平衡逆向移动,不利于NO 的
2
吸附。
(2) -958.3 1.28 0.2
(3) 以1号原子的坐标为(0,0,0) 4:3
(4) CH -8e-+4O2-=CO +2H O 当电路中转移2nmol的电子,Y室生成2nmol的NaOH,同时
4 2 2
nmolCa2+从X室移动到产品室,2nmol的 从原料室进入产品室,生成nmol的Ca(H PO ) 。
2 4 2
【详解】(1)①当MOFs多孔材料吸附NO 到质量不再发生变化时,即 反应达到平衡状态。
2
A.因为NO 为红棕色气体,因此反应达到平衡状态时,废气颜色不再发生变化,A正确;
2
B.当反应达到平衡状态时,各物质物质的量不再发生改变,n(NO )、n(N O )不变,B错误;
2 2 4
C.当反应达到平衡状态时,正逆反应速率相等,即 ,C错误;D.该反应体系反应前后气体系数和不相等,混合气体的平均分子质量不再发生变化可作为反应达到平衡
状态的标志,D正确。
①故答案为:A、D
② ﹤0,该反应是放热反应,升温,平衡逆向移动,不利于NO 的吸附;
2
②故答案为: ﹤0,该反应是放热反应,升温,平衡逆向移动,不利于NO 的吸附。
2
(2)①CH (g)+2O (g)=CO (g)+2H O(l)ΔH =-890.3kJ/mol,由盖斯定律可知,
4 2 2 2 3
ΔH=ΔH -ΔH -ΔH ,即ΔH=-958.3 kJ/mol;
3 1 2
①故答案为:-958.3
②已知向恒容密闭容器中充入气体 发生反应
初始压强为192kPa,温度为 时,由图1可知,
的平衡转化率为20%。
设充入n(CH )为nmol,则n(NO )为2nmol
4 2
P =204.8kPa
平衡
则10min内平均反应速率
用平衡分压代替浓度计算的平衡常数,
②故答案为:1.28,0.2(3)①2号原子位于体对角线的1/4位置,且坐标为 ,可知测定该原子坐标的方法是以1号原子
坐标为(0,0,0);
①故答案为:以1号原子的坐标为(0,0,0)
②根据晶胞结构可知,1个C周围等距且最近的N有4个,故C的配位数为4,同理1个N周围等距且最近
的C有3个,故N的配位数为3,因此C、N原子的配位数之比为4:3;
②故答案为:4:3
(4)①燃料电池的a电极通入甲烷为负极,则负极的电极反应式为CH -8e-+4O2-=CO +2H O;
4 2 2
①故答案为:CH -8e-+4O2-=CO +2H O
4 2 2
②当电路中转移2nmol的电子,Y室生成2nmol的NaOH,同时nmolCa2+从X室移动到产品室,2nmol的
从原料室进入产品室,生成nmol的Ca(H PO ) 。因此相同时间内NaOH的产量是 的
2 4 2
2倍。
②故答案为:当电路中转移2nmol的电子,Y室生成2nmol的NaOH,同时nmolCa2+从X室移动到产品室,
2nmol的从原料室进入产品室,生成nmol的Ca(H PO )
2 4 2
15.(1)+127.4
(2) b c 减压或升温
(3) 过多地占据催化剂表面,导致催化剂对丙烷的吸附率降低 8.1
(4) 炭与 反应生成CO,脱离催化剂表面
(5) 1∶3∶4
【详解】(1)设碳碳双键的键能为x,则由 得
, ,则主反应:
的(2)①升高温度,平衡正向移动,丙烷的体积分数减小,丙烯的体积分数增大,则a、c为丙烯的体积分
数变化曲线,b、d为丙烷的体积分数变化曲线, 与 相比,压强增大,平衡逆向移动,从
而得出表示丙烷体积分数的变化曲线为b,表示丙烯体积分数的变化曲线为c。
②丙烷直接催化脱氢制丙烯的反应正向是气体体积增大的吸热反应,改变外界条件时,化学平衡将向着减
弱这种改变量的方向移动,因此升高温度、降低压强均能使平衡正向移动,从而提高丙烷转化率;
(3)①相同温度下,水烃比远大于15∶1时,说明水蒸气多, 的浓度过低,反应速率减慢,另一方
面是 过多地占据催化剂表面,导致催化剂对丙烷的吸附率降低,也导致 的反应速率明显下降。
②M点对应的水烃比为10∶1,设 的物质的量为1 mol, 的物质的量为10 mol。 转化了
0.75 mol,根据 的选择性为60%知,生成 的物质的量为0.45 mol, 的物质的量为0.45 mol,
的物质的量为0.3 mol, 的物质的量为0.3mol。体系中总的物质的量为
。 、 、 的分压分别为2.5kPa、4.5kPa、
4.5kPa, ;
(4)①由图知,反应(ⅱ)的化学方程式为 ;
②由于炭与 反应生成CO,脱离催化剂表面,该工艺可以有效消除催化剂表面的积炭,维持催化剂活性;
(5)根据均摊法,晶体中Ni的个数为 ;Mg的个数为 ,Fe的个数为4,则 ,
中 , , ,则
16.(1)(2)改良后 的催化剂有更多的Pt活性位点和相邻的氧空位,更有利于吸附NO等氮氧化物,有
利于脱除反应快速进行
(3)AC
(4) 脱硝率逐渐降低 随着氧气浓度增大,氨气与氧气发生反应,生成氮氧化物,同时与氮氧化物
反应的氨气减少,导致脱硝率降低
(5) 400
【详解】(1)根据图片信息中的反应过程,Pt催化剂表面NO被还原为 ,故热化学反应方程式为
。
(2)根据信息提示,“研究表明,当催化剂表面有Pt活性位且有相邻的氧空位时,与Pt活性位直接吸附
NO相比,更有利于 的生成。”改良后催化剂效果更好的原因是:改良后的 催化剂有更多
Pt活性位和相邻的氧空位,更有利于吸附NO等氮氧化物,有利于脱除反应快速进行。
(3)A.由图左侧低温区可知,NO与催化剂表面的吸附O结合为 ,最终转化为 ,A正确;
B.由图右侧高温区可知,NO先被氧化为 ,再转化为 ,最终转化为 ,B错误;
C.适当增大 的用量,有利于在催化剂表面形成吸附O,在低温区时,会加快与NO的反应速率,提高
的脱除率,C正确;
D.恒温恒容体系充入惰性气体,对反应物和生成物浓度基本无影响,基本不改变氮氧化物脱除率,D错误。
故选AC。
(4)根据图示,随横坐标增大,脱硝率逐渐降低;在较高温度下,当氧气浓度达到一定程度时,氨气和
氧气反应,与氨气和一氧化氮反应形成竞争反应,氧气越多,氨气与一氧化氮反应越少,同时氨气和氧气
反应会生成氮的氧化物,使氮的氧化物浓度在一定程度上增加,脱硝率下降。
(5)温度较低时,氢气和一氧化碳的脱硝率非常低,不适合低温脱硝,氨气在800~1000℃左右时脱硝率
明显上升,优于甲烷,1350℃左右时甲烷和氨气脱硝率基本相同,温度继续升高,甲烷脱硝率上升,因此,在较低温度下时,氨气是比较适宜的还原剂。
根据投料及脱硝率64%、甲烷转化率80%,参加反应的甲烷为10×80%=8mol;三行式如下:
故 。