文档内容
易错点 1 化学用语
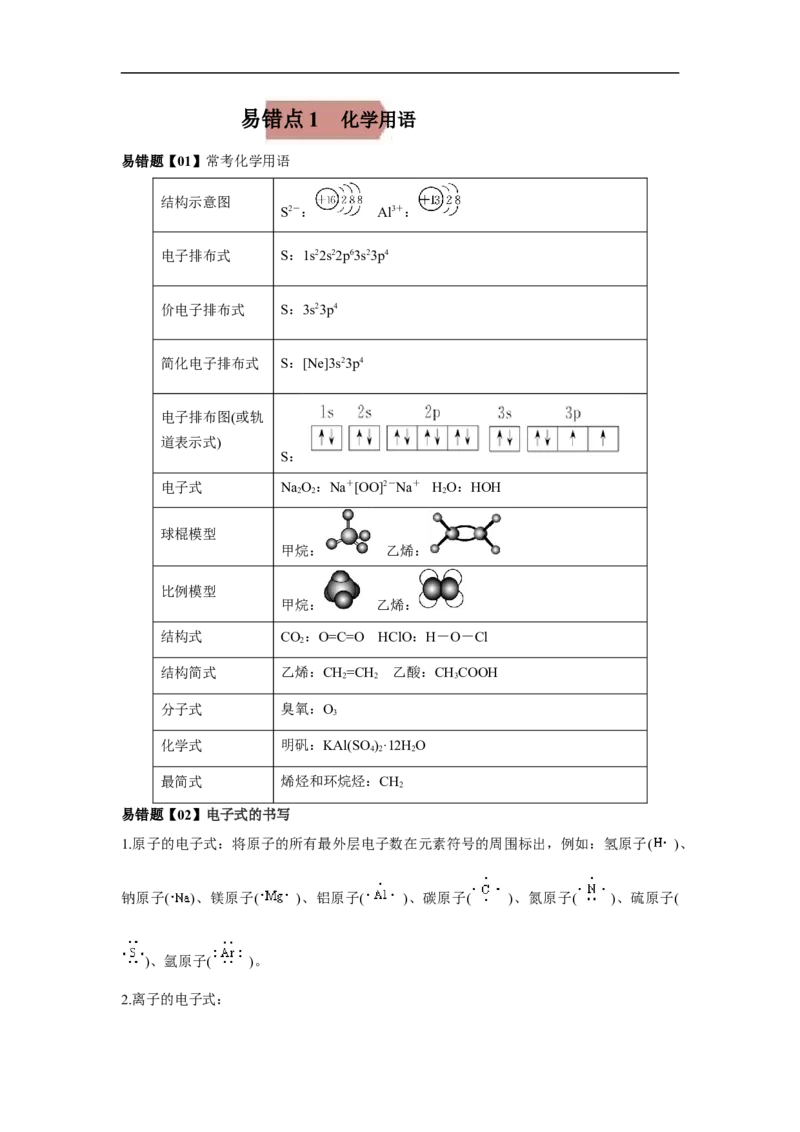
易错题【01】常考化学用语
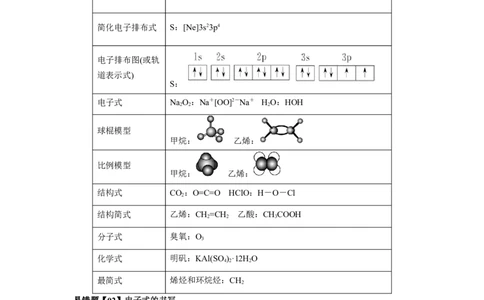
结构示意图
S2-: Al3+:
电子排布式 S:1s22s22p63s23p4
价电子排布式 S:3s23p4
简化电子排布式 S:[Ne]3s23p4
电子排布图(或轨
道表示式)
S:
电子式 NaO:Na+[OO]2-Na+ HO:HOH
2 2 2
球棍模型
甲烷: 乙烯:
比例模型
甲烷: 乙烯:
结构式 CO:O=C=O HClO:H-O-Cl
2
结构简式 乙烯:CH=CH 乙酸:CHCOOH
2 2 3
分子式 臭氧:O
3
化学式 明矾:KAl(SO )·12H O
4 2 2
最简式 烯烃和环烷烃:CH
2
易错题【02】电子式的书写
1.原子的电子式:将原子的所有最外层电子数在元素符号的周围标出,例如:氢原子( )、
钠原子( )、镁原子( )、铝原子( )、碳原子( )、氮原子( )、硫原子(
)、氩原子( )。
2.离子的电子式:(1)阴离子:在书写阴离子的电子式时,须在阴离子符号的周围标出其最外层的 8个电子
(H-为2个电子),外加方括号,再在括号外的右上角注明阴离子所带的电荷数,例如S2-的
电子式为[ ]2- ,OH-的电子式为 。
(2)阳离子:对于简单阳离子,其电子式即为阳离子符号,如钠离子 Na+、镁离子Mg2+
等,对于带正电荷的原子团,书写方法与阴离子类似,区别在于在方括号右上角标上阳离
子所带的正电荷数,如NH +电子式为 。
4
3.离子化合物的电子式:离子化合物电子式的书写,是将阴阳离子(阳离子在前,阴离子在
后)拼在一起,对于不同价态的离子,也按其绝对值,遵照“大值在中间、小值在周边”的
原则书写,如CaCl 的电子式应为 。
2
4.共价型单质分子:必须正确地表示出共用电子对数,并满足每个原子的稳定结构,例如:
。
5.共价化合物:共价化合物电子式的书写,基本与共价型单质分子相同,一般为正价者在
前。对于不同价态的元素的原子,一般将化合价绝对值大的写在中间,绝对值小的写在周
边,例如: 。
易错题【03】化学用语常见错误
(1)结构简式需保留官能团,如CH===CH ,不能写成CHCH ,还要注意有机物中原子
2 2 2 2
的连接情况,如—NO ,不能写成—ON。
2 2
(2)各“式”切勿张冠李戴:名称还是化学式、分子式还是实验式、结构式还是结构简式、
原子还是离子结构示意图、化学方程式还是离子方程式等。
(3)化学方程式或离子方程式要遵守质量守恒,化学计量数要最简,注明反应条件并注意
“↑”“↓”“”“===”“―→”符号的使用。
(4)化学专用名词书写错误。如“铵盐”写成“氨盐”,“油脂”写成“油酯”,“酯
化”写成“脂化”,“苯”写成“笨”,“硝化”写成“消化”等。
(5)电子式书写错误:书写化合物的电子式时要切实注意明确离子化合物还是共价化合物;
切勿漏掉未成键电子对;理清原子的排列顺序,如HOCl。(6)混淆物质组成的几种表达方法:任何纯净物均有化学式,只有由分子组成的物质才有
分子式,SiO 、NaCl属化学式,P 、C H 是分子式;球棍模型表示有机分子中各原子之间
2 4 2 4
的键的情况和相对空间位置;比例模型表示分子中各原子的大小比例和相对位置,两种模
型若原子大小比例不同,表示的物质不同,例如CH 和 CCl 等;结构简式需保留官能团,
4 4
如CH==CH ,不能写成CHCH ,还要注意有机物中原子的连接情况,如 ON—,不能写
2 2 2 2 2
成NO —;各“式”切勿张冠李戴,名称还是化学式,分子式还是实验式,结构式还是结
2
构简式,原子还是离子结构示意图,化学方程式还是离子方程式等。
典例分析
例1、下列有关化学用语表示正确的是
A.中子数为16的磷原子:
B. 的电子式:Ca2+
C.乙烯的结构简式:
D.K+的结构示意图:
D【解析】A.中子数为16的磷原子的质子数为15、质量数为31,原子符号为 ,故A
错误;B.氯化钙是离子化合物,电子式为 ,故B错误;C.乙烯的分子式
为C H,结构简式为CH=CH ,故C错误;D.钾离子的核电荷数为19,核外有3个电子
2 4 2 2
层,最外层电子数为8,离子的结构示意图为 ,故D正确。
例2、硒(Se)可用作光敏材料、电解锰行业催化剂等,是周期表中第34号元素。已知:
NaSe +2H+=2Na++Se+H Se。下列有关化学用语表示错误的是
2 2 2
A.中子数为40的硒原子: Se B.HSe的结构式:H—Se—H
2C.NaSe 的电子式: D.Na+的结构示意图:
2 2
C【解析】A.中子数为40的硒原子,其质子数=40+34=74,则为 Se,A项正确;B.
HSe中Se的化合价为-2价,则结构式:H—Se—H,B项正确;C.NaSe 的电子式为:
2 2 2
,C项错误;D.钠原子失去一个电子后变为钠离子,则Na+的
结构示意图: ,D项正确。
例3、工业合成尿素的原理:CO+2NH CO(NH)+H O,有关化学用语表示正
2 3 2 2 2
确的是
A.中子数为8的碳原子:8C
B.NH 的电子式:
3
C.氧原子的核外电子轨道表示式:
D.CO(NH) 的结构简式:
2 2
D【解析】A.中子数为8的碳原子表示为14C或 ,A错误;B.NH 的N最外层达到8
3
电子稳定结构,其电子式为 ,B错误;C.还差1s轨道的2个电子,C错误;D.
CO(NH) 是2个氨基与羰基碳相连,其结构简式为 ,D正确。
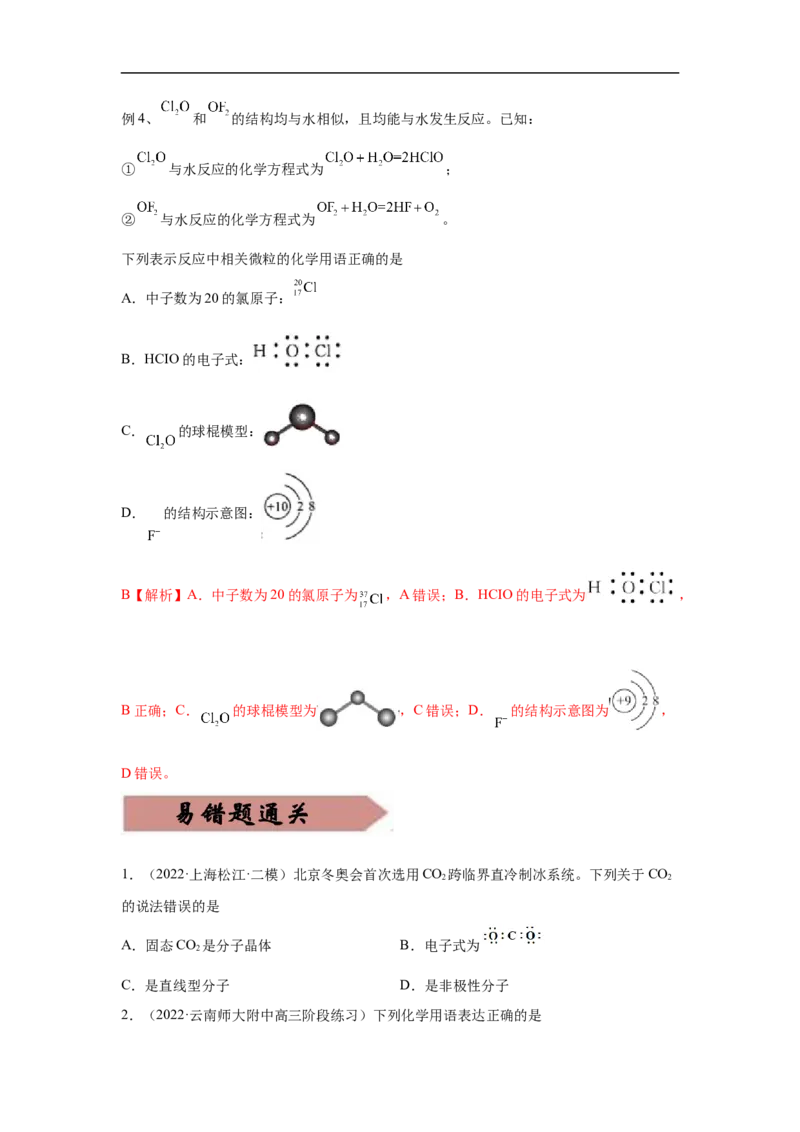
2 2例4、 和 的结构均与水相似,且均能与水发生反应。已知:
① 与水反应的化学方程式为 ;
② 与水反应的化学方程式为 。
下列表示反应中相关微粒的化学用语正确的是
A.中子数为20的氯原子:
B.HCIO的电子式:
C. 的球棍模型:
D. 的结构示意图:
B【解析】A.中子数为20的氯原子为 ,A错误;B.HCIO的电子式为 ,
B正确;C. 的球棍模型为 ,C错误;D. 的结构示意图为 ,
D错误。
1.(2022·上海松江·二模)北京冬奥会首次选用CO 跨临界直冷制冰系统。下列关于CO
2 2
的说法错误的是
A.固态CO 是分子晶体 B.电子式为
2
C.是直线型分子 D.是非极性分子
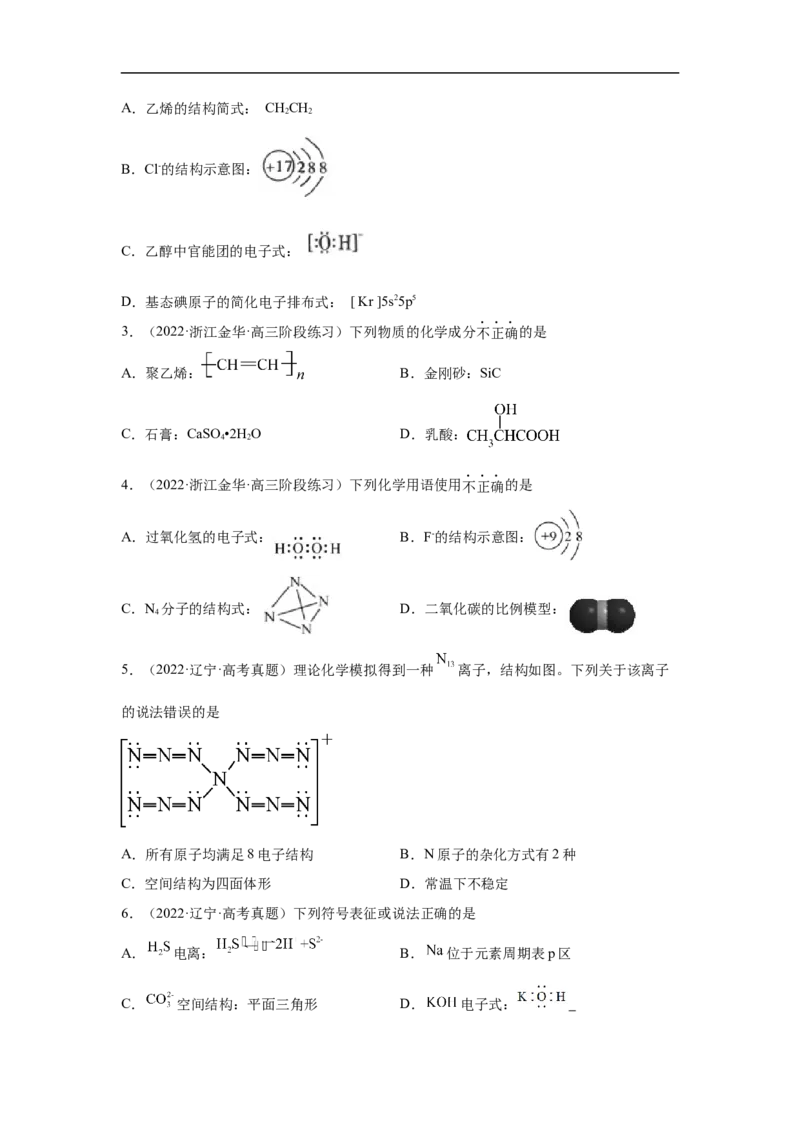
2.(2022·云南师大附中高三阶段练习)下列化学用语表达正确的是A.乙烯的结构简式: CHCH
2 2
B.Cl-的结构示意图:
C.乙醇中官能团的电子式:
D.基态碘原子的简化电子排布式: [ Kr ]5s25p5
3.(2022·浙江金华·高三阶段练习)下列物质的化学成分不正确的是
A.聚乙烯: B.金刚砂:SiC
C.石膏:CaSO•2H O D.乳酸:
4 2
4.(2022·浙江金华·高三阶段练习)下列化学用语使用不正确的是
A.过氧化氢的电子式: B.F-的结构示意图:
C.N 分子的结构式: D.二氧化碳的比例模型:
4
5.(2022·辽宁·高考真题)理论化学模拟得到一种 离子,结构如图。下列关于该离子
的说法错误的是
A.所有原子均满足8电子结构 B.N原子的杂化方式有2种
C.空间结构为四面体形 D.常温下不稳定
6.(2022·辽宁·高考真题)下列符号表征或说法正确的是
A. 电离: B. 位于元素周期表p区
C. 空间结构:平面三角形 D. 电子式:7.(2021·天津静海·高三阶段练习)下列化学用语和描述均正确的是
A.空气中电子式为 的分子含量过多会造成温室效应
B. 原子价电子轨道表示式
C.比例模型为 的分子可发生加成反应
D.核内质子数为117,核内中子数为174的核素 可表示为:
8.(2022·山西大同·高三期末)反应NH Cl+NaNO =NaCl+N↑+2H O放热且产生气体,可
4 2 2 2
用于冬天石油开采。下列表示反应中相关微粒的化学用语正确的是
A.HO的空间充填模型:
2
B.NH Cl的电子式:
4
C.N 的结构式:N=N
2
D.Na+的结构示意图:
9.(2022·辽宁沈阳·三模)下列化学用语使用正确的是
A.氯气的共价键电子云轮廓图:
B.基态 的价层电子排布图:
C.用电子式表示 的形成过程:D. 的空间填充模型:
10.(2022·湖北·华中师大一附中模拟预测)下列关于物质的组成、分类和化学用语,表
达错误的是
A.新型热电转换材料Sn-Te(Ag、Cd、Se掺杂),属于合金
B.雾是胶体,大雾可看作是一种分散剂为水的分散系
C.Ca(OH) 的电子式:
2
D.四氯化碳的球棍模型:
11.(2022·上海上海·模拟预测)氯仿保存不当会产生光气:2CHCl +O → 2HCl+
3 2
2COCl ,下列相关化学用语正确的是
2
A.CHCl 的球棍模型: B.O原子的轨道表示式:
3
C.氯离子的结构示意图: D.光气的电子式:
12.(2022·上海普陀·二模)关于CH≡CH和 的结构与性质,下列说法错误的是
A.CH≡CH是非极性分子 B. 存在单双键交替的结构
C.两者的最简式都是CH D.CH≡CH的空间构型是直线形
13.(2022·辽宁·渤海大学附属高级中学模拟预测)反应2NaO+2CO =2Na CO+O 可用于
2 2 2 2 3 2
呼吸面具。下列相关微粒的说法正确的是
A.中子数为8的碳原子: C
B.X射线衍射法确定CO 分子空间结构为直线型
2
C.基态钠原子的电子排布图为1s22s2 2p6 3s1D.NaO 的电子式:
2 2
14.(2022·江苏·高考真题)少量 与 反应生成 和 。下列说法正确的
是
A. 的电子式为 B. 的空间构型为直线形
C. 中O元素的化合价为-1 D. 仅含离子键
15.(2022·广东·高三阶段练习)肼(N H)是发射航天飞船常用的高能燃料,可通过反应
2 4
2NH +NaClO=N H+NaCl+HO制备。下列有关微粒的描述不正确的是
3 2 4 2
A.NH 的电子式为 B.NH 的结构式为
3 2 4
C. 的结构示意图: D.NaClO中存在离子键和共价键
16.(2022·重庆八中模拟预测)下列化学用语对事实的表述不正确的是
A.常温时,0.1mol·L-1氨水的pH=11.1;NH ·H O +OH-
3 2
⇌
B.由Na和Cl形成离子键的过程:
C.除锅炉水垢前加入NaCO 溶液预处理:CaSO(s)+ (aq) CaCO (a)+ (aq)
2 3 4 3
⇌
D.硬脂酸与乙醇的酯化反应:C H COOH+C H18OH Cl H COOC H+H 18O
17 35 2 5 35 35 2 5 2
17.(2022·河南·二模)2021年诺贝尔化学奖授予利斯特和麦克米伦,以表彰他们在不对
称有机催化剂领域的重要贡献。如在合成R—(+)苦杏仁腈时(结构中—Ph为苯基),D—羟
腈酶就是该反应的不对称有机催化剂,其合成过程如图所示。下列说法错误的是A.不对称有机催化剂对产物有选择性,从而使合成更加“绿色”
B.反应物氰化氢的电子式为
C.酶发挥催化功能需要适宜的条件
D.R—(+)苦杏仁腈和S—(—)苦杏仁腈互为同分异构体
18.(2022·北京市十一学校三模)关于乙烯水化法制乙醇:
,下列化学用语不正确的是
A.乙烯的电子式: B.中子数为8的氧的核素:
C.水的结构式: D.碳的原子结构示意图:
19.(2022·全国·高三专题练习)我国学者发明了一种低压高效电催化还原CO 的新方法,
2
其原理可以表示为:NaCl+CO CO+NaClO,下列有关化学用语表示正确的
2
是
A.中子数为12的钠离子:
B.NaClO的电子式:
C.CO 的比例模型:
2
D.CO晶体模型:
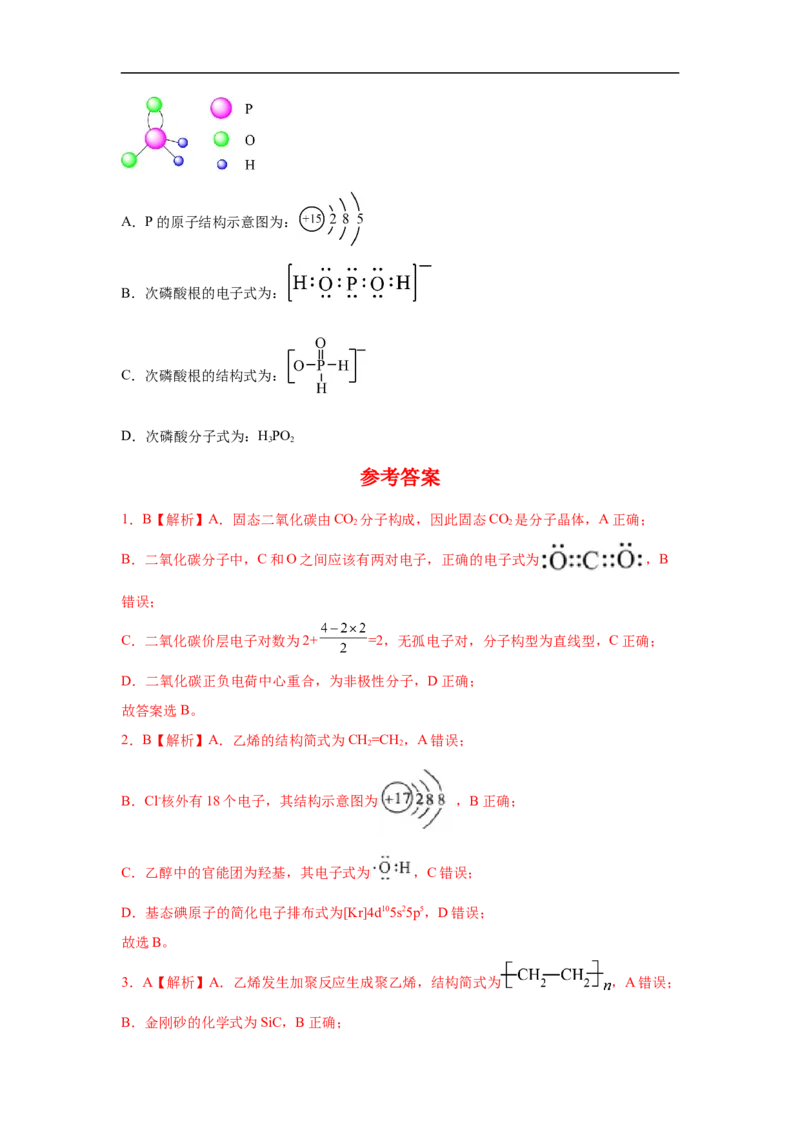
20.(2021·重庆·高三学业考试)次磷酸根( )的球棍模型如题4图所示,下列说法错
误的是A.P的原子结构示意图为:
B.次磷酸根的电子式为:
C.次磷酸根的结构式为:
D.次磷酸分子式为:HPO
3 2
参考答案
1.B【解析】A.固态二氧化碳由CO 分子构成,因此固态CO 是分子晶体,A正确;
2 2
B.二氧化碳分子中,C和O之间应该有两对电子,正确的电子式为 ,B
错误;
C.二氧化碳价层电子对数为2+ =2,无孤电子对,分子构型为直线型,C正确;
D.二氧化碳正负电荷中心重合,为非极性分子,D正确;
故答案选B。
2.B【解析】A.乙烯的结构简式为CH=CH ,A错误;
2 2
B.Cl-核外有18个电子,其结构示意图为 ,B正确;
C.乙醇中的官能团为羟基,其电子式为 ,C错误;
D.基态碘原子的简化电子排布式为[Kr]4d105s25p5,D错误;
故选B。
3.A【解析】A.乙烯发生加聚反应生成聚乙烯,结构简式为 ,A错误;
B.金刚砂的化学式为SiC,B正确;C.石膏的化学式为CaSO•2H O,C正确;
4 2
D.乳酸的结构简式为 ,D正确;
答案选A。
4.D【解析】A. 过氧化氢的中两个氧原子间形成一对共用电子对,电子式: ,
故A正确;
B. F是9号元素,有两个电子层,最外层得1个电子形成离子,F-的结构示意图:
,故B正确;
C. 与白磷结构相似,N 分子的结构式: ,故C正确;
4
D. 二氧化碳分子是直线型结构,且C原子半径大于O原子半径,则二氧化碳的比例模型
为 ,故D错误;
故选D。
5.B【解析】A.由 的结构式可知,所有N原子均满足8电子稳定结构,A正确;
B.中心N原子为 杂化,与中心N原子直接相连的N原子为 杂化,与端位N原子直
接相连的N原子为 杂化,端位N原子为 杂化,则N原子的杂化方式有3种,B错误;
C.中心N原子为 杂化,则其空间结构为四面体形,C正确;
D. 中含叠氨结构( ),常温下不稳定,D正确;
故答案选B。
6.C【解析】A. 是二元弱酸,电离分步进行,其一级电离方程式为,A错误;
B.基态 原子的价电子排布式是 ,最后一个电子填充在s能级,位于元素周期表s区,
B错误;
C. 中心碳原子的价层电子对数为 ,故其空间结构为平面
三角形,C正确;
D. 是离子化合物,电子式为 ,D错误;
故答案选C。
7.C【解析】A.CO 过多会造成温室效应,CO 是共价化合物,其结构式为O=C=O,碳
2 2
原子和氧原子之间有2对电子,其电子式为 ,故A错误;
B.该表达式违背了洪特规则,基态P原子的价电子排布式是3s23p3,轨道表示式为
,故B错误;
C. 为乙烯的比例模型,乙烯含有碳碳双键,可发生加成反应,故C正确;
D.核内质子数为117,核内中子数为174核素的质量数为117+174=291,核素Ts可表示为
,故D错误;
故选:C。
8.D【解析】A. O原子半径比H的大,HO的空间充填模型: ,故A错误;
2
B. 氯离子的电子式要加括号,NH Cl的电子式: ,故B错误;
4
C. 氮原子与氮原子形成叁键,N 的结构式:N≡N,故C错误;
2D. Na+的结构示意图: ,故D正确;
故选D。
9.A【解析】A.氯气分子中含氯氯单键,Cl原子的3p轨道“头碰头”形成的 电子云,
其共价键电子云轮廓图: ,A正确;
B.Fe的原子序数为26,核外价层电子排布为:3d64s2,基态 为Fe原子失去最外层两
个电子所得到的离子,所以其价层电子排布图: ,B错误;
C.氯化镁形成过程中,镁原子失去两个电子分别给两个氯原子,从而形成离子键,用电
子式表示为: ,C错误;
D. 为直线形分子,所以空间填充模型应为: ,D错误;
故选A。
10.B【解析】A.新型热电转换材料Sn-Te(Ag、Cd、Se掺杂)是热、电的量导体,具有金
属的形状,属于合金材料,A正确;
B.雾是胶体,大雾可看作是分散剂是空气,分散质主要是水的分散系,B错误;
C.Ca(OH) 是离子化合物,Ca2+与OH-之间以离子键结合,在阴离子OH-中H与O原子之
2
间以共价单键结合,故Ca(OH) 的电子式: ,C正确;
2
D.四氯化碳是由CCl 分子构成的分子晶体,分子呈四面体结构,由于原子半径:Cl>C,
4
所以该图示可以表示CCl 的空间结构的球棍模型,D正确;
4
故合理选项是B。11.A【解析】A.CH 为四面体结构,则CHCl 也应为四面体结构,原子半径Cl>C>
4 3
H,所以CHCl 的球棍模型为 ,A正确;
3
B.O原子的电子排布式为1s22s22p4,则2p轨道容纳4个电子,其中有2个轨道各容纳1个
电子,但自旋方向应相同,轨道表示式: ,B不正确;
C.氯离子的核电荷数为17,核外电子数为18,则结构示意图为 ,C不正确;
D.光气的化学式为COCl ,电子式为 ,D不正确;
2
故选A。
12.B【解析】A.乙炔分子结构对称,正负电荷重合,为非极性分子,A正确;
B.苯中不存在碳碳双键,B错误;
C.二者最简式都为CH,C正确;
D.乙炔为直线形分子,D正确;
故选B。
13.B【解析】A. 中A为质量数=中子数+质子数,Z为质子数。则中子数为8的碳原
子为 ,A项错误;
B.CO 中C为sp杂化,分子立体构型为直线型,B项正确;
2
C.基态钠原子的电子排布式为1s22s2 2p6 3s1,C项错误;
D.NaO 为离子化合物,其电子式为 ,D项错误;
2 2
故选B。
14.C【解析】A.过氧化钠是离子化合物,电子式是 ,A错误;
B. 中氧原子的成键电子对是2,孤电子对是2,根据价层电子对为4,根据价层电子对互斥理论,其空间构型为V形,B错误;
C. 中H显+1价,根据正负化合价为0,可计算出O的化合价为-1,C正确;
D. 中O和H之间是共价键,D错误;
故选C。
15.A【解析】A.NH 的电子式为 ,A项错误;
3
B.N的原子序数为7,最外层电子数为5,则NH 的结构式为 ,B项正确;
2 4
C.氯原子的原子序数为17,最外层电子数为7容易得到1个电子变为稳定结构,则 的
结构示意图: ,C项正确;
D.NaClO可电离出 和 ,则NaClO为离子化合物,存在离子键和共价键,D项正
确;
答案选A。
16.D【解析】A中根据溶液中的氢氧根离子的浓度判断是否发生完全电离,根据电离程
度判断碱性;B中根据电子式进行书写离子化合物的形成过程;C中根据沉淀转化原理进
行判断;D中根据酯化反应的反应机理,判断反应方程式。
A.氨水中一水合氨是一元碱,根据pH=11.1,氢氧根离子浓度约是0.001mol/L,说明一水
合氨属于弱碱,故电离方程式正确;故A正确;
B.根据氯化钠的形成过程,利用电子式表示其形成过程,故B正确;
C.硫酸钙微溶于水,碳酸钙难溶于水,根据沉淀转化,书写化学方程式,故C正确;
D.酯化反应的原理为“酸脱羟基醇脱氢”,生成物应为C H COl8OC H 和HO,故D不
17 35 2 5 2
正确;
故选答案D。
17.B【解析】A.不对称有机催化剂在使用时可以对产物有更好的选择性,从而制取更多
的目标产物,可以使合成更加“绿色”,减少副产物的产生,A正确;
B.反应物氰化氢HCN分子中C原子与H原子形成1个共价键,与N原子形成3个共价键,从而使物质分子中各个原子都达到稳定结构,其电子式为 ,B错误;
C.酶是具有生物活性的蛋白质,其只有在一定温度及酸碱性环境中才能最大程度发挥其
催化活性,因此酶发挥其催化功能需要适宜的条件,C正确;
D.R—(+)苦杏仁腈和S—(—)苦杏仁腈分子式相同,而结构不同,因此二者互为同分异构
体,D正确;
故合理选项是B。
18.A【解析】A.乙烯的结构简式为CH=CH ,电子式为 ,故A错误;
2 2
B.中子数为8的氧的核素质量数为16,表示为 ,故B正确;
C.水分子中含有2个O-H键,结构式为 ,故C正确;
D.碳的原子核外有6个电子,结构示意图为 ,故D正确;
选A。
19.B【解析】A.对于一种核素构成的微粒,元素符号左上角的数字表示质量数,所以中
子数为12的钠离子应表示为: ,A不正确;
B.NaClO为离子化合物,由Na+和ClO-构成,且Cl与O原子间形成1对共用电子对,其
电子式为 ,B正确;
C.CO 分子呈直线形结构,但C原子半径比O原子大,比例模型为: ,C
2
不正确;
D.固体CO为分子晶体, 为CO 的共价晶体模型,D不正确;
2故选B。
20.B【解析】A.P是15号元素,质子数为15,核外电子数为15,原子结构示意图为:
,A正确;
B.次磷酸根中其中一个O与P原子共用2对电子对,正确的电子式为: ,B
错误;
C.由次磷酸根( )的球棍模型,可得次磷酸根的结构式为: ,C正
确;
D.次磷酸根为 ,次磷酸为一元弱酸,则次磷酸分子式为:HPO ,D正确;
3 2
故选:B。