文档内容
江苏省海安市 2022-2023 学年高三上学期期初学业质量监测
试卷
化学试题
可能用到的相对原子质量::H 1 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Mn 55 Fe 56
第Ⅰ卷(选择题,共39分)
一、单项选择题:(共13分,每题3分,共39分。每题只有一个选项最符合题意。)
1. 化学与生产、生活密切相关。下列说法不正确的是
A. 我国成功研制出多款新冠疫苗,采用冷链运输疫苗,可以防止蛋白质变性
B. 用聚乳酸塑料代替聚乙烯塑料,可以减少白色污染
C. 北斗卫星导航系统由中国自主研发、独立运行,其所用芯片的主要成分为SiO
2
D. “神州13号”宇宙飞船返回舱所用高温结构陶瓷,属于新型无机非金属材料
【答案】C
2. 可发生水解: 。下列相关化学用语
正确 的是
A. 第一电离能:N>O>Mg B. 的结构式:
C. 的结构示意图: D. 基态O原子核外电子轨道表示式
【答案】A
3. 下列有关物质的性质与用途具有对应关系的是
A. 具有强氧化性,可用于制备硝酸铵
B. 具有还原性,可用于纸浆漂白
C. 具有两性,可用于电解冶炼铝
D. 溶液显碱性,可用于制胃酸中和剂
【答案】D
4. 能与悬浮在大气中的海盐粒子作用,反应为 (CINO
各原子均达到8电子稳定结构)。下列说法正确的是
A. 晶体属于分子晶体 B. ClNO的结构式为
C. NaCl晶胞中 的配位数为12 D. 是由极性键构成的非极性分
下载最新免费模拟卷,到公众号:一枚试卷君子
【答案】B
5. 短周期主族元素X、Y、Z、W原子序数依次增大,且X、Z同主族,Y的基态原子中含11种
运动状态不同的电子,Z原子的最外层电子数与核外电子总数之比为3:8,下列说法正确的
是
A. 原子的半径:
B. X与Y组成的化合物中均只含离子键
C. 简单气态氢化物的沸点X的比Z的高
D. X、Y、W组成的化合物的水溶液一定呈碱性
【答案】C
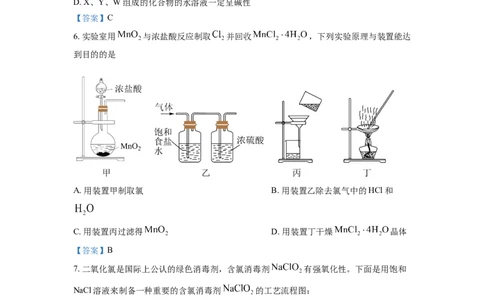
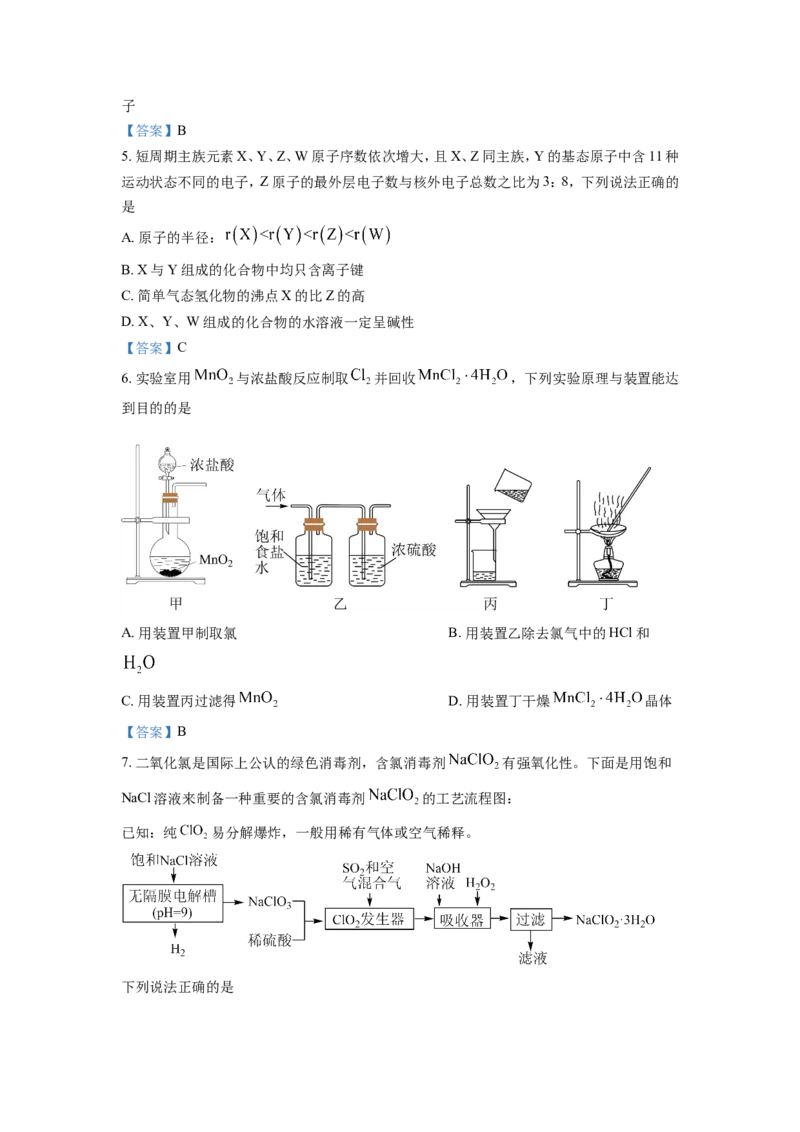
6. 实验室用 与浓盐酸反应制取 并回收 ,下列实验原理与装置能达
到目的的是
A. 用装置甲制取氯 B. 用装置乙除去氯气中的HCl和
C. 用装置丙过滤得 D. 用装置丁干燥 晶体
【答案】B
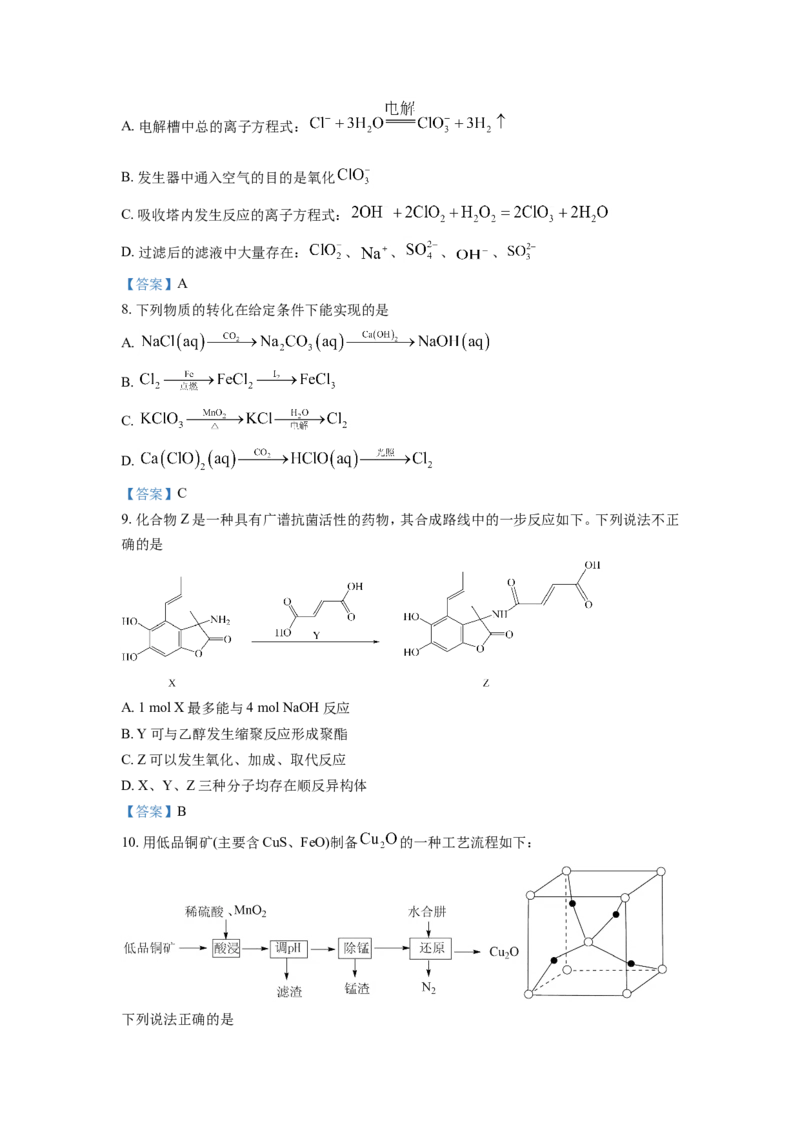
7. 二氧化氯是国际上公认的绿色消毒剂,含氯消毒剂 有强氧化性。下面是用饱和
NaCl溶液来制备一种重要的含氯消毒剂 的工艺流程图:
已知:纯 易分解爆炸,一般用稀有气体或空气稀释。
下列说法正确的是A. 电解槽中总的离子方程式:
B. 发生器中通入空气的目的是氧化
C. 吸收塔内发生反应的离子方程式:
D. 过滤后的滤液中大量存在: 、 、 、 、
【答案】A
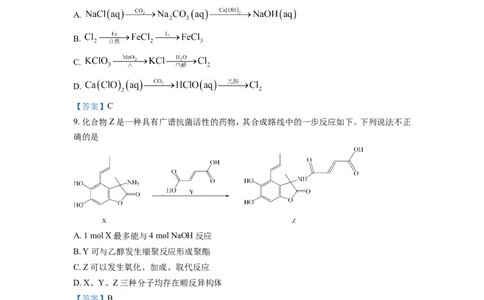
8. 下列物质的转化在给定条件下能实现的是
A.
B.
C.
D.
【答案】C
9. 化合物Z是一种具有广谱抗菌活性的药物,其合成路线中的一步反应如下。下列说法不正
确的是
A. 1 mol X最多能与4 mol NaOH反应
B. Y可与乙醇发生缩聚反应形成聚酯
C. Z可以发生氧化、加成、取代反应
D. X、Y、Z三种分子均存在顺反异构体
【答案】B
10. 用低品铜矿(主要含CuS、FeO)制备 的一种工艺流程如下:
下列说法正确的是A. “酸浸”过程中CuS发生反应的离子方程式为:
B. 已知酸浸液中含 ,为检验是否含有 ,可先加入KSCN溶液,再加氯水观察现象
C. 1个 晶胞(如图)中含4个氧原子
D. 水合肼浓度过大, 产率下降,可能的原因是 进一步被还原成单质铜
【答案】D
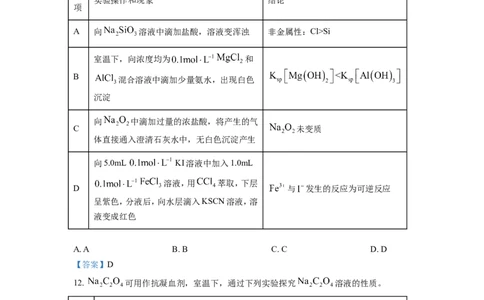
11. 根据下列实验操作和现象所得到的结论正确的是
选
实验操作和现象 结论
项
A 向 溶液中滴加盐酸,溶液变浑浊 非金属性:Cl>Si
室温下,向浓度均为 和
B
混合溶液中滴加少量氨水,出现白色
沉淀
向 中滴加过量的浓盐酸,将产生的气
C 未变质
体直接通入澄清石灰水中,无白色沉淀产生
向5.0mL KI溶液中加入1.0mL
溶液,用 萃取,下层
D 与 发生的反应为可逆反应
呈紫色,分液后,向水层滴入KSCN溶液,溶
液变成红色
A. A B. B C. C D. D
【答案】D
12. 可用作抗凝血剂,室温下,通过下列实验探究 溶液的性质。
选
实验操作和现象
项
1 测得 溶液的
向 溶液中加入等体积 盐酸,测得混合后溶液的
2
3 向酸性 溶液中滴加几滴 溶液,振荡,溶液颜色变浅向 溶液中加入等体积 溶液,产生白色沉
4
淀
下列有关说法正确的是
A. 溶液中存在
B. 实验2得到的溶液中有
C. 实验3中 被还原成 ,则反应的离子方程式为
D. 依据实验4可推测
【答案】D
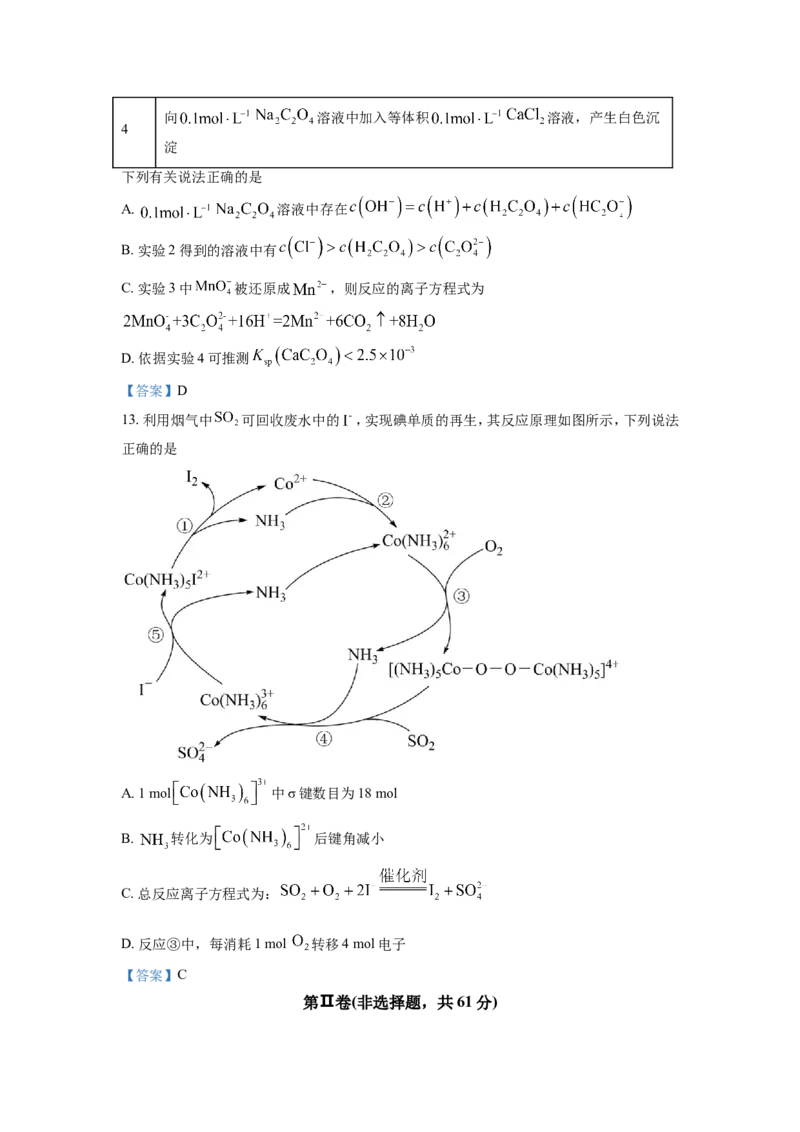
13. 利用烟气中 可回收废水中的 ,实现碘单质的再生,其反应原理如图所示,下列说法
正确的是
A. 1 mol 中σ键数目为18 mol
B. 转化为 后键角减小
C. 总反应离子方程式为:
D. 反应③中,每消耗1 mol 转移4 mol电子
【答案】C
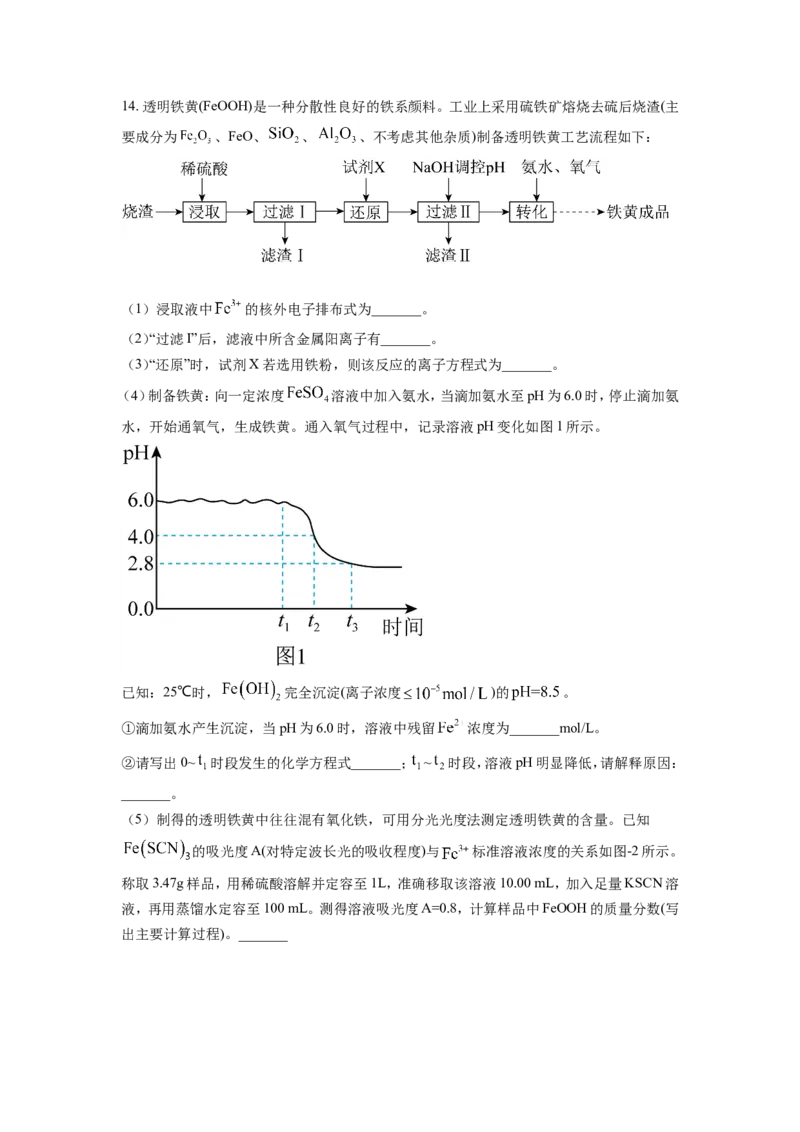
第Ⅱ卷(非选择题,共61分)14. 透明铁黄(FeOOH)是一种分散性良好的铁系颜料。工业上采用硫铁矿熔烧去硫后烧渣(主
要成分为 、FeO、 、 、不考虑其他杂质)制备透明铁黄工艺流程如下:
(1)浸取液中 的核外电子排布式为_______。
(2)“过滤I”后,滤液中所含金属阳离子有_______。
(3)“还原”时,试剂X若选用铁粉,则该反应的离子方程式为_______。
(4)制备铁黄:向一定浓度 溶液中加入氨水,当滴加氨水至pH为6.0时,停止滴加氨
水,开始通氧气,生成铁黄。通入氧气过程中,记录溶液pH变化如图1所示。
已知:25℃时, 完全沉淀(离子浓度 )的 。
①滴加氨水产生沉淀,当pH为6.0时,溶液中残留 浓度为_______mol/L。
②请写出0~ 时段发生的化学方程式_______; ~ 时段,溶液pH明显降低,请解释原因:
_______。
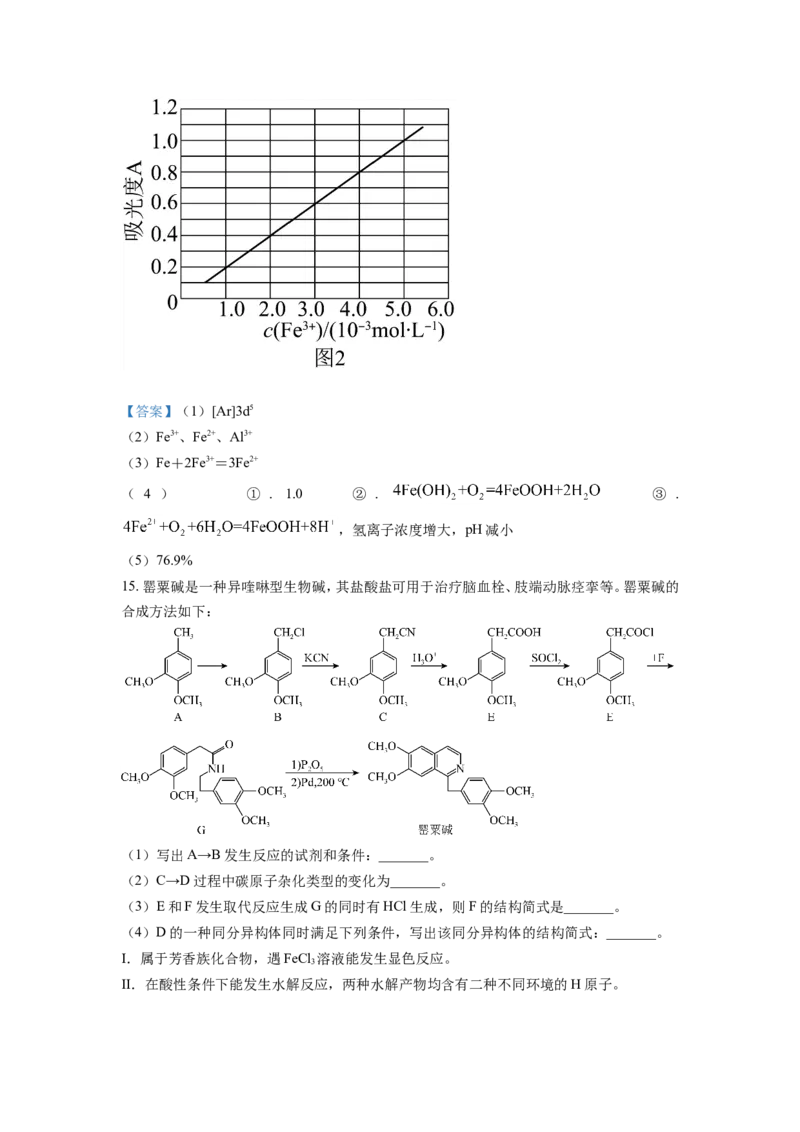
(5)制得的透明铁黄中往往混有氧化铁,可用分光光度法测定透明铁黄的含量。已知
的吸光度A(对特定波长光的吸收程度)与 标准溶液浓度的关系如图-2所示。
称取3.47g样品,用稀硫酸溶解并定容至1L,准确移取该溶液10.00 mL,加入足量KSCN溶
液,再用蒸馏水定容至100 mL。测得溶液吸光度A=0.8,计算样品中FeOOH的质量分数(写
出主要计算过程)。_______【答案】(1)[Ar]3d5
(2)Fe3+、Fe2+、Al3+
(3)Fe+2Fe3+=3Fe2+
( 4 ) ① . 1.0 ② . ③ .
,氢离子浓度增大,pH减小
(5)76.9%
15. 罂粟碱是一种异喹啉型生物碱,其盐酸盐可用于治疗脑血栓、肢端动脉痉挛等。罂粟碱的
合成方法如下:
(1)写出A→B发生反应的试剂和条件:_______。
(2)C→D过程中碳原子杂化类型的变化为_______。
(3)E和F发生取代反应生成G的同时有HCl生成,则F的结构简式是_______。
(4)D的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:_______。
I.属于芳香族化合物,遇FeCl 溶液能发生显色反应。
3
II.在酸性条件下能发生水解反应,两种水解产物均含有二种不同环境的H原子。(5) 。根据已有知识
并结合相关信息,写出以溴乙烷为原料制备 的合成路线流程图(无机试剂、有
机溶剂任用,合成路线流程图示例见本题题干)_______。
【答案】(1)氯气、光照
(2)由sp变为sp2
( 3 ) ( 4 ) ( 5 )
16. 高纯碳酸锰在电子工业中有重要的应用,湿法浸出软锰矿(主要成分为 ,含少量
Fe、Al等杂质元素)制备高纯碳酸锰的实验过程如下。
(1)“浸出”时,硫酸的作用是催化植物粉水解生成还原性糖。当硫酸浓度过高时,锰元素浸出
率下降,其可能的原因是_______。
(2)“除杂”时主要操作为加入一定量的双氧水,调节浸出液的pH为3.5~5.5,过滤。该过程中
双氧水实际用量比理论值大的原因是_______。
(3)“沉淀”:在30℃~35℃下,将碳酸氢铵溶液滴加到硫酸锰净化液中,控制反应液的最终pH
在6.5~7.0,得到 沉淀。该反应的化学方程式为_______;生成的 沉淀需经充
分洗涤,检验洗涤是否完全的方法是_______。
(4) 是黑色不溶于水的固体,常用于生产计算机的磁芯、磁盘等。已知:反应温度和
溶液pH对 的纯度和产率影响分别如图-1、图-2所示。请设计以硫酸锰净化液为原料
制备 的实验方案:_______,真空干燥4小时得产品 。(实验中须使用的试剂:
氨水、空气)【答案】(1)浓硫酸具有强氧化性和脱水性,当硫酸浓度过高时,还原性糖可能被浓硫酸破坏
导致锰元素浸出率下降
(2)二氧化锰也能够作为催化剂使过氧化氢分解为氧气
(3) ①. MnSO +2NHHCO +(NH)SO +CO +H O ②. 取最后一
4 4 3 4 2 4 2 2
次的洗涤滤液1-2mL于试管中,向其中滴加用盐酸酸化的BaCl 溶液,若无白色沉淀产生,则
2
表明已洗涤干净
(4)50℃时,向硫酸锰溶液中加入一定量的氨水先制得氢氧化锰固体,调节溶液pH为8.5,然
后将固体氢氧化锰调浆通空气氧化制得
17. 工业上常用微生物法、吸收法、电解法、还原法等消除硫、氮等引起的污染。
(1)微生物法脱硫
富含有机物的弱酸性废水在SBR细菌作用下产生 、 等物质,可将废水中
还原为 ,同时用 或 将 从水中吹出,再用碱液吸收。
① 的空间构型为_______。
② 与 在SBR细菌作用下生成 和 的离子方程式为_______。
③将 从水中吹出时,用 比 效果更好,其原因是_______。
(2)吸收法脱硫
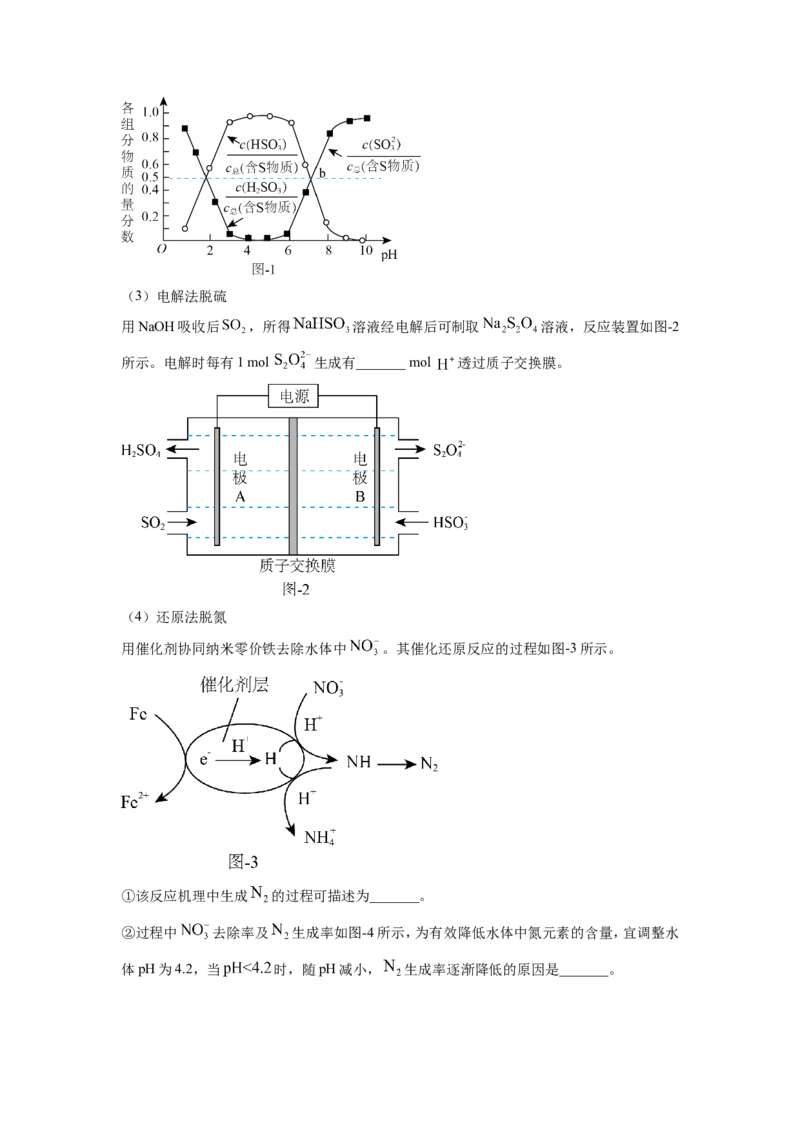
烟气中的 可以用“亚硫酸铵吸收法”处理,发生的反应为
,测得25℃时溶液pH与各组分物质的量分数的
变化关系如图-1所示。b点时溶液 ,则 _______。(3)电解法脱硫
用NaOH吸收后 ,所得 溶液经电解后可制取 溶液,反应装置如图-2
所示。电解时每有1 mol 生成有_______ mol 透过质子交换膜。
(4)还原法脱氮
用催化剂协同纳米零价铁去除水体中 。其催化还原反应的过程如图-3所示。
①该反应机理中生成 的过程可描述为_______。
②过程中 去除率及 生成率如图-4所示,为有效降低水体中氮元素的含量,宜调整水
体pH为4.2,当 时,随pH减小, 生成率逐渐降低的原因是_______。【 答 案 】 ( 1 ) ① . 正 四 面 体 形 ② .
③. 二氧化碳吹出时可增强
溶液的酸性,抑制硫化氢的溶解,有利于将硫化氢吹出
(2)3:1 (3)2
(4) ①. 纳米零价铁在催化剂表面失去电子变为亚铁离子,在催化剂层中氢离子得到电
子变为氢原子,在酸性条件下氢原子还原硝酸根变为NH,NH失去氢原子变为氮气 ②.
pH越小,氢离子浓度越大,会生成更多的氢原子,使硝酸根生成的中间产物NH更多的与氢
原子反应生成铵根离子,从而减少氮气的生成