文档内容
河北正定中学 2022-2023 学年(上)第三次月考
高三化学
(试卷总分:100分 考试时间:90分钟 )
注意事项:
1.答题时,务必将自己的姓名、班级、准考证号填写在答题卡规定的位置上。
2.答选择题时,用2B铅笔将答题卡上对应的答案标号涂黑。如需改动,用橡皮擦
干净后,再选涂其他答案标号。
3.答非选择题时,必须使用0.5毫米黑色黑色签字笔把答案写在答题卡规定的位
置上。答案如需改正,请先划掉原来的答案,再写上新答案,不准使用涂改液、
胶带纸、修正带。
4.考试结束后,只将答题卡交回。
一、选择题:(本题共 14小题,每题3分,共42分.在每小题给出的四个
选项中,只有一项是符合题目要求的).
1.下列变化属于物理变化的是( )
A.煤的干馏 B.石油的分馏 C.重油的裂化 D.石油的裂解
2.下列说法正确的是
A.过氧化氢的电子式为
B. I和 I 互为同位素
2
C.质子数为17,中子数为20的氯原子可表示为 Cl
D.在Mg18O 晶体中,阴离子结构示意图可表示为
3.合成氨是工业上的重要反应:N2(g)+3H2(g) 2NH3(g),下
列说法不正确的是
A.反应达平衡状态后,各物质浓度不变,反应停止
B.反应达平衡状态后,单位时间内生成1mol N2的同时消耗3mol H2
C.在上述条件下,N2不可能100%转化为NH3
D.使用催化剂是为了加快反应速率,提高生产效率
4.下列有关实验装置进行的相应实验,能达到实验目的的是A.图①向容量瓶中转移溶液
B.图②用于NaO 和HO反应制取少量的O
2 2 2 2
C.图③比较碳酸钠和碳酸氢钠的热稳定性
D.图④制备Fe(OH) 并能较长时间观察到白色
2
5.奥司他韦(C H NO)可抑制流感病毒在人体内的传播,起到治疗流行性感冒的作
16 28 2 4
用。下列对奥司他韦的说法正确的是( )
A.从分类角度看:属于无机物
B.从量的角度看:碳、氢元素的质量比为4:7
C.从组成角度看:含有氧元素,属于氧化物
D.从结构角度看:分子中碳、氢、氮、氧原子个数比为8:14:1:2
6.甲、乙、丙、丁四种易溶于水的物质,分别由Ba2+、Mg2+、H+、OH-、Cl-、SO 、
NH 、CO 中的不同阳离子和阴离子各一种组成,已知:①将甲溶液分别与其他三种
物质的溶液混合均有白色沉淀生成;②0.1mol•L-1乙溶液中c(H+)=0.2mol•L-1;③向丙
溶液中滴入AgNO 溶液有不溶于稀硝酸的白色沉淀生成。下列结论不正确的是
3
A.甲溶液中含有Ba2+ B.乙溶液中含有SO
C.丙溶液中含有Cl- D.丁溶液中含有Mg2+
7.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.含有0.1 mol Na SiO 的溶液全部转化为硅酸胶体,其中含有的胶体粒子数为0.1N
2 3 A
B.18g 中的电子数为11N
A
C.SO 的沸点为317K,则标准状况下44.8L SO 的分子数为2N
3 3 A
D.若Cl 与足量NaOH的溶液反应生成 和 各0.1 mol,则生成的 数目为
2
0.4N
A
8.V、W、X、Y、Z为原子序数依次增大的短周期主族元素,W与X、X与Z在周期
表中位置分别相邻,化合物甲可表示为WVY(ZX ),其中除含有Y3+外,另外两种离
4 4 2子的结构如图所示,下列判断错误的是
A.化合物甲的水溶液可用于净水
B.W的单质很稳定,常用于保存粮食
C.简单氢化物的沸点:X>W>Z
D.简单离子半径:Y>Z>X
9.已知:①2 +10Cl-+16H+=2Mn2++5Cl↑+8H O;②2Fe2++Br =2Fe3++2Br-;
2 2 2
③2Br-+Cl=2Cl-+Br 。根据上述反应,判断下列结论错误的是
2 2
A.反应①中,Mn2+是 的还原产物
B.反应③中,Cl 发生还原反应,显示还原性
2
C.氧化性强弱顺序为 >Cl>Br >Fe3+
2 2
D.溶液中可发生反应:2Fe2++Cl=2Fe3++2Cl-
2
10.可逆反应:2NO 2NO+O 在恒温恒容密闭容器中反应,下列条件可判断该反
2 2
应已经达到平衡状态的是( )
(1)单位时间内生成nmolO 的同时生成2nmolNO
2 2
(2)单位时间内生成nmolO 的同时,生成2nmolNO
2
(3)用NO 、NO、O 的物质的量浓度变化表示的反应速率的比为2:2:1的状态
2 2
(4)混合气体的颜色不再改变的状态
(5)混合气体的密度不再改变的状态
(6)混合气体的平均相对分子质量不再改变的状态
A.(1)(4)(6) B.(2)(3)(5)
C.(1)(3)(4) D.(1)(2)(3)(4)(5)(6)
11.周杰伦在歌曲《青花瓷》中唱到“帘外芭蕉惹骤雨,门环惹铜绿”,其中“铜
绿”的化学成分是碱式碳酸铜。铜在潮湿的空气中生锈的化学反应为:
。下列有关该反应的说法正确的是
A.该反应是氧化还原反应,发生化合价变化的有三种元素
B. 失去电子,发生的是还原反应C.由此反应可知,化合反应一定是氧化还原反应
D.碱式碳酸铜属于盐类
12.下列说法错误的是
①当碰撞的分子具有足够的能量和适当的取向时,才能发生化学反应
②发生有效碰撞的分子一定是活化分子
③活化分子间的碰撞一定是有效碰撞
④活化分子间每次碰撞都发生化学反应
⑤能发生有效碰撞的分子必须具有相当高的能量
⑥活化能指活化分子多出反应物分子平均能量的那部分能量
A.①④ B.③④ C.④⑤⑥ D.②⑤
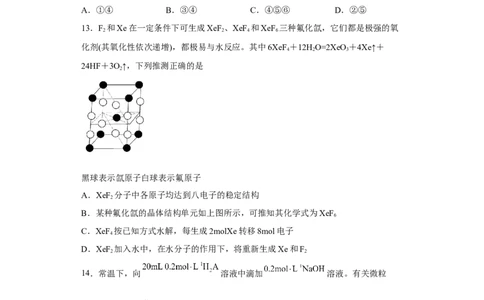
13.F 和Xe在一定条件下可生成XeF 、XeF 和XeF 三种氟化氙,它们都是极强的氧
2 2 4 6
化剂(其氧化性依次递增),都极易与水反应。其中6XeF +12HO=2XeO +4Xe↑+
4 2 3
24HF+3O↑,下列推测正确的是
2
黑球表示氙原子白球表示氟原子
A.XeF 分子中各原子均达到八电子的稳定结构
2
B.某种氟化氙的晶体结构单元如上图所示,可推知其化学式为XeF
6
C.XeF 按已知方式水解,每生成2molXe转移8mol电子
4
D.XeF 加入水中,在水分子的作用下,将重新生成Xe和F
2 2
14.常温下,向 溶液中滴加 溶液。有关微粒
物质的量变化如图。下列各粒子浓度之间关系不正确的是
A.图中的Ⅱ线,代表 的变化
B.当加入 体积为20mL时,溶液中:C.当加入 体积为40mL时,溶液中:
D. 的第一步电离平衡常数
二、填空题:58分
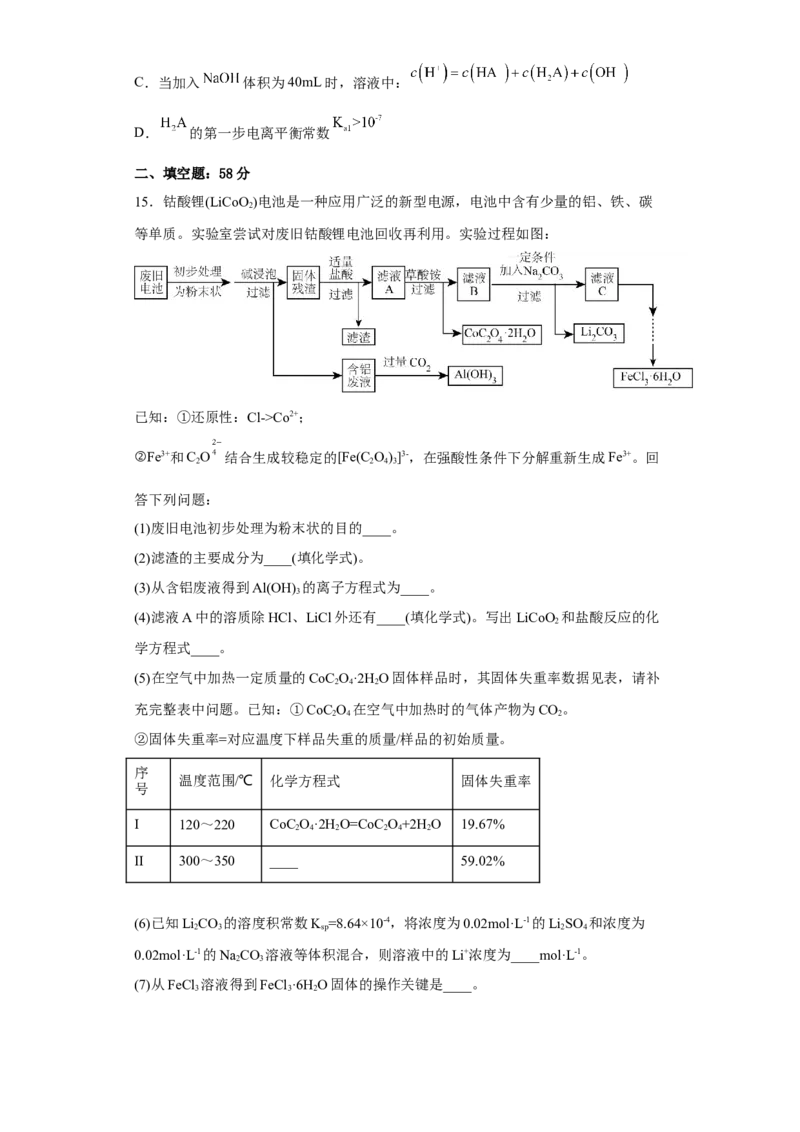
15.钴酸锂(LiCoO )电池是一种应用广泛的新型电源,电池中含有少量的铝、铁、碳
2
等单质。实验室尝试对废旧钴酸锂电池回收再利用。实验过程如图:
已知:①还原性:Cl->Co2+;
②Fe3+和C O 结合生成较稳定的[Fe(C O)]3-,在强酸性条件下分解重新生成Fe3+。回
2 2 4 3
答下列问题:
(1)废旧电池初步处理为粉末状的目的____。
(2)滤渣的主要成分为____(填化学式)。
(3)从含铝废液得到Al(OH) 的离子方程式为____。
3
(4)滤液A中的溶质除HCl、LiCl外还有____(填化学式)。写出LiCoO 和盐酸反应的化
2
学方程式____。
(5)在空气中加热一定质量的CoC O·2H O固体样品时,其固体失重率数据见表,请补
2 4 2
充完整表中问题。已知:①CoC O 在空气中加热时的气体产物为CO。
2 4 2
②固体失重率=对应温度下样品失重的质量/样品的初始质量。
序
温度范围/℃ 化学方程式 固体失重率
号
I 120~220 CoC O·2H O=CoC O+2H O 19.67%
2 4 2 2 4 2
II 300~350 ____ 59.02%
(6)已知LiCO 的溶度积常数K =8.64×10-4,将浓度为0.02mol·L-1的LiSO 和浓度为
2 3 sp 2 4
0.02mol·L-1的NaCO 溶液等体积混合,则溶液中的Li+浓度为____mol·L-1。
2 3
(7)从FeCl 溶液得到FeCl ·6H O固体的操作关键是____。
3 3 216.高铁酸钾(KFeO)具有极强的氧化性,是一种优良的水处理剂。
2 4
(1)请完成FeO2-与水反应的方程式:4FeO2-+10HO 4Fe(OH) +8OH-+
4 4 2 3
_____。KFeO 在处理水的过程中所起的作用是___________和___________。
2 4
(2)常温下,Fe(OH) 的K = 4.0×10-38,请写出Fe(OH) 在水中的溶解平衡方程式
3 sp 3
______________
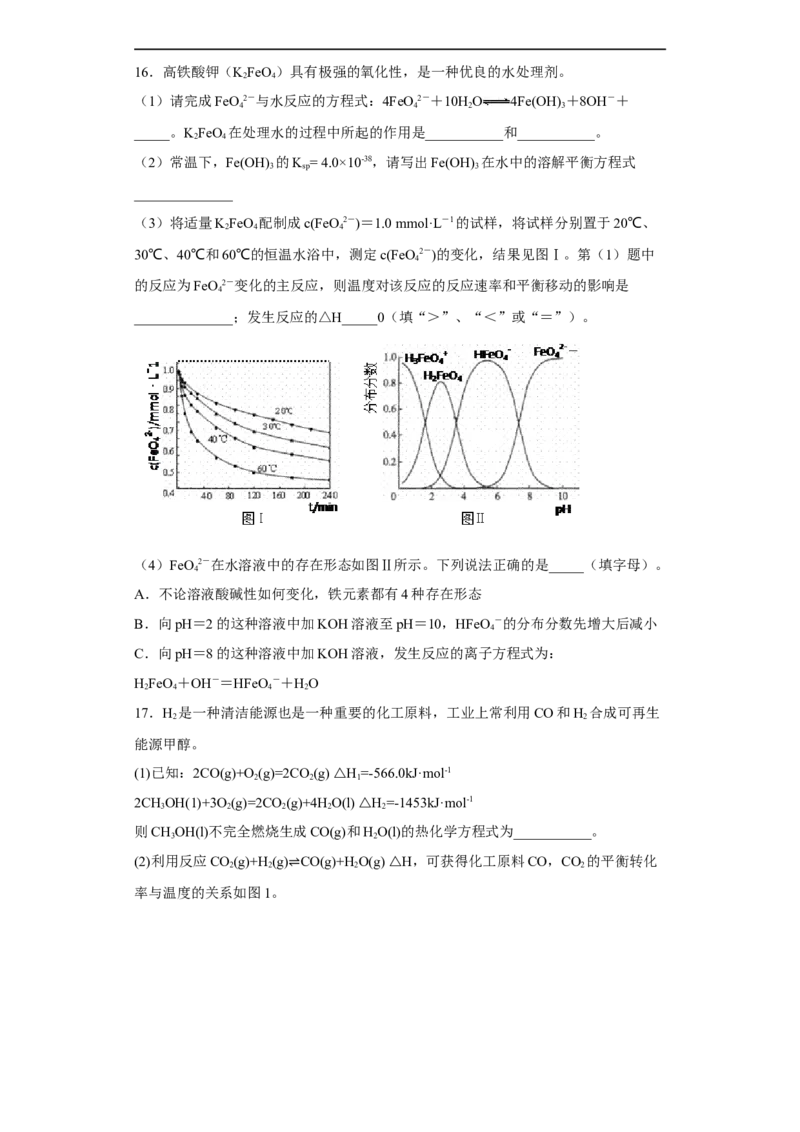
(3)将适量KFeO 配制成c(FeO2-)=1.0 mmol·L-1的试样,将试样分别置于20℃、
2 4 4
30℃、40℃和60℃的恒温水浴中,测定c(FeO2-)的变化,结果见图Ⅰ。第(1)题中
4
的反应为FeO2-变化的主反应,则温度对该反应的反应速率和平衡移动的影响是
4
______________;发生反应的△H_____0(填“>”、“<”或“=”)。
(4)FeO2-在水溶液中的存在形态如图Ⅱ所示。下列说法正确的是_____(填字母)。
4
A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.向pH=2的这种溶液中加KOH溶液至pH=10,HFeO -的分布分数先增大后减小
4
C.向pH=8的这种溶液中加KOH溶液,发生反应的离子方程式为:
HFeO+OH-=HFeO -+HO
2 4 4 2
17.H 是一种清洁能源也是一种重要的化工原料,工业上常利用CO和H 合成可再生
2 2
能源甲醇。
(1)已知:2CO(g)+O(g)=2CO (g) △H =-566.0kJ·mol-1
2 2 1
2CHOH(1)+3O (g)=2CO (g)+4HO(l) △H =-1453kJ·mol-1
3 2 2 2 2
则CHOH(l)不完全燃烧生成CO(g)和HO(l)的热化学方程式为___________。
3 2
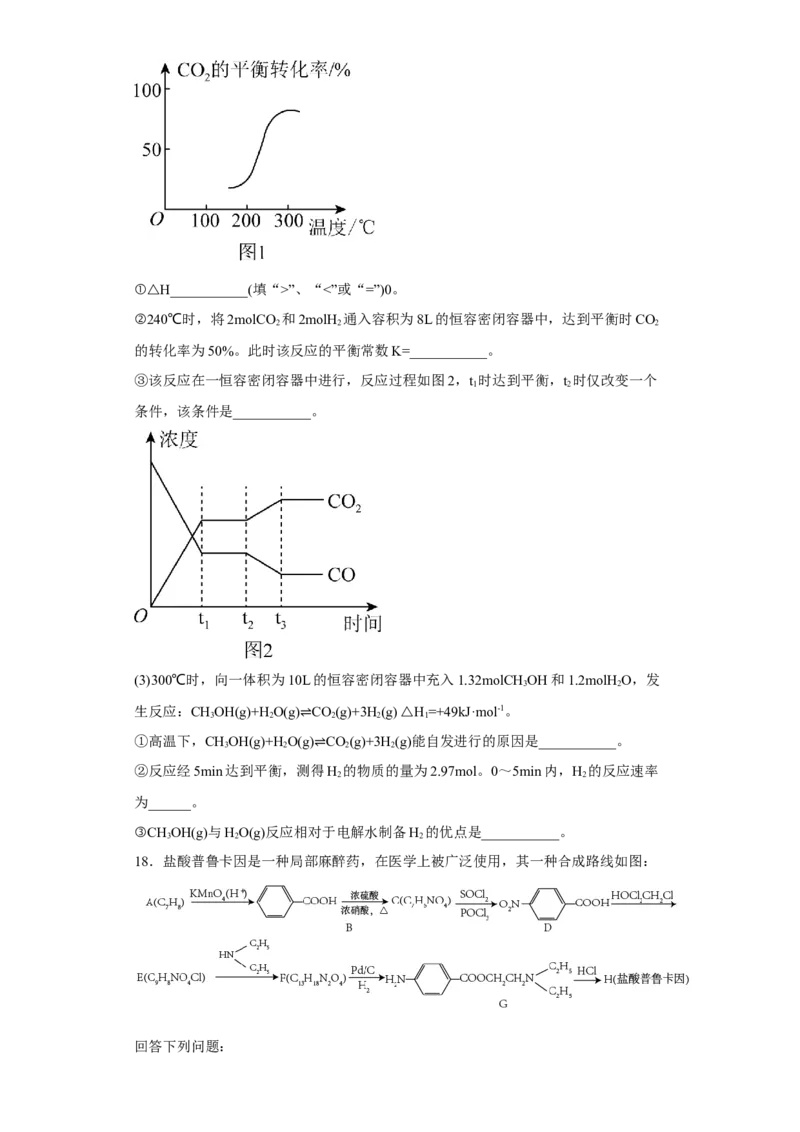
(2)利用反应CO(g)+H(g) CO(g)+HO(g) △H,可获得化工原料CO,CO 的平衡转化
2 2 2 2
率与温度的关系如图1。⇌①△H___________(填“>”、“<”或“=”)0。
②240℃时,将2molCO 和2molH 通入容积为8L的恒容密闭容器中,达到平衡时CO
2 2 2
的转化率为50%。此时该反应的平衡常数K=___________。
③该反应在一恒容密闭容器中进行,反应过程如图2,t 时达到平衡,t 时仅改变一个
1 2
条件,该条件是___________。
(3)300℃时,向一体积为10L的恒容密闭容器中充入1.32molCHOH和1.2molHO,发
3 2
生反应:CHOH(g)+H O(g) CO(g)+3H(g) △H =+49kJ·mol-1。
3 2 2 2 1
①高温下,CH
3
OH(g)+H
2
O(⇌g) CO
2
(g)+3H
2
(g)能自发进行的原因是___________。
②反应经5min达到平衡,测得⇌H
2
的物质的量为2.97mol。0~5min内,H
2
的反应速率
为______。
③CH OH(g)与HO(g)反应相对于电解水制备H 的优点是___________。
3 2 2
18.盐酸普鲁卡因是一种局部麻醉药,在医学上被广泛使用,其一种合成路线如图:
回答下列问题:(1)A的名称为___。
(2)E中含氧官能团的名称为___。
(3)F的结构简式为___。
(4)B→C的化学方程式为___;其反应类型为___。
(5)芳香族化合物M与F互为同分异构体,符合下列条件的M的结构有___种。
①分子内只含硝基一种官能团②分子内不含甲基③苯环上只有一个取代基
(6)参照上述流程,设计以苯和1,3—丁二烯为原料制备 的合成路线___。
(无机试剂任选)参考答案
1.B 2.D 3.A 4.D 5.D 6.D 7.D 8.D 9.B 10.A 11.D 12.B 13.C 14.
C
15.(1)增大接触面积,加快反应速率,提高浸出率
(2)C
(3)AlO +CO +2H O=Al(OH) ↓+HCO
2 2 3
(4) FeCl 、CoCl 2LiCoO +8HCl=2LiCl+2CoCl +Cl↑+4H O
3 2 2 2 2 2
(5)2CoC O+O 2CoO+4CO
2 4 2 2
(6)0.02
(7)加入适量盐酸(或通入HCl气体)抑制Fe3+的水解
16. 3O 杀菌消毒 吸附(净水) Fe(OH) (S) Fe3+
2 3
(aq)+ 3 OH-(aq) 温度升高,反应速率加快,平衡向正反应方向移动
> B
17.(1)CH OH(l)+O (g)=CO(g)+2HO(l)△H=-443.5kJ•mol-1
3 2 2
(2) > 3 降低温度或分离出氢气或增加水蒸气的浓度
(3) 该反应是熵增反应 0.0594mol/(L•min) 前者耗能更少
18. 甲苯 硝基、酯基
+HNO
3
+H O 取代反应(或硝化反应) 16
2