文档内容
河北省衡水中学 2023 届上学期高三年级四调考试
化 学
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。共8页,总分100分,考试时间75
分钟。
可能用到的相对原子质量: H 1 Li 7 C 12 N 14 O 16 Na 23 Mg 24 Al
27
Si 28 S 32 K 39 Fe 56 Cu 64
第Ⅰ卷(选择题 共45分)
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.《博物新编》有关于磺强水制法的记载:“以铅作一密炉,炉底贮以清水,焚硝磺于炉中,使
硝磺之气重坠入水,然后将水再行蒸炼,一如蒸酒甑油之法,务使水汽尽行升散,则所存者是
磺强水矣。”(提示:“硝”指KNO,“磺”指硫黄)。下列有关磺强水的说法正确的是
3
A.“焚硝磺”时发生的是氧化还原反应 B.磺强水是一种易挥发的强电解质
C.0.01 mol · L−1的磺强水溶液的pH=2 D.磺强水溶液中不存在分子
2.下列有关电解质溶液的说法正确的是
A.100℃时,pH=12的NaOH溶液中,c(OH−)=0.01 mol · L−1
B.常温下,将pH=9的CHCOONa溶液与pH=9的NaOH溶液混合,混合溶液pH仍为9
3
C.常温下,将pH=1的稀盐酸与pH=13的AOH溶液等体积混合,所得溶液pH一定为7
D.将冰醋酸加水稀释,冰醋酸的电离程度逐渐增大,c(H+ )逐渐增大
3.常温下,下列说法错误的是
A.向0.01 mol · L−1 NH HSO 溶液中滴加NaOH溶液至中性:
4 4
c(Na+) > c(SO2− ) > c(NH+ ) > c(OH−) = c(H+)
4 4
B.FeS溶于稀硫酸,而CuS不溶于稀硫酸,则K (FeS) > K (CuS)
sp sp
c(NH+
)
C.向盐酸中加入氨水至中性,溶液中 4 >1
c(Cl−
)
D.0.01 mol · L−1 NaHCO 溶液:c(H+ )+c(H CO) =c(OH−)+c(CO2− )
3 2 3 3
4.实验室常用酸性KMnO 溶液标定摩尔盐[(NH )Fe(SO )·6HO]溶液,可用过二硫酸钠(Na SO)
4 4 2 4 2 2 2 2 8
使MnO−
全部再生。下列说法错误的是
4
A.氧化性:S O2− > MnO− > Fe3+
2 8 4
B.滴定时,KMnO 溶液和摩尔盐溶液都用酸式滴定管盛装
4
C.过二硫酸结构如图所示,则S O2−含有两个四面体结构
2 8
D.滴定过程中,消耗的摩尔盐和过二硫酸钠物质的量之比为1:25.某种由六种元素形成的抗癌药物的结构简式如图所示,其中W、X、Y、Z是原子序数依次增大
的短周期主族元素,W、Y同主族,Y、Z的最外层电子数之和是X的最外层电子数的2倍。下
列叙述错误的是
A.W的最简单氢化物与Z的单质混合后可产生白烟
B.X与W的第一电离能:X < W
C.WZ 和YZ 键角前者小于后者
3 3
D.X的一种单质和化合物ZX 均可用于自来水消毒
2
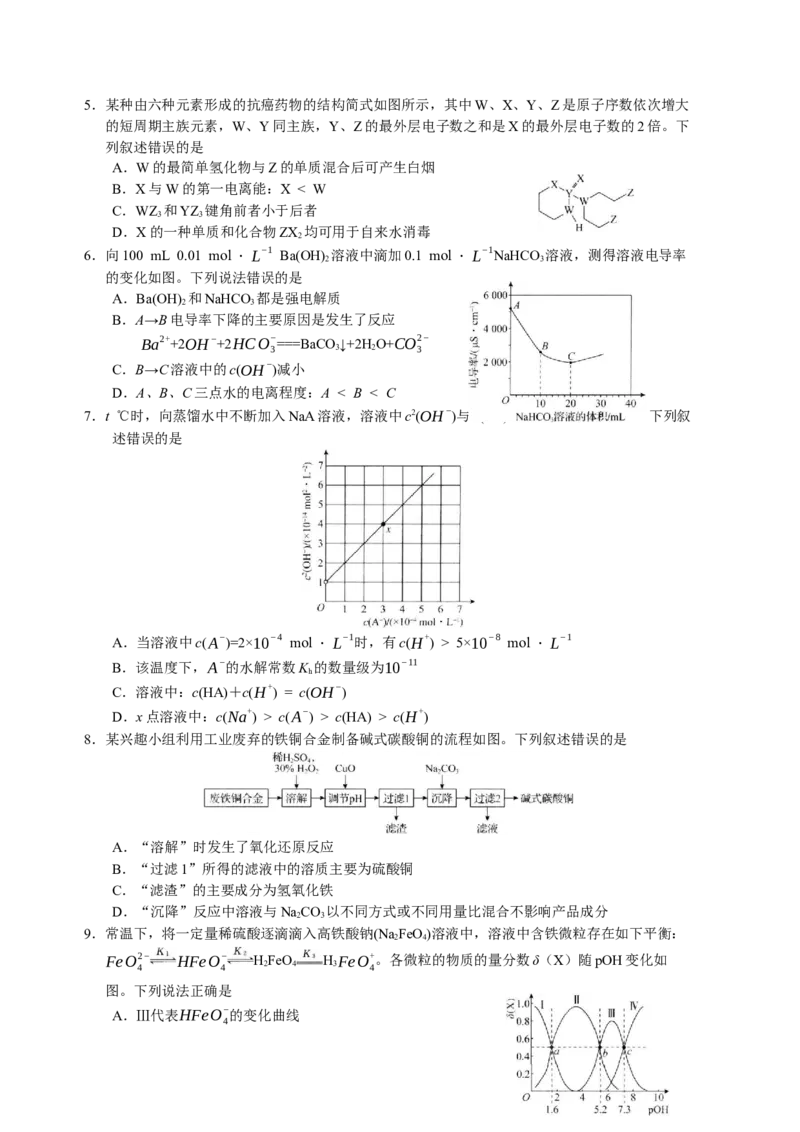
6.向100 mL 0.01 mol · L−1 Ba(OH) 溶液中滴加0.1 mol · L−1NaHCO 溶液,测得溶液电导率
2 3
的变化如图。下列说法错误的是
A.Ba(OH) 和NaHCO 都是强电解质
2 3
B.A→B电导率下降的主要原因是发生了反应
Ba2++2OH−+2HCO−
===BaCO↓+2H
O+CO2−
3 3 2 3
C.B→C溶液中的c(OH−)减小
D.A、B、C三点水的电离程度:A < B < C
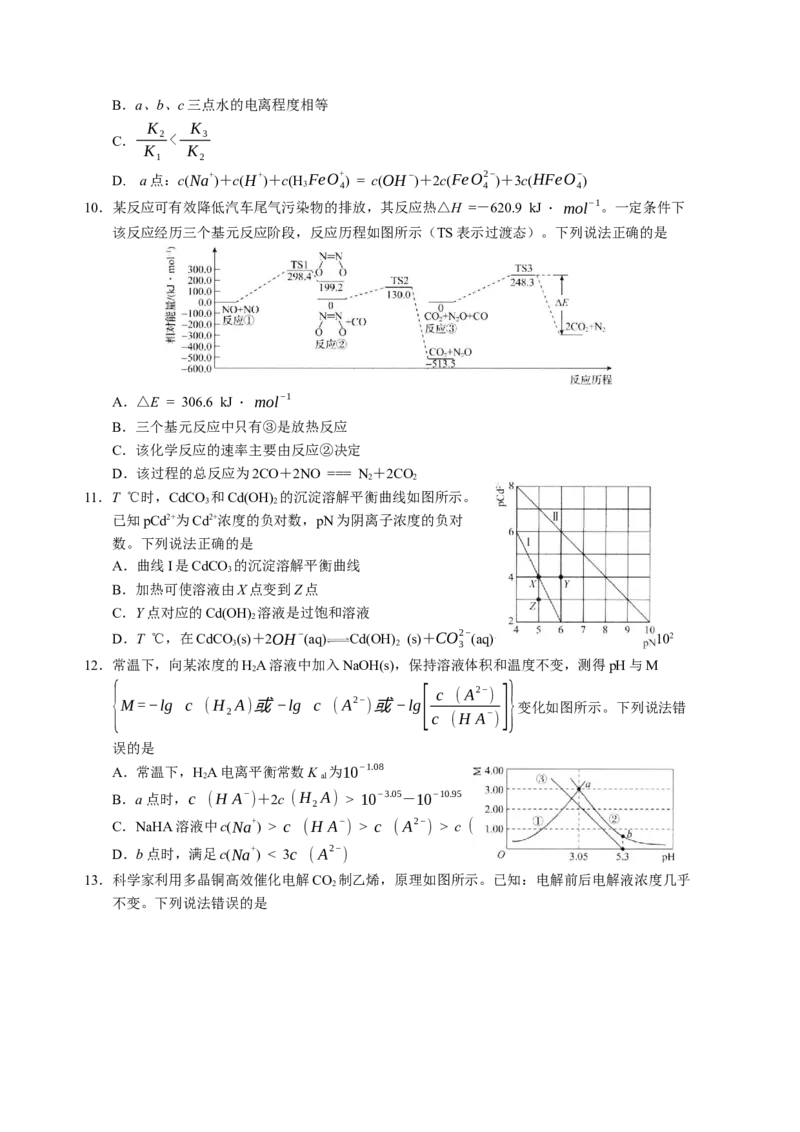
7.t ℃时,向蒸馏水中不断加入NaA溶液,溶液中c2(OH−)与c(A−)的变化关系如图所示。下列叙
述错误的是
A.当溶液中c(A−)=2×10−4 mol · L−1时,有c(H+ ) > 5×10−8 mol · L−1
B.该温度下,A−的水解常数K 的数量级为10−11
h
C.溶液中:c(HA)+c(H+ ) = c(OH−)
D.x点溶液中:c(Na+ ) > c(A−) > c(HA) > c(H+ )
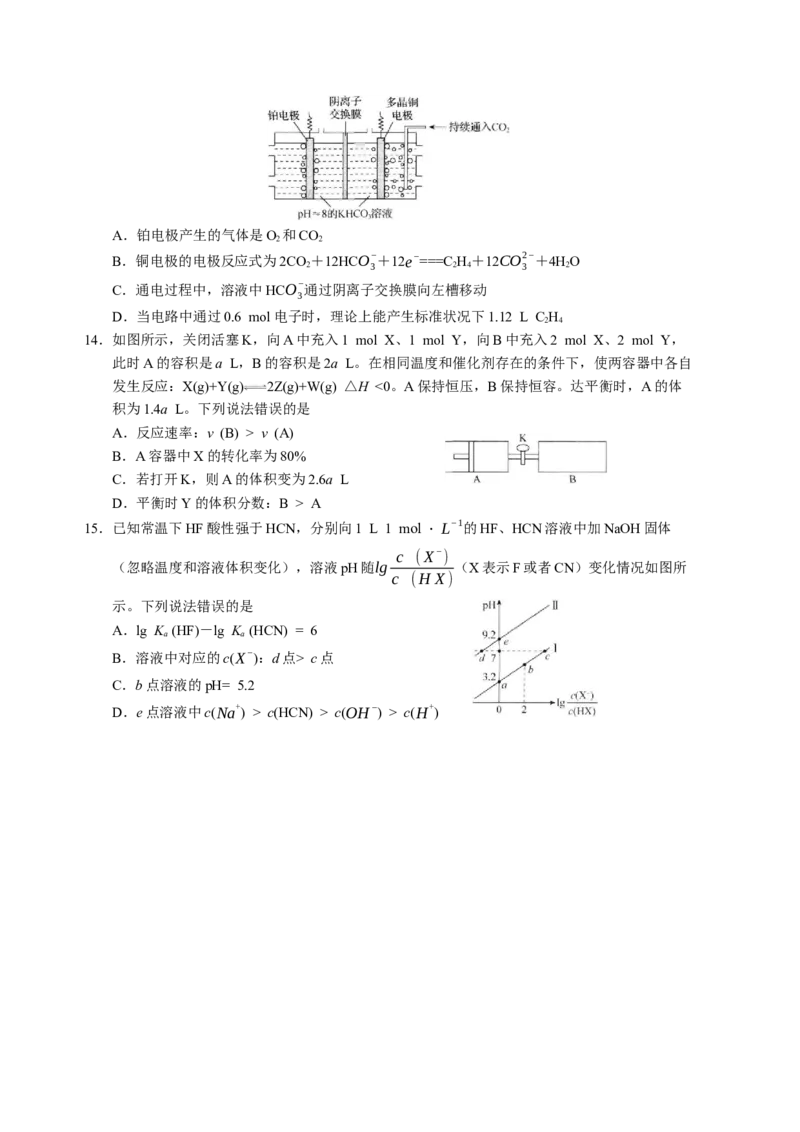
8.某兴趣小组利用工业废弃的铁铜合金制备碱式碳酸铜的流程如图。下列叙述错误的是
A.“溶解”时发生了氧化还原反应
B.“过滤1”所得的滤液中的溶质主要为硫酸铜
C.“滤渣”的主要成分为氢氧化铁
D.“沉降”反应中溶液与NaCO 以不同方式或不同用量比混合不影响产品成分
2 3
9.常温下,将一定量稀硫酸逐滴滴入高铁酸钠(Na FeO)溶液中,溶液中含铁微粒存在如下平衡:
2 4
FeO2− HFeO− HFeO H FeO+。各微粒的物质的量分数δ(X)随pOH变化如
4 4 2 4 3 4
图。下列说法正确是
A.Ⅲ代表HFeO−的变化曲线
4B.a、b、c三点水的电离程度相等
K K
C. 2 < 3
K K
1 2
D. a点:c(Na+ )+c(H+ )+c(H FeO+ ) = c(OH−)+2c(FeO2− )+3c(HFeO− )
3 4 4 4
10.某反应可有效降低汽车尾气污染物的排放,其反应热△H =-620.9 kJ · mol−1。一定条件下
该反应经历三个基元反应阶段,反应历程如图所示(TS表示过渡态)。下列说法正确的是
A.△E = 306.6 kJ · mol−1
B.三个基元反应中只有③是放热反应
C.该化学反应的速率主要由反应②决定
D.该过程的总反应为2CO+2NO === N+2CO
2 2
11.T ℃时,CdCO 和Cd(OH) 的沉淀溶解平衡曲线如图所示。
3 2
已知pCd2+为Cd2+浓度的负对数,pN为阴离子浓度的负对
数。下列说法正确的是
A.曲线I是CdCO 的沉淀溶解平衡曲线
3
B.加热可使溶液由X点变到Z点
C.Y点对应的Cd(OH) 溶液是过饱和溶液
2
D.T ℃,在CdCO(s)+2OH−(aq) Cd(OH) (s)+CO2− (aq)平衡体系中,平衡常数K=102
3 2 3
12.常温下,向某浓度的HA溶液中加入NaOH(s),保持溶液体积和温度不变,测得pH与M
2
{ [ c (A2− ) ]}
M=−lg c (H A)或−lg c (A2− )或−lg 变化如图所示。下列说法错
2 c (H A− )
误的是
A.常温下,HA电离平衡常数K 为10−1.08
2 al
B.a点时,c (H A− )+2c (H A) > 10−3.05-10−10.95
2
C.NaHA溶液中c(Na+ ) > c (H A− ) > c (A2− ) > c (H A)
2
D.b点时,满足c(Na+ ) < 3c (A2− )
13.科学家利用多晶铜高效催化电解CO 制乙烯,原理如图所示。已知:电解前后电解液浓度几乎
2
不变。下列说法错误的是A.铂电极产生的气体是O 和CO
2 2
B.铜电极的电极反应式为2CO+12HCO−+12e−===C H+12CO2−+4HO
2 3 2 4 3 2
C.通电过程中,溶液中HCO−通过阴离子交换膜向左槽移动
3
D.当电路中通过0.6 mol电子时,理论上能产生标准状况下1.12 L C H
2 4
14.如图所示,关闭活塞K,向A中充入1 mol X、1 mol Y,向B中充入2 mol X、2 mol Y,
此时A的容积是a L,B的容积是2a L。在相同温度和催化剂存在的条件下,使两容器中各自
发生反应:X(g)+Y(g) 2Z(g)+W(g) △H <0。A保持恒压,B保持恒容。达平衡时,A的体
积为1.4a L。下列说法错误的是
A.反应速率:v (B) > v (A)
B.A容器中X的转化率为80%
C.若打开K,则A的体积变为2.6a L
D.平衡时Y的体积分数:B > A
15.已知常温下HF酸性强于HCN,分别向1 L 1 mol · L−1的HF、HCN溶液中加NaOH固体
c (X− )
(忽略温度和溶液体积变化),溶液pH随lg (X表示F或者CN)变化情况如图所
c (H X)
示。下列说法错误的是
A.lg K (HF)-lg K (HCN) = 6
a a
B.溶液中对应的c(X−):d点> c点
C.b点溶液的pH= 5.2
D.e点溶液中c(Na+ ) > c(HCN) > c(OH−) > c(H+ )第Ⅱ卷(非选择题 共55分)
二、非选择题:本题共4小题,共55分。
16.(15分)氮、磷、铁、铜、钇在现代工农业、科技等领域中都有着广泛的应用。回答下列问
题:
(1)基态磷原子核外电子共有_____种空间运动状态。磷原子在成键时,使一个3s能级电子激发
进入3d能级而参与成键,写出该激发态磷原子的核外电子排布式_______。
(2)已知偏二甲肼[(CH )NNH]、肼(N H)均可作运载火箭的主体燃料,其熔沸点见表。
3 2 2 2 4
物质 熔点 沸点
偏二甲肼 -58℃ 63.9℃
肼 1.4℃ 113.5℃
偏二甲肼中氮原子的杂化方式为________,二者熔沸点存在差异的主要原因是
_________。
(3)N
H2+
只有一种化学环境的氢原子,结构如图所示。其中的大π键可表示为
4 6
______(分子中的大π键可用符号Πn表示,其中m代表参与形成的大π键原子
m
数,n代表参与形成的大π键电子数,如苯分子中的大π键可表示为Π6)。
6
(4) Cu2+可形成[Cu(X) ]2+,其中X代表CH-NH-CH-CH-NH 。1 mol [Cu(X) ]2+中,
2 3 2 2 2 2
VSEPR模型为四面体的非金属原子共有______mol。
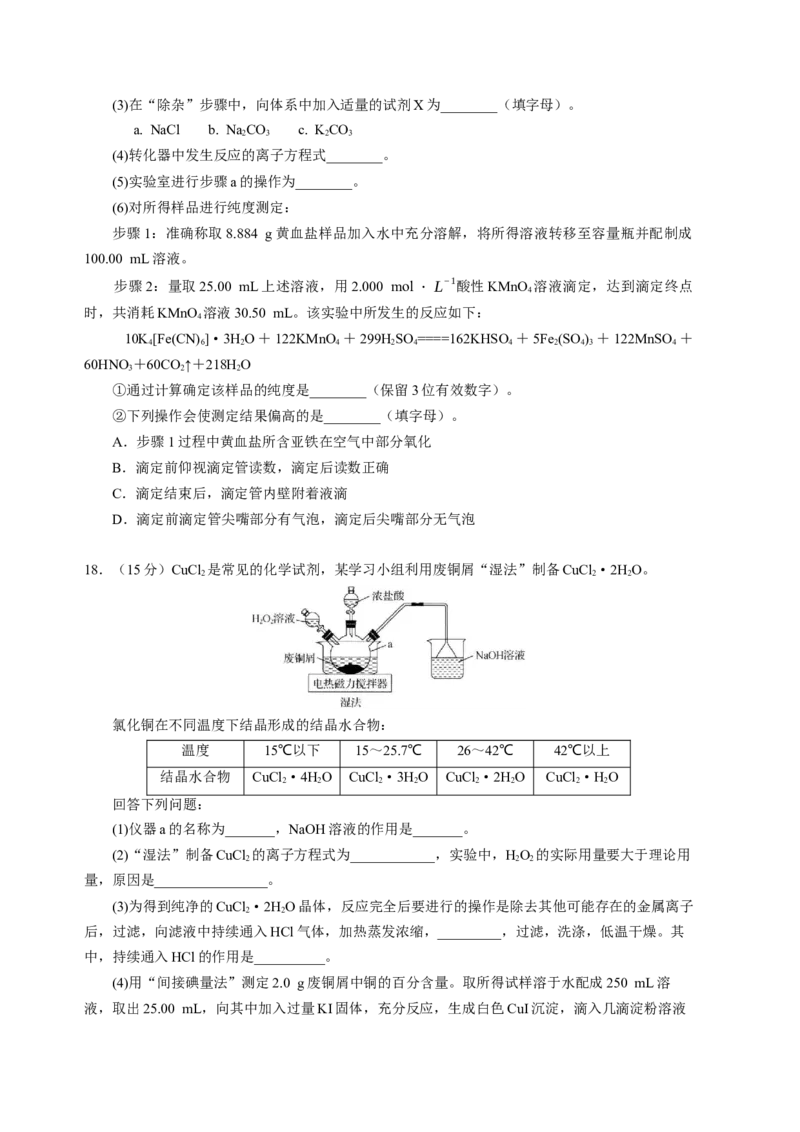
(5)铁酸钇是一种典型的单相多铁性材料,其正交相晶胞结构如图。
1
铁酸钇的化学式为______。已知1号O原子分数坐标为(0,0, ),2号O原子分数坐标为
4
1 1 1
( , −m, −n),则3号Fe原子的分数坐标为______。已知铁酸钇的摩尔质量为M g·mol−1,
2 2 4
晶体密度为ρ g·cm−3,阿伏加德罗常数的值为N ,该晶胞的体积为____pm3(列出表达式)。
A
17.(13分)亚铁氰化钾晶体,化学式为K[Fe(CN) ]·3HO(M =422 g·mol−1),俗名黄血盐,
4 6 2
可溶于水,不溶于乙醇,在电镀、食品添加剂等方面有广泛用途。用含NaCN的废液合成黄血
盐的主要工艺流程如图所示:
(1)实验室用绿矾晶体配制硫酸亚铁溶液时,为了防止其变质需要添加的试剂为________。
(2)反应器中发生的主要反应的化学方程式为________。(3)在“除杂”步骤中,向体系中加入适量的试剂X为________(填字母)。
a. NaCl b. NaCO c. KCO
2 3 2 3
(4)转化器中发生反应的离子方程式________。
(5)实验室进行步骤a的操作为________。
(6)对所得样品进行纯度测定:
步骤1:准确称取8.884 g黄血盐样品加入水中充分溶解,将所得溶液转移至容量瓶并配制成
100.00 mL溶液。
步骤2:量取25.00 mL上述溶液,用2.000 mol · L−1酸性KMnO 溶液滴定,达到滴定终点
4
时,共消耗KMnO 溶液30.50 mL。该实验中所发生的反应如下:
4
10K[Fe(CN) ]·3HO+122KMnO +299HSO====162KHSO +5Fe (SO) +122MnSO +
4 6 2 4 2 4 4 2 4 3 4
60HNO+60CO↑+218HO
3 2 2
①通过计算确定该样品的纯度是________(保留3位有效数字)。
②下列操作会使测定结果偏高的是________(填字母)。
A.步骤1过程中黄血盐所含亚铁在空气中部分氧化
B.滴定前仰视滴定管读数,滴定后读数正确
C.滴定结束后,滴定管内壁附着液滴
D.滴定前滴定管尖嘴部分有气泡,滴定后尖嘴部分无气泡
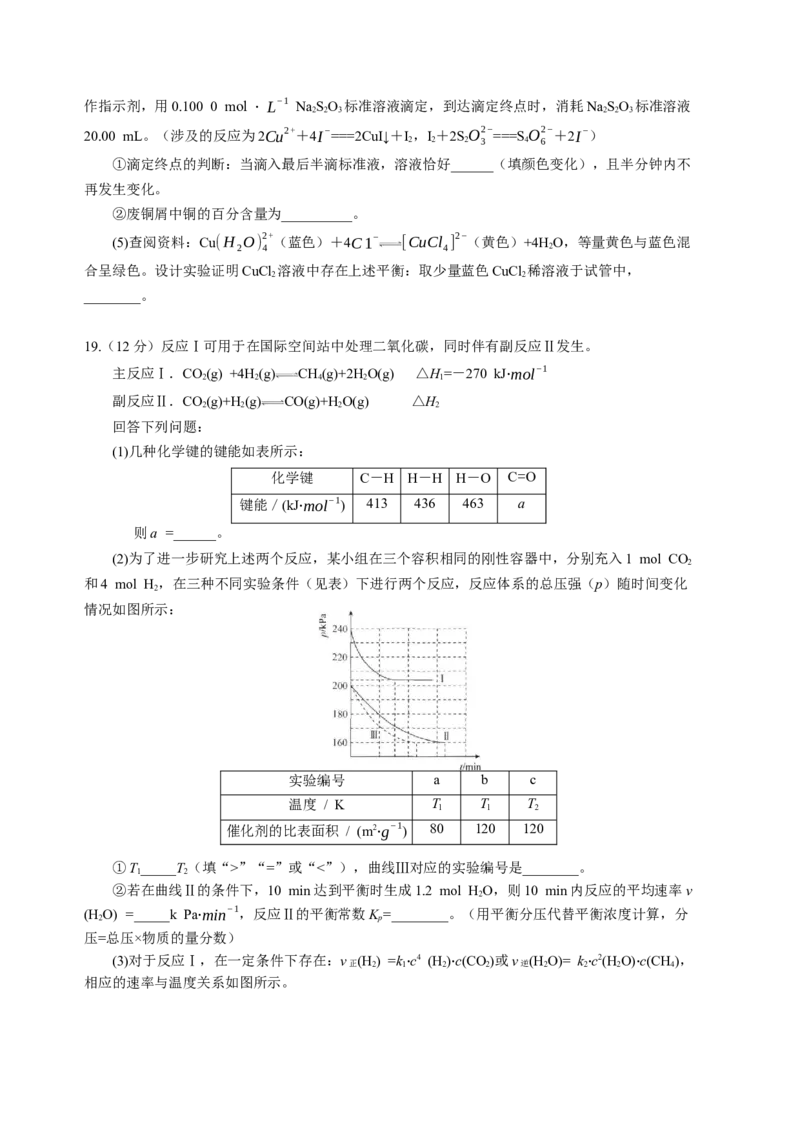
18.(15分)CuCl 是常见的化学试剂,某学习小组利用废铜屑“湿法”制备CuCl ·2HO。
2 2 2
氯化铜在不同温度下结晶形成的结晶水合物:
温度 15℃以下 15~25.7℃ 26~42℃ 42℃以上
结晶水合物 CuCl·4HO CuCl ·3HO CuCl ·2HO CuCl ·HO
2 2 2 2 2 2 2 2
回答下列问题:
(1)仪器a的名称为_______,NaOH溶液的作用是_______。
(2)“湿法”制备CuCl 的离子方程式为____________,实验中,HO 的实际用量要大于理论用
2 2 2
量,原因是________________。
(3)为得到纯净的CuCl ·2HO晶体,反应完全后要进行的操作是除去其他可能存在的金属离子
2 2
后,过滤,向滤液中持续通入HCl气体,加热蒸发浓缩,_________,过滤,洗涤,低温干燥。其
中,持续通入HCl的作用是__________。
(4)用“间接碘量法”测定2.0 g废铜屑中铜的百分含量。取所得试样溶于水配成250 mL溶
液,取出25.00 mL,向其中加入过量KI固体,充分反应,生成白色CuI沉淀,滴入几滴淀粉溶液作指示剂,用0.100 0 mol · L−1 NaSO 标准溶液滴定,到达滴定终点时,消耗NaSO 标准溶液
2 2 3 2 2 3
20.00
mL。(涉及的反应为2Cu2++4I−===2CuI↓+I,I+2SO2− ===SO2−+2I−)
2 2 2 3 4 6
①滴定终点的判断:当滴入最后半滴标准液,溶液恰好______(填颜色变化),且半分钟内不
再发生变化。
②废铜屑中铜的百分含量为__________。
(5)查阅资料:Cu(H O) 2+ (蓝色)+4C1− [CuCl ] 2−(黄色)+4H O,等量黄色与蓝色混
2 4 4 2
合呈绿色。设计实验证明CuCl 溶液中存在上述平衡:取少量蓝色CuCl 稀溶液于试管中,
2 2
________。
19.(12分)反应Ⅰ可用于在国际空间站中处理二氧化碳,同时伴有副反应Ⅱ发生。
主反应Ⅰ.CO(g) +4H (g) CH(g)+2HO(g) △H=-270 kJ·mol−1
2 2 4 2 1
副反应Ⅱ.CO(g)+H(g) CO(g)+HO(g) △H
2 2 2 2
回答下列问题:
(1)几种化学键的键能如表所示:
化学键 C-H H-H H-O C=O
键能/(kJ·mol−1) 413 436 463 a
则a =______。
(2)为了进一步研究上述两个反应,某小组在三个容积相同的刚性容器中,分别充入1 mol CO
2
和4 mol H,在三种不同实验条件(见表)下进行两个反应,反应体系的总压强(p)随时间变化
2
情况如图所示:
实验编号 a b c
温度 / K T T T
l l 2
催化剂的比表面积 / (m2·g−1) 80 120 120
①T_____T(填“>”“=”或“<”),曲线Ⅲ对应的实验编号是________。
1 2
②若在曲线Ⅱ的条件下,10 min达到平衡时生成1.2 mol HO,则10 min内反应的平均速率v
2
(H O) =_____k Pa·min−1,反应Ⅱ的平衡常数K =________。(用平衡分压代替平衡浓度计算,分
2 p
压=总压×物质的量分数)
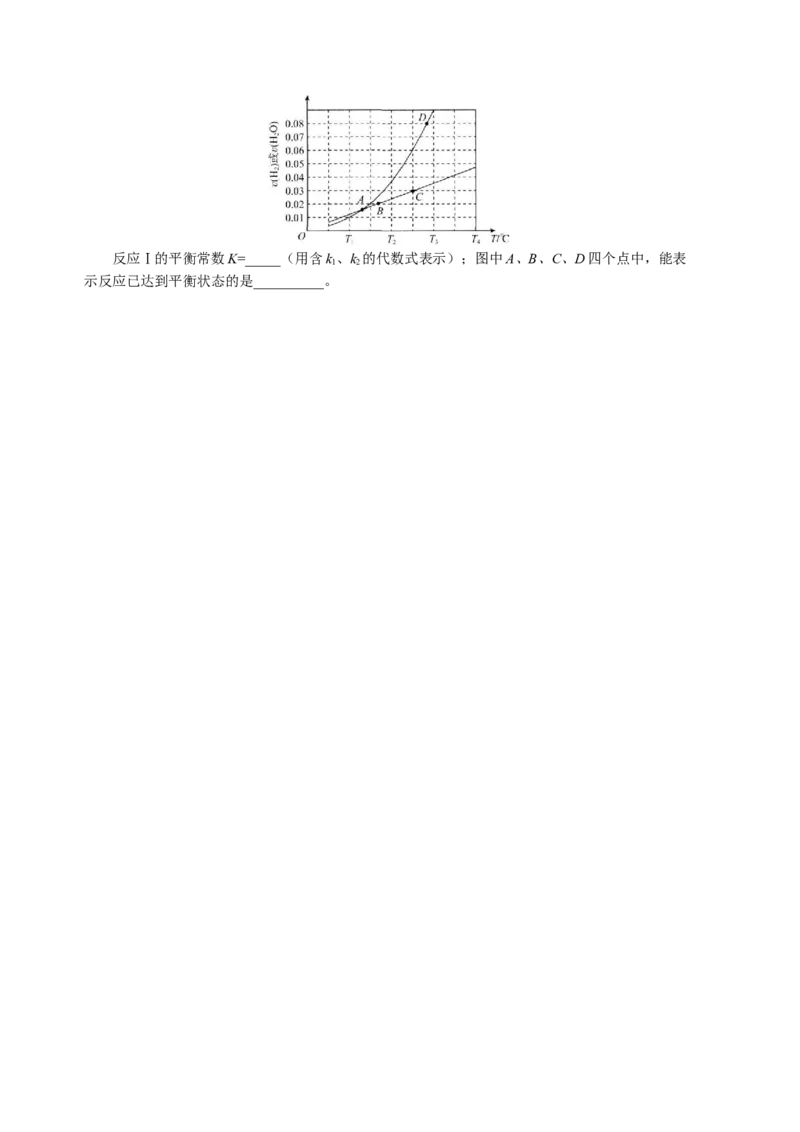
(3)对于反应Ⅰ,在一定条件下存在:v (H ) =k·c4 (H )·c(CO)或v (H O)= k·c2(H O)·c(CH),
正 2 1 2 2 逆 2 2 2 4
相应的速率与温度关系如图所示。反应Ⅰ的平衡常数K=_____(用含k、k 的代数式表示);图中A、B、C、D四个点中,能表
1 2
示反应已达到平衡状态的是__________。化学参考答案一、选择题
1.A【解析】根据题意,磺强水制法为KNO 受热分解生成NO 、O ,S与O 加热反应生成SO ,然后发
3 2 2 2 2
生反应NO +SO NO+SO ,SO +H O==HSO ,由此解答。由分析可知,“焚硝磺”时,N和S的
2 2 3 3 2 2 4
化合价均发生了变化,A项正确;磺强水是硫酸,硫酸属于难挥发的强电解质,B项错误;0.01 mol ·
L−1的磺强水溶液中c(H+) = 0.02 mol · L−1,pH<2,C项错误;磺强水溶液中存在水分子,D项错
误。
2.B【解析】温度升高,促进水的电离,水的离子积增大,因此100℃时水的离子积大于1×10−14,100℃
时,pH=12的NaOH溶液中,c(H+ ) = 1×10−12 mol · L−1,则c(OH−) > 0.01 mol · L−1,A错误;
CHCOONa与NaOH不发生反应,常温下,相同pH的两种溶液混合后,溶液pH仍为9,B正确;如
3
果AOH为弱碱,则pH=13的AOH物质的量浓度大于0.1 mol · L−1,等体积混合后,溶质为AOH和
ACl,此时溶液可能显碱性,C错误;冰醋酸加水稀释,促进醋酸的电离,醋酸的电离程度增大,随着
水量的增大,c(H+ )先增大后减小,D错误。
3.C【解析】向0.01 mol · L−1 NH HSO 溶液中滴加NaOH溶液,若加入等物质的量的NaOH,溶液呈
4 4
酸性,若呈中性,则加入的NaOH应多于硫酸氢铵,但小于硫酸氢铵物质的量的 2倍,溶液中存在
NH+ 和NH ·H O,故有c(Na+ ) > c(SO2− ) > c(NH+ ) > c(OH−) = c(H+ ),A正确;CuS不溶于稀硫
4 3 2 4 4
酸,说明CuS溶解产生的S2−不足以与H+发生反应生成HS气体,而FeS溶于稀硫酸,说明FeS溶解产
2
生的S2−可以与H+发生反应生成HS气体,导致固体不断溶解,证明K (FeS) > K (CuS),B正确;向
2 sp sp
c(NH+
)
盐酸中加入氨水至中性,则 c(H+ ) =c (OH−),由电荷守恒可知,溶液中 4 =1,C错误;
c(Cl−
)
NaHCO
溶液中,根据电荷守恒c(Na+ )+c(H+
)
=2c(CO2− )+c(HCO− )+c(OH−),根据物料守恒c(Na+
3 3 3
) = c(CO2− )+c(HCO− )+c(H CO),故c(H+ )+c(H CO) =c(OH−)+c(CO2− ),D正确。
3 3 2 3 2 3 3
4.D【解析】常用酸性 KMnO 溶液标定摩尔盐,氧化性MnO− > Fe3+,用过二硫酸钠可使
4 4
MnO− 全部再生,氧化性S O2− > MnO−,故氧化性S O2− > MnO− > Fe3+,A 正确;
4 2 8 4 2 8 4
KMnO 溶液具有氧化性,摩尔盐溶液呈酸性,滴定时,KMnO 溶液和摩尔盐溶液都选用酸式滴定管盛
4 4
装,B正确;根据过二硫酸结构图可知,中心硫原子价层电子对数为4,则S O2−中含有两个四面体结
2 8
构,C正确;滴定过程中,根据化合价升降相等,可知2Fe2+~S O2−~2SO2−,消耗的摩尔盐和过二
2 8 4
硫酸钠物质的量之比为2:1,D错误。
5.C【解析】W、X、Y、Z是原子序数依次增大的短周期主族元素,由 W、Y同主族,W、Y分别形成3
个、5个共价键可知,W为N元素、Y为P元素;抗癌药物中X形成2个共价键,则X为O元素;Y、
Z的最外层电子数之和是X的最外层电子数的2倍,则Z为Cl元素。氨与氯气反应生成氮气和氯化
铵,反应中会产生大量白烟,故A正确;同周期元素,从左到右第一电离能呈增大趋势,氮原子的 2p
轨道为半充满稳定结构,第一电离能大于相邻元素,则氧元素的第一电离能小于氮元素,故B正确;
三氯化氮和三氯化磷的空间构型都为三角锥形,氮元素的电负性强于磷元素,氮原子的原子半径小于
磷原子,三氯化氮中成键电子对间的斥力大于三氯化磷,所以三氯化氮键角大于三氯化磷,故C错误;臭氧和二氧化氯都有强氧化性,可用于自来水消毒, 故D正确。
6.B【解析】Ba(OH) 和NaHCO 在溶液中均完全电离,均属于强电解质,故A正确;A→B加入NaHCO
2 3 3
的物质的量小于Ba(OH) 的物质的量,发生的反应为Ba2+ +2OH−+HCO− ==BaCO↓+H O,故B错误;
2 3 3 2
B→C加入的NaHCO 继续消耗氢氧根离子,C点两者恰好完全反应,因此B→C溶液中c(OH−)减小,
3
故C正确;酸或碱抑制水的电离,盐类水解促进水的电离,A点溶液是Ba(OH) 溶液,水的电离受到抑
2
制,电离程度最小,B点Ba(OH) 反应一半,C点Ba(OH) 和NaHCO 恰好完全反应,因此水的电离程
2 2 3
度A 5×10−8 mol·L−1
√3×10−7
,故A正确;NaA溶液中存在A−的水解平衡和水的电离平衡,溶液中A−浓度越大,溶液中OH−与HA
c(HA) c(OH− ) c2 (OH− )
的浓度越接近,A−的水解常数K ≈ ≈ ,由图可知,A−浓度较大时K ≈
h c (A− ) c (A− ) h
1×10−10,数量级为10−10,故B错误;NaA溶液中存在质子守恒关系c(HA)+c(H+) = c(OH−),故C
正确;由图可知,x点溶液中A−浓度为3×10−4 mol·L−1,溶液中氢氧根离子浓度为2×10−7 mol·L−1,
由C项分析可知NaA溶液中c(HA)+c(H+ ) = c(OH−),溶液中HA的浓度小于氢氧根离子浓度,氢离
子浓度为5×10−8 mol · L−1,则溶液中各微粒浓度的大小顺序为c(Na+ ) > c(A−) > c(HA) > c(H+ ),
故D正确。
8.D【解析】废弃的铁铜合金中加入稀硫酸和双氧水溶解,得到硫酸铁、硫酸铜的混合溶液,之后加入
CuO调节pH除去Fe3+,过滤除去Fe(OH) 沉淀,加入碳酸钠沉降得到碱式碳酸铜,过滤得到产品。溶
3
解过程中双氧水在酸性环境中可以将Fe、Cu氧化,A正确;根据分析可知,加入CuO调节pH可以除
去Fe3+,所得滤液中的溶质主要为硫酸铜,B、C正确;“沉降”反应中溶液是CuSO 溶液,与NaCO
4 2 3
的混合方式应该是将NaCO 加入CuSO。溶液中,如果将CuSO 溶液加入NaCO 溶液中,将会生成氢
2 3 4 2 3
氧化铜沉淀,影响碱式碳酸铜的生成,D错误。
9.C【解析】本题考查含铁微粒分布分数图像分析,稀硫酸逐滴滴入高铁酸钠(Na FeO)溶液中,溶液
2 4
pOH不断增大,OH−的浓度不断减小,可知I代表FeO2−的变化曲线,Ⅱ代表HFeO−的变化曲线,Ⅲ
4 4
代表HFeO 的变化曲线,Ⅳ代表H FeO+ 的变化曲线。由分析可知,Ⅱ代表HFeO−的变化曲线,故A
2 4 3 4 4
项错误;a、b、c三点溶液中微粒成分不同,溶液pOH不同,对水的电离影响程度不同,故B错误;
c(OH− )∙c(HFeO−
)
FeO2−+HO HFeO−+OH−的平衡常数K = 4 ,a点c (FeO2− )=
4 2 4 1 c (FeO2− ) 4
4
c(HFeO− ),pOH=1.6,则K =c(OH−)=10−1.6,同理可知HFeO−+HO HFeO+OH−的平衡常数
4 1 4 2 2 4K K
K =10−5.2,HFeO+HO H FeO++OH−的平衡常数K =10−7.3,由此推出 2 < 3,故C正
2 2 4 2 3 4 3 K K
1 2
确;a点溶液中c (FeO2− )=c(HFeO− ),溶液中存在电荷守恒c(Na+ )+c(H+ )+c(H FeO+ ) = c(OH−)
4 4 3 4
+2c(FeO2− )+c(HFeO− )+2c(SO2− ),从O到a点溶液中发生反应2Na FeO+HSO ===
4 4 4 2 4 2 4
2NaHFeO +NaSO,溶液中c(SO2− )≠c(HFeO− ),则a点溶液中c(Na+ )+c(H+ )+c(H FeO+ ) ≠c(
4 2 4 4 4 3 4
OH−)+2c(FeO2− )+3c(HFeO− ),故D项错误。
4 4
10.D【解析】总反应=反应①+反应②+反应③,△H+△H+△H =-620.9 kJ · mol−1,即199.2 kJ
1 2 3
· mol−1-513.5 kJ · mol−1+248.3kJ · mol−1-△E=-620.9 kJ · mol−1,△E = 554.9kJ · mol−1
,故A错误;由图可知,三个基元反应中,反应②和反应③的反应物总能量大于生成物的总能量,均
属于放热反应,故B错误;正反应活化能最大的是反应①,活化能越大反应速率越慢,整个反应由最
慢的一步决定,则该化学反应的速率主要由反应①决定,故C错误;由始态和终态可知,该过程的总
反应为2CO+2NO === N+2CO,故D正确。
2 2
11.D【解析】pCd2++2pOH=-lg K [Cd(OH) ]、 pCd2++pCO2− =-lg K (CaCO),根据斜率可知,
sp 2 3 sp 3
CdCO 的沉淀溶解平衡曲线应为曲线Ⅱ,A错误。由A项分析可知,曲线I是Cd(OH) 的沉淀溶解平
3 2
衡曲线,Cd(OH) (s) Cd2+(aq)+2OH−(aq),加热平衡正向移动,Cd2+、OH−浓度均增大,而X点与
2
Z点OH−浓度相同,B错误。曲线上的点达到了沉淀溶解平衡,pCd2+为Cd2+浓度的负对数,pN为阴离
子浓度的负对数,则数值越大,离子浓度越小,Y点在曲线上方,说明离子浓度小,故为不饱和溶液,
C错误。T℃,由图可知,pN=4时,CdCO 中pCd2+为8,即K ( CdCO ) = c(CO2− )c(Cd2+)= 10−12;
3 sp 3 3
pN=4时,Cd(OH) 中pCd2+为6,即K [Cd(OH) ]=c2(OH−) c(Cd2+) = 10−14;在CdCO (s)+2OH−(aq)
2 sp 2 3
c(CO2−
)
c(CO2− )c(Cd2+
)
Cd (OH) (s)+CO2− (aq)平衡体系中,平衡常数K= 3 = 3 =
2 3 c2 (OH−
)
c2 (OH− )c(Cd2+
)
K (CdCO )
sp 3
=
102,D正确。
K [Cd(OH) ]
sp 2
12.A【解析】向某浓度HA溶液中加入NaOH溶液时,由于二者发生反应,所以HA逐渐减少, -lg
2 2
c(H A)会逐渐增大,所以图中曲线①为-lg c(H A)与pH的变化关系;HA H++H A−,H A−
2 2 2
H++A2−,A2−会逐渐增大,−lg c (A2− )会逐渐减小,但是不会等于0,所以曲线②为
[ c (A2− ) ]
−lg c(A2− )与pH的变化关系;曲线③则是−lg 与pH的变化关系,以此解题。电离常
c (H A− )
c(H+ )⋅(H A− ) c(H+ )⋅(A2− ) c2 (H+ ).c(A2− )
数的表达式为K = ,K = ,K ⋅K = ,当
a1 c(H A) a2 c(H A− ) a1 a2 c(H A)
2 2
pH=3.05时,−lg c (A2− )与-lg c(H A)相等,即c(A2− )=c(H A),可得K ⋅K =( 10−3.05)2=
2 2 a1 a2
c(A2−
)
10−6.1;由曲线③可知,当pH=5.3时,−lg[ ]=0,即c(A2− )=c(H A− ),即K = 10−5.3
c(H A− ) a2
10−6.1
,所以K = =10−0.8 ,A错误;a点时,根据电荷守恒c(Na+ )+c(H+ )= 2c (A2− )+c(H A− )
a1 10−5.3+c(OH−),可得c (H+ )−c(OH−) = 2c (A2− )+c(H A− )−c(Na+ ),a点时,pH=3.05,所以c(H+ )
= 10−3.05,c(OH−)=10−10.95,因为c(H A)=c (A2− ),所以 10−3.05−10−10.95=2c(H A)+
2 2
c(H A− )−c(Na+ ),因为c(Na+ )>0,所以c(H A− )+2c(H A) > 10−3.05− 10−10.95,B正确;NaHA
2
溶液中H A−既存在电离又存在水解,所以c(Na+ ) > c(H A− ),H A− H+ +A2−,H A−+HO
2
H A+ OH−, c(A2− ) 与c(H A) 的大小取决于电离和水解的程度,K = 10−5.3, H A−的水解
2 2 a2
K 10−14
常数K = w = =10−13.2<10−5.3 ,所以H A−的水解程度小于H A−的电离程度,所以c(H A)<
ℎ K 10−0.8 2
a1
c(A2− ),故NaHA溶液中c(Na+) > c(H A− ) > c (A2− ) >c(H A),C正确;b点时,根据电荷守
2
[ c (A2− ) ]
恒c(Na+ )+c(H+ )=2c (A2− )+c(H A− )+c(OH−),此时pH=5.3,−lg =0,即
c (H A− )
c (A2− )=c(H A− ),所以c(Na+)+c(H+ )=3(A2− )+c(OH−),因为c(OH−) v(A),A正确;B项,设平衡时X转化了b mol,根据三段式:
X(g)+Y(g) 12Z(g)+W(g)
起始/mol 1 1 0 0
转化/mol b b 2b b
平衡/mol 1−b 1−b 2b b
2+b 0.8mol
由题意得, =1.4,b=0.8,所以X的转化率a(X)= ×100%=80%,B正确;C项,若
2 1mol
m 1.4aL
打开K,达到新平衡时等效为A中达到的平衡,设总体积为m,则 = ,m=4.2aL,所以A的
6 2
体积应变为4.2aL−2aL=2.2aL,C错误;D项,由于B中压强大,平衡左移,所以B中Y的体积
分数大,D正确。
15.B【解析】由题干信息可知,常温下HF酸性强于HCN,即K (HF)>K (HCN),当横坐标为0时,即
a a
c (F− ) c (CN− )
lg =0或者lg =0,即c (F− )=c(H F)或c (CN− )=c (HCN),则有
c (H F) c (HCN)
c (F− )c (H+ ) c (CN− )c (H+ )
K (HF)= =c (H+ )=10−3.2 ,K (HCN)= =c (H+ )=10−9.2 ,即I
a
c (H F)
a
c (HCN)
代表HF溶液中的变化,Ⅱ代表HCN溶液中的变化,据此分析解题。由分析可知,K (HF)=10−3.2,
ac (CN− )
K (HCN)=10−9.2,则lgK (HF)−lg K (HCN)=6,A正确。d点lg <0,即
a a a
c (HCN)
c (CN− )0,即c (F− )>c (H F),由于c (F− )+c (H F) =1 mol · L−1,所以
c (H F)
c (F− )>0.5 mol · L−1,故溶液中对应的c (X− ):c点 > d点,B错误。由分析可知,K (HF)
a
c (F− ) c(H F)K (HF)
=10−3.2,b点溶液中lg =2,则c(H+ )= a =10−5.2 ,故b点对应溶液的
c (H F) c (F− )
c (CN− )
pH=5.2,C正确。由图像可知,e点溶液中pH为9.2,c (H+ )c(H+
),则有c(Na+ )>c (CN− )>c(OH−)>c(H+ ),故c(Na+ ) > c(HCN) > c(OH−) > c(H+ ),D正确。
二、非选择题
16.(1)9(1分)1s2 2s2 2p6 3s13p3 3d1(2分)
(2) sp3(1分) 肼分子间氢键数目多于偏二甲肼 (2分)
(3)Π6(2分)
4
(4)10(2分)
1 1 3 2M
(5) YFeO(1分) ( , +m, )(2分) ×1030 (2分)
3 2 2 4 N ⋅ρ
A
【解析】(1)基态磷原子核外电子排布式为1s2 2s2 2p6 3s23p3 ,原子核外每一个原子轨道即一种电子
空间运动状态,s能级有1个轨道,p能级有3个轨道,所以共有9个轨道,即9种空间运动状态。磷原子
在成键时,使一个3s能级电子激发进入3d能级,则激发态磷原子的核外电子排布式为1s2 2s2 2p6 3s13p3
3d1。
(2)偏二甲肼中的氮原子均有3个σ键和1个孤电子对,所以氮原子的杂化方式为sp3。NH 分子和偏二
2 4
甲肼均存在分子间氢键,但NH 分子间氢键数目多于(CH)NNH,所以NH 的熔沸点高于(CH)NNH。
2 4 3 2 2 2 4 3 2 2
(3)由N
H2+
的结构可知,每个N原子形成3个σ键,且4个N原子失去了2个电子,最后N原子剩余
4 6
价电子数为5×4−2−3×4=6个,即参与形成大π键电子数为6,原子数为4,可表示为Π6。
4
(4)[Cu(X) ]2+中C、N原子共5个且价层电子对数均为4,即VSEPR模型为四面体,1 mol
2
[Cu(X) ]2+中,VSEPR模型为四面体的非金属原子有2×5 mol =10 mol。
2
1 1
(5)由晶胞结构图,利用均摊法计算可得Fe原子个数为2,Y原子个数为8× +4× =2个,O原子个
8 4
1
数为8× +4=6个,故铁酸钇的化学式为YFeO,根据晶胞结构图与1、2号原子的分数坐标可知,3号
4 3
1 1 3 m 2M
Fe原子的分数坐标为( , +m, )。由公式V = 可得晶胞体积为 ×1030pm3 。
2 2 4 ρ N ⋅ρ
A17.(1)铁粉、稀硫酸(2分)
(2) 6NaCN+FeSO+CaCl ===Na[Fe(CN) ]+CaSO↓+2NaCl(2分)
4 2 4 6 4
(3) b(1分)
(4) 4K++[Fe(CN) ] 4−+3HO=== K[Fe(CN) ]·3H O↓(2分)
6 2 4 6 2
(5)用玻璃棒引流向漏斗中加入乙醇至没过沉淀,待乙醇自然流下,重复操作2~3次(2分)
(6)①95.0%(2分) ②CD(2分)
18.(1)三颈烧瓶(1分) 吸收挥发出来的HC1,防止污染空气(2分)
(2) Cu+HO+2H+ Cu2++2HO(2分)
2 2 2
HO 受热或在Cu2+的催化作用下会分解导致损耗(2分)
2 2
(3)降温至26~42℃结晶(1分)
抑制Cu2+水解、增大Cl−浓度,有利于CuCl ·2HO结晶(2分)
2 2
(4)①溶液蓝色褪去(1分) ②64%(2分)
(5)向其中加入少量NaCl固体,振荡,溶液由蓝色变为黄绿色(2分)
19.(1)745(2分)
4
(2)①<(1分) b(1分) ②4.8(2分) (2分)
9
k
(3) 1 (2分) C(2分)
2k
2
【解析】(1)根据反应热=反应物的总键能−生成物的总键能,
△H=-270 kJ·mol−1=2a kJ·mol−1+436kJ·mol−1×4-413 kJ·mol−1×4-463kJ·mol−1×4,则a= 745。
1
(2)①分析图表可知,曲线Ⅱ、Ⅲ对应同一温度TK,曲线I对应温度TK,曲线I先达到平衡,速率
1 2
大,对应温度高,故T