文档内容
2022 年湖北省荆荆宜三校高三上学期 9 月联考
高三化学答案
一、选择题:本题共15小题,每小题3分,共45分。
1. 答案A
A.青铜神树表面的绿色物质的主要成分为Cu (OH) CO ,A正确;B.黄金面具保存良好,
2 2 3
是因为单质金化学性质不活泼,B 错误;C.丝绸的主要成分为蛋白质,C 错误;D.陶瓷
以黏土(主要成分为含水的铝硅酸盐)为主要原料制得,D错误。
2. 答案 B
A. 是四氯化碳分子球棍模型,A错误;C.葡萄糖的实验式CH O,C错误;
2
D.HClO的结构式为H-O-Cl,D错误。
3. 答案B
青蒿素的分子式为C H O ,B错误;其他选项正确。
15 22 5
4. 答案 A
B.NH HCO 溶液和足量NaOH溶液混合NH+ +HCO- +2OH-=CO2- +H O + NH ·H O,B错
4 3 4 3 3 2 3 2
误;C.Cl 通入水中Cl +H O HClO + H+ + Cl-,C错误;D.FeCl 溶液中加Na O 后会
2 2 2 3 2 2
生成Fe(OH) ,D错误。
3
5. 答案B
B.过氧化钠与水反应生成氧气的同时生成强碱NaOH,鱼池缺氧时,不可以用过氧化钠
做供氧剂,B错误。
6. 答案D
A. 铝热剂加入盐酸再加入KSCN溶液,溶液变红色,铝热剂中金属氧化物可能是Fe O 或
2 3
Fe O ,A错误;B.将水蒸气通过灼热的铁粉,生成黑色Fe O ,B错误;C.加入NaNO
3 4 3 4 3
后,发生反应3Cu + 8H+ + 2NO- =3Cu2+ + 2NO↑ + 4H O,NaNO 不是催化剂,C错误。
3 2 3
7. 答案B
X、Y、Z、M分别为H、C、N、S。A.简单氢化物的沸点NH > CH ,A错误;B.第一
3 4
电离能:N > O > S,B正确; C.N H 中,N原子采用sp3杂化,所有原子不在同一平面,
2 4
C错误;D.C、N、S的氧化物不一定为酸性氧化物,如CO,D错误。
8. 答案 B
A.HCO -、Al3+ 之间发生完全双水解反应,不能大量共存,A错误;B.使甲基橙变红的
3
溶液呈酸性,Mg2+、Na+、SO2−、NO− 在酸溶液中能够大量共存,B正确;C.pH=12的溶
4 3
液呈碱性,Fe2+不能在碱性溶液中大量存在,C错误;D.与铝反应产生大量氢气的溶液可
能呈酸性,也可能呈强碱性,NH+ 不能在碱性溶液中大量存在;NO− 在酸性条件下有强氧
4 3
化性,与铝反应不生成氢气,D错误。
9. 答案C
A.黑磷晶体中层与层之间的作用力是范德华力,A 错误;B.黑磷晶体中磷原子杂化方式
湖北省新高考联考体*化学答案(共4页)第1页为 sp3杂化,B 错误;C.黑磷、白磷、红磷都是磷元素形成的结构不同的单质,互为同素
异形体,C正确;D.黑磷晶体是混合晶体,D错误。
10. 答案C
A、B、D正确,碱性条件下,Cr O + 3H O + 4OH- ═ 2CrO2−+ 4H O,C错误。
2 3 2 2 4 2
11. 答案D
A. 尿素是极性分子,A错误;B. 尿素为有机物,B错误;C. 1 mol尿素中共价键数目为8
N ,C错误;D. 尿素中有酰胺键,在硫酸催化下水解,并生成CO 和硫酸铵,D正确。
A 2
12. 答案D
A.盐酸与氯酸钠会发生反应生成Cl ,溶解过程中不可用盐酸代替稀硫酸,A错误;
2
B.氧化性:H O < ClO < ClO-,B错误;C.发生器中鼓入空气的主要目的是稀释
2 2 2 3
ClO ,C错误;D.吸收塔内温度过高,H O 分解,NaClO 产率下降,D正确。
2 2 2 2
13. 答案B
A.上述循环过程中,Co的配位数为4或5,其配位数发生了变化,A正确;B.上述过程
中有C-O的断裂(如CO中碳氧三键最后变成碳氧双键),B错误;C.丙烯醛基化总反应
为CH CH=CH +CO+H →CH CH CH CHO,C正确;D.HCo(CO) 是该反应的催化剂,催
3 2 2 3 2 2 3
化剂可降低反应的活化能,D正确。
14. 答案B
A.电子不能从电解质溶液经过,A错误;B.充电时,P极反应式为:ZnMn O -2e-=
2 4
Zn2+ + 2MnO ,Q极反应式为:Zn2++2e-=Zn,依据转移电子守恒知,溶液中Zn2+也守
2
恒,溶液质量不变,B正确;C.放电时,P极反应为:Zn2++ 2MnO + 2e-=ZnMn O ,
2 2 4
C错误;D.充电时,a电极接外接电源正极,D错误。
15. 答案 D
A.根据图示知,a点时,pOH = -lgc(OH-) = 12.6,则c(OH-) = 10-12.6,c(H+) = 10-1.4,
水 水 水
pH = 1.4,A正确;B.随着NaOH溶液的滴入,b点、c点、d点溶液中水的电离程度逐渐增
大,B正确;C.e点,氢氧化钠过量,溶液为碱性,C正确;D.d点,溶液的溶质为Na X
2
,X2-水解呈碱性,又根据H X = H+ + HX-知,HX-只电离不水解,故Na X溶液中不存在
2 2
H X分子,根据物料守恒知c(Na+) = 2c(HX-) + 2c(X2-),D项错误。
2
二、非选择题:本题4小题,共55分。
16.(14分,除标注外每空2分)
(1)分液漏斗(1分) 增大Cl 和KOH溶液的接触面积,提高Cl 的利用率(1分)
2 2
(2)
湖北省新高考联考体*化学答案(共4页)第2页
5
3
mol
(3)缓慢滴加浓盐酸
(4) Fe(NO ) 3ClO- +2Fe3+ +10OH-=2FeO2- + 3Cl- + 5H O
3 3 4 2
(5) 4K FeO +10H O=4Fe(OH) ↓ +8KOH +3O ↑
2 4 2 3 2
(6) b【解析】(3)由于该反应放热,若反应率太快,单位时间放出的热量多,使反应体系温度升
高,可能生成KClO ,因此应缓慢滴加浓盐酸,以降低通入氯气的速率。
3
(4)根据题目信息,K FeO 在Fe3+和Fe(OH) 催化作用下发生分解,且K FeO 在酸性至弱碱
2 4 3 2 4
性条件下,能与水反应,因此,应将Fe(NO ) 饱和溶液缓慢滴加到KClO饱和溶液中。
3 3
(6)根据题目信息,K FeO 可溶于水、微溶于浓KOH溶液,因此用浓KOH洗涤可降低产
2 4
品溶解度,然后用异丙醇洗涤可除去产品表面的杂质离子并快速干燥。
17.(14分)
(1) 2-氯甲苯(或邻氯甲苯)(1分); 醛基(1分)
(2) FeCl (或Fe)、Cl (1分,没写全或见错无分) 取代反应(1分,只写取代不给分)
3 2
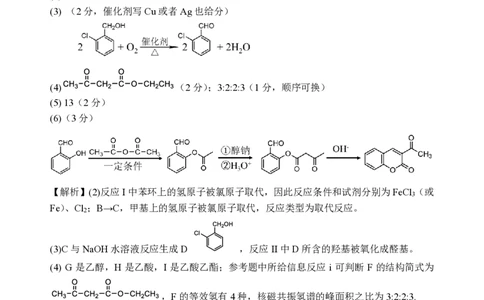
(3) (2分,催化剂写Cu或者Ag也给分)
(4) (2分);3:2:2:3(1分,顺序可换)
(5) 13(2分)
(6)(3分)
【解析】(2)反应I中苯环上的氢原子被氯原子取代,因此反应条件和试剂分别为FeCl (或
3
Fe)、Cl ;B→C,甲基上的氢原子被氯原子取代,反应类型为取代反应。
2
(3)C与NaOH水溶液反应生成D ,反应II中D所含的羟基被氧化成醛基。
(4) G 是乙醇,H 是乙酸,I 是乙酸乙酯;参考题中所给信息反应 i 可判断 F 的结构简式为
,F的等效氢有4种,核磁共振氢谱的峰面积之比为3:2:2:3.
(5)遇FeCl 溶液显紫色的D的同分异构体含有酚羟基,根据D的分子式,苯环上有-OH、
3
-CH 、-Cl三个取代基的同分异构体有10种,苯环上有-OH、-CH Cl两个取代基的同
3 2
分异构体有3种,因此,遇FeCl 溶液显紫色的D的同分异构体共有13种。
3
18.(13分,除标注外每空2分)
(1)适当升高温度;搅拌;将软锰矿烧渣进行粉碎(任意答对一种可得1分)
(2) 2Mn (SO ) + 2H O=4MnSO + O ↑+ 2H SO
2 4 3 2 4 2 2 4
(3) 4.7≤pH<8.1(写4.7~8.1也给分) 1.0×10-9.5
(4) 防止Mn(Ⅱ)在碱性环境中被空气氧化(1分)
湖北省新高考联考体*化学答案(共4页)第3页2MnSO +2NaHCO +H O=Mn (OH) SO + Na SO +2CO ↑ (漏掉“↑”扣1分)
4 3 2 2 2 4 2 4 2
(5) 27.8%
【解析】
(2)结合前后流程,“水浸”过程中Mn (SO ) 转化为MnSO ,生成的气体只能为O ,发生
2 4 3 4 2
反应:2Mn(SO ) + 2H O=2MnSO + O ↑ + 2H SO 。
4 2 2 4 2 2 4
(3)“调pH”时将溶液中的Fe3+、Al3+转化为Fe(OH) 、Al(OH) 沉淀除去,结合表中数据
3 3
pH范围为:4.7~8.1。当溶液中Al3+已沉淀完全时pH为4.7,c(OH-)= 1.0×10-9.3 mol/L,结
合K [Fe(OH) ])=10-37.4,则 c(Fe3+)= 1.0×10-9.5 mol/L
sp 3
(4) 通入惰性气体排除空气,防止了 Mn2+在碱性环境中被空气氧化;“合成”步骤中加入
NaHCO 溶液,发生反应:2MnSO +2NaHCO + H O=Mn (OH) SO + Na SO + 2CO ↑,然
3 4 3 2 2 2 4 2 4 2
后结晶、洗涤、干燥得到产品。
(5)根据反应过程得关系式:Mn2+~ MnO- ~5Fe2+
4
该产品中锰元素的质量分数为:
19.(14分,除标注外每空2分)
(1) 2NH + 2e-=H ↑ + 2NH﹣
3 2 2
(2) -90.5
(3) >(1分) 800℃时,K 远大于K
p2 p1
(4) AC
(5) 60% 3/4或0.75
(6)干冰可用于人工降雨;制碳酸饮料(1分,其他合理答案也可给分)
【解析】(1)产生H 的电极为阴极,得电子发生还原反应,根据元素守恒和电荷守恒配平得:
2
2NH + 2e- == H ↑ + 2NH﹣
3 2 2
(2)根据盖斯定律得:△H =△H -△H
3 1 2
(3)K 越大,正反应进行的程度越大,即该反应进行的越完全。
p
(4)使用高效催化剂可降低反应的活化能,增大活化分子百分数,加快化学反应速率,A 正
确;该反应正向为放热反应,则反应物总能量大于生成物总能量,B错误;M=m/n,该反应
前后气体质量守恒,反应前后气体分子数发生变化,气体平均相对分子质量为变量,变量不
变达平衡,C正确;反应的化学平衡常数只受温度影响,故增大压强,反应的化学平衡常数
不变,D错误。
(5)根据题目信息列出三段式:
CO (g)+3H (g) CH OH(g)+H O(g) CO (g)+H (g) CO(g)+H O(g)
2 2 3 2 2 2 2
初始/mol 0.5 0.9 0 0 0.5 0.9 0 0
转化/mol x 3x x x y y y y
平衡/mol (0.5-x-y) (0.9-3x-y) x (x+y) (0.5-x-y) (0.9-3x-y) y (x+y)
根据n(H )=n(CH OH)=0.2 mol得:(0.9-3x-y) =0.2 mol x =0.2 mol 得出:y=0.1
2 3
则CO 的转化率为:(0.1+0.2)/0.5=60%
2
湖北省新高考联考体*化学答案(共4页)第4页反应2的化学平衡常数K =(0.1×0.3)/(0.2×0.2)=3/4或0.75。
c
湖北省新高考联考体*化学答案(共4页)第5页