文档内容
专项训练 滴定后的误差分析
1.(2023·天津·统考三模)用标准的盐酸滴定未知浓度的NaOH溶液,下列各操作中,
不会引起实验误差的是
A.用蒸馏水洗净酸式滴定管后,装入标准盐酸进行滴定
B.用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗后装入一定体积的NaOH溶液
C.取10.00 mL NaOH溶液放入洗净的锥形瓶中,再加入适量蒸馏水
D.取10.00 mL的NaOH溶液,放入锥形瓶后,把碱式滴定管尖嘴液滴吹去
2.(2023春·海南海口·高二海南中学校考期中)用标准的NaOH溶液滴定未知浓度的
盐酸,若测定结果偏低,其原因可能是
A.碱式滴定管未用标准溶液润洗
B.锥形瓶用蒸馏水洗过后未用未知浓度的盐酸润洗
C.用酚酞作指示剂,当观察到溶液由无色变为浅红色时立即停止滴定
D.滴定终点读数时,仰视滴定管的刻度,其他操作正确
3.(2023·山东威海·威海市第一中学统考二模)实验室常用基准物质NaC O 标定
2 2 4
KMnO 溶液的浓度。将NaC O 溶液置于锥形瓶中,并加入稀硫酸,反应时温度不宜
4 2 2 4
过高。为提高初始速率,常滴加几滴MnSO 溶液。下列说法错误的是
4
A.应选用碱式滴定管量取NaC O 溶液
2 2 4
B.加MnSO 溶液的作用是做催化剂
4
C.若溶液温度过高、酸性过强,生成的草酸易分解,将导致结果偏高
D.已知 ,若初期滴加过快、温度过高,发生该
反应,将导致结果偏高
4.(2023春·四川遂宁·高二射洪中学校考期中)准确移取20.00mL某待测HCl溶液于
锥形瓶中,用0.1000mol•L-1NaOH溶液滴定。下列说法正确的是
A.滴定管用蒸馏水洗涤后,装入NaOH溶液进行滴定
B.滴定达终点时,发现滴定管尖嘴部分有悬滴,则测定结果偏大
C.用酚酞作指示剂,当滴入最后一滴溶液,锥形瓶中溶液由红色变为无色且半分钟不
再改变,即达滴定终点
D.随着NaOH溶液滴入,锥形瓶中溶液pH由大变小
5.(2023秋·河南驻马店·高二统考期末)用标准NaOH溶液滴定未知浓度的盐酸,若
测定结果偏低,则原因可能是
A.用滴定管量取标准液时,先俯视后仰视
B.锥形瓶洗净后瓶内残留有少量蒸馏水
1
学科网(北京)股份有限公司C.滴定到终点读数时,发现滴定管尖嘴处悬挂了一滴溶液
D.配制标准溶液的固体NaOH中混有NaO杂质
2
6.(2023春·江苏苏州·高二江苏省木渎高级中学校考期中)用一定浓度的NaOH标准
溶液滴定未知浓度的醋酸溶液,下列情况会使测定的醋酸溶液物质的量浓度偏低的是
A.碱式滴定管用蒸馏水洗净后,直接注入NaOH标准溶液
B.锥形瓶用蒸馏水洗净后,直接装入未知浓度的醋酸溶液
C.滴定到终点读数时,俯视刻度线(滴定前平视)
D.碱式滴定管尖端滴定前有气泡,滴定后气泡消失
7.(2023春·安徽·高二校联考期中)下列操作会导致实验结果偏大的是
A.配制一定物质的量浓度的NaOH溶液时,未进行洗涤操作
B.实验时用醋酸代替盐酸测定中和热ΔH
C.用标准NaOH溶液滴定醋酸来测定其浓度,选择甲基橙作指示剂
D.用标准NaOH溶液滴定未知浓度的盐酸,酸式滴定管未用待测液润洗
8.(2023春·山东·高三校联考阶段练习)用c 酸性 溶液滴定 mL未
知浓度的草酸溶液,达到滴定终点时消耗滴定液xmL。下列说法正确的是
A.滴定终点时溶液由粉红色变为无色
B.需要锥形瓶、碱式滴定管
C.若用草酸溶液润洗锥形瓶,使测得结果偏低
D.测得草酸浓度
9.(2023春·四川绵阳·高二四川省绵阳南山中学校考阶段练习)用0.1000
溶液滴定待测 溶液,下列说法正确的是
A.碱式滴定管用蒸馏水洗涤后,加入 溶液,赶出气泡,调节液面,记录读数
B.用待测 溶液润洗锥形瓶后,准确滴入25.00 待测 溶液于锥形瓶中
C.用酚酞作指示剂,当锥形瓶中溶液由无色变红色时停止滴定
D.其他操作正确,滴定过程中,有部分 溶液滴在锥形瓶外,测定结果偏大
10.(2022秋·高二课时练习)下列有关滴定操作的说法正确的是
A.用25 mL滴定管进行中和滴定时,用去标准液的体积为21.7 mL
B.用未知浓度的盐酸滴定标准KOH溶液时,若读数时,滴定前仰视,滴定到终点后
俯视,会导致测定结果偏高
C.用标准KOH溶液滴定未知浓度的盐酸,配制标准溶液的固体KOH中含有NaOH
杂质,则测定结果偏高
D.用标准KOH溶液滴定未知浓度的盐酸,洗净碱式滴定管后直接取标准KOH溶液
试卷第2页,共9页进行滴定,则测定结果偏低
11.(2021·浙江·高三竞赛)室温下,向20.00 mL 0.1000 mol·L-1盐酸中滴加0.
1000mol·L-1 NaOH溶液。下 列说法不正确的是
A.NaOH与盐酸恰好完全反应时,pH=7
B.选择变色点与滴定终点pH相接近的指示剂,可减小实验误差
C.选择酚酞指示反应终点,误差比甲基橙的大
D.待测液和标准溶液浓度变大时,滴定曲线的突跃范围将变大
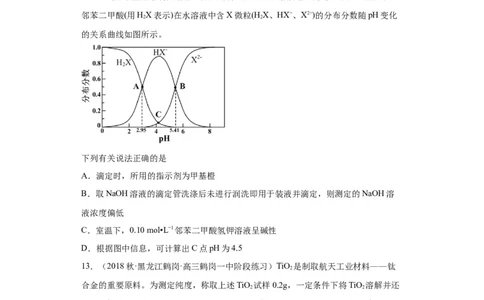
12.(2020·全国·模拟预测)室温下,称取一定质量的邻苯二甲酸氢钾置于锥形瓶中,
加入一定体积蒸馏水将其溶解,然后用待测的NaOH溶液进行滴定。已知:室温下,
邻苯二甲酸(用HX表示)在水溶液中含X微粒(H X、HX−、X2−)的分布分数随pH变化
2 2
的关系曲线如图所示。
下列有关说法正确的是
A.滴定时,所用的指示剂为甲基橙
B.取NaOH溶液的滴定管洗涤后未进行润洗即用于装液并滴定,则测定的NaOH溶
液浓度偏低
C.室温下,0.10 mol•L−1邻苯二甲酸氢钾溶液呈碱性
D.根据图中信息,可计算出C点pH为4.5
13.(2018秋·黑龙江鹤岗·高三鹤岗一中阶段练习)TiO 是制取航天工业材料——钛
2
合金的重要原料。为测定纯度,称取上述TiO 试样0.2g,一定条件下将TiO 溶解并还
2 2
原为Ti3+,得到待测液约30mL,再用0.1 mol·L-1NH Fe(SO ) 标准溶液滴定Ti3+至全部
4 4 2
生成Ti4+(假设杂质不参与以上反应)。下列说法中错误的是
A.欲配制0.1 mol·L-1NH Fe(SO ) 标准溶液400mL,需要NH Fe(SO ) 固体质量13.3g
4 4 2 4 4 2
B.再进行滴定之前,应向锥形瓶中的待测样品滴加几滴KSCN溶液做指示剂
C.滴定前仰视读数,滴定结束后俯视读数,将导致测定结果偏大
D.在其他滴定实验操作均正确时,消耗标准液20.00mL,则样品的纯度为80%
14.(2023秋·山东青岛·高二山东省青岛第十七中学校考期末)下列叙述不正确的是
A.用玻璃棒蘸取 溶液点在水湿润的pH试纸上,则测得的该溶液pH值偏
3
学科网(北京)股份有限公司大
B.滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁
C.邻苯二甲酸氢钾可用于标定NaOH溶液的浓度。假如称量邻苯二甲酸氢钾时电子天
平读数比实际质量偏大,则测得的NaOH溶液浓度比实际浓度偏小
D.“中和滴定实验中,锥形瓶用蒸馏水洗净后即可使用,滴定管用蒸馏水洗净后,
必须干燥或润洗后方可使用
15.(2023春·河南·高二校联考阶段练习)下列不当操作可能导致实验结果偏小的是
A.配制一定浓度 溶液时未将待转移液体冷却至室温就定容
B.实验中使用铜搅拌器代替玻璃搅拌器测定中和反应的反应热
C.用标准 溶液滴定醋酸来测定其浓度,选择甲基橙作指示剂
D.用标准 溶液滴定盐酸来测定其浓度,滴定终点读数时仰视
16.(2023春·云南昆明·高二安宁中学校考阶段练习)某同学想了解食用白醋(主要是
醋酸的水溶液)的准确浓度,现从市场上买来一瓶某品牌食用白醋,用实验室标准
NaOH溶液(浓度有0.1000mol/L和0.0100mol/L两种)对其进行滴定。下列说法正确的是
A.该实验应选用甲基橙作指示剂
B.对装标准液的滴定管,滴定前仰视读数,滴定后平视读数,会使测定结果偏低
C.用0.1000mol/L标准NaOH溶液滴定时误差更小
D.滴定时,眼睛一直注视着刻度线,以防止液面下降到滴定管最大刻度以下
17.(2023春·河南安阳·高二安阳一中校考开学考试)下列滴定实验中仪器或指示剂
选择正确,但操作造成测定值偏大的是
A.用标准NaOH溶液滴定未知浓度的盐酸时,用石蕊作指示剂
B.两次所取的未知浓度的NaOH溶液的体积不相同,都用同浓度的盐酸滴定,用甲基
橙作指示剂
C.用标准 溶液滴定未知浓度的NaOH溶液,读数如图Ⅰ
D.用标准酸性 溶液滴定未知浓度的稀 溶液,读数如图Ⅱ
试卷第4页,共9页18.(2022秋·浙江杭州·高二杭州四中校考期中)某学生以酚酞为指示剂用已知物质
的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液,三次实验分别记录有关数
据如下表:
0.1000 mol/L盐酸的体积/mL
滴定次数 待测氢氧化钠溶液的体积/mL
滴定前刻度 滴定后刻度
第一次 25.00 0.00 28.85
第二次 25.00 0.00 28.90
第三次 25.00 0.00 17.55
下列说法正确的是
A.该氢氧化钠溶液中c(NaOH)=0.1155mol/L
B.当溶液从无色刚好变成红色时,则达到滴定终点
C.达滴定终点时,滴定管尖嘴有气泡,则测定结果偏高
D.实验中锥形瓶应用待测氢氧化钠溶液润洗
19.(2023秋·江苏南通·高二统考期末)常温下,将
溶液置于锥形㼛中,将 溶液置于滴定管中,用 溶液滴定
,实验中的下列情形会导致达到滴定终点时,消耗 溶液体积小于
的是
A.装 溶液的滴定管水洗后未用待装液润洗
B.滴定管滴定前尖嘴处有气泡,滴定后气泡消失
C.滴定过程中,用蒸馏水将附着在瓶壁上的液体冲入溶液中
D.滴定结束时,俯视滴定管进行读数
20.(2023春·江苏徐州·高二统考期中)白云石 中钙含量测定常用
滴定的方法。具体做法是将其酸溶后转化为草酸钙,过滤后用酸溶解,再用
滴定。则下列说法错误的是
A. 滴定草酸发生反应的离子方程式为
,标准状况下产生 气体
5
学科网(北京)股份有限公司理论上转移
B.实验过程中两次用酸溶解,均需使用稀盐酸
C.若滴定前滴定管尖嘴处有气泡,滴定后消失,则测定结果偏高
D.滴入最后半滴标准液时,锥形瓶中液体变浅紫红色且半分钟内不褪色,则达到滴
定终点
21.(2023秋·山东菏泽·高二山东省鄄城县第一中学校考期末)实验室用标准KMnO
4
溶液滴定未知浓度的FeSO 溶液,下列说法或操作正确的是
4
A.滴定前锥形瓶用FeSO 溶液润洗2~3次
4
B.将标准KMnO 溶液置于碱式滴定管中备用
4
C.滴定前俯视读数、滴定后仰视读数会导致滴定结果偏高
D.当锥形瓶内溶液颜色由浅绿色变为紫红色时,立即记下滴定管液面所在刻度
22.(2023·山东·统考高考真题)一定条件下,乙酸酐 醇解反应
可进行完全,利用此反应定量测定
有机醇 中的羟基含量,实验过程中酯的水解可忽略。实验步骤如下:
①配制一定浓度的乙酸酐-苯溶液。
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入 样品,充分反应后,加适
量水使剩余乙酸酐完全水解: 。
③加指示剂并用 甲醇标准溶液滴定至终点,消耗标准溶液 。
④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加
指示剂并用 -甲醇标准溶液滴定至终点,消耗标准溶液 。根据上
述实验原理,下列说法正确的是
A.可以用乙酸代替乙酸酐进行上述实验
B.若因甲醇挥发造成标准溶液浓度发生变化,将导致测定结果偏小
C.步骤③滴定时,不慎将锥形瓶内溶液溅出,将导致测定结果偏小
D.步骤④中,若加水量不足,将导致测定结果偏大
23.(2023秋·吉林·高二吉林松花江中学校考期末)下列实验操作会使实验最终结果
偏高的是
试卷第6页,共9页A.用0.0001mol∙L-1盐酸滴定20.00mLNaOH溶液时,未排尽滴定管尖嘴处的气泡
B.测定中和热的数值时,将0.5mol∙L-1NaOH溶液倒入盐酸后,立即读数
C.用0.0001mol∙L-1盐酸滴定20.00mLNaOH溶液,滴定前仰视,滴定后平视
D.用湿润的pH试纸测定NaOH的pH
24.(2023秋·河南·高二校联考期末)在实验室里可用 标准溶液滴定醋酸溶液
的方法准确测定某醋酸的物质的量浓度,下列操作会导致测定结果偏低的是
A.滴定前锥形瓶未干燥
B.未用 标准溶液润洗滴定管
C.滴定后俯视读数
D.盛放标准液的滴定管滴定至终点时有一滴悬在管口
25.(2022·北京海淀·高三统考专题练习)食醋中含有醋酸等有机酸及少量氨基酸。食
醋的酸度是指每 食醋中含酸(均折合成醋酸计)的质量。国家标准规定酿造食醋
酸度不得低于 。可用滴定法测定食醋的酸度。某小组同学量取 自
制食醋样品稀释至 (溶液几乎无色),每次量取 于锥形瓶中,加入
中性甲醛溶液(掩蔽氨基的碱性),以酚酞为指示剂,用 标
准溶液滴定,滴定管读数记录如下表。
第一
溶液的体积 第二次 第三次
次
滴定前 溶液的体积读数 0.00 1.00 2.00
滴定后 溶液的体积读数 9.90 11.00 12.10
下列说法不正确的是
A.醋酸易溶于水与“醋酸分子和水分子之间能形成氢键”有关
B.锥形瓶中溶液由无色变为粉红色,且半分钟内不褪色时停止滴定
C.该自制食醋样品的酸度不符合国家标准
D.若不加甲醛溶液,测定结果会偏低
26.(2022秋·辽宁葫芦岛·高二兴城市高级中学校联考阶段练习)下列实验中,由于
错误操作导致所测出的数据一定偏低的是
A.滴定前尖嘴中气泡未排出即进行滴定,滴定后尖嘴无气泡
B.用标准盐酸滴定未知浓度的NaOH溶液,酸式滴定管未用标准盐酸润洗,所测出的
碱液的浓度值
C.同一滴定实验,一般做三次,取三次实验的平均值进行计算,但某同学只做了一次
7
学科网(北京)股份有限公司D.达到滴定终点时,俯视读数标准液滴定未知物质的量浓度的HCl溶液
27.(2022秋·山东济宁·高二统考期中)下列叙述不正确的是
A.邻苯二甲酸氢钾可用于标定 溶液的浓度。假如称量邻苯二甲酸氢钾时电子
天平读数比实际质量偏大,则测得的 溶液浓度比实际浓度偏小
B.“中和滴定”实验中,锥形瓶用蒸馏水洗净后即可使用,滴定管用蒸馏水洗净后,
必须干燥或润洗后方可使用
C.用玻璃棒蘸取 溶液点在水湿润的 试纸上,则测得的该溶液 值偏
大
D.滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁
28.(2022春·内蒙古呼和浩特·高二校考期中)用0.2500mol/L的盐酸滴定20ml某未
知浓度的氢氧化钠溶液实验中,所测数据如表:
实验次数 1 2 3
消耗盐酸的体积 25.05 24.95 20.95
下列说法正确的是( )
A.用蒸馏水洗涤后的酸式滴定管即可装入盐酸标准溶液
B.氢氧化钠溶液的浓度为0.3125mol/L
C.滴定过程中可以选用石蕊溶液做指示剂
D.若酸式滴定管在滴定前尖端有气泡,而滴定后气泡消失,则氢氧化钠溶液浓度偏
低
29.(2022秋·湖北·高三校联考阶段练习) 号称绿色氧化剂,一般以30%或60%
的水溶液形式存放,俗称双氧水,适用于医用伤口消毒、环境消毒和食品消毒。某制
备方法及装置如图:
已知:① ;
② 、HX等杂质易使催化剂Ni中毒。
试卷第8页,共9页下列说法正确的是
A.可用装置A在相应位置盛装二氧化锰和浓盐酸制氯气
B.装置B可为盛装饱和食盐水的洗气瓶或装有碱石灰的干燥管
C.反应结束后,过滤三颈烧瓶中混合物,加水萃取,分液,减压蒸馏,此过程用到的
玻璃仪器有8种(除三颈烧瓶)
D.在用酸性 标准溶液滴定法测定 产品纯度过程中,若在滴定终点读数
时俯视,则结果偏低
30.(2023·全国·高三专题练习)测定水的总硬度一般采用配位滴定法,即在pH=10
的氨性溶液中,以铬黑 作为指示剂,用EDTA(乙二胺四乙酸)标准溶液直接滴定水中
的Ca2+、Mg2+测定中涉及的反应有:①M2+ (金属离子)+Y4-(EDTA)=MY2-;
②M2++EBT(铬黑T,蓝色)=MEBT(酒红色);
③MEBT+Y4-(EDTA)=MY2-+EBT。下列说法正确的是
A.配合物MEBT的稳定性大于MY2-
B.在滴定过程中眼睛要随时观察滴定管中液面的变化
C.达到滴定终点的现象是溶液恰好由酒红色变为蓝色,且半分钟内不恢复原色
D.实验时装有EDTA标准液的滴定管只用蒸馏水洗涤而未用标准液润洗,测定结果
将偏小
9
学科网(北京)股份有限公司