文档内容
高考热点专项 3 对数图像分析
目录
01考情透视·目标导航............................................................................................................................
02知识导图·思维引航............................................................................................................................
03核心精讲·题型突破............................................................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.常用对数的运算法则.........................................................................................................................................
2.常考对数图像的类型.........................................................................................................................................
3.图像中数据的数学含义.....................................................................................................................................
4.破解对数图像的步骤.........................................................................................................................................
【命题预测】...........................................................................................................................................................
考向1 坐标为简单的对数或负对数......................................................................................................................
考向2 坐标为某些微粒浓度的比值的对数或负对数..........................................................................................
考点要求 考题统计 考情分析
(2024·辽吉黑卷,15,3分;2024·福建卷,10,4
分;2024·广西卷,1,3分;2024·全国甲卷,7,6
分) 2023•湖南卷,12,3分;2023•辽宁省选择性 近年来借助数学的对
考试,15,3分;2023•全国甲卷,13,6分; 数知识,把浓度的对
坐标为简单的对
2023•山东卷,15,3分;2023•全国新课标卷, 数融于离子反应平衡
数或负对数 13,6分;2023•海南卷,14,3分;2022•福建 图象中,把所要考查
卷,7,3分;2022•湖南选择性卷,10,3分; 的知识简明、直观、
2022•海南省选择性卷,14,3分;2022·浙江省1 形象的寓于坐标曲线
月卷,23,2分; 上。预计 2025 年用
图象仍时表述化学反
应过程或者呈现信息
坐标为某些微粒
情景是常见的表达方
浓度的比值的对 2024·河北卷,11,3分; 式。
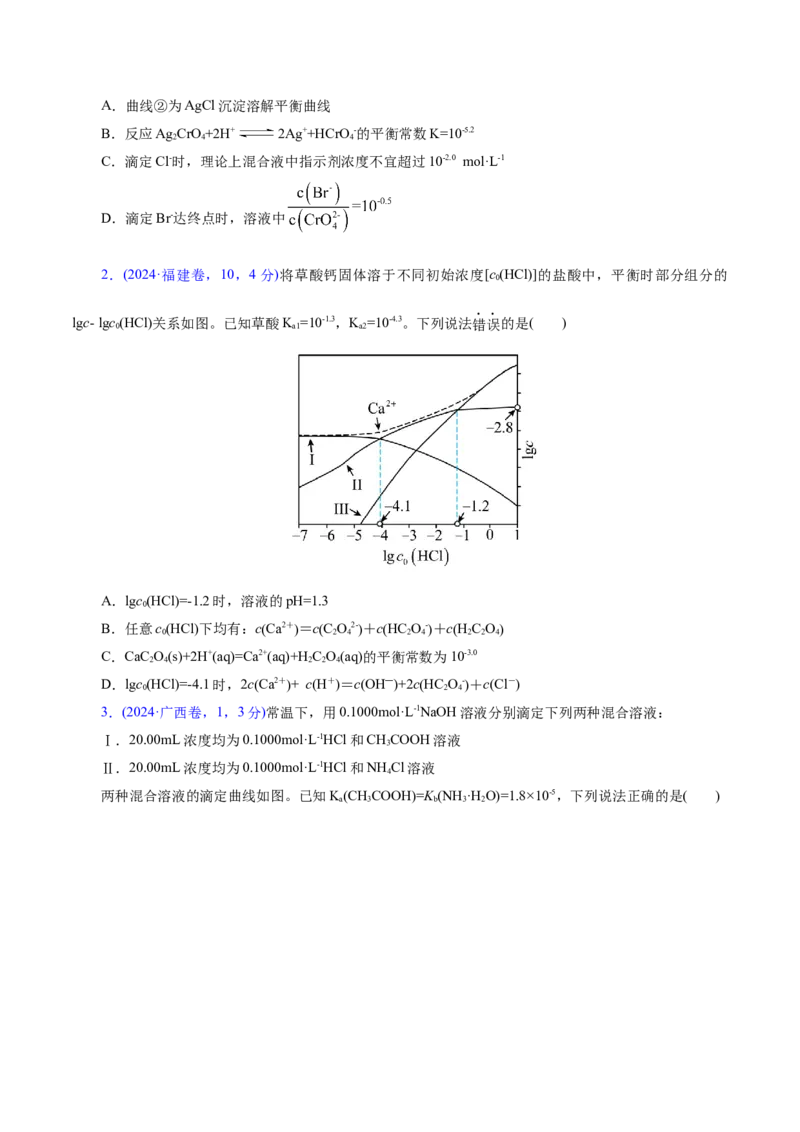
数或负对数1.(2024·辽吉黑卷,15,3分) 下,AgCl、AgBr和Ag CrO 的沉淀溶解平衡曲线如下图所示。某
2 4
实验小组以KCrO 为指示剂,用AgNO 标准溶液分别滴定含Cl-水样、含Br-水样。
2 4 3
已知:①Ag CrO 为砖红色沉淀;
2 4
②相同条件下AgCl溶解度大于AgBr;
③ 时, , 。
下列说法错误的是( )A.曲线②为AgCl沉淀溶解平衡曲线
B.反应Ag CrO+2H+ 2Ag++HCrO-的平衡常数K=10-5.2
2 4 4
C.滴定Cl-时,理论上混合液中指示剂浓度不宜超过10-2.0 mol·L-1
D.滴定Br-达终点时,溶液中
2.(2024·福建卷,10,4分)将草酸钙固体溶于不同初始浓度[c(HCl)]的盐酸中,平衡时部分组分的
0
lgc- lgc(HCl)关系如图。已知草酸K =10-1.3,K =10-4.3。下列说法错误的是( )
0 a1 a2
A.lgc(HCl)=-1.2时,溶液的pH=1.3
0
B.任意c(HCl)下均有:cCa2+=cC O2-+cHC O-+cHC O
0 2 4 2 4 2 2 4
C.CaC O(s)+2H+(aq)=Ca2+(aq)+H C O(aq)的平衡常数为10-3.0
2 4 2 2 4
D.lgc(HCl)=-4.1时,2cCa2++ c(H+)=c(OH―)+2cHC O-+c(Cl-)
0 2 4
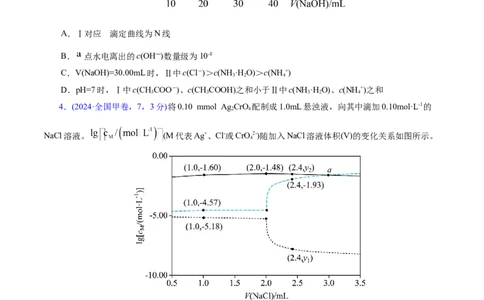
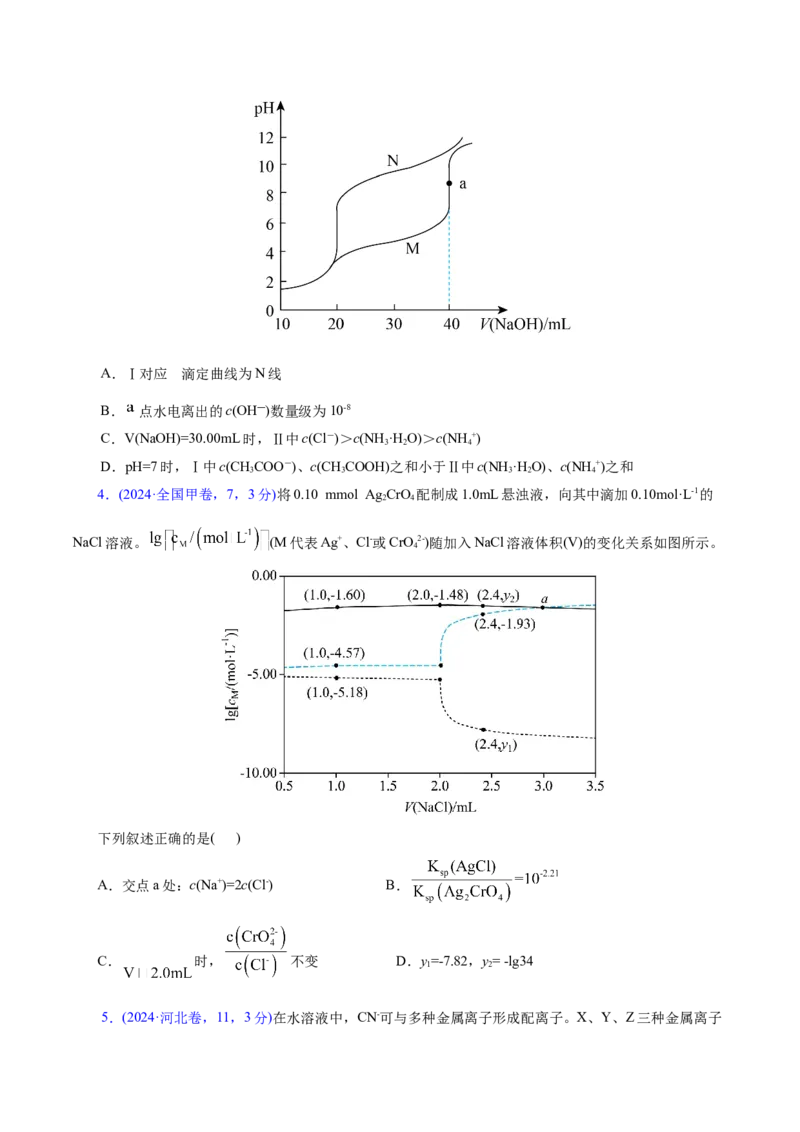
3.(2024·广西卷,1,3分)常温下,用0.1000mol·L-1NaOH溶液分别滴定下列两种混合溶液:
Ⅰ.20.00mL浓度均为0.1000mol·L-1HCl和CHCOOH溶液
3
Ⅱ.20.00mL浓度均为0.1000mol·L-1HCl和NH Cl溶液
4
两种混合溶液的滴定曲线如图。已知K(CHCOOH)=K (NH ·H O)=1.8×10-5,下列说法正确的是( )
a 3 b 3 2的
A.Ⅰ对应 滴定曲线为N线
B. 点水电离出的c(OH―)数量级为10-8
C.V(NaOH)=30.00mL时,Ⅱ中c(Cl-)>c(NH ·H O)>c(NH +)
3 2 4
D.pH=7时,Ⅰ中c(CHCOO-)、c(CHCOOH)之和小于Ⅱ中c(NH ·H O)、c(NH +)之和
3 3 3 2 4
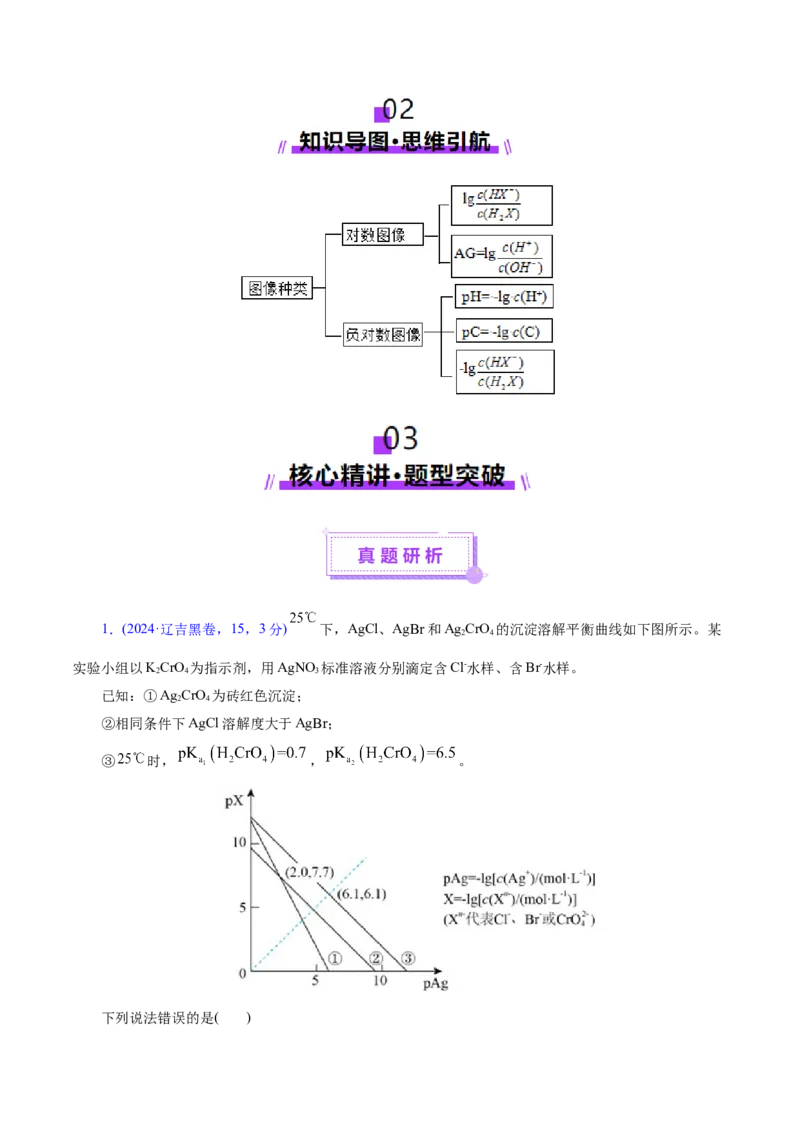
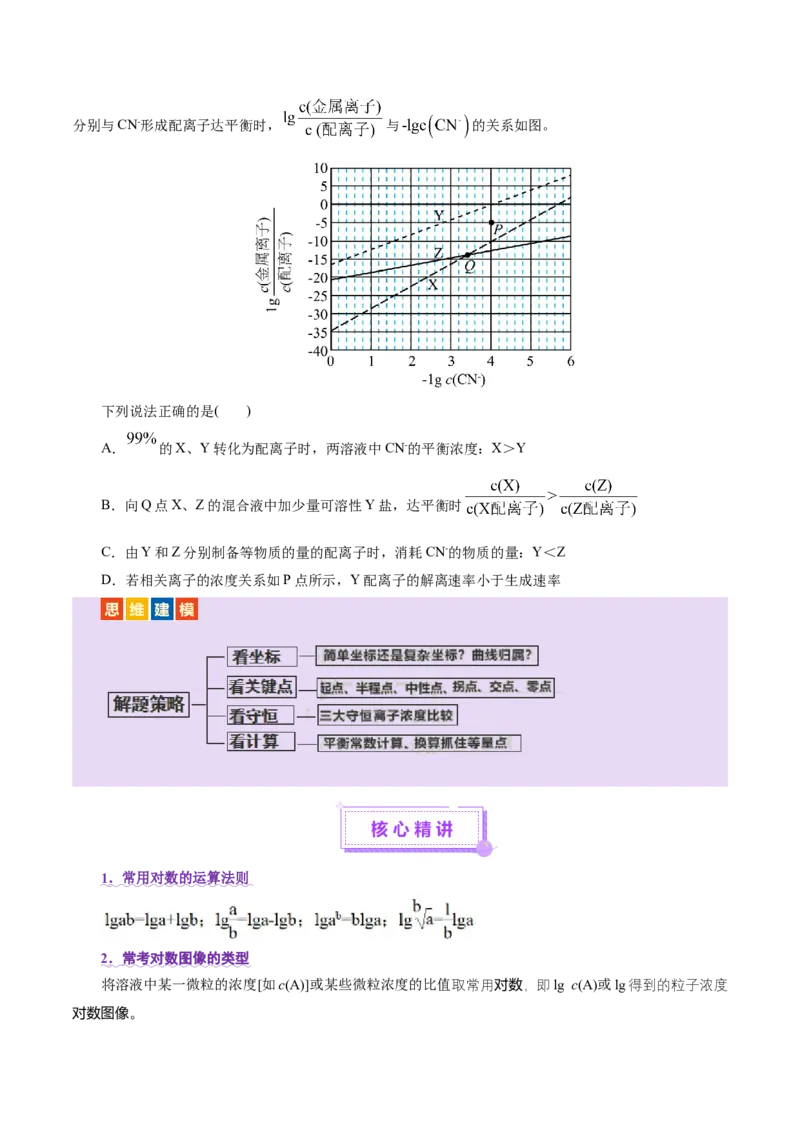
4.(2024·全国甲卷,7,3分)将0.10 mmol Ag CrO 配制成1.0mL悬浊液,向其中滴加0.10mol·L-1的
2 4
NaCl溶液。 (M代表Ag+、Cl-或CrO2-)随加入NaCl溶液体积(V)的变化关系如图所示。
4
下列叙述正确的是( )
A.交点a处:c(Na+)=2c(Cl-) B.
C. 时, 不变 D.y=-7.82,y= -lg34
1 2
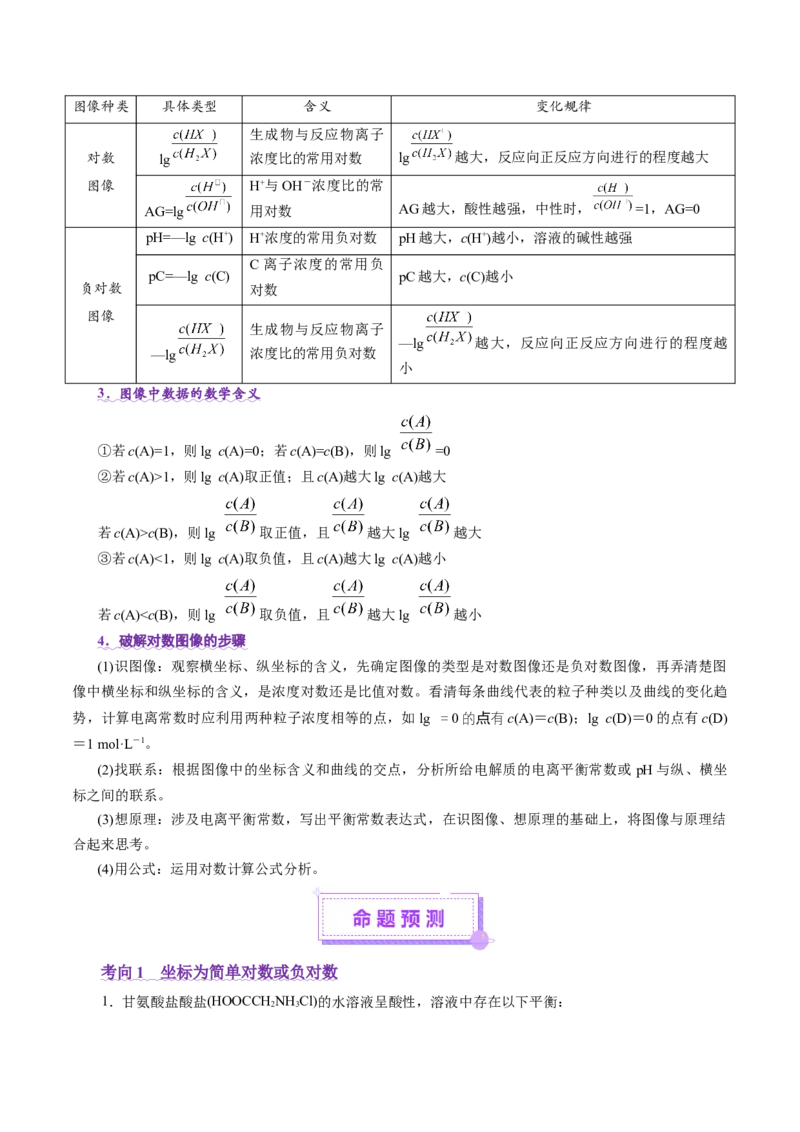
5.(2024·河北卷,11,3分)在水溶液中,CN-可与多种金属离子形成配离子。X、Y、Z三种金属离子分别与CN-形成配离子达平衡时, 与 的关系如图。
下列说法正确的是( )
A. 的X、Y转化为配离子时,两溶液中CN-的平衡浓度:X>Y
B.向Q点X、Z的混合液中加少量可溶性Y盐,达平衡时
C.由Y和Z分别制备等物质的量的配离子时,消耗CN-的物质的量:Y<Z
D.若相关离子的浓度关系如P点所示,Y配离子的解离速率小于生成速率
1 .常用对数的运算法则
2 . 常考对数图像的类型
将溶液中某一微粒的浓度[如c(A)]或某些微粒浓度的比值取常用对数,即lg c(A)或lg得到的粒子浓度
对数图像。图像种类 具体类型 含义 变化规律
生成物与反应物离子
对数 lg 浓度比的常用对数 lg 越大,反应向正反应方向进行的程度越大
图像 H+与OH-浓度比的常
AG=lg 用对数 AG越大,酸性越强,中性时, =1,AG=0
pH=—lg c(H+) H+浓度的常用负对数 pH越大,c(H+)越小,溶液的碱性越强
C离子浓度的常用负
pC=—lg c(C) pC越大,c(C)越小
负对数 对数
图像
生成物与反应物离子
—lg 越大,反应向正反应方向进行的程度越
—lg 浓度比的常用负对数
小
3 .图像中数据的数学含义
①若c(A)=1,则lg c(A)=0;若c(A)=c(B),则lg =0
②若c(A)>1,则lg c(A)取正值;且c(A)越大lg c(A)越大
若c(A)>c(B),则lg 取正值,且 越大lg 越大
③若c(A)<1,则lg c(A)取负值,且c(A)越大lg c(A)越小
若c(A)X
B.X→P过程中: 逐渐增大
C.P点的溶液中:c(HOOCCH NH +)+c(H+)=c(-OOCCH NH )+c(OH-)
2 3 2 2
D.当 时,混合溶液中的溶质主要为NaOOCCHNH 和NaCl
2 2
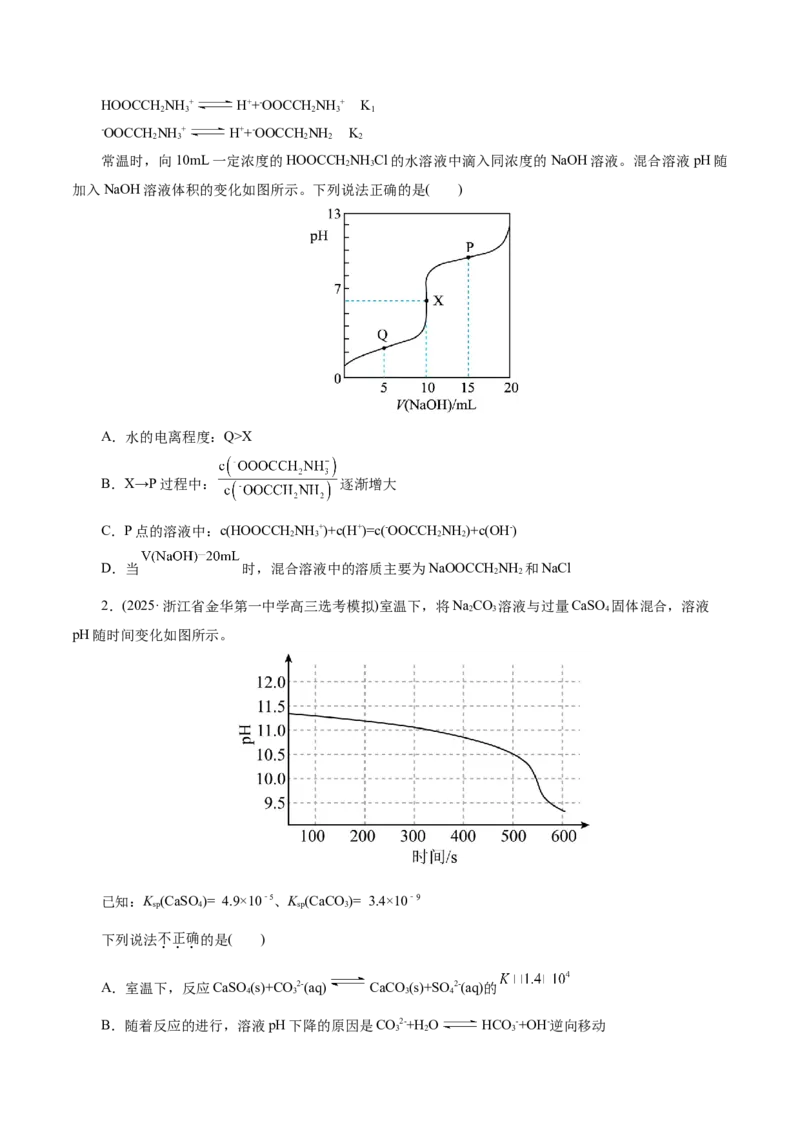
2.(2025·浙江省金华第一中学高三选考模拟)室温下,将NaCO 溶液与过量CaSO 固体混合,溶液
2 3 4
pH随时间变化如图所示。
已知:K (CaSO)= 4.9×10-5、K (CaCO)= 3.4×10-9
sp 4 sp 3
下列说法不正确的是( )
A.室温下,反应CaSO(s)+CO2-(aq) CaCO (s)+SO 2-(aq)的
4 3 3 4
B.随着反应的进行,溶液pH下降的原因是CO2-+H O HCO -+OH-逆向移动
3 2 3C.0~600s内上层清液中存在:cNa++2cCa2+>cHCO -+2cCO2-+2cSO 2-
3 3 4
D.反应过程中,溶液中始终存在:cNa+=2cCO2-+2cHCO -+2cHCO
3 3 2 3
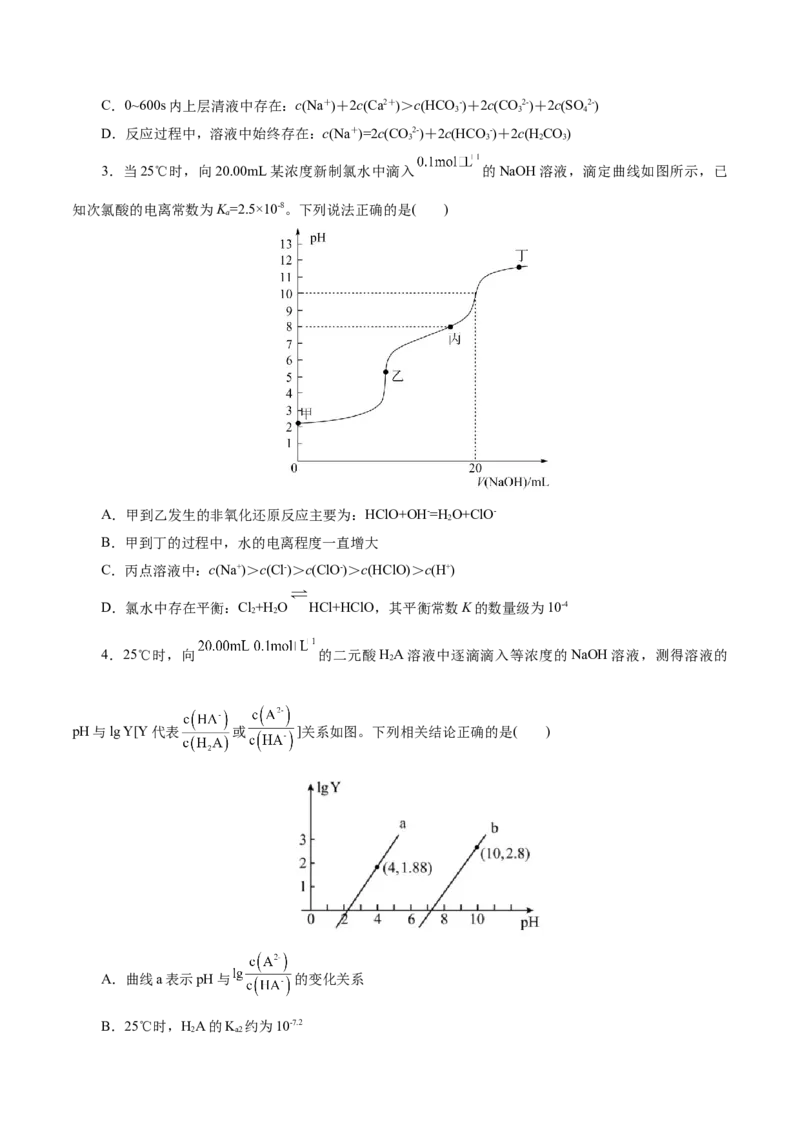
3.当25℃时,向20.00mL某浓度新制氯水中滴入 的NaOH溶液,滴定曲线如图所示,已
知次氯酸的电离常数为K =2.5×10-8。下列说法正确的是( )
a
A.甲到乙发生的非氧化还原反应主要为:HClO+OH-=H O+ClO-
2
B.甲到丁的过程中,水的电离程度一直增大
C.丙点溶液中:c(Na+)>c(Cl-)>c(ClO-)>c(HClO)>c(H+)
D.氯水中存在平衡:Cl+H O HCl+HClO,其平衡常数K的数量级为10-4
2 2
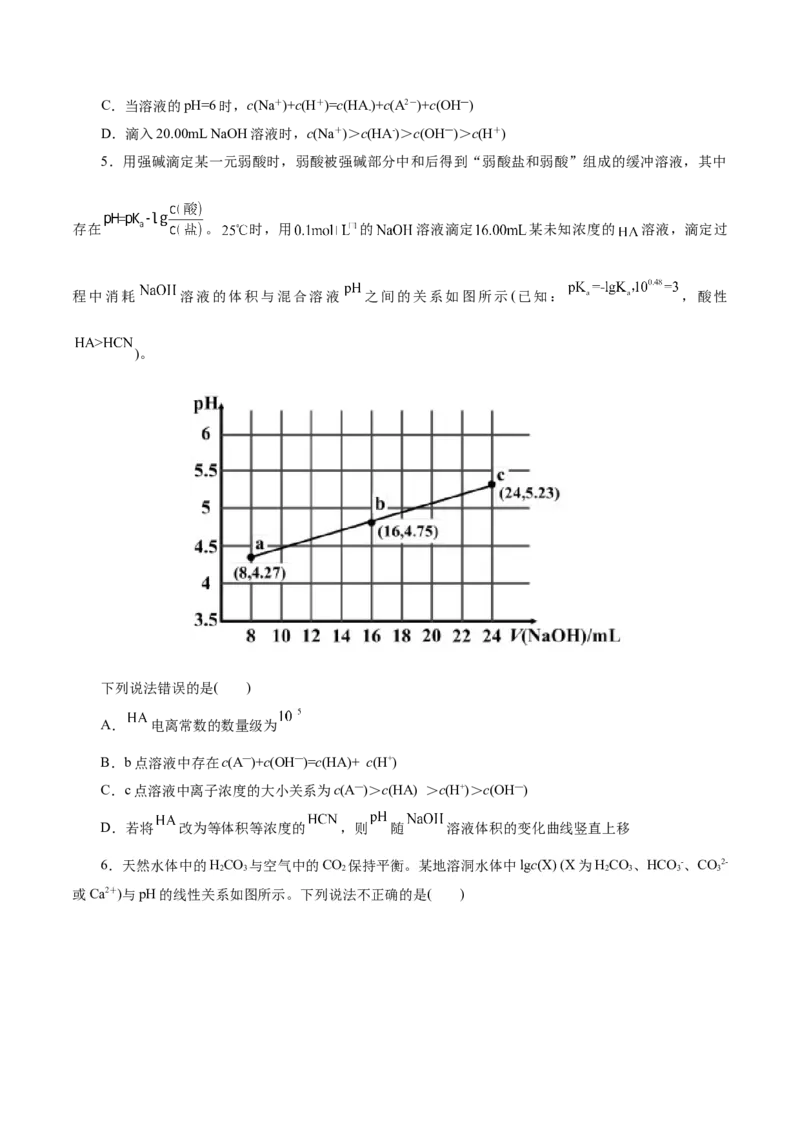
4.25℃时,向 的二元酸HA溶液中逐滴滴入等浓度的NaOH溶液,测得溶液的
2
pH与lg Y[Y代表 或 ]关系如图。下列相关结论正确的是( )
A.曲线a表示pH与 的变化关系
B.25℃时,HA的K 约为10-7.2
2 a2C.当溶液的pH=6时,c(Na+)+c(H+)=c(HA)+c(A2-)+c(OH―)
-
D.滴入20.00mL NaOH溶液时,c(Na+)>c(HA-)>c(OH―)>c(H+)
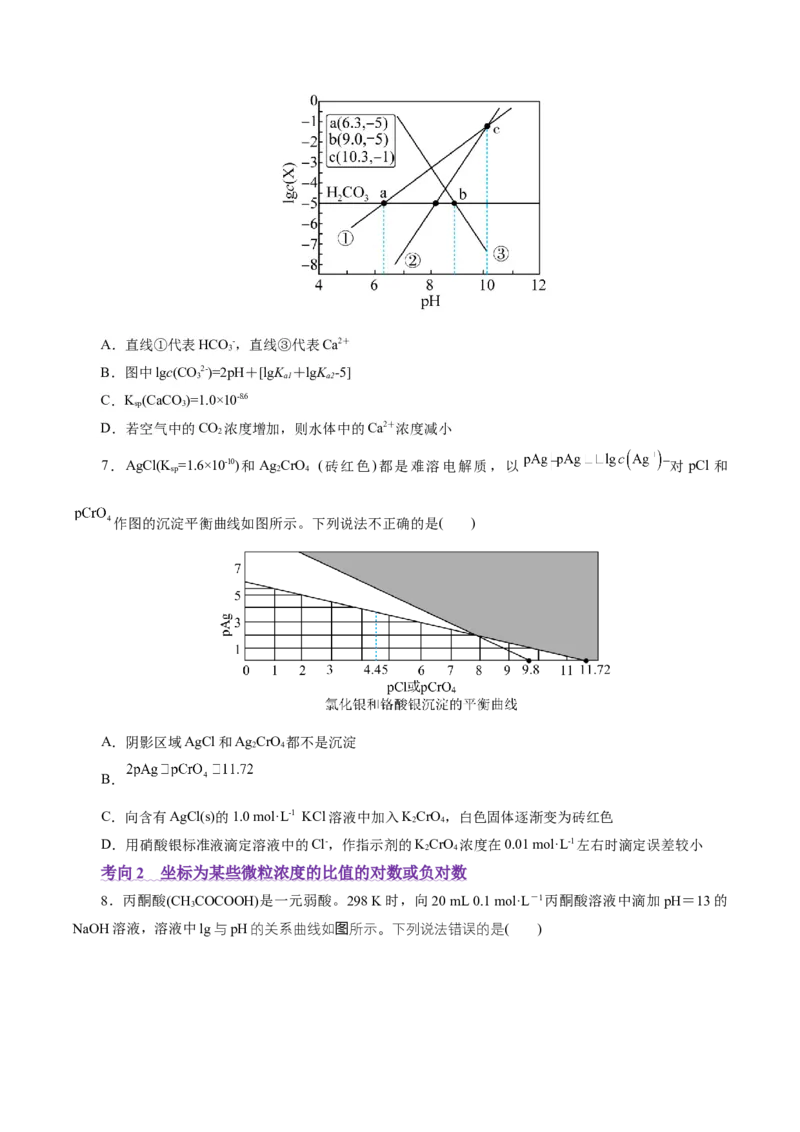
5.用强碱滴定某一元弱酸时,弱酸被强碱部分中和后得到“弱酸盐和弱酸”组成的缓冲溶液,其中
存在 。 时,用 的 溶液滴定 某未知浓度的 溶液,滴定过
程中消耗 溶液的体积与混合溶液 之间的关系如图所示(已知: ,酸性
)。
下列说法错误的是( )
A. 电离常数的数量级为
B.b点溶液中存在c(A—)+c(OH—)=c(HA)+ c(H+)
C.c点溶液中离子浓度的大小关系为c(A—)>c(HA) >c(H+)>c(OH—)
D.若将 改为等体积等浓度的 ,则 随 溶液体积的变化曲线竖直上移
6.天然水体中的HCO 与空气中的CO 保持平衡。某地溶洞水体中lgc(X) (X为HCO、HCO -、CO2-
2 3 2 2 3 3 3
或Ca2+)与pH的线性关系如图所示。下列说法不正确的是( )A.直线①代表HCO -,直线③代表Ca2+
3
B.图中lgc(CO2-)=2pH+[lgK +lgK -5]
3 a1 a2
C.K (CaCO)=1.0×10-8.6
sp 3
D.若空气中的CO 浓度增加,则水体中的Ca2+浓度减小
2
7.AgCl(K =1.6×10-10)和 Ag CrO (砖红色)都是难溶电解质,以 对 pCl 和
sp 2 4
作图的沉淀平衡曲线如图所示。下列说法不正确的是( )
A.阴影区域AgCl和Ag CrO 都不是沉淀
2 4
B.
C.向含有AgCl(s)的1.0 mol·L-1 KCl溶液中加入KCrO,白色固体逐渐变为砖红色
2 4
D.用硝酸银标准液滴定溶液中的Cl-,作指示剂的KCrO 浓度在0.01 mol·L-1左右时滴定误差较小
2 4
考向 2 坐标为某些微粒浓度的比值的对数或负对数
8.丙酮酸(CHCOCOOH)是一元弱酸。298 K时,向20 mL 0.1 mol·L-1丙酮酸溶液中滴加pH=13的
3
NaOH溶液,溶液中lg与pH的关系曲线如图所示。下列说法错误的是( )A.298 K时,CHCOCOOH的电离常数的数量级为10-3
3
B.E点溶液中,a=2
C.G点对应的NaOH溶液的体积为20 mL
9.常温下,往100 mL0.1mol·L-1的HR溶液(此时为a点)中不断加入NaOH固体,溶液中由水电离出
2
来的c (H+)的负对数[ ]与 的变化关系如图所示,下列说法正确的是( )
水
A.HR的电离方程式为: ,
2
B.b点时,加入的NaOH的质量为0.6g
C.c、e两点溶液均显中性
D.d的坐标为(5,6)
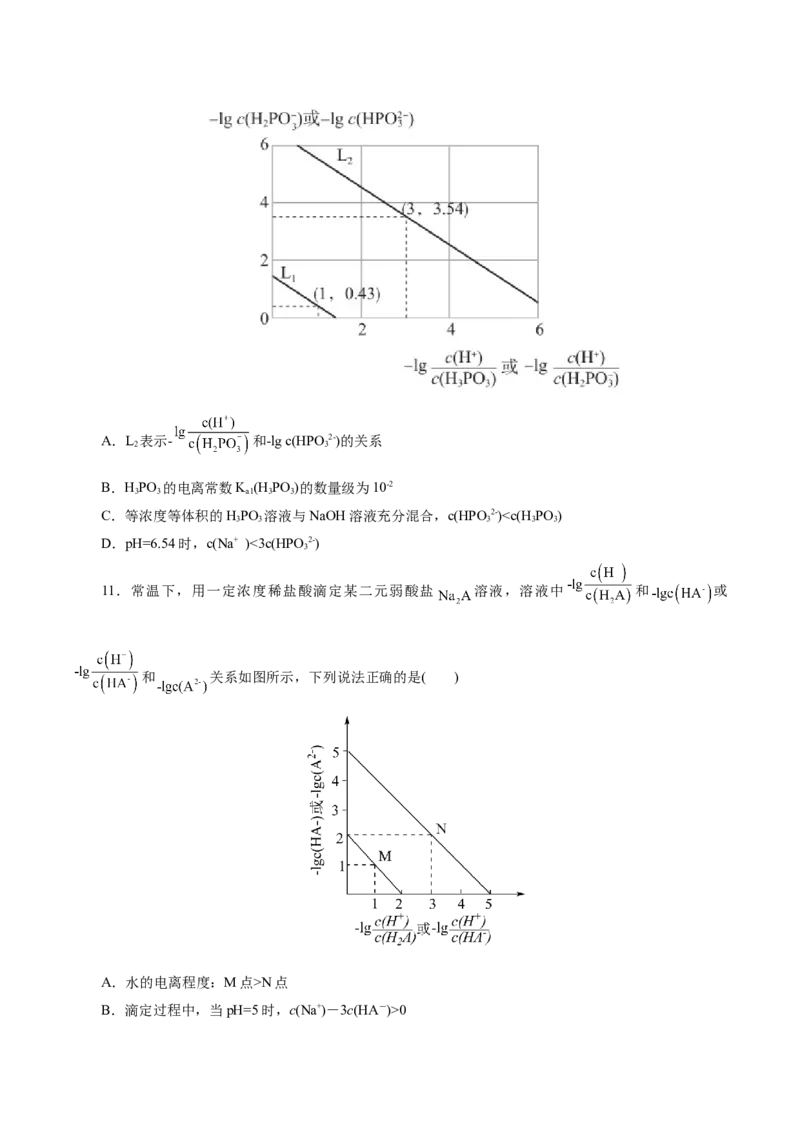
10.常温下,用 NaOH 溶液滴定二元弱酸亚磷酸溶液,溶液中- 和-lgc( )或-
和-lgc( )的关系如图所示,下列说法错误的是( )A.L 表示- 和-lg c(HPO 2-)的关系
2 3
B.HPO 的电离常数K (H PO )的数量级为10-2
3 3 a1 3 3
C.等浓度等体积的HPO 溶液与NaOH溶液充分混合,c(HPO 2-)N点
B.滴定过程中,当pH=5时,c(Na+)-3c(HA-)>0C.若c(HA-)>c(A2-)>c(H A),则pH范围3.5