文档内容
福 建 省 福 州 第 一 中 学
2023 届高三第一次调研测试
化学
一、选择题;本题共14小题,每小题3分,共42分.在每小题给出的四个选项中,
只有一项是符合题目要求的.
1.化学与生活密切相关。下列说法不正确的是
A.CO、NO 或SO 都会导致酸雨的形成
2 2 2
B.疫苗一般应冷藏存放,以避免蛋白质变性
C.泡沫灭火器可用于一般的起火,但不适用于电器起火
D.水中的钢闸门连接电源的负极,可防止钢闸门被腐蚀
2.ClO 是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得
2
ClO :2KClO+H C O+H SO 2ClO ↑+K SO +2CO ↑+2H O (方程式中H为+1价,O
2 3 2 2 4 2 4 2 2 4 2 2
为-2价)下列说法正确的是
A.KClO 在反应中失电子 B.ClO 是氧化产物
3 2
C.HC O 在反应中被氧化 D.1 molKClO 参加反应有2mol电子转
2 2 4 3
移
3.下列说法正确的是
A. 的一溴代物和 的一溴代物都有4种(不考虑立
体异构)
B.CHCH=CHCH 分子中的四个碳原子在同一直线上
3 3C.按系统命名法,化合物 的名称是2,3,4—三甲基
—2—乙基戊烷
D. 与 互为同系物
4.设N 为阿伏加德罗常数的值,下列说法中正确的是
A
A.常温常压下,4g氦气含有的原子数目为N
A
B.标准状况下,11.2L四氯化碳含有的分子数为0.5N
A
C.通常状况下,1mol氧气中含有的氧气分子数为2N
A
D.化学反应中,2.4g金属镁变成镁离子时失去的电子数为0.3N
A
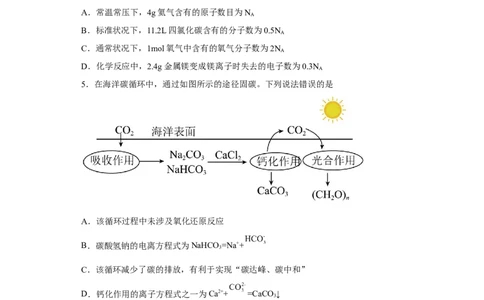
5.在海洋碳循环中,通过如图所示的途径固碳。下列说法错误的是
A.该循环过程中未涉及氧化还原反应
B.碳酸氢钠的电离方程式为NaHCO =Na++
3
C.该循环减少了碳的排放,有利于实现“碳达峰、碳中和”
D.钙化作用的离子方程式之一为Ca2++ =CaCO ↓
3
6.下列离子方程式书写不正确的是
A.向BaCl 溶液中通入SO 气体:Ba2++SO+H O=BaSO↓+2H+
2 2 2 2 3
B.Cu和浓HNO 反应:Cu+4H++2 =Cu2++2NO↑+2H O
3 2 2
C.NaAlO 溶液中通入过量CO: +2H O+CO=Al(OH) ↓+
2 2 2 2 3
D.少量碳酸氢钠溶液与足量澄清石灰水混合:
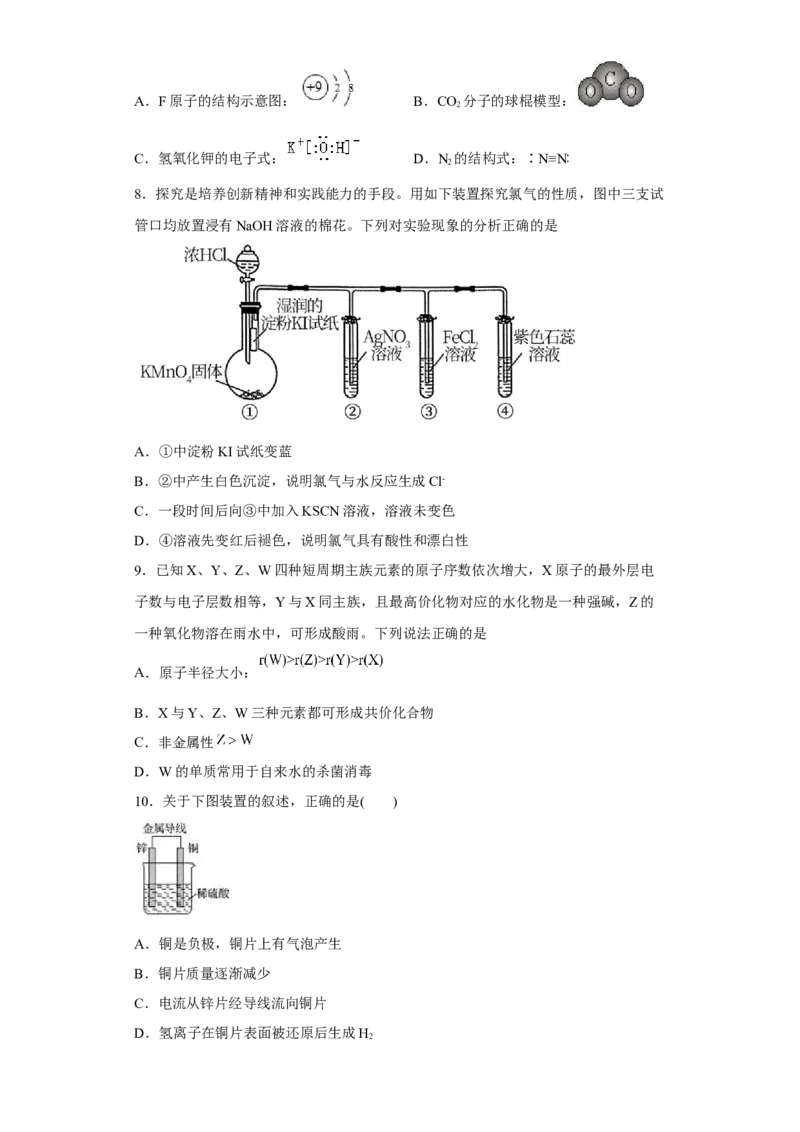
7.下列表达正确的是A.F原子的结构示意图: B.CO 分子的球棍模型:
2
C.氢氧化钾的电子式: D.N 的结构式:∶N≡N∶
2
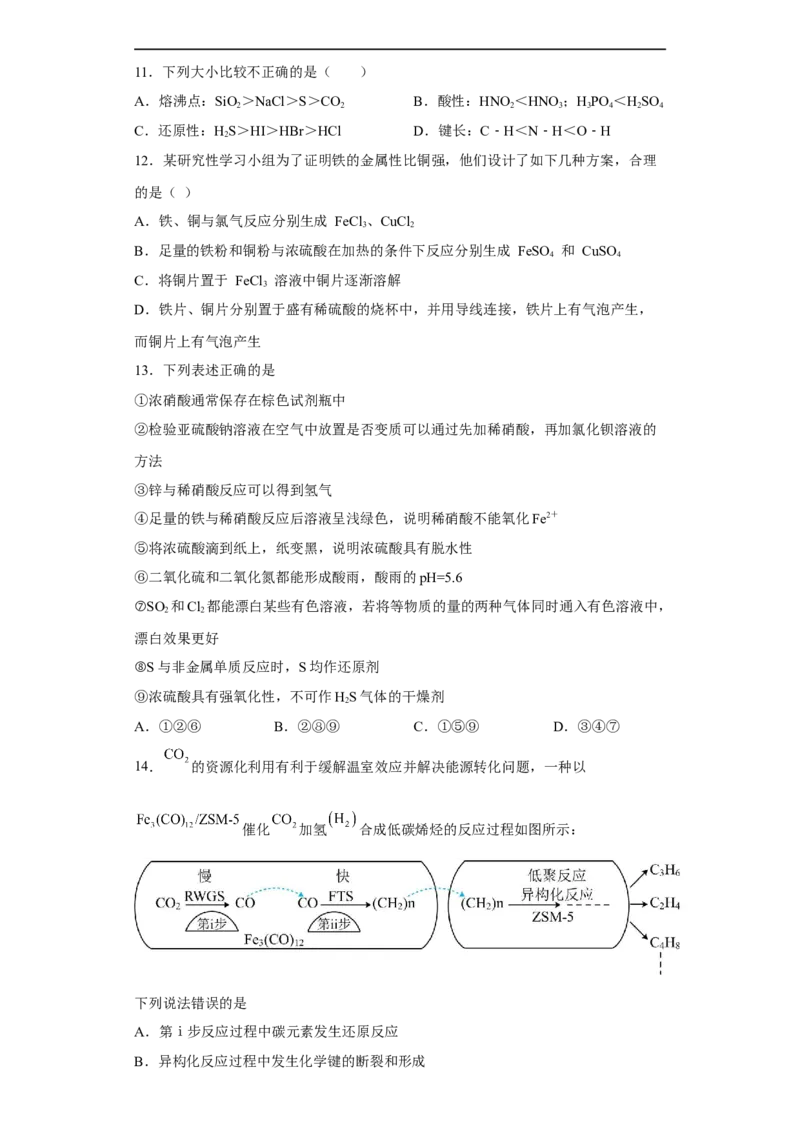
8.探究是培养创新精神和实践能力的手段。用如下装置探究氯气的性质,图中三支试
管口均放置浸有NaOH溶液的棉花。下列对实验现象的分析正确的是
A.①中淀粉KI试纸变蓝
B.②中产生白色沉淀,说明氯气与水反应生成Cl-
C.一段时间后向③中加入KSCN溶液,溶液未变色
D.④溶液先变红后褪色,说明氯气具有酸性和漂白性
9.已知X、Y、Z、W四种短周期主族元素的原子序数依次增大,X原子的最外层电
子数与电子层数相等,Y与X同主族,且最高价化物对应的水化物是一种强碱,Z的
一种氧化物溶在雨水中,可形成酸雨。下列说法正确的是
A.原子半径大小:
B.X与Y、Z、W三种元素都可形成共价化合物
C.非金属性
D.W的单质常用于自来水的杀菌消毒
10.关于下图装置的叙述,正确的是( )
A.铜是负极,铜片上有气泡产生
B.铜片质量逐渐减少
C.电流从锌片经导线流向铜片
D.氢离子在铜片表面被还原后生成H
211.下列大小比较不正确的是( )
A.熔沸点:SiO>NaCl>S>CO B.酸性:HNO<HNO;HPO <HSO
2 2 2 3 3 4 2 4
C.还原性:HS>HI>HBr>HCl D.键长:C﹣H<N﹣H<O﹣H
2
12.某研究性学习小组为了证明铁的金属性比铜强,他们设计了如下几种方案,合理
的是( )
A.铁、铜与氯气反应分别生成 FeCl 、CuCl
3 2
B.足量的铁粉和铜粉与浓硫酸在加热的条件下反应分别生成 FeSO 和 CuSO
4 4
C.将铜片置于 FeCl 溶液中铜片逐渐溶解
3
D.铁片、铜片分别置于盛有稀硫酸的烧杯中,并用导线连接,铁片上有气泡产生,
而铜片上有气泡产生
13.下列表述正确的是
①浓硝酸通常保存在棕色试剂瓶中
②检验亚硫酸钠溶液在空气中放置是否变质可以通过先加稀硝酸,再加氯化钡溶液的
方法
③锌与稀硝酸反应可以得到氢气
④足量的铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化Fe2+
⑤将浓硫酸滴到纸上,纸变黑,说明浓硫酸具有脱水性
⑥二氧化硫和二氧化氮都能形成酸雨,酸雨的pH=5.6
⑦SO 和Cl 都能漂白某些有色溶液,若将等物质的量的两种气体同时通入有色溶液中,
2 2
漂白效果更好
⑧S与非金属单质反应时,S均作还原剂
⑨浓硫酸具有强氧化性,不可作HS气体的干燥剂
2
A.①②⑥ B.②⑧⑨ C.①⑤⑨ D.③④⑦
14. 的资源化利用有利于缓解温室效应并解决能源转化问题,一种以
催化 加氢 合成低碳烯烃的反应过程如图所示:
下列说法错误的是
A.第ⅰ步反应过程中碳元素发生还原反应
B.异构化反应过程中发生化学键的断裂和形成C.该反应总过程的原子利用率为100%
D. 不影响 加氢合成低碳烯烃的
二、非选择题:58分
天然铝土矿中Al O 的含量为50% ~70%,杂质主要为SiO、Fe O、MgO等,工业上
2 3 2 2 3
用天然铝土矿生产铝锭的工艺流程如下:
已知部分氢氧化物沉淀的pH如下表:
沉淀物 Al(OH) Fe(OH) Mg(OH)
3 3 2
开始沉淀时的pH(离子初始浓度
3.7 2.2 9.6
为0.01 mol/L)
完全沉淀时的pH(离子浓度<10-5
4.7 3.2 11.1
mol/L)
请回答下列问题:
(1)为了加快反应速率,提高氧化铝的利用率,通常会将铝土矿先进行“操作①”后再
加入盐酸,“操作①”为______________________。
(2)加入盐酸时,氧化铝发生反应的离子方程式为_____________________。
(3)上述流程中多次重复的操作的名称为________________,该操作用到的玻璃仪器除
烧杯外还需要________________ 。
(4)“溶液B"中加入物质C调节pH的范围为________________,溶液中的Mg2+是在操
作________________ (填序号)中分离出去的。
(5)固体A的主要成分为_________________(填化学式,下同);固体F的主要成分为
________________。
(6)“操作⑥”在电解槽中进行,电解氧化铝一般是石墨和铁作两个电极,写出石墨电极上
发生反应的电极反应式:________________。若电解过程中转移了3 mol电子,则阴
极上生成物的质量为_________________g。
16.反应Fe+H SO =FeSO +H ↑的能量变化趋势,如图所示:
2 4 4 2(1)该反应为______反应(填“吸热”或“放热”)。
(2)若要使该反应的反应速率加快,下列措施可行的是______(填字母)。
A.改铁片为铁粉 B.增大压强 C.升高温度 D.将稀硫酸改为98%的浓硫酸
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为____极(填“正”
或“负”)。铜片上产生的现象为______,该极上发生的电极反应为______。
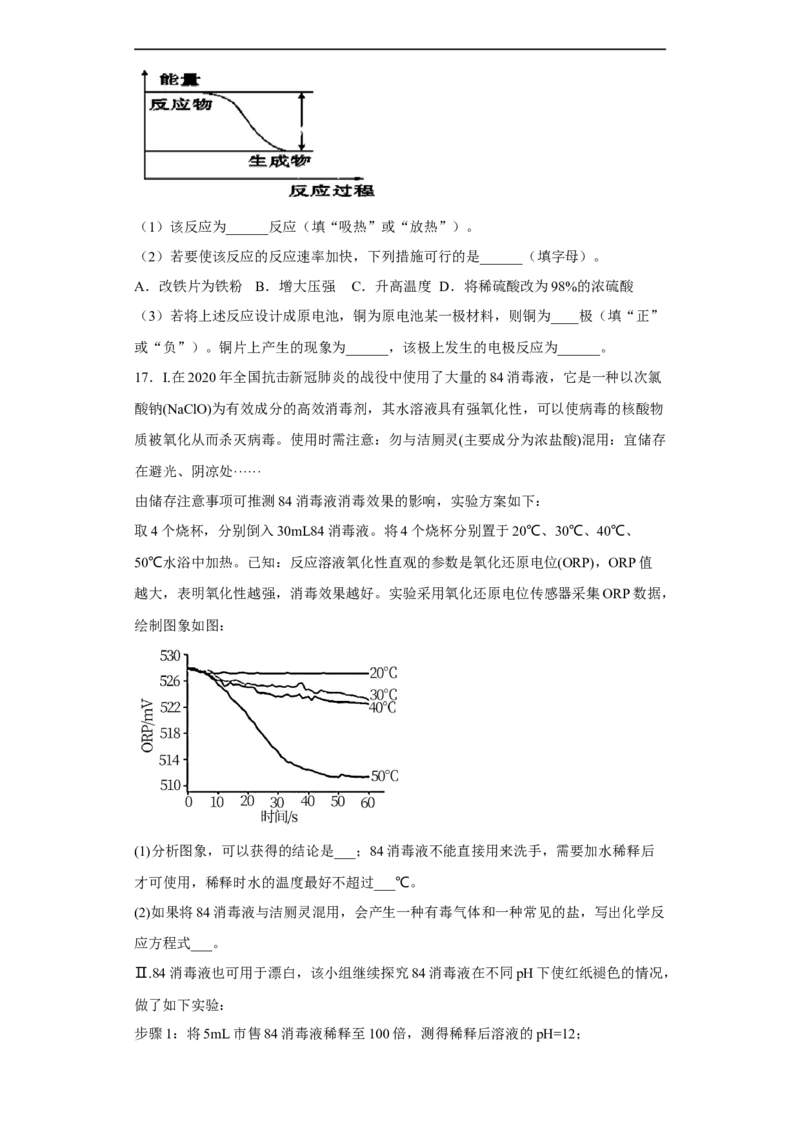
17.I.在2020年全国抗击新冠肺炎的战役中使用了大量的84消毒液,它是一种以次氯
酸钠(NaClO)为有效成分的高效消毒剂,其水溶液具有强氧化性,可以使病毒的核酸物
质被氧化从而杀灭病毒。使用时需注意:勿与洁厕灵(主要成分为浓盐酸)混用:宜储存
在避光、阴凉处······
由储存注意事项可推测84消毒液消毒效果的影响,实验方案如下:
取4个烧杯,分别倒入30mL84消毒液。将4个烧杯分别置于20℃、30℃、40℃、
50℃水浴中加热。已知:反应溶液氧化性直观的参数是氧化还原电位(ORP),ORP值
越大,表明氧化性越强,消毒效果越好。实验采用氧化还原电位传感器采集ORP数据,
绘制图象如图:
(1)分析图象,可以获得的结论是___;84消毒液不能直接用来洗手,需要加水稀释后
才可使用,稀释时水的温度最好不超过___℃。
(2)如果将84消毒液与洁厕灵混用,会产生一种有毒气体和一种常见的盐,写出化学反
应方程式___。
Ⅱ.84消毒液也可用于漂白,该小组继续探究84消毒液在不同pH下使红纸褪色的情况,
做了如下实验:
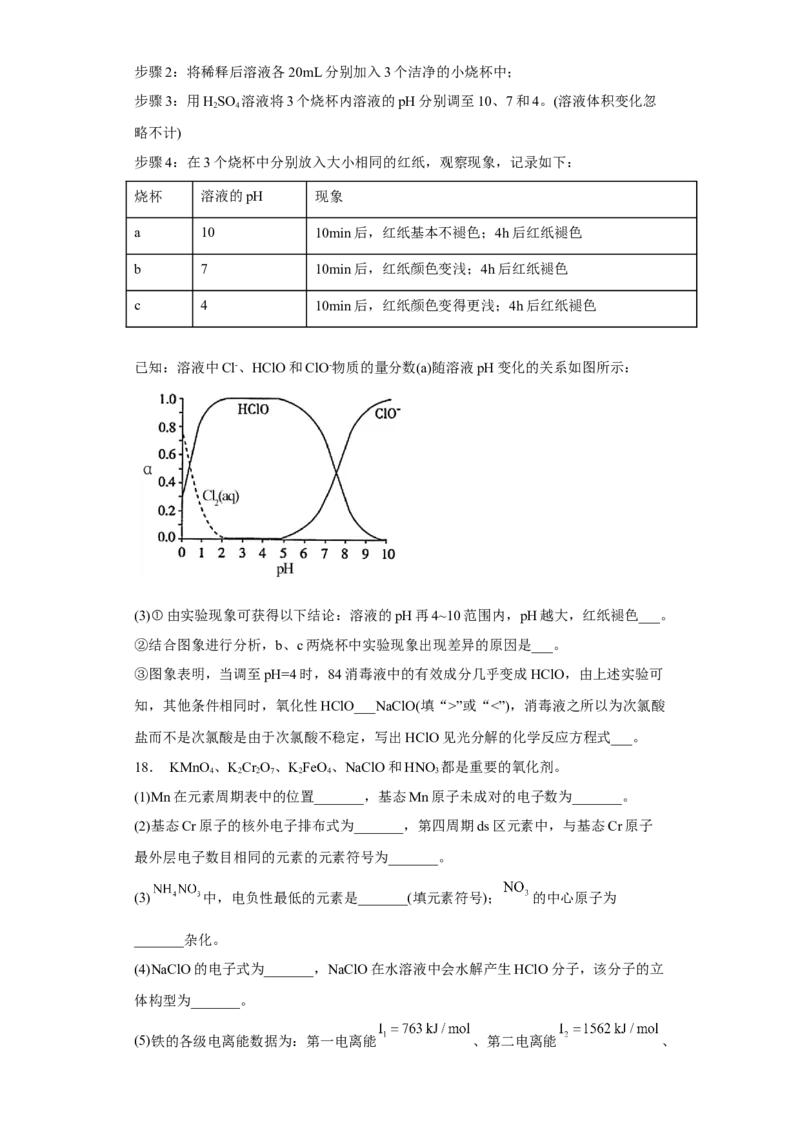
步骤1:将5mL市售84消毒液稀释至100倍,测得稀释后溶液的pH=12;步骤2:将稀释后溶液各20mL分别加入3个洁净的小烧杯中;
步骤3:用HSO 溶液将3个烧杯内溶液的pH分别调至10、7和4。(溶液体积变化忽
2 4
略不计)
步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
烧杯 溶液的pH 现象
a 10 10min后,红纸基本不褪色;4h后红纸褪色
b 7 10min后,红纸颜色变浅;4h后红纸褪色
c 4 10min后,红纸颜色变得更浅;4h后红纸褪色
已知:溶液中Cl-、HClO和ClO-物质的量分数(a)随溶液pH变化的关系如图所示:
(3)①由实验现象可获得以下结论:溶液的pH再4~10范围内,pH越大,红纸褪色___。
②结合图象进行分析,b、c两烧杯中实验现象出现差异的原因是___。
③图象表明,当调至pH=4时,84消毒液中的有效成分几乎变成HClO,由上述实验可
知,其他条件相同时,氧化性HClO___NaClO(填“>”或“<”),消毒液之所以为次氯酸
盐而不是次氯酸是由于次氯酸不稳定,写出HClO见光分解的化学反应方程式___。
18. KMnO 、KCr O、KFeO、NaClO和HNO 都是重要的氧化剂。
4 2 2 7 2 4 3
(1)Mn在元素周期表中的位置_______,基态Mn原子未成对的电子数为_______。
(2)基态Cr原子的核外电子排布式为_______,第四周期ds区元素中,与基态Cr原子
最外层电子数目相同的元素的元素符号为_______。
(3) 中,电负性最低的元素是_______(填元素符号); 的中心原子为
_______杂化。
(4)NaClO的电子式为_______,NaClO在水溶液中会水解产生HClO分子,该分子的立
体构型为_______。
(5)铁的各级电离能数据为:第一电离能 、第二电离能 、第三电离能 、第四电离能 、第五电离能
, 明显大于 的原因是_______。
(6)与CO 相同,COS中所有原子最外层也都满足8电子结构,COS属于_______分子
2
(填“极性”或“非极性”)。参考答案
1.A 2.C 3.A 4.A 5.A 6.A 7.C 8.A 9.D 10.D 11.D 12.D 13.C 14.
C
15. 粉碎 Al O+6H+=2Al3++3H O 过滤 玻璃棒、漏
2 3 2
斗 3. 2≤pH<3.7 ④ SiO Al(OH) 2O2- -4e-=O ↑ 27
2 3 2
16. 放热 AC 正 有气泡产生 2H++2e-=H ↑
2
17.(1) 低于40℃时,NaClO能稳定存在;高于40℃时,NaClO易分解 40
(2)NaClO+2HCl=NaCl+Cl +H O
2 2
(3) 越慢 b烧杯中溶液的pH大于c烧杯中溶液的pH,HClO的浓度较小,反应
速率较慢,褪色较慢 > 2HClO 2HCl+O ↑
2
18.(1) 第四周期ⅦB族 5
(2) 1s22s22p63s23p63d54s1或[Ar]3d54s1 Cu
(3) H sp2
(4) V(角)形
(5)铁的价层电子排布式为3d64s2,当失去第四个电子时需要破坏半充满的较稳定状态,所
需能量更高,因此I 明显大于I
4 3
(6)极性