文档内容
第 03 讲 氮及其重要化合物
目录
01 模拟基础练
【题型一】氮气及其化合物
【题型二】氮的固定和氮循环
【题型三】 氮的氧化物
【题型四】氨气和铵盐
【题型五】硝酸的性质
【题型六】硝酸的计算
【题型七】氮及其化合物综合实验探究
02 重难创新练
03 真题实战练
题型一 氮气及其化合物
1.(2024·浙江省宁波市镇海中学选考模拟)氮及其化合物的转化具有重要应用,下列说法不正确的是(
)
A.工业上模拟自然界“雷雨发庄稼”的过程生产HNO
3
B.自然固氮、人工固氮都是将N 转化为含氮化合物
2
C.氨气是重要的工业原料,可用于制备化肥和纯碱等大宗化学品
D.多种形态的氮及其化合物间的转化形成了自然界的“氮循环”
2.下列说法中正确的是( )
A.氮气的化学性质不如磷活泼,故氮元素的非金属性弱于磷元素
B.磷酸比硝酸稳定,所以磷元素的非金属性比氮元素强
C.“雷雨发庄稼”所包含的化学变化有:N→NO→NO →HNO→硝酸盐
2 2 3
D.NO与O 反应生成NO ,属于氮的固定
2 2
3.不同价态含氮物质的转化如图所示,图中线路①②③是工业生产硝酸的主要途径。下列说法正确
的是( )。A.①中的反应属于置换反应
B.②中的反应属于氮的固定
C.③中的化学方程式:2NO +H O 2HNO
2 2 3
D.使用CuO作氧化剂可以实现④的转化
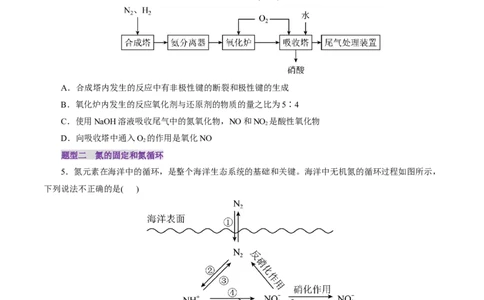
4.(2024·浙江省义乌中学模拟)氨既是一种重要的化工产品,又是一种重要的化工原料。如图为合成
氨以及氨氧化制硝酸的流程示意图。下列说法不正确的是( )
A.合成塔内发生的反应中有非极性键的断裂和极性键的生成
B.氧化炉内发生的反应氧化剂与还原剂的物质的量之比为5∶4
C.使用NaOH溶液吸收尾气中的氮氧化物,NO和NO 是酸性氧化物
2
D.向吸收塔中通入O 的作用是氧化NO
2
题型二 氮的固定和氮循环
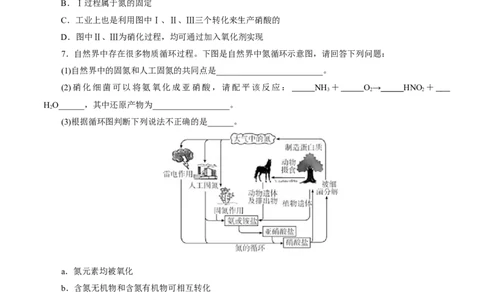
5.氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程如图所示,
下列说法不正确的是( )
A.海洋中的氮循环起始于氮的氧化
B.海洋中存在游离态的氮和化合态的氮
C.②中的含氮物质转化属于氮的固定
D.向海洋排放含NO -的废水会影响海洋中NH +的含量
3 4
6.自然界中的氮循环部分转化关系如图所示。下列说法错误的是( )
A.氮气分子结构稳定,常温很难和其他物质发生反应
B.Ⅰ过程属于氮的固定
C.工业上也是利用图中Ⅰ、Ⅱ、Ⅲ三个转化来生产硝酸的
D.图中Ⅱ、Ⅲ为硝化过程,均可通过加入氧化剂实现
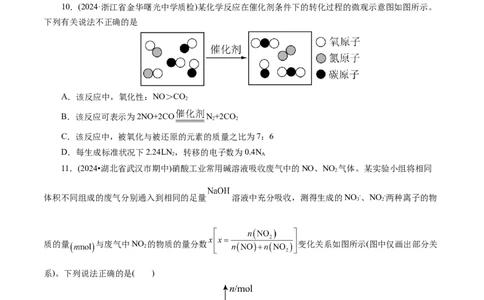
7.自然界中存在很多物质循环过程。下图是自然界中氮循环示意图,请回答下列问题:
(1)自然界中的固氮和人工固氮的共同点是_________________________。
(2)硝化细菌可以将氨氧化成亚硝酸,请配平该反应: NH + O→ HNO +
3 2 2
HO______,其中还原产物为__________________。
2
(3)根据循环图判断下列说法不正确的是______。
a.氮元素均被氧化
b.含氮无机物和含氮有机物可相互转化
c.工业合成氨属于人工固氮
d.模拟生物固氮是人工固氮发展的方向
题型三 氮的氧化物
8.标况下,将一盛有等体积NO、NO 的试管倒立在水槽中,充分反应后,下列叙述不正确的是(设试
2
管中的溶质不往试管外扩散)( )
A.溶液体积占试管容积的2/3
B.此反应中水既不作氧化剂也不作还原剂
C.试管内溶液中溶质的物质的量浓度为1/22.4mol/LD.若将试管中的气体改为氯化氢或氨气,则水充满试管
9.在一定温度和催化剂作用下,NO跟NH 可以发生反应生成N 和HO。现有NO和NH 的混合物1
3 2 2 3
mol,充分反应后所得产物中,经还原得到的N 比经氧化得到的N 多1.4 g。已知反应的化学方程式:
2 2
4NH +6NO=====5N+6HO,则下列说法正确的是( )
3 2 2
A.当转移的电子数约为3.612×1023时,则标准状况下有4.48 L氨气被还原
B.氧化产物和还原产物的物质的量比为3∶2
C.若以上反应进行完全,原混合物中NO与NH 的物质的量之比为可能为3∶7
3
D.若有混合物中有0.2 mol NH ,则参与反应的NO为0.8 mol
3
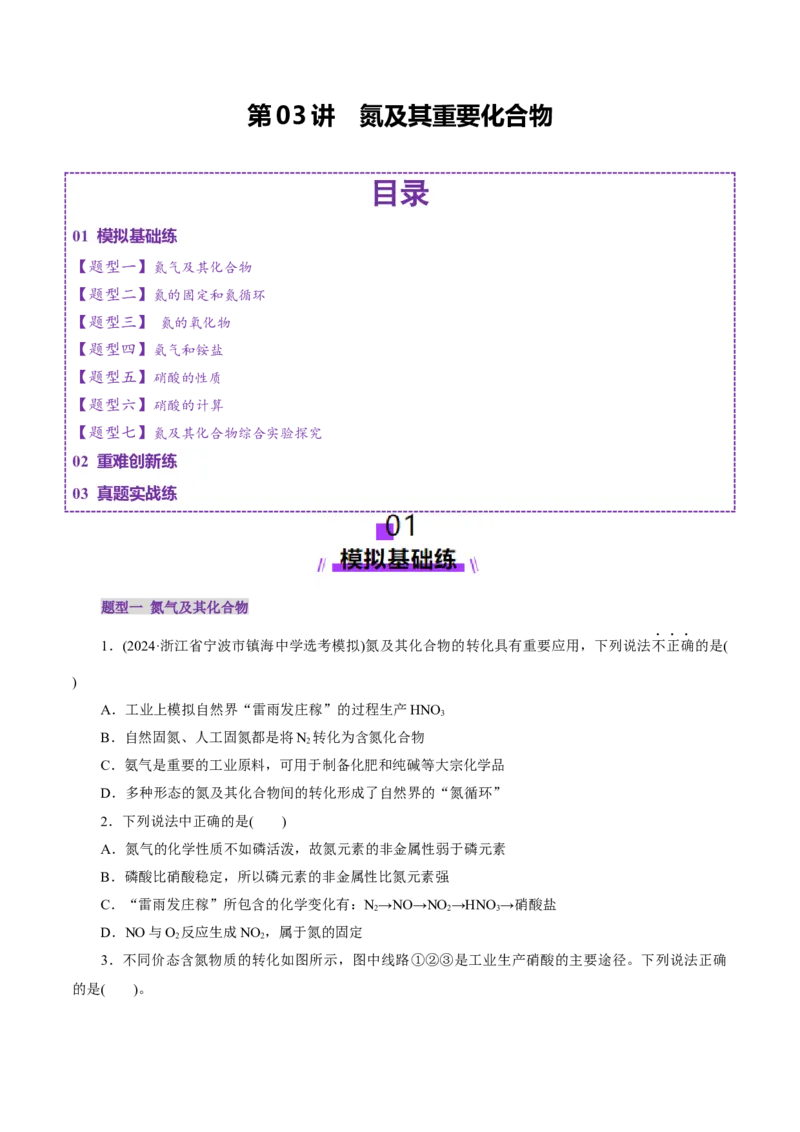
10.(2024·浙江省金华曙光中学质检)某化学反应在催化剂条件下的转化过程的微观示意图如图所示。
下列有关说法不正确的是
A.该反应中,氧化性:NO>CO
2
B.该反应可表示为2NO+2CO N+2CO
2 2
C.该反应中,被氧化与被还原的元素的质量之比为7:6
D.每生成标准状况下2.24LN ,转移的电子数为0.4N
2 A
11.(2024•湖北省武汉市期中)硝酸工业常用碱溶液吸收废气中的NO、NO 气体。某实验小组将相同
2
体积不同组成的废气分别通入到相同的足量 溶液中充分吸收,测得生成的NO -、NO -两种离子的物
3 2
质的量 与废气中NO 的物质的量分数 变化关系如图所示(图中仅画出部分关
2
系)。下列说法正确的是( )
A.参与反应的NaOH物质的量为 B.随 值增大,溶液中n(NO -) + n(NO -)增大
3 2
C.当 时, D.当 时,反应中转移的电子为题型四 氨气和铵盐
12.某同学探究氨气和铵盐的性质,对相关实验操作及现象描述正确的是( )
A.室温下测定等浓度氨水和NaOH溶液的pH,比较氨水和NaOH碱性强弱
B.向试管中滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口,若试纸不变蓝,则原溶液中无NH
C.液氨作为清洁能源的反应原理是4NH +5O=====4NO+6HO
3 2 2
D.加热可除去NH Cl中的少量NaHCO
4 3
13.实验室制取氨、收集、验证其还原性并进行尾气处理的装置和原理能达到实验目的的是( )
A.用装置甲制取氨
B.用装置乙收集氨时气体应该从a口进b口出
C.装置丙中黑色固体变成红色时还原产物一定为铜
D.可以用装置丁吸收氨,进行尾气处理
14.如下图,利用培养皿探究氨的性质。实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣
在上面。下表中对实验现象所做的解释正确的是( )
选项 实验现象 解释
A 浓盐酸附近产生白烟 NH 与浓盐酸反应产生了NH Cl固体
3 4
B 浓硫酸附近无明显现象 NH 与浓硫酸不发生反应
3
C 氯化物溶液变浑浊 该溶液一定是AlCl 溶液
3
干燥红色石蕊试纸不变色,湿润
D NH 是一种可溶性碱
3
红色石蕊试纸变蓝
题型五 硝酸的性质
15.下述实验中均有红棕色气体产生,对比分析所得结论错误的是( )
① ② ③
A.由①中的红棕色气体,推断产生的气体一定是混合气体B.红棕色气体不能表明②中木炭与浓硝酸发生了反应
C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D.③的气体产物中检测出CO,由此说明木炭一定与浓硝酸发生了反应
2
16.下列有关实验操作、现象和解释或结论都正确的是( )
实验操作 现象 解释或结论
过量的 Fe 粉中加入稀 HNO ,充
① 3 溶液呈红色 稀HNO 将Fe氧化为Fe3+
分反应后,滴入KSCN溶液 3
② 浓HNO 久置或光照 变黄色 HNO 不稳定易分解
3 3
Al箔表面被HNO 氧化,
③ Al箔插入稀HNO 中 无现象 3
3 形成致密的氧化膜
用玻璃棒蘸取浓HNO 点到蓝色石 试纸先变红色后褪 浓 HNO 具有酸性和强氧
④ 3 3
蕊试纸上 色 化性
A.①② B.③④ C.②③④ D.②④
17.实验室可用 KNO 固体与酸反应制取硝酸,其实验装置如图所示(加热装置已省略)。
3
下列说法错误的是( )
A.该装置不用橡皮塞和橡皮管,可避免被酸腐蚀
B.制取硝酸时曲颈甑中盛放的是硝酸钾和稀硫酸
C.用流水冷却,可促进硝酸蒸气冷凝,避免形成酸雾
D.该装置用于制取液溴时,可在曲颈甑中加入 NaBr、MnO 及浓硫酸
2
18.一定温度下探究铜与稀硝酸的反应,反应过程如图:
下列说法不正确的是( )
A.过程Ⅰ中生成气体的离子方程式为3Cu+8H++2NO===3Cu2++2NO↑+4HO
2
B.过程Ⅲ反应速率比过程Ⅰ快的原因是反应放热使温度升高致使速率加快
C.当活塞不再移动时,即使再抽入空气,金属铜屑也不继续溶解
D.②振荡时,针管内可能会发生的反应有4NO +O+2HO===4HNO
2 2 2 3
题型六 硝酸的计算19. 1.92g铜投入一定量浓HNO 中,铜完全溶解,生成气体颜色越来越浅,共收集到672mL气体(标
3
准情况)。将盛有此气体的容器倒扣在水中,通入标准情况下一定体积的O,恰好使气体完全溶于水中,
2
则通入O 的体积为( )
2
A.672mL B.168mL C.504mL D.336mL
20.某稀溶液中含有4 mol KNO 和2.5 mol H SO ,向其中加入1.5 mol Fe,充分反应(已知NO被还原
3 2 4
为NO)。
下列说法正确的是( )
A.反应后生成NO的体积为28 L
B.所得溶液中c(Fe2+)∶c(Fe3+)=1∶1
C.所得溶液中c(NO)=2.75 mol·L-1
D.所得溶液中的溶质只有FeSO
4
21.将质量为32g的铜与150mL的一定浓度的硝酸反应,铜完全溶解,产生标准状况下11.2L的NO
和NO 的混合气体,将生成的混合气体与一定体积的氧气一起通入足量 NaOH溶液中,气体恰好被吸收生
2
成NaNO 。下列说法不正确的是( )
3
A.标准状况下,通入的O 体积为5.6L
2
B.向反应后的溶液加NaOH,使铜沉淀完全,需要NaOH的物质的量至少为1.0mol
C.标准状况下,混合气体构成是5.6L的NO和5.6L的NO
2
D.硝酸的物质的量浓度为10.0mol·L−1
22.向500 mL稀硝酸中加入一定质量的铁粉,恰好使铁粉完全溶解,放出NO气体5.6 L(标准状况),
同时溶液质量增加9.3 g。下列判断正确的是( )
A.原溶液中投入铁粉物质的量是0.25 mol
B.原溶液中HNO 的浓度是 2.0 mol·L-1
3
C.反应后的溶液中还可溶解9.6 g铜
D.反应后的溶液中 c(Fe2+)∶c(Fe3+)=1∶2
23.足量铜与一定量的浓硝酸反应,得到硝酸铜溶液和NO 、NO的混合气体2.24 L(标准状况下),这
2
些气体与一定体积O(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液
2
中加入4 mol·L-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是50 mL,下列说法正确的是(
)。
A.参加反应的硝酸的物质的量为0.2 mol
B.消耗氧气的体积为2.24 L(标准状况下)
C.铜和硝酸反应过程中转移电子的物质的量为0.3 mol
D.混合气体中含NO 1.12 L(标准状况下)
2
题型七 氮及其化合物综合实验探究
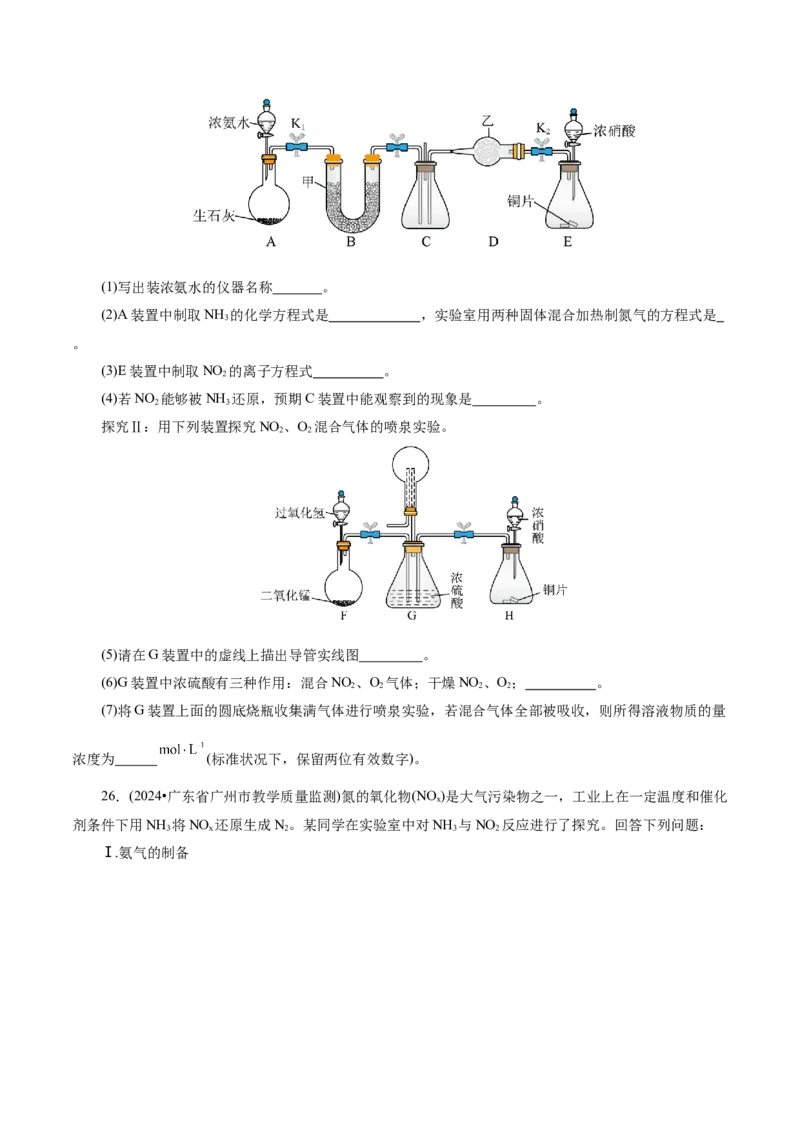
24.(2024·河北省部分学校高三七调考试)某化学教师利用如图装置(部分装置省略)改进铜与硝酸及相关反应。
回答下列问题:
(1)按图所示装置组装实验仪器,打开K、K、K、K,关闭K,并向两侧烧杯中加水至 ,
1 2 3 5 4
用气压法检查装置气密性。
(2)在集气瓶中的下层加入四氯化碳,上层加入水,并将绕有铜丝固定的封铁短玻璃导管固定于下层;
关闭K、K、K、K,打开K,用磁铁固定绕有铜丝固定的封铁短玻璃导管于试管口,加入 浓硝酸,
2 3 4 5 1
关闭 ,打开K、K、K,将铜丝移入浓硝酸中,其中四氯化碳的作用是 ;铜与浓硝酸反应
2 3 5
现象为 ;其反应的离子方程式为 。
(3) 传感器读数逐步下降到1以下时,将铜丝与浓硝酸脱离, (填操作),此时右侧烧杯
内的 溶液会倒吸入具支试管中,同时产生蓝色沉淀。
(4)用磁铁将集气瓶中的铜丝移至水层,水层中产生无色气体,同时溶液变为蓝色,水层发生反应的离
子方程式为 。
(5)针筒中充满红棕色气体,颜色逐渐变浅,并产生白烟,白烟名称为 。
(6)左侧烧杯中 溶液的作用: 。
(7)任写一条该实验设计的优点: 。
25.(2024•福建省福州市福建师大附中期中)某化学自主实验小组通过实验探究NH 、NO 的性质。
3 2
探究Ⅰ:利用如图所示装置探究NO 能否被NH 还原(K 、K 为止水夹,夹持固定装置略去)。
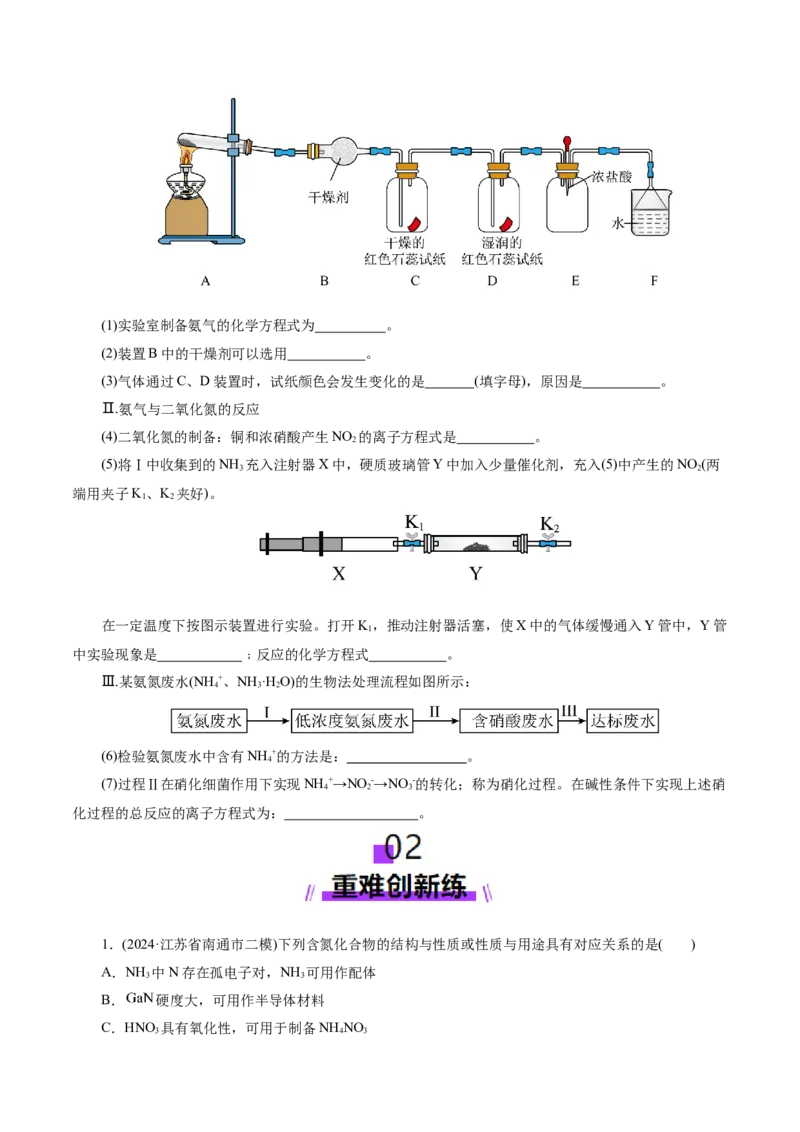
2 3 1 2(1)写出装浓氨水的仪器名称 。
(2)A装置中制取NH 的化学方程式是 ,实验室用两种固体混合加热制氮气的方程式是
3
。
(3)E装置中制取NO 的离子方程式 。
2
(4)若NO 能够被NH 还原,预期C装置中能观察到的现象是 。
2 3
探究Ⅱ:用下列装置探究NO 、O 混合气体的喷泉实验。
2 2
(5)请在G装置中的虚线上描出导管实线图 。
(6)G装置中浓硫酸有三种作用:混合NO 、O 气体;干燥NO 、O; 。
2 2 2 2
(7)将G装置上面的圆底烧瓶收集满气体进行喷泉实验,若混合气体全部被吸收,则所得溶液物质的量
浓度为 (标准状况下,保留两位有效数字)。
26.(2024•广东省广州市教学质量监测)氮的氧化物(NO )是大气污染物之一,工业上在一定温度和催化
x
剂条件下用NH 将NO 还原生成N。某同学在实验室中对NH 与NO 反应进行了探究。回答下列问题:
3 x 2 3 2
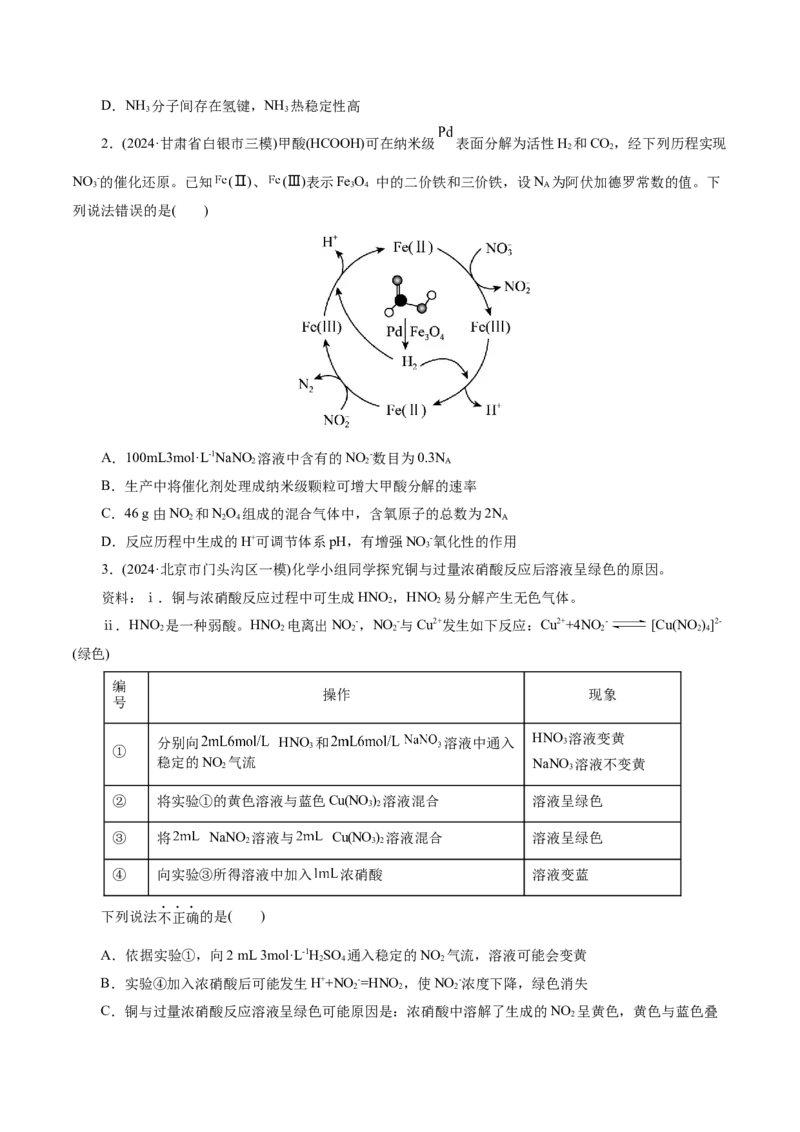
Ⅰ.氨气的制备(1)实验室制备氨气的化学方程式为 。
(2)装置B中的干燥剂可以选用 。
(3)气体通过C、D装置时,试纸颜色会发生变化的是 (填字母),原因是 。
Ⅱ.氨气与二氧化氮的反应
(4)二氧化氮的制备:铜和浓硝酸产生NO 的离子方程式是 。
2
(5)将Ⅰ中收集到的NH 充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入(5)中产生的NO (两
3 2
端用夹子K、K 夹好)。
1 2
在一定温度下按图示装置进行实验。打开K,推动注射器活塞,使X中的气体缓慢通入Y管中,Y管
1
中实验现象是 ﹔反应的化学方程式 。
Ⅲ.某氨氮废水(NH +、NH ·H O)的生物法处理流程如图所示:
4 3 2
(6)检验氨氮废水中含有NH +的方法是: 。
4
(7)过程Ⅱ在硝化细菌作用下实现NH +→NO -→NO -的转化;称为硝化过程。在碱性条件下实现上述硝
4 2 3
化过程的总反应的离子方程式为: 。
1.(2024·江苏省南通市二模)下列含氮化合物的结构与性质或性质与用途具有对应关系的是( )
A.NH 中N存在孤电子对,NH 可用作配体
3 3
B. 硬度大,可用作半导体材料
C.HNO 具有氧化性,可用于制备NH NO
3 4 3D.NH 分子间存在氢键,NH 热稳定性高
3 3
2.(2024·甘肃省白银市三模)甲酸(HCOOH)可在纳米级 表面分解为活性H 和CO,经下列历程实现
2 2
NO -的催化还原。已知 (Ⅱ)、 (Ⅲ)表示Fe O 中的二价铁和三价铁,设N 为阿伏加德罗常数的值。下
3 3 4 A
列说法错误的是( )
A.100mL3mol·L-1NaNO 溶液中含有的NO -数目为0.3N
2 2 A
B.生产中将催化剂处理成纳米级颗粒可增大甲酸分解的速率
C.46 g由NO 和NO 组成的混合气体中,含氧原子的总数为2N
2 2 4 A
D.反应历程中生成的H+可调节体系pH,有增强NO -氧化性的作用
3
3.(2024·北京市门头沟区一模)化学小组同学探究铜与过量浓硝酸反应后溶液呈绿色的原因。
资料:ⅰ.铜与浓硝酸反应过程中可生成HNO,HNO 易分解产生无色气体。
2 2
ⅱ.HNO 是一种弱酸。HNO 电离出NO -,NO -与Cu2+发生如下反应:Cu2++4NO- [Cu(NO )]2-
2 2 2 2 2 2 4
(绿色)
编
操作 现象
号
HNO 溶液变黄
分别向 HNO 和 溶液中通入 3
① 3
稳定的NO 气流 NaNO 溶液不变黄
2 3
② 将实验①的黄色溶液与蓝色Cu(NO ) 溶液混合 溶液呈绿色
3 2
③ 将 NaNO 溶液与 Cu(NO ) 溶液混合 溶液呈绿色
2 3 2
④ 向实验③所得溶液中加入 浓硝酸 溶液变蓝
下列说法不正确的是( )
A.依据实验①,向2 mL 3mol·L-1HSO 通入稳定的NO 气流,溶液可能会变黄
2 4 2
B.实验④加入浓硝酸后可能发生H++NO-=HNO ,使NO -浓度下降,绿色消失
2 2 2
C.铜与过量浓硝酸反应溶液呈绿色可能原因是:浓硝酸中溶解了生成的NO 呈黄色,黄色与蓝色叠
2加呈绿色
D.铜与过量浓硝酸反应溶液呈绿色可能原因是:铜与浓硝酸反应过程中,生成[Cu(NO )]2-使溶液呈
2 4
绿色
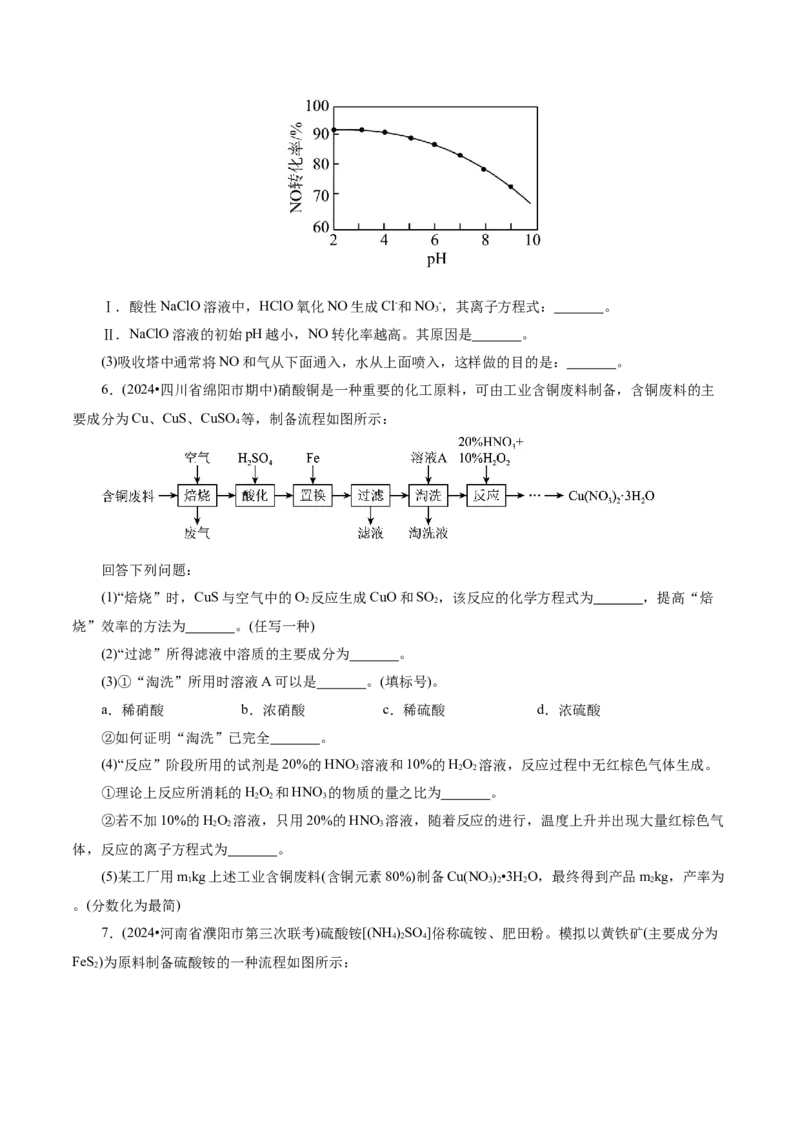
4.(2024·安徽省淮北市一模)实验室中用如图装置,以氨气和钠为原料加热至 制备氨基钠
(NaNH ),并检验气体产物.已知:NaNH 极易水解.下列说法正确的是( )
2 2
A.装置A中的药品是氯化铵固体
B.装置B和装置D均只起到干燥作用
C.实验时先点燃C处酒精灯,再点燃A处酒精灯
D.装置E中黑色粉末变成红色,证明有氢气生成\
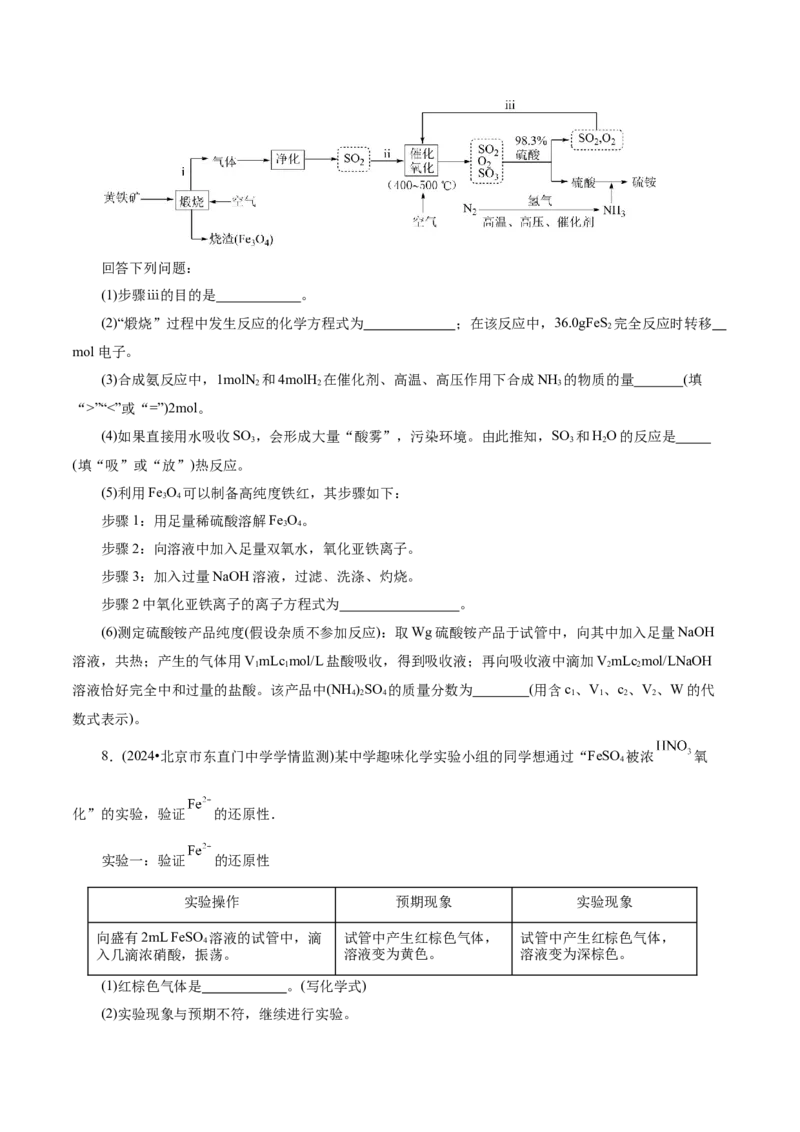
5.(2024•江苏省扬州大学附属中学月考)氨是工业生产硝酸的重要原料,请根据以下工业制硝酸的原
理示意图回答含氮化合物相关的问题:
(1)氨气在“氧化炉”中所发生反应的化学方程式为 。
(2)“吸收塔”尾部会有含NO、NO 等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以
2
下两种方法处理:
①氨转化法。已知7mol氨恰好能将含NO和NO 共6mol的混合气体完全转化为N,则混合气体中
2 2
NO和NO 的物质的量之比为 。
2
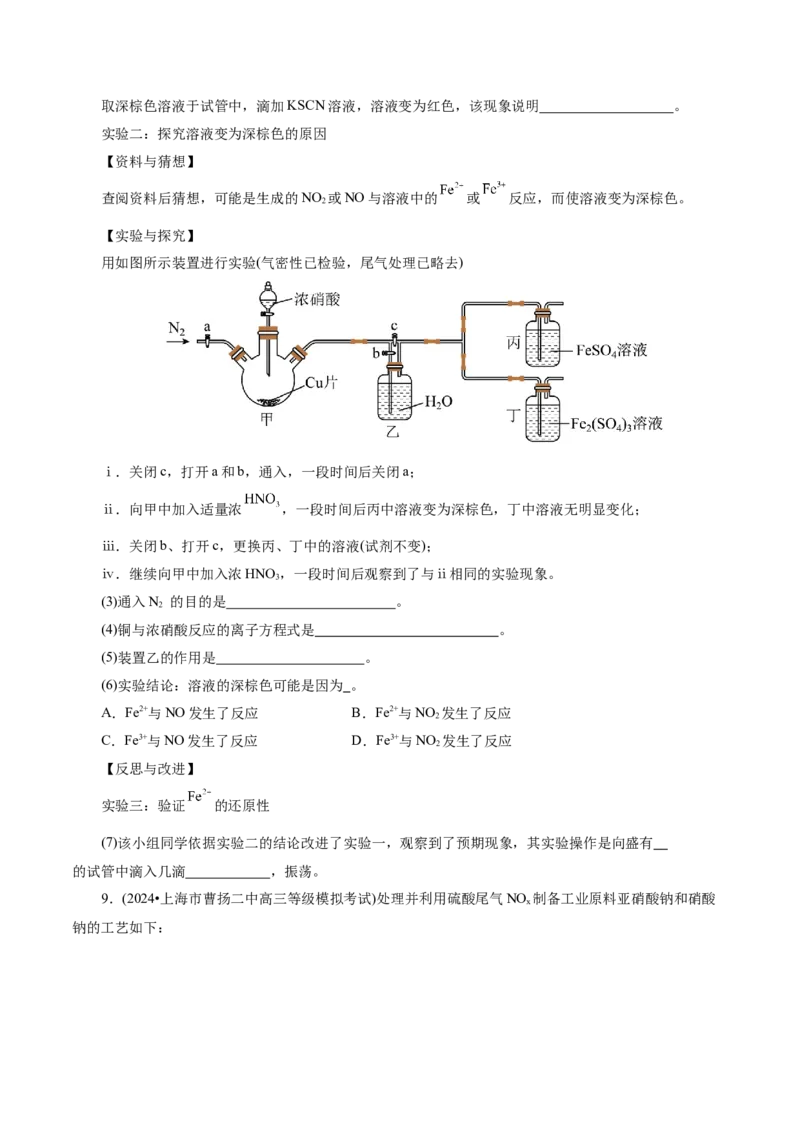
②NaClO溶液氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,
NO转化为NO -的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示:
3Ⅰ.酸性NaClO溶液中,HClO氧化NO生成Cl-和NO -,其离子方程式: 。
3
Ⅱ.NaClO溶液的初始pH越小,NO转化率越高。其原因是 。
(3)吸收塔中通常将NO和气从下面通入,水从上面喷入,这样做的目的是: 。
6.(2024•四川省绵阳市期中)硝酸铜是一种重要的化工原料,可由工业含铜废料制备,含铜废料的主
要成分为Cu、CuS、CuSO 等,制备流程如图所示:
4
回答下列问题:
(1)“焙烧”时,CuS与空气中的O 反应生成CuO和SO ,该反应的化学方程式为 ,提高“焙
2 2
烧”效率的方法为 。(任写一种)
(2)“过滤”所得滤液中溶质的主要成分为 。
(3)①“淘洗”所用时溶液A可以是 。(填标号)。
a.稀硝酸 b.浓硝酸 c.稀硫酸 d.㳖硫酸
②如何证明“淘洗”已完全 。
(4)“反应”阶段所用的试剂是20%的HNO 溶液和10%的HO 溶液,反应过程中无红棕色气体生成。
3 2 2
①理论上反应所消耗的HO 和HNO 的物质的量之比为 。
2 2 3
②若不加10%的HO 溶液,只用20%的HNO 溶液,随着反应的进行,温度上升并出现大量红棕色气
2 2 3
体,反应的离子方程式为 。
(5)某工厂用mkg上述工业含铜废料(含铜元素80%)制备Cu(NO )•3H O,最终得到产品mkg,产率为
1 3 2 2 2
。(分数化为最简)
7.(2024•河南省濮阳市第三次联考)硫酸铵[(NH )SO ]俗称硫铵、肥田粉。模拟以黄铁矿(主要成分为
4 2 4
FeS)为原料制备硫酸铵的一种流程如图所示:
2回答下列问题:
(1)步骤ⅲ的目的是 。
(2)“煅烧”过程中发生反应的化学方程式为 ;在该反应中,36.0gFeS 完全反应时转移
2
mol电子。
(3)合成氨反应中,1molN 和4molH 在催化剂、高温、高压作用下合成NH 的物质的量 (填
2 2 3
“>”“<”或“=”)2mol。
(4)如果直接用水吸收SO ,会形成大量“酸雾”,污染环境。由此推知,SO 和HO的反应是
3 3 2
(填“吸”或“放”)热反应。
(5)利用Fe O 可以制备高纯度铁红,其步骤如下:
3 4
步骤1:用足量稀硫酸溶解Fe O。
3 4
步骤2:向溶液中加入足量双氧水,氧化亚铁离子。
步骤3:加入过量NaOH溶液,过滤﹑洗涤、灼烧。
步骤2中氧化亚铁离子的离子方程式为 。
(6)测定硫酸铵产品纯度(假设杂质不参加反应):取Wg硫酸铵产品于试管中,向其中加入足量NaOH
溶液,共热;产生的气体用VmLcmol/L盐酸吸收,得到吸收液;再向吸收液中滴加VmLcmol/LNaOH
1 1 2 2
溶液恰好完全中和过量的盐酸。该产品中(NH )SO 的质量分数为 (用含c、V、c、V、W的代
4 2 4 1 1 2 2
数式表示)。
8.(2024•北京市东直门中学学情监测)某中学趣味化学实验小组的同学想通过“FeSO 被浓 氧
4
化”的实验,验证 的还原性.
实验一:验证 的还原性
实验操作 预期现象 实验现象
向盛有2mL FeSO 溶液的试管中,滴 试管中产生红棕色气体, 试管中产生红棕色气体,
4
入几滴浓硝酸,振荡。 溶液变为黄色。 溶液变为深棕色。
(1)红棕色气体是 。(写化学式)
(2)实验现象与预期不符,继续进行实验。取深棕色溶液于试管中,滴加KSCN溶液,溶液变为红色,该现象说明 。
实验二:探究溶液变为深棕色的原因
【资料与猜想】
查阅资料后猜想,可能是生成的NO 或NO与溶液中的 或 反应,而使溶液变为深棕色。
2
【实验与探究】
用如图所示装置进行实验(气密性已检验,尾气处理已略去)
ⅰ.关闭c,打开a和b,通入,一段时间后关闭a;
ⅱ.向甲中加入适量浓 ,一段时间后丙中溶液变为深棕色,丁中溶液无明显变化;
ⅲ.关闭b、打开c,更换丙、丁中的溶液(试剂不变);
ⅳ.继续向甲中加入浓HNO,一段时间后观察到了与ⅱ相同的实验现象。
3
(3)通入N 的目的是 。
2
(4)铜与浓硝酸反应的离子方程式是 。
(5)装置乙的作用是 。
(6)实验结论:溶液的深棕色可能是因为 。
A.Fe2+与NO发生了反应 B.Fe2+与NO 发生了反应
2
C.Fe3+与NO发生了反应 D.Fe3+与NO 发生了反应
2
【反思与改进】
实验三:验证 的还原性
(7)该小组同学依据实验二的结论改进了实验一,观察到了预期现象,其实验操作是向盛有
的试管中滴入几滴 ,振荡。
9.(2024•上海市曹扬二中高三等级模拟考试)处理并利用硫酸尾气NO 制备工业原料亚硝酸钠和硝酸
x
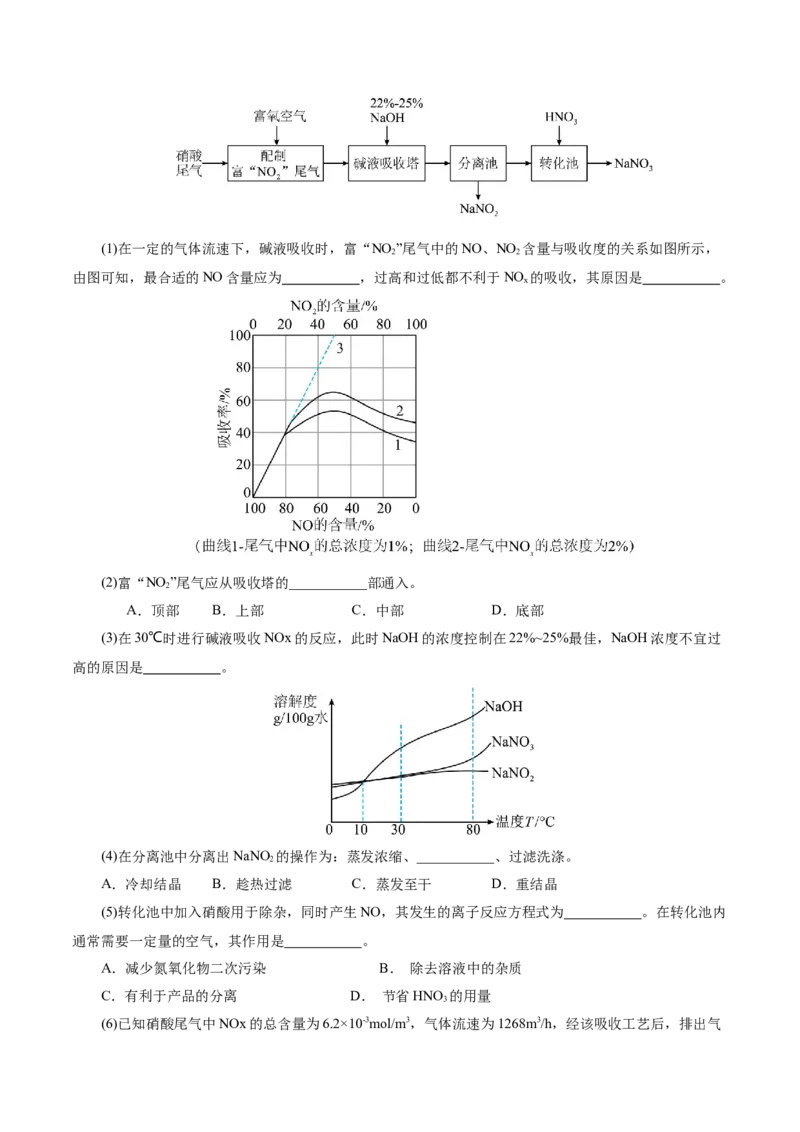
钠的工艺如下:(1)在一定的气体流速下,碱液吸收时,富“NO ”尾气中的NO、NO 含量与吸收度的关系如图所示,
2 2
由图可知,最合适的NO含量应为 ,过高和过低都不利于NO 的吸收,其原因是 。
x
(2)富“NO ”尾气应从吸收塔的___________部通入。
2
A.顶部 B.上部 C.中部 D.底部
(3)在30℃时进行碱液吸收NOx的反应,此时NaOH的浓度控制在22%~25%最佳,NaOH浓度不宜过
高的原因是 。
(4)在分离池中分离出NaNO 的操作为:蒸发浓缩、___________、过滤洗涤。
2
A.冷却结晶 B.趁热过滤 C.蒸发至干 D.重结晶
(5)转化池中加入硝酸用于除杂,同时产生NO,其发生的离子反应方程式为 。在转化池内
通常需要一定量的空气,其作用是 。
A.减少氮氧化物二次污染 B. 除去溶液中的杂质
C.有利于产品的分离 D. 节省HNO 的用量
3
(6)已知硝酸尾气中NOx的总含量为6.2×10-3mol/m3,气体流速为1268m3/h,经该吸收工艺后,排出气体中NOx的总含量降低为5.0×10-4mol/m3,则每小时至少需要质量分数为25%的NaOH溶液(密度为1.04g/
cm3) m3(保留2位有效数字)。
1.(2023•山东卷,2)实验室中使用盐酸、硫酸和硝酸时,对应关系错误的是( )
A.稀盐酸:配制AlCl 溶液
3
B.稀硫酸:蔗糖和淀粉的水解
C.稀硝酸:清洗附有银镜的试管
D.浓硫酸和浓硝酸的混合溶液:苯的磺化
2.(2023•辽宁省选择性考试,3)下列有关物质的工业制备反应错误的是( )
A.合成氨:N+3H 2NH B.制HCl:H+Cl 2HCl
2 2 3 2 2
C.制粗硅:SiO+2C Si+2CO D.冶炼镁:2MgO(熔融) 2Mg+O↑
2 2
3.(2023•浙江省1月选考,5)下列关于元素及其化合物的性质说法不正确的是( )
A. 和乙醇反应可生成H B.工业上煅烧黄铁矿(FeS )生产SO
2 2 2
C.工业上用氨的催化氧化制备NO D.常温下铁与浓硝酸反应可制备NO
2
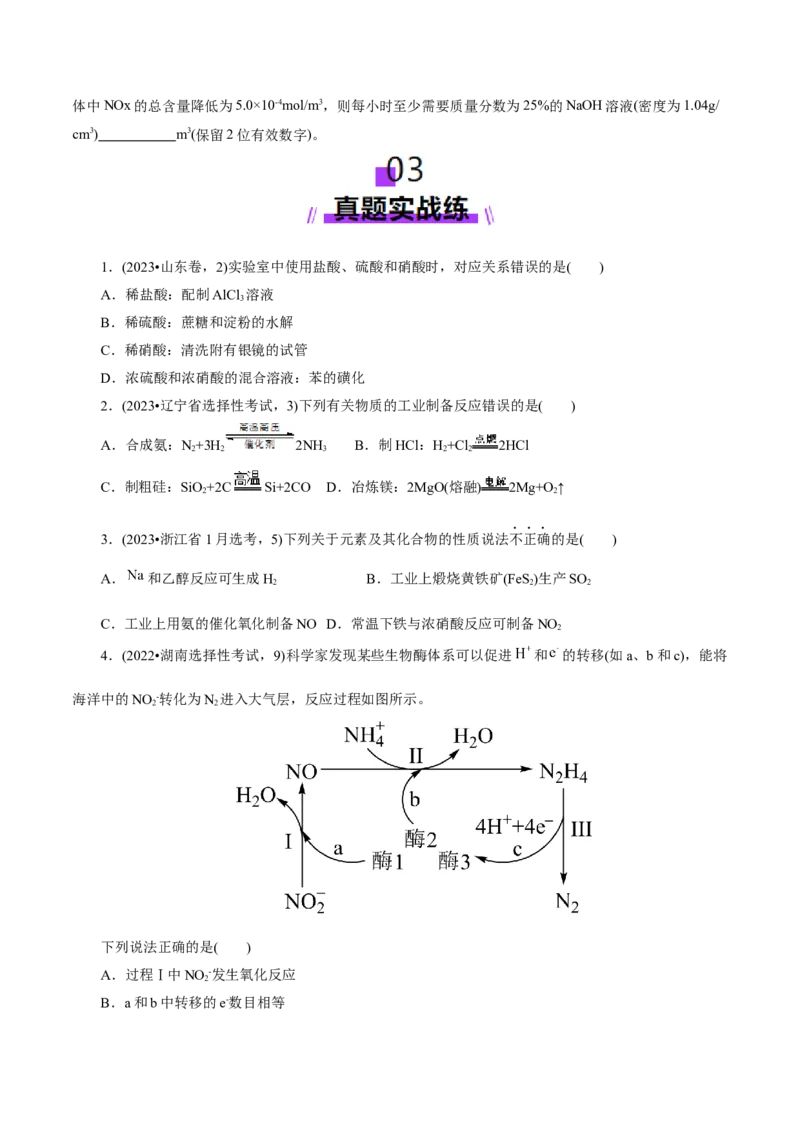
4.(2022•湖南选择性考试,9)科学家发现某些生物酶体系可以促进 和 的转移(如a、b和c),能将
海洋中的NO -转化为N 进入大气层,反应过程如图所示。
2 2
下列说法正确的是( )
A.过程Ⅰ中NO -发生氧化反应
2
B.a和b中转移的e-数目相等C.过程Ⅱ中参与反应的n(NO):n(NH +)=1:4
4
D.过程Ⅰ→Ⅲ的总反应为NO -+NH+=N ↑+2H O
2 4 2 2
5.(2021•浙江6月选考,16)关于化合物ClONO 的性质,下列推测不合理的是( )
2
A.具有强氧化性B.与NaOH溶液反应可生成两种钠盐
C.与盐酸作用能产生氯气 D.水解生成盐酸和硝酸
6.(2021·河北高考)关于非金属含氧酸及其盐的性质,下列说法正确的是( )
A.浓HSO 具有强吸水性,能吸收糖类化合物中的水分并使其炭化
2 4
B.NaClO、KClO 等氯的含氧酸盐的氧化性会随溶液的pH减小而增强
3
C.加热NaI与浓HPO 混合物可制备HI,说明HPO 比HI酸性强
3 4 3 4
D.浓HNO 和稀HNO 与Cu反应的还原产物分别为NO 和NO,故稀HNO 氧化性更强
3 3 2 3