文档内容
第 03 讲 氧化还原反应
【化学学科素养】
证据推理与模型认知:建立氧化还原反应的观点,掌握氧化还原反应的规律,结合常见的氧化还原反
应理解有关规律;通过分析、推理等方法认识氧化还原反应的特征和实质,建立氧化还原反应计算和配平
的思维模型。
科学探究与创新意识:认识科学探究是进行科学解释和发现。创造和应用的科学实践活动;能从氧化
还原反应的角度,设计探究方案,进行实验探究,加深对物质氧化性、还原性的理解。
【必备知识解读】
一、氧化还原反应
1.氧化还原反应的本质和特征
(1)氧化还原反应的本质是电子转移;
(2)氧化还原反应的特征反应过程中有化合价的变化。
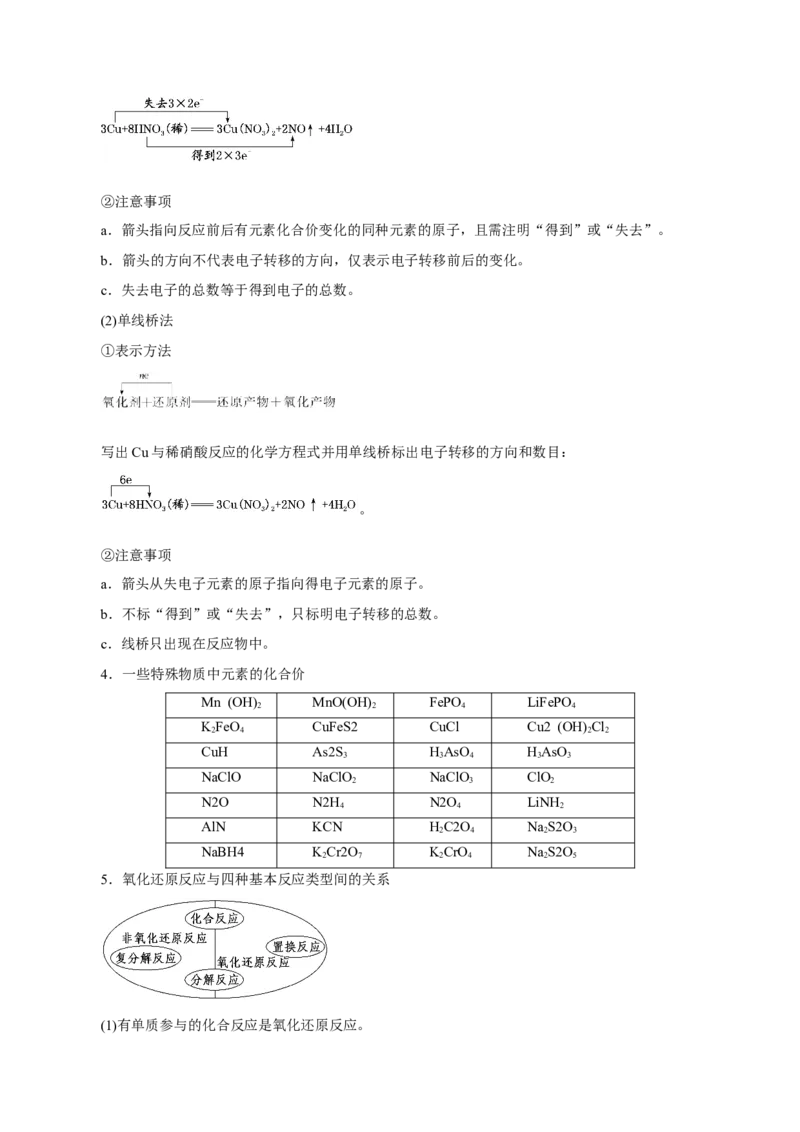
2.氧化还原反应的相关概念及其关系
例如,反应MnO +4HCl(浓)=====MnCl +Cl↑+2HO中,氧化剂是MnO ,还原剂是HCl,氧化产
2 2 2 2 2
物是Cl。生成1 mol Cl 时转移电子数目为2N ,被氧化的HCl的物质的量是2mol,盐酸表现的性质是酸
2 2 A
性和还原性。
【特别提醒】元素由化合态变为游离态时,该元素不一定被还原。如:Cu2+→Cu时,铜元素被还原,
Cl-→Cl 时,氯元素被氧化。
2
3.氧化还原反应中电子转移的表示方法
(1)双线桥法
①表示方法
写出Cu与稀硝酸反应的化学方程式并用双线桥标出电子转移的方向和数目:②注意事项
a.箭头指向反应前后有元素化合价变化的同种元素的原子,且需注明“得到”或“失去”。
b.箭头的方向不代表电子转移的方向,仅表示电子转移前后的变化。
c.失去电子的总数等于得到电子的总数。
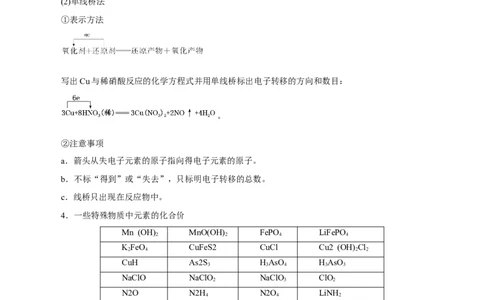
(2)单线桥法
①表示方法
写出Cu与稀硝酸反应的化学方程式并用单线桥标出电子转移的方向和数目:
。
②注意事项
a.箭头从失电子元素的原子指向得电子元素的原子。
b.不标“得到”或“失去”,只标明电子转移的总数。
c.线桥只出现在反应物中。
4.一些特殊物质中元素的化合价
Mn (OH) MnO(OH) FePO LiFePO
2 2 4 4
KFeO CuFeS2 CuCl Cu2 (OH) Cl
2 4 2 2
CuH As2S HAsO HAsO
3 3 4 3 3
NaClO NaClO NaClO ClO
2 3 2
N2O N2H N2O LiNH
4 4 2
AlN KCN HC2O NaS2O
2 4 2 3
NaBH4 KCr2O KCrO NaS2O
2 7 2 4 2 5
5.氧化还原反应与四种基本反应类型间的关系
(1)有单质参与的化合反应是氧化还原反应。(2)有单质生成的分解反应是氧化还原反应。
(3)有单质参加或生成的化学反应,不一定是氧化还原反应,如3O=====2O。
2 3
(4)所有的置换反应都是氧化还原反应。
(5)所有的复分解反应都不是氧化还原反应。
二、氧化剂与还原剂
1.常见氧化剂
常见氧化剂包括某些非金属单质、含有高价态元素的化合物、过氧化物等。如:
【特别提醒】
(1)O、O 在水溶液中的还原产物,其中酸性条件下是HO,中性、碱性条件下是OH-;而当还原
2 3 2
产物为固态时是O2-或O。
(2)浓硝酸的还原产物是NO ,稀HNO 的还原产物是NO。
2 3
2.常见还原剂
常见还原剂包括活泼的金属单质、非金属离子及低价态化合物、低价金属阳离子、非金属单质及其氢
化物等。如:
3.既可作氧化剂,又可作还原剂的物质或粒子
具有中间价态的物质或粒子既具有氧化性,又具有还原性,当遇到强还原剂反应时,作氧化剂,表现
氧化性;当遇到强氧化剂反应时,作还原剂,表现还原性。常考物质或粒子归纳如下:
【特别提醒】同一种氧化剂(或还原剂)所对应的还原产物(或氧化产物)不是一成不变的,而是决定于还原剂(或氧化剂)的性质、反应条件、反应物的浓度、反应介质的酸碱性等多种因素。如KMnO 在酸性溶液
4
中的还原产物一般是Mn2+;在中性或碱性溶液中的还原产物一般是锰的较高价态的化合物,如MnO 、
2
KMnO 等。
2 4
【归纳总结】
三、氧化性、还原性强弱的认识
1.氧化性指物质得电子的性质(或能力);还原性指物质失电子的性质(或能力)。
2.氧化性、还原性的强弱取决于物质得、失电子的难易程度,与得、失电子数目的多少无关。例如:
Na-e-===Na+,Al-3e-===Al3+,根据金属活动性顺序可知,Na比Al活泼,更易失去电子,所以Na比
Al的还原性强。
3.从元素的价态考虑:最高价态——只有氧化性,如 HSO 、KMnO 等;最低价态——只有还原性,
2 4 4
如金属单质、Cl-、S2-等;中间价态——既有氧化性,又有还原性,如Fe2+、S、Cl 等。
2
四、氧化还原反应方程式的书写与配平
1.氧化还原方程式配平的基本原则
2.氧化还原方程式配平的一般步骤以上方法步骤以Cu与稀HNO 反应的方程式配平为例说明如下:
3
(1)标变价
Cu+HNO(稀)——Cu (NO )+NO+HO
3 3 2 2
(2)列变化
Cu+HNO(稀)——Cu (NO )+NO+HO
3 3 2 2
(3)求总数
Cu+HNO(稀)——Cu (NO )+NO+HO
3 3 2 2
(4)定系数
3Cu+8HNO(稀)===3Cu(NO )+2NO↑+4HO
3 3 2 2
(5)查守恒,其他原子在配平时相等,最后利用O原子守恒来进行验证。
【方法技巧】配平的基本方法
(1)全变从左边配:氧化剂、还原剂中某元素化合价是全变的,一般从左边反应物着手配平。
(2)自变从右边配:自身氧化还原反应(包括分解、歧化)一般从右边着手配平。
(3)缺项配平法:先将得失电子数配平,再观察两边电荷。若反应物这边缺正电荷,一般加H+,生成
物一边加水;若反应物这边缺负电荷,一般加OH-,生成物一边加水,然后进行两边电荷数配平。
(4)当方程式中有多个缺项时,应根据化合价的变化找准氧化剂、还原剂、氧化产物、还原产物。
(5)整体配平:指某一氧化还原反应中,有三种元素的化合价发生了变化,但其中一种反应物中同时有
两种元素化合价升高或降低,这时要进行整体配平。
【关键能力拓展】
一、氧化性、还原性强弱的比较方法
物质氧化性(得电子的能力)、还原性(失电子的能力)的强弱取决于物质得失电子的难易,与得失电子的
数目无关,但也与外界因素(如反应条件、反应物浓度、酸碱性等)有关,具体判断方法如下:
1.依据氧化还原反应原理来判断
(1)氧化性强弱:氧化剂>氧化产物。
(2)还原性强弱:还原剂>还原产物。
2.依据“二表、一律”判断
(1)依据元素周期表判断
①同主族元素对应单质的氧化性从上到下逐渐减弱,对应阴离子的还原性逐渐增强。②同周期元素对应单质的还原性从左到右逐渐减弱,氧化性逐渐增强。
―――――――――――――――――――――――――→
(2)依据元素的活动性顺序表判断
(3)依据元素周期律判断
①非金属元素的最高价氧化物对应水化物的酸性越强,其对应单质的氧化性越强。
如酸性:HClO>H SO >H PO >H CO>H SiO,则氧化性:Cl>S>P>C>Si。
4 2 4 3 4 2 3 2 3 2
②金属元素的最高价氧化物对应水化物的碱性越强,其对应单质的还原性越强。
如碱性:NaOH>Mg(OH) >Al(OH) ,则还原性:Na>Mg>Al。
2 3
3.依据产物中元素价态的高低判断
(1)相同条件下,不同氧化剂作用于同一种还原剂,氧化产物价态高的其氧化性强。
例如:根据2Fe+3Cl=====2FeCl ,Fe+S=====FeS,可以推知氧化性:Cl>S。
2 3 2
(2)相同条件下,不同还原剂作用于同一种氧化剂,还原产物价态低的其还原性强。
例如:根据Cu+2Fe3+===Cu2++2Fe2+,3Zn+2Fe3+===3Zn2++2Fe,可以推知还原性:Zn>Cu。
4.依据电化学原理判断
(1)原电池:一般情况下,两种不同的金属构成原电池的两极,其还原性:负极>正极。
(2)电解池:用惰性电极电解混合溶液时,在阴极先放电的阳离子的氧化性较强,在阳极先放电的阴离
子的还原性较强。
5.依据影响因素判断
(1)浓度:同一种物质,浓度越大,氧化性(或还原性)越强。如氧化性:浓HSO >稀HSO ,浓HNO>
2 4 2 4 3
稀HNO;还原性:浓HCl>稀HCl。
3
(2)温度:同一种物质,温度越高其氧化性越强。如热的浓硫酸的氧化性比冷的浓硫酸的氧化性强。
(3)酸碱性:同一种物质,所处环境酸(碱)性越强其氧化(还原)性越强。如氧化性:KMnO (酸
4
性)>KMnO (中性)>KMnO (碱性)。
4 4
6.依据反应条件判断
同一种物质,浓度越大,氧化性(或还原性)越强。如氧化性:浓HSO >稀
浓度 2 4
HSO ,浓HNO>稀HNO;还原性:浓HCl>稀HCl
2 4 3 3同一种物质,温度越高其氧化性越强。如热的浓硫酸的氧化性比冷的浓硫酸的
温度
氧化性强
二、氧化还原反应概念的“五个误区”
误区一:某元素由化合态变为游离态时,该元素不一定被还原,也不一定被氧化。因为元素处于化合
态时,其化合价可能为正,也可能为负。若元素由负价变为0价,则其被氧化,若元素由正价变为0价,
则其被还原。
误区二:在氧化还原反应中,非金属单质不一定只作氧化剂,大部分非金属单质往往既具有氧化性又
具有还原性,只是以氧化性为主。如在反应Cl+HO HCl+HClO中,Cl 既表现氧化性又表现还原性。
2 2 2
误区三:物质的氧化性或还原性的强弱取决于元素原子得失电子的难易程度,与得失电子数目的多少
无关。
误区四:氧化还原反应中的反应物不一定都是氧化剂或还原剂,有的反应物可能既不是氧化剂也不是
还原剂。如Cl+HO HCl+HClO,HO既不是氧化剂,也不是还原剂。
2 2 2
误区五:在氧化还原反应中,一种元素被氧化,不一定有另一种元素被还原,也可能是同一元素既被
氧化又被还原。如:2NaO+2HO===4NaOH+O↑中,NaO 既是氧化剂又是还原剂,氧元素一部分化合
2 2 2 2 2 2
价升高,一部分化合价降低。
三、氧化还原反应的规律及其应用
(一)价态规律
1.升降规律
氧化还原反应中,化合价有升必有降,升降总值相等。
2.价态归中规律
含不同价态的同种元素的物质间发生氧化还原反应时,该元素价态的变化一定遵循“高价+低价―→
中间价”,而不会出现交叉现象。简记为“两相靠,不相交”。
3.歧化反应规律
“中间价―→高价+低价”。具有多种价态的元素(如氯、硫、氮和磷元素等)均可发生歧化反应。
例如:Cl+2NaOH===NaCl+NaClO+HO。
2 2
(二)强弱规律
1.根据氧化性和还原性规律判断
同一个反应中,氧化剂的氧化性强(填“强”或“弱”)于氧化产物的氧化性,还原剂的还原性强于还
原产物的还原性。如反应2FeCl +2KI===2FeCl +I+2KCl中,氧化性:Fe3+>I ;还原性:I->Fe2+。
3 2 2 2
2.根据金属活动性或非金属活动性顺序判断
K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag,由左至右,单质的还原性逐渐减弱;K+、Ca2+、Na+、Mg2+、Al3+、Zn2+、Fe2+、Sn2+、Pb2+、(H+)、Cu2+、Hg2+、Ag+,由左至右,阳离子的
氧化性逐渐增强;F 、Cl 、Br 、I 、S,由左至右,单质的氧化性逐渐减弱;F-、Cl-、Br-、I-、S2-,由
2 2 2 2
左至右,阴离子的还原性逐渐增强。
3.根据产物中元素价态的高低判断
如2Fe+3Cl=====2FeCl ,Fe+S=====FeS,则氧化性:Cl>(填“>”或“<”)S。
2 3 2
(三)先后规律
(1)同时含有几种还原剂时将按照还原性由强到弱的顺序依次反应。如:在 FeBr 溶液中通入少量Cl 时,
2 2
因为还原性:Fe2+>Br-,所以Fe2+先与Cl 反应。
2
(2)同时含有几种氧化剂时将按照氧化性由强到弱的顺序依次反应。如:在含有Fe3+、Cu2+、H+的溶
液中加入铁粉,因为氧化性:Fe3+>Cu2+>H+,所以铁粉先与Fe3+反应,然后再依次与Cu2+、H+反应。
(四)守恒规律
氧化还原反应中,氧化剂得电子总数等于还原剂失电子总数。
四、电子守恒思想在氧化还原反应计算中的应用
1.对于氧化还原反应的计算,要根据氧化还原反应的实质——反应中氧化剂得到的电子总数与还原
剂失去的电子总数相等,即得失电子守恒。利用守恒思想,可以抛开繁琐的反应过程,可不写化学方程式,
不追究中间反应过程,只要把物质分为始态和终态,从得电子与失电子两个方面进行整体思维,便可迅速
获得正确结果。
2.守恒法解题的思维流程
(1)找出氧化剂、还原剂及相应的还原产物和氧化产物。
(2)找准一个原子或离子得失电子数(注意化学式中粒子的个数)。
(3)根据题中物质的物质的量和得失电子守恒列出等式。
n(氧化剂)×变价原子个数×化合价变化值(高价-低价)=n(还原剂)×变价原子个数×化合价变化值(高价
-低价)。
3.氧化还原反应计算的常用方法——得失电子守恒法
得失电子守恒是指在发生氧化还原反应时,氧化剂得到的电子总数一定等于还原剂失去的电子总数。
得失电子守恒法常用于氧化还原反应中氧化剂、还原剂、氧化产物、还原产物的有关计算及电解过程中电
极产物的有关计算等。
(1)应用电子守恒解题的一般步骤——“一、二、三”。
①“一找各物质”:找出氧化剂、还原剂及相应的还原产物和氧化产物。
②“二定得失数”:确定一个原子或离子得失电子数(注意化学式中原子的个数)。
③“三列关系式”:根据题中物质的物质的量和电子守恒列出等式。n(氧化剂)×变价原子个数×化合价变化值=n(还原剂)×变价原子个数×化合价变化值。
(2)多步连续进行的氧化还原反应的有关计算:对于多步连续进行的氧化还原反应,只要中间各步反应
过程中电子没有损耗,可直接找出起始物和最终产物,删去中间产物,建立二者之间的电子守恒关系,快
速求解。应用以上方法解答有关氧化还原反应的计算题时,可化难为易,化繁为简。
【核心题型例解】
高频考点一 氧化还原反应与非氧化还原反应
例1.(2023·全国乙卷)下列应用中涉及到氧化还原反应的是
A. 使用明矾对水进行净化 B. 雪天道路上撒盐融雪
C. 暖贴中的铁粉遇空气放热 D. 荧光指示牌被照发光
【答案】C
【解析】使用明矾对水进行净化过程中,明矾电离出的铝离子发生水解生成氢氧化铝胶体,氢氧化铝
胶体粒子吸附水中的悬浮颗粒并沉降下来而水变得澄清,该过程中没有任何一种元素的化合价发生变化,
因此没有涉及到氧化还原反应,A不符合题意;雪天道路上撒盐融雪,是因为雪遇到盐而使其熔点降低并
熔化,该过程中没有任何一种元素的化合价发生变化,因此没有涉及到氧化还原反应,B不符合题意;暖
贴中的铁粉遇空气放热,是因为暖贴中含有的铁粉、碳粉、氯化钠、水等物质,形成当这些物质遇到空气
后形成无数微小原电池并开始工作,化学能转化为电能,无数微小原电池堆积在一起使得电能又转化为热
能,该过程中铁元素和氧元素的化合价发生变化,因此,该过程涉及到氧化还原反应,C符合题意;荧光
指示牌被照发光,是因为光被指示牌发生了反射,该过程中没有任何一种元素的化合价发生变化,因此没
有涉及到氧化还原反应,D不符合题意;故选C。
【变式探究】许多古迹是人类宝贵的文化遗产。下列古迹在传承过程中遇到的问题属于化学变化且未
发生氧化还原反应的是
A.石质阶梯被游客踩 B.大理石雕像被 C.铜质雕像逐渐 D.木质中轴塔在
踏磨损 酸雨腐蚀 变为绿色 火灾中坍塌
【答案】B
【解析】石质阶梯被游客磨损,没有生成新的物质,是物理变化,A错误;石质雕像主要成分为碳酸
盐,被酸雨腐蚀,生成新物质,属于化学变化,但不是氧化还原反应,B正确;铜质雕像逐渐变为绿色,
铜单质变为碱式碳酸铜,生成新物质,属于氧化还原反应,C错误;在火灾中发生燃烧而坍塌,燃烧属于氧化还原反应,D错误;故选B。
【举一反三】下列应用不涉及物质氧化性或还原性的是( )
A.用葡萄糖制镜或保温瓶胆
B.铜铸塑像上出现铜绿[Cu (OH) CO]
2 2 3
C.用NaSiO 溶液制备木材防火剂
2 3
D.用浸泡过高锰酸钾溶液的硅藻土保鲜水果
【答案】C
【解析】葡萄糖与银氨溶液发生氧化还原反应,生成银单质,葡萄糖作还原剂被氧化,故A不选;高
锰酸钾可氧化具有催熟作用的乙烯,从而达到保鲜水果的目的,故D不选。
高频考点二 氧化还原反应规律
例2.已知I-、Fe2+、SO 、Cl-和HO 均有还原性,它们在酸性溶液中还原性的强弱顺序为
2 2 2
Cl-<Fe2+<HO<I-<SO ,则下列反应不能发生的是( )
2 2 2
A.2Fe3++SO +2HO===2Fe2++SO+4H+
2 2
B.I+SO +2HO===H SO +2HI
2 2 2 2 4
C.HO+HSO ===SO↑+O↑+2HO
2 2 2 4 2 2 2
D.2Fe2++Cl===2Fe3++2Cl-
2
【答案】C
【解析】A项,还原性:SO >Fe2+,反应能发生;B项,还原性:SO >I-,反应能发生;C项,还
2 2
原性:HO<SO ,反应不能发生。
2 2 2
【变式探究】氯气跟氢氧化钾溶液在一定条件下发生如下反应:Cl+KOH―→KX+KY+HO(未配
2 2
平),KX在一定条件下能自身反应:KX―→KY+KZ(未配平,KY与KZ的物质的量之比为1∶3),以上
KX、KY、KZ均是含氯元素的一元酸的钾盐,由以上条件推知在KX中氯元素的化合价是( )
A.+1 B.+3 C.+5 D.+7
【答案】C
【解析】反应:Cl+KOH―→KX+KY+HO是Cl 的歧化反应,KX、KY中的氯元素分别显正价和
2 2 2
-1价;由于KX也发生歧化反应:KX―→KY+KZ,可断定KY为KCl,化合价高低:KZ中Cl>KX中
Cl(均为正价)。假设KX中Cl元素为+a价,KZ中Cl元素的化合价为+b价,依据得失电子守恒原理及
KX―→KY+3KZ,有a+1=3(b-a),把a=1、a=3、a=5代入上式讨论,可知a=5时,b=7符合题意。
则KX中Cl元素的化合价为+5。
高频考点三 氧化还原反应的配平
例3.一定条件下,硝酸铵受热分解的化学方程式(未配平)为NH NO ―→HNO+N↑+HO,下列说
4 3 3 2 2法错误的是( )
A.配平后HO的化学计量数为6
2
B.NH NO 既是氧化剂又是还原剂
4 3
C.该反应既是分解反应也是氧化还原反应
D.氧化产物和还原产物的物质的量之比为5∶3
【答案】A
【解析】由配平后的化学方程式可知,HO的化学计量数为9,A错误;NH NO 中NH所含N元素价
2 4 3
态升高,部分NO所含N元素价态降低,则NH NO 既是氧化剂又是还原剂,B正确;该反应中反应物只
4 3
有一种,则属于分解反应,该反应中含有变价元素,则属于氧化还原反应,C正确;氧化产物(5NH→N)
2
和还原产物(3NO→N)的物质的量之比为∶=5∶3,D正确。
2
【变式探究】已知离子方程式:As S+HO+NO―→AsO+SO+NO↑+________(未配平),下列说法
2 3 2
错误的是( )
A.配平后水的化学计量数为4
B.反应后的溶液呈酸性
C.配平后氧化剂与还原剂的分子数之比为3∶28
D.氧化产物为AsO和SO
【答案】C
【解析】As S 转化成AsO和SO,而NO转化为NO,根据得失电子守恒、原子守恒和电荷守恒,配
2 3
平后的离子方程式为3As S+4HO+28NO===6AsO+9SO+28NO↑+8H+,水的化学计量数为4,A正确;
2 3 2
反应产生H+,反应后的溶液呈酸性,B正确;N元素化合价降低,NO作氧化剂,As和S元素化合价升高,
As S 作还原剂,由上述离子方程式知,氧化剂与还原剂的分子数之比为28∶3,C错误;As S 作还原剂,
2 3 2 3
氧化产物为AsO和SO,D正确。
高频考点四 氧化还原反应的相关计算
的
例4.(2023·浙江选考)关于反应 ,下列说法正确 是( )
A. 生成1molN O,转移4mol电子 B. NH OH是还原产物
2 2
C. NH OH既是氧化剂又是还原剂 D. 若设计成原电池,Fe2+为负极产物
2
【答案】A
【解析】由方程式可知,反应生成1molN O,转移4mol电子,故A正确;由方程式可知,反应中氮
2
元素的化合价升高被氧化,NH OH是反应的还原剂,故B错误;由方程式可知,反应中氮元素的化合价升
2
高被氧化,NH OH是反应的还原剂,铁元素的化合价降低被还原,铁离子是反应的氧化剂,故C错误;由
2方程式可知,反应中铁元素的化合价降低被还原,铁离子是反应的氧化剂,若设计成原电池,Fe3+在正极
得到电子发生还原反应生成亚铁离子,Fe2+为正极产物,故D错误;故选A。
【方法技巧】守恒法解题的思维流程
(1)一找各物质:找出氧化剂、还原剂及相应的还原产物和氧化产物。
(2)二定得失数:确定一个原子或离子得失电子数(注意化学式中的原子个数)。
(3)三列关系式:根据题中物质的物质的量和得失电子守恒列出关系式。
n(氧化剂)×变价原子个数×化合价变化值=n(还原剂)×变价原子个数×化合价变化值。
【变式探究】在一定条件下,PbO 与Cr3+反应,产物是Pb2+和Cr O,则与1 mol Cr3+反应所需PbO
2 2 2
的物质的量为( )
A.3.0 mol B.1.5 mol
C.1.0 mol D.0.75 mol
【答案】B
【解析】1 mol Cr3+反应可生成0.5 mol Cr O,失去3 mol电子,1 mol PbO 得到2 mol电子生成Pb2+,
2 2
根据得失电子守恒可知,1 mol Cr3+反应失去3 mol电子需1.5 mol PbO 。
2
【举一反三】有关反应14CuSO +5FeS+12HO===7Cu S+5FeSO +12HSO 的下列说法中错误的是(
4 2 2 2 4 2 4
)
A.FeS 既是氧化剂也是还原剂
2
B.CuSO 在反应中被还原
4
C.被还原的S和被氧化的S的质量之比为3∶7
D.14 mol CuSO 氧化了1 mol FeS
4 2
【答案】C
【解析】方程式中的化合价变化为:14个CuSO 中+2价的铜得电子化合价降低为7个Cu S中的14
4 2
个+1价的Cu;5个FeS 中10个-1价的S有7个化合价降低得到7个Cu S中-2价的S,有3个化合价
2 2
升高得到3个SO中+6价的S(生成物中有17个硫酸根离子,其中有14个来自反应物中的硫酸铜)。所以
反应中FeS 中S的化合价有升高有降低,FeS 既是氧化剂又是还原剂,选项A正确;硫酸铜中Cu的化合
2 2
价都降低,所以硫酸铜只是氧化剂,选项B正确;10个-1价的S有7个化合价降低,有3个化合价升高,
所以被还原的S和被氧化的S的质量之比为7∶3,选项C错误;14 mol CuSO 在反应中得电子的物质的量为
4
14 mol。FeS 被氧化时,应该是-1价的S被氧化为+6价,所以1个FeS 会失去14个电子。根据得失电
2 2
子守恒,14 mol CuSO 氧化了1 mol FeS ,选项D正确。
4 2
高频考点五 氧化还原反应的应用例5.取x g铜镁合金完全溶于浓硝酸中,反应过程中硝酸被还原只产生8 960 mL的NO 气体和672
2
mL的NO 气体(都已折算到标准状况),在反应后的溶液中加入足量的氢氧化钠溶液,生成沉淀质量为
2 4
17.02 g。则x等于( )
A.8.64 B.9.20
C.9.00 D.9.44
【答案】B
【解析】反应流程为
――→
x g=17.02 g-m(OH-),而OH-的物质的量等于镁、铜失去电子的物质的量,等于浓HNO 得电子的
3
物质的量,即n(OH-)=×1+×2×1=0.46 mol,所以x g=17.02 g-0.46 mol×17 g·mol-1=9.20 g。
【变式探究】足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO 、NO、NO的混合气体,将这些
2 2 4
气体与1.68 L O (标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加
2
入5 mol·L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
A.60 mL B.45 mL
C.30 mL D.15 mL
【答案】A
【解析】由题意可知,HNO------→,则Cu失去的电子数与O 得到的电子数相等。即n(Cu)=2n(O )
3 2 2
=2×=0.15 mol。根据质量守恒及NaOH和Cu(NO ) 的反应可得关系式:n(NaOH)=2n[Cu(NO )]=2n(Cu)
3 2 3 2
=0.3 mol,则V[NaOH(aq)]==0.06 L=60 mL。
高频考点六 氧化还原滴定中的计算
例6.某废水中含有Cr O,为了处理有毒的Cr O,需要先测定其浓度:取20 mL废水,加入适量稀硫
2 2
酸,再加入过量的V mL c mol·L-1 (NH )Fe(SO ) 溶液,充分反应(还原产物为Cr3+)。用c mol ·L-1
1 1 4 2 4 2 2
KMnO 溶液滴定过量的Fe2+至终点,消耗KMnO 溶液V mL。则原废水中c(CrO)为________________。
4 4 2 2
【答案】 mol·L-1
【解析】Cr O+6Fe2++14H+===2Cr3++6Fe3++7HO,5Fe2++MnO+8H+===5Fe3++Mn2++4HO。利
2 2 2
用得失电子守恒列等式:c mol·L-1×V mL×10-3 L ·mL-1=20 mL×10-3 L·mL-1×6c(CrO)+5c mol·L-1×V
1 1 2 2 2
mL×10-3 L·mL-1,解得:c(CrO)= mol·L-1。
2
【变式探究】亚硫酰氯(SOCl ,熔点-104.5℃,沸点76-78℃,易水解生成SO 和HCl)是一种重要的化
2 2
学试剂,广泛用于有机合成。制备亚硫酰氯的两种方法:
方法1:以五氯化磷和二氧化硫为原料,发生反应:SO + PCl = SOCl +POCl
2 5 2 3方法2:以三氧化硫和二氯化硫为原料。
(1)方法1反应的过程中是否存在电子转移_______?
(2)写出方法2的化学方程式_______。
(3)某科研小组测定亚硫酰氯产品的纯度。步骤如下:
步骤一、用分析天平准确称取 样品,小心地将样品溶于 的氢氧化钠溶液中,充
分反应后,配成 500ml试样溶液。
步骤二、用移液管吸取 50ml试样溶液于 250ml碘量瓶中,加入两滴对硝基苯酚指示剂,滴加
盐酸至黄色刚好消失,加入 碘标准溶液,避光放置 。
步骤三、用 标准溶液返滴定过量的I,近终点时加入淀粉溶液,继续滴定至终
2
点,消耗标准溶液 。
①指出步骤一中“配成 500ml试样溶液”所必需的定量玻璃仪器的名称_______。
②指出步骤二中滴加盐酸的目的_______。
③叙述步骤三中滴定终点的现象_______。
④计算样品的纯度(用含有V的代数式表示) _______。
【答案】(1)否 (2) SO + SCl = SOCl +SO
3 2 2 2
(3) 500ml容量瓶 中和过量的NaOH,防止I 在碱性条件下歧化 滴入最后一滴NaSO 标准
2 2 2 3
溶液,锥形瓶中的溶液由蓝色变为无色,且半分钟内不恢复
【解析】(1)由方程式可知,方法1发生的反应中没有元素发生化合价变化,不存在电子转移,故答
案为:否;
(2)由题意可知,方法2发生的反应为三氧化硫和二氯化硫反应生成亚硫酰氯和二氧化硫,反应的化
学方程式为SO + SCl = SOCl +SO ;
3 2 2 2
(3)①由配制一定物质的量浓度溶液配制的步骤为计算、称量、溶解、移液、洗涤、定容、摇匀、
装瓶可知,步骤一中“配成500mL试样溶液”所必需的定量玻璃仪器为500mL容量瓶;
②由题意可知,步骤二中滴加盐酸的目的是中和过量的氢氧化钠溶液,防止加入的碘溶液与氢氧化钠
溶液发生歧化反应,使得滴定时消耗硫代硫酸钠溶液的体积偏小,导致所测样品的纯度偏大;
③当步骤三中碘溶液与NaSO 溶液恰好反应时,滴入最后一滴NaSO 溶液,溶液由蓝色变为无色,
2 2 3 2 2 3
且半分钟内不恢复说明滴定达到滴定终点;
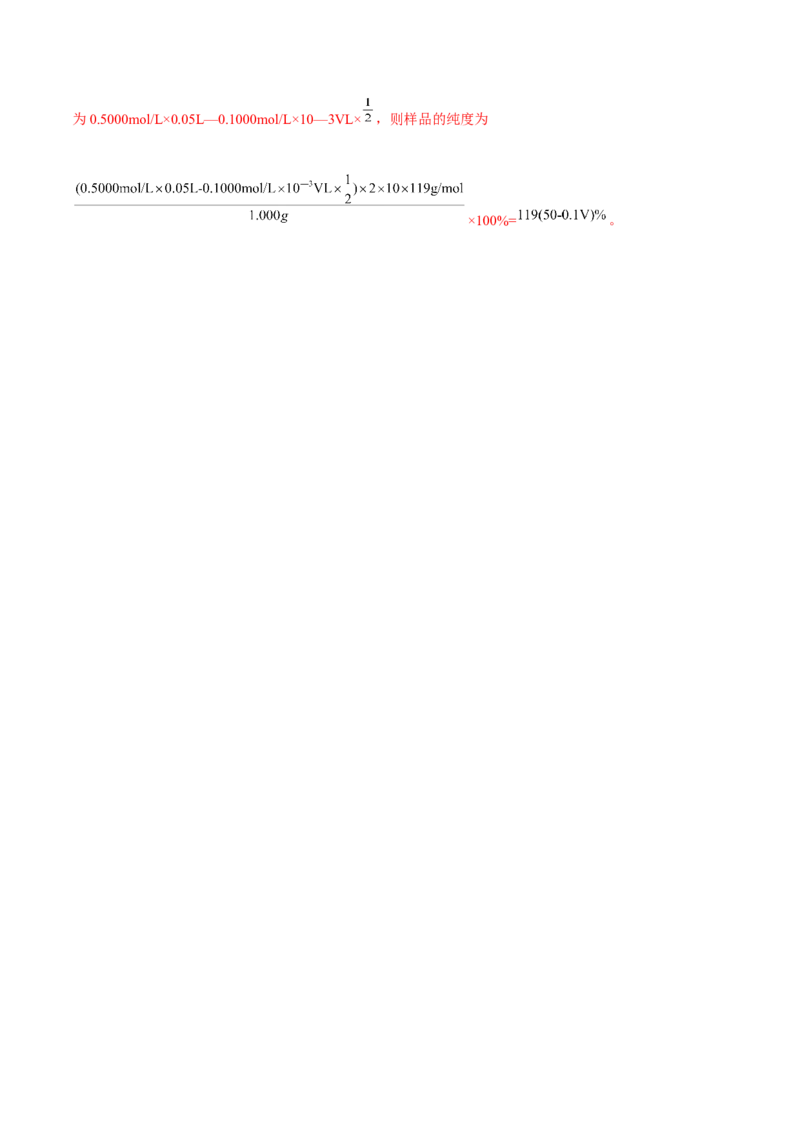
④由滴定消耗VmL 0.1000mol/L硫代硫酸钠溶液可知,与亚硫酰氯反应的碘的物质的量为0.5000mol/L×0.05L—0.1000mol/L×10—3VL× ,则样品的纯度为
×100%= 。