文档内容
第一章 有机化合物的结构特点与研究方法
第一节 有机化合物的结构特点
第 2 课时 有机化合物中的共价键和同分异构现象
学习导航 1.了解有机化合物中共价键的类型,理解键的极性与有机反应的关系。
2.理解有机化合物的同分异构现象,学会同分异构体的书写方法,能判断有机物的同分异构
体。
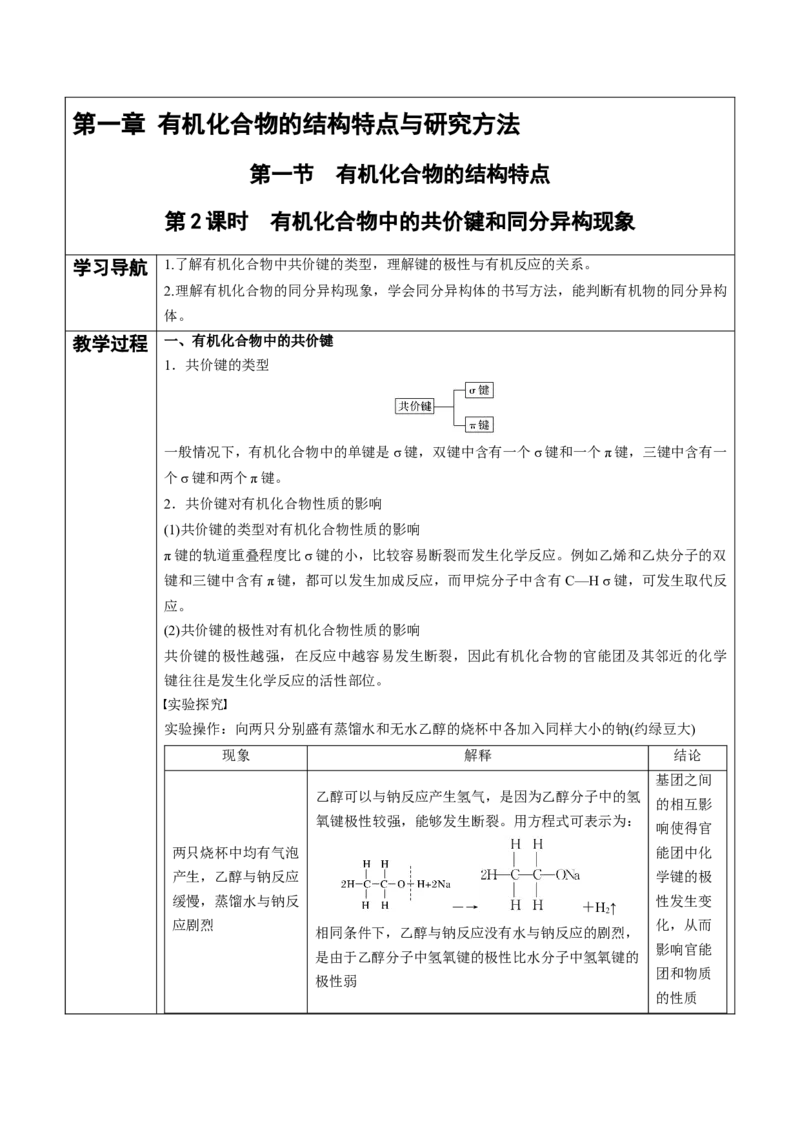
教学过程 一、有机化合物中的共价键
1.共价键的类型
一般情况下,有机化合物中的单键是σ键,双键中含有一个σ键和一个π键,三键中含有一
个σ键和两个π键。
2.共价键对有机化合物性质的影响
(1)共价键的类型对有机化合物性质的影响
π键的轨道重叠程度比σ键的小,比较容易断裂而发生化学反应。例如乙烯和乙炔分子的双
键和三键中含有π键,都可以发生加成反应,而甲烷分子中含有C—H σ键,可发生取代反
应。
(2)共价键的极性对有机化合物性质的影响
共价键的极性越强,在反应中越容易发生断裂,因此有机化合物的官能团及其邻近的化学
键往往是发生化学反应的活性部位。
实验探究
实验操作:向两只分别盛有蒸馏水和无水乙醇的烧杯中各加入同样大小的钠(约绿豆大)
现象 解释 结论
基团之间
乙醇可以与钠反应产生氢气,是因为乙醇分子中的氢
的相互影
氧键极性较强,能够发生断裂。用方程式可表示为:
响使得官
两只烧杯中均有气泡 能团中化
产生,乙醇与钠反应 学键的极
缓慢,蒸馏水与钠反 性发生变
―→ +H↑
2
应剧烈 化,从而
相同条件下,乙醇与钠反应没有水与钠反应的剧烈,
影响官能
是由于乙醇分子中氢氧键的极性比水分子中氢氧键的
团和物质
极性弱
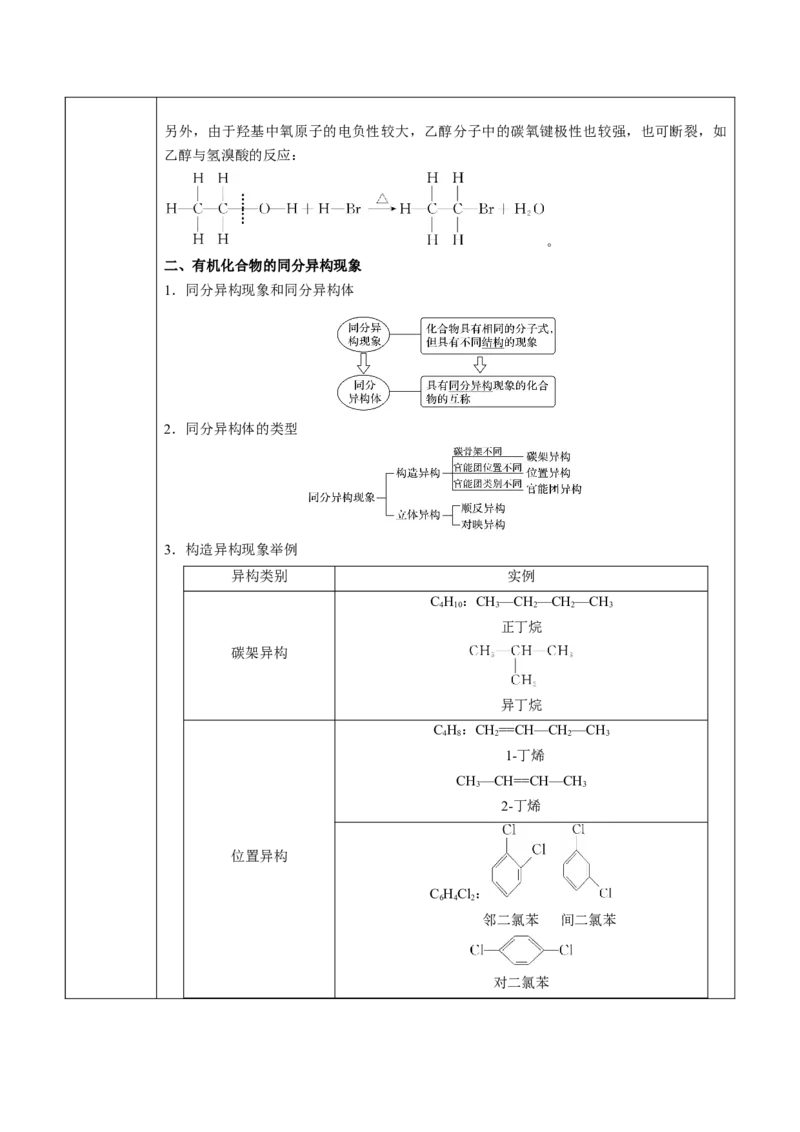
的性质另外,由于羟基中氧原子的电负性较大,乙醇分子中的碳氧键极性也较强,也可断裂,如
乙醇与氢溴酸的反应:
。
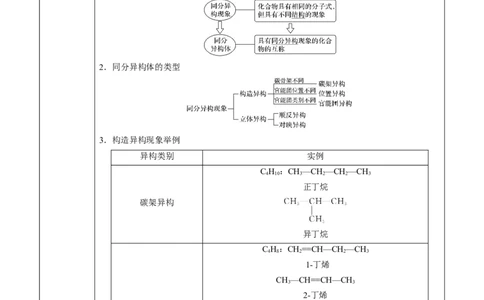
二、有机化合物的同分异构现象
1.同分异构现象和同分异构体
2.同分异构体的类型
3.构造异构现象举例
异构类别 实例
C H :CH—CH—CH—CH
4 10 3 2 2 3
正丁烷
碳架异构
异丁烷
C H:CH==CH—CH—CH
4 8 2 2 3
1-丁烯
CH—CH==CH—CH
3 3
2-丁烯
位置异构
C HCl:
6 4 2
邻二氯苯 间二氯苯
对二氯苯官能团异构
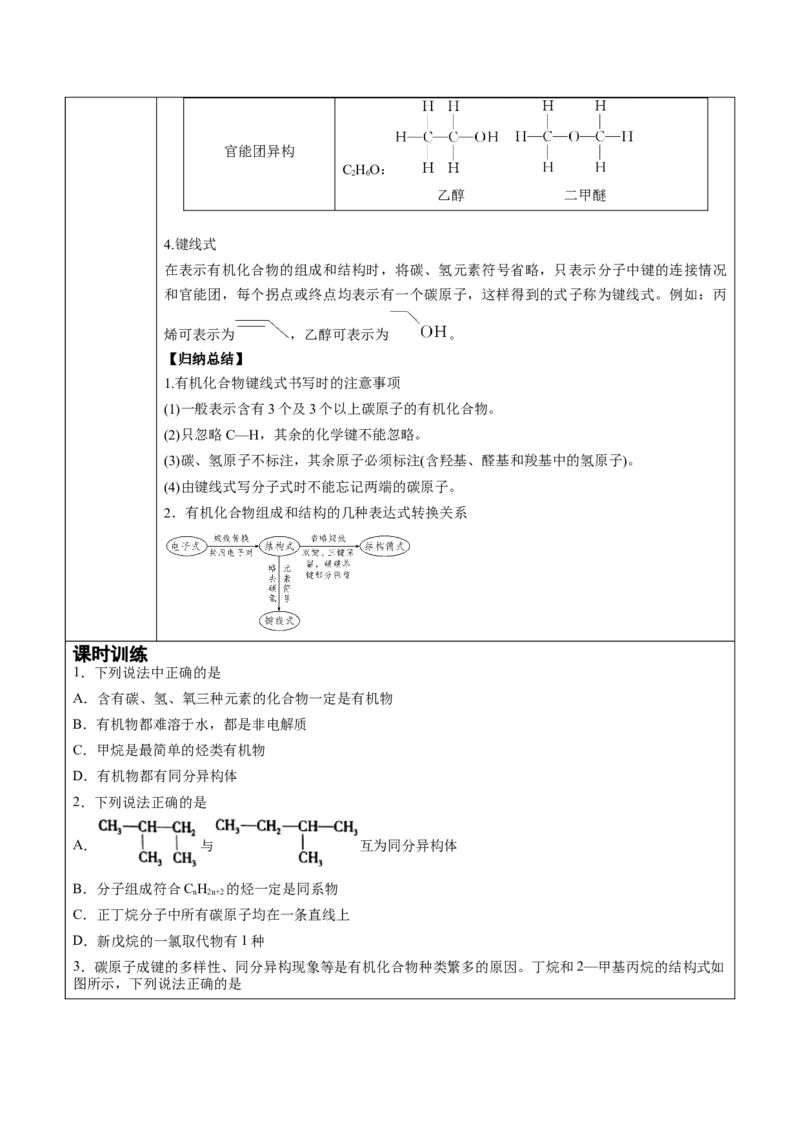
C HO:
2 6
乙醇 二甲醚
4.键线式
在表示有机化合物的组成和结构时,将碳、氢元素符号省略,只表示分子中键的连接情况
和官能团,每个拐点或终点均表示有一个碳原子,这样得到的式子称为键线式。例如:丙
烯可表示为 ,乙醇可表示为 。
【归纳总结】
1.有机化合物键线式书写时的注意事项
(1)一般表示含有3个及3个以上碳原子的有机化合物。
(2)只忽略C—H,其余的化学键不能忽略。
(3)碳、氢原子不标注,其余原子必须标注(含羟基、醛基和羧基中的氢原子)。
(4)由键线式写分子式时不能忘记两端的碳原子。
2.有机化合物组成和结构的几种表达式转换关系
课时训练
1.下列说法中正确的是
A.含有碳、氢、氧三种元素的化合物一定是有机物
B.有机物都难溶于水,都是非电解质
C.甲烷是最简单的烃类有机物
D.有机物都有同分异构体
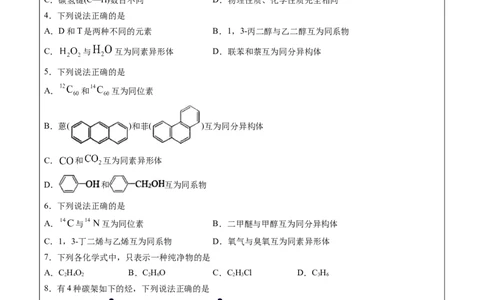
2.下列说法正确的是
A. 与 互为同分异构体
B.分子组成符合C H 的烃一定是同系物
n 2n+2
C.正丁烷分子中所有碳原子均在一条直线上
D.新戊烷的一氯取代物有1种
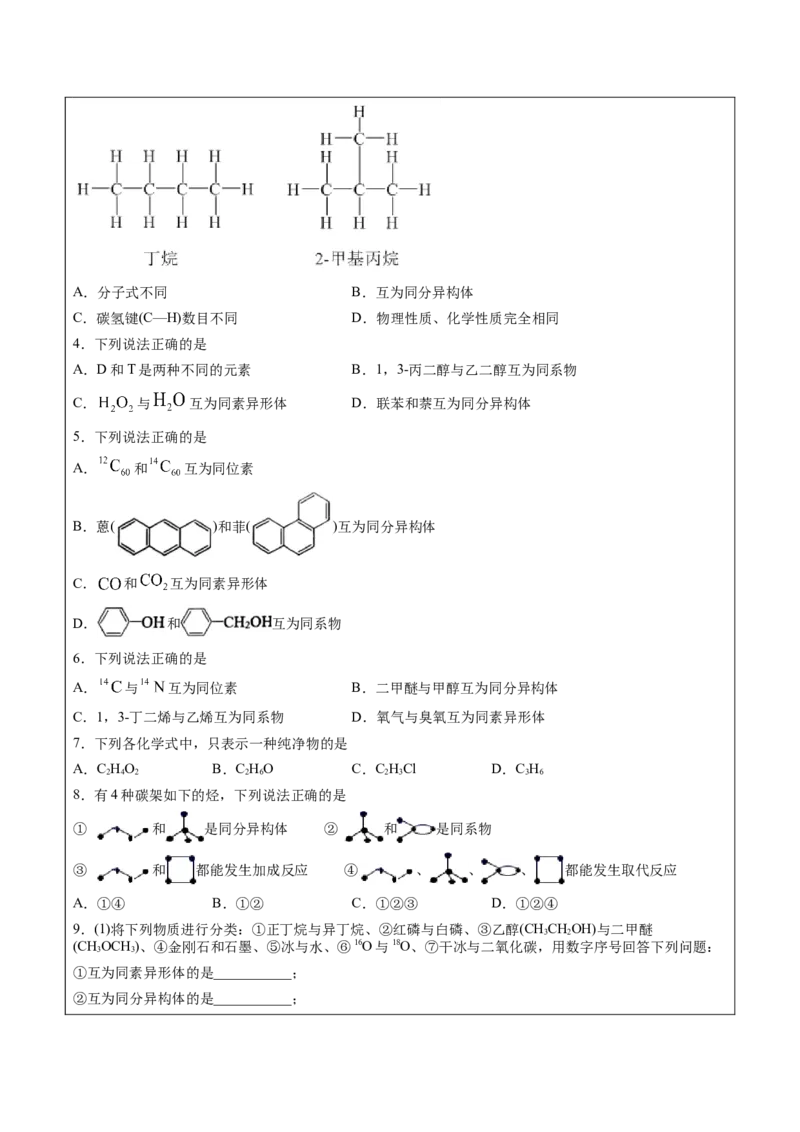
3.碳原子成键的多样性、同分异构现象等是有机化合物种类繁多的原因。丁烷和2—甲基丙烷的结构式如
图所示,下列说法正确的是A.分子式不同 B.互为同分异构体
C.碳氢键(C—H)数目不同 D.物理性质、化学性质完全相同
4.下列说法正确的是
A.D和T是两种不同的元素 B.1,3-丙二醇与乙二醇互为同系物
C. 与 互为同素异形体 D.联苯和萘互为同分异构体
5.下列说法正确的是
A. 和 互为同位素
B.蒽( )和菲( )互为同分异构体
C. 和 互为同素异形体
D. 和 互为同系物
6.下列说法正确的是
A. 与 互为同位素 B.二甲醚与甲醇互为同分异构体
C.1,3-丁二烯与乙烯互为同系物 D.氧气与臭氧互为同素异形体
7.下列各化学式中,只表示一种纯净物的是
A.C HO B.C HO C.C HCl D.C H
2 4 2 2 6 2 3 3 6
8.有4种碳架如下的烃,下列说法正确的是
① 和 是同分异构体 ② 和 是同系物
③ 和 都能发生加成反应 ④ 、 、 、 都能发生取代反应
A.①④ B.①② C.①②③ D.①②④
9.(1)将下列物质进行分类:①正丁烷与异丁烷、②红磷与白磷、③乙醇(CHCHOH)与二甲醚
3 2
(CHOCH )、④金刚石和石墨、⑤冰与水、⑥16O与18O、⑦干冰与二氧化碳,用数字序号回答下列问题:
3 3
①互为同素异形体的是___________;
②互为同分异构体的是___________;③属于同位素的是___________;
④属于同一种化合物的是___________;
(2)乙醇(CHCHOH)在铜作催化剂时与氧气反应的方程式___________。
3 2
(3)铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中,如图所示,则铁被腐蚀的速率由慢到快的顺序是___________(填
序号)。
10.(1)根据要求回答下列问题:
① H 、D、T;②白磷与红磷;③ Cl 与 Cl;④液氯与氯水;⑤ 与 ⑥
2 2 2
和 ⑦C H 和C H ⑧ 和 ,在上述各组
3 8 8 18
物质中:
互为同位素的是_______;互为同素异形体的是 _______;互为同分异构体的是_______;属于同系物的是
_______。(填序号)
(2)有机物A 0.02 mol 在氧气中完全燃烧生成4.4g CO 和2.16g HO,无其它物质生成。下列说法中正确的
2 2
是_______( 填序号 )
A.该化合物肯定含O元素 B.该化合物可能不含O元素
C.该化合物常温下可能为气体 D.该分子中C:H的个数比为5:6
若A为烃,此烃可能的结构简式为:_______。
答案解析
1.C
【详解】
A.含有碳、氢、氧三种元素的化合物不一定是有机物,如HCO 是无机物,故A错误;
2 3
B.某些有机物(如乙酸)易溶于水,其水溶液能导电,乙酸是电解质,故B错误;
C.甲烷是最简单的烷烃,也是最简单的烃类有机物,故C正确;
D.有机物如甲烷无同分异构体,故D错误;
故选C。
2.D
【详解】
A. 与 分子式、结构均相同,为同一种物质,A错误;
B.分子组成符合C H 的烃不一定是同系物,也可能是同分异构体,B错误;
n 2n+2
C.根据甲烷中4个C-H键的空间位置关系可知正丁烷分子中所有碳原子不可能在同一条直线上,应呈锯齿状,C错误;
D.新戊烷只有如图所述一种氢原子 ,一氯代物只有一种,D正确;
故答案为D。
3.B
【详解】
A.丁烷和2-甲基丙烷分子式相同,故A错误;
B.丁烷和2-甲基丙烷分子式相同,结构不同,为同分异构体,故B正确;
C.丁烷和2-甲基丙烷中氢原子数相同,碳氢键(C-H)数目相同,故C错误;
D.丁烷和2-甲基丙烷分子式相同,结构不同,物理性质不同、化学性质相似,故D错误;
答案选B。
4.B
【详解】
A.D和T是氢元素的两种核素,不是两种不同的元素,故A错误;
B. 1,3-丙二醇与乙二醇结构相似,在组成上相差一个CH,则两者互为同系物,故B正确;
2
C. 与 是相同元素组成的化合物,同素异形体是相同元素组成的单质,故C错误;
D.联苯的结构简式 ,分子式是C H ,萘的结构简式 ,分子式是C H,则二者
12 10 10 8
不是同分异构体,故D错误;
本题答案B。
5.B
【详解】
A. 和 由碳的不同同位素组成的单质,两者互为同位素,故A错误;
B.蒽( )和菲( )分子式都是C H 、结构不同,互为同分异构体,故B正确;
14 10
C. 和 是碳、氧两种元素组成的不同化合物,故C错误;
D. 属于酚类, 属于醇类,不是同系物,故D错误;
选B。
6.D
【详解】
A. 与 两种核素质子数不同,不是互为同位素,是两种不同元素的核素,故A错误;B. 二甲醚与甲醇分子式不同,分别为C HO和CHO,不是互为同分异构体,故B错误;
2 6 4
C. 1,3-丁二烯中有两个碳碳双键,乙烯中只有1个碳碳双键,不是互为同系物,故C错误;
D. 氧气与臭氧是由氧元素组成的两种不同的单质,互为同素异形体,故D正确;
故选D。
7.C
【详解】
A.C HO 存在同分异构体:CHCOOH、HCOOCH ,所以C HO 不能只表示一种物质,A错误;
2 4 2 3 3 2 4 2
B.C HO存在同分异构体,可以是CHCHOH或CHOCH ,所以C HO不能只表示一种物质,B错误;
2 6 3 2 3 3 2 6
C.C HCl只有1种结构:CH=CHCl,所以C HCl只表示一种物质,C正确;
2 3 2 2 3
D.C H 存在同分异构体:丙烯或环丙烷,所以C H 不能只表示一种物质,D错误;
3 6 3 6
答案为C
8.A
【详解】
①左边是CHCHCHCH,右边是(CH)CHCH ,两者是因碳链不同而形成的同分异构体,正确;
3 2 2 3 3 2 3
②左边是新戊烷,分子式是C H ,右边是异丁烯,分子式为C H,分子组成没有相差至少一个CH,所
5 12 4 8 2
以不是同系物,错误;
③两者均不存在不饱和键,如双键,均不可以发生加成反应,错误;
④形成四个单键的饱和碳原子上的碳氢键可以发生类似甲烷在光照下与氯气的取代反应,分析这四者的结
构,可以发现均能发生取代反应,正确。
由上分析易知A项合理,故答案选A。
9.②④ ①③ ⑥ ⑤⑦ 2CHCHOH+O 2CHCHO+2HO Ⅱ<Ⅲ<Ⅰ
3 2 2 3 2
【详解】
(1)①由同种元素形成的结构与性质不同的单质互为同素异形体,则互为同素异形体的是:②红磷与白磷和
④金刚石和石墨;
②分子式相同而结构不同的物质互为同分异构体,则互为同分异构体的是:①正丁烷与异丁烷和③乙醇
(CHCHOH)与二甲醚(CHOCH );
3 2 3 3
③质子数相同而中子数不同的核素互为同位素,则属于同位素的是⑥16O与18O ;
④⑤冰与水和⑦干冰与二氧化碳只是物质所处的状态不同,它们分别属于同一种化合物;
(2)乙醇(CHCHOH)在铜作催化剂时与氧气发生催化氧化生成乙醛和水,反应的方程式为:2CHCHOH+
3 2 3 2
O 2CHCHO+2HO;
2 3 2
(3)铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中,据图可知,在Ⅰ中Fe为原电池的负极,Fe腐蚀的速率加快,在
Ⅱ中Fe为原电池的正极,Fe受到保护,发生腐蚀的速率最慢,在Ⅲ中,Fe发生化学腐蚀,腐蚀的速率小
于Ⅰ中形成原电池时腐蚀的速率,则铁被腐蚀的速率由慢到快的顺序是:Ⅱ<Ⅲ<Ⅰ。
10.③ ② ⑤ ⑦ BC CH CHCHCHCH、CHCH(CH )CHCH、C(CH)
3 2 2 2 3 3 3 2 3 3 4
【详解】
(1)同位素是质子数相同而中子数不同的同元素的不同原子,③ Cl 与 Cl属于;同素异形体是同种元素
组成的性质不同的单质之间的互称,②白磷与红磷属于;同分异构体是具有相同的分子式和不同结构的有机物之间的互称,⑤ 与 属于;结构相似分子组成上相差n个CH 单位有机物的
2
叫同系物,⑦C H 和C H 属于;
3 8 8 18
(2)有机物A 0.02mol 在氧气中完全燃烧生成4.4g CO 和2.16g HO,生成的二氧化碳的物质的量为:n=m/
2 2
M=4.4g/44g/mol=0.1mol,水的物质的量为:n=m/M=2.16g/18g/mol=0.12mol,该有机物分子中C、H数目分
别为:0.1mol/0.02mol=5、0.12mol×2/0.02=12,由于氧气中含有氧元素,所以无法确定A中是否含有O元
素,
A. 无法确定A中是否含有O元素,A错误;
B.该化合物可能不含O元素,B正确;
C.该化合物碳的个数是5,可能是新戊烷,常温下可能为气体,C正确;
D.该分子中C:H的个数比为5:12,D错误;
故选:BC;
若A为烃,分子式为C H ,为饱和烃,此烃可能的结构简式为:CHCHCHCHCH、
5 12 3 2 2 2 3
CHCH(CH )CHCH、C(CH)。
3 3 2 3 3 4