文档内容
2006 年全国初中初中化学素质和实验能力竞赛
湖北省赛区初赛试题
试卷说明:
1、本试卷包括第Ⅰ一卷和第二卷。第一卷为选择题,1-4页,共40分;第二卷为
非选择题,5-8页,共60分。全卷满分100分。考试时间120分钟。
2、可能用到的相对原子质量:
H—1 C—12 N—14 O-16 Na-23 Al-27
Si-28 S-32 Cl-35.5 Ca- 40 Fe -56 Zn-65
附Ⅰ、Ⅱ卷计分表:
题号 一 二 三 四 总分 总分人
得分
第Ⅰ卷(选择题,40 分)
一、选择题(本题包括20小题,每小题2分,共40分。每小题有1个或2个选项符
合题意。若有两个正确答案,只选对1个,得1分;只要有1个选项选错,该小题
即为0分。请将所选答案的序号填写在下表相应的空格内,只写在试题旁无效。)
第Ⅰ卷选择题答题表:
题号
答案
题号
答案
1、下列有关环境保护的叙述中,错误的是
A.温室气体主要是指CO 、CH 等导致地球气温升高的气体
2 4
B.白色污染只要是指白色粉尘对环境的污染
C.大气中的二氧化硫和二氧化氮是形成酸雨的主要物质
D.绿色化学是指对环境无负面影响的化学
2、2005年给我们留下了许多深刻的记忆。10月中旬,世界上海拔最高、线路最长,
穿越冻土里程也最长的高原铁路——青藏铁路全线铺通;11月13日,中国石油
吉化公司双苯厂苯胺装置发生爆炸,造成松花江水体严重污染;11月17日,神六
载人航天“多人多天”飞行圆满成功。关于上述事实,下列说法不正确有是
A.在运送飞船的火箭推进器中盛有液态肼(N H )和液态双氧水(H O ),当它们混
2 4 2 2
合反应时,即产生大量的氮气、二氧化碳和水蒸气,并放出大量的热
B.化学给人类带来灾难,应取缔所有的化工厂
C.用于制造钢轨的合金材料——高锰钢,具有很好的韧性和耐磨性
D.尽管青藏高原气候寒冷、空气稀薄,在选择钢轨时仍要注意钢材的防锈功能
3、下列说法正确的是A.使用含氟牙膏可预防龋齿
B.人若缺锌元素,会引起健贫血
C.“99.999999999%的高纯硅通常认为是纯净物
D.某物质与NaOH溶液反应生成盐和水,则该物质一定是酸
4、从化学角度看,下列广告用语没有科学性错误的是
A.“K”牌咖啡,滴滴香浓,决下含任何化学物质
B.“雪山牌”矿泉水,真正的纯水
C.“大自然”牌蔬菜,天然种植,不含任何元素,真正的“绿色”食品
D.食用合格“碘盐”,可预防甲状腺肿大
5、若用实验证明FeCl 溶液显黄色不是由Cl-离子造成的,下列实验无意义的是
3
A.观察KCl溶液的颜色
B.向FeCl 溶液中滴加适量氢氧化钠溶液振荡后静置,溶液黄色消失
3
C.向FeCl 溶液中滴加适量无色硝酸银溶液,振荡后静置,溶液黄色未消失
3
D.加水稀释后FeCl 溶液黄色变浅
3
6、纯碱溶于水中会发生水解反应,使溶液中OH-的个数比H+的多。下列说法不正
确的是
A.Na CO 溶液显碱性,可使无色酚酞试液变红色
2 3
B.向Na CO 溶液中加入适量的NaOH可抑制Na CO 水解反应的进行
2 3 2 3
C.可用稀盐酸来判断Na CO 溶液中是否含NaOH
2 3
D.可用食醋不区别纯碱和NaOH
7、随着生活节奏的加快,方便的小包装食品越来越受到人们的欢迎。为了防止富
脂食品氧化变质和受潮,生产厂家往往在食品包装袋中放入有某些化学物质的小
袋。你认为放在这些小袋中的物质应该是
A蔗糖 无水硫酸铜 B.食盐 生石灰
C.还原铁粉 生石灰 D.烧碱 生石灰
8、食品卫生与身体健康密切相关,下列做法对人体无害的是
A.烧鱼时加点食醋
B.香肠中添加过量的亚硝酸钠
C.白酒中掺入工业用酒精
D.食品原料中添加“苏丹红一号”
9、下列说法中,不正确的是
A.不定期量的红磷在充满空气的密闭容器中燃烧,可除去容器内的氧气
B.“曾青得铁则化为铜”是指将铁片放放氯化铜、硝酸铜等溶液中都可置换出铜
来
C.用紫色包菜汁可鉴别盐酸和氢氧化钠溶液
D.使用活性炭净化自然界的水,可得到软水
10、下列实验能达到目的的是
A.用铜和稀盐酸反应制取氢气
B.用石灰石和稀硫酸反应制取大量二氧化碳
C.用锌和浓硫酸反应制取氢气
D.用氧化铁和过氧化氢溶液制取氧气
11、榨苹果汁时,由于苹果中含有的Fe 在空气中极易被氧化,使榨出的果汁由淡
2+
绿色变为棕黄色。若向果汁中加入适量的维生素C,就可有效防止果汁变色现象
的发生。该事实说明维生素C具有A.氧化性 B.还原性 C.碱性 D.酸性
12、市场上销售的某“84”消毒液,其商品标牌上有如下叙述:①本品为无色液
体,呈碱性;②使用时加水稀释;③可对餐具、衣物进行消毒,可漂白浅色衣物。你
认为“84”消毒液的有效成分可能是
A.Na CO B.SO C.NaClO D.KMnO
2 3 2 4
13、正常人胃液的pH在0.9~1.5之间,胃酸(一般以盐表示)过多,则需要治疗。
一般可用含MgCO 或NaHCO 的药物治疗胃酸过多。这主要是由于
3 3
A.硝酸镁、碳酸氢钠的水溶液都呈碱性
B.碳酸镁、碳酸氢钠都属于碱
C.Na+和Mg2+都是人体中的微量元素
D.MgCO 、NaHCO 与胃酸作用生成CO ,在服药后喝汽水的舒服感
3 3 2
14、在人体所需的十多种微量元素中,有一种被称为“生命元素”的R元素,对
延长人类寿命起重要的作用。已知R元素的原子核个有4个电子层,其最高价氧
化物的化学式为RO ,则R元素的名称为
3
A.硫 B.砷 C.硒 D.硅
15、在一个密闭的容器内有X、Y、Z、Q四种物质,在一定条件下反应一定时间后,
测得反应前后各物质的质量如下:
物质 x Y Z Q
反应前质量/g 20 20 20 20
反应后质量/g 20 30 16 14
该密闭容器中发生化学反应的基本类型可能是
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
16、在30℃时,甲、乙两烧杯中分别盛有250 g、350 g氯化铵饱和溶液,要使两杯
析出相同质量的氯化铵晶体,下列措施正确的是
A.各蒸发掉20 g水并恢复至原温度
B.同时降温至10℃
C.甲杯蒸发掉25 g水,乙杯蒸发掉35 g水
D.同时升高温度至40℃
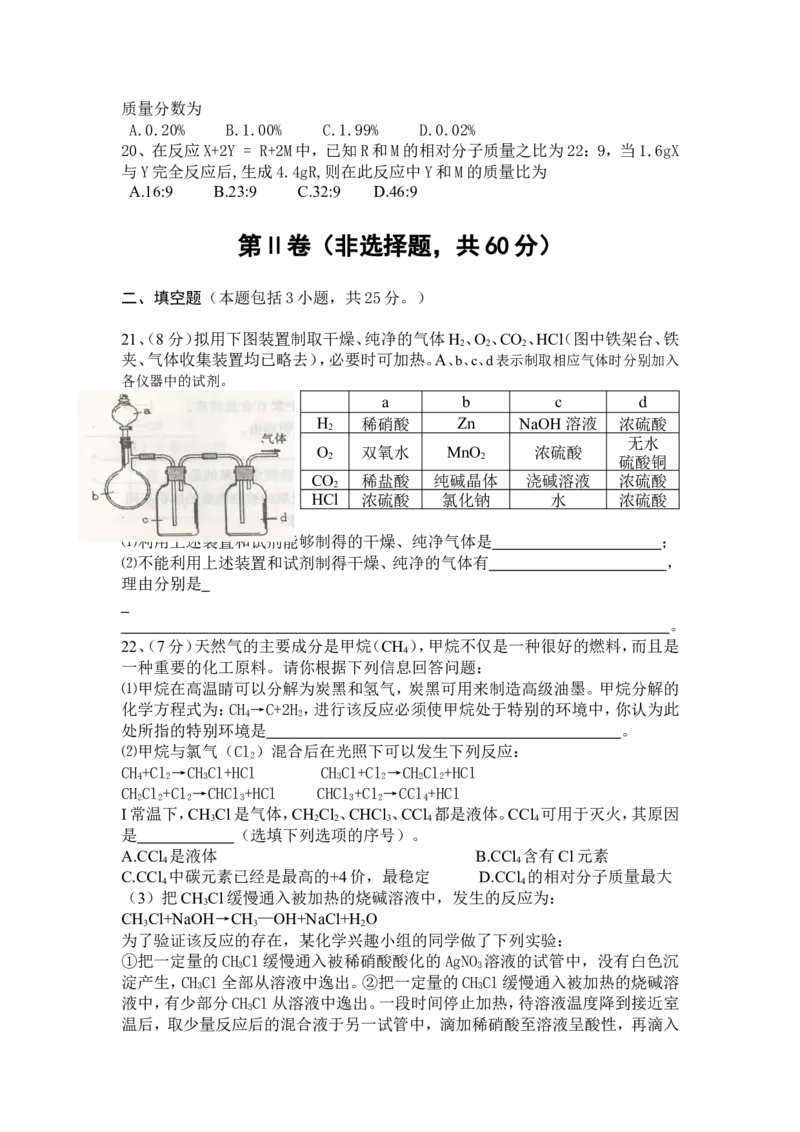
17、烧杯中盛有x溶液,逐滴加入(或通入)y物质,烧杯内溶液的pH变化如图所
示。则符合该变化的一组物质是
x y
A NaOH溶液 稀HCl(过量)
B 稀H SO BaCl 溶液(少量)
2 4 2
C Ca(OH) CO (适量)
2 2
D 稀H SO H O
2 4 2
18、已知Si+2NaOH+H O = Na SiO +2H ↑2Al+2NaOH+2H O = 2NaAl +3H ↑,硅不与
2 2 3 2 2 2 2
盐酸反应。将含铁铝硅的合金样品分为等质量的两份,分别与足量的稀盐酸和烧
碱溶液充分反应,测得放出氢气的质量相同。则该合金样品中铁铝硅的质量比不
可能是
A.112:81:28 B.336:27:84 C.324:135:36 D.56:81:56
19、人尿中含氮0.93%,如这些氮只存在于尿素中,则人尿中含尿素[CO(NH2)2]的质量分数为
A.0.20% B.1.00% C.1.99% D.0.02%
20、在反应X+2Y = R+2M中,已知R和M的相对分子质量之比为22:9,当1.6gX
与Y完全反应后,生成4.4gR,则在此反应中Y和M的质量比为
A.16:9 B.23:9 C.32:9 D.46:9
第Ⅱ卷(非选择题,共 60 分)
二、填空题(本题包括3小题,共25分。)
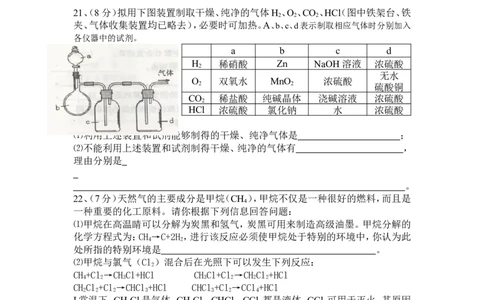
21、(8分)拟用下图装置制取干燥、纯净的气体H 、O 、CO 、HC(l 图中铁架台、铁
2 2 2
夹、气体收集装置均已略去),必要时可加热。A、b、c、d表示制取相应气体时分别加入
各仪器中的试剂。
a b c d
H 稀硝酸 Zn NaOH溶液 浓硫酸
2
无水
O 双氧水 MnO 浓硫酸
2 2 硫酸铜
CO 稀盐酸 纯碱晶体 浇碱溶液 浓硫酸
2
HCl 浓硫酸 氯化钠 水 浓硫酸
⑴利用上述装置和试剂能够制得的干燥、纯净气体是 ;
⑵不能利用上述装置和试剂制得干燥、纯净的气体有 ,
理由分别是
。
22、(7分)天然气的主要成分是甲烷(CH ),甲烷不仅是一种很好的燃料,而且是
4
一种重要的化工原料。请你根据下列信息回答问题:
⑴甲烷在高温睛可以分解为炭黑和氢气,炭黑可用来制造高级油墨。甲烷分解的
化学方程式为:CH →C+2H ,进行该反应必须使甲烷处于特别的环境中,你认为此
4 2
处所指的特别环境是 。
⑵甲烷与氯气(Cl )混合后在光照下可以发生下列反应:
2
CH +Cl →CH Cl+HCl CH Cl+Cl →CH Cl +HCl
4 2 3 3 2 2 2
CH Cl +Cl →CHCl +HCl CHCl +Cl →CCl +HCl
2 2 2 3 3 2 4
I常温下,CH Cl是气体,CH Cl 、CHCl 、CCl 都是液体。CCl 可用于灭火,其原因
3 2 2 3 4 4
是 (选填下列选项的序号)。
A.CCl 是液体 B.CCl 含有Cl元素
4 4
C.CCl 中碳元素已经是最高的+4价,最稳定 D.CCl 的相对分子质量最大
4 4
(3)把CH Cl缓慢通入被加热的烧碱溶液中,发生的反应为:
3
CH Cl+NaOH→CH —OH+NaCl+H O
3 3 2
为了验证该反应的存在,某化学兴趣小组的同学做了下列实验:
①把一定量的CH Cl缓慢通入被稀硝酸酸化的AgNO 溶液的试管中,没有白色沉
3 3
淀产生,CH Cl全部从溶液中逸出。②把一定量的CH Cl缓慢通入被加热的烧碱溶
3 3
液中,有少部分CH Cl从溶液中逸出。一段时间停止加热,待溶液温度降到接近室
3
温后,取少量反应后的混合液于另一试管中,滴加稀硝酸至溶液呈酸性,再滴入AgNO 溶液,发现有白色沉淀产生。
3
该实验第①步的目的是 ,该实
验现象说明了什么? 。
实验②中,滴加稀硝酸至溶液呈酸性的原因是
。
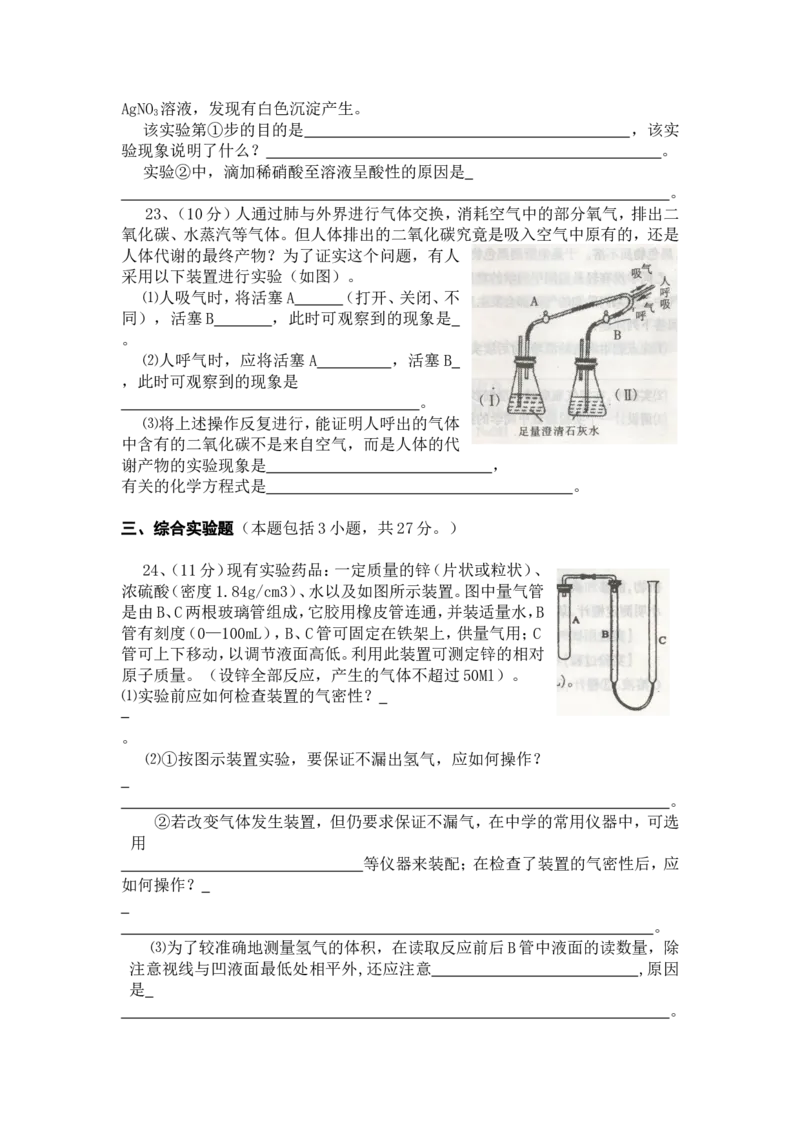
23、(10分)人通过肺与外界进行气体交换,消耗空气中的部分氧气,排出二
氧化碳、水蒸汽等气体。但人体排出的二氧化碳究竟是吸入空气中原有的,还是
人体代谢的最终产物?为了证实这个问题,有人
采用以下装置进行实验(如图)。
⑴人吸气时,将活塞A (打开、关闭、不
同),活塞B ,此时可观察到的现象是
。
⑵人呼气时,应将活塞A ,活塞B
,此时可观察到的现象是
。
⑶将上述操作反复进行,能证明人呼出的气体
中含有的二氧化碳不是来自空气,而是人体的代
谢产物的实验现象是 ,
有关的化学方程式是 。
三、综合实验题(本题包括3小题,共27分。)
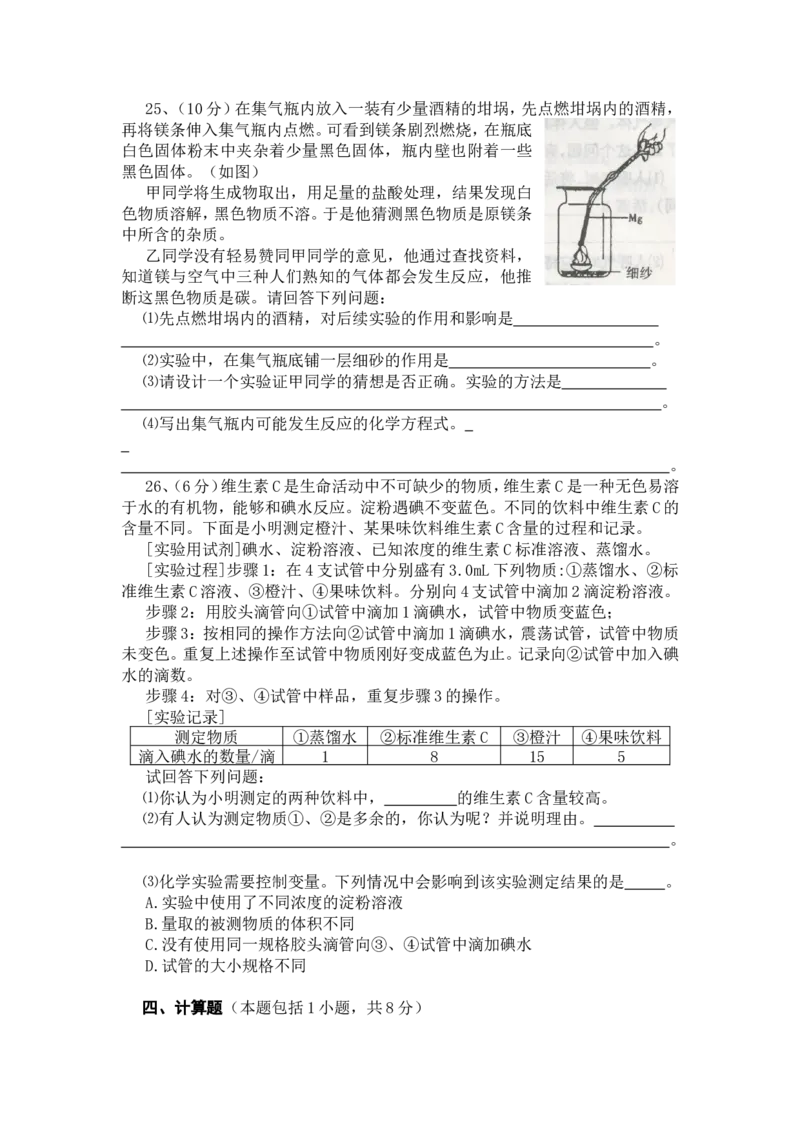
24、(11分)现有实验药品:一定质量的锌(片状或粒状)、
浓硫酸(密度1.84g/cm3)、水以及如图所示装置。图中量气管
是由B、C两根玻璃管组成,它胶用橡皮管连通,并装适量水,B
管有刻度(0—100mL),B、C管可固定在铁架上,供量气用;C
管可上下移动,以调节液面高低。利用此装置可测定锌的相对
原子质量。(设锌全部反应,产生的气体不超过50Ml)。
⑴实验前应如何检查装置的气密性?
。
⑵①按图示装置实验,要保证不漏出氢气,应如何操作?
。
②若改变气体发生装置,但仍要求保证不漏气,在中学的常用仪器中,可选
用
等仪器来装配;在检查了装置的气密性后,应
如何操作?
。
⑶为了较准确地测量氢气的体积,在读取反应前后B管中液面的读数量,除
注意视线与凹液面最低处相平外,还应注意 ,原因
是
。25、(10分)在集气瓶内放入一装有少量酒精的坩埚,先点燃坩埚内的酒精,
再将镁条伸入集气瓶内点燃。可看到镁条剧烈燃烧,在瓶底
白色固体粉末中夹杂着少量黑色固体,瓶内壁也附着一些
黑色固体。(如图)
甲同学将生成物取出,用足量的盐酸处理,结果发现白
色物质溶解,黑色物质不溶。于是他猜测黑色物质是原镁条
中所含的杂质。
乙同学没有轻易赞同甲同学的意见,他通过查找资料,
知道镁与空气中三种人们熟知的气体都会发生反应,他推
断这黑色物质是碳。请回答下列问题:
⑴先点燃坩埚内的酒精,对后续实验的作用和影响是
。
⑵实验中,在集气瓶底铺一层细砂的作用是 。
⑶请设计一个实验证甲同学的猜想是否正确。实验的方法是
。
⑷写出集气瓶内可能发生反应的化学方程式。
。
26、(6分)维生素C是生命活动中不可缺少的物质,维生素C是一种无色易溶
于水的有机物,能够和碘水反应。淀粉遇碘不变蓝色。不同的饮料中维生素C的
含量不同。下面是小明测定橙汁、某果味饮料维生素C含量的过程和记录。
[实验用试剂]碘水、淀粉溶液、已知浓度的维生素C标准溶液、蒸馏水。
[实验过程]步骤1:在4支试管中分别盛有3.0mL下列物质:①蒸馏水、②标
准维生素C溶液、③橙汁、④果味饮料。分别向4支试管中滴加2滴淀粉溶液。
步骤2:用胶头滴管向①试管中滴加1滴碘水,试管中物质变蓝色;
步骤3:按相同的操作方法向②试管中滴加1滴碘水,震荡试管,试管中物质
未变色。重复上述操作至试管中物质刚好变成蓝色为止。记录向②试管中加入碘
水的滴数。
步骤4:对③、④试管中样品,重复步骤3的操作。
[实验记录]
测定物质 ①蒸馏水 ②标准维生素C ③橙汁 ④果味饮料
滴入碘水的数量/滴 1 8 15 5
试回答下列问题:
⑴你认为小明测定的两种饮料中, 的维生素C含量较高。
⑵有人认为测定物质①、②是多余的,你认为呢?并说明理由。
。
⑶化学实验需要控制变量。下列情况中会影响到该实验测定结果的是 。
A.实验中使用了不同浓度的淀粉溶液
B.量取的被测物质的体积不同
C.没有使用同一规格胶头滴管向③、④试管中滴加碘水
D.试管的大小规格不同
四、计算题(本题包括1小题,共8分)27、(8分)白色粉末X是Na CO 与NaHCO 的混合物。取三份质量不同的样品甲、
2 3 3
乙、丙,分别跟50g相同浓度的稀盐酸充分反应,得到气体的质量与X的质量关系
如下表:
试计算样品中Na CO 与NaHCO 的质量分数各是多少。(结果精确到0.1%)
2 3 3
实验组别 甲 乙 丙
稀盐酸的质量/g 50 50 50
样品的质量/g 3.80 6.20 7.20
气体的质量/g 1.76 2.62 2.62