文档内容
第一章 有机化合物的结构特点与研究方法
第二节 研究有机化合物的一般方法
第 1 课时 有机化合物的分离、提纯
学习导航 1.通过对蒸馏法、萃取法、重结晶法实验原理和基本操作的学习,认识科学探究过程的步
骤,学会设计科学探究方案,培养严谨的科学态度和科学的思维方式。
2.结合常见有机化合物分离、提纯方法的学习,能根据有机化合物性质的差异选择有机化合
物分离、提纯的正确方法。
教学过程 一、研究有机化合物的一般步骤
分离、提纯―→确定实验式―→确定分子式―→确定分子结构
二、有机物的分离、提纯方法
1.蒸馏
(1)适用条件
①液态有机化合物含有少量杂质且该有机化合物热稳定性较高;
②有机化合物的沸点与杂质的沸点相差较大。
(2)蒸馏装置及注意事项
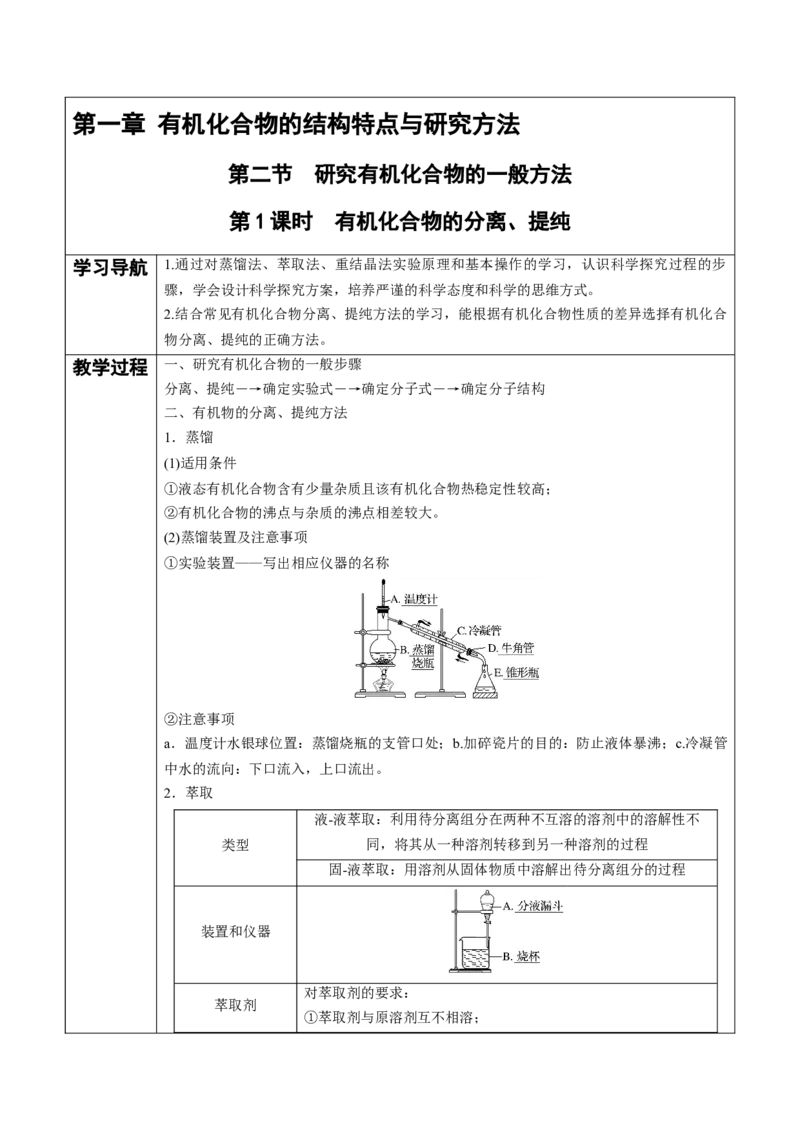
①实验装置——写出相应仪器的名称
②注意事项
a.温度计水银球位置:蒸馏烧瓶的支管口处;b.加碎瓷片的目的:防止液体暴沸;c.冷凝管
中水的流向:下口流入,上口流出。
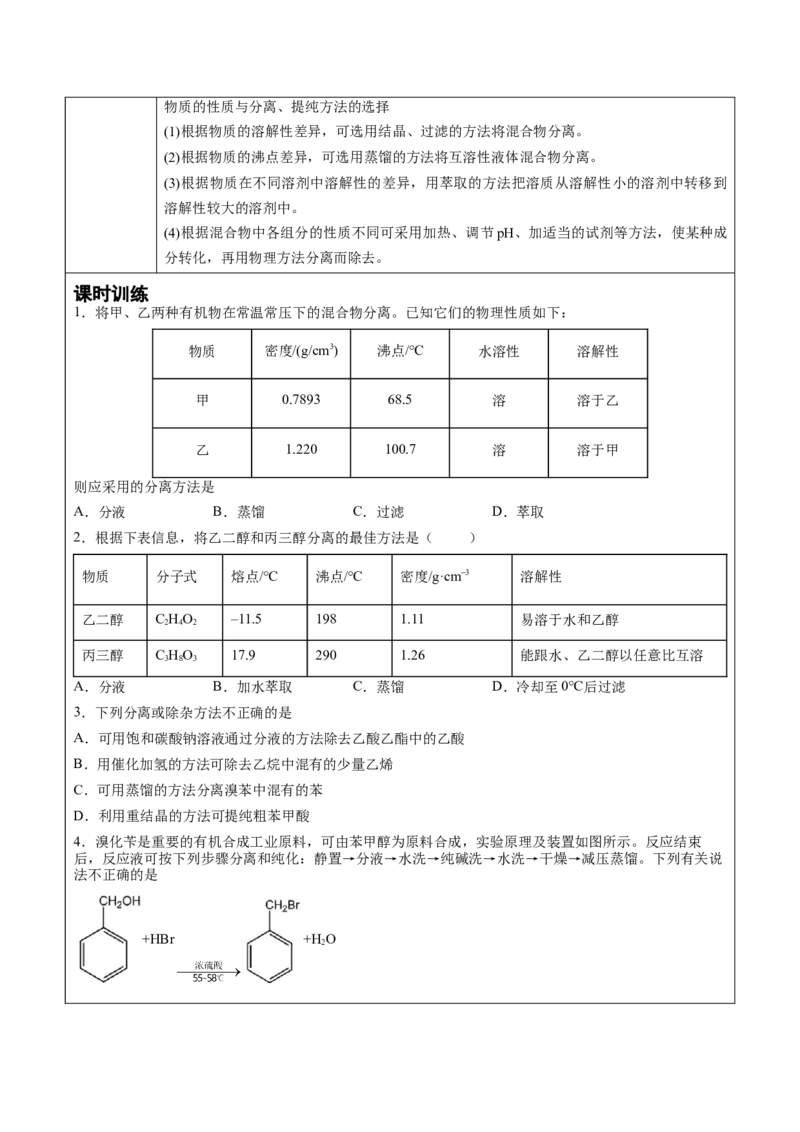
2.萃取
液-液萃取:利用待分离组分在两种不互溶的溶剂中的溶解性不
类型 同,将其从一种溶剂转移到另一种溶剂的过程
固-液萃取:用溶剂从固体物质中溶解出待分离组分的过程
装置和仪器
对萃取剂的要求:
萃取剂
①萃取剂与原溶剂互不相溶;②溶质在萃取剂中的溶解度远大于在原溶剂中的溶解度;
③萃取剂与原溶液中的成分不反应
常用萃取剂:乙醚、乙酸乙酯、二氯甲烷等
定义 将萃取后的两层液体分开的操作
加入萃取剂后充分振荡,静置分层,然后打开分液漏斗上方的玻
分液
操作 璃塞和下方的活塞将两层液体分离,下层液体从下口流出,并及
时关闭活塞,上层液体从上口倒出
3.重结晶
(1)
(2)实验探究:重结晶法提纯含有少量氯化钠和泥沙杂质的苯甲酸。
已知:纯净的苯甲酸为无色结晶,熔点122 ℃,可用作食品防腐剂,苯甲酸微溶于水,在
水中不同温度的溶解度如下表:
温度/℃ 25 50 75
溶解度/g 0.34 0.85 2.2
提纯苯甲酸的实验步骤如下:
①观察粗苯甲酸样品的状态。
②将1.0 g粗苯甲酸放入100 mL烧杯,再加入50 mL蒸馏水。加热,搅拌,使粗苯甲酸充
分溶解。
③用漏斗趁热将溶液过滤到另一个烧杯中,将滤液静置,使其缓慢冷却结晶。
④待滤液完全冷却后滤出晶体,并用少量蒸馏水洗涤。将晶体铺在干燥的滤纸上,晾干后
称其质量。
⑤计算重结晶收率。
4.色谱法
当样品随着流动相经过固定相时,因样品中不同组分在两相间的分配不同而实现分离,这
样的一类分离分析方法被称为色谱法。
【归纳总结】物质的性质与分离、提纯方法的选择
(1)根据物质的溶解性差异,可选用结晶、过滤的方法将混合物分离。
(2)根据物质的沸点差异,可选用蒸馏的方法将互溶性液体混合物分离。
(3)根据物质在不同溶剂中溶解性的差异,用萃取的方法把溶质从溶解性小的溶剂中转移到
溶解性较大的溶剂中。
(4)根据混合物中各组分的性质不同可采用加热、调节pH、加适当的试剂等方法,使某种成
分转化,再用物理方法分离而除去。
课时训练
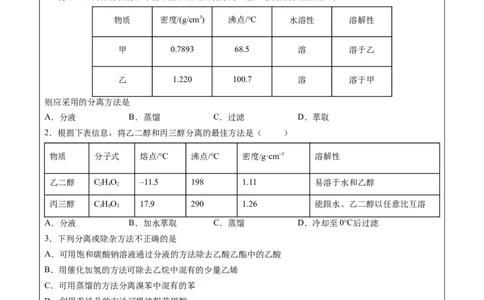
1.将甲、乙两种有机物在常温常压下的混合物分离。已知它们的物理性质如下:
物质 密度/(g/cm3) 沸点/℃ 水溶性 溶解性
甲 0.7893 68.5 溶 溶于乙
乙 1.220 100.7 溶 溶于甲
则应采用的分离方法是
A.分液 B.蒸馏 C.过滤 D.萃取
2.根据下表信息,将乙二醇和丙三醇分离的最佳方法是( )
物质 分子式 熔点/℃ 沸点/℃ 密度/g·cm–3 溶解性
乙二醇 C HO –11.5 198 1.11 易溶于水和乙醇
2 4 2
丙三醇 C HO 17.9 290 1.26 能跟水、乙二醇以任意比互溶
3 8 3
A.分液 B.加水萃取 C.蒸馏 D.冷却至0℃后过滤
3.下列分离或除杂方法不正确的是
A.可用饱和碳酸钠溶液通过分液的方法除去乙酸乙酯中的乙酸
B.用催化加氢的方法可除去乙烷中混有的少量乙烯
C.可用蒸馏的方法分离溴苯中混有的苯
D.利用重结晶的方法可提纯粗苯甲酸
4.溴化苄是重要的有机合成工业原料,可由苯甲醇为原料合成,实验原理及装置如图所示。反应结束
后,反应液可按下列步骤分离和纯化:静置→分液→水洗→纯碱洗→水洗→干燥→减压蒸馏。下列有关说
法不正确的是
+HBr +H O
2下列有关说法不正确的是
A.实验时,应该先从冷凝管接口b处通水,后加热至反应温度
B.该实验适宜用水浴加热
C.浓硫酸作催化剂和吸水剂
D.在水洗操作中往往因为振摇而使得分液漏斗中出现大量气体,可以通过打开上口瓶塞的方式来放气
5.下列关于物质的分离、提纯实验中的一些操作或做法,正确的是
A.在组装蒸馏装置时,温度计的水银球应伸入液面下
B.分离碘与CCl 的混合物,不可采用蒸馏的方法
4
C.在苯甲酸重结晶实验中,粗苯甲酸加热溶解后还要加入少量蒸馏水
D.在苯甲酸重结晶实验中,待粗苯甲酸完全溶解后要冷却到常温再过滤
6.下列关于实验的描述错误的是
A.摩尔盐制备过程可以用含少量水的乙醇洗涤晶体,可以提高产品纯度,但会降低产率
B.实验室制备对氨基苯磺酸,可以用冷水洗涤晶体除杂
C.对氨基苯磺酸在水中的溶解度随温度升高而增大,制备对氨基苯磺酸,若晶体颜色过深,可以将粗产
品用沸水溶解,加入活性炭脱色,冷却结晶,抽滤
D.从硫酸铜溶液得到胆矾晶体时,加热到溶液表面出现晶膜时停止加热
7.把碘从碘的四氯化碳溶液里分离出来,有下列操作步骤:①静置后分液:②把碘的四氯化碳溶液倒入
分液漏斗;③加入浓氢氧化钠溶液,再充分振荡;④得固态碘;⑤静置后过滤;⑥在水层加入45%的硫酸
溶液得悬浊液。正确的操作顺序是
A.①②③⑤⑥④ B.⑥⑤④③②① C.②③①⑥⑤④ D.⑥⑤④③①②
8.用KMnO 氧化甲苯制备苯甲酸。苯甲酸的熔点为122.13℃,微溶于水,易溶于酒精。实验方法:将甲
4
苯和KMnO 溶液在100℃反应一段时间后停止反应,过滤,将含有苯甲酸钾(C HCOOK)和甲苯的滤液
4 6 5
按如下流程分离苯甲酸并回收未反应的甲苯。
下列说法正确的是( )
A.无色液体A是苯甲酸,白色固体B是甲苯
B.操作Ⅰ的名称为蒸馏,操作II的名称为分液C.为了得到更多的白色固体B,冷却结晶时温度越低越好
D.加入浓盐酸酸化的目的是为了将苯甲酸钾转化为产物苯甲酸
9.(1)键线式 表示的分子式___结构简式___名称是_____。
(2)含有杂质的工业乙醇的蒸馏装置中,玻璃仪器有酒精灯、蒸馏瓶、______、_____、尾接管、锥形瓶。
(3)写出丁基的结构简式有_______。
(4)0.1mol某烃在足量的氧气中完全燃烧,生成CO 和水各0.6mol,则该烃的分子式为_____.若该烃能使
2
溴水褪色,且能在催化剂作用下与H 发生加成反应,生成2,2﹣二甲基丁烷,则此烃属于__烃,结构简
2
式为_____,名称是____,该加成反应的化学方程式为_____。
10.2-(对甲基苯基)苯并咪唑( )是合成对甲基苯甲醛(PTAL)的中间体,其沸点为
270℃。利用邻苯二胺( )和对甲基苯甲酸( )合成2-(对甲基苯基)苯并咪唑的反应过程如
下:
向反应装置(如图)中加入0.1 mol邻苯二胺和0.15 mol对甲基苯甲酸后,再加入适量多聚磷酸(能与水互溶
的质子酸),搅拌成糊状物,慢慢升温至100℃并搅拌1h,继续加热至190℃,回流2h,冷却。用10%的
NaOH溶液调至微碱性,有大量固体出现,分离晶体,水洗,经重结晶提纯后,得白色针状晶体产品14.6
g.回答下列问题:
(1)仪器A的名称为___________,冷却水的流向为___________(填“a进b出”或“b进a出”)。
(2)制备过程中需在190℃下回流2h,可采取的加热方式为___________(填“水浴加热”或“油浴加热”)。
(3)“分离结晶”得到晶体与母液,其操作名称为___________,加入10%的NaOH溶液的作用为
___________;分离完成后“水洗”的具体操作为___________。
(4)粗产品一般需要通过重结晶的方法来提纯,步骤为加热溶解→活性炭脱色→趁热过滤→冷却结晶→过滤
→洗涤→干燥,其中需要趁热过滤的原因是___________;趁热过滤时所得滤渣中一定含有
___________(填名称)。
(5)2-(对甲基苯基)苯并咪唑的产率为___________(保留三位有效数字)。
答案解析1.B
【详解】
由表格中数据可以知道,二者互溶,但沸点不同,可利用蒸馏分离甲乙两种混合物,而萃取、分液不能分
离二者,其中过滤用于固体与溶液的分离;综上所述,本题选B。
2.C
【详解】
A.由表格中数据分析可知,乙二醇和丙三醇的溶解性相差不大,无法用分液方法分离,A项错误;
B.由表格中数据分析可知,乙二醇和丙三醇都溶解于水,无法用加水萃取方法分离,B项错误;
C.由表格中数据分析可知,乙二醇和丙三醇的沸点相差较大,故可利用蒸馏法进行分离,C项正确;
D.由表格中数据分析可知,乙二醇和丙三醇的熔点相差不大,冷却至0℃结晶后过滤,效果不佳,D项错
误;
答案选C。
3.B
【详解】
A.乙酸可以和碳酸钠溶液反应,而乙酸乙酯难溶于饱和碳酸钠溶液,A正确;
B.加氢的量无法控制,用催化加氢的方法除去乙烷中混有的少量乙烯,会引入新的杂质,B错误;
C.溴苯和苯的沸点差异较大,蒸馏常用于分离沸点不同的液体混合物,C正确;
D.苯甲酸的溶解度受温度影响较大,控制不同的温度可以使苯甲酸的溶解度发生变化,从而从溶液中分
离出来,所以利用重结晶的方法可提纯粗苯甲酸,D正确;
综上所述答案为B。
4.D
【详解】
A.为防止原料加热蒸发损失,同时达到冷凝回流效果,应先从冷凝管接口b处通水,再先加热至反应温
度,故A正确;
B.该实验要求温度较准确,适宜用热水浴加热,以便控制温度,故B正确;
C.从反应方程式看,浓硫酸作催化剂,产物中有水,通过浓硫酸吸水,促进反应更完全,故C正确;
D.在水洗操作中,放气操作需要将分液漏斗向上倾斜,再打开活塞进行放气,故D错误;
故选:D。
5.C
【详解】
A.蒸馏时,测定馏分的温度,则温度计的水银球应在蒸馏烧瓶支管口处,故A错误;
B.碘与CCl 的沸点不同,所以分离碘与CCl 的混合物,可采用蒸馏的方法,故B错误;
4 4
C.水在加热过程中会蒸发,苯甲酸能溶于水,减少过滤时苯甲酸的损失,防止过饱和提前析出结晶,加
热溶解后还要加少量蒸馏水,故C正确;
D.苯甲酸的溶解度不大,温度高时溶解度大,所以待粗苯甲酸完全溶解后要趁热过滤,减少苯甲酸的损
耗,故D错误;
故选C。
6.C【详解】
A.用乙醇溶解水,使水在晶体表面的浓度降低,洗涤后晶体表面的低浓度水乙醇溶液会很快挥发,则摩
尔盐制备过程可以用含少量水的乙醇洗涤晶体,可以提高产品纯度,但会降低产率,A描述正确;
B.用少量冷水洗涤对氨基苯磺酸晶体,可降低晶体的溶解度,则实验室制备对氨基苯磺酸,可以用冷水
洗涤晶体除杂,B描述正确;
C.对氨基苯磺酸在水中的溶解度随温度升高而增大,若晶体颜色过深,可以将粗产品用沸水溶解,冷却
结晶,抽滤,利用重结晶进行提纯,C描述错误;
D.从硫酸铜溶液得到胆矾晶体时,加热到溶液表面出现晶膜时停止加热,温度逐渐下降,溶解度也逐渐
下降,有利于晶体的生长,D描述正确;
答案为C。
7.C
【详解】
把碘从碘的四氯化碳溶液里分离出来,首先把碘的四氯化碳溶液倒入分液漏斗;然后加入浓氢氧化钠溶
液,充分振荡,I 与NaOH反应产生NaI、NaIO、HO;再经静置后分液分离出四氯化碳层;然后在水层加
2 2
入45%的硫酸溶液,发生反应:I-+IO-+2H+=I +H O,由于I 的溶解度在水中不大,得到悬浊液;再静置后
2 2 2
过滤;最后可得固态碘,故正确的操作顺序是②③①⑥⑤④,故合理选项是C。
8.D
【详解】
A.由分析知:无色液体A是苯,白色固体B是苯甲酸,故A错误;
B.由分析知操作Ⅰ的名称为分液,操作II的名称为蒸馏,故B错误;
C.温度太低杂质溶解度降低,可析出杂质,导致产物纯度降低,故C错误;
D.根据强酸制取弱酸原理,加入浓盐酸将 转化成溶解度较小的苯甲酸,故D正确;
故答案为D。
9.C H (CH )CHCH CHCH 2-甲基戊烷 温度计 冷凝管 -CHCHCHCH,-
6 14 3 2 2 2 3 2 2 2 3
CH(CH ) CH CH,-CHCH(CH ),-C(CH) C H 单烯 (CH)CCH=CH 3,3-二甲基-1-
3 2 3 2 3 2 3 3 6 12 3 2
丁烯 (CH)CCH=CH +H C(CH)CHCH
3 2 2 3 3 2 3
【详解】
(1) 分子中含有6个碳原子,属于饱和烃,分子式为C H ,该有机物主链上有5个C,2号C
6 14
一个甲基,结构简式为(CH)CHCH CHCH,命名为2-甲基戊烷,因此,本题正确答案是:C H ;
3 2 2 2 3 6 14
(CH)CHCH CHCH;2-甲基戊烷;
3 2 2 2 3
(2)含有杂质的工业乙醇的蒸馏装置中需要使用的玻璃仪器为酒精灯、蒸馏瓶、温度计、冷凝管、尾接管、
锥形瓶还缺少温度计和冷凝管,因此,本题正确答案是:温度计;冷凝管;
(3)丁烷含有正丁烷和异丁烷两种同分异构体,正丁烷去掉一个H后剩下的部分可为:
-CHCHCHCH,-CH(CH ) CH CH,异丁烷去掉一个H后剩下的部分可为
2 2 2 3 3 2 3
-CHCH(CH ),-C(CH),因此,本题正确答案是:-CHCHCHCH,-CH(CH ) CH CH,-
2 3 2 3 3 2 2 2 3 3 2 3
CHCH(CH ),-C(CH);
2 3 2 3 3
(4) 0.1mol某烃在足量的氧气中完全燃烧生成CO 和水各0.6mol,根据原子守恒可以知道,0. 6mol该烃的
2分子中N(C)= =6,N(H)= =12,故该烃的分子式为C H ,该烃能使溴水褪色说明分子
6 12
中含有1个C=C键,该烃属于烯烃,在催化剂作用下与H 加成生成2,2﹣二甲基丁烷,相邻两个碳原子
2
都含有H原子为C=C双键位置,该烃的结构简式为:(CH)CCH=CH ,名称为3,3-二甲基-1-丁烯;与氢
3 2
气发生加成反应的化学方程式为(CH)CCH=CH +H C(CH)CHCH,因此,本题正确答案是:
3 2 2 3 3 2 3
C H ;单烯;
6 12
(CH)CCH=CH ;3,3-二甲基-1-丁烯;(CH)CCH=CH +H C(CH)CHCH。
3 2 3 2 2 3 3 2 3
10.三颈烧瓶 a进b出 油浴加热 过滤 中和多聚磷酸,反应掉过量的对甲基苯甲酸 向
漏斗中加入蒸馏水至浸没晶体,然后让水自然流下,反复操作2~3次,直至晶体洗涤干净 防止产品因
结晶而损失 活性炭 70.2%
【详解】
(1)仪器A的名称为三颈烧瓶,冷却水应下进上出,则流向为:a进b出;
(2)加热温度为190℃,大于水的沸点,所以选择油浴加热;
(3)分离晶体得到晶体和母液的操作为:过滤;加入氢氧化钠的目的是调节溶液为碱性、除去多余的反应物
对甲基苯甲酸,使目标产物结晶;水洗晶体的步骤为:向漏斗中加入蒸馏水至浸没晶体,然后让水自然流
下,反复操作2~3次,直至晶体洗涤干净;
(4)趁热过滤的原因:在热的条件下大多溶质杂质在溶剂中溶解度较高,能完全溶解,从而较好地分离杂质
和产物,防止产品因结晶而损失。活性炭的溶解度不好,所以滤渣中一定含有活性炭;
(5) 根据反应方程式:
,0.1 mol邻苯二胺理论上得到产
物2-(对甲基苯基)苯并咪唑的物质的量为0.1mol,则质量为m=nM=0.1mol×208g/mol=20.8g,则产率为
。