文档内容
第 04 讲 离子反应 离子方程式
第一部分:高考真题感悟
1.(2022·全国·高考真题)能正确表示下列反应的离子方程式为
A.硫化钠溶液和硝酸混合:S2-+2H+=H S↑
2
B.明矾溶液与过量氨水湿合:Al3++4NH+2H O=AlO +4NH
3 2
C.硅酸钠溶液中通入二氧化碳:SiO +CO +H O=HSiO +HCO
2 2
D.将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:Ba2++2OH-+2H++SO
2 4 4
=BaSO ↓+2H O
4 2
2.(2022·浙江·高考真题)下列物质属于非电解质的是
A.CH B.KI C.NaOH D.CHCOOH
4 3
3.(2021·浙江·高考真题)下列反应的方程式不正确的是
A.石灰石与醋酸反应:CO +2CH COOH=2CH COO- +CO ↑+H O
3 3 2 2
B.铜片上电镀银的总反应(银作阳极,硝酸银溶液作电镀液):Ag(阳极) Ag(阴极)
C.铜与稀硝酸反应:3Cu+2NO +8H+=3Cu2+ +2NO↑+4HO
2
D.明矾溶液中加入少量氢氧化钡溶液:2Al3+ +3SO + 3Ba2++6OH-=2Al(OH) ↓+ 3BaSO↓
3 4
4.(2021·浙江·高考真题)不能正确表示下列变化的离子方程式是
A.碳酸镁与稀盐酸反应:
B.亚硫酸氢钠的水解:
C.锌溶于氢氧化钠溶液:
D.亚硝酸钠与氯化铵溶液受热反应:
5.(2022·浙江·高考真题)下列反应的离子方程式不正确的是
A.盐酸中滴加 溶液:B. 溶液中通入过量 :
C.乙醇与 酸性溶液反应:
D.溴与冷的 溶液反应:
6.(2022·广东·高考真题)下列关于 的化合物之间转化反应的离子方程式书写正确的是
A.碱转化为酸式盐:
B.碱转化为两种盐:
C.过氧化物转化为碱:
D.盐转化为另一种盐:
7.(2022·湖南·高考真题)下列离子方程式正确的是
A. 通入冷的 溶液:
B.用醋酸和淀粉 溶液检验加碘盐中的 :
C. 溶液中加入 产生沉淀:
D. 溶液与少量的 溶液混合:
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2022·湖南怀化·一模)以电石渣[主要成分为 ,含少量 等杂质]为原料制备纳米碳酸钙的
一种工艺流程如下:下列说法错误的是
A.“浸渍”时,适当提高温度,有利于提高 浸取率
B.滤液II中主要成分是 ,可以循环使用
C.“碳化”中反应的离子方程式为
D.已知 ,则滤液II中 沉淀完全时, 小于
2.(2022·河北衡水中学一模)下列过程涉及的离子方程式不正确的是
A.用烧碱溶液处理使用时过量的衣物除锈剂(主要成分为 溶液):
B.用过量氨水吸收废气中的 :
C.磁性氧化铁溶于HI溶液:
D.用稀 溶液鉴别铜合金制的假金币:
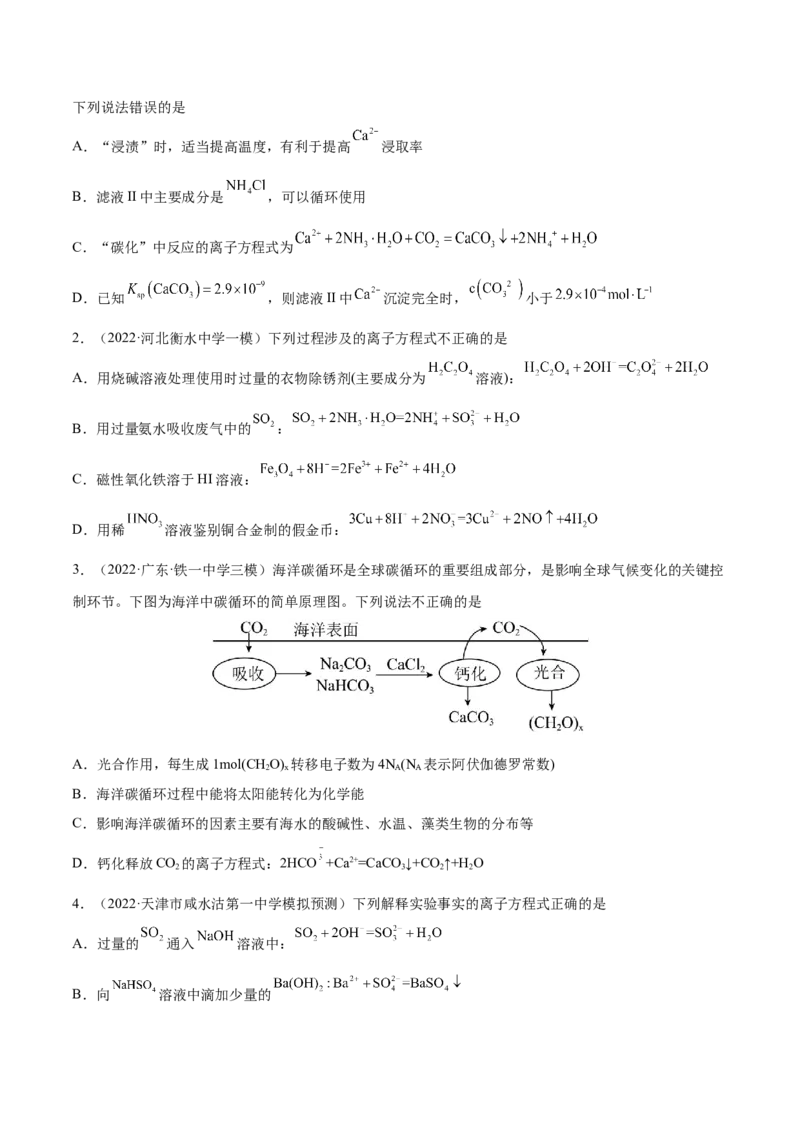
3.(2022·广东·铁一中学三模)海洋碳循环是全球碳循环的重要组成部分,是影响全球气候变化的关键控
制环节。下图为海洋中碳循环的简单原理图。下列说法不正确的是
A.光合作用,每生成1mol(CH O) 转移电子数为4N (N 表示阿伏伽德罗常数)
2 x A A
B.海洋碳循环过程中能将太阳能转化为化学能
C.影响海洋碳循环的因素主要有海水的酸碱性、水温、藻类生物的分布等
D.钙化释放CO 的离子方程式:2HCO +Ca2+=CaCO ↓+CO ↑+H O
2 3 2 2
4.(2022·天津市咸水沽第一中学模拟预测)下列解释实验事实的离子方程式正确的是
A.过量的 通入 溶液中:
B.向 溶液中滴加少量的C.白醋除去水壶中的水垢的反应:
D.向 中加入过量的 溶液:
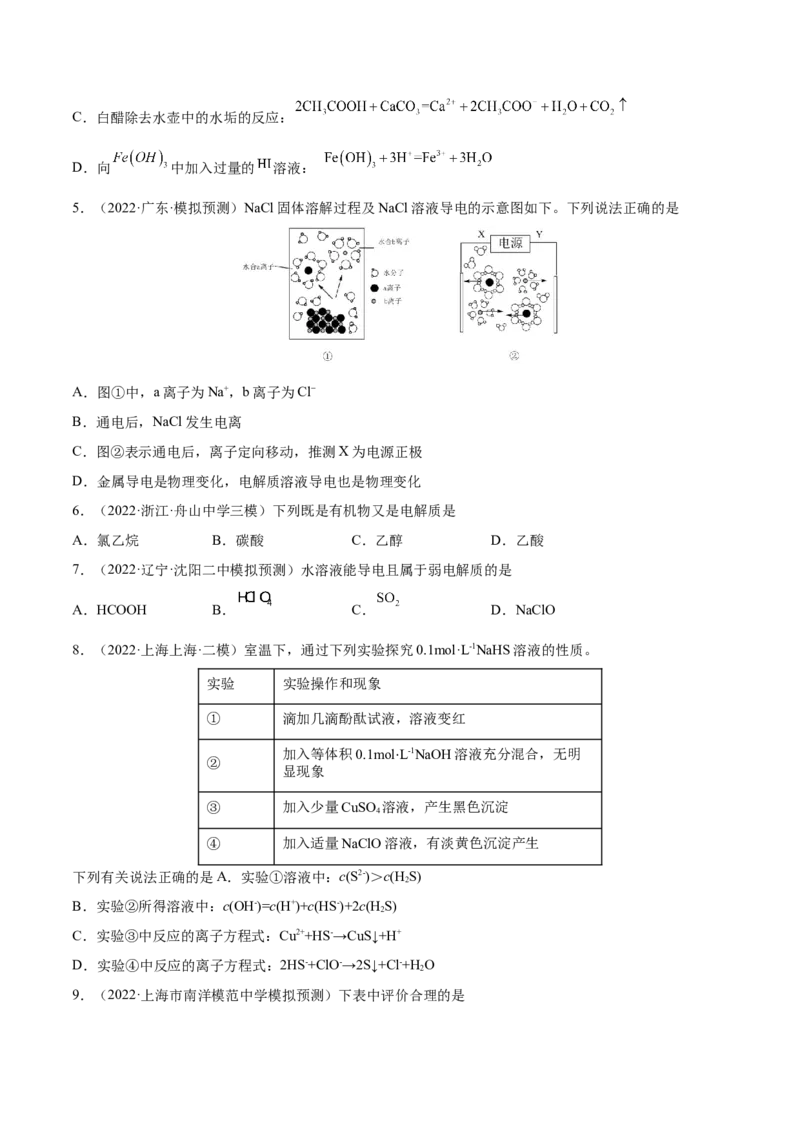
5.(2022·广东·模拟预测)NaCl固体溶解过程及NaCl溶液导电的示意图如下。下列说法正确的是
A.图①中,a离子为Na+,b离子为Cl−
B.通电后,NaCl发生电离
C.图②表示通电后,离子定向移动,推测X为电源正极
D.金属导电是物理变化,电解质溶液导电也是物理变化
6.(2022·浙江·舟山中学三模)下列既是有机物又是电解质是
A.氯乙烷 B.碳酸 C.乙醇 D.乙酸
7.(2022·辽宁·沈阳二中模拟预测)水溶液能导电且属于弱电解质的是
A.HCOOH B. C. D.NaClO
8.(2022·上海上海·二模)室温下,通过下列实验探究0.1mol·L-1NaHS溶液的性质。
实验 实验操作和现象
① 滴加几滴酚酞试液,溶液变红
加入等体积0.1molL-1NaOH溶液充分混合,无明
②
显现象
⋅
③ 加入少量CuSO 溶液,产生黑色沉淀
4
④ 加入适量NaClO溶液,有淡黄色沉淀产生
下列有关说法正确的是A.实验①溶液中:c(S2-)>c(H S)
2
B.实验②所得溶液中:c(OH-)=c(H+)+c(HS-)+2c(H S)
2
C.实验③中反应的离子方程式:Cu2++HS-→CuS↓+H+
D.实验④中反应的离子方程式:2HS-+ClO-→2S↓+Cl-+H O
2
9.(2022·上海市南洋模范中学模拟预测)下表中评价合理的是编
化学反应 离子方程式 评价
号
错误。碳酸钙是弱电解质,不
A 碳酸钙与醋酸反应 CO +2CH 3 COOH→CO 2 ↑+H 2 O+2CH 3 CO
O- 应写成离子形式
次氯酸钠溶液中通入
B 少量CO 2ClO-+CO 2 +H 2 O→CO +2HClO 正确。
2
错误。水解方程式误写成电离
C NaHSO 3 的水解 HSO +H 2 O SO +H 3 O+ 方程式
等物质的量的FeBr 和 错误。Fe2+与Br-的物质的量之
D 2 2Fe2++2Br-+2Cl→2Fe3++Br +4Cl-
Cl 反应 2 2 比与化学式不符
2
10.(2022·湖南·模拟预测)下列离子方程式中,书写正确的是
A.向 溶液中通入过量 :
B.向饱和 溶液中滴入几滴稀 溶液:
C.向沸水中滴加饱和氯化铁溶液得到红褐色液体:
D.室温下用稀NaOH溶液吸收 :
11.(2022·浙江·三模)下列反应的离子方程式正确的是
A.丙烯醛与足量溴水反应:CH=CHCHO+2Br+H O→CH BrCHBrCOOH+2H++2Br-
2 2 2 2
B.H18O中投入NaO 固体:2H18O+2Na O=4Na++4OH-+18O↑
2 2 2 2 2 2 2
C.少量Cl 通入NaSO 溶液中:SO +Cl+H O=2H++2Cl-+SO
2 2 3 2 2
D.用酸性高锰酸钾溶液滴定草酸:2MnO +16H++5C O =2Mn2++10CO ↑+8H O
2 2 2
12.(2022·江苏南通·模拟预测)以铬矿石烧渣(主要含 、 、 和 )为主要原料
制取重铬酸钠晶体( )的流程如下。已知“水浸”时 发生的反应为
下列说法不正确的是
A.“水浸”时适当升高温度和搅拌有利于加快浸取的速率
B.“酸化”时 发生反应的离子方程式为
C.“滤渣”的成分为
D.“母液”中主要存在离子是 和
二、主观题(共4小题,共40分)
13.(2020·青铜峡市高级中学高三开学考试)(8分)正确书写下列离子反应方程式
(1)将少量NaHSO 溶液滴加到Ba(OH) 溶液中,当恰好完全沉淀时,反应的离子方程式为____。
4 2
(2)在酸性条件下,向含铬废水中加入FeSO ,可将 还原为Cr3+,该过程的离子反应方程式为_。
4
(3)在淀粉碘化钾溶液中,滴加少量次氯酸钠碱性溶液,立即会看到溶液变蓝色,离子方程式为____。
(4)已知酸性环境下,ClO-可将Mn2+氧化成MnO ,自身被还原成Cl-,该过程的离子反应方程式为_。
2
14.(18分)(2021·天津·高三)请按要求书写下列离子方程式:
(1)利用FeCl 溶液制备胶体的离子方程式为_______
3
(2)工业上用次氯酸钠和FeCl 在碱性条件下制备新型绿色消毒剂高铁酸钠(Na FeO)该反应的离子方程式是:
3 2 4
_______。
(3)FeSO 的酸性溶液与HO 反应试写出该反应的离子方程式:_______
4 2 2
(4)Fe3+可腐蚀印刷电路板上的铜箔,反应的离子方程式为_______。
(5)向NaClO溶液中通入少量的CO 离子方程式为_______。
2
(6)FeBr 溶液中通入等物质的量的Cl 气体,离子方程式为:_______
2 2
15.(14分)以硅藻土为载体的五氧化二钒(V O)是接触法生产硫酸的催化剂。从废矾催化剂中回收 VO
2 5 2 5
既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为
物质 VO VO KSO SiO Fe O Al O
2 5 2 4 2 4 2 2 3 2 3
质量分数/% 2.2~2.9 2.8~3.1 22~28 60~65 1~2 <1
以下是一种废钒催化剂回收工艺路线:
回答下列问题:
(1)已知“酸浸”时,VO 转化为VO,请写出该反应的离子方程式_________,同时将VO 转成VO2+,反
2 5 2 4应的离子方程式为_____,“废渣1”的主要成分是____。
(2)工艺中“氧化”步骤使VO2+变为VO反应的离子方程式为__________,欲使3 mol的VO2+变为VO +,
2
则需要氧化剂KClO 至少为_____mol。
3
(3)工艺中“中和”步骤生成“废渣2”的离子方程式为____________________________。
(4)“离子交换”和“洗脱”可简单表示为 4ROH+VOR VO +4OH-(ROH为强碱性阴离子交换树
4 4 4 12
脂)。为了提高洗脱效率,淋洗液应该呈__________性(填“酸”“碱”或“中”)。