文档内容
专题 02 海水中的重要元素——钠和氯
第 05 练 氯及其化合物
1.浩瀚的海洋中蕴藏着丰富的资源,其中可为人类利用的氯化物含量相当高。海水中含量最多的氯
化物是( )
A.NaCl B.MgCl C.KCl D.CaCl
2 2
2.下列物质中,不能由Cl 直接反应制得的是
2
A.CuCl B.FeCl C.Ca(ClO) D.NaCl
2 2 2
3.下列不能使有色布条褪色的物质是( )
A.氯水 B.次氯酸钠溶液 C.漂白粉溶液 D.氯化钙溶液
4.有关Cl 的性质,下列说法不正确的是( )
2
A.Cl 在通常状况下呈黄绿色 B.能与NaOH溶液反应
2
C.铁丝在Cl 中燃烧,反应生成FeCl D.H 在Cl 中燃烧,产生苍白色火焰
2 2 2 2
5.下列关于新制氨水、氯水的描述不正确的是( )
A.“两水”都能与SO 反应 B.“两水”中都存在可逆反应
2
C.“两水”都有刺激性气味 D.“两水”中所含微粒种类数目相同
6.下列有关氯气的说法正确的是( )
A.Cl 虽然是一种有毒气体,但控制用量,可以用于自来水的消毒、杀菌
2
B.铁丝在氯气中燃烧,产生棕褐色的烟,加水溶解后,溶液呈浅绿色
C.氯气通入水中形成的氯水能使有色布条褪色,说明氯气有漂白性
D.Cl 具有很强的氧化性,在化学反应中只能作氧化剂
2
7.下列有关物质性质与用途具有对应关系的是( )
A.漂白粉具有还原性,可用于生活用水的消毒
B.ClO 具有强氧化性,可用于自来水的杀菌消毒
2
C.NaClO溶液显碱性,可用于杀菌、消毒
D.次氯酸具有弱酸性,可用作有色物质的漂白剂
8.下列药品的保存方法正确的是( )
A.氢氟酸保存在棕色细口玻璃瓶中B.氯水密封于无色试剂瓶中
C.液溴易挥发,保存在带有橡胶塞的棕色试剂瓶中,并应加水液封
D.碘单质保存在带有玻璃塞的棕色广口玻璃瓶中
9.氯化碘(ICl)的化学性质跟氯气相似,预计它跟水反应的最初生成物是( )
A.HI和HCl B.HCl和HIO C.HClO 和HIO D.HClO和HIO
3
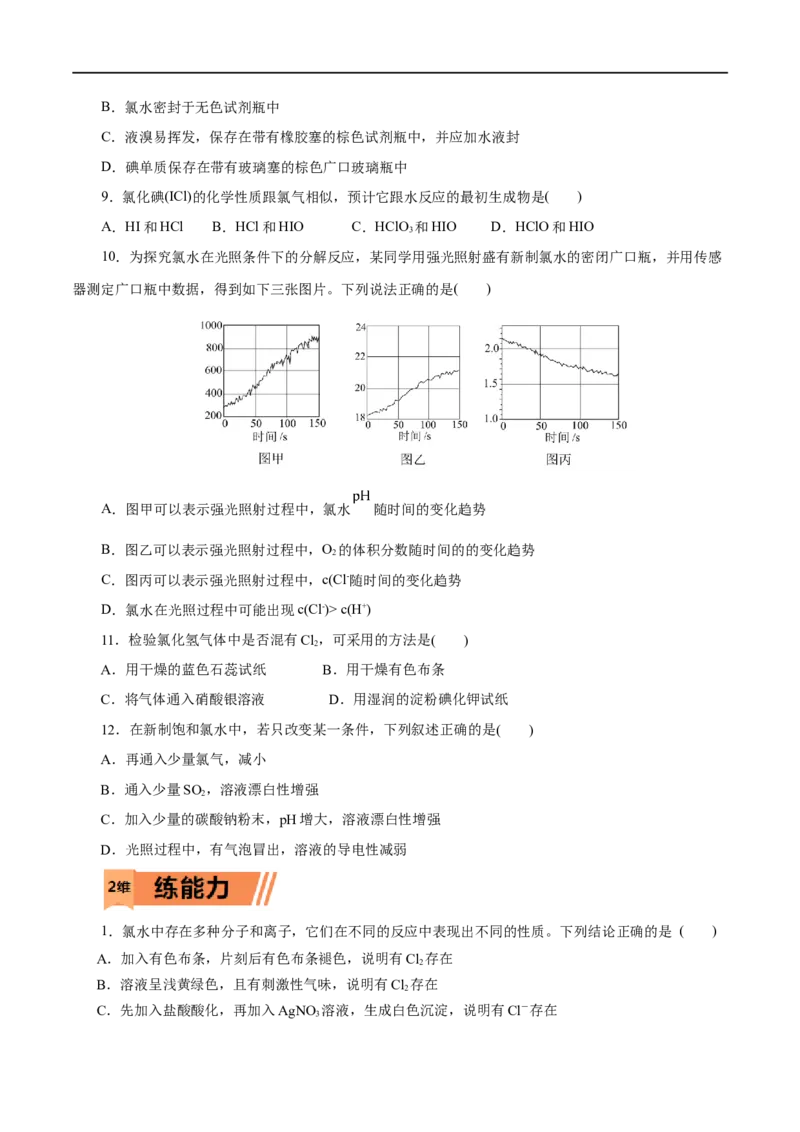
10.为探究氯水在光照条件下的分解反应,某同学用强光照射盛有新制氯水的密闭广口瓶,并用传感
器测定广口瓶中数据,得到如下三张图片。下列说法正确的是( )
A.图甲可以表示强光照射过程中,氯水 随时间的变化趋势
B.图乙可以表示强光照射过程中,O 的体积分数随时间的的变化趋势
2
C.图丙可以表示强光照射过程中,c(Cl-随时间的变化趋势
D.氯水在光照过程中可能出现c(Cl-)> c(H+)
11.检验氯化氢气体中是否混有Cl,可采用的方法是( )
2
A.用干燥的蓝色石蕊试纸 B.用干燥有色布条
C.将气体通入硝酸银溶液 D.用湿润的淀粉碘化钾试纸
12.在新制饱和氯水中,若只改变某一条件,下列叙述正确的是( )
A.再通入少量氯气,减小
B.通入少量SO ,溶液漂白性增强
2
C.加入少量的碳酸钠粉末,pH增大,溶液漂白性增强
D.光照过程中,有气泡冒出,溶液的导电性减弱
1.氯水中存在多种分子和离子,它们在不同的反应中表现出不同的性质。下列结论正确的是 ( )
A.加入有色布条,片刻后有色布条褪色,说明有Cl 存在
2
B.溶液呈浅黄绿色,且有刺激性气味,说明有Cl 存在
2
C.先加入盐酸酸化,再加入AgNO 溶液,生成白色沉淀,说明有Cl-存在
3D.加入NaOH溶液,氯水的浅黄绿色消失,说明有HClO存在
2.设N 代表阿伏加德罗常数的数值,下列各项中指定数目一定为N 的是( )
A A
A.含2 mol HCl的浓盐酸与43.5 g MnO 反应:被氧化的HCl分子数
2
B.11.2 L Cl 与足量钠反应:转移的电子数
2
C.KClO+6HCl(浓)===KCl+3Cl↑+3HO中生成13.44 L(标准状况)Cl 转移的电子数
3 2 2 2
D.1 mol Cl 与足量NaOH反应:氧化剂的分子数
2
3.75%乙醇和84消毒液等均能有效灭活新冠病毒。84消毒液的主要成分是次氯酸钠。设N 为阿伏加
A
德罗常数的值,下列说法正确的是( )
A.74.5g次氯酸钠中含有的离子数目为2N
A
B.1mol次氯酸钠与足量盐酸反应转移的电子数为2N
A
C.46g 75%乙醇中含有的氧原子数大于6N
A
D.利用氯气和氢氧化钠溶液反应制取0.1 mol次氯酸钠需要消耗2.24L氯气
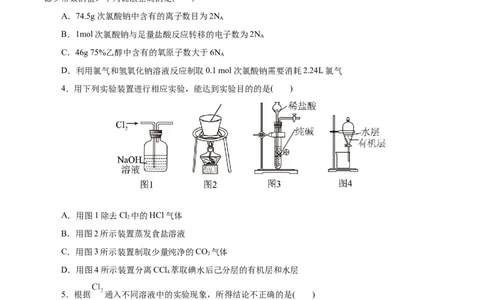
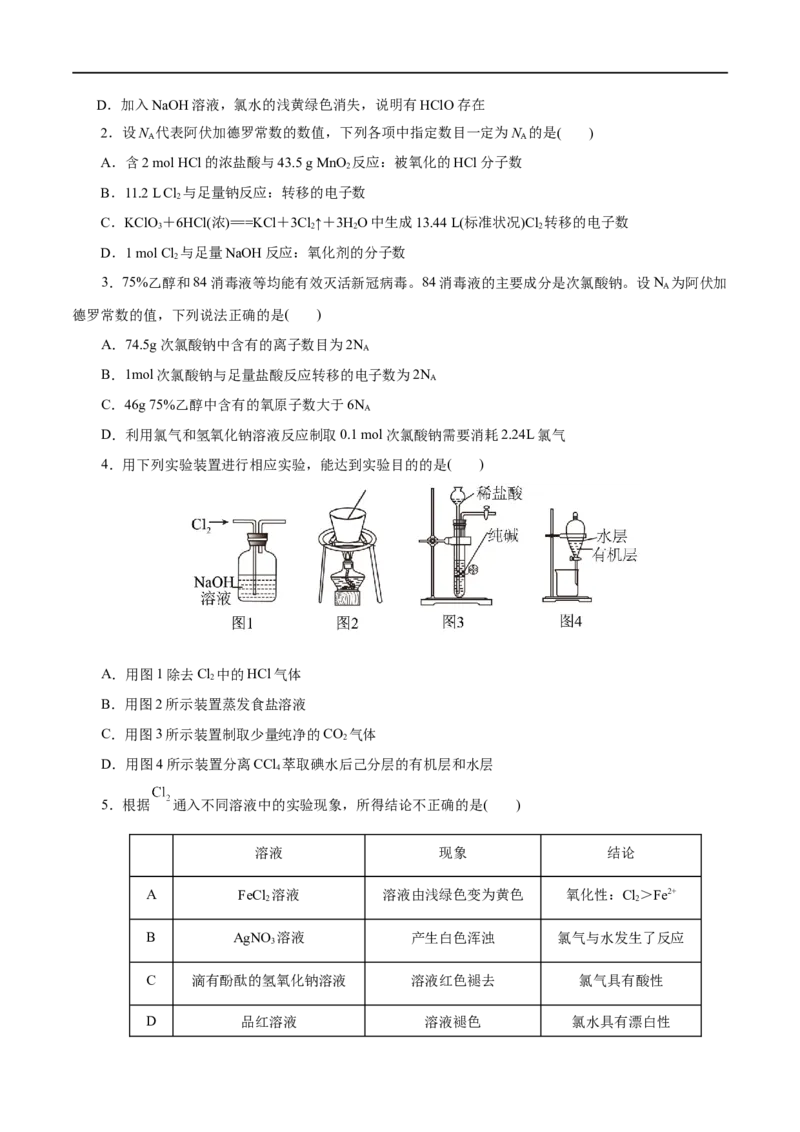
4.用下列实验装置进行相应实验,能达到实验目的的是( )
A.用图1除去Cl 中的HCl气体
2
B.用图2所示装置蒸发食盐溶液
C.用图3所示装置制取少量纯净的CO 气体
2
D.用图4所示装置分离CCl 萃取碘水后己分层的有机层和水层
4
5.根据 通入不同溶液中的实验现象,所得结论不正确的是( )
溶液 现象 结论
A FeCl 溶液 溶液由浅绿色变为黄色 氧化性:Cl>Fe2+
2 2
B AgNO 溶液 产生白色浑浊 氯气与水发生了反应
3
C 滴有酚酞的氢氧化钠溶液 溶液红色褪去 氯气具有酸性
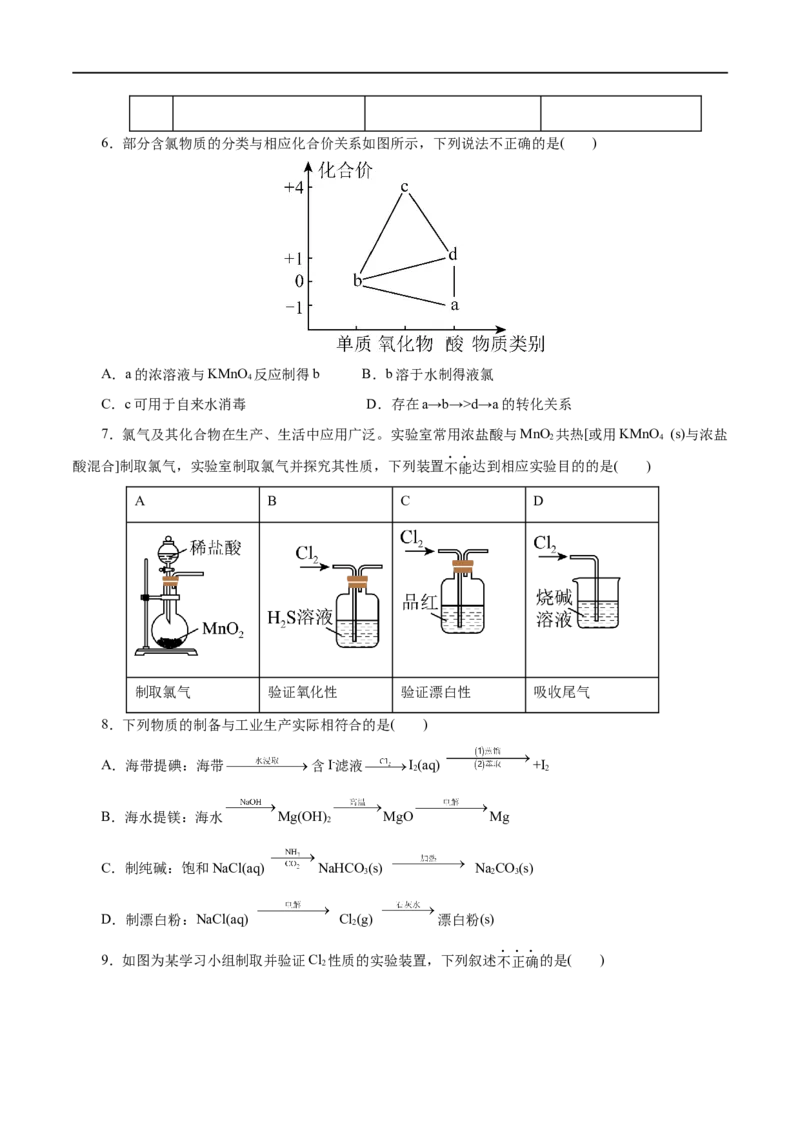
D 品红溶液 溶液褪色 氯水具有漂白性6.部分含氯物质的分类与相应化合价关系如图所示,下列说法不正确的是( )
A.a的浓溶液与KMnO 反应制得b B.b溶于水制得液氯
4
C.c可用于自来水消毒 D.存在a→b→>d→a的转化关系
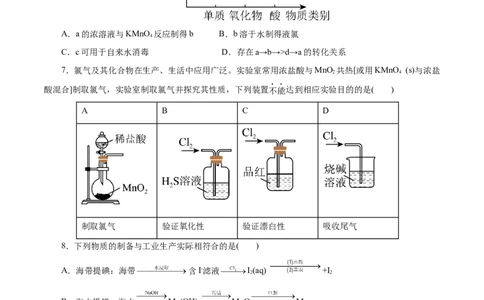
7.氯气及其化合物在生产、生活中应用广泛。实验室常用浓盐酸与MnO 共热[或用KMnO (s)与浓盐
2 4
酸混合]制取氯气,实验室制取氯气并探究其性质,下列装置不能达到相应实验目的的是( )
A B C D
制取氯气 验证氧化性 验证漂白性 吸收尾气
8.下列物质的制备与工业生产实际相符合的是( )
A.海带提碘:海带 含I-滤液 I(aq) +I
2 2
B.海水提镁:海水 Mg(OH) MgO Mg
2
C.制纯碱:饱和NaCl(aq) NaHCO (s) Na CO(s)
3 2 3
D.制漂白粉:NaCl(aq) Cl (g) 漂白粉(s)
2
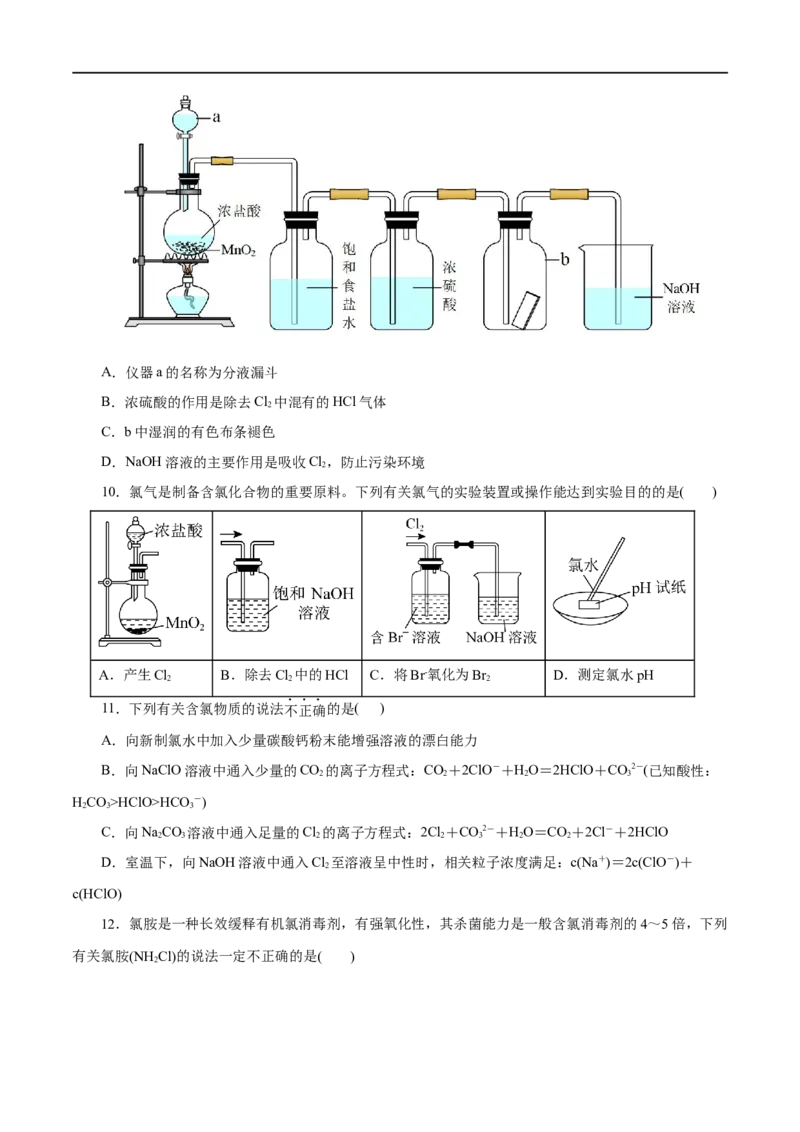
9.如图为某学习小组制取并验证Cl 性质的实验装置,下列叙述不正确的是( )
2A.仪器a的名称为分液漏斗
B.浓硫酸的作用是除去Cl 中混有的HCl气体
2
C.b中湿润的有色布条褪色
D.NaOH溶液的主要作用是吸收Cl,防止污染环境
2
10.氯气是制备含氯化合物的重要原料。下列有关氯气的实验装置或操作能达到实验目的的是( )
A.产生Cl B.除去Cl 中的HCl C.将Br-氧化为Br D.测定氯水pH
2 2 2
11.下列有关含氯物质的说法不正确的是( )
A.向新制氯水中加入少量碳酸钙粉末能增强溶液的漂白能力
B.向NaClO溶液中通入少量的CO 的离子方程式:CO+2ClO-+HO=2HClO+CO2-(已知酸性:
2 2 2 3
HCO>HClO>HCO -)
2 3 3
C.向NaCO 溶液中通入足量的Cl 的离子方程式:2Cl+CO2-+HO=CO+2Cl-+2HClO
2 3 2 2 3 2 2
D.室温下,向NaOH溶液中通入Cl 至溶液呈中性时,相关粒子浓度满足:c(Na+)=2c(ClO-)+
2
c(HClO)
12.氯胺是一种长效缓释有机氯消毒剂,有强氧化性,其杀菌能力是一般含氯消毒剂的4~5倍,下列
有关氯胺(NH Cl)的说法一定不正确的是( )
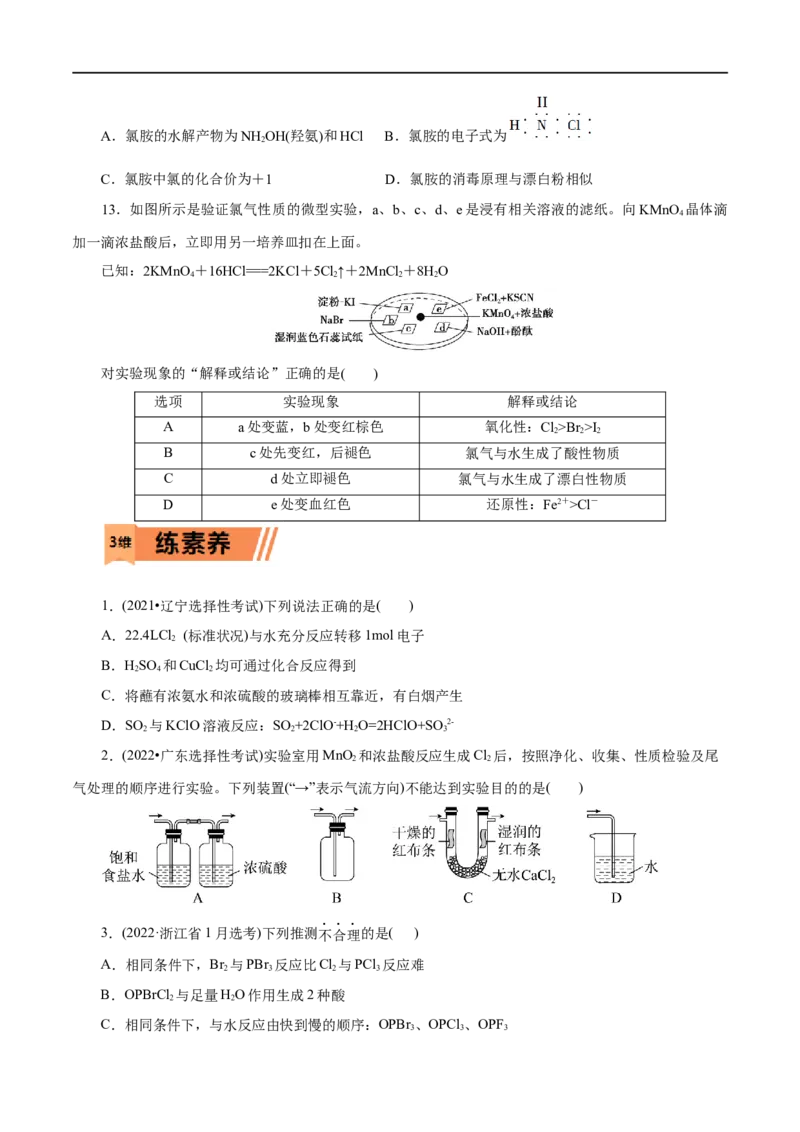
2A.氯胺的水解产物为NH OH(羟氨)和HCl B.氯胺的电子式为
2
C.氯胺中氯的化合价为+1 D.氯胺的消毒原理与漂白粉相似
13.如图所示是验证氯气性质的微型实验,a、b、c、d、e是浸有相关溶液的滤纸。向KMnO 晶体滴
4
加一滴浓盐酸后,立即用另一培养皿扣在上面。
已知:2KMnO +16HCl===2KCl+5Cl↑+2MnCl +8HO
4 2 2 2
对实验现象的“解释或结论”正确的是( )
选项 实验现象 解释或结论
A a处变蓝,b处变红棕色 氧化性:Cl>Br >I
2 2 2
B c处先变红,后褪色 氯气与水生成了酸性物质
C d处立即褪色 氯气与水生成了漂白性物质
D e处变血红色 还原性:Fe2+>Cl-
1.(2021•辽宁选择性考试)下列说法正确的是( )
A.22.4LCl (标准状况)与水充分反应转移1mol电子
2
B.HSO 和CuCl 均可通过化合反应得到
2 4 2
C.将蘸有浓氨水和浓硫酸的玻璃棒相互靠近,有白烟产生
D.SO 与KClO溶液反应:SO +2ClO-+H O=2HClO+SO 2-
2 2 2 3
2.(2022•广东选择性考试)实验室用MnO 和浓盐酸反应生成Cl 后,按照净化、收集、性质检验及尾
2 2
气处理的顺序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是( )
3.(2022·浙江省1月选考)下列推测不合理的是( )
A.相同条件下,Br 与PBr 反应比Cl 与PCl 反应难
2 3 2 3
B.OPBrCl 与足量HO作用生成2种酸
2 2
C.相同条件下,与水反应由快到慢的顺序:OPBr 、OPCl 、OPF
3 3 3D.PBr 与足量C HOH作用可得到P(OC H)
3 2 5 2 5 3
4.由一种阳离子与两种酸根阴离子组成的盐称为混盐,CaOCl 是一种常见的混盐。下列说法不正确
2
的是( )
A.CaOCl 有较强的氧化性
2
B.CaOCl 水溶液呈碱性
2
C.由氯气为原料,每生成1molCaOCl ,转移的电子为2mol
2
D.CaOCl 的溶液中加入足量浓硫酸,可有黄绿色的气体产生
2
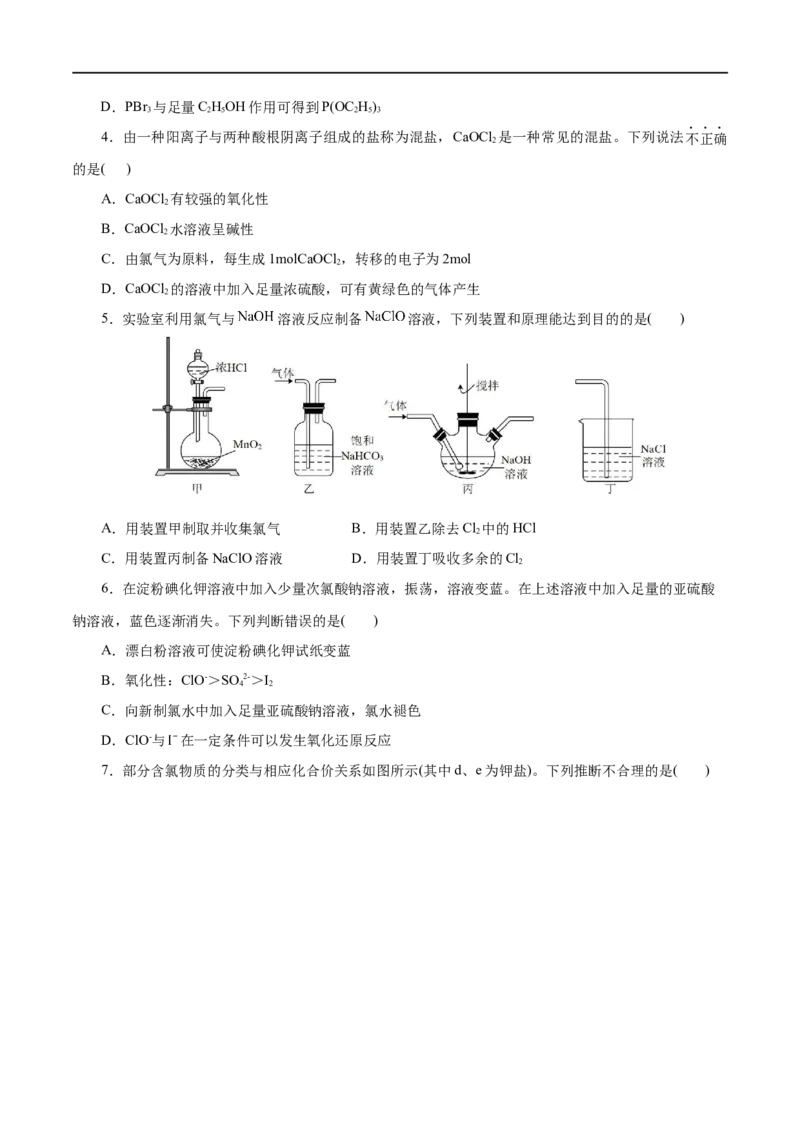
5.实验室利用氯气与 溶液反应制备 溶液,下列装置和原理能达到目的的是( )
A.用装置甲制取并收集氯气 B.用装置乙除去Cl 中的HCl
2
C.用装置丙制备NaClO溶液 D.用装置丁吸收多余的Cl
2
6.在淀粉碘化钾溶液中加入少量次氯酸钠溶液,振荡,溶液变蓝。在上述溶液中加入足量的亚硫酸
钠溶液,蓝色逐渐消失。下列判断错误的是( )
A.漂白粉溶液可使淀粉碘化钾试纸变蓝
B.氧化性:ClO->SO 2->I
4 2
C.向新制氯水中加入足量亚硫酸钠溶液,氯水褪色
D.ClO-与 在一定条件可以发生氧化还原反应
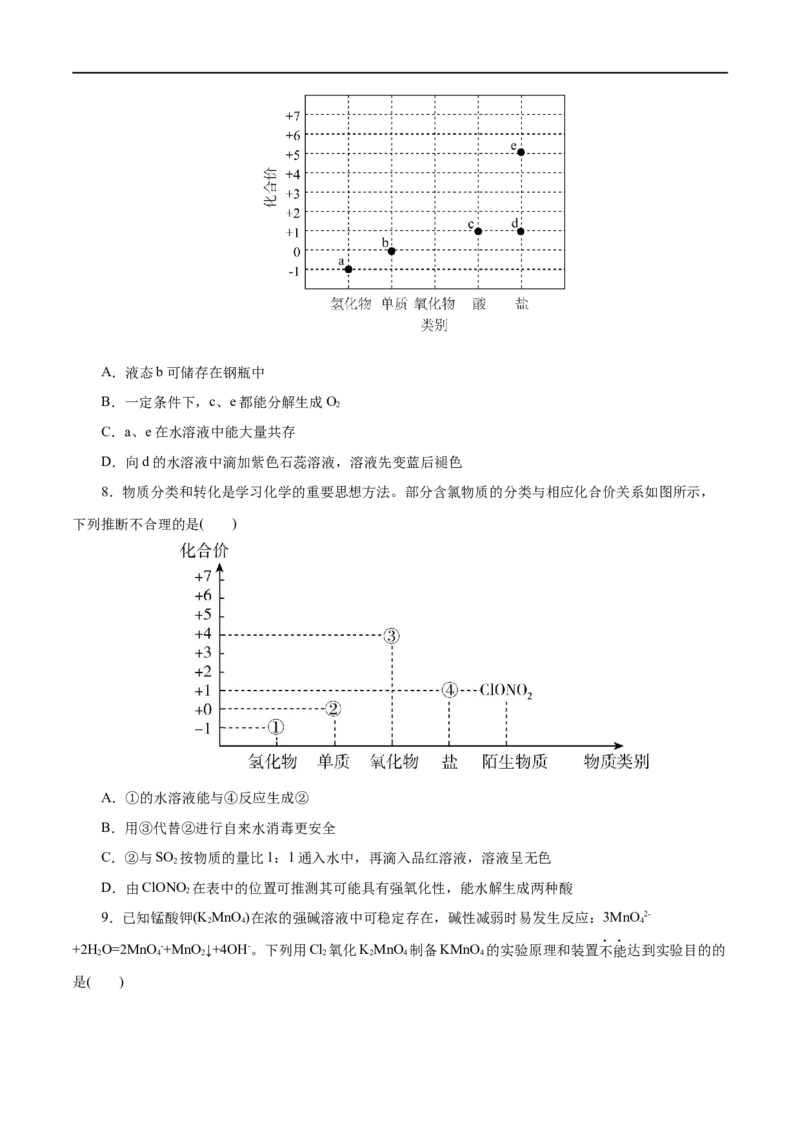
7.部分含氯物质的分类与相应化合价关系如图所示(其中d、e为钾盐)。下列推断不合理的是( )A.液态b可储存在钢瓶中
B.一定条件下,c、e都能分解生成O
2
C.a、e在水溶液中能大量共存
D.向d的水溶液中滴加紫色石蕊溶液,溶液先变蓝后褪色
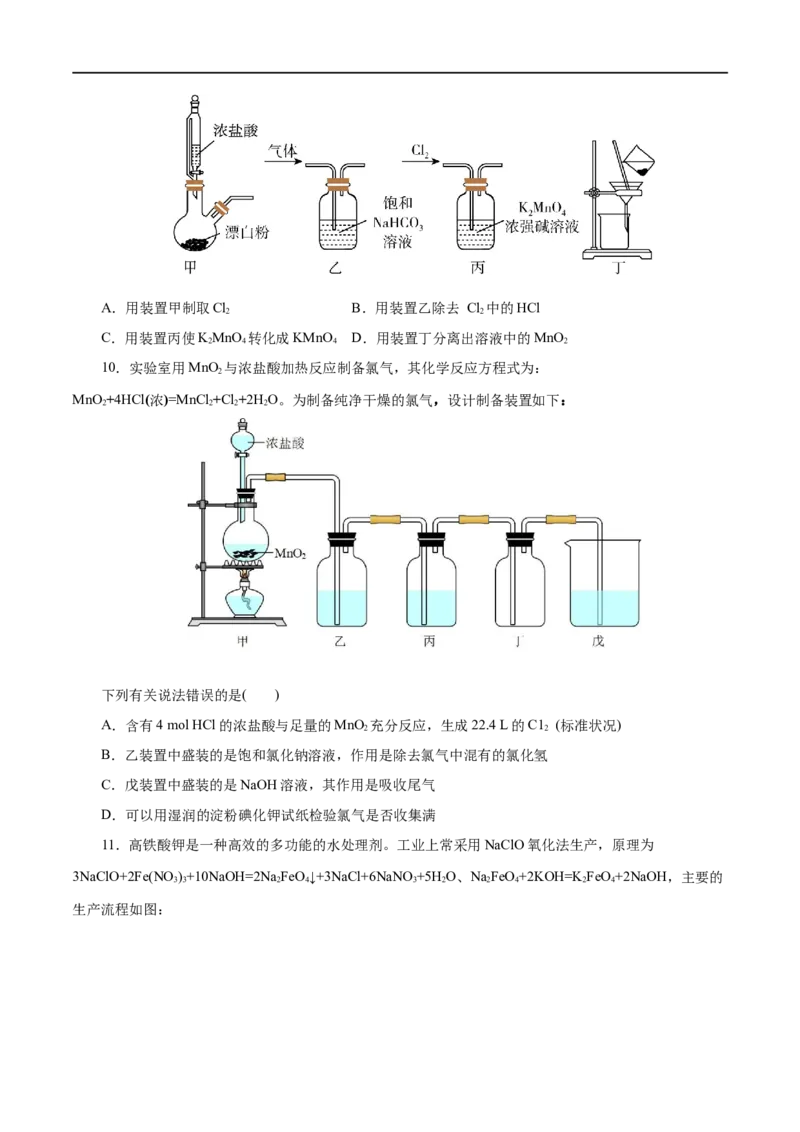
8.物质分类和转化是学习化学的重要思想方法。部分含氯物质的分类与相应化合价关系如图所示,
下列推断不合理的是( )
A.①的水溶液能与④反应生成②
B.用③代替②进行自来水消毒更安全
C.②与SO 按物质的量比1:1通入水中,再滴入品红溶液,溶液呈无色
2
D.由ClONO 在表中的位置可推测其可能具有强氧化性,能水解生成两种酸
2
9.已知锰酸钾(K MnO )在浓的强碱溶液中可稳定存在,碱性减弱时易发生反应:3MnO 2-
2 4 4
+2H O=2MnO -+MnO↓+4OH-。下列用Cl 氧化KMnO 制备KMnO 的实验原理和装置不能达到实验目的的
2 4 2 2 2 4 4
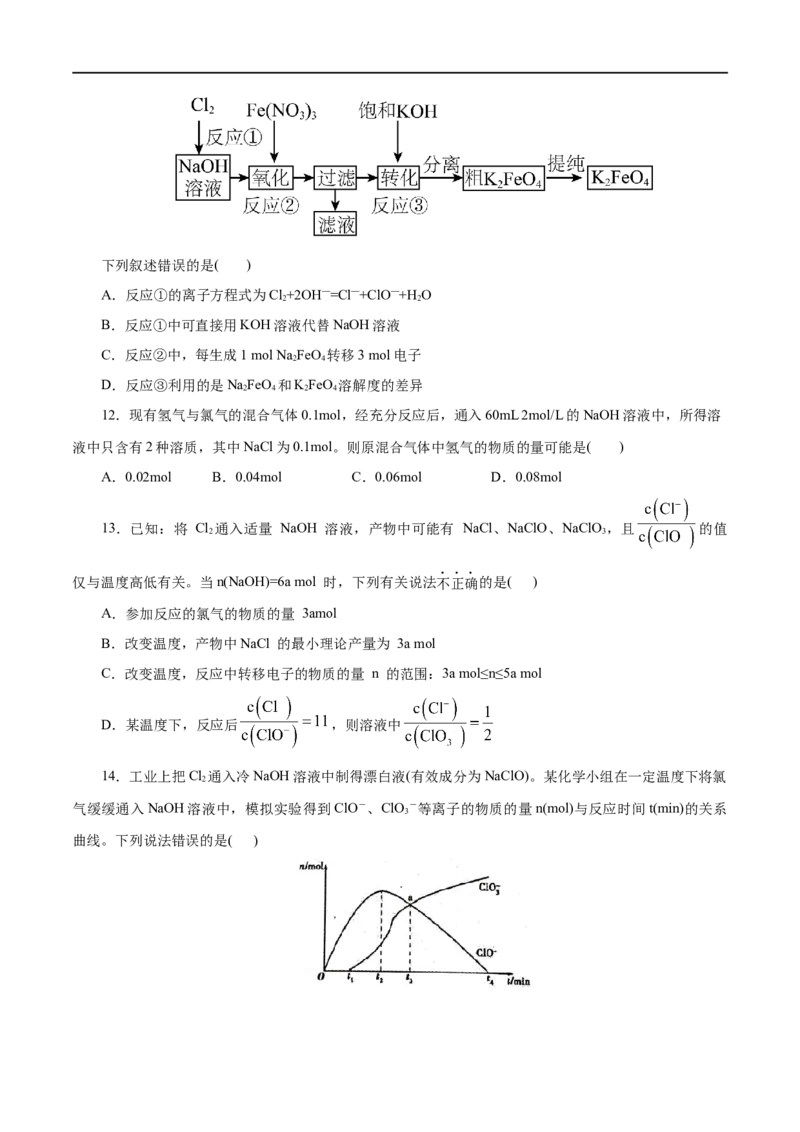
是( )A.用装置甲制取Cl B.用装置乙除去 Cl 中的HCl
2 2
C.用装置丙使KMnO 转化成KMnO D.用装置丁分离出溶液中的MnO
2 4 4 2
10.实验室用MnO 与浓盐酸加热反应制备氯气,其化学反应方程式为:
2
MnO +4HCl(浓)=MnCl +Cl+2HO。为制备纯净干燥的氯气,设计制备装置如下:
2 2 2 2
下列有关说法错误的是( )
A.含有4 mol HCl的浓盐酸与足量的MnO 充分反应,生成22.4 L的C1 (标准状况)
2 2
B.乙装置中盛装的是饱和氯化钠溶液,作用是除去氯气中混有的氯化氢
C.戊装置中盛装的是NaOH溶液,其作用是吸收尾气
D.可以用湿润的淀粉碘化钾试纸检验氯气是否收集满
11.高铁酸钾是一种高效的多功能的水处理剂。工业上常采用NaClO氧化法生产,原理为
3NaClO+2Fe(NO )+10NaOH=2Na FeO↓+3NaCl+6NaNO +5H O、NaFeO+2KOH=K FeO+2NaOH,主要的
3 3 2 4 3 2 2 4 2 4
生产流程如图:下列叙述错误的是( )
A.反应①的离子方程式为Cl+2OH—=Cl—+ClO—+H O
2 2
B.反应①中可直接用KOH溶液代替NaOH溶液
C.反应②中,每生成1 mol Na FeO 转移3 mol电子
2 4
D.反应③利用的是NaFeO 和KFeO 溶解度的差异
2 4 2 4
12.现有氢气与氯气的混合气体0.1mol,经充分反应后,通入60mL 2mol/L的NaOH溶液中,所得溶
液中只含有2种溶质,其中NaCl为0.1mol。则原混合气体中氢气的物质的量可能是( )
A.0.02mol B.0.04mol C.0.06mol D.0.08mol
13.已知:将 Cl 通入适量 NaOH 溶液,产物中可能有 NaCl、NaClO、NaClO ,且 的值
2 3
仅与温度高低有关。当n(NaOH)=6a mol 时,下列有关说法不正确的是( )
A.参加反应的氯气的物质的量 3amol
B.改变温度,产物中NaCl 的最小理论产量为 3a mol
C.改变温度,反应中转移电子的物质的量 n 的范围:3a mol≤n≤5a mol
D.某温度下,反应后 ,则溶液中
14.工业上把Cl 通入冷NaOH溶液中制得漂白液(有效成分为NaClO)。某化学小组在一定温度下将氯
2
气缓缓通入NaOH溶液中,模拟实验得到ClO-、ClO -等离子的物质的量n(mol)与反应时间t(min)的关系
3
曲线。下列说法错误的是( )A.参加反应所需NaOH与氯气的物质的量之比一定为2:1
B.a点时溶液中n(NaCl):n(NaClO):n(NaClO)=6:1:1
3
C.t~t,ClO-离子的物质的量下降的原因可能是3ClO-=2Cl-+ClO -
2 4 3
D.使用漂白液时,为了增强漂白效果,可以向漂白液中通入二氧化硫