文档内容
第三章 金属及其化合物
第07讲 钠及其重要化合物(精练)
完卷时间:50分钟
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Cl 35.5
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2021·上海奉贤区·高三二模)如图向盛有饱和 溶液的烧杯中,加入小块金属钠。以下说法
错误的是
A.钠浮在液面上四处游动
B.钠熔化成一个光亮的小球
C.恢复到室温时,溶液中的Na+数目减小
D.恢复到室温时, 溶液的浓度增大
【答案】D
【解析】A. 钠投入饱和NaOH溶液中,发生的反应为2Na+2HO===2NaOH+H↑,其现象与钠在水中的反应
2 2
现象相同,故钠浮在液面上四处游动,A正确;B. 钠投入饱和NaOH溶液中,发生的反应为2Na+
2H2O===2NaOH+H2↑,其现象与钠在水中的反应现象相同,故钠熔化成一个光亮的小球,B正确;C. 原溶
液是饱和的,反应消耗水,析出NaOH固体,故Na+数目减少,故C正确;D. 原溶液是饱和的,反应消耗水,
析出NaOH固体,恢复到室温,溶液仍未饱和溶液,NaOH 溶液的浓度不变,故D错误;故选D。
2.(2021·重庆高三一模)化学与生产、生活密切相关,下列物质用途不正确的是
A.次氯酸钠:漂白剂 B.碳酸氢钠:候氏制碱法的初始原料
C.硅酸钠:木材防火剂 D.过氧化钠:呼吸面具的供氧剂
【答案】B
【解析】A.次氯酸钠具有氧化性,是家庭常用的漂白剂,故A正确;B.侯氏制碱法的初始原料是 、
、 和 ,反应先生成碳酸氢钠,受热分解后得到纯碱碳酸钠,故B错误;C.硅酸钠不易燃,常用作木材防火剂,故C正确;D.过氧化钠与水、二氧化碳均能反应生成氧气,可以作为呼吸面具的供氧
剂,故D正确;故选B。
3.(2020·吉林油田第十一中学高三月考)关于NaO和NaO 的叙述正确的是
2 2 2
A.等物质的量时所含阴离子数目相同 B.颜色相同
C.所含化学键类型相同 D.化合物种类不同
【答案】A
【解析】A.NaO阴离子是O2-离子,NaO 阴离子是O2-离子,等物质的量时所含阴离子数目相同,故A正确;
2 2 2 2
B.NaO固体为白色,NaO 固体为淡黄色,故B错误;C.NaO中含有离子键,NaO 中含有离子键和共价键,
2 2 2 2 2 2
故C错误;D.NaO和NaO 都属于金属氧化物,故D错误;故答案选A。
2 2 2
4.(2021·上海虹口区·高三二模)测定一定质量小苏打中NaHCO 的含量(杂质为NaCl),下列实验方案
3
不可行的是
A.加热至恒重,称量剩余固体质量
B.加入足量稀硫酸,测定生成气体的体积
C.溶解后以甲基橙为指示剂,用标准盐酸溶液滴定
D.溶解后加入足量CaCl 溶液,过滤、洗涤、干燥后称量沉淀质量
2
【答案】D
【解析】A.NaHCO 受热易分解生成碳酸钠、水和二氧化碳,所以通过加热分解利用差量法即可计算出
3
NaHCO 的含量,故A可行;B.混合物中NaHCO 与足量稀硫酸充分反应,会生成水和二氧化碳,所以逸出的
3 3
气体是二氧化碳,测定生成气体的体积,能测定NaHCO 的含量,故B可行;C.NaHCO 溶液呈碱性,用盐酸
3 3
滴定 NaHCO 溶液,NaHCO 反应完成时,滴入盐酸,溶液显酸性,甲基橙由黄色变为橙色,可用消耗的标准
3 3
盐酸溶液的量来计算NaHCO 的含量,故C可行;D.CaCl 与NaHCO 不发生反应,没有沉淀产生,故D不可
3 2 3
行;故选:D。
5.(2021·辽宁沈阳市·高三一模)某些氧化物在一定条件下能与 反应,且反应极有规律,如
, 。据此判断下列反应方程式错误的是
A. B.
C. D.
【答案】A
【解析】根据题给信息可知:NaO 可与某些元素的最高价氧化物反应,生成对应的盐(或碱)和O,NaO 具
2 2 2 2 2有强氧化性,与所含元素不是最高价态的氧化物反应时,生成其最高价的盐,而不生成O。
2
A.NO 中的氮也不是最高价,所以不产生氧气,不符合上述规律,故A错误;B.NO 中N元素的化合价为
2 3 2
+4价,不是最高价态,与NaO 反应时不生成O,反应的化学方程式为NaO+2NO=2NaNO,故B正确;C.
2 2 2 2 2 2 3
NO 中N元素的化合价为+5价,是最高价态,与NaO 反应时生成O,反应的化学方程式为
2 5 2 2 2
2NaO+2NO═4NaNO+O,故C正确;D.MnO 中Mn元素的化合价为+7价,处于最高价态,与NaO 反应时
2 2 2 5 3 2 2 7 2 2
生成O,反应的化学方程式为 ,故D正确;故选A。
2
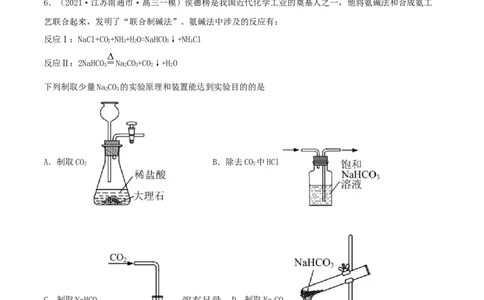
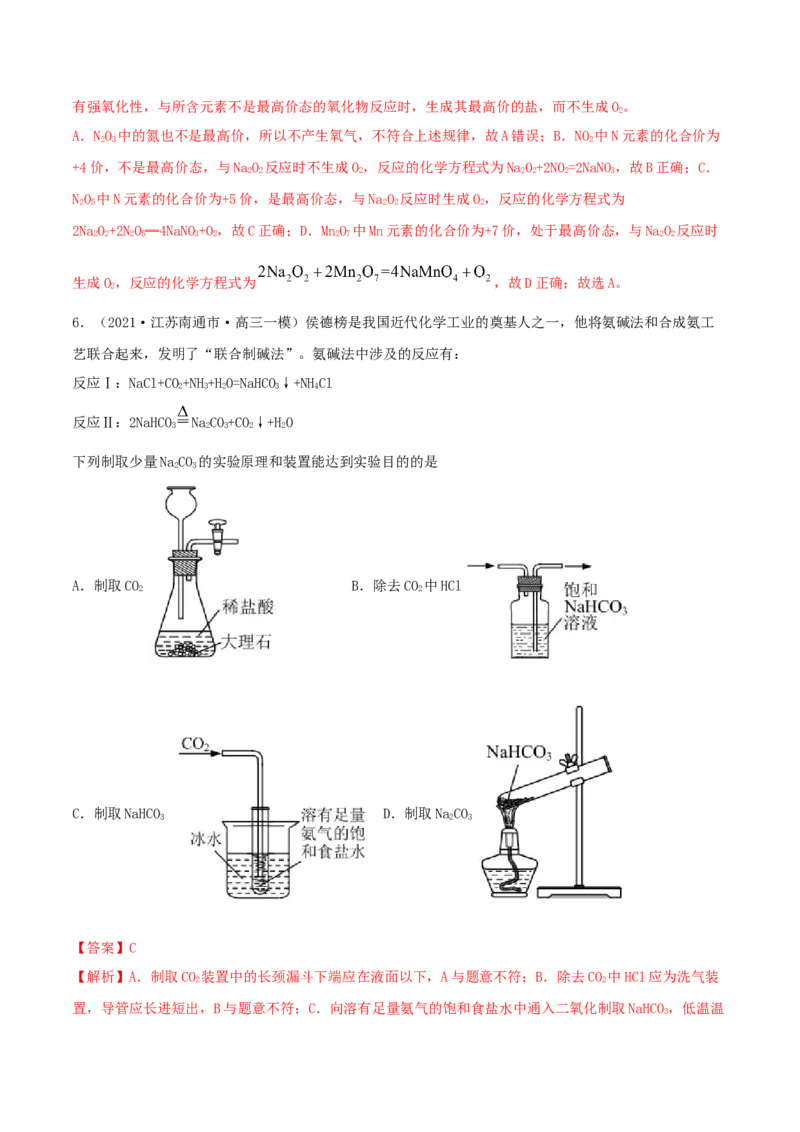
6.(2021·江苏南通市·高三一模)侯德榜是我国近代化学工业的奠基人之一,他将氨碱法和合成氨工
艺联合起来,发明了“联合制碱法”。氨碱法中涉及的反应有:
反应Ⅰ:NaCl+CO+NH+HO=NaHCO↓+NHCl
2 3 2 3 4
反应Ⅱ:2NaHCO NaCO+CO↓+HO
3 2 3 2 2
下列制取少量NaCO 的实验原理和装置能达到实验目的的是
2 3
A.制取CO B.除去CO 中HCl
2 2
C.制取NaHCO D.制取NaCO
3 2 3
【答案】C
【解析】A.制取CO 装置中的长颈漏斗下端应在液面以下,A与题意不符;B.除去CO 中HCl应为洗气装
2 2
置,导管应长进短出,B与题意不符;C.向溶有足量氨气的饱和食盐水中通入二氧化制取NaHCO,低温温
3度可降低NaHCO 溶解度,生成更多的NaHCO,C符合题意;D.加热NaCO 固体应试管口略低于试管底部,
3 3 2 3
D与题意不符;答案为C。
7.(2021·上海杨浦区·高三一模)为测定某NaO 试样(含少量NaO)中NaO 的质量分数,设计如下实验:
2 2 2 2 2
下列分析错误的是
A.操作Ⅰ和Ⅱ都需要玻璃棒 B.需称量样品和NaCl的质量
C.操作Ⅱ若损失部分固体,测定结果偏大 D.若溶液转移不完全,测定结果偏小
【答案】D
【解析】有题干信息可知,操作Ⅰ是让试样和盐酸充分反应,2NaO+4HCl=4NaCl+2HO+O↑,
2 2 2 2
NaO+2HCl=2NaCl+HO,操作Ⅱ是蒸发浓缩,然后冷却结晶,称量所得到的固体NaCl,设试样中NaO 的物
2 2 2 2
质的量为nmol,NaO的物质的量为nmol,则有78n+62n=m(试样) 58.5(2n+2n)=m(NaCl),解联合方程
1 2 2 1 2 1 2
即可求出n= ,也就能求出NaO 的质量分数。
1 2 2
A.操作Ⅰ用玻璃棒搅拌,加快反应速率并使反应进行更完全,操作Ⅱ用玻璃棒则可防止暴沸,A正确;
B.有分析可知,要求出NaO 的质量分数,需称量样品和NaCl的质量,B正确;C.有分析可求出,n=
2 2 1
,故操作Ⅱ若损失部分固体,导致m(NaCl)偏小,则n 的值偏大,故NaO 的质
1 2 2
量分数测定结果偏大,C正确;D.由C项分析可知,若溶液转移不完全,导致m(NaCl)偏小,则n 的值偏
1
大,故NaO 的质量分数测定结果偏大,D错误;故答案为:D。
2 2
8.(2020·莒南第二中学高三月考)探究NaO 与水的反应,实验如图:(已知:HO H++ 、
2 2 2 2
H++ )下列分析不正确的是A.①、⑤中产生的气体能使带火星的木条复燃
B.①、④中均发生了氧化还原反应和复分解反应
C.②、⑤中KMnO 与MnO 的作用不同,产生气体的量也不同
4 2
D.通过③能比较酸性:HCl>HO
2 2
【答案】D
【解析】过氧化钠和水反应生成气体为氧气,反应后的溶液加入高锰酸钾酸性溶液,生成气体,且高锰酸
钾溶液褪色,说明过氧化钠与水反应生成过氧化氢,可被高锰酸钾氧化生成氧气,加入氯化钡生成BaO 沉
2
淀,加入稀硫酸生成硫酸钡沉淀和HO,加入二氧化锰,可分解生成氧气。
2 2
A.试管①中过氧化钠与水反应最终生成氢氧化钠和氧气,试管⑤中过氧化氢在二氧化锰催化作用下分解
产生水和氧气,①、⑤中产生的气体能使带火星的木条复燃,故A正确;B.①中的反应机理可以认为过氧
化钠与水反应生成氢氧化钠和过氧化氢,过氧化氢分解产生水和氧气;④中BaO 沉淀,加入稀硫酸生成硫
2
酸钡沉淀和HO,过氧化氢分解产生水和氧气,均发生氧化还原反应,均为复分解反应,故B正确;C.②、
2 2
⑤中KMnO 与MnO 的作用不同,②中过氧化氢被KMnO 氧化生成氧气,⑤中过氧化氢在二氧化锰催化条件下
4 2 4
自身发生氧化还原反应生成氧气,产生气体的量也不同,故C正确;D.③说明BaO 不溶于盐酸,没有生
2
成可溶性的钡盐,不能用于比较酸性强弱,且盐酸为强酸,由题中信息可知过氧化氢为弱酸,故D错误;
答案选D。
9.(2020·上海奉贤区·高三二模)在生活中 NaCO 和NaHCO 都可作食用碱。下列对其性质的描述用化
2 3 3
学方程式或离子方程式表示正确的是
A.NaHCO 可作发酵粉:2NaHCO NaCO + CO↑ + HO
3 3 2 3 2 2
B.饱和NaCO 溶液中通入CO: CO2- +CO+ HO → HCO-
2 3 2 3 2 2 3
C.NaCO 溶液呈碱性:CO2-+ 2HO → HCO+ 2OH-
2 3 3 2 2 3
D.饱和NaCO 溶液除去CHCOOCH 中的CHCOOH:CO2- + 2H+ →CO↑ + HO
2 3 3 2 5 3 3 2 2
【答案】A
【解析】A.NaHCO 可作发酵粉的原理是利用其分解产生CO,A正确;B.因为NaCO 的溶解度大于
3 2 2 3
NaHCO,对于饱和NaCO 溶液,转化成的NaHCO 溶液则是过饱和的,所以会有晶体析出(沉淀生成),正
3 2 3 3确的离子方程式应该是:2Na++CO2- +CO+ HO =2NaHCO ,B错误;C.NaCO 溶液呈碱性是因为CO2-的水
3 2 2 3 2 3 3
解,但其水解要分布写,且第一步为主,CO2-+ HO HCO-+ OH-,C错误;D.CHCOOH是弱酸,写
3 2 3 3
离子方程式时候不能拆,D错误;答案选A。
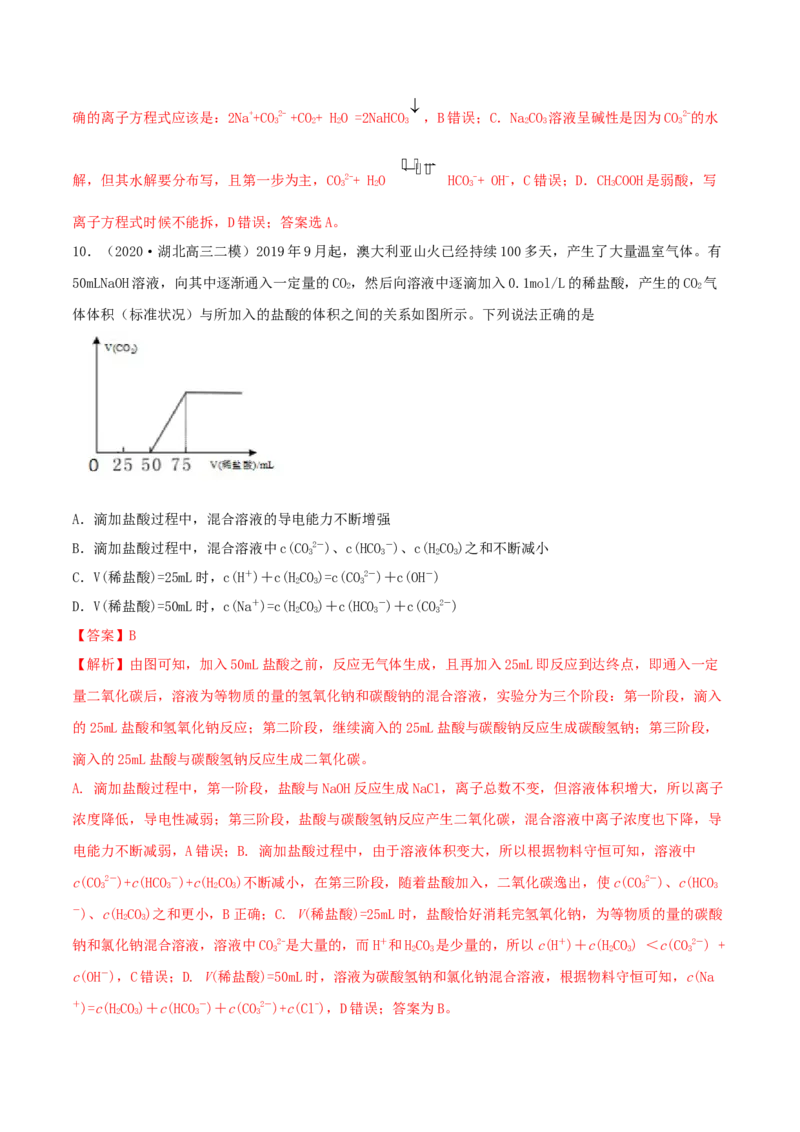
10.(2020·湖北高三二模)2019年9月起,澳大利亚山火已经持续100多天,产生了大量温室气体。有
50mLNaOH溶液,向其中逐渐通入一定量的CO,然后向溶液中逐滴加入0.1mol/L的稀盐酸,产生的CO 气
2 2
体体积(标准状况)与所加入的盐酸的体积之间的关系如图所示。下列说法正确的是
A.滴加盐酸过程中,混合溶液的导电能力不断增强
B.滴加盐酸过程中,混合溶液中c(CO2-)、c(HCO-)、c(HCO)之和不断减小
3 3 2 3
C.V(稀盐酸)=25mL时,c(H+)+c(HCO)=c(CO2-)+c(OH-)
2 3 3
D.V(稀盐酸)=50mL时,c(Na+)=c(HCO)+c(HCO-)+c(CO2-)
2 3 3 3
【答案】B
【解析】由图可知,加入50mL盐酸之前,反应无气体生成,且再加入25mL即反应到达终点,即通入一定
量二氧化碳后,溶液为等物质的量的氢氧化钠和碳酸钠的混合溶液,实验分为三个阶段:第一阶段,滴入
的25mL盐酸和氢氧化钠反应;第二阶段,继续滴入的25mL盐酸与碳酸钠反应生成碳酸氢钠;第三阶段,
滴入的25mL盐酸与碳酸氢钠反应生成二氧化碳。
A. 滴加盐酸过程中,第一阶段,盐酸与NaOH反应生成NaCl,离子总数不变,但溶液体积增大,所以离子
浓度降低,导电性减弱;第三阶段,盐酸与碳酸氢钠反应产生二氧化碳,混合溶液中离子浓度也下降,导
电能力不断减弱,A错误;B. 滴加盐酸过程中,由于溶液体积变大,所以根据物料守恒可知,溶液中
c(CO2-)+c(HCO-)+c(HCO)不断减小,在第三阶段,随着盐酸加入,二氧化碳逸出,使c(CO2-)、c(HCO
3 3 2 3 3 3
-)、c(HCO)之和更小,B正确;C. V(稀盐酸)=25mL时,盐酸恰好消耗完氢氧化钠,为等物质的量的碳酸
2 3
钠和氯化钠混合溶液,溶液中CO2-是大量的,而H+和HCO 是少量的,所以c(H+)+c(HCO) <c(CO2-) +
3 2 3 2 3 3
c(OH-),C错误;D. V(稀盐酸)=50mL时,溶液为碳酸氢钠和氯化钠混合溶液,根据物料守恒可知,c(Na
+)=c(HCO)+c(HCO-)+c(CO2-)+c(Cl-),D错误;答案为B。
2 3 3 311.(2020·河南郑州市·郑州一中高三开学考试)充分加热如图所示的密闭容器中放置有固体试剂的两
个位置, 若钠与氧化银均反应完全且恢复到原来的温度,U形管左右两侧液面相平。下列有关说法中错误
的是
A.反应前后装置内空气的成分保持不变
B.反应前装置内钠与AgO物质的量之比为2:1
2
C.热稳定性:生成的钠的氧化物强于Ag O
2
D.反应后有淡黄色固体生成
【答案】B
【解析】A.U形管左右两侧液面相平,这说明压强不变,装置内钠与氧气反应,消耗掉的氧气与AgO分解
2
生成的氧气的量相等,故A正确;B.钠与氧气反应:2Na+O 2NaO,氧化银受热分解:2AgO
2 2 2 2
4Ag+O↑,U形管左右两侧液面相平,消耗掉的氧气与AgO分解生成的氧气的量相等,装置内钠与AgO物
2 2 2
质的量比为1:1,故B错误;C.同一密闭容器中,氧化银受热分解,钠与氧气反应,说明钠的氧化物强
于AgO,故C正确;D.钠与氧气反应:2Na+O 2NaO,生成过氧化钠,有淡黄色固体生成,故D正确;
2 2 2 2
故答案为B。
12.(2010·江西上高县·高三一模)由NO、H、CO 组成的混合气体,通过足量的NaO 充分反应后,再
2 2 2 2
用电火花引燃使其充分反应后,最终只得到质量分数为70%的硝酸,无其他气体剩余。则原混合气体中
NO、H、CO 的体积比
2 2
A.2:4:7 B.2:4:5 C.2:4:3 D.3:5:8
【答案】A
【解析】涉及的反应有2NaO+2CO=2NaCO+O,2H+O=2HO,4NO+3O+2HO=4HNO,得到浓度为70%的硝酸
2 2 2 2 3 2 2 2 2 2 2 3
溶液,设硝酸为70g,则水为30g,则有n(HNO)= = mol,n(HO)= = mol,则:
3 2所以n(NO)= mol,
n(H)=n(HO)= mol+ mol= mol,
2 2
n(O)= mol
2 2
n(O)= n(O)+ n(O)= mol+ × mol= mol,
2 1 2 2 2
根据2NaO+2CO=2NaCO+O,
2 2 2 2 3 2
2 1
n(CO) mol
2
n(CO)= 2n(O)=2× mol= mol,
2 2
则n(NO):n(H):n(CO)= mol: mol: mol=2:4:7,故答案为A。
2 2
二、主观题(共3小题,共40分)
13.(2021·河南信阳市·高三零模)(16分)大苏打 、苏打、小苏打被称为“苏氏
三兄弟”。它们在生活、生产中有广泛应用。
(1)工业上,将 和 以 的物质的量之比配成溶液。再通入 可制取 ,同时放出 ,写出该反应的化学方程___________。 溶液在空气中久置,会生成浅黄色物质,经测定该
物质具有与过氧化钠相似的结构,该物质的电子式为___________。
(2) 标准溶液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高。用离子方程式表示
其原因___________。
(3)下列关于苏打和小苏打的说法正确的是___________(选填字母序号)。
A.纯碱是一种重要的化工原料,在玻璃、肥皂、造纸等工业中都有重要的应用
B.苏打和小苏打的相互转化属于可逆反应
C.苏打(含氯化钠杂质)可用滴定法测苏打的质量分数,使用石蕊溶液做指示剂更准确
D.牙膏中加入小苏打可以让小苏打颗粒直接摩擦牙齿,帮助清洁牙垢
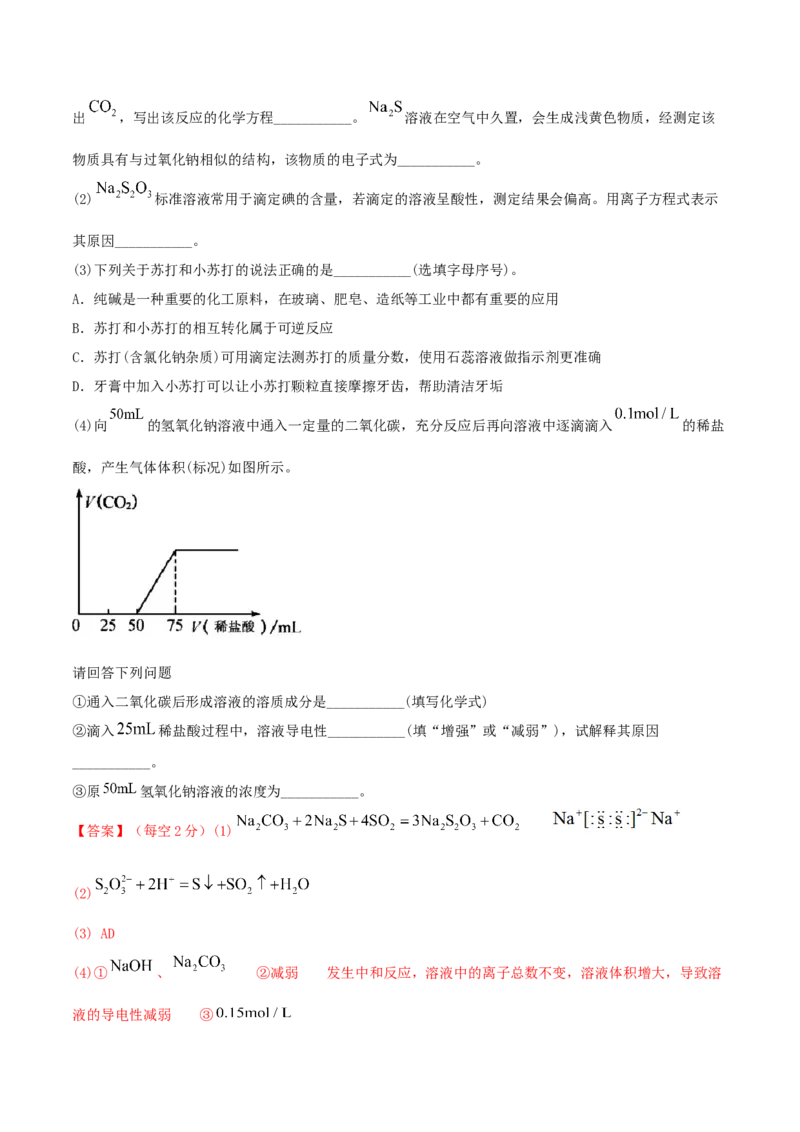
(4)向 的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后再向溶液中逐滴滴入 的稀盐
酸,产生气体体积(标况)如图所示。
请回答下列问题
①通入二氧化碳后形成溶液的溶质成分是___________(填写化学式)
②滴入 稀盐酸过程中,溶液导电性___________(填“增强”或“减弱”),试解释其原因
___________。
③原 氢氧化钠溶液的浓度为___________。
【答案】(每空2分)(1)
(2)
(3) AD
(4)① 、 ②减弱 发生中和反应,溶液中的离子总数不变,溶液体积增大,导致溶
液的导电性减弱 ③【解析】(1)因为反应的物质的量之比等于化学计量数之比, 和 的物质的量之比为 ,所
以方程式为 ,因为浅黄色物质与过氧化钠相似的结构,该
物质的电子式为 ;
(2)酸性条件下, 会发生歧化反应 ;
(3) A.纯碱是一种重要的化工原料,可以制备玻璃、肥皂,在造纸等工业中也有重要的应用,A正确;
B.苏打和小苏打的相互转化是在不同条件下进行的,不是可逆反应B错误;C.石蕊不能用作滴定反应的
指示剂,C错误;D.牙膏中加入小苏打可以让小苏打颗粒直接摩擦牙齿,帮助清洁牙垢,D正确;故选
AD。
(4)由图像0到50为产生气体,50到75产生气体,可以知道溶质为 、 ,0到25时主要发
生的反应为 ,溶液中的离子总数不变,溶液体积增大,导致溶液的导电性减弱,③当盐
酸加入75mL时,溶液恰好生成氯化钠,所以氢氧化钠的物质的量等于氯化氢的物质的量,所以
,所以物质的量浓度为:
。
14.(2021·上海松江区·高三一模)(12分)为测定NaCO·10HO、NaHCO 的混合物中NaHCO 的含量,
2 3 2 3 3
设计如下实验:取一定质量的混合物,通过测量反应前后③装置质量的变化,测定该混合物中NaHCO 的质
3
量分数。
完成下列问题:
(1)U型管①②③盛装的均为固态物质,可选试剂依次为______________(选填编号)。U型管③吸收的气体
为___________。a.碱石灰 b.无水氯化钙 c.无水硫酸铜
(2)干燥管中无水硫酸铜的作用是___________。实验装置最后的干燥管中碱石灰的作用___________。
(3)实验停止加热后,继续通入空气一段时间的原因是___________。
(4)再设计一种测定上述混合物中NaHCO 含量的方案,并注明需要测定的物理量___________。
3
【答案】(每空2分)(1)a b a CO
2
(2)检验水蒸气是否已经被完全除去
(3)防止空气中的CO 和水蒸气被③吸收,导致③质量增大 将反应产生的CO 全部赶入装置③
2 2
(4)方案一:取样品m克配成100mL溶液,取出20mL溶液用一定浓度标准盐酸进行滴定(用甲基橙或酚酞作
指示),消耗盐酸VmL,数据处理或方案二:取样品m 克,置于已知质量的坩埚中灼烧、冷却、称量,并做
1
恒重操作得m 克,数据处理。
2
【解析】根据实验装置图可知,该实验方案的原理是:加热样品,发生反应NaCO·10HO
2 3 2
NaCO+10HO、2NaHCO NaCO+HO+CO↑,通过测定样品受热产生的CO 的质量确定NaHCO 的含量;为了
2 3 2 3 2 3 2 2 2 3
使CO 测量准确,加热样品前要先通入空气,经U型管①吸收空气中的CO 和HO(g),用不含CO 和HO(g)
2 2 2 2 2
的空气排尽装置中的空气,然后对样品加热,使样品充分反应,U型管②吸收反应生成的HO(g),无水硫
2
酸铜用于检验反应生成的HO(g)是否被完全吸收,U型管③吸收反应生成的CO,U型管③反应前后增加的
2 2
质量即为反应生成的CO 的质量;为使反应生成的CO 在U型管③中全部被吸收,停止加热后需继续通入一
2 2
段时间的空气将反应产生的CO 全部赶入U型管③中;为防止外界空气的CO 和HO(g)进入U型管③中,最
2 2 2
后干燥管中的碱石灰用于吸收外界空气的中CO 和水蒸气;
2
(1) U型管①②③盛装的均为固态物质,根据分析,U型管①中试剂用于吸收空气中的CO 和HO(g),选用
2 2
碱石灰,选a;U型管②中试剂用于吸收反应生成的HO(g)、不吸收CO,选用无水CaCl,选b;U型管③
2 2 2
中试剂用于吸收反应生成的CO,选用碱石灰,选a;故答案为:a;b;a;CO。
2 2
(2)为使CO 的测量准确,U型管②必须将反应生成的HO(g)完全吸收,故干燥管中无水硫酸铜的作用是检
2 2
验水蒸气是否已经被完全除去,若被完全除去,则无水硫酸铜不变蓝;实验装置最后的干燥管中碱石灰的
作用是防止外界空气中的CO 和水蒸气被③吸收,导致③质量增大;故答案为:检验水蒸气是否已经被完
2
全除去;防止空气中的CO 和水蒸气被③吸收,导致③质量增大。
2
(3)停止加热后,有部分CO 残留在硬质玻璃管、U型管②、导管中等,继续通入空气一段时间可将反应产
2
生的CO 全部赶入装置③,使反应生成的CO 全部被③中碱石灰吸收;故答案为:将反应产生的CO 全部赶
2 2 2入装置③。
(4)常用的测定混合物含量的实验方法有:滴定分析法、重量分析法等;根据NaCO·10HO和NaHCO 的性
2 3 2 3
质,可采用滴定分析法,实验方案为:取样品m克配成100mL溶液,取出20mL溶液用一定浓度标准盐酸进
行滴定(用甲基橙或酚酞作指示),消耗盐酸VmL,数据处理;也可采用重量分析法,实验方案为:取样品
m 克,置于已知质量的坩埚中灼烧、冷却、称量,并做恒重操作得m 克,数据处理;故答案为:方案一:
1 2
取样品m克配成100mL溶液,取出20mL溶液用一定浓度标准盐酸进行滴定(用甲基橙或酚酞作指示),消耗
盐酸VmL,数据处理或方案二:取样品m 克,置于已知质量的坩埚中灼烧、冷却、称量,并做恒重操作得
1
m 克,数据处理。
2
15.(2020·上海宝山区·高三二模)(12分)某种含有少量氧化钠的过氧化钠试样(已知试样质量为
1.560g、锥形瓶和水的质量为190.720g),利用如图装置测定混合物中NaO 的质量分数,每隔相同时间
2 2
读得电子天平的数据如下表:
(1)写出NaO 和HO反应的化学方程式_______。
2 2 2
(2)计算过氧化钠质量分数时,除了试样的质量,锥形瓶和水的质量,还必需的数据是______,不必作
第6次读数的原因是______。
(3)根据上述数据,过氧化钠的质量分数是_____(保留2位小数)。
(4)测定上述样品(1.560g)中NaO 质量分数的另一种方案,其操作流程如图:
2 2
①操作Ⅰ的名称是_____。
②需直接测定的物理量是_____。
③操作Ⅱ需要的仪器除了酒精灯,还需要_____(固定、夹持仪器除外)。
④在转移溶液时,如溶液转移不完全,则NaO 质量分数的测定结果_____(填“偏大”、“偏小”或“不
2 2
变”)。
【答案】(除标注外,每空2分)(1)2NaO+2HO=4NaOH+O↑
2 2 2 2(2)第4次或第5次的读数 第5次与第4次的读数相同,锥形瓶内质量已达恒重
(3) 0.84
(4)①溶解(1分)②生成NaCl的质量(1分)③玻璃棒、蒸发皿(1分)④偏大(1分)
【解析】(1)NaO 和HO反应的化学方程式:2NaO+2HO=4NaOH+O↑;
2 2 2 2 2 2 2
(2)计算过氧化钠质量分数时,应用过氧化钠完全反应的数据,根据称量的锥形瓶+水+试样总质量变化
计算生成氧气的质量,根据氧气的质量计算过氧化钠的质量,故需要知道试样的质量、锥形瓶+水的质量,
还有第4次或第5次读数;由表中数据可知,第4、5次读数相等,锥形瓶内的质量已达到恒重,不必作第
6次读数;
(3)2NaO+2HO=4NaOH+O↑,由反应方程式可知,由于过氧化钠与水反应生成氧气,反应前后质量减少,
2 2 2 2
质量的变化量就是氧气的质量,即m(O)= 1.560g +190.720g-192.010=0.270g,n(O)=
2 2
=0.0084mol,在化学反应中,反应物、生成物的物质的量变化之比等于化学计量数之比,故n(NaO)
2 2
=2(O)=0.0168mol,过氧化钠的质量分数是:
2
=84% ;
(4)①由流程图可知,操作Ⅰ是将样品在稀盐酸中溶解;
②最终蒸发浓缩、冷却结晶得到的晶体为氯化钠,故应测定生成NaCl的质量;
③操作Ⅱ是从溶液中获得的晶体,蒸发浓缩、冷却结晶,需要的仪器有酒精灯、玻璃棒、蒸发皿;
④在转移溶液时,如溶液转移不完全,烧杯内壁沾有少量的氯化钠,测定的氯化钠的质量偏小,样品中钠
元素的质量分数偏低,由于过氧化钠中钠元素的质量分数小于氧化钠中钠元素的质量分数,故过氧化钠的
质量分数偏大。