文档内容
第十讲 铁及其化合物
【基础巩固】
1.我国清代《本草纲目拾遗》中叙述了“铁线粉”:“粤中洋行有舶上铁丝,……日久起销,用刀刮其
销,……,所刮下之销末,名铁线粉”。这里的“铁线粉”是指( )
A.Fe B.FeCl C.FeO D.Fe O
3 2 3
2.(2022·四川德阳模拟)青矾矿石(主要成分为FeSO ·7H O)在《唐本草》中记载:“本来绿色,新出窟未
4 2
见风者,正如琉璃……烧之赤色……”。下列关于FeSO ·7H O的说法正确的是( )
4 2
A.可用于制净水剂 B.溶于水形成无色溶液
C.在干燥空气中稳定存在 D.在空气中加热转化为Fe O
3 4
3.下列关于铁及其化合物的说法正确的是( )
A.FeS 在沸腾炉中与O 反应主要生成SO (2020·浙江7月选考,12C)
2 2 3
B.Mg加入到过量FeCl 溶液中可得Fe(2020·浙江7月选考,12B)
3
C.钢铁在潮湿空气中生锈主要是发生了电化学腐蚀(2020·浙江7月选考,8D)
D.室温下,Fe与浓HSO 反应生成FeSO (2020·江苏,6D)
2 4 4
4.在100 mL 1.00 mol·L-1 HSO 溶液中加入足量铁屑,生成的气体在标准状况下的体积为( )
2 4
A.11.2 L B.6.72 L C.4.48 L D.2.24 L
5.下列有关铁及其化合物的说法正确的是( )
A.Fe(OH) 易被氧化成Fe(OH) ,说明稳定性:Fe(OH) <Fe(OH)
2 3 2 3
B.铁是较活泼的金属,它与卤素单质(X )反应的生成物均为FeX
2 3
C.氢氧化铁与氢碘酸反应:Fe(OH) +3HI===FeI +3HO
3 3 2
D.铁与水蒸气在高温下的反应产物为Fe O 和H
2 3 2
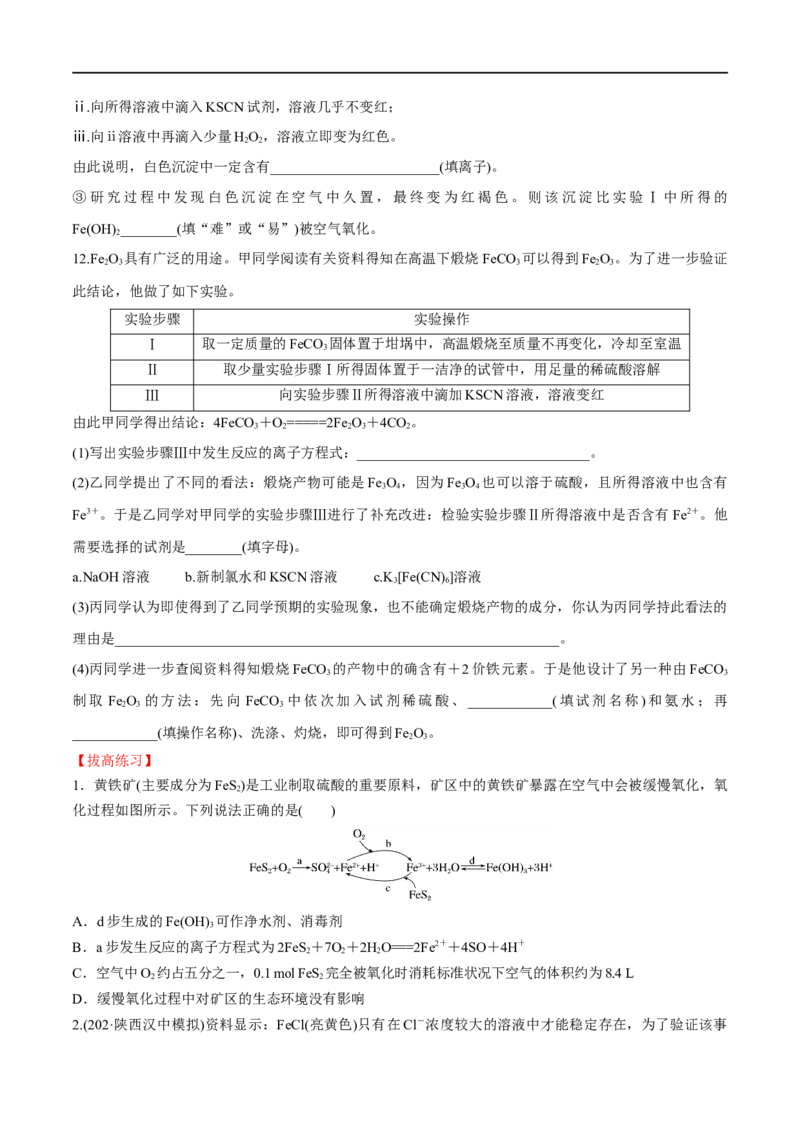
6.已知:普通铁+水蒸气――――→铁的氧化物+氢气,铁的氧化物+氢气――――→“引火铁”+水蒸气,
“引火铁”为颗粒很细、反应活性很高的铁粉。某实验小组使用普通铁粉、20%的盐酸及其他试剂制备
“引火铁”,装置(铁架台、铁夹、铁网、陶土网、加热仪器等略去)如图所示。
关于上述装置和实验,下列分析错误的是( )
A.A、I中加入普通铁粉,G中可加入碱石灰 B.A中生成磁性氧化铁,E中生成“引火铁”
C.需要加热的仪器只有A、E D.D用于收集氢气
7.聚合硫酸铁[Fe(OH)SO ] 能用作净水剂(絮凝剂),可由绿矾(FeSO ·7H O)和KClO 在水溶液中反应得到。
4 n 4 2 3
下列说法不正确的是( )
A.KClO 作氧化剂,每生成1 mol [Fe(OH)SO ] 消耗 mol KClO
3 4 n 3
B.生成聚合硫酸铁后,水溶液的pH增大C.聚合硫酸铁可在水中形成氢氧化铁胶体而净水
D.在相同条件下,Fe3+比[Fe(OH)]2+的水解能力更强
8.下列离子方程式书写正确的是( )
A.铁与稀盐酸反应:Fe+6H+===Fe3++3H↑
2
B.氯气与氯化亚铁溶液反应:Cl+Fe2+===Fe3++2Cl-
2
C.氯化铁溶液与铜反应:3Cu+2Fe3+===2Fe+3Cu2+
D.氯化铁溶液与硫化氢反应:2Fe3++HS===2Fe2++S↓+2H+
2
9.(2023·西安模拟)工业废水中含有的重铬酸根离子(CrO)有毒,必须处理达标后才能排放。工业上常用绿
2
矾(FeSO ·7H O)作处理剂,反应的离子方程式为6Fe2++Cr O+14H+===6Fe3++2Cr3++7HO,下列说法正
4 2 2 2
确的是( )
A.氧化剂与还原剂的物质的量之比为6∶1 B.用绿矾作处理剂,不仅可去除毒性,还可净水
C.酸化试剂可以用盐酸或硫酸 D.不能用草酸溶液代替绿矾作处理剂
10.向含有Cu(NO ) 、Zn(NO ) 、Fe(NO ) 、AgNO 各0.1 mol的混合溶液中加入0.1 mol Fe,充分搅拌后
3 2 3 2 3 3 3
Fe溶解,溶液中不存在Fe3+,同时析出0.1 mol Ag。下列结论错误的是( )
A.氧化性:Zn2+>Cu2+>Fe3+>Ag+ B.Fe3+的氧化性大于Cu2+
C.溶液中Cu2+与Fe2+的物质的量之比为1∶2 D.1 mol Fe可还原2 mol Fe3+
11.实验小组研究二价铁的还原性,设计如下实验。
序号 实验方案 现象
现象a:生成白色沉淀,3 min后沉淀基
Ⅰ
本变为红褐色
现象b:生成白色沉淀,3 min后沉淀颜
Ⅱ
色几乎不变
(1)实验所用的FeSO 溶液由Fe (SO ) 溶液和足量铁粉反应制得,反应的离子方程式是________________。
4 2 4 3
(2)实验Ⅰ中沉淀变为红褐色的化学方程式是_________________________________________。
(3)关于实验Ⅱ中白色沉淀的组成,小组同学展开研究。①已知Fe(HCO ) 在水中不存在。对沉淀组成做出
3 2
如下假设,请补充完整。
假设a:依据NaHCO 溶液显________性,推测白色沉淀可能为Fe(OH) ;
3 2
假设b:白色沉淀可能为________。
②研究白色沉淀组成的实验如下:
ⅰ.取少量白色沉淀,充分洗涤,向其中加入稀硫酸,沉淀完全溶解,产生无色气泡;ⅱ.向所得溶液中滴入KSCN试剂,溶液几乎不变红;
ⅲ.向ⅱ溶液中再滴入少量HO,溶液立即变为红色。
2 2
由此说明,白色沉淀中一定含有________________________(填离子)。
③研究过程中发现白色沉淀在空气中久置,最终变为红褐色。则该沉淀比实验Ⅰ中所得的
Fe(OH) ________(填“难”或“易”)被空气氧化。
2
12.Fe O 具有广泛的用途。甲同学阅读有关资料得知在高温下煅烧FeCO 可以得到Fe O 。为了进一步验证
2 3 3 2 3
此结论,他做了如下实验。
实验步骤 实验操作
Ⅰ 取一定质量的FeCO 固体置于坩埚中,高温煅烧至质量不再变化,冷却至室温
3
Ⅱ 取少量实验步骤Ⅰ所得固体置于一洁净的试管中,用足量的稀硫酸溶解
Ⅲ 向实验步骤Ⅱ所得溶液中滴加KSCN溶液,溶液变红
由此甲同学得出结论:4FeCO+O=====2Fe O+4CO。
3 2 2 3 2
(1)写出实验步骤Ⅲ中发生反应的离子方程式:_________________________________。
(2)乙同学提出了不同的看法:煅烧产物可能是Fe O ,因为Fe O 也可以溶于硫酸,且所得溶液中也含有
3 4 3 4
Fe3+。于是乙同学对甲同学的实验步骤Ⅲ进行了补充改进:检验实验步骤Ⅱ所得溶液中是否含有Fe2+。他
需要选择的试剂是________(填字母)。
a.NaOH溶液 b.新制氯水和KSCN溶液 c.K [Fe(CN) ]溶液
3 6
(3)丙同学认为即使得到了乙同学预期的实验现象,也不能确定煅烧产物的成分,你认为丙同学持此看法的
理由是_______________________________________________________________。
(4)丙同学进一步查阅资料得知煅烧FeCO 的产物中的确含有+2价铁元素。于是他设计了另一种由FeCO
3 3
制取 Fe O 的方法:先向 FeCO 中依次加入试剂稀硫酸、____________(填试剂名称)和氨水;再
2 3 3
____________(填操作名称)、洗涤、灼烧,即可得到Fe O。
2 3
【拔高练习】
1.黄铁矿(主要成分为FeS)是工业制取硫酸的重要原料,矿区中的黄铁矿暴露在空气中会被缓慢氧化,氧
2
化过程如图所示。下列说法正确的是( )
A.d步生成的Fe(OH) 可作净水剂、消毒剂
3
B.a步发生反应的离子方程式为2FeS+7O+2HO===2Fe2++4SO+4H+
2 2 2
C.空气中O 约占五分之一,0.1 mol FeS 完全被氧化时消耗标准状况下空气的体积约为8.4 L
2 2
D.缓慢氧化过程中对矿区的生态环境没有影响
2.(202·陕西汉中模拟)资料显示:FeCl(亮黄色)只有在Cl-浓度较大的溶液中才能稳定存在,为了验证该事实,某实验小组取三份2 mL黄色的工业盐酸分别做了一系列实验,记录如下:
操作 现象
实验Ⅰ:直接滴加2滴KSCN溶液 无明显变化
实验Ⅱ:加10 mL蒸馏水稀释,后滴入2滴浓KSCN溶
稀释后溶液几乎变为无色,加KSCN溶液显红色
液
实验Ⅲ:滴加2滴AgNO 饱和溶液 产生白色沉淀,溶液亮黄色消失
3
下列说法不正确的是( )
A.工业盐酸显黄色是因为其中混有FeCl
B.实验Ⅰ中,未检测到Fe3+
C.实验Ⅲ中,AgNO 溶液稀释了样品是溶液亮黄色消失的主要原因
3
D.通过上述实验,可以证明FeCl只有在Cl-浓度较大的溶液中才能稳定存在
3.(2022·山东淄博模拟)中药材铁华粉的主要成分是醋酸亚铁,检测的流程如图。下列说法错误的是( )
A.气体X中含有醋酸蒸气
B.该铁华粉中可能含有铁单质
C.向滤液中滴入酸性KMnO 溶液,可用于证明Fe2+具有还原性
4
D.产生蓝色沉淀的反应为K++Fe2++[Fe(CN) ]3-===KFe[Fe(CN) ]↓
6 6
4.(2022·陕西铜川模拟)高铁酸钾(K FeO)具有强氧化性,是一种环保、高效、多功能的饮用水处理剂,可
2 4
以用如下流程进行制备。下列说法正确的是( )
A.“酸溶”前,可用热的NaCO 溶液处理铁屑表面的油污
2 3
B.“氧化”过程中反应的离子方程式为2Fe2++O+4H+===2Fe3++2HO
2 2
C.“制备NaFeO”中氧化剂和还原剂的物质的量之比为2∶3
2 4
D.“转化”中析出KFeO 晶体的原因可能是相同条件下其溶解度大于NaFeO
2 4 2 4
5.铁元素是人体重要的微量元素,参与人体血红蛋白的形成,Fe2+易被人体吸收,下列有关铁及其化合物的
说法中正确的是
A.缺铁性贫血症可以服用维生素C将难吸收的Fe3+氧化为Fe2+,促进铁元素的吸收
B.高温下红热的铁与水蒸气反应,可得到红色的氧化铁
C.将过氧化钠投入氯化亚铁溶液中,最终生成白色沉淀
D.FeO不稳定,在空气中加热迅速被氧化成Fe O
2 36.(2023·辽宁·校联考模拟预测)根据氯单质及其化合物在水溶液中的反应书写下列离子方程式,其中不
正确的是( )
A.能证明氧化性 的反应:
B.氯化亚铁和氯气发生化合反应:
C.氯气和过量碳酸钠溶液发生反应:
D.两种盐在水中发生氧化还原反应:
7.(2023·浙江杭州·浙江省临安中学校联考一模)铁及其化合物应用广泛,下列说法正确的是
A.Fe元素位于周期表VIIIB族 B.Fe(SCN) 属于弱电解质
3
C.Fe(SO ) 可用作补血剂 D.Fe元素位于周期表ds区
4 3
8.(2023·广东汕头·统考二模)铁及其化合物在生活中应用广泛,下列有关离子方程式书写正确的是
A.将铁片投入到稀硝酸中:
B.向 溶液中通入少量 :
C.用铁氰化钾溶液检验 :
D.往Fe(SO ) 溶液中加入过量Zn粉:
4 3
9.(2023·广东·高三专题练习)下列有关铁及其化合物转化过程中的离子方程式书写正确的是
A.氧化亚铁溶于稀硝酸:FeO+2H+=Fe2++HO B.铁溶于盐酸:2Fe+6H+ = 2Fe3++3H ↑
2 2
C.醋酸除铁锈:Fe O +6H+ = 2Fe3++3HO D.三氯化铁腐蚀铜板:Cu+2Fe3+=2Fe2++Cu2+
2 3 2
10.(2023·上海金山·统考二模)如图所示是铁及其化合物的价类二维图,下列有关叙述正确的是
A.物质X是Fe O
3 4
B.Fe O→Fe的转化,Fe O 发生氧化反应
2 3 2 3
C.在空气中Z→Y的现象是白色沉淀迅速变成灰绿色,最终变成红褐色
D.可通过复分解反应实现FeCl 和FeCl 的相互转化
2 311.(2023·上海·高三专题练习)铁及其化合物在人类生活中有着极其重要的作用。完成下列填空:
(1)铁的原子结构示意图为 。由此可知,铁是第_______周期元素,铁原子核外3d轨道上共填充
了_______个电子。
(2)古代中国四大发明之一的司南是由天然的磁石制成的,其主要成分是_______(选填编号)。
a.Fe b.FeO c.Fe O d.Fe O
2 3 3 4
(3)FeSO 可以用来净水、治疗缺铁性贫血等,实验室在配制FeSO 溶液时,为了防止FeSO 变质,经常向溶
4 4 4
液中加入铁粉,其原因是_______(用离子方程式表示)。
(4)向新配制的FeSO 溶液中,加入一定量的稀硝酸,发生如下反应:
4
_______Fe2++_______H++_______NO =_______Fe3++_______NO↑+_______H O
2
①配平上述反应_______。
②每生成0.5molNO气体,转移的电子数为_______。
③要检验该反应后的溶液中是否还含有Fe2+,实验方案是_______。
现在可以利用铁氧化物循环裂解水制备氢气,其过程如图所示:
(5)写出反应Ⅲ的平衡常数表达式_______。
(6)写出铁氧化物循环裂解水制氢的总反应的化学方程式:_______。
(7)Fe O 和CO的反应过程与温度密切相关。向某容器中加入Fe O 与CO,当其它条件一定时,达到平衡时
3 4 3 4
CO的体积百分含量随温度的变化关系如图所示。
已知:①Fe
3
O
4
+CO⇌3FeO+CO
2
-Q
1
(Q
1
>0) ②Fe
3
O
4
+4CO⇌3Fe+4CO
2
+Q
2
(Q
2
>0)
推测当温度达到570℃,平衡时CO体积百分含量最高的原因:_______。
12.(2023·重庆九龙坡·统考二模)草酸及其盐在化工生产中具有重要价值,某实验小组做以下实验。Ⅰ.制取草酸
反应原理: (葡萄糖) (浓) ,装置如图(加热和夹
持装置略)。
(1)检验淀粉是否水解完全所用的试剂为____________,装置B的作用是___________。
(2)检查图1装置气密性的方法是_____________________________________。在图1的装置B、C之间添加
装置D,可在D中得到 ,通入气体X是_______。
Ⅱ.三草酸合铁(Ⅲ)酸钾晶体的制取及组成测定
已知:三草酸合铁酸钾晶体 呈绿色,可落于水,难溶于乙醇,见光易分解。
(一)制取晶体
步骤1:向盛有3.000g黄色晶体 的烧杯中,加入 溶液,加热至40℃左右,缓慢
滴入过量的 ,一段时间后,出现红褐色沉淀。
步骤2:加热至沸腾,分两次缓慢加入8~9mL 溶液,至沉淀溶解,得翠绿色溶液。加热浓缩、加
入无水乙醇、结晶,抽滤干燥得7.860g三草酸合铁酸钾晶体。
(3)完成该过程的化学方程式并配平:_______。
_______FeC O ·2H O _______+_______+_______ _______2K [Fe(C O ) ]·3H O
2 4 2 3 2 4 3 2
(4)步骤1中,生成三草酸合铁酸钾与另一种铁的化合物,该化合物为_______(填化学式),步骤2加入无水
乙醇的目的是_______。
(5)实验小组完成实验后发现产率偏低,其主要原因可能是_______。
(二)测定组成
称取5.000g所得的三草酸合铁酸钾晶体配制成250mL溶液。取25.00mL溶液,用0.1000mol/L酸性KMnO
4溶液滴定,终点时消耗KMnO 溶液13.50mL。另取25.00mL溶液,用SnCl —TiCl 联合还原法,将还原为
4 2 3
Fe3+,再用0.1000mol/L酸性KMnO 溶液滴定,终点时消耗KMnO 溶液15.50mL。
4 4
(6)第一次滴定终点时的现象为_______,通过上述实验,测定出该晶体中C O 2-与Fe3+的配位比
2 4
_______。
13.(2023·上海·高三专题练习)铁、铜及其化合物是中学化学中常见化学物质,阅读材料回答问题:
(一)氯化铁是重要的化工原料,FeCl ·6H O的实验室制备流程图如下:
3 2
(1)废铁屑表面往往含有油污,去除废铁屑表面的油污的方法是___________。操作①要用到的玻璃仪器有
玻璃棒、烧杯和___________。
(2)加入含有少量铜的废铁屑比加入纯铁屑反应更快,原因为___________。操作②涉及的过程为:加热浓
缩、___________、过滤、洗涤、干燥。
(3)检验FeCl 稀溶液中是否残留Fe2+的试剂可以是___________。为增大FeCl 溶液的浓度,向稀FeCl 溶液
3 3 3
中加入纯Fe粉后通入Cl 。此过程中发生的主要反应的离子方程式为___________、___________。
2
(二)为测定CuSO 溶液的浓度,某同学设计了如下方案:
4
(4)判断SO 2-沉淀完全的操作为___________。
4
(5)固体质量为w g,则c(CuSO )=___________mol/L。若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测得
4
c(CuSO )___________(填“偏高”、“偏低”或“无影响”)。
4