文档内容
第 10 讲 金属材料及金属矿物的开发利用
目录
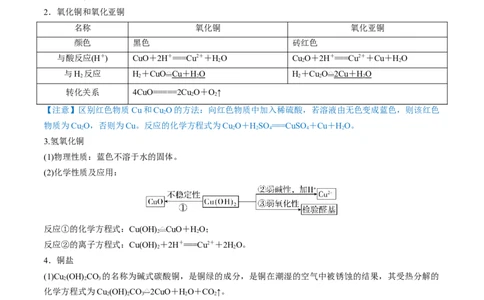
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
第三部分:典型例题剖析
高频考点1 考查铜及其化合物的性质和应用
高频考点2 考查铜及其化合物的制备
高频考点3 考查合金的性质及应用
高频考点4 考查金属矿物的开发与利用
高频考点5 考查以金属及其化合物化工生产为背景的工艺流程分析
正文
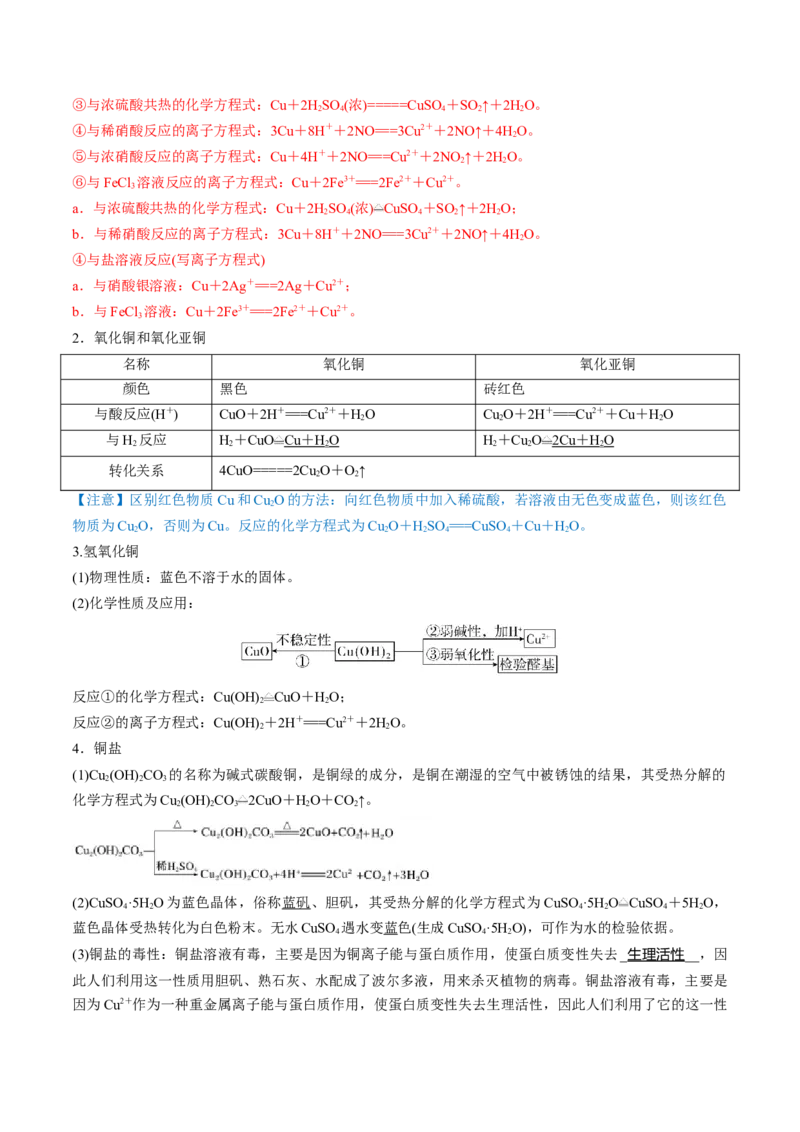
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
知识点一 铜及其化合物
1.单质铜
(1)物理性质:紫红色固体,具有良好的延展性、导热性和导电性。
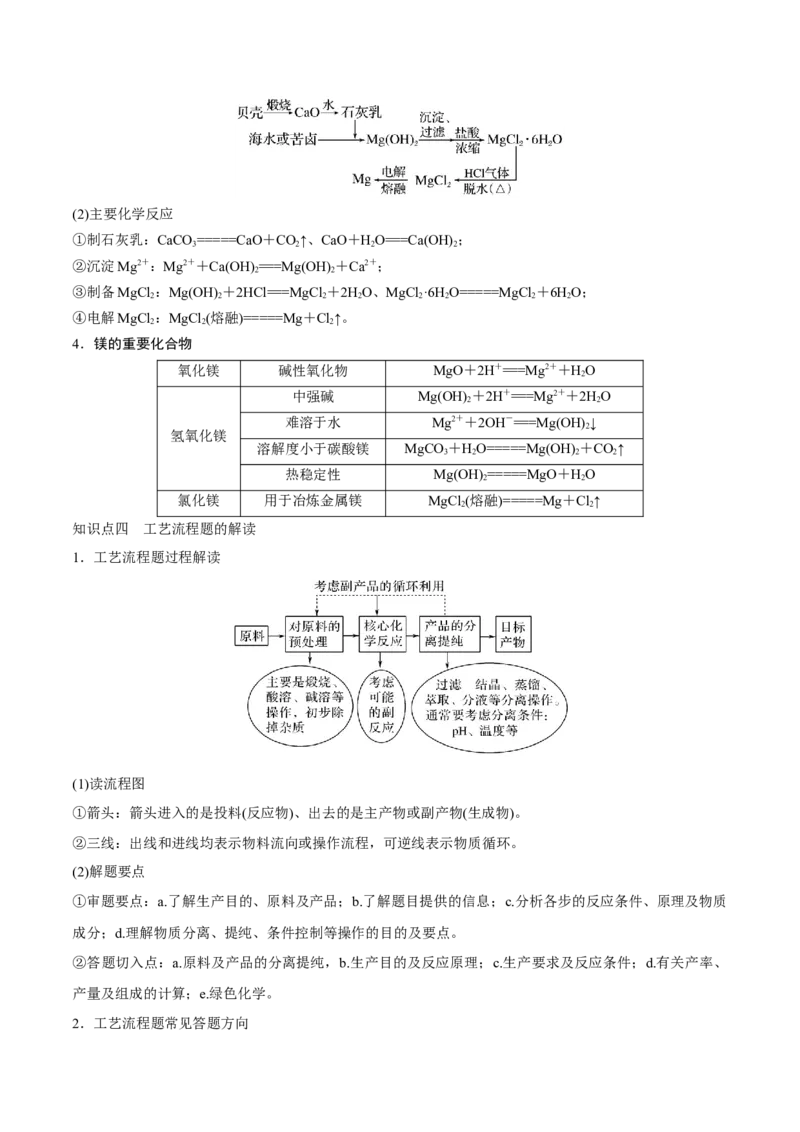
(2)化学性质
①生成铜绿的化学方程式:2Cu+O+CO+HO===Cu (OH) CO(绿色固体)。
2 2 2 2 2 3
②Cu和S反应的化学方程式:2Cu+S=====Cu S。
2③与浓硫酸共热的化学方程式:Cu+2HSO (浓)=====CuSO +SO ↑+2HO。
2 4 4 2 2
④与稀硝酸反应的离子方程式:3Cu+8H++2NO===3Cu2++2NO↑+4HO。
2
⑤与浓硝酸反应的离子方程式:Cu+4H++2NO===Cu2++2NO ↑+2HO。
2 2
⑥与FeCl 溶液反应的离子方程式:Cu+2Fe3+===2Fe2++Cu2+。
3
a.与浓硫酸共热的化学方程式:Cu+2HSO (浓) CuSO +SO ↑+2HO;
2 4 4 2 2
b.与稀硝酸反应的离子方程式:3Cu+8H++2NO===3Cu2++2NO↑+4HO。
2
④与盐溶液反应(写离子方程式)
a.与硝酸银溶液:Cu+2Ag+===2Ag+Cu2+;
b.与FeCl 溶液:Cu+2Fe3+===2Fe2++Cu2+。
3
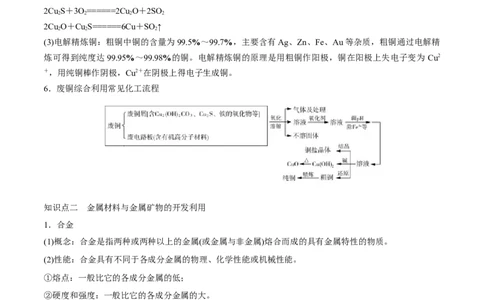
2.氧化铜和氧化亚铜
名称 氧化铜 氧化亚铜
颜色 黑色 砖红色
与酸反应(H+) CuO+2H+===Cu2++HO Cu O+2H+===Cu2++Cu+HO
2 2 2
与H 反应 H+CuO Cu + H O H+Cu O 2Cu + H O
2 2 2 2 2 2
转化关系 4CuO=====2Cu O+O↑
2 2
【注意】区别红色物质Cu和Cu O的方法:向红色物质中加入稀硫酸,若溶液由无色变成蓝色,则该红色
2
物质为Cu O,否则为Cu。反应的化学方程式为Cu O+HSO ===CuSO+Cu+HO。
2 2 2 4 4 2
3.氢氧化铜
(1)物理性质:蓝色不溶于水的固体。
(2)化学性质及应用:
反应①的化学方程式:Cu(OH) CuO+HO;
2 2
反应②的离子方程式:Cu(OH) +2H+===Cu2++2HO。
2 2
4.铜盐
(1)Cu (OH) CO 的名称为碱式碳酸铜,是铜绿的成分,是铜在潮湿的空气中被锈蚀的结果,其受热分解的
2 2 3
化学方程式为Cu (OH) CO 2CuO+HO+CO↑。
2 2 3 2 2
(2)CuSO ·5H O为蓝色晶体,俗称蓝矾、胆矾,其受热分解的化学方程式为CuSO ·5H O CuSO +5HO,
4 2 4 2 4 2
蓝色晶体受热转化为白色粉末。无水CuSO 遇水变蓝色(生成CuSO ·5H O),可作为水的检验依据。
4 4 2
(3)铜盐的毒性:铜盐溶液有毒,主要是因为铜离子能与蛋白质作用,使蛋白质变性失去_生理活性__,因
此人们利用这一性质用胆矾、熟石灰、水配成了波尔多液,用来杀灭植物的病毒。铜盐溶液有毒,主要是
因为Cu2+作为一种重金属离子能与蛋白质作用,使蛋白质变性失去生理活性,因此人们利用了它的这一性质用胆矾、熟石灰、水配成了波尔多液,用来杀灭植物的病毒。
【特别提醒】(1)通常利用反应2Cu+O 2CuO除去某些混合气体中的少量O。
2 2
(2)铜为变价金属,与Cl 反应生成CuCl ,与S反应生成Cu S,由此可知氧化性:Cl >S。
2 2 2 2
(3)Cu与稀硫酸不反应,但在通入O 的条件下,Cu可在稀硫酸中逐渐溶解:2Cu+O +2H SO ==2CuSO +2H O。
2 2 2 4 4 2
(4)无水CuSO 只能作为检验水的试剂,不能作为水蒸气的吸收试剂而用于除杂。
4
5.铜的冶炼
(1)湿法炼铜:Fe+CuSO ===FeSO+Cu。
4 4
(2)高温炼铜:工业上用高温冶炼黄铜矿的方法获得铜(粗铜):
2CuFeS+4O=====Cu S+3SO +2FeO(炉渣)
2 2 2 2
2Cu S+3O======2Cu O+2SO
2 2 2 2
2Cu O+Cu S======6Cu+SO ↑
2 2 2
(3)电解精炼铜:粗铜中铜的含量为99.5%~99.7%,主要含有Ag、Zn、Fe、Au等杂质,粗铜通过电解精
炼可得到纯度达99.95%~99.98%的铜。电解精炼铜的原理是用粗铜作阳极,铜在阳极上失电子变为 Cu2
+,用纯铜棒作阴极,Cu2+在阴极上得电子生成铜。
6.废铜综合利用常见化工流程
知识点二 金属材料与金属矿物的开发利用
1.合金
(1)概念:合金是指两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质。
(2)性能:合金具有不同于各成分金属的物理、化学性能或机械性能。
①熔点:一般比它的各成分金属的低;
②硬度和强度:一般比它的各成分金属的大。
【特别提醒】①构成合金的成分不一定是两种或两种以上的金属,也可以是金属与非金属,合金中一定含
金属元素。合金一定是混合物。
②常温下,多数合金是固态,但钾、钠合金呈液态。
③合金的性质不是各成分金属的性质之和。合金具有许多良好的物理、化学和机械性能,在许多方面不同
于各成分金属,不是简单加和;但在化学性质上,一般认为合金体现的是各成分金属的化学性质。
2.常见金属材料
(1)黑色金属材料——钢铁
①钢是用量最大、用途最广的合金。②钢
(2)有色金属材料——铜和铝
①铝及铝合金
②铜及铜合金
【特别提醒】合金的组成与性质
(1)构成合金的成分不一定是两种或两种以上的金属,也可以是金属与非金属,合金中一定含金属元素。合
金一定是混合物。
(2)常温下,多数合金是固态,但钾、钠合金呈液态。
(3)合金的性质不是各成分金属的性质之和。合金具有许多良好的物理、化学和机械性能,在许多方面不同
于各成分金属,不是简单加和;但在化学性质上,一般认为合金体现的是各成分金属的化学性质。
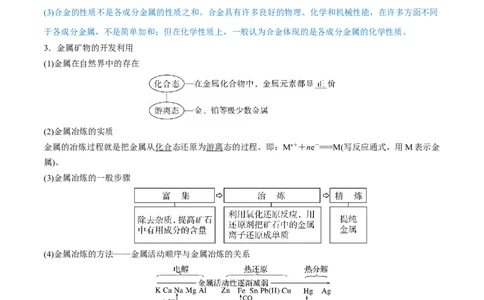
3.金属矿物的开发利用
(1)金属在自然界中的存在
(2)金属冶炼的实质
金属的冶炼过程就是把金属从化合态还原为游离态的过程。即:Mn++ne-===M(写反应通式,用M表示金
属)。
(3)金属冶炼的一般步骤
(4)金属冶炼的方法——金属活动顺序与金属冶炼的关系
①热分解法:适用于不活泼的金属,如Hg和Ag。由HgO冶炼Hg的化学方程式:2HgO=====2Hg+
O↑;由Ag O冶炼Ag的化学方程式:2Ag O=====4Ag+O↑。
2 2 2 2
②热还原法:用还原剂(C、CO、H、Al等)还原金属氧化物,适合较活泼的金属。
2
a.CO还原Fe O:Fe O+4CO=====3Fe+4CO;
3 4 3 4 2
b.C还原ZnO:ZnO+C=====Zn+CO↑;
c.H 还原WO:WO+3H=====W+3HO。
2 3 3 2 2【注意】在高炉炼铁中,加入的还原剂是焦炭,但反应中真正作还原剂的是CO。
③电解法:适合冶炼金属活动性很强的金属(一般指在金属活动性顺序中排在锌前面的金属)。
工业上用电解法冶炼Na、Mg、Al的化学方程式分别为2NaCl(熔融)=====2Na+Cl↑、
2
MgCl (熔融)=====Mg+Cl↑、2Al O=====4Al+3O↑。
2 2 2 3 2
(5)铝热反应
Al和某些金属氧化物在高温下进行,反应迅速并放出大量的热,新生成的金属
实验原理
单质呈熔融态且易与Al O 分离
2 3
实验
装置
实验 ①镁带剧烈燃烧,放出一定的热,并发出耀眼的白光,氧化铁和铝粉在较高
现象 温度下发生剧烈的反应;②纸漏斗的下部被烧穿,有熔融物落入沙中
实验 高温下,铝与氧化铁发生反应,放出大量的热,反应的化学方程式为2Al+
结论 Fe O=====2Fe+Al O
2 3 2 3
原理 ①制取熔点较高、活泼性弱于Al的金属铬、锰、钨等;②金属焊接,如野
应用 外焊接钢轨等
【特别提醒】铝热反应的三个注意事项
①铝热反应是在高温干态下进行的置换反应,铝只能与金属活动性顺序中排在铝之后的金属的氧化物反应。
②铝热反应会放出大量的热(这一特性常出现在推断题中)。Mg条、KClO 的作用是产生高温,引发铝热反
3
应。
③铝热反应不能用来冶炼大量的金属铁、铜等(要考虑冶炼成本)。
知识点三 镁 海水提镁
1.镁的存在
自然界中的镁主要以化合态的形式存在于地壳和海水中,海水中镁的总储量约为1.8×1015t。
2.镁的性质
分别写出镁与①O、②N、③Cl、④H+、⑤NH Cl溶液反应的化学方程式,是离子反应的写离子方程式:
2 2 2 4
①2Mg+O=====2MgO;
2
②3Mg+N=====MgN;
2 3 2
③Mg+Cl=====MgCl ;
2 2
④Mg+2H+===Mg2++H↑;
2
⑤Mg+2NH===Mg2++2NH ↑+H↑。
3 2
3.镁的提取
(1)从海水中提取镁的流程(2)主要化学反应
①制石灰乳:CaCO =====CaO+CO↑、CaO+HO===Ca(OH) ;
3 2 2 2
②沉淀Mg2+:Mg2++Ca(OH) ===Mg(OH) +Ca2+;
2 2
③制备MgCl :Mg(OH) +2HCl===MgCl +2HO、MgCl ·6H O=====MgCl +6HO;
2 2 2 2 2 2 2 2
④电解MgCl :MgCl (熔融)=====Mg+Cl↑。
2 2 2
4.镁的重要化合物
氧化镁 碱性氧化物 MgO+2H+===Mg2++HO
2
中强碱 Mg(OH) +2H+===Mg2++2HO
2 2
难溶于水 Mg2++2OH-===Mg(OH) ↓
2
氢氧化镁
溶解度小于碳酸镁 MgCO +HO=====Mg(OH) +CO↑
3 2 2 2
热稳定性 Mg(OH) =====MgO+HO
2 2
氯化镁 用于冶炼金属镁 MgCl (熔融)=====Mg+Cl↑
2 2
知识点四 工艺流程题的解读
1.工艺流程题过程解读
(1)读流程图
①箭头:箭头进入的是投料(反应物)、出去的是主产物或副产物(生成物)。
②三线:出线和进线均表示物料流向或操作流程,可逆线表示物质循环。
(2)解题要点
①审题要点:a.了解生产目的、原料及产品;b.了解题目提供的信息;c.分析各步的反应条件、原理及物质
成分;d.理解物质分离、提纯、条件控制等操作的目的及要点。
②答题切入点:a.原料及产品的分离提纯,b.生产目的及反应原理;c.生产要求及反应条件;d.有关产率、
产量及组成的计算;e.绿色化学。
2.工艺流程题常见答题方向工艺操作(结果) 目的评价(或操作名称)
研磨(粉碎) 增大接触面积,加快反应(溶解)速率
煅烧(焙烧) 矿物分解、燃烧,转化为易溶于酸、碱的物质
方法措施
水浸 利用水溶性把物质进行分离
利用物质与酸(碱)反应除掉杂质或把目标物质转化为
酸浸(碱浸)
可溶性离子
调节溶液pH 某些金属离子的沉淀,控制物质的溶解
加快反应速率,促进平衡移动;物质的溶解、析出、
控制温度
挥发等
控制条件
增大某反应
增大另一反应物的转化率(产率)
物用量
某种试剂的选择 是否带入杂质、是否影响产品的纯度
不相溶液体 分液
相溶性液体 蒸馏
难溶性固体 过滤
易溶性固体 蒸发浓缩、冷却结晶
分离提纯
趁热过滤 防止温度降低,某物质析出
冰水洗涤 减少晶体的溶解损失
乙醇、有机
减少晶体的水溶性损失
溶剂洗涤
第三部分:典型例题剖析
高频考点1 考查铜及其化合物的性质和应用
【典例1】(2022·上海上海·模拟预测)焊接两根漆包铜线(铜线表面有绝缘油漆)的操作是:①先把漆包铜
线放在火上灼烧,②立即在酒精中蘸一下,③然后焊接铜线头。有关叙述正确的是
A.①中只有铜发生了氧化反应
B.②中的乙醇做溶剂
C.经历①②的变化后铜线的质量不变
D.长期使用后的酒精会有香味
【解析】焊接两根漆包铜线操作中,①先把漆包铜线放在火上灼烧,油漆燃烧,Cu和氧气反应变为氧化铜,
②立即在酒精中蘸一下,氧化铜和酒精反应生成Cu、乙醛和水;A.①先把漆包铜线放在火上灼烧,油漆
燃烧,Cu和氧气反应变为氧化铜,A错误;B.②立即在酒精中蘸一下,氧化铜和酒精反应生成Cu、乙醛
和水,乙醇作反应物,B错误;C.经历①②的变化后,Cu的量不变,但铜线表面油漆燃烧,铜线质量减
小,C错误;D.乙醇和CuO反应生成乙醛,乙醛氧化会生成乙酸,长期使用后乙酸和乙醇反应生成乙酸
乙酯,酒精会有香味,D正确;故选D。
【答案】D【题后归纳】铜及其化合物的颜色、状态及溶解性
物质 颜色 状态及溶解性 物质 颜色 状态及溶解性
紫红色,有 固态,难溶于非氧化性
Cu CuSO 白色 粉末,易溶于水,水溶液呈蓝色
金属光泽 酸,易溶于强氧化性酸 4
CuO 黑色 粉末,可溶于酸溶液 CuSO ·5HO 蓝色 晶体
4 2
固体,难溶于水,可溶
Cu (OH) CO
Cu O 砖红色 于酸溶液(生成Cu和 2 2 绿色 粉末,难溶于水,可溶于酸溶液
2
Cu2+) 3
CuCl
白色 粉末,难溶于水 Cu(OH) 蓝色 难溶于水,可溶于酸溶液
2
CuI
粉末,难溶于水及非氧
CuS 黑色 [Cu(NH )]2+ 深蓝色 络合离子,溶于水
化性强酸 3 4
【变式训练】(2022·广东·模拟预测)广东南华寺还存有北齐孝昭帝皇建元年(公元560年)的铜佛造像,下
列关于铜的电化学腐蚀与保护的说法正确的是
A.铜在潮湿空气中易发生析氢腐蚀
B.铜在潮湿空气发生化学腐蚀比发生电化学腐蚀更普遍
C.铜表面的铜绿的主要成分是
D.用稀硝酸可以清洗铜佛造像表面的铜绿
【解析】A.铜在潮湿空气中易腐蚀生成铜绿即 ,则发生吸氧腐蚀,A错误;B.电化学腐
蚀速率比化学腐蚀快,且绝大多数铜都含有杂质易形成原电池反应,故铜在潮湿空气发生电化学腐蚀比发
生化学腐蚀更普遍,B错误;C.铜表面的铜绿的主要成分是碱式碳酸铜即 ,C正确;D.由
于稀硝酸在常温下也能腐蚀铜单质,故不能用稀硝酸可以清洗铜佛造像表面的铜绿,可用稀硫酸来清洗铜
佛像表面的铜绿,D错误;故答案为:C。
【答案】C
高频考点2 考查铜及其化合物的制备
例2.(2022·山东聊城·二模) 是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法
错误的是A.Y可以是甲酸乙酯
B.利用途径①制备 硫酸铜,消耗的硝酸至少为
C.Cu元素参与了3个氧化还原反应
D.途径⑤中若 ,则X为
【解析】铜经过反应①、②得到硫酸铜,硫酸铜经过反应⑤分解生成氧气、X和Cu O;硫酸铜与过量的氢
2
氧化钠反应得到新制备的氢氧化铜悬浊液,与Y反应得到Cu O,说明Y中含醛基。A.甲酸乙酯中含有醛
2
基,可以与氢氧化铜反应得到Cu O,A正确;B.铜与稀硝酸反应的离子反应式为:
2
,防有硫酸存在时,硫酸提供大量的氢离子,这时消耗的硝酸的量最
少,途径①制备24g硫酸铜,硫酸铜的物质的量为0.15mol,根据方程式可知硝酸的物质的量为0.10mol,
B正确;C. Cu元素参与了反应①、②、④、⑤4个氧化还原反应,C错误;D.当途径⑤中若
n(O ):n(Cu O)=3:2,根据元素守恒可配平化学方程式, ,根据方程式得失
2 2
电子数也守恒,故X为二氧化硫,D正确;故选C。
【答案】C
【变式训练】(2022·重庆·模拟预测)碱式氯化铜[CuCl(OH)·xH O]是一种重要的无机杀虫剂,它的制备
a b c 2
流程如下,下列有关说法正确的是
A.FeCl 的作用是增强盐酸的氧化性
3
B.加入少量CuO目的是为了除去Fe3+
C.石灰乳可用纯碱代替
D.若制备1mol的CuCl ,理论上消耗11.2L空气
2【解析】A.最终产物中不含Fe元素,FeCl 与Cu反应后,又被O 氧化成FeCl ,FeCl 起催化剂的作用,
3 2 3 3
故A错误;B.加入CuO调节溶液pH,使Fe3+生成Fe(OH) 沉淀,而除去,故B正确;C.纯碱代替石灰
3
乳可能会生成碳酸铜或碱式碳酸铜,故C错误;D.未说明气体是否在标准状态,无法进行计算,故D错
误;故答案为B。
【答案】B
高频考点3 考查合金的性质及应用
例1.(2022·全国·高三专题练习)“嫦娥五号”中使用了大量合金。下列有关金属或合金的说法中不正确
的是
A.生铁属于合金
B.一般合金的熔点比各成分金属的低
C.合金的化学性质与其成分金属的化学性质不同
D.改变原料的配比、生成合金的条件,可以得到具有不同性能的合金
【解析】A.生铁由铁和碳等元素组成,属于合金,故A正确;B.形成合金后,结构发生了改变,一般
合金的熔点比各成分金属的低,故B正确;C.合金的化学性质与其成分金属的化学性质相同,故C错误;
D.改变原料的配比、生成合金的条件,组成合金的成分、结构不同,对合金的性质产生不同的影响,可
以得到具有不同性能的合金,故D正确;故答案选C。
【答案】C
【变式训练】(2020·河北省衡水中学调研)国产大型客机C919首飞成功,即将量产。C919机身部分采用
第三代新型铝锂合金材料。下列关于铝锂合金的认识不正确的是( )
A. 铝锂合金密度较小,强度较大,硬度大于纯铝,熔点低于锂单质
B. 改变原料的配比,可以制得性能不同的铝锂合金
C. 铝锂合金具有金属光泽,可导电导热
D. 铝锂合金的性质与各成分金属的性质完全相同
【解析】合金的熔点比它的各成分金属的熔点低,硬度大于其成分金属,故A正确;合金的性质与成分的
含量有关,所以改变原料的配比,可以制得性能不同的铝锂合金,故B正确;铝锂合金具有金属材料的一
些通性,有金属光泽,可导电导热,故C正确.合金的熔点比它的各成分金属的熔点低,硬度大于其成分
金属,所以铝锂合金的性质与各成分金属的性质不完全相同,故D错误。
【答案】 D
高频考点4 考查金属矿物的开发与利用
例2.(2021·河北唐山·一模)工业上利用无机矿物资源生产部分材料的流程示意图如下(铝土矿中含有),下列说法正确的是
A.铝土矿制备Al的过程涉及的操作有过滤、蒸馏、灼烧、电解
B.石灰石、纯碱、石英、玻璃都属于盐,都能与盐酸反应
C.在制粗硅时,氧化剂与还原剂的物质的量之比为1:2
D.黄铜矿 与 反应产生的 、 均是还原产物
【解析】A.铝土矿除杂过程中没有分离液体混合物的操作,不需要蒸馏,A错误;B.石英为SiO,属于
2
酸性氧化物,不是盐,B错误;C.制取粗硅时氧化剂为SiO,被还原成Si,C为还原剂,被氧化为CO,
2
根据电子守恒可知氧化剂与还原剂的物质的量之比为1:2,C正确;D.生成SO 时S元素化合价升高,
2
SO 为氧化产物,D错误;综上所述答案为C。
2
【答案】C
【特别提醒】(1)电解法冶炼活泼金属使用的是熔融的金属盐或金属氧化物,而不是盐溶液。
(2)铜除了用热还原法冶炼外,还可以用湿法炼铜或电解法进行冶炼。
【变式训练】 (2021·辽宁·模拟预测)氧化铝是工业上电解制铝的原料,工业上用铝土矿(主要成分
Al O,还含有Fe O,SiO 等)为原料制取氧化铝的流程如图所示,下列说法错误的是
2 3 2 3 2
A.滤渣可用于炼铁
B.实验室可在蒸发皿中加热分解氢氧化铝
C.步骤①、②、③中均不涉及氧化还原反应
D.实验室中进行过滤时,用到的玻璃仪器有烧杯、漏斗、玻璃棒
【解析】铝土矿(主要成分Al O,还含有Fe O,SiO 等)加入足量烧碱,Al O、SiO 溶解得到偏铝酸钠和
2 3 2 3 2 2 3 2硅酸钠,加入氧化硅,得到硅酸钙沉淀,滤液2中还含有NaOH和偏铝酸钠,通入足量的二氧化碳,偏铝
酸钠反应生成氢氧化铝沉淀,氢氧化铝高温灼烧得到氧化铝。A.流程中滤渣主要成分为氧化铁,可用于
炼铁,A项正确;B.固体加热要在坩埚中进行,B项错误;C.流程中第一步发生反应
、 ,第二步发生反应
,第三步是二氧化碳和氢氧化钠和偏铝酸钠的反应,都不涉及氧
化还原反应,C项正确;D.过滤时,必须有烧杯、漏斗和玻璃棒,D项正确;综上所述答案为B。
【答案】B
高频考点5 考查以金属及其化合物化工生产为背景的工艺流程分析
例5.(2020·课标全国Ⅲ,26)某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有
少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO ·7H O):
4 2
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Ni2+ Al3+ Fe3+ Fe2+
开始沉淀时(c=0.01 mol·L−1)的pH 7.2 3.7 2.2 7.5
沉淀完全时(c=1.0×10−5 mol·L−1)的pH 8.7 4.7 3.2 9.0
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是______________。为回收金属,用稀硫酸将“滤液①”调为中性,
生成沉淀。写出该反应的离子方程式______________。
(2)“滤液②”中含有的金属离子是______________。
(3)“转化”中可替代HO 的物质是______________。若工艺流程改为先“调pH”后“转化”,即
2 2
“滤液③”中可能含有的杂质离子为______________。
(4)利用上述表格数据,计算Ni(OH) 的K =______________(列出计算式)。如果“转化”后的溶液中Ni2+浓
2 sp度为1.0 mol·L−1,则“调pH”应控制的pH范围是______________。
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子
方程式______________。
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是______________。
【解析】由工艺流程分析可得,向废镍催化剂中加入NaOH溶液进行碱浸,可除去油脂,并发生反应
2Al+2NaOH+2H O=2NaAlO +3H ↑、2Al O+4NaOH=4NaAlO +2H O将Al及其氧化物溶解,得到的滤液①
2 2 2 2 3 2 2
含有NaAlO ,滤饼①为Ni、Fe及其氧化物和少量其他不溶性杂质,加稀HSO 酸浸后得到含有Ni2+、
2 2 4
Fe2+、Fe3+的滤液②,Fe2+经HO 氧化为Fe3+后,加入NaOH调节pH使Fe3+转化为Fe(OH) 沉淀除去,再控
2 2 3
制pH浓缩结晶得到硫酸镍的晶体。
(1)根据分析可知,向废镍催化剂中加入NaOH溶液进行碱浸,可除去油脂,并将Al及其氧化物溶解,滤
液①中含有NaAlO (或Na[Al(OH)]),加入稀硫酸可发生反应 +H++H O=Al(OH) ↓或
2 4 2 3
+H+=Al(OH) ↓+H O;
3 2
(2)加入稀硫酸酸浸,Ni、Fe及其氧化物溶解,所以“滤液②”中含有的金属离子是Ni2+、Fe2+、Fe3+;
(3)“转化”在HO 的作用是将Fe2+氧化为Fe3+,可用O 或空气替代;若将工艺流程改为先“调pH”后“转
2 2 2
化”,会使调pH过滤后的溶液中含有Fe2+,则滤液③中可能含有转化生成的Fe3+,故答案为:O 或空气;
2
Fe3+;
(4)由上述表格可知,Ni2+完全沉淀时的pH=8.7,此时c(Ni2+)=1.0×10-5mol·L-1,c(H+)=1.0×10-8.7mol·L-1,则
c(OH-)= ,则Ni(OH) 的 ;或者当Ni2+开始
2
沉淀时pH=7.2,此时c(Ni2+)=0.01mol·L-1,c(H+)=1.0×10-7.2mol·L-1,则c(OH-)= ,
则Ni(OH) 的 ;如果“转化”后的溶液中Ni2+浓度为1.0mol·L-1,为
2
避免镍离子沉淀,此时 ,则,即pH=6.2;Fe3+完全沉淀的pH为3.2,因此“调节pH”应控制的pH范围
是3.2~6.2;
(5)由题干信息,硫酸镍在强碱中被NaClO氧化得到NiOOH沉淀,即反应中Ni2+被氧化为NiOOH沉淀,
ClOˉ被还原为Clˉ,则根据氧化还原得失电子守恒可得离子方程式为2Ni2+
+ClOˉ+4OHˉ=2NiOOH↓+Clˉ+H O;
2
(6)分离出硫酸镍晶体后的母液中还含有Ni2+,可将其收集、循环使用,从而提高镍的回收率。
【答案】(1)除去油脂、溶解铝及其氧化物 +H++H O=Al(OH) ↓或 +H+=Al(OH) ↓+H O
2 3 3 2
(2)Ni2+、Fe2+、Fe3+ (3)O 或空气 Fe3+ (4) 3.2~6.2
2
(5)2Ni2++ClOˉ+4OHˉ=2NiOOH↓+Clˉ+H O
2
(6)提高镍回收率
【名师点睛】本题以金属及其化合物化工生产为背景考查金属及其化合物的性质、沉淀溶解平衡常数Ksp
的计算、氧化还原离子反应方程式的书写等知识点,需要学生具有很好的综合迁移能力,解答关键在于正
确分析出工艺流程原理,难点在于Ksp的计算及“调pH”时pH的范围确定。
【变式训练】(2021·四川成都摸底测试)硫酸锌是制造锌钡白和锌盐的主要原料,也可用作木材的防腐剂等。
用氧化锌烟尘(主要成分为ZnO,还含有少量PbO、CuO、Fe O、FeO等)生产ZnSO·7H O的流程如下:
2 3 4 2
有关金属离子[c(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
金属离子 Fe3+ Fe2+ Zn2+ Cu2+
开始沉淀的pH 1.5 6.3 6.2 4.7
沉淀完全的pH 2.8 8.3 8.2 6.7
(1)“酸浸”时用的稀酸是________;滤渣1的主要成分是________。
(2)“氧化”时的离子方程式为____________________________;
加入ZnO除杂时溶液的pH控制范围是________~5.0。
(3)滤渣3含有锌和________;由滤液得到ZnSO·7H O的操作是_________________________、洗涤、干燥。
4 2
(4)取14.35 g ZnSO ·7H O加热至不同温度,剩余固体的质量如下表:
4 2
温度/℃ 100 250 680 930质量/g 8.95 8.05 6.72 4.05
则680 ℃时剩余固体的化学式为________(填序号)。
A.ZnO B.ZnO(SO ) C.ZnSO D.ZnSO·H O
3 4 2 4 4 2
【解析】流程分析如下:
(1)因制备的是ZnSO·7H O,“酸浸”时为不引入杂质,应用稀硫酸;由于PbSO 不溶于稀硫酸,故滤渣1
4 2 4
的主要成分是PbSO 。
4
(2)加入NaClO可将溶液中的Fe2+氧化为Fe3+,故“氧化”时的离子方程式为2Fe2++ClO-+2H+===2Fe3+
+Cl-+HO;由表中数据可知,Fe3+完全转化为Fe(OH) 沉淀时的pH为2.8,故加入ZnO除杂时pH最小
2 3
为2.8。
(3)由于Cu2+完全转化为Cu(OH) 沉淀时的pH为6.7,故加入ZnO调pH除杂后溶液中还有Cu2+,当加入过
2
量锌粉时发生置换反应:Zn+Cu2+===Zn2++Cu,则滤渣3含有过量的锌和生成的铜;从滤液中得到
ZnSO·7H O的操作是蒸发浓缩、冷却结晶、过滤、洗涤、干燥。
4 2
(4)根据Zn原子守恒计算14.35 g ZnSO ·7H O的物质的量为0.05 mol,若加热得到ZnSO·H O,则剩余固体
4 2 4 2
质量为8.95 g,此时温度为100 ℃;若加热得到ZnSO ,则剩余固体质量为8.05 g,此时温度为250 ℃;若
4
加热得到ZnO,则剩余固体质量为4.05 g,此时温度为930 ℃,若加热得到ZnO(SO ) ,则剩余固体质量
3 4 2
为6.72 g,此时温度为680 ℃,故680 ℃时剩余固体的化学式为ZnO(SO )。
3 4 2
【答案】(1)稀硫酸(或HSO ) PbSO
2 4 4
(2)2Fe2++ClO-+2H+===2Fe3++Cl-+HO 2.8
2
(3)铜(或Cu) 蒸发浓缩、冷却结晶、过滤
(4)B