文档内容
1.(2021·湖南1月适应性考试,15)蛋壳是一种很好的绿色钙源,其主要成分为CaCO 。以
3
蛋壳为原料制备葡萄糖酸钙晶体(M[Ca(C H O)·H O]=448 g·mol-1),并对其纯度进行测定,
6 11 7 2 2
过程如下:
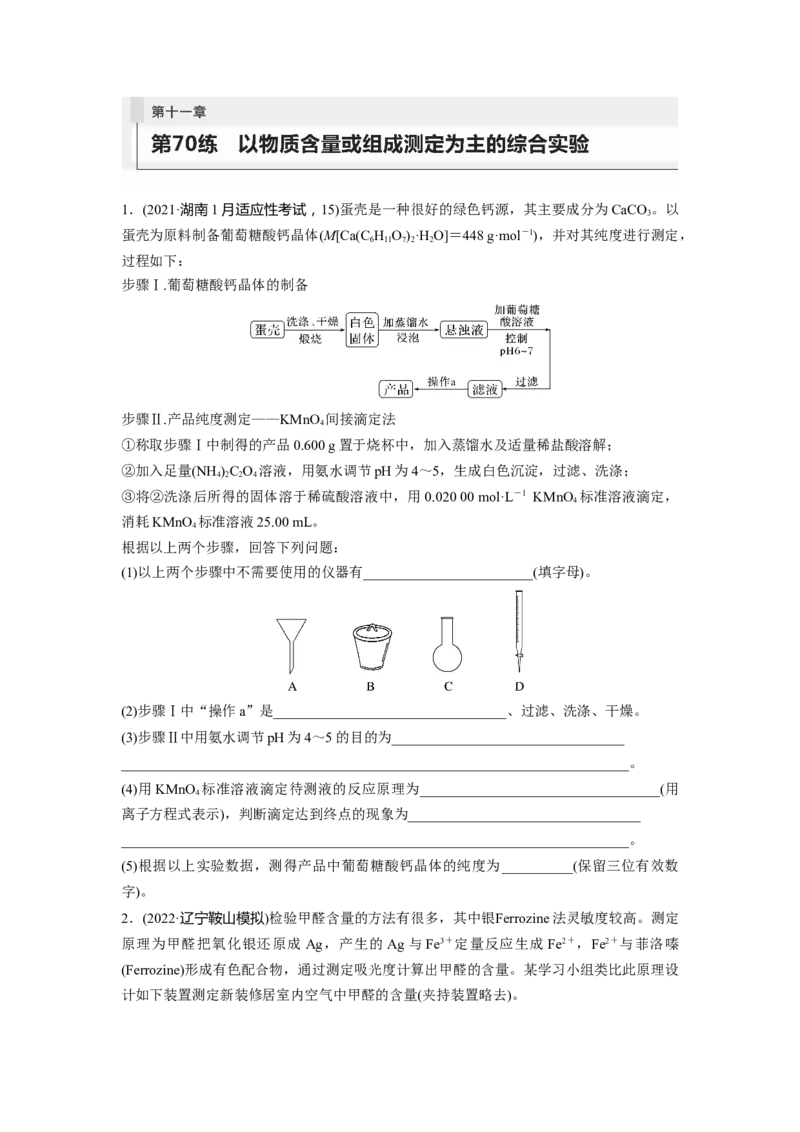
步骤Ⅰ.葡萄糖酸钙晶体的制备
步骤Ⅱ.产品纯度测定——KMnO 间接滴定法
4
①称取步骤Ⅰ中制得的产品0.600 g置于烧杯中,加入蒸馏水及适量稀盐酸溶解;
②加入足量(NH )C O 溶液,用氨水调节pH为4~5,生成白色沉淀,过滤、洗涤;
4 2 2 4
③将②洗涤后所得的固体溶于稀硫酸溶液中,用0.020 00 mol·L-1 KMnO 标准溶液滴定,
4
消耗KMnO 标准溶液25.00 mL。
4
根据以上两个步骤,回答下列问题:
(1)以上两个步骤中不需要使用的仪器有________________________(填字母)。
(2)步骤Ⅰ中“操作a”是_________________________________、过滤、洗涤、干燥。
(3)步骤Ⅱ中用氨水调节pH为4~5的目的为_________________________________
________________________________________________________________________。
(4)用KMnO 标准溶液滴定待测液的反应原理为__________________________________(用
4
离子方程式表示),判断滴定达到终点的现象为_________________________________
________________________________________________________________________。
(5)根据以上实验数据,测得产品中葡萄糖酸钙晶体的纯度为__________(保留三位有效数
字)。
2.(2022·辽宁鞍山模拟)检验甲醛含量的方法有很多,其中银Ferrozine法灵敏度较高。测定
原理为甲醛把氧化银还原成 Ag,产生的Ag与Fe3+定量反应生成Fe2+,Fe2+与菲洛嗪
(Ferrozine)形成有色配合物,通过测定吸光度计算出甲醛的含量。某学习小组类比此原理设
计如下装置测定新装修居室内空气中甲醛的含量(夹持装置略去)。已知:甲醛和银氨溶液反应生成单质银和CO ,氮化镁与水反应放出NH ,毛细管内径不
2 3
超过1 mm。
请回答下列问题:
(1)A装置中反应的化学方程式为___________________________________________,用饱
和食盐水代替水制备NH 的原因是____________________________________________
3
________________________________________________________________________。
(2)B中装有AgNO 溶液,仪器B的名称为________________。
3
(3)银氨溶液的制备。关闭K 、K ,打开K ,打开__________________________,使饱和
1 2 3
食盐水慢慢滴入圆底烧瓶中,当观察到B中__________________________,停止通NH 。
3
(4)室内空气中甲醛含量的测定。
①用热水浴加热B,打开K ,将滑动隔板慢慢由最右端抽到最左端,吸入1 L室内空气,
1
关闭K;后续操作是________________________________________________________
1
________________________________________________________________________;
再重复上述操作3次。毛细管的作用是______________________________________
________________________________________________________________________。
②向上述B中充分反应后的溶液中加入稀硫酸调节溶液pH=1,再加入足量Fe (SO ) 溶液,
2 4 3
充分反应后立即加入菲洛嗪,Fe2+与菲洛嗪形成有色物质,在562 nm处测定吸光度,测得
生成1.12 mg Fe2+,空气中甲醛的含量为__________mg·L-1。
3.钢材在社会发展中应用广泛。为研究某种碳素钢(含少量碳和硫)的成分,科研小组进行
了如下探究活动。
称取碳素钢(已除表面氧化物)24.0 g放入耐高温反应管中与O 反应,除去未反应的O ,收
2 2
集到干燥混合气体X 1.12 L(已折算成标准状况下的体积)。
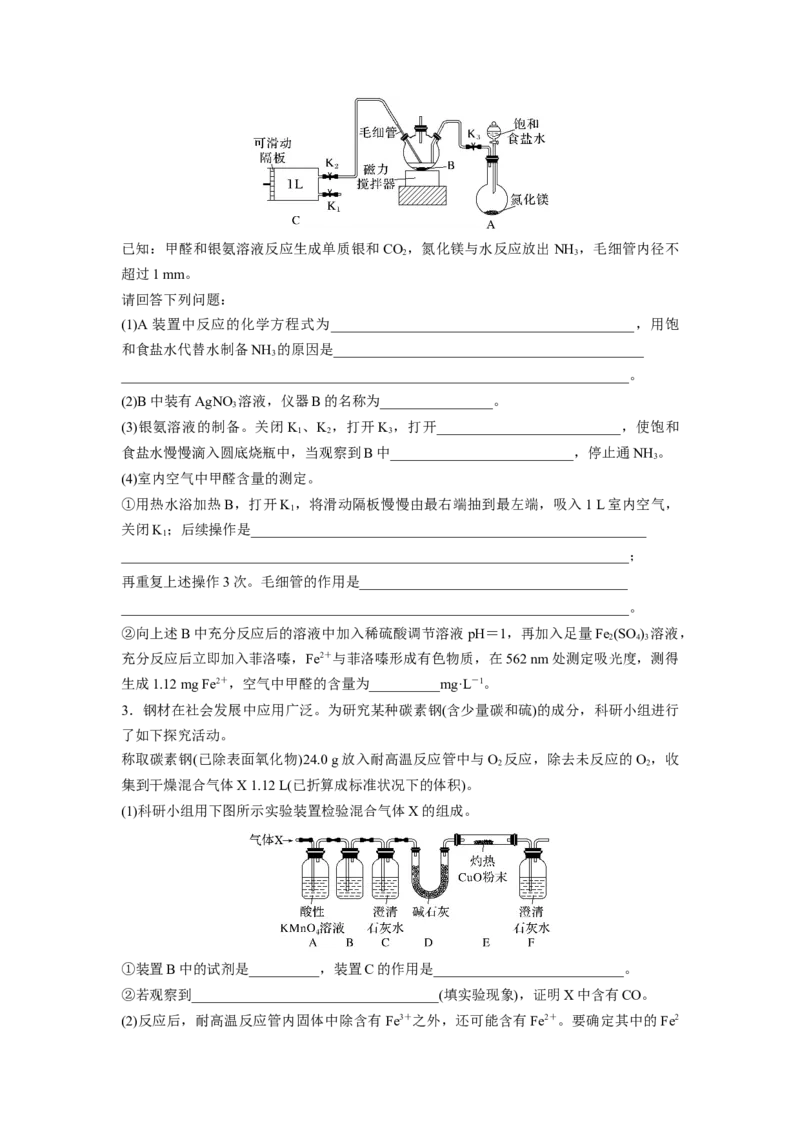
(1)科研小组用下图所示实验装置检验混合气体X的组成。
①装置B中的试剂是__________,装置C的作用是___________________________。
②若观察到___________________________________(填实验现象),证明X中含有CO。
(2)反应后,耐高温反应管内固体中除含有Fe3+之外,还可能含有Fe2+。要确定其中的Fe2+,可选用________(填字母)。
a.KSCN溶液和氯水
b.KSCN溶液和铁粉
c.稀盐酸和K[Fe(CN) ]溶液
3 6
d.稀硫酸和KMnO 溶液
4
(3)科研小组用下图所示装置(部分)测定SO 的体积分数,并计算碳素钢的含碳量。将气体
2
X缓慢通过实验装置,当观察到____________________________(填实验现象)时,停止通
气,此时气体流量仪显示的流量为112 mL(已换算成标准状况下的体积)。则气体X中SO
2
的体积分数为________,碳素钢中碳元素的质量分数为____________(结果保留一位小数)。
4.过氧化尿素是一种新型漂白剂、消毒剂,漂白、消毒的效果优于HO 和过氧乙酸。
2 2
某工业用过氧化尿素的部分参数见下表:
分子式 外观 热分解温度 熔点 水溶性/20 ℃
CO(NH)·H O 白色晶体 45 ℃ 75~85 ℃ 500 g·L-1
2 2 2 2
合成过氧化尿素的流程及反应器的示意图如图:
回答下列问题:
(1)流程中操作①的名称为________,仪器X的名称是____________________。
(2)流程中操作②的具体过程是__________(填字母)。
A.盐析、过滤
B.减压蒸馏、结晶、过滤
C.分液、过滤
D.常压蒸馏、萃取
(3)搅拌器选用的材质是玻璃而不是铁质的原因是______________________________
________________________________________________________________________。
(4)为测定产品中活性氧的含量(若含双氧水34%,则其中活性氧为16%),一般采用KMnO
4
标准溶液进行滴定,但由于KMnO 的强氧化性,其溶液很容易被空气或水中的少量还原性
4物质还原,生成难溶性物质MnO(OH) ,因此配制KMnO 标准溶液有如下步骤:
2 4
a.利用氧化还原滴定方法,在70~80 ℃条件下用基准试剂(纯度高、相对分子质量较大、
稳定性较好的物质)溶液标定其浓度
b.过滤得到的KMnO 溶液贮存于棕色试剂瓶中并放在暗处
4
c.称取稍多于所需量的KMnO 固体溶于水中,将溶液加热并保持微沸1 h
4
d.用微孔玻璃漏斗过滤除去难溶的MnO(OH)
2
①请按照正确的流程对上述步骤进行排序:______________(填字母,下同)。
②在下列物质中,用于标定KMnO 溶液的基准试剂最好选用______________。
4
A.HC O·2H O B.FeSO
2 2 4 2 4
C.浓盐酸 D.NaSO
2 3
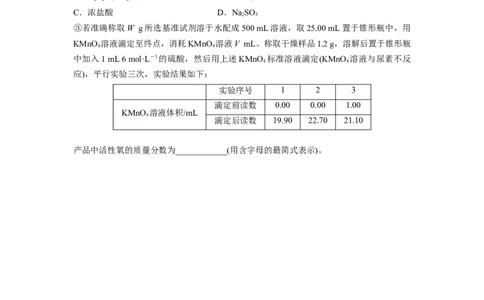
③若准确称取W g所选基准试剂溶于水配成500 mL溶液,取25.00 mL置于锥形瓶中,用
KMnO 溶液滴定至终点,消耗KMnO 溶液V mL。称取干燥样品1.2 g,溶解后置于锥形瓶
4 4
中加入1 mL 6 mol·L-1的硫酸,然后用上述KMnO 标准溶液滴定(KMnO 溶液与尿素不反
4 4
应),平行实验三次,实验结果如下:
实验序号 1 2 3
滴定前读数 0.00 0.00 1.00
KMnO 溶液体积/mL
4
滴定后读数 19.90 22.70 21.10
产品中活性氧的质量分数为____________(用含字母的最简式表示)。