文档内容
第 70 讲 以物质含量或组成测定为主的综合实验
[复习目标] 1.掌握物质组成或含量测定的一般方法。 2.掌握定量测定实验的思维模型。
类型一 物质含量的测定
1.重量分析法
(1)在重量分析中,一般首先采用适当的方法,使被测组分以单质或化合物的形式从试样中
与其他组分分离。
(2)重量分析法不需要指示剂,实验的关键是准确判断反应是否完全,以及反应前后固体(或
液体)质量的变化。
(3)重量分析法的过程包括分离和称量两个过程。根据分离的方法不同,重量分析法又可分
为沉淀法、挥发法、萃取法等。
(4)计算方法
采用重量分析法进行定量计算时,可根据实验中发生反应的化学方程式或原子守恒确定相
关物质之间的定量关系,再结合实验数据列出关系式,并进行相关计算。
2.滴定分析法
(1)滴定分析法是将已知准确浓度的标准溶液,滴加到待测溶液中(或者将待测溶液滴加到标
准溶液中),直到所加的标准溶液与待测溶液按化学计量关系定量反应完全为止,然后测量
标准溶液消耗的体积,根据标准溶液的浓度和所消耗的体积,计算出待测物质的含量。
(2)实验的关键是准确量取待测溶液,根据指示剂的颜色变化确定滴定终点。
(3)根据标准溶液和待测溶液间反应类型的不同,可将滴定分析法分为四大类:中和滴定、
氧化还原滴定、络合滴定和沉淀滴定。
3.气体体积法
(1)通过测量反应生成气体的体积进行定量分析的方法,实验的关键是准确测量生成气体的
体积。
(2)测气体体积的方法分为直接测量法和间接测量法:
将气体通入带有刻度的容器中,直接读取气体的体积。根据所用测量仪
直接测量法
器的不同,直接测量法可分为倒置量筒法和滴定管法两种
利用气体将液体(通常为水)排出,通过测量所排出液体的体积从而得到
间接测量法 气体体积。常用的测量装置为用导管连接的装满液体的广口瓶和空量
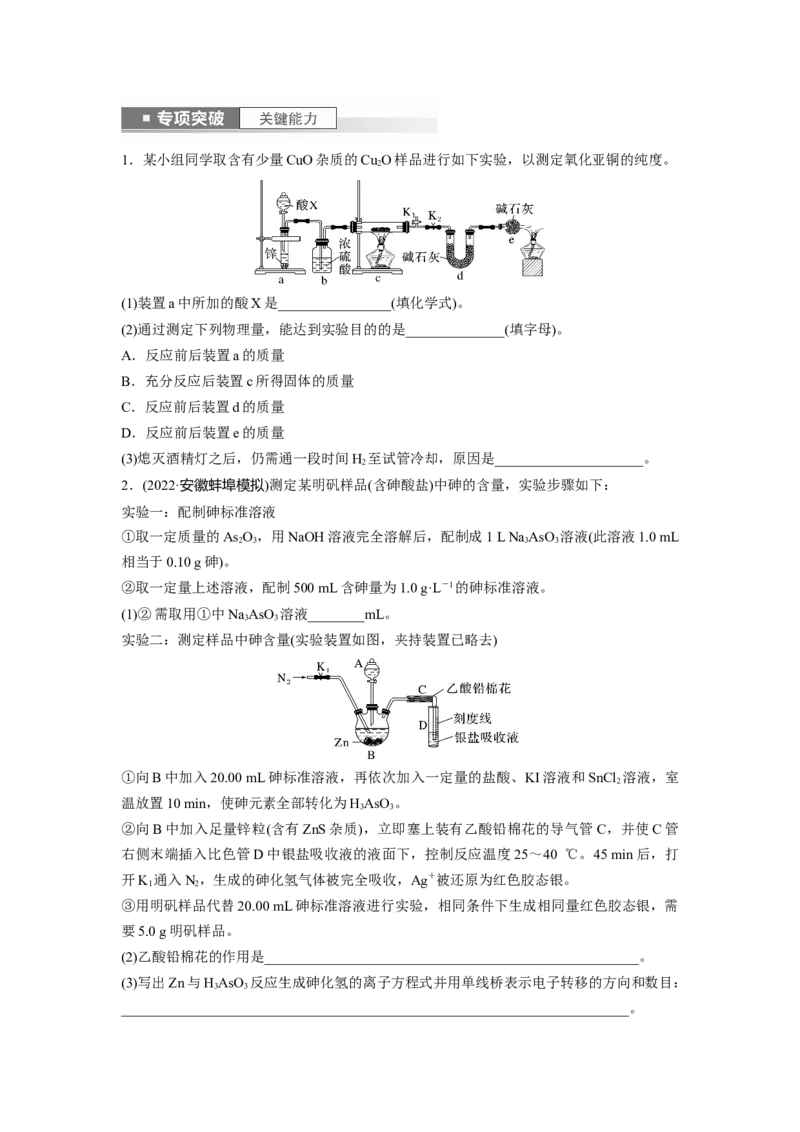
筒。排水法收集气体时,要保证“短进长出”1.某小组同学取含有少量CuO杂质的Cu O样品进行如下实验,以测定氧化亚铜的纯度。
2
(1)装置a中所加的酸X是________________(填化学式)。
(2)通过测定下列物理量,能达到实验目的的是______________(填字母)。
A.反应前后装置a的质量
B.充分反应后装置c所得固体的质量
C.反应前后装置d的质量
D.反应前后装置e的质量
(3)熄灭酒精灯之后,仍需通一段时间H 至试管冷却,原因是_____________________。
2
2.(2022·安徽蚌埠模拟)测定某明矾样品(含砷酸盐)中砷的含量,实验步骤如下:
实验一:配制砷标准溶液
①取一定质量的As O,用NaOH溶液完全溶解后,配制成1 L Na AsO 溶液(此溶液1.0 mL
2 3 3 3
相当于0.10 g砷)。
②取一定量上述溶液,配制500 mL含砷量为1.0 g·L-1的砷标准溶液。
(1)②需取用①中NaAsO 溶液________mL。
3 3
实验二:测定样品中砷含量(实验装置如图,夹持装置已略去)
①向B中加入20.00 mL砷标准溶液,再依次加入一定量的盐酸、KI溶液和SnCl 溶液,室
2
温放置10 min,使砷元素全部转化为HAsO 。
3 3
②向B中加入足量锌粒(含有ZnS杂质),立即塞上装有乙酸铅棉花的导气管C,并使C管
右侧末端插入比色管D中银盐吸收液的液面下,控制反应温度25~40 ℃。45 min后,打
开K 通入N,生成的砷化氢气体被完全吸收,Ag+被还原为红色胶态银。
1 2
③用明矾样品代替20.00 mL砷标准溶液进行实验,相同条件下生成相同量红色胶态银,需
要5.0 g明矾样品。
(2)乙酸铅棉花的作用是_____________________________________________________。
(3)写出Zn与HAsO 反应生成砷化氢的离子方程式并用单线桥表示电子转移的方向和数目:
3 3
________________________________________________________________________。(4)控制B中反应温度的方法是_____________________________________________,
反应中通入N 的作用是___________________________________________________。
2
(5)明矾样品中砷的含量为__________%。
类型二 物质组成的测定
确定物质组成的注意事项
1.测定实验中要有消除干扰气体的意识
如用惰性气体将干扰气体排出,或用溶液吸收干扰气体等。
2.测定实验中要有被测量气体全部被测量的意识
如可采取反应结束后继续向装置中通入惰性气体以使被测量气体全部被吸收剂吸收的方法。
3.测定实验中要有“数据”的采集处理意识
(1)称量固体质量时,中学一般用托盘天平,可估读到0.1 g,精确度要求高的实验中可以用
分析天平或电子天平。
(2)测量液体体积时,一般实验中选用适当规格的量筒,可估读到 0.1 mL,准确度要求高的
定量实验如中和滴定中选用滴定管,可估读到0.01 mL。
(3)气体除了量取外,还可以称量。称气体的质量时一般有两种方法:一种方法是称反应装
置在放出气体前后的质量减小值;另一种方法是称吸收装置前后的质量增大值。
(4)用pH试纸(测得整数值)或pH计(精确到0.01)直接测出溶液的pH,经过计算可以得到溶
液中H+或OH-的物质的量浓度。
1.某浅绿色晶体X[x(NH )SO ·yFeSO ·zHO]在分析化学中常用作还原剂。为确定其组成,
4 2 4 4 2
某小组同学进行如下实验:
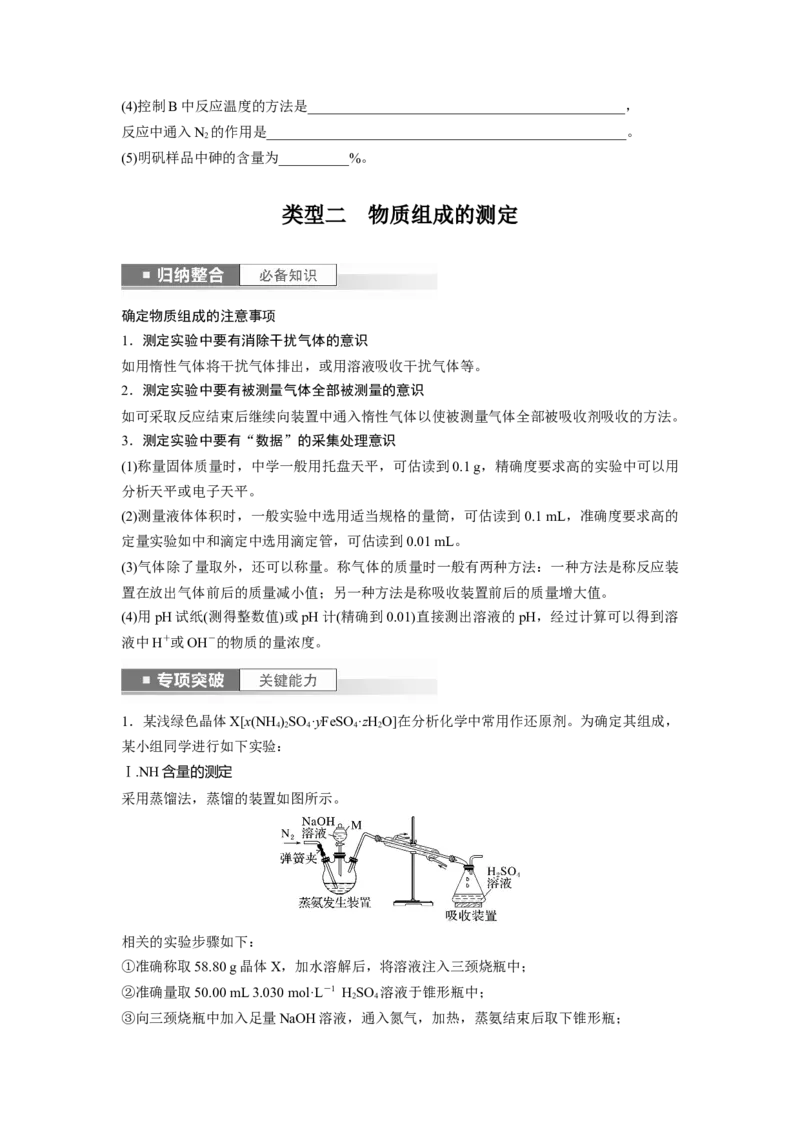
Ⅰ.NH含量的测定
采用蒸馏法,蒸馏的装置如图所示。
相关的实验步骤如下:
①准确称取58.80 g晶体X,加水溶解后,将溶液注入三颈烧瓶中;
②准确量取50.00 mL 3.030 mol·L-1 HSO 溶液于锥形瓶中;
2 4
③向三颈烧瓶中加入足量NaOH溶液,通入氮气,加热,蒸氨结束后取下锥形瓶;④用0.120 mol·L-1的NaOH标准溶液滴定锥形瓶中过量的硫酸,滴定终点时消耗 25.00 mL
NaOH标准溶液。
(1)仪器M的名称为____________。
(2)步骤③中,发生的氧化还原反应的化学方程式为____________________________
________________________________________________________________________,
蒸氨结束后,为了减少实验误差,还需要对直形冷凝管进行“处理”,“处理”的操作方
法是______________________________________________________________________
________________________________________________________________________。
(3)步骤④中,若振荡时锥形瓶中有液体溅出,则所测得的n(NH)的值将________(填“偏
大”“偏小”或“不变”)。
Ⅱ.SO含量的测定
采用重量分析法,实验步骤如下:
①另准确称取58.80 g晶体X于烧杯中,加水溶解,边搅拌边加入过量的BaCl 溶液;
2
②将得到的溶液用无灰滤纸(灰分质量很小,可忽略)过滤,洗涤沉淀3~4次;
③用滤纸包裹好沉淀取出,灼烧滤纸包至滤纸完全灰化;
④继续灼烧沉淀至恒重,称量,得沉淀质量为69.90 g。
(4)步骤①中,判断BaCl 溶液已过量的实验操作和现象是______________________
2
________________________________________________________________________。
(5)步骤②中,采用冷水洗涤沉淀,其主要目的是_____________________________。
(6)结合实验 Ⅰ、Ⅱ 通过计算得出晶体X的化学式为_________________________。
2.碱式碳酸钴[Co(OH)(CO)]可用作电子材料、磁性材料的添加剂,受热时可分解生成
x y 3 2
三种氧化物。为了确定其组成,某化学兴趣小组同学设计了如图所示装置进行实验。
(1)请完成下列实验步骤:
①称取3.65 g样品置于硬质玻璃管内,分别称量乙、丙装置的质量;
②按如图所示装置组装好仪器,并检查装置气密性;
③加热甲装置中硬质玻璃管,当乙装置中___________________________________
____________________________________________________(填实验现象),停止加热;
④打开活塞K,缓缓通入空气数分钟后,称量乙、丙装置的质量;
⑤计算。
(2)步骤④中缓缓通入空气数分钟的目的是____________________________________
________________________________________________________________________。
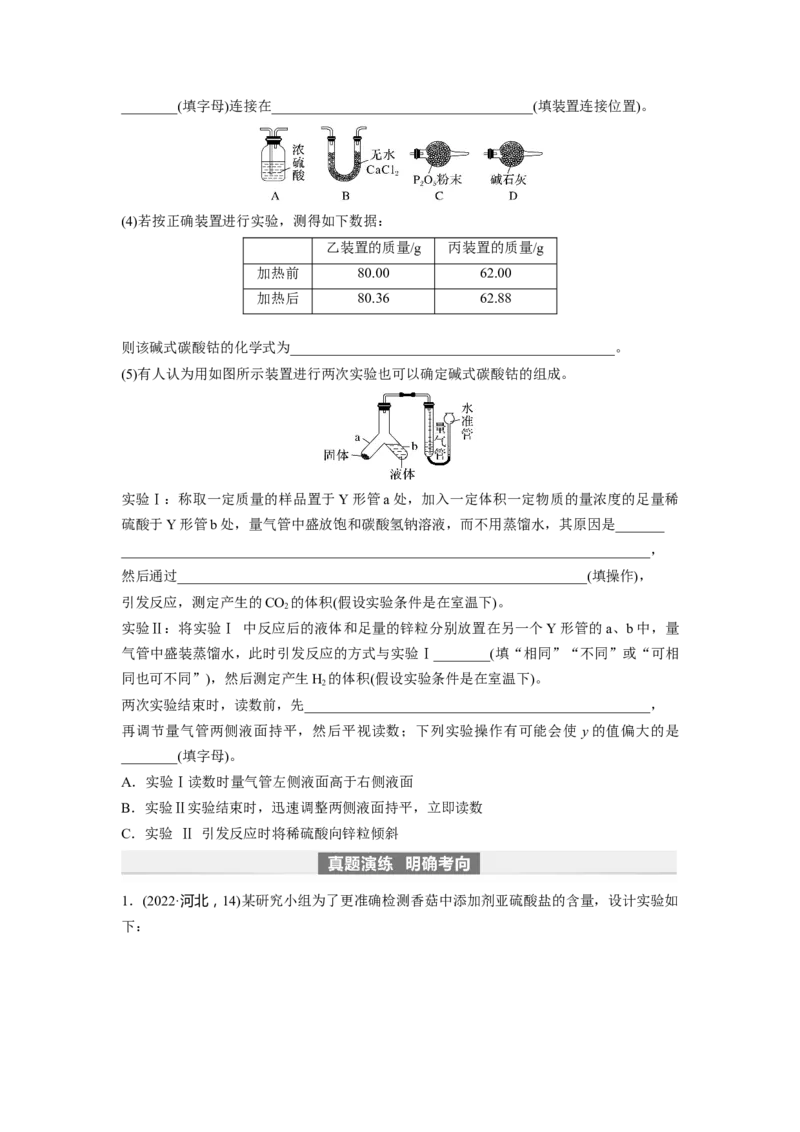
(3)某同学认为上述实验装置中存在一个明显缺陷,为解决这一问题,可选用下列装置中的________(填字母)连接在_____________________________________(填装置连接位置)。
(4)若按正确装置进行实验,测得如下数据:
乙装置的质量/g 丙装置的质量/g
加热前 80.00 62.00
加热后 80.36 62.88
则该碱式碳酸钴的化学式为______________________________________________。
(5)有人认为用如图所示装置进行两次实验也可以确定碱式碳酸钴的组成。
实验Ⅰ:称取一定质量的样品置于Y形管a处,加入一定体积一定物质的量浓度的足量稀
硫酸于Y形管b处,量气管中盛放饱和碳酸氢钠溶液,而不用蒸馏水,其原因是_______
___________________________________________________________________________,
然后通过__________________________________________________________(填操作),
引发反应,测定产生的CO 的体积(假设实验条件是在室温下)。
2
实验Ⅱ:将实验Ⅰ 中反应后的液体和足量的锌粒分别放置在另一个Y形管的a、b中,量
气管中盛装蒸馏水,此时引发反应的方式与实验Ⅰ________(填“相同”“不同”或“可相
同也可不同”),然后测定产生H 的体积(假设实验条件是在室温下)。
2
两次实验结束时,读数前,先_________________________________________________,
再调节量气管两侧液面持平,然后平视读数;下列实验操作有可能会使 y的值偏大的是
________(填字母)。
A.实验Ⅰ读数时量气管左侧液面高于右侧液面
B.实验Ⅱ实验结束时,迅速调整两侧液面持平,立即读数
C.实验 Ⅱ 引发反应时将稀硫酸向锌粒倾斜
1.(2022·河北,14)某研究小组为了更准确检测香菇中添加剂亚硫酸盐的含量,设计实验如
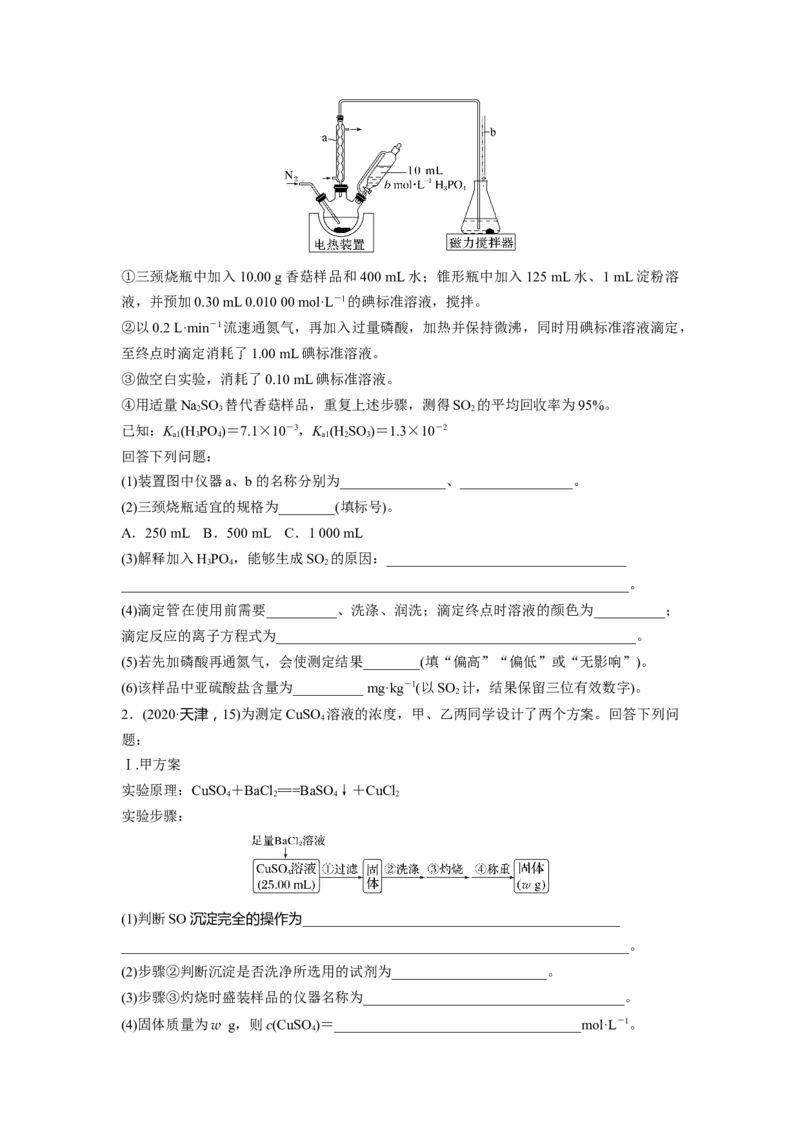
下:①三颈烧瓶中加入10.00 g香菇样品和400 mL水;锥形瓶中加入125 mL水、1 mL淀粉溶
液,并预加0.30 mL 0.010 00 mol·L-1的碘标准溶液,搅拌。
②以0.2 L·min-1流速通氮气,再加入过量磷酸,加热并保持微沸,同时用碘标准溶液滴定,
至终点时滴定消耗了1.00 mL碘标准溶液。
③做空白实验,消耗了0.10 mL碘标准溶液。
④用适量NaSO 替代香菇样品,重复上述步骤,测得SO 的平均回收率为95%。
2 3 2
已知:K (H PO )=7.1×10-3,K (H SO )=1.3×10-2
a1 3 4 a1 2 3
回答下列问题:
(1)装置图中仪器a、b的名称分别为_______________、________________。
(2)三颈烧瓶适宜的规格为________(填标号)。
A.250 mL B.500 mL C.1 000 mL
(3)解释加入HPO ,能够生成SO 的原因:__________________________________
3 4 2
________________________________________________________________________。
(4)滴定管在使用前需要__________、洗涤、润洗;滴定终点时溶液的颜色为__________;
滴定反应的离子方程式为___________________________________________________。
(5)若先加磷酸再通氮气,会使测定结果________(填“偏高”“偏低”或“无影响”)。
(6)该样品中亚硫酸盐含量为__________ mg·kg-1(以SO 计,结果保留三位有效数字)。
2
2.(2020·天津,15)为测定CuSO 溶液的浓度,甲、乙两同学设计了两个方案。回答下列问
4
题:
Ⅰ.甲方案
实验原理:CuSO +BaCl ===BaSO↓+CuCl
4 2 4 2
实验步骤:
(1)判断SO沉淀完全的操作为_____________________________________________
________________________________________________________________________。
(2)步骤②判断沉淀是否洗净所选用的试剂为______________________。
(3)步骤③灼烧时盛装样品的仪器名称为_____________________________________。
(4)固体质量为w g,则c(CuSO )=___________________________________mol·L-1。
4(5)若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测得c(CuSO )______(填“偏高”“偏低”
4
或“无影响”)。
Ⅱ.乙方案
实验原理:Zn+CuSO ===ZnSO+Cu
4 4
Zn+HSO ===ZnSO+H↑
2 4 4 2
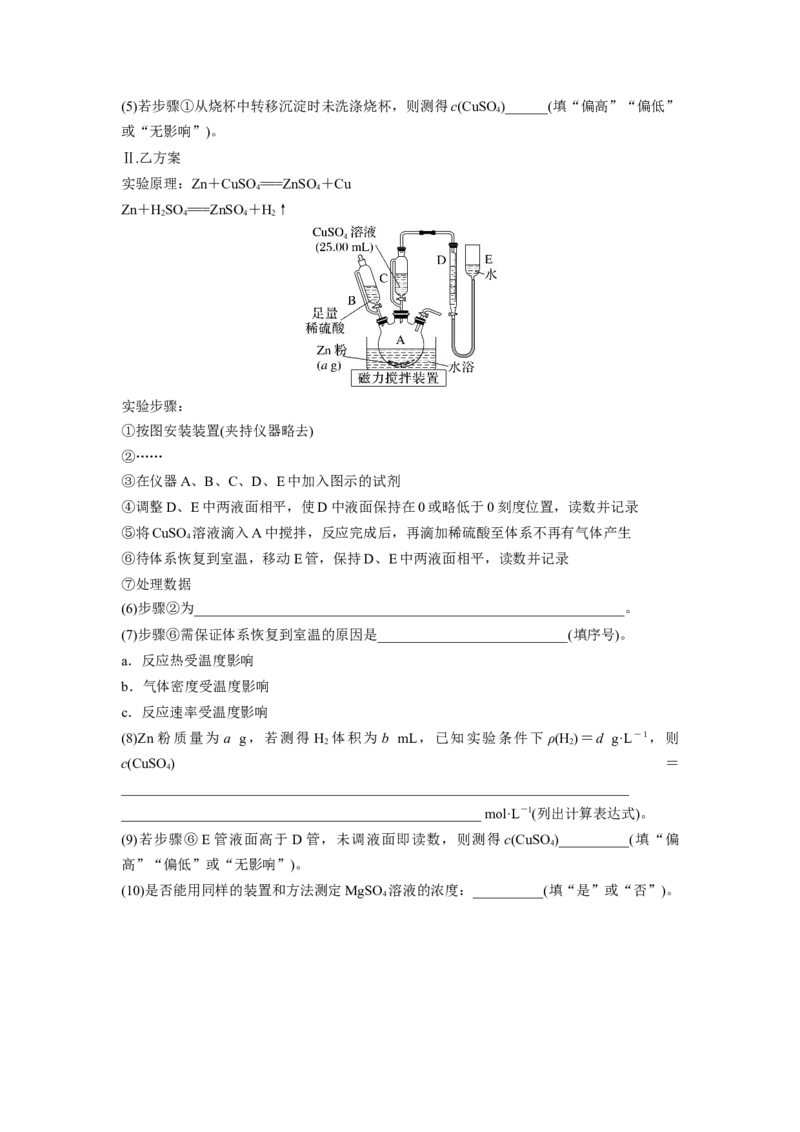
实验步骤:
①按图安装装置(夹持仪器略去)
②……
③在仪器A、B、C、D、E中加入图示的试剂
④调整D、E中两液面相平,使D中液面保持在0或略低于0刻度位置,读数并记录
⑤将CuSO 溶液滴入A中搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生
4
⑥待体系恢复到室温,移动E管,保持D、E中两液面相平,读数并记录
⑦处理数据
(6)步骤②为_____________________________________________________________。
(7)步骤⑥需保证体系恢复到室温的原因是___________________________(填序号)。
a.反应热受温度影响
b.气体密度受温度影响
c.反应速率受温度影响
(8)Zn 粉质量为 a g,若测得 H 体积为 b mL,已知实验条件下 ρ(H )=d g·L-1,则
2 2
c(CuSO ) =
4
________________________________________________________________________
___________________________________________________ mol·L-1(列出计算表达式)。
(9)若步骤⑥E管液面高于D管,未调液面即读数,则测得c(CuSO )__________(填“偏
4
高”“偏低”或“无影响”)。
(10)是否能用同样的装置和方法测定MgSO 溶液的浓度:__________(填“是”或“否”)。
4