文档内容
专题 06 化学反应与能量
第 16 练 化学反应的速率与限度
1.下列表示化学反应速率的单位正确的是( )
A.mol·min-1 B.mol·s-1 C.mol·L-1 D.mol·L-1·s-1
2.不同的化学反应有不同的反应速率,决定化学反应速率的主要因素是( )
A.温度 B.浓度 C.催化剂 D.反应物的性质
3.下列措施一定能使化学反应速率增大的是( )
A.增大反应物的量 B.增大压强 C.升高温度 D.使用催化剂
4.在不同条件下分别测得反应2SO (g)+O(g) 2SO (g)的化学反应速率,其中表示该反应进行得
2 2 3
最快的是( )
A. B.
C. D.
5.反应 在四种不同的情况下进行,表示该反应的化学反应速率最快的是(
)
A. B.
C. D.
6.在铝与稀硫酸的反应中,已知10s末硫酸的浓度减少了0.6 mol/L,若不考虑反应过程中溶液体积的
变化,则10s内生成硫酸铝的平均反应速率是( )
A.0.02 mol/(L•min) B.1.8mol/(L•min) C.1.2 mol/(L•min) D.0.18 mol/(L•min)
7.在一定条件下容积不变的密闭容器中,发生可逆反应N(g)+3H(g) 2NH (g)下列情况不能说明该反
2 2 3
应一定达到化学平衡的是( ) ⇌
A.NH 的质量保持不变 B.N、H 和NH 的物质的量之比为1:3:2
3 2 2 3
C.正反应和逆反应的速率相等 D.容器内压强不再改变
8.下列说法正确的是( )A.既没有气体参与也没有气体生成的反应,压强改变几乎不会影响化学反应速率
B.化学反应速率常用反应物浓度的减少量或生成物浓度的增加量表示
C.平衡时的转化率是指平衡时反应物的物质的量与其初始物质的量之比
D.化学平衡是所有可逆反应都存在的一种状态,达到这一状态时反应停止
9.在一定温度下,向某固定容积的密闭容器中加入1 mol N 和3 mol H ,发生如下反应:N(g)+3H(g)
2 2 2 2
2NH (g)。此反应达到平衡的标志是( )
3
A.容器内气体密度不再发生变化 B.容器内各物质的浓度不再发生变化
C.正反应和逆反应都已停止 D.单位时间消耗0.1 mol N 的同时生成0.2 mol NH
2 3
10.一定温度下在一容积不变的密闭容器中发生可逆反应2X(g) Y(g)+Z(s),以下不能说明该反
应达到化学平衡状态的是 ( )
A.混合气体的密度不再变化
B.反应容器中Y的质量分数不变
C.X的分解速率与Y的消耗速率相等
D.单位时间内生成1 mol Y的同时生成2 mol X
11.在容积不变的密闭容器中发生反应N (g)+3H(g) 2NH (g),下列叙述能说明该反应一定处
2 2 3
于化学平衡状态的是( )
A.N、H、NH 的浓度之比为1∶3∶2
2 2 3
B.N 的正反应速率与NH 的逆反应速率相等
2 3
C.当有 断裂时,有 生成
D.单位时间内生成 ,同时生成
12.在一定温度下的恒容密闭容器中,能说明反应X(g)+Y(g) 2XY(g)已达到平衡状态的是(
2 2
)
A.容器内气体的密度不再变化
B.容器内气体总物质的量不随时间变化而变化
C.每断开1个X—X键的同时,有2个X—Y键形成
D.XY的分解速率是Y 的消耗速率的两倍
2
13.常温下,可逆反应2NO 2NO+O 在恒容密闭容器中进行,下列叙述能够说明反应已达到平
2 2
衡状态的是( )
A.单位时间内生成n mol O 的同时生成2n mol NO
2 2
B.单位时间内生成n mol O 的同时生成2n mol NO
2
C.混合气体的密度不再改变D.容器中NO 、NO、O 的物质的量之比为2∶2∶1
2 2
14.工业制硫酸中一步重要的反应是: SO 在400~ 500 °C的条件下进行催化氧化: 2SO +O
2 2 2
2SO ,其正反应为放热反应,如果该反应是在密闭容器中进行的,下列有关说法中错误的是( )
3
A.使用催化剂是为了加快反应速率,提高生产效率
B.在上述条件下,反应达平衡时容器中存在SO 、O、SO 三种物质
2 2 3
C.达到平衡时,正逆反应速率为0
D.通过调控反应条件,可以提高反应进行的程度
9.一定条件下,将2molA气体和2molB气体通入体积为2L的密闭容器中发生如下反应:2A(g)+B(g)
x C(g) +2D(s),在2min末测得剩余B的物质的量为1.2mol,生成C的物质的量为2.4mol。下列有
关说法错误的是( )
A.x的数值为3
B.2min末,A的浓度为0.2 mol∙L−1
C.2min内,用D表示的反应的平均速率为
D.将容器的容积变为3L,化学反应速率将减小
1.化学反应速率和化学反应的限度是化工生产研究的主要问题,下列对化学反应速率和反应限度的
认识错误的是( )
A.决定化学反应速率的客观因素有温度、浓度、压强和催化剂等
B.对任何化学反应来说,反应速率越快,对应现象越明显
C.使用催化剂能加快反应速率,提高生产效率
D.任何可逆反应都有一定的限度,且限度是可以改变的
2.工业上通常在温度为 ,压强为 合成氨:N(g)+3H(g) 2NH (g),
2 2 3
该反应的正反应是放热反应,如果反应在密闭容器中进行,下列有关说法正确的是( )
A.使用催化剂是为了提高原料的利用率
B.升高温度,增大压强,可以提高反应速率,实现N 的完全转化
2
C.当容器内各物质浓度不再变化时,说明该可逆反应已达到化学平衡状态
D.充入一定量的惰性气体,可以增大该反应速率,提高反应进行的程度
3.把下列四种X溶液分别加入四个盛有10mL 2mol/L盐酸的烧杯中,均加水稀释到50mL,此时,X
和盐酸缓慢地进行反应,其中反应最快的是( )A.10℃20mL 3mol/L的X溶液 B.20℃30mL 2mol/L的X溶液
C.20℃10mL 4mol/L的X溶液 D.10℃10mL 2mol/L的X溶液
4.某实验探究小组模拟汽车尾气催化处理过程,在一定温度下,向5L容积固定的密闭容器中充入
2molCO(g)和2molNO(g),发生反应2CO(g)+2NO(g) N(g)+2CO (g)。下列有关说法一定正确的是(
2 2
)
A.经过足够长时间,NO的浓度能减小为0
B.CO与CO 的浓度之比为1∶1时,此反应一定达到了化学反应限度
2
C.在反应过程中,CO与NO物质的量始终相等
D.在反应过程中,容器中气体的压强一直没有变化
5.在一定条件下发生反应 2SO (g) 2SO (g)+O(g),将2 mol SO 通入2 L容积恒定的密闭容器甲
3 2 2 3
中,若维持容器内温度不变,5 min末测得SO 的物质的量为0.8 mol。则下列说法正确的是( )
3
A.0~5min,SO 的生成速率v(SO )=0.12mol·L-1·min-1
2 2
B.若起始时充入3 mol SO ,起始时SO 分解速率不变
3 3
C.若某时刻消耗了1 molSO 同时生成了0.5molO,则表明该反应达到了平衡状态
3 2
D.达到平衡时,SO 和SO 的浓度相等
2 3
6.一定温度下,体积不变的密闭容器中,可逆反应X(g)+3Y(g) 2Z(g)达到平衡的标志是( )
A.气体总质量保持不变 B.X、Y、Z的浓度都相等
C.X、Y、Z的浓度不再发生变化 D.X、Y、Z的分子数之比为1∶3∶2
7.2SO (g)+O(g) 2SO (g)(反应正向放热)是工业制硫酸的重要反应,下列说法不正确的是( )
2 2 3
A.其他条件不变,使用催化剂能同时提高反应速率和 SO 的平衡转化率
2
B.其他条件不变,升高温度能加快反应速率,但 SO 的平衡转化率降低
2
C.其他条件不变,通入过量空气能提高 SO 的平衡转化率
2
D.其他条件不变,增大压强能同时提高反应速率和 SO 的平衡转化率,但成本增加
2
8.一定温度下,物质的量均为0.3mol的X(g)与Y(g)在容积为2L的恒容密闭容器中发生反应:X(g)
+3Y(g) 2Z(g),5min达到平衡状态,测得密闭容器中Z的物质的量为0.12mol,下列说法错误的是(
)
A.5min内,用Y表示的该反应平均反应速率为0.018mol·L-1·min-1
B.达到平衡时,容器内的压强是反应前的0.4倍
C.达到平衡时,n(X)=2n(Y)
D.达到平衡时,增加少量氦气(不参与反应),反应速率不发生变化
9.在1L的恒容密闭容器中,发生反应:4A (s))+3B(g) 2 C(g) +2D (g), 末B的浓度减
少了 。对该反应反应速率的正确表示是( )A.用A表示的反应速率是
B.用B、C、D分别表示的反应速率,其比值是3∶2∶1
C.在 末用B表示的反应速率为
D. 内,用B表示的反应速率的值逐渐减小,用C表示的反应速率的值逐渐增大
10.在不同条件下进行过氧化氢分解实验,有关数据如下。四组实验中,收集相同体积(折算成标准
状况)的氧气,所需时间最短的一组是( )
组别
A B C D
实验条件
过氧化氢溶液体积/mL 10 10 10 10
过氧化氢溶液质量分数 6% 6% 3% 6%
温度/℃ 20 40 40 40
MnO 质量/g 0.05 0.05 0.05 0
2
11.反应N(g)+3H(g) 2NH (g) ΔH<0,若在恒压绝热容器中发生,下列选项表明反应一定
2 2 3
已达平衡状态的是( )
A.容器内的温度不再变化
B.容器内的压强不再变化
C.相同时间内,断开H-H键的数目和生成N-H键的数目相等
D.容器内气体的浓度c(N ):c(H ):c(NH )=1:3:2
2 2 3
12.一定温度下,在2 L的恒容密闭容器中发生反应A(g)+2B(g) 3C(g)。反应过程中的部分数
据如下表所示:
n/mol
n(A) n(B) n(C)
t/min
0 2.0 2.4 0
5 0.9
10 1.6
15 1.6
下列说法正确的是( )
A.0~5 min用A表示的平均反应速率为0.09 mol·L−1·min−1
B.容器内压强不变,说明反应已达到平衡状态
C.平衡状态时c(C)=0.6 mol·L−1且不再发生变化
D.升高温度,正反应速率增大,逆反应速率减小
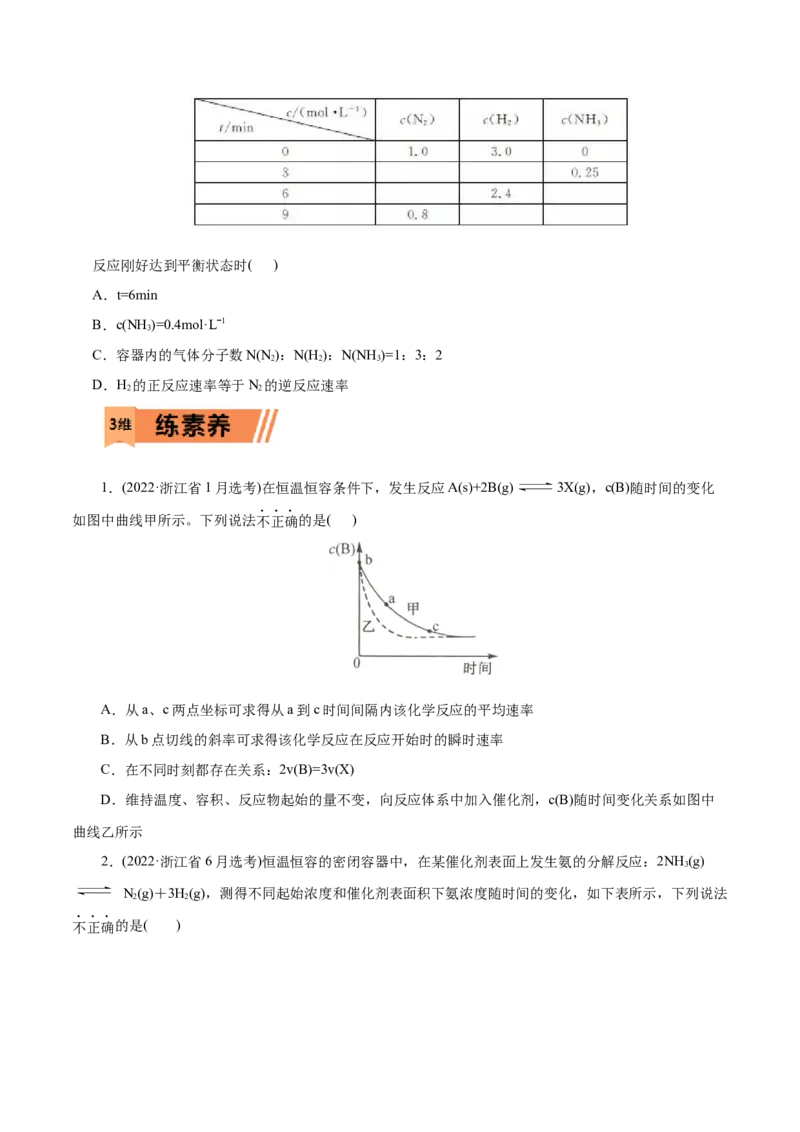
13.一定温度下,在体积恒定的密闭容器中发生反应:N(g)+3H(g) 2NH (g)。反应过程中的部
2 2 3
分数据如下表所示:反应刚好达到平衡状态时( )
A.t=6min
B.c(NH )=0.4mol·Lˉ1
3
C.容器内的气体分子数N(N ):N(H ):N(NH)=1:3:2
2 2 3
D.H 的正反应速率等于N 的逆反应速率
2 2
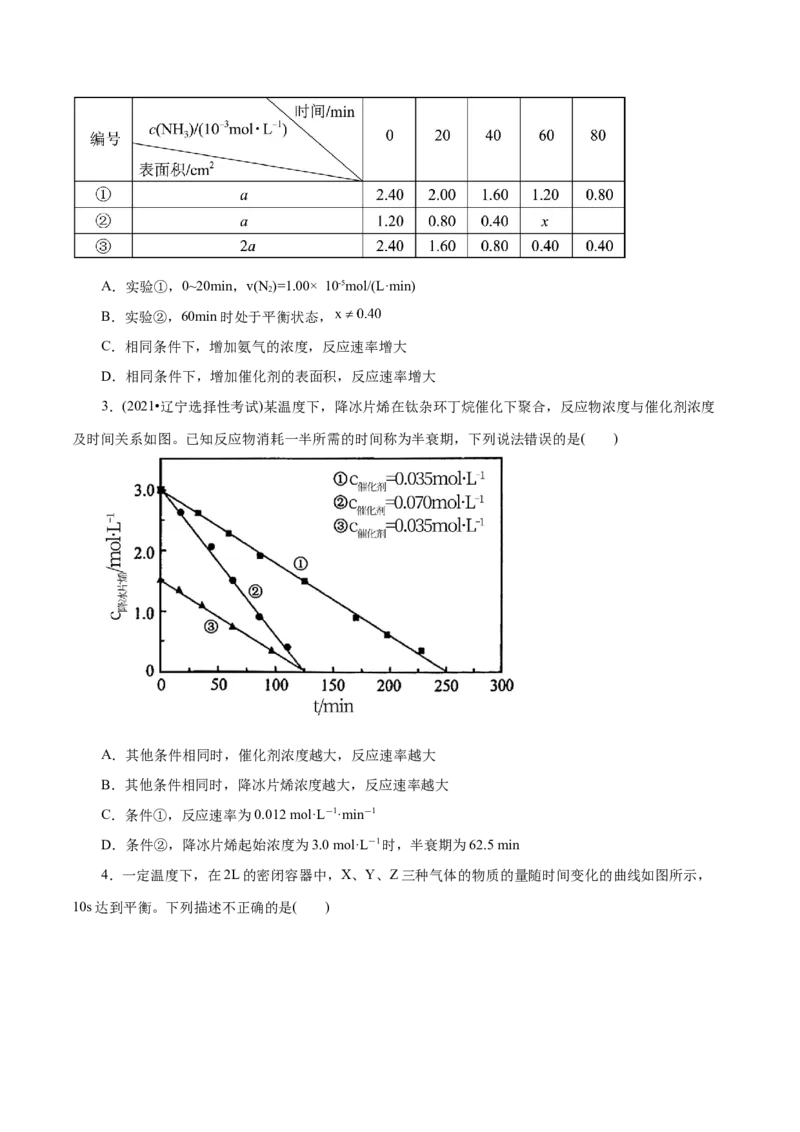
1.(2022·浙江省1月选考)在恒温恒容条件下,发生反应A(s)+2B(g) 3X(g),c(B)随时间的变化
如图中曲线甲所示。下列说法不正确的是( )
A.从a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率
B.从b点切线的斜率可求得该化学反应在反应开始时的瞬时速率
C.在不同时刻都存在关系:2v(B)=3v(X)
D.维持温度、容积、反应物起始的量不变,向反应体系中加入催化剂,c(B)随时间变化关系如图中
曲线乙所示
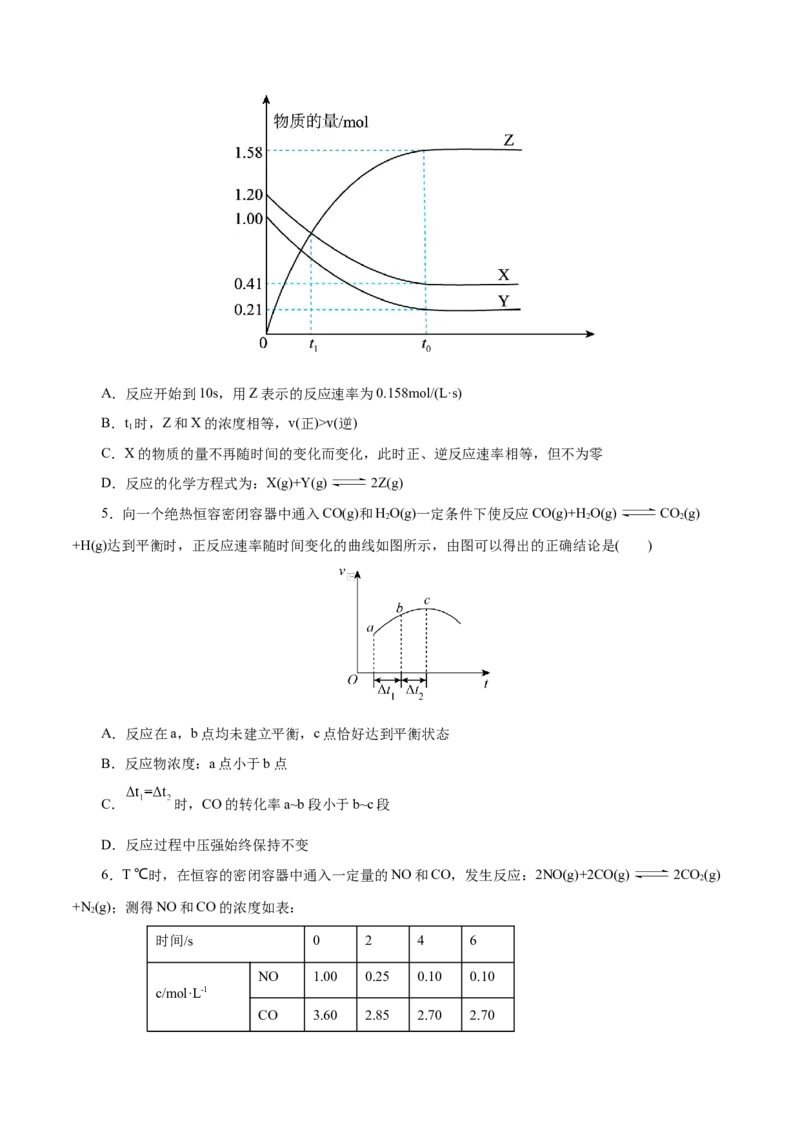
2.(2022·浙江省6月选考)恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应:2NH (g)
3
N(g)+3H(g),测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下列说法
2 2
不正确的是( )A.实验①,0~20min,v(N )=1.00× 10-5mol/(L·min)
2
B.实验②,60min时处于平衡状态,
C.相同条件下,增加氨气的浓度,反应速率增大
D.相同条件下,增加催化剂的表面积,反应速率增大
3.(2021•辽宁选择性考试)某温度下,降冰片烯在钛杂环丁烷催化下聚合,反应物浓度与催化剂浓度
及时间关系如图。已知反应物消耗一半所需的时间称为半衰期,下列说法错误的是( )
A.其他条件相同时,催化剂浓度越大,反应速率越大
B.其他条件相同时,降冰片烯浓度越大,反应速率越大
C.条件①,反应速率为0.012 mol·L-1·min-1
D.条件②,降冰片烯起始浓度为3.0 mol·L-1时,半衰期为62.5 min
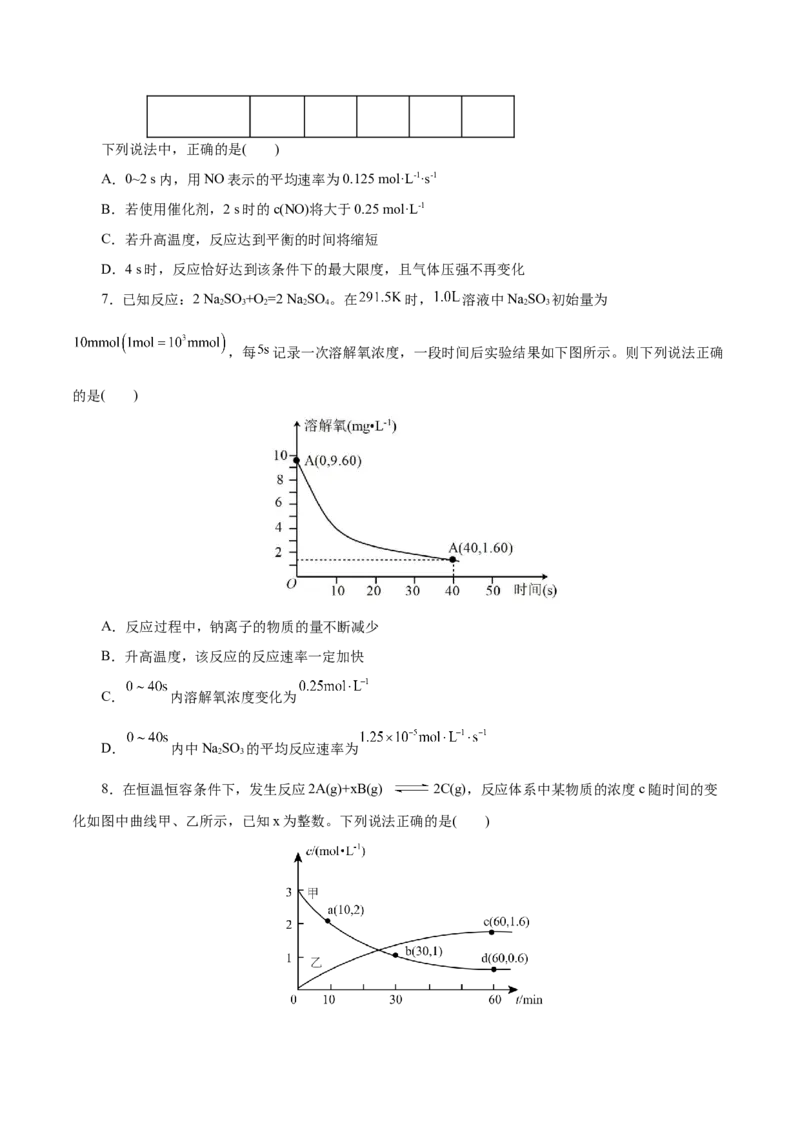
4.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,
10s达到平衡。下列描述不正确的是( )A.反应开始到10s,用Z表示的反应速率为0.158mol/(L·s)
B.t 时,Z和X的浓度相等,v(正)>v(逆)
1
C.X的物质的量不再随时间的变化而变化,此时正、逆反应速率相等,但不为零
D.反应的化学方程式为:X(g)+Y(g) 2Z(g)
5.向一个绝热恒容密闭容器中通入CO(g)和HO(g)一定条件下使反应CO(g)+HO(g) CO(g)
2 2 2
+H(g)达到平衡时,正反应速率随时间变化的曲线如图所示,由图可以得出的正确结论是( )
A.反应在a,b点均未建立平衡,c点恰好达到平衡状态
B.反应物浓度:a点小于b点
C. 时,CO的转化率a~b段小于b~c段
D.反应过程中压强始终保持不变
6.T ℃时,在恒容的密闭容器中通入一定量的NO和CO,发生反应:2NO(g)+2CO(g) 2CO(g)
2
+N (g);测得NO和CO的浓度如表:
2
时间/s 0 2 4 6
NO 1.00 0.25 0.10 0.10
c/mol·L-1
CO 3.60 2.85 2.70 2.70下列说法中,正确的是( )
A.0~2 s内,用NO表示的平均速率为0.125 mol·L-1·s-1
B.若使用催化剂,2 s时的c(NO)将大于0.25 mol·L-1
C.若升高温度,反应达到平衡的时间将缩短
D.4 s时,反应恰好达到该条件下的最大限度,且气体压强不再变化
7.已知反应:2 Na SO +O =2 Na SO 。在 时, 溶液中NaSO 初始量为
2 3 2 2 4 2 3
,每 记录一次溶解氧浓度,一段时间后实验结果如下图所示。则下列说法正确
的是( )
A.反应过程中,钠离子的物质的量不断减少
B.升高温度,该反应的反应速率一定加快
C. 内溶解氧浓度变化为
D. 内中NaSO 的平均反应速率为
2 3
8.在恒温恒容条件下,发生反应2A(g)+xB(g) 2C(g),反应体系中某物质的浓度c随时间的变
化如图中曲线甲、乙所示,已知x为整数。下列说法正确的是( )A.x=3
B.曲线乙表示的是物质A在反应进程中的浓度变化
C.10~30min内v(C)=0.05mol·L-1·min-1
D.c点对应物质的浓度与d点对应物质的浓度相等
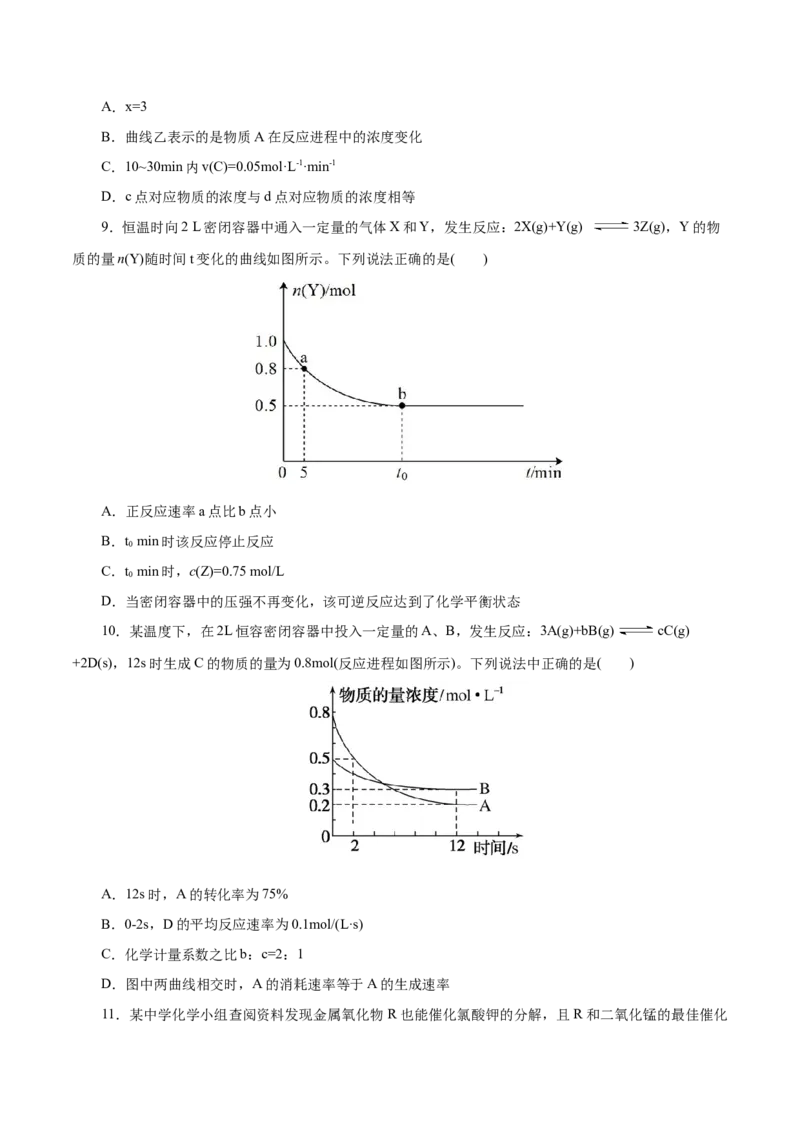
9.恒温时向2 L密闭容器中通入一定量的气体X和Y,发生反应:2X(g)+Y(g) 3Z(g),Y的物
质的量n(Y)随时间t变化的曲线如图所示。下列说法正确的是( )
A.正反应速率a点比b点小
B.t min时该反应停止反应
0
C.t min时,c(Z)=0.75 mol/L
0
D.当密闭容器中的压强不再变化,该可逆反应达到了化学平衡状态
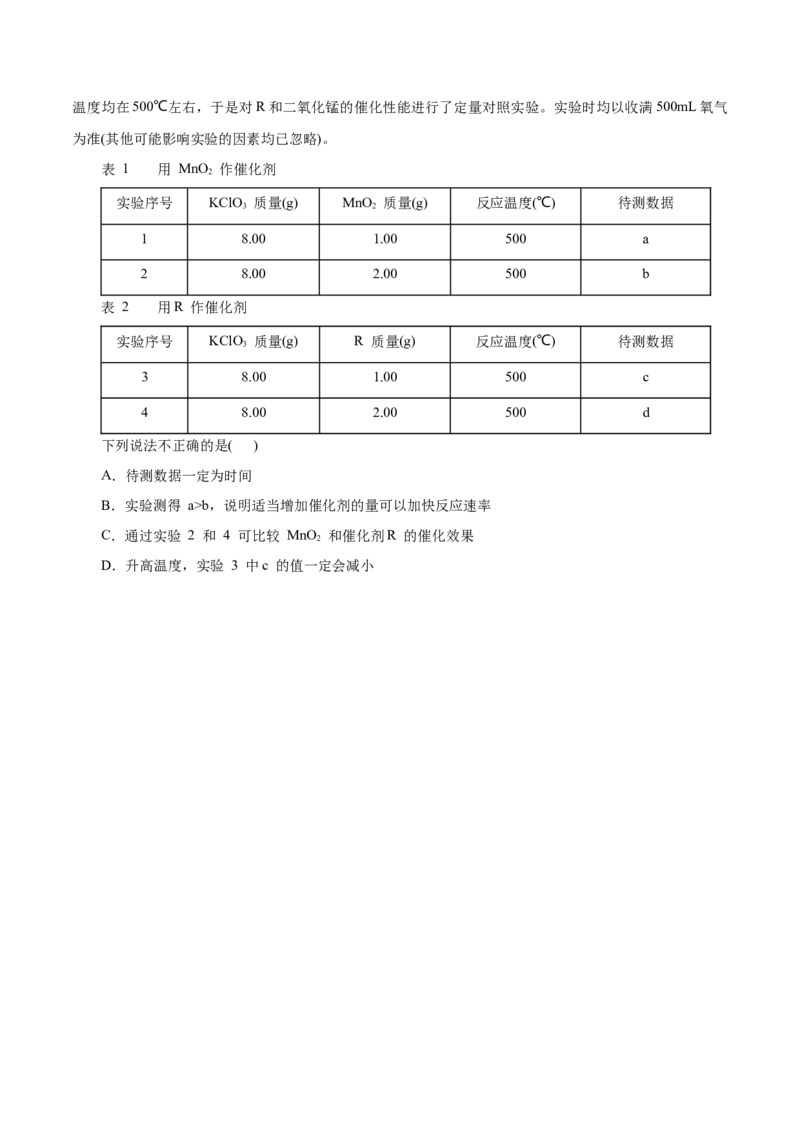
10.某温度下,在2L恒容密闭容器中投入一定量的A、B,发生反应:3A(g)+bB(g) cC(g)
+2D(s),12s时生成C的物质的量为0.8mol(反应进程如图所示)。下列说法中正确的是( )
A.12s时,A的转化率为75%
B.0-2s,D的平均反应速率为0.1mol/(L·s)
C.化学计量系数之比b:c=2:1
D.图中两曲线相交时,A的消耗速率等于A的生成速率
11.某中学化学小组查阅资料发现金属氧化物R也能催化氯酸钾的分解,且R和二氧化锰的最佳催化温度均在500℃左右,于是对R和二氧化锰的催化性能进行了定量对照实验。实验时均以收满500mL氧气
为准(其他可能影响实验的因素均已忽略)。
表 1 用 MnO 作催化剂
2
实验序号 KClO 质量(g) MnO 质量(g) 反应温度(℃) 待测数据
3 2
1 8.00 1.00 500 a
2 8.00 2.00 500 b
表 2 用R 作催化剂
实验序号 KClO 质量(g) R 质量(g) 反应温度(℃) 待测数据
3
3 8.00 1.00 500 c
4 8.00 2.00 500 d
下列说法不正确的是( )
A.待测数据一定为时间
B.实验测得 a>b,说明适当增加催化剂的量可以加快反应速率
C.通过实验 2 和 4 可比较 MnO 和催化剂R 的催化效果
2
D.升高温度,实验 3 中c 的值一定会减小