文档内容
非金属及其化合物
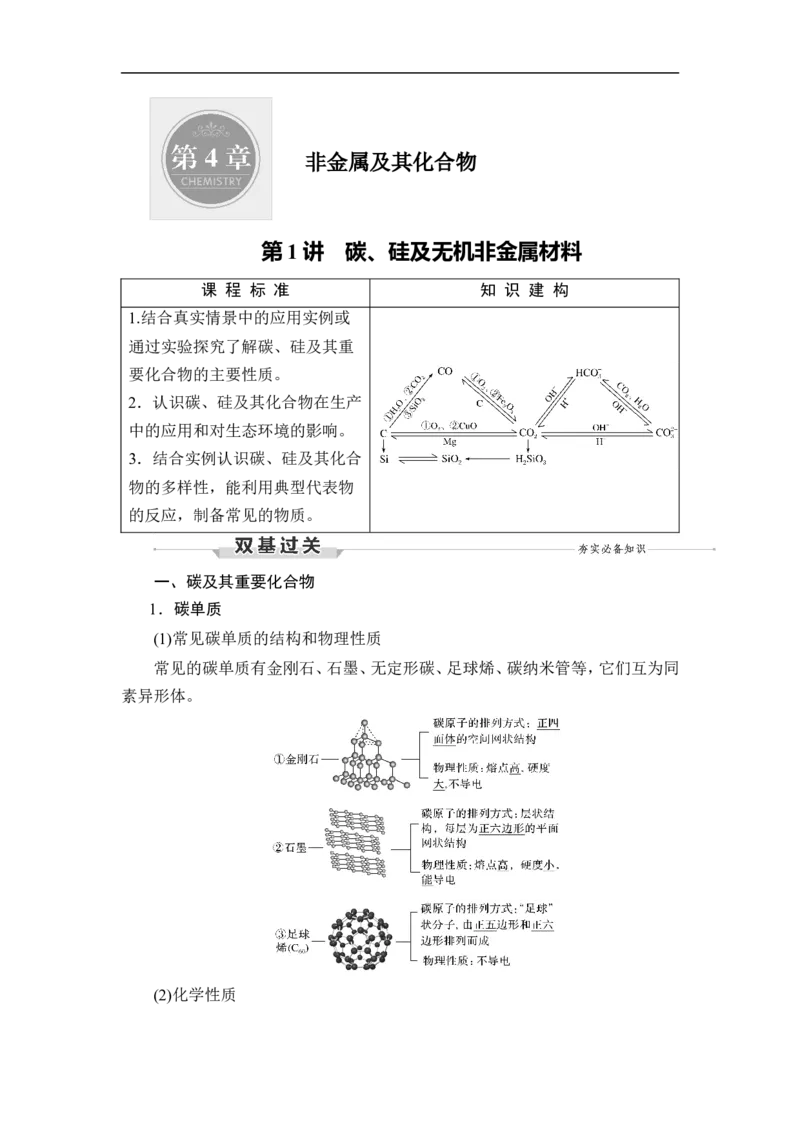
第 1 讲 碳、硅及无机非金属材料
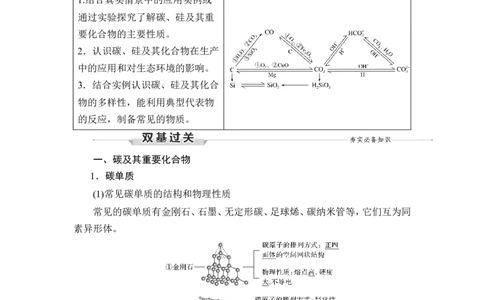
课 程 标 准 知 识 建 构
1.结合真实情景中的应用实例或
通过实验探究了解碳、硅及其重
要化合物的主要性质。
2.认识碳、硅及其化合物在生产
中的应用和对生态环境的影响。
3.结合实例认识碳、硅及其化合
物的多样性,能利用典型代表物
的反应,制备常见的物质。
一、碳及其重要化合物
1.碳单质
(1)常见碳单质的结构和物理性质
常见的碳单质有金刚石、石墨、无定形碳、足球烯、碳纳米管等,它们互为同
素异形体。
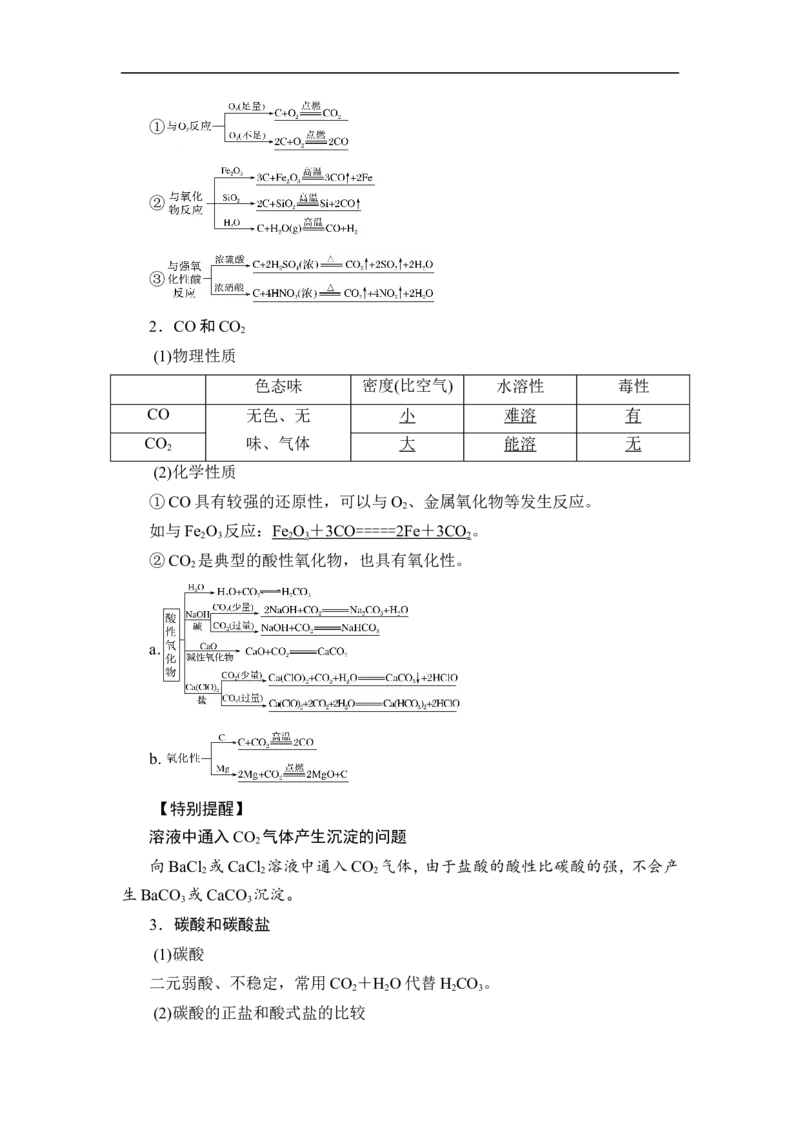
(2)化学性质①
②
③
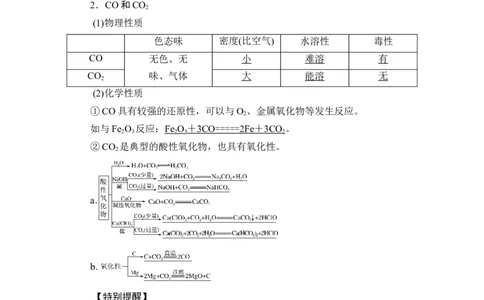
2.CO和CO
2
(1)物理性质
色态味 密度(比空气) 水溶性 毒性
CO 无色、无 小 难溶 有
CO 味、气体 大 能溶 无
2
(2)化学性质
①CO具有较强的还原性,可以与O 、金属氧化物等发生反应。
2
如与Fe O 反应:Fe O + 3CO ==== = 2F e + 3CO 。
2 3 2 3 2
②CO 是典型的酸性氧化物,也具有氧化性。
2
a.
b.
【特别提醒】
溶液中通入CO 气体产生沉淀的问题
2
向BaCl 或CaCl 溶液中通入CO 气体,由于盐酸的酸性比碳酸的强,不会产
2 2 2
生BaCO 或CaCO 沉淀。
3 3
3.碳酸和碳酸盐
(1)碳酸
二元弱酸、不稳定,常用CO +H O代替H CO 。
2 2 2 3
(2)碳酸的正盐和酸式盐的比较正盐(CO) 酸式盐(HCO)
溶解性 只有钾、钠、铵盐可溶 一般都可溶
热稳定性 正盐>酸式盐
溶液pH 同浓度:正盐>酸式盐
CO
相互转化
HCO
【诊断1】 判断下列说法是否正确,正确的打√,错误的打×。
(1)石墨烯、足球烯结构不同,但都属于烯烃( )
(2)石墨转变为金刚石的反应属于氧化还原反应( )
(3)向空气中排放二氧化碳会形成酸雨( )
(4)向CaCl 溶液中通入CO 气体,溶液变浑浊,继续通入CO 至过量,浑浊消
2 2 2
失( )
(5)氨化的饱和食盐水中通入足量的CO 气体,会析出晶体( )
2
(6)碳酸钡可用于胃肠X射线造影检查( )
答案 (1)× (2)× (3)× (4)× (5)√ (6)×
二、硅 无机非金属材料
1.硅
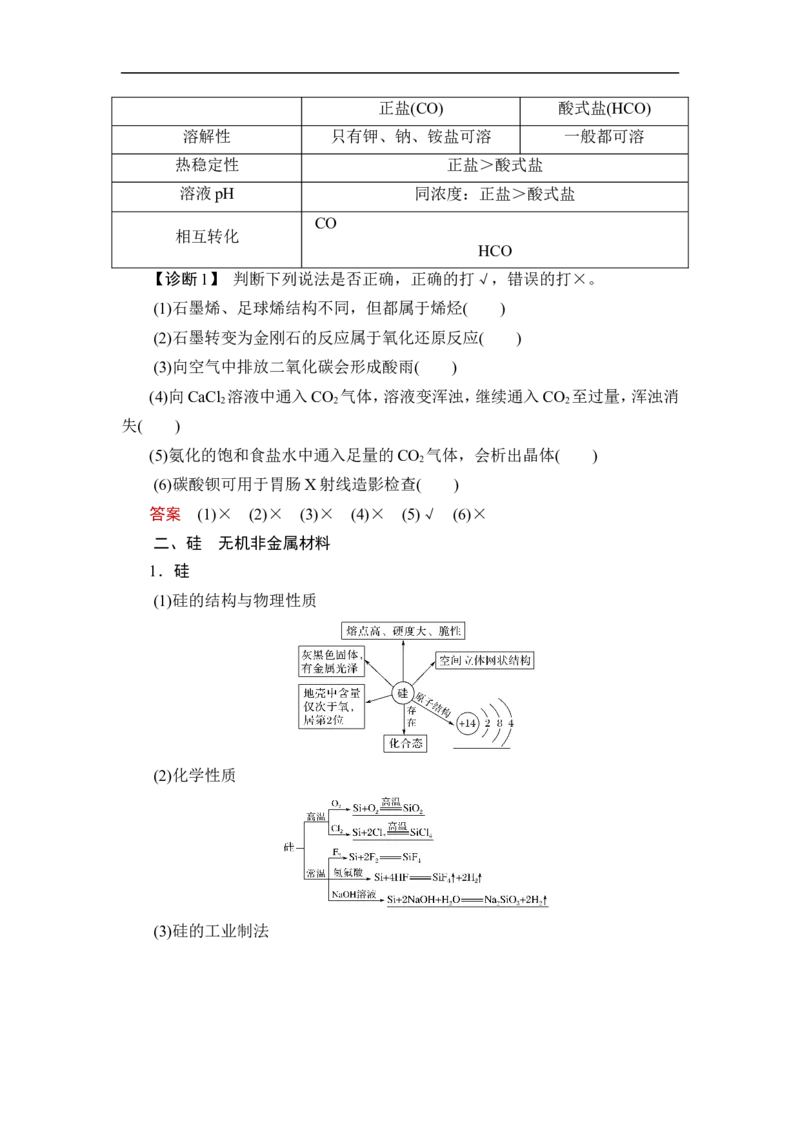
(1)硅的结构与物理性质
(2)化学性质
(3)硅的工业制法(4)用途:半导体材料、太阳能电池、计算机芯片。
2.二氧化硅
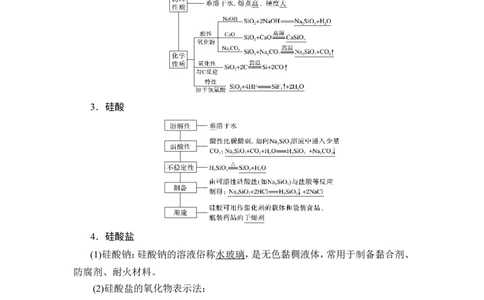
3.硅酸
4.硅酸盐
(1)硅酸钠:硅酸钠的溶液俗称水玻璃,是无色黏稠液体,常用于制备黏合剂、
防腐剂、耐火材料。
(2)硅酸盐的氧化物表示法:
氧化物的书写顺序:活泼金属氧化物→较活泼金属氧化物→二氧化硅→水,
不同氧化物间以“·”隔开。
如硅酸钠(Na SiO )可表示为Na O·SiO ,
2 3 2 2
长石(KAlSi O )可表示为K O·Al O ·6SiO 。
3 8 2 2 3 2
【特别提醒】
硅酸盐的氧化物写法中系数的配置原则
硅酸盐改写为氧化物形式时,各元素的化合价保持不变,且满足化合价代数
和为零,各元素原子个数比符合原来的组成。当系数配置出现分数时一般应化为整数。如上例中KAlSi O ,将K O·Al O ·3SiO ,写成K O·Al O ·6SiO 。
3 8 2 2 3 2 2 2 3 2
5.无机非金属材料
(1)传统无机非金属材料,如水泥、玻璃、陶瓷等硅酸盐材料。
①常见硅酸盐材料比较
水泥 玻璃 陶瓷
生产原料 石灰石、黏土 纯碱、石灰石、石英 黏土
主要设备 水泥回转窑 玻璃窑 陶瓷窑
②玻璃生产中的两个重要反应:Na CO + SiO ==== = N a SiO + CO ↑;CaCO
2 3 2 2 3 2 3
+ SiO ==== = CaSiO + CO ↑。
2 3 2
(2)新型无机非金属材料,如高温结构陶瓷、光导纤维、生物陶瓷、压电陶瓷等
【诊断2】 判断下列说法是否正确,正确的打√,错误的打×。
(1)硅在自然界中只以化合态的形式存在( )
(2)晶体硅熔点高、硬度大,故可用于制作半导体材料( )
(3)Si和SiO 都可用于制造光导纤维( )
2
(4)非金属性:C>Si,则热稳定性:CH >SiH ( )
4 4
(5)硅的化学性质不活泼,常温下不与任何物质反应( )
(6)SiO 是酸性氧化物,可溶于强碱,不溶于任何酸( )
2
(7)水玻璃是一种特殊的玻璃,泡花碱属于碱( )
答案 (1)√ (2)× (3)× (4)√ (5)× (6)× (7)×
考点一 碳及其化合物的性质及应用
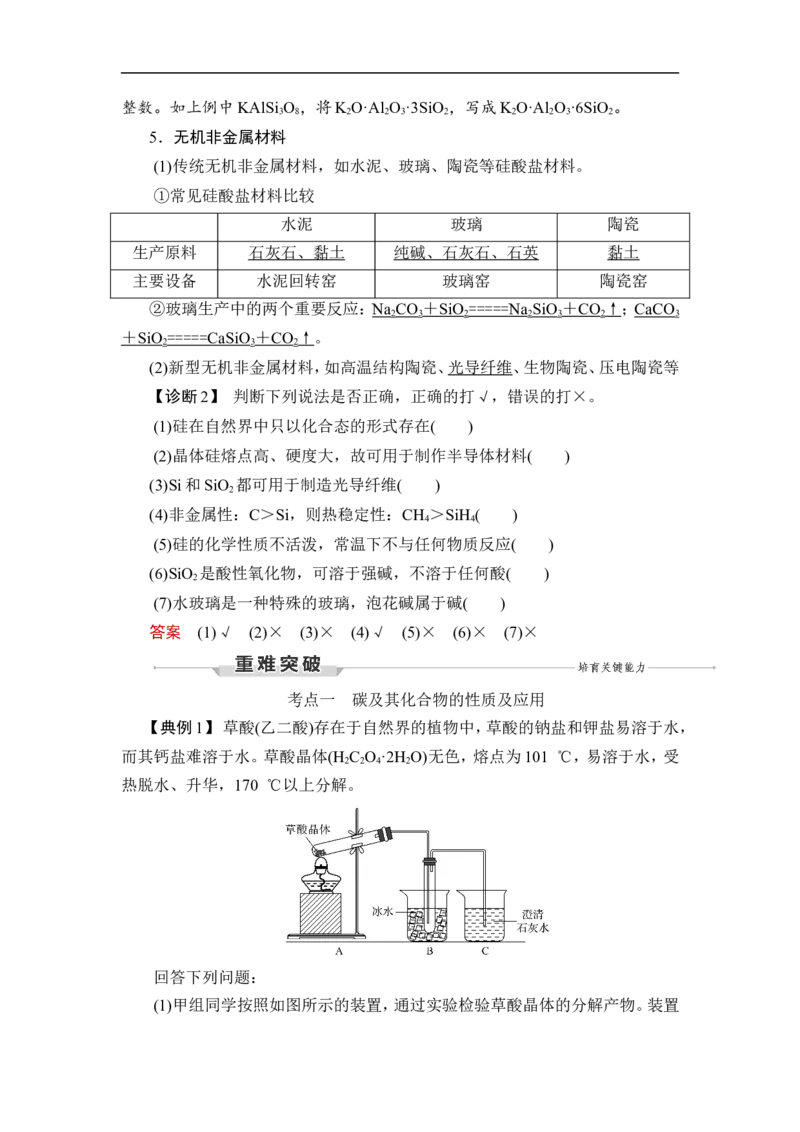
【典例1】 草酸(乙二酸)存在于自然界的植物中,草酸的钠盐和钾盐易溶于水,
而其钙盐难溶于水。草酸晶体(H C O ·2H O)无色,熔点为101 ℃,易溶于水,受
2 2 4 2
热脱水、升华,170 ℃以上分解。
回答下列问题:
(1)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物。装置C中可观察到的现象是____________________________________________,
反应的离子方程式为____________________________________________,
说明分解产物中含有________。装置B的主要作用是
_________________________________________________________________
___________________________________________________________________。
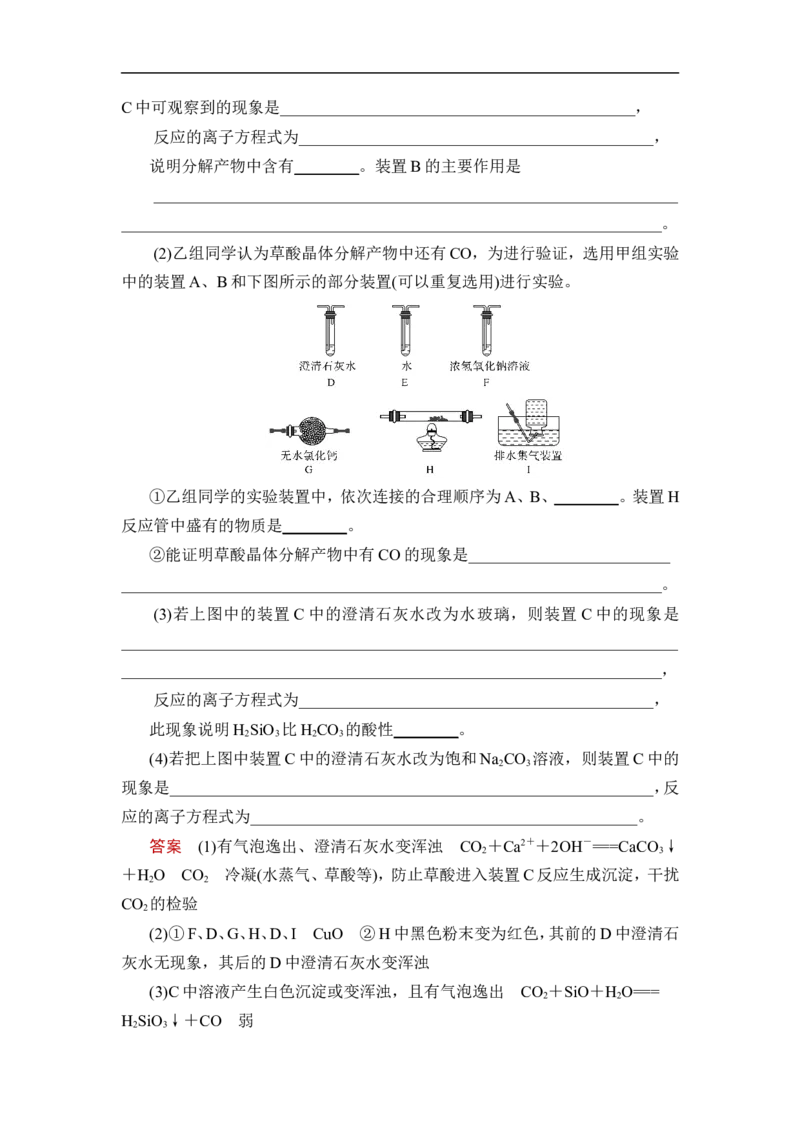
(2)乙组同学认为草酸晶体分解产物中还有CO,为进行验证,选用甲组实验
中的装置A、B和下图所示的部分装置(可以重复选用)进行实验。
①乙组同学的实验装置中,依次连接的合理顺序为A、B、________。装置H
反应管中盛有的物质是________。
②能证明草酸晶体分解产物中有CO的现象是_________________________
___________________________________________________________________。
(3)若上图中的装置 C中的澄清石灰水改为水玻璃,则装置 C中的现象是
_____________________________________________________________________
___________________________________________________________________,
反应的离子方程式为____________________________________________,
此现象说明H SiO 比H CO 的酸性________。
2 3 2 3
(4)若把上图中装置C中的澄清石灰水改为饱和Na CO 溶液,则装置C中的
2 3
现象是____________________________________________________________,反
应的离子方程式为________________________________________________。
答案 (1)有气泡逸出、澄清石灰水变浑浊 CO +Ca2++2OH-===CaCO ↓
2 3
+H O CO 冷凝(水蒸气、草酸等),防止草酸进入装置C反应生成沉淀,干扰
2 2
CO 的检验
2
(2)①F、D、G、H、D、I CuO ②H中黑色粉末变为红色,其前的D中澄清石
灰水无现象,其后的D中澄清石灰水变浑浊
(3)C中溶液产生白色沉淀或变浑浊,且有气泡逸出 CO +SiO+H O===
2 2
H SiO ↓+CO 弱
2 3(4)产生白色沉淀或变浑浊,有气泡逸出 2Na++CO+CO +H O===
2 2
2NaHCO ↓
3
解析 (1)草酸受热分解可能生成CO 、H O,CO 能使澄清石灰水变浑浊,故
2 2 2
在C观察到的现象为有气泡产生,澄清石灰水变浑浊;根据C中澄清石灰水变浑
浊可知草酸晶体分解产物中有CO ;草酸和Ca2+反应生成难溶物草酸钙,冰水起
2
到冷凝水蒸气和草酸的作用,防止草酸进入装置 C和Ca2+反应生成沉淀,干扰
CO 的检验。
2
(2)①要检验草酸分解产物可能存在CO,可通过先除去CO 和可能蒸发出的
2
未分解的草酸,可通过将气体通入浓氢氧化钠溶液除去CO ,之后对气体进行干
2
燥处理,则需通入无水氯化钙,然后再通入灼热的CuO,若有CO,则发生反应CO
+CuO=====Cu+CO ,再将产生的气体通入澄清石灰水中检验是否有CO 生成,
2 2
由于CO不一定完全反应,CO为有毒气体,则最后需连接尾气处理装置,故依次
连接的合理顺序为A、B、F、D、G、H、D、I;CO和CuO反应生成CO 和Cu,故装
2
置H中的物质为CuO。
②若存在CO,CO+CuO=====Cu+CO ,H中黑色的CuO被还原为红色Cu,
2
同时生成CO ,则D中观察到澄清石灰水变浑浊。
2
检验CO 中是否存在CO的装置及作用
2
各装置的作用是:
A——除去混合气体中的CO
2
B——检验混合气体中CO 是否除尽
2
C——干燥气体
D——CO还原CuO:CO+CuO=====Cu+CO
2
E——安全瓶,防倒吸
F——验证CO的氧化产物CO
2
G——除去尾气中的CO,防止污染环境
确定混合气体中含有CO的实验现象是:
D中的物质由黑色变成光亮的红色,B中无明显现象,F中的澄清石灰水变浑浊。
【对点练 1】 (CO 的性质)(2020·安徽省淮北模拟)有以下六种饱和溶液
2
①CaCl ;②Ca(OH) ;③Na SiO ;④Na CO ;⑤NaAlO ;⑥NH 和NaCl。分别持
2 2 2 3 2 3 2 3
续通入CO ,最终不会得到沉淀或析出晶体的是( )
2
A.①② B.③⑤
C.①⑥ D.④⑥
答案 A
解析 ①碳酸比盐酸酸性弱,CO 与CaCl 溶液不会反应,无沉淀生成,故①
2 2
正确;②酸性氧化物能与碱反应,过量的 CO 与 Ca(OH) 反应:Ca(OH) +
2 2 2
2CO ===Ca(HCO ) ,无沉淀生成,故②正确;③碳酸比硅酸强,过量的CO 与
2 3 2 2
Na SiO 溶液反应:2CO +Na SiO +2H O ===2NaHCO +H SiO ↓,产生硅酸沉
2 3 2 2 3 2 3 2 3
淀,故③错误;④过量的CO 通入饱和Na CO 溶液中发生反应:Na CO +H O+
2 2 3 2 3 2
CO ===2NaHCO ↓,因为相同温度下碳酸氢钠溶解度比碳酸钠小,所以有
2 3
NaHCO 晶体析出,故④错误;⑤NaAlO 溶液通入过量的二氧化碳,由于碳酸酸
3 2
性比氢氧化铝强,所以生成氢氧化铝白色沉淀和碳酸氢钠,2H O+NaAlO +
2 2
CO ===Al(OH) ↓+NaHCO ,故⑤错误;⑥通入CO 与NH 和NaCl反应生成氯
2 3 3 2 3
化铵和碳酸氢钠,碳酸氢钠的溶解度较小,则最终析出碳酸氢钠晶体,故⑥错误;
故选A。
【对点练2】 (碳的氧化物的性质及应用)(2020·湘赣皖十五校第一次联考模拟
题)通过资源化利用的方式将CO 转化为具有工业应用价值的产品(如图所示),是
2
一种较为理想的减排方式,下列说法中不正确的是( )
A.CO 经催化分解为C、CO、O 的反应为吸热反应
2 2
B.除去Na CO 固体中少量NaHCO 可用热分解的方法
2 3 3
C.过氧化尿素和SO 都能使品红溶液褪色,其原理不相同
2D.由CO 和H 合成甲醇,原子利用率达100%
2 2
答案 D
解析 该反应应为吸热反应,A正确;碳酸氢钠受热易分解生成碳酸钠、水和
二氧化碳,因此除去Na CO 固体中少量NaHCO 可用热分解的方法,B正确;过
2 3 3
氧化尿素使品红溶液褪色是利用它的强氧化性,而二氧化硫使品红溶液褪色是利
用它与品红化合生成不稳定的无色物质,原理不相同,C正确;由碳氧原子个数
比可知,二氧化碳与氢气合成甲醇的原子利用率不是100%,D错误。
考点二 硅、无机非金属材料的性质与应用
【典例2】 将足量CO 气体通入Na SiO 溶液中,然后加热蒸干,再在高温下
2 2 3
充分灼烧,最后得到的固体物质是( )
A.Na SiO B.Na CO 、Na SiO
2 3 2 3 2 3
C.Na CO 、SiO D.SiO
2 3 2 2
答案 A
解析 将足量CO 气体通入水玻璃中,发生反应:2CO +Na SiO +
2 2 2 3
2H O===H SiO ↓+2NaHCO ;加热蒸干高温灼烧时发生反应:H SiO =====H O
2 2 3 3 2 3 2
+SiO 2NaHCO =====Na CO +CO ↑+H O;SiO +Na CO =====Na SiO +
2, 3 2 3 2 2 2 2 3 2 3
CO ↑,最后所得固体物质是Na SiO ,故选A。
2 2 3
【对点练3】 (硅和二氧化硅的特性)由下列实验事实得出的结论正确的是(
)
A.由SiO 不能与水反应生成H SiO ,可知SiO 不是H SiO 的酸酐
2 2 3 2 2 3
B.由SiO +2C=====Si+2CO↑,可知碳的非金属性强于硅
2
C.CO 通入Na SiO 溶液产生白色沉淀,可知酸性H CO >H SiO
2 2 3 2 3 2 3
D.SiO 可与NaOH溶液反应,也可与氢氟酸反应,可知SiO 为两性氧化物
2 2
答案 C
【对点练4】 (硅酸盐的性质和写法)(2020·湖南怀化市高三期末)青石棉是一
种致癌物质,是《鹿特丹公约》中受限制的46种化学品之一,其化学式为
Na Fe Si O (OH) 。青石棉用稀硝酸处理时,还原产物只有NO,下列说法不正确
2 5 8 22 2
的是( )
A.青石棉是一种硅酸盐产品
B.青石棉中含有一定量的石英晶体
C.青石棉的化学组成可表示为Na O·3FeO·Fe O ·8SiO ·H O
2 2 3 2 2
D.1 mol青石棉能还原1 mol HNO
3答案 B
解析 硅酸盐指的是Si、O与其他化学元素结合而成的化合物的总称,根据
青石棉的化学式可知,青石棉是一种硅酸盐产品,故A说法正确;硅酸盐中不含
有SiO ,因此青石棉中不含石英晶体,故B说法错误;按照硅酸盐写成氧化物形
2
式,青石棉的化学式组成用氧化物的形式可表示为Na O·3FeO·Fe O ·8SiO ·H O,
2 2 3 2 2
故C说法正确;根据C选项分析,青石棉中含有+2价的铁,与硝酸发生氧化还原
反应,根据得失电子数目守恒可知,1 mol青石棉能还原1 mol HNO ,故D说法正
3
确。
【对点练5】 (无机非金属材料)硅是构成无机非金属材料的一种主要元素,下
列有关硅的化合物的叙述错误的是( )
A.氮化硅陶瓷是一种新型无机非金属材料,其化学式为Si N
3 4
B.碳化硅(SiC)的硬度大,其硬度大于金刚石的硬度
C.光导纤维是一种新型无机非金属材料,其主要成分为SiO
2
D.二氧化硅为立体网状结构,其晶体中硅原子和硅氧单键个数之比为1∶4
答案 B
1.(2020·山东学业水平等级考试,4)下列关于C、Si及其化合物结构与性质
的论述错误的是( )
A.键能C—C>Si—Si、C—H>Si—H,因此C H 稳定性大于Si H
2 6 2 6
B.立方型SiC是与金刚石成键、结构均相似的共价晶体,因此具有很高的硬
度
C.SiH 中Si的化合价为+4,CH 中C的化合价为-4,因此SiH 还原性小于
4 4 4
CH
4
D.Si原子间难形成双键而C原子间可以,是因为Si的原子半径大于C,难
形成p—p π键
答案 C
解析 化合物中键能越大,该物质越稳定,由于键能C—C>Si—Si、C—H>Si
—H,故可判断稳定性:C H >Si H ,A项正确;SiC与金刚石均为立体网状的共价
2 6 2 6
晶体,二者成键和结构均相似,均具有很高的硬度,B项正确;根据非金属性
C>Si,可知还原性:SiH >CH ,C项错误;由于原子半径:Si>C,Si原子间难形成p
4 4
-p π键,故决定了Si原子间很难形成双键,D项正确。
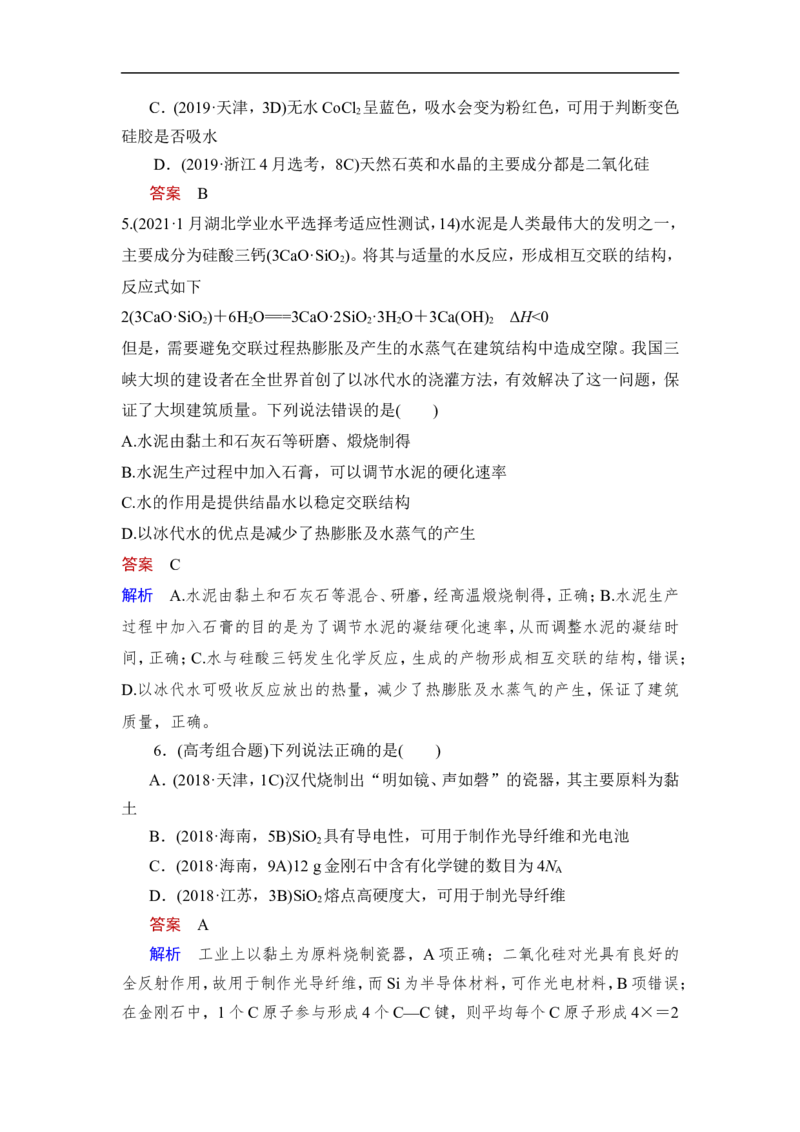
2.(2020·课标全国Ⅱ,9)二氧化碳的过量排放可对海洋生物的生存环境造成很大影响,其原理如图所示。下列叙述错误的是( )
A.海水酸化能引起HCO浓度增大、CO浓度减小
B.海水酸化能促进CaCO 的溶解,导致珊瑚礁减少
3
C.CO 能引起海水酸化,其原理为HCOH++CO
2
D.使用太阳能、氢能等新能源可改善珊瑚的生存环境
答案 C
解析 根据图示可知CO 的过量排放,能导致海水中CO +H OH CO
2 2 2 2 3
H++HCO平衡右移;H+又能与珊瑚礁溶解生成的CO结合生成HCO,促使
CaCO Ca2++CO平衡右移,从而使珊瑚礁减少。结合上述分析可知海水酸化
3
海水中H+和HCO的浓度均增大,使海水中CO的浓度减小,A项正确;H+可结
合珊瑚礁溶解产生的CO,故能促进CaCO 的溶解,使珊瑚礁减少,B项正确;CO
3 2
引起海水酸化的原理为CO +H OH CO H++HCO,C项错误;使用太阳
2 2 2 3
能、氢能等新能源,能有效减少CO 的排放,利于改善珊瑚的生存环境,D项正确。
2
3.(2020·7月浙江选考,24)Ca SiO 是硅酸盐水泥的重要成分之一,其相关性
3 5
质的说法不正确的是( )
A.可发生反应:Ca SiO +4NH Cl=====CaSiO +2CaCl +4NH ↑+2H O
3 5 4 3 2 3 2
B.具有吸水性,需要密封保存
C.能与SO 反应生成新盐
2
D.与足量盐酸作用,所得固体产物主要为SiO
2
答案 D
解析 加热时氯化铵分解生成HCl和氨气,HCl与Ca SiO 反应得到硅酸钙、
3 5
氯化钙和水,A项正确;水泥吸水会变硬,需密封保存,B项正确;Ca SiO 能与二
3 5
氧化硫反应得到亚硫酸钙,C项正确;由上述分析可知,Ca SiO 与足量盐酸反应
3 5
得不到二氧化硅,D项错误。
4.(高考组合题)化学与生活密切相关。下列叙述错误的是( )
A.(2019·全国卷Ⅲ,7A)高纯硅可用于制作光感电池
B.(2019·全国卷Ⅲ,7C)活性炭具有除异味和杀菌作用C.(2019·天津,3D)无水CoCl 呈蓝色,吸水会变为粉红色,可用于判断变色
2
硅胶是否吸水
D.(2019·浙江4月选考,8C)天然石英和水晶的主要成分都是二氧化硅
答案 B
5.(2021·1月湖北学业水平选择考适应性测试,14)水泥是人类最伟大的发明之一,
主要成分为硅酸三钙(3CaO·SiO )。将其与适量的水反应,形成相互交联的结构,
2
反应式如下
2(3CaO·SiO )+6H O===3CaO·2SiO ·3H O+3Ca(OH) ΔH<0
2 2 2 2 2
但是,需要避免交联过程热膨胀及产生的水蒸气在建筑结构中造成空隙。我国三
峡大坝的建设者在全世界首创了以冰代水的浇灌方法,有效解决了这一问题,保
证了大坝建筑质量。下列说法错误的是( )
A.水泥由黏土和石灰石等研磨、煅烧制得
B.水泥生产过程中加入石膏,可以调节水泥的硬化速率
C.水的作用是提供结晶水以稳定交联结构
D.以冰代水的优点是减少了热膨胀及水蒸气的产生
答案 C
解析 A.水泥由黏土和石灰石等混合、研磨,经高温煅烧制得,正确;B.水泥生产
过程中加入石膏的目的是为了调节水泥的凝结硬化速率,从而调整水泥的凝结时
间,正确;C.水与硅酸三钙发生化学反应,生成的产物形成相互交联的结构,错误;
D.以冰代水可吸收反应放出的热量,减少了热膨胀及水蒸气的产生,保证了建筑
质量,正确。
6.(高考组合题)下列说法正确的是( )
A.(2018·天津,1C)汉代烧制出“明如镜、声如磬”的瓷器,其主要原料为黏
土
B.(2018·海南,5B)SiO 具有导电性,可用于制作光导纤维和光电池
2
C.(2018·海南,9A)12 g金刚石中含有化学键的数目为4N
A
D.(2018·江苏,3B)SiO 熔点高硬度大,可用于制光导纤维
2
答案 A
解析 工业上以黏土为原料烧制瓷器,A项正确;二氧化硅对光具有良好的
全反射作用,故用于制作光导纤维,而Si为半导体材料,可作光电材料,B项错误;
在金刚石中,1个C原子参与形成4个C—C键,则平均每个C原子形成4×=2个C—C键,n(金刚石)==1 mol,所以12 g金刚石中含有2N 个化学键,C项错
A
误;SiO 作光导纤维是由于SiO 具有光学性质,与熔点和硬度无关,D项错误。
2 2
一、选择题(每小题只有一个选项符合题意)
1.大多数物质的俗名是根据其特殊的物理性质或用途得来的。下列物质的
俗名与化学性质或用途不相符的一组是( )
选项 俗名 主要成分(化学式) 用途
A 石英 SiO 集成电路
2
B 纯碱 Na CO 制备玻璃
2 3
C 水玻璃 Na SiO 制备硅胶
2 3
用作油漆和涂
D 铁红 Fe O
2 3
料
答案 A
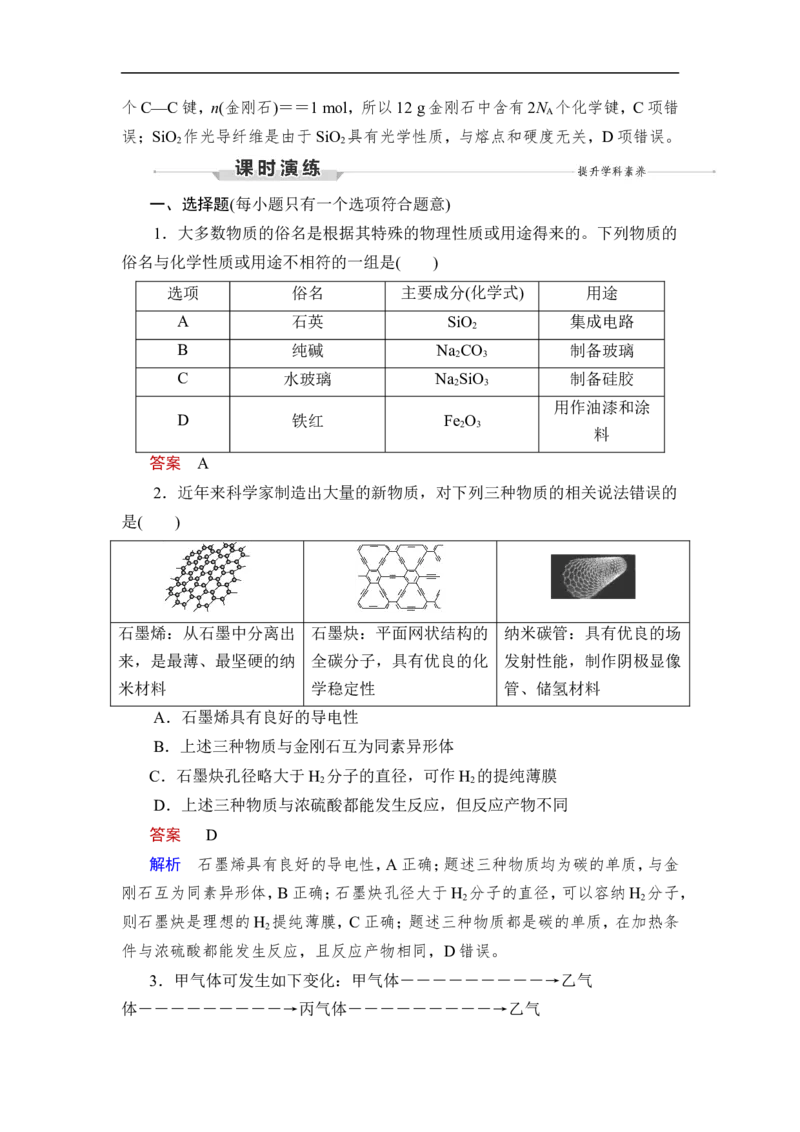
2.近年来科学家制造出大量的新物质,对下列三种物质的相关说法错误的
是( )
石墨烯:从石墨中分离出 石墨炔:平面网状结构的 纳米碳管:具有优良的场
来,是最薄、最坚硬的纳 全碳分子,具有优良的化 发射性能,制作阴极显像
米材料 学稳定性 管、储氢材料
A.石墨烯具有良好的导电性
B.上述三种物质与金刚石互为同素异形体
C.石墨炔孔径略大于H 分子的直径,可作H 的提纯薄膜
2 2
D.上述三种物质与浓硫酸都能发生反应,但反应产物不同
答案 D
解析 石墨烯具有良好的导电性,A正确;题述三种物质均为碳的单质,与金
刚石互为同素异形体,B正确;石墨炔孔径大于H 分子的直径,可以容纳H 分子,
2 2
则石墨炔是理想的H 提纯薄膜,C正确;题述三种物质都是碳的单质,在加热条
2
件与浓硫酸都能发生反应,且反应产物相同,D错误。
3.甲气体可发生如下变化:甲气体―――――――――→乙气
体―――――――――→丙气体―――――――――→乙气体―――――――――→丁固体。则甲、乙、丙、丁分别为( )
A.CO 、CO、O 、CaO B.O 、CO、CO 、CaCO
2 2 2 2 3
C.O 、CO 、CO、CaCO D.CO、CO 、O 、Ca(OH)
2 2 3 2 2 2
答案 C
解析 以丙气体为突破口,丙通过灼热的CuO后,生成的乙气体可与澄清石
灰水反应生成丁固体,说明乙是CO ,则逆推出丙是CO,则甲是O ,丁是CaCO 。
2 2 3
4.半导体工业中,有一句行话: “从沙滩到用户”,即由SiO 制取Si。制取过
2
程中不涉及的化学反应是( )
A.2C+SiO =====Si+2CO↑
2
B.SiO +2NaOH===Na SiO +H O
2 2 3 2
C.Si+2Cl =====SiCl
2 4
D.SiCl +2H =====Si+4HCl
4 2
答案 B
解析 由SiO 制取Si时要先制得粗硅,反应为2C+SiO =====Si+2CO↑,
2 2
然后再进行提纯,反应依次为Si+2Cl =====SiCl 、SiCl +2H =====Si+4HCl。
2 4 4 2
5.下列硅元素及其化合物的有关说法正确的是( )
A.SiO 既能与NaOH溶液反应,又能与氢氟酸反应,故为两性氧化物
2
B.高温下SiO 能与Na CO 固体反应生成Na SiO 和CO ,说明硅酸酸性强
2 2 3 2 3 2
于碳酸
C.因为玻璃中含有SiO ,所以不能用带磨口玻璃塞的试剂瓶盛装碱性溶液
2
D.Si→SiO →H SiO →SiO →SiO均能一步转化
2 2 3 2
答案 C
解析 A项,SiO 与氢氟酸反应生成的SiF 不是盐,SiO 不是两性氧化物;B
2 4 2
项,碳酸比硅酸酸性强;D项,SiO 不能一步转化为H SiO 。
2 2 3
6.下列说法正确的是( )
①合成纤维和光导纤维都是新型无机非金属材料 ②硅酸可制备硅胶,硅胶
可用作袋装食品、瓶装药品的干燥剂
③Mg2+、H+、SiO、SO在水溶液中能大量共存 ④向含K+、Na+、
Br-、SiO的溶液中通入CO 后仍能大量共存 ⑤SiO 不与任何酸反应,可用石
2 2
英制造耐酸容器
⑥硅酸钠可制备木材防火剂,也可用于制备硅酸胶体
A.①⑤⑥ B.②⑥C.①②⑥ D.③④⑥
答案 B
解析 合成纤维属于有机合成材料,①不正确;Mg2+、H+均不能与SiO大量
共存,③不正确;SiO+CO +H O===H SiO ↓+CO,④不正确;SiO +
2 2 2 3 2
4HF===SiF ↑+2H O,⑤不正确,正确答案为B。
4 2
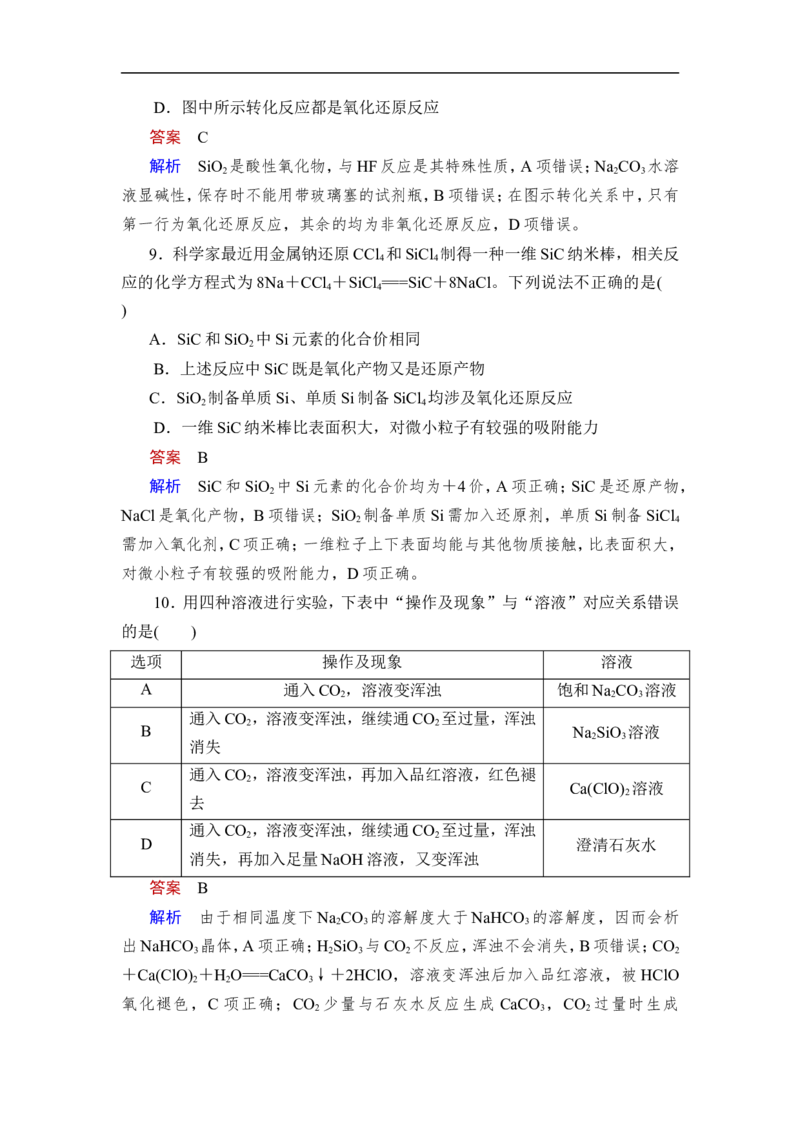
7.(2020·成都调研)科技的进步为二氧化碳资源化利用提供了广阔的前景。
下列说法错误的是( )
A.CO 是自然界碳循环中的重要物质
2
B.CO 加氢转化为乙烯,CO 被还原
2 2
C.CO 电催化时,在阳极转化为燃料
2
D.CO 与环氧丙烷可合成可降解塑料
2
答案 C
解析 含碳燃料燃烧以及动植物呼吸都会产生二氧化碳,植物光合作用消耗
二氧化碳,所以CO 是自然界碳循环中的重要物质,故A正确;CO 加氢转化为
2 2
乙烯,C的化合价降低,CO 得电子,被还原,故B正确;CO 中C为+4价,只能
2 2
发生得电子的还原反应,CO 在阴极得电子转化为燃料,阳极为失电子的氧化反
2
应,故C错误;CO 与环氧丙烷发生加聚反应,可合成可降解塑料,故D正确。
2
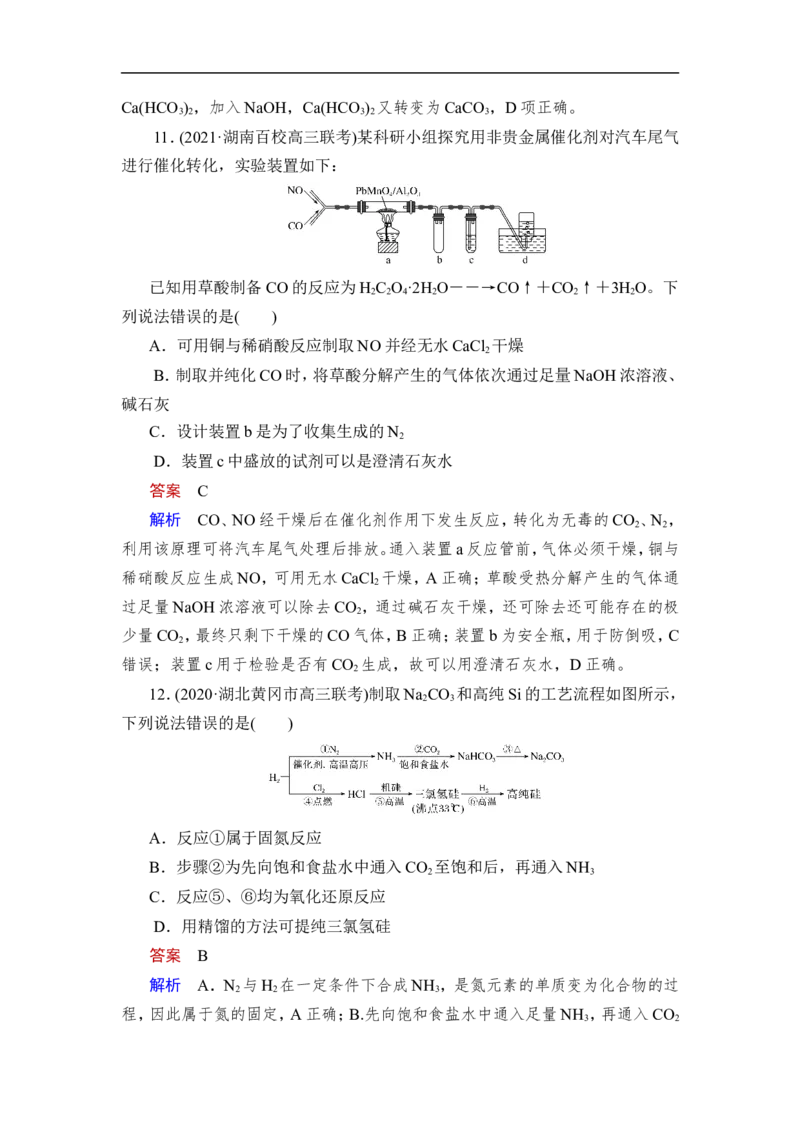
8.如图是利用二氧化硅制备硅及其化合物的流程,下列说法正确的是( )
A.SiO 除能与HF反应外,还能与其他强酸反应
2
B.盛放Na CO 溶液的试剂瓶能用玻璃塞
2 3
C.硅胶吸水后可重复再生D.图中所示转化反应都是氧化还原反应
答案 C
解析 SiO 是酸性氧化物,与HF反应是其特殊性质,A项错误;Na CO 水溶
2 2 3
液显碱性,保存时不能用带玻璃塞的试剂瓶,B项错误;在图示转化关系中,只有
第一行为氧化还原反应,其余的均为非氧化还原反应,D项错误。
9.科学家最近用金属钠还原CCl 和SiCl 制得一种一维SiC纳米棒,相关反
4 4
应的化学方程式为 8Na+CCl +SiCl ===SiC+8NaCl。下列说法不正确的是(
4 4
)
A.SiC和SiO 中Si元素的化合价相同
2
B.上述反应中SiC既是氧化产物又是还原产物
C.SiO 制备单质Si、单质Si制备SiCl 均涉及氧化还原反应
2 4
D.一维SiC纳米棒比表面积大,对微小粒子有较强的吸附能力
答案 B
解析 SiC和SiO 中Si元素的化合价均为+4价,A项正确;SiC是还原产物,
2
NaCl是氧化产物,B项错误;SiO 制备单质Si需加入还原剂,单质Si制备SiCl
2 4
需加入氧化剂,C项正确;一维粒子上下表面均能与其他物质接触,比表面积大,
对微小粒子有较强的吸附能力,D项正确。
10.用四种溶液进行实验,下表中“操作及现象”与“溶液”对应关系错误
的是( )
选项 操作及现象 溶液
A 通入CO ,溶液变浑浊 饱和Na CO 溶液
2 2 3
通入CO ,溶液变浑浊,继续通CO 至过量,浑浊
2 2
B Na SiO 溶液
2 3
消失
通入CO ,溶液变浑浊,再加入品红溶液,红色褪
2
C Ca(ClO) 溶液
2
去
通入CO ,溶液变浑浊,继续通CO 至过量,浑浊
2 2
D 澄清石灰水
消失,再加入足量NaOH溶液,又变浑浊
答案 B
解析 由于相同温度下Na CO 的溶解度大于NaHCO 的溶解度,因而会析
2 3 3
出NaHCO 晶体,A项正确;H SiO 与CO 不反应,浑浊不会消失,B项错误;CO
3 2 3 2 2
+Ca(ClO) +H O===CaCO ↓+2HClO,溶液变浑浊后加入品红溶液,被HClO
2 2 3
氧化褪色,C 项正确;CO 少量与石灰水反应生成 CaCO ,CO 过量时生成
2 3 2Ca(HCO ) ,加入NaOH,Ca(HCO ) 又转变为CaCO ,D项正确。
3 2 3 2 3
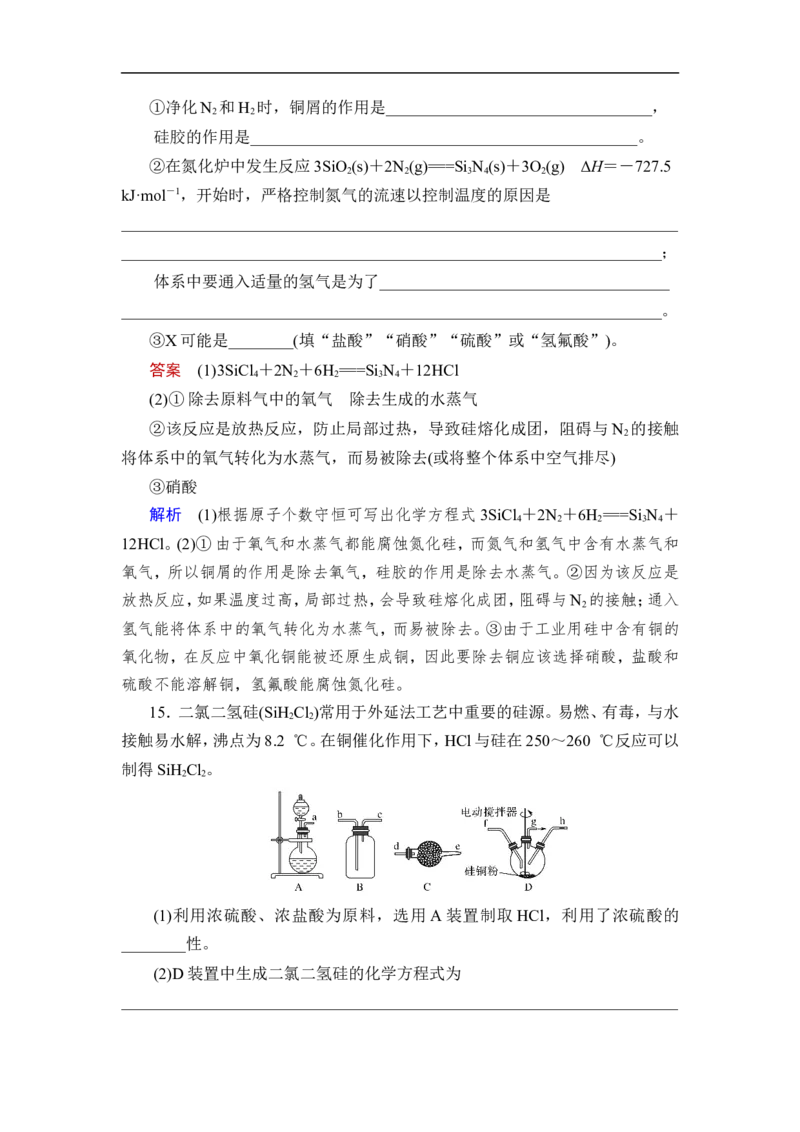
11.(2021·湖南百校高三联考)某科研小组探究用非贵金属催化剂对汽车尾气
进行催化转化,实验装置如下:
已知用草酸制备CO的反应为H C O ·2H O――→CO↑+CO ↑+3H O。下
2 2 4 2 2 2
列说法错误的是( )
A.可用铜与稀硝酸反应制取NO并经无水CaCl 干燥
2
B.制取并纯化CO时,将草酸分解产生的气体依次通过足量NaOH浓溶液、
碱石灰
C.设计装置b是为了收集生成的N
2
D.装置c中盛放的试剂可以是澄清石灰水
答案 C
解析 CO、NO经干燥后在催化剂作用下发生反应,转化为无毒的CO 、N ,
2 2
利用该原理可将汽车尾气处理后排放。通入装置a反应管前,气体必须干燥,铜与
稀硝酸反应生成NO,可用无水CaCl 干燥,A正确;草酸受热分解产生的气体通
2
过足量NaOH浓溶液可以除去CO ,通过碱石灰干燥,还可除去还可能存在的极
2
少量CO ,最终只剩下干燥的CO气体,B正确;装置b为安全瓶,用于防倒吸,C
2
错误;装置c用于检验是否有CO 生成,故可以用澄清石灰水,D正确。
2
12.(2020·湖北黄冈市高三联考)制取Na CO 和高纯Si的工艺流程如图所示,
2 3
下列说法错误的是( )
A.反应①属于固氮反应
B.步骤②为先向饱和食盐水中通入CO 至饱和后,再通入NH
2 3
C.反应⑤、⑥均为氧化还原反应
D.用精馏的方法可提纯三氯氢硅
答案 B
解析 A.N 与H 在一定条件下合成NH ,是氮元素的单质变为化合物的过
2 2 3
程,因此属于氮的固定,A正确;B.先向饱和食盐水中通入足量NH ,再通入CO
3 2气体,B错误;C.反应⑤、⑥中均有元素化合价的变化,因此这两个反应均为氧化
还原反应,C正确;D.由于三氯氢硅沸点只有33 ℃,比较低,与其他杂质的沸点
不同,因此可通过蒸馏(精馏)的方法分离提纯,D正确。
二、非选择题(本题包括3小题)
13.我国科学家制得了SiO 超分子纳米管,微观结构如图所示。回答相关问
2
题。
(1)干冰属于________晶体,石英属于________晶体,晶体结构中最小环上原
子个数为________。
(2)高纯度的二氧化硅广泛用于制作光导纤维,但光导纤维遇强碱会造成信
号中断,原因是______________________________________________________
____________________________________________________________________
(用化学方程式表示)。
(3)熔化纯碱时不能选用普通坩埚,理由是____________________________
_____________________________________________________________________
_________________________________________________(用化学方程式表示)。
答案 (1)分子 原子 12 (2)2NaOH+SiO ===Na SiO +H O (3)Na CO
2 2 3 2 2 3
+SiO =====Na SiO +CO ↑
2 2 3 2
14.硅是带来人类文明的重要元素之一,从传统材料到信息材料的发展过程
中创造了一个又一个奇迹。
(1)新型陶瓷Si N 的熔点高、硬度大、化学性质稳定。工业上可以采用化学气
3 4
相沉积法,在H 的保护下,使SiCl 与N 反应生成Si N 沉积在石墨表面,写出该
2 4 2 3 4
反应的化学方程式:____________________________________________。
(2)一种工业用硅(含少量钾、钠、铁、铜的氧化物),已知硅的熔点是1 420 ℃,
高温下氧气及水蒸气能明显腐蚀氮化硅。一种合成氮化硅的主要工艺流程如下:①净化N 和H 时,铜屑的作用是_________________________________,
2 2
硅胶的作用是________________________________________________。
②在氮化炉中发生反应3SiO (s)+2N (g)===Si N (s)+3O (g) ΔH=-727.5
2 2 3 4 2
kJ·mol-1,开始时,严格控制氮气的流速以控制温度的原因是
_____________________________________________________________________
___________________________________________________________________;
体系中要通入适量的氢气是为了____________________________________
___________________________________________________________________。
③X可能是________(填“盐酸”“硝酸”“硫酸”或“氢氟酸”)。
答案 (1)3SiCl +2N +6H ===Si N +12HCl
4 2 2 3 4
(2)①除去原料气中的氧气 除去生成的水蒸气
②该反应是放热反应,防止局部过热,导致硅熔化成团,阻碍与N 的接触
2
将体系中的氧气转化为水蒸气,而易被除去(或将整个体系中空气排尽)
③硝酸
解析 (1)根据原子个数守恒可写出化学方程式3SiCl +2N +6H ===Si N +
4 2 2 3 4
12HCl。(2)①由于氧气和水蒸气都能腐蚀氮化硅,而氮气和氢气中含有水蒸气和
氧气,所以铜屑的作用是除去氧气,硅胶的作用是除去水蒸气。②因为该反应是
放热反应,如果温度过高,局部过热,会导致硅熔化成团,阻碍与N 的接触;通入
2
氢气能将体系中的氧气转化为水蒸气,而易被除去。③由于工业用硅中含有铜的
氧化物,在反应中氧化铜能被还原生成铜,因此要除去铜应该选择硝酸,盐酸和
硫酸不能溶解铜,氢氟酸能腐蚀氮化硅。
15.二氯二氢硅(SiH Cl )常用于外延法工艺中重要的硅源。易燃、有毒,与水
2 2
接触易水解,沸点为8.2 ℃。在铜催化作用下,HCl与硅在250~260 ℃反应可以
制得SiH Cl 。
2 2
(1)利用浓硫酸、浓盐酸为原料,选用 A装置制取HCl,利用了浓硫酸的
________性。
(2)D装置中生成二氯二氢硅的化学方程式为
________________________________________________________________________________________________________________________________________。
(3)按照气体从左到右的方向,制取SiH Cl 的装置(h处用止水夹夹好)连接顺
2 2
序为
a→( )→( )→( )→( )→( )→( )→( )(填仪器接口的
字母,其中装置C用到2次)。
(4)按从左到右的顺序,前面装置C中装的药品为________,后面装置C的作
用为______________________________________________________________
___________________________________________________________________。
(5)反应除生成二氯二氢硅之外,还会生成H 和________、________等。
2
(6)新的制取SiH Cl 的方法是:往硅粉中先通入Cl ,在300~350 ℃反应生成
2 2 2
SiCl ,然后再与HCl在250~260 ℃反应,可以大大提高产率。如果通入气体顺序
4
相反,结果会_________________________________________________
____________________________________________________________________
(用化学方程式表示)。
答案 (1)吸水
(2)Si+2HCl=========SiH Cl
2 2
(3)d e f g b c d
(4)P O 或CaCl 尾气处理和防止空气中的水进入B中
2 5 2
(5)SiCl SiHCl
4 3
(6)SiH Cl +2Cl =====SiCl +2HCl(或SiH Cl +Cl =====SiHCl +HCl)
2 2 2 4 2 2 2 3
解析 (3)A装置制取HCl,连接C装置干燥,从f进入D中反应,SiH Cl 从g
2 2
处挥发出来,在B装置中收集,SiH Cl 的密度比空气大,导气管应长进短出,为防
2 2
止空气中的水进入B中,则应在B后接干燥管。(4)前面的装置C是用来干燥氯化
氢气体的,应选用P O 或CaCl ,后面装置C的作用为尾气处理和防止空气中的
2 5 2
水进入B中。(6)如果通入气体顺序相反,SiH Cl 会与Cl 继续反应,生成SiCl 、
2 2 2 4
SiHCl 。
3