文档内容
第 21 讲 电离平衡
1.从电离、离子反应、化学平衡的角度认识电解质水溶液的组成、性质和反应,如酸碱性、导电性
等。
2.认识弱电解质在水溶液中存在电离平衡,了解电离平衡常数的含义。
3.能运用化学用语正确表示水溶液中的离子反应与平衡,能通过实验证明水溶液中存在的离子平衡,
能举例说明离子反应与平衡在生产、生活中的应用。
【核心素养分析】
1.变化观念与平衡思想:认识弱电解质的电离有一定限度,是可以调控的,能多角度、动态地分析弱
电解质的电离平衡,并运用平衡移动原理解决实际问题。
2.科学研究与创新意识:能发现和提出有关弱电解质的判断问题;能问题和假设出发,确定探究目的,
设计探究方案,进行哙验探究。
3.证据推理与模型认知:知道可以通过分析、推理等方法认识电离平衡的本质特征,建立模型。能运
用模型解释电离平衡的移动,揭示现象的本质和规律。
知识点一 弱电解质的电离平衡
1.弱电解质
(1)概念
(2)与化合物类型的关系
强电解质主要是大部分离子化合物及某些共价化合物,弱电解质主要是某些共价化合物。
2.弱电解质的电离概念
(1)电离平衡的建立
在一定条件下(如温度、压强等),当弱电解质电离产生离子的速率和离子结合成分子的速率相等时,
电离过程达到了平衡。(2)电离平衡的建立与特征
①开始时,v(电离)最大,而v(结合)为0。
②平衡的建立过程中,v(电离)>v(结合)。
③当v(电离)=v(结合)时,电离过程达到平衡状态。
3.外因对电离平衡的影响
(1)浓度:在一定温度下,同一弱电解质溶液,浓度越小,越易电离。
(2)温度:温度越高,电离程度越大。
(3)同离子效应:加入与弱电解质具有相同离子的电解质时,可使电离平衡向结合成弱电解质分子的方
向移动。
(4)化学反应:加入能与弱电解质电离出的离子反应的物质时,可使电离平衡向电离方向移动。如:
以0.1 mol·L-1 CHCOOH溶液为例,填写外界条件对CHCOOH CHCOO-+H+ ΔH>0的影响。
3 3 3
改变条件 平衡移动方向 n(H+) c(H+) 导电能力 K
a
加水稀释 向右 增大 减小 减弱 不变
加入少量冰醋酸 向右 增大 增大 增强 不变
通入HCl(g) 向左 增大 增大 增强 不变
加NaOH(s) 向右 减小 减小 增强 不变
加CHCOONa(s) 向左 减小 减小 增强 不变
3
加入镁粉 向右 减小 减小 增强 不变
升高温度 向右 增大 增大 增强 增大
知识点二 电离平衡常数及其应用
1.表达式
(1)一元弱酸HA的电离常数:根据HA H++A-,可表示为K=。
a
(2)一元弱碱BOH的电离常数:根据BOH B++OH-,可表示为K =。
b
2.特点
(1)电离平衡常数与温度有关,与浓度无关,升高温度,K值增大。
(2)电离平衡常数反映弱电解质的相对强弱,K越大,表示弱电解质越易电离,酸性或碱性越强。
例如,在25 ℃时,K(HNO)=4.6×10-4,K(CHCOOH)=1.8×10-5,因而HNO 的酸性比CHCOOH强。
2 3 2 3
(3)多元弱酸的各级电离常数的大小关系是K K K ……,故其酸性取决于第一步电离。
1 2 3
3.电离度 ≫ ≫
(1)概念在一定条件下的弱电解质达到电离平衡时,已经电离的电解质分子数占原电解质总数的百分比。
(2)表示方法
α=×100%
也可表示为α=×100%
(3)影响因素
①相同温度下,同一弱电解质,浓度越大,其电离度(α)越小。
②相同浓度下,同一弱电解质,温度越高,其电离度(α)越大。
4.一元强酸(HCl)与一元弱酸(CHCOOH)的比较
3
(1)相同物质的量浓度、相同体积的盐酸与醋酸溶液的比较
比较项目 与活泼金属反应 开始与金属反
c(H+) pH 中和碱的能力
酸 产生H 2 的量 应的速率
盐酸 大 小 大
相同 相同
醋酸溶液 小 大 小
(2)相同pH、相同体积的盐酸与醋酸溶液的比较
比较项目 与足量活泼金属 开始与金属
c(H+) c(酸) 中和碱的能力
酸 反应产生H 2 的量 反应的速率
盐酸 小 小 少
相同 相同
醋酸溶液 大 大 多
5.一元强酸(HCl)与一元弱酸(CHCOOH)稀释图像比较
3
(1)相同体积、相同浓度的盐酸、醋酸
加水稀释到相同的pH,盐酸加入的水
加水稀释相同的倍数,醋酸的pH大
多
(2)相同体积、相同pH值的盐酸、醋酸
加水稀释到相同的pH,醋酸加入的水
加水稀释相同的倍数,盐酸的pH大
多
高频考点一 弱电解质的电离平衡【例1】(2022·全国乙卷)常温下,一元酸 的 。在某体系中, 与A-离子不
能穿过隔膜,未电离的 可自由穿过该膜(如图所示)。
设溶液中 ,当达到平衡时,下列叙述正确的是
A. 溶液Ⅰ中
B. 溶液Ⅱ中的HA的电离度 为
C. 溶液Ⅰ和Ⅱ中的 不相等
D. 溶液Ⅰ和Ⅱ中的 之比为
【变式探究】(2020·全国卷Ⅱ节选)次氯酸为一元弱酸,具有漂白和杀菌作用,其电离平衡体系中各成
分的组成分数δ[δ(X)=,X为HClO或ClO-]与pH的关系如图所示。HClO的电离常数K 值为________。
a
【归纳总结】外界条件对电离平衡影响的四个“不一定”
(1)稀醋酸加水稀释时,溶液中不一定所有的离子浓度都减小。
因为温度不变,K =c(H+)·c(OH-)是定值,稀醋酸加水稀释时,溶液中的c(H+)减小,故c(OH-)增大。
w
(2)电离平衡右移,电解质分子的浓度不一定减小,离子的浓度不一定增大,电离程度也不一定增大。
如对于CHCOOH CHCOO-+H+,平衡后,加入冰醋酸,c(CHCOOH)增大,平衡右移,根据勒夏特
3 3 3
列原理,只能“减弱”而不能“消除”,再次平衡时,c(CHCOOH)比原平衡时大;加水稀释或加少量
3
NaOH固体,都会使平衡右移,但 c(CHCOOH)、c(H+)都比原平衡时要小;加水稀释或增大弱电解质的浓
3
度,都使平衡右移,但加水稀释时弱电解质的电离程度增大,而增大弱电解质的浓度时弱电解质的电离程度减小。
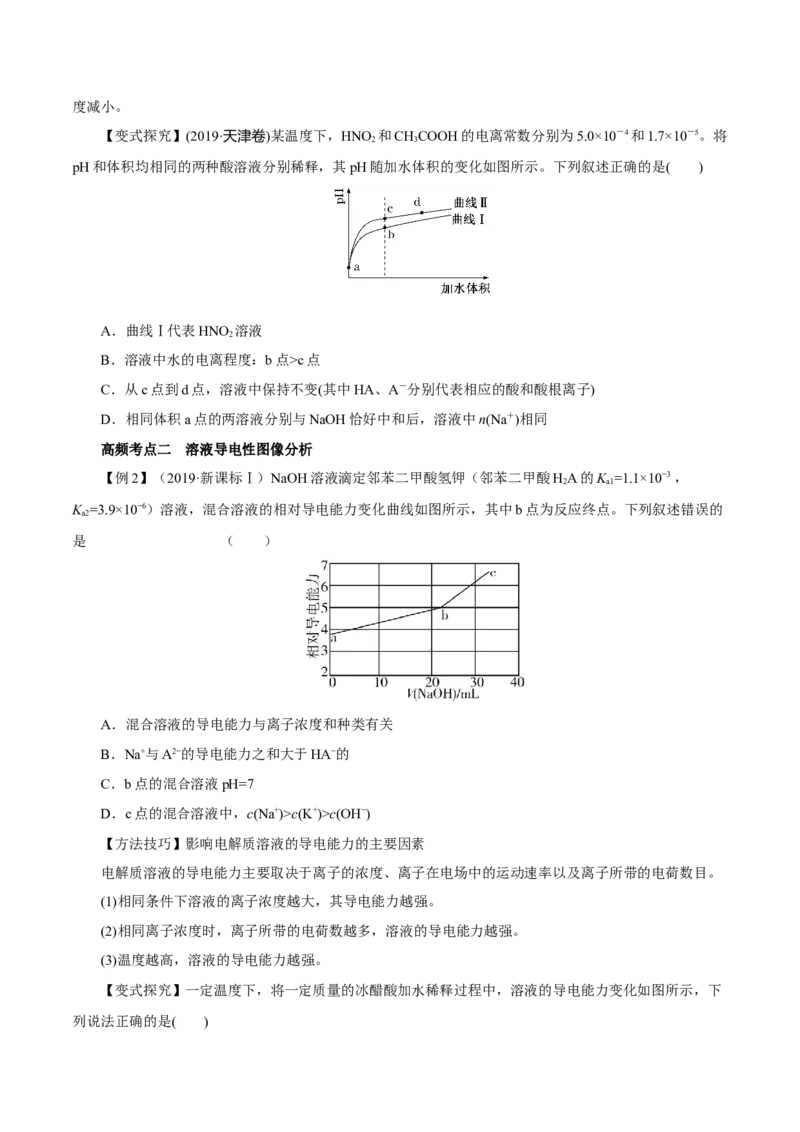
【变式探究】(2019·天津卷)某温度下,HNO 和CHCOOH的电离常数分别为5.0×10-4和1.7×10-5。将
2 3
pH和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是( )
A.曲线Ⅰ代表HNO 溶液
2
B.溶液中水的电离程度:b点>c点
C.从c点到d点,溶液中保持不变(其中HA、A-分别代表相应的酸和酸根离子)
D.相同体积a点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同
高频考点二 溶液导电性图像分析
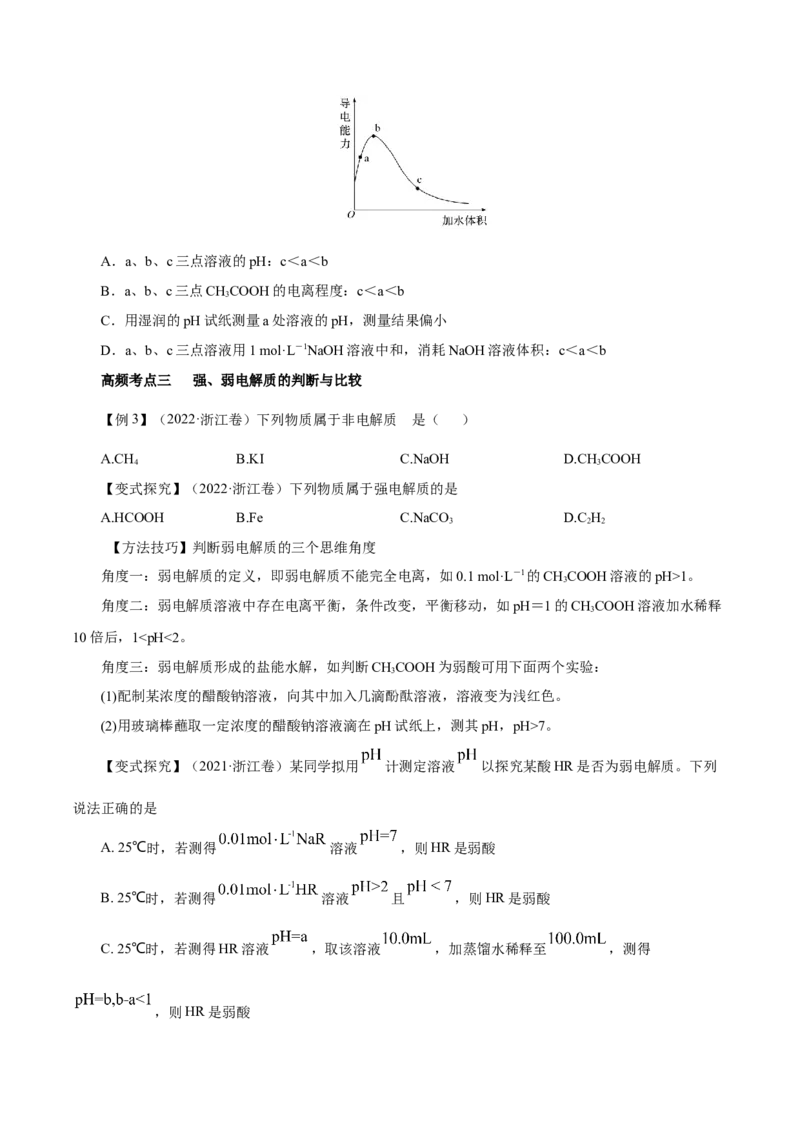
【例2】(2019·新课标Ⅰ)NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸HA的K =1.1×10−3 ,
2 a1
K =3.9×10−6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的
a2
是 ( )
A.混合溶液的导电能力与离子浓度和种类有关
B.Na+与A2−的导电能力之和大于HA−的
C.b点的混合溶液pH=7
D.c点的混合溶液中,c(Na+)>c(K+)>c(OH−)
【方法技巧】影响电解质溶液的导电能力的主要因素
电解质溶液的导电能力主要取决于离子的浓度、离子在电场中的运动速率以及离子所带的电荷数目。
(1)相同条件下溶液的离子浓度越大,其导电能力越强。
(2)相同离子浓度时,离子所带的电荷数越多,溶液的导电能力越强。
(3)温度越高,溶液的导电能力越强。
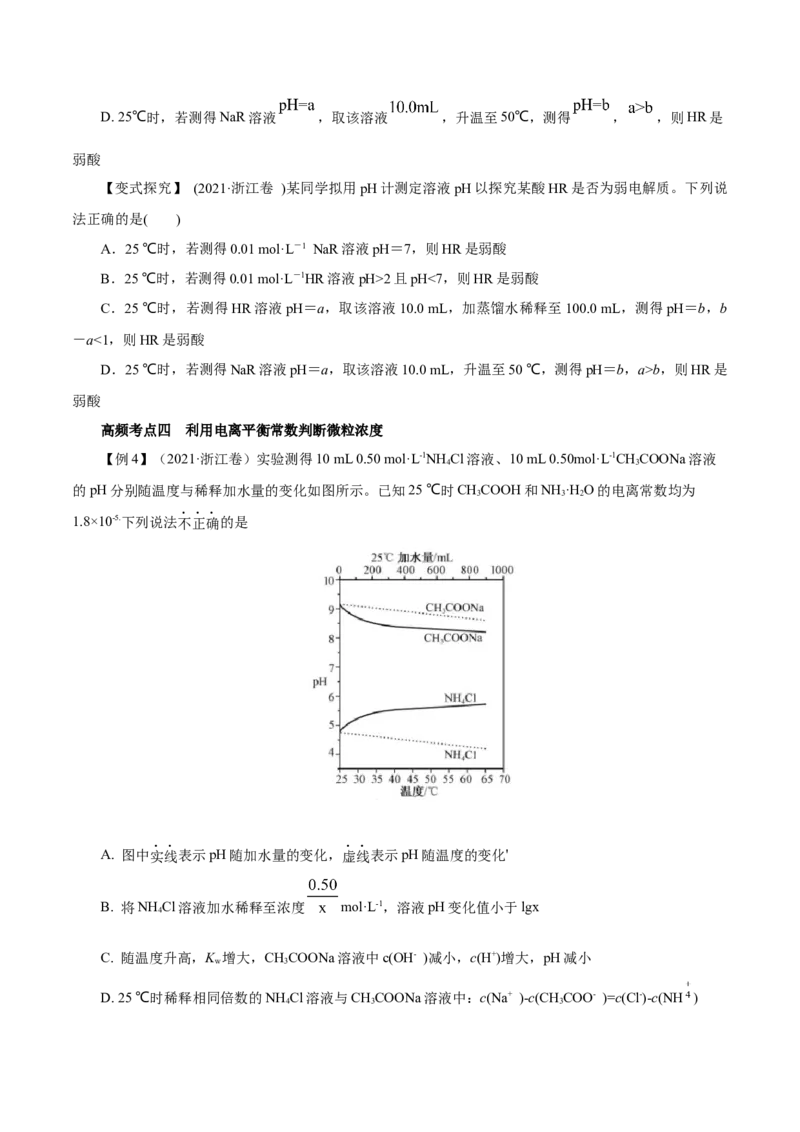
【变式探究】一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下
列说法正确的是( )A.a、b、c三点溶液的pH:c<a<b
B.a、b、c三点CHCOOH的电离程度:c<a<b
3
C.用湿润的pH试纸测量a处溶液的pH,测量结果偏小
D.a、b、c三点溶液用1 mol·L-1NaOH溶液中和,消耗NaOH溶液体积:c<a<b
高频考点三 强、弱电解质的判断与比较
的
【例3】(2022·浙江卷)下列物质属于非电解质 是( )
A.CH B.KI C.NaOH D.CHCOOH
4 3
【变式探究】(2022·浙江卷)下列物质属于强电解质的是
A.HCOOH B.Fe C.NaCO D.C H
3 2 2
【方法技巧】判断弱电解质的三个思维角度
角度一:弱电解质的定义,即弱电解质不能完全电离,如0.1 mol·L-1的CHCOOH溶液的pH>1。
3
角度二:弱电解质溶液中存在电离平衡,条件改变,平衡移动,如pH=1的CHCOOH溶液加水稀释
3
10倍后,17。
【变式探究】(2021·浙江卷)某同学拟用 计测定溶液 以探究某酸HR是否为弱电解质。下列
说法正确的是
A. 25℃时,若测得 溶液 ,则HR是弱酸
B. 25℃时,若测得 溶液 且 ,则HR是弱酸
C. 25℃时,若测得HR溶液 ,取该溶液 ,加蒸馏水稀释至 ,测得
,则HR是弱酸D. 25℃时,若测得NaR溶液 ,取该溶液 ,升温至50℃,测得 , ,则HR是
弱酸
【变式探究】 (2021·浙江卷 )某同学拟用pH计测定溶液pH以探究某酸HR是否为弱电解质。下列说
法正确的是( )
A.25 ℃时,若测得0.01 mol·L-1 NaR溶液pH=7,则HR是弱酸
B.25 ℃时,若测得0.01 mol·L-1HR溶液pH>2且pH<7,则HR是弱酸
C.25 ℃时,若测得HR溶液pH=a,取该溶液10.0 mL,加蒸馏水稀释至100.0 mL,测得pH=b,b
-a<1,则HR是弱酸
D.25 ℃时,若测得NaR溶液pH=a,取该溶液10.0 mL,升温至50 ℃,测得pH=b,a>b,则HR是
弱酸
高频考点四 利用电离平衡常数判断微粒浓度
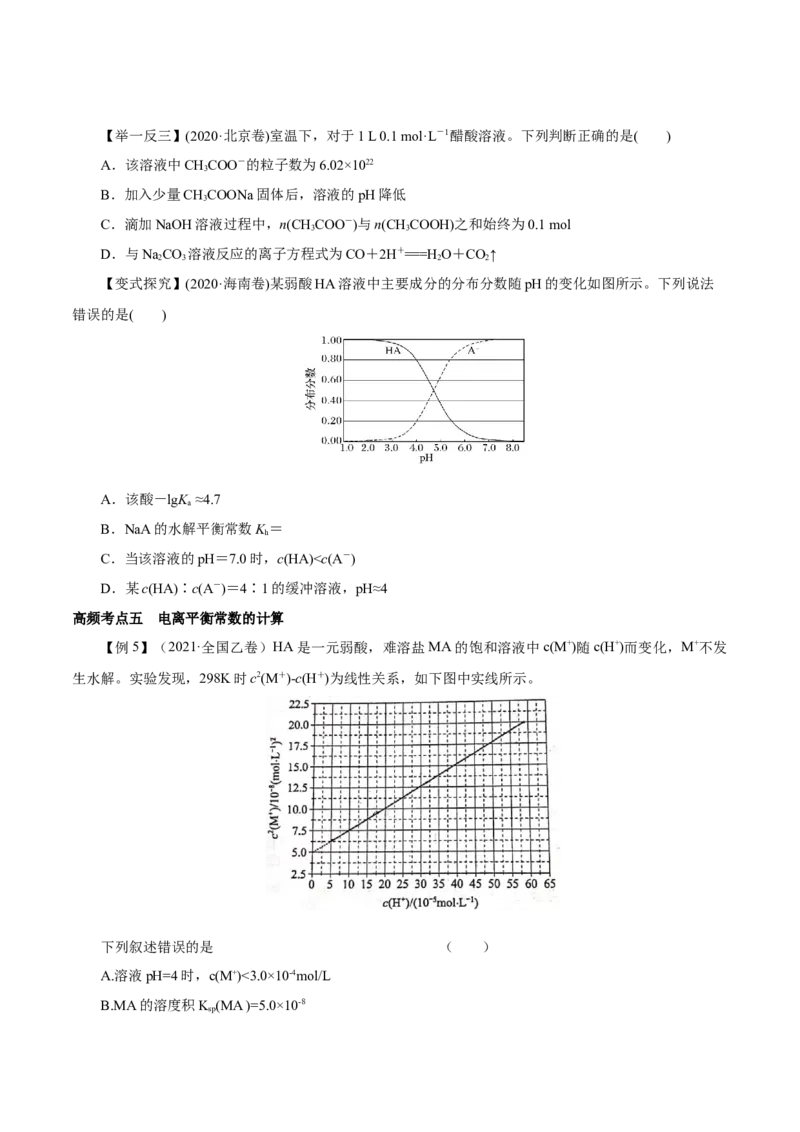
【例4】(2021·浙江卷)实验测得10 mL 0.50 mol·L-1NH Cl溶液、10 mL 0.50mol·L-1CHCOONa溶液
4 3
的pH分别随温度与稀释加水量的变化如图所示。已知25 ℃时CHCOOH和NH ·H O的电离常数均为
3 3 2
1.8×10-5.下列说法不正确的是
A. 图中实线表示pH随加水量的变化,虚线表示pH随温度的变化'
B. 将NH Cl溶液加水稀释至浓度 mol·L-1,溶液pH变化值小于lgx
4
C. 随温度升高,K 增大,CHCOONa溶液中c(OH- )减小,c(H+)增大,pH减小
w 3
D. 25 ℃时稀释相同倍数的NH Cl溶液与CHCOONa溶液中:c(Na+ )-c(CHCOO- )=c(Cl-)-c(NH )
4 3 3【举一反三】(2020·北京卷)室温下,对于1 L 0.1 mol·L-1醋酸溶液。下列判断正确的是( )
A.该溶液中CHCOO-的粒子数为6.02×1022
3
B.加入少量CHCOONa固体后,溶液的pH降低
3
C.滴加NaOH溶液过程中,n(CHCOO-)与n(CHCOOH)之和始终为0.1 mol
3 3
D.与NaCO 溶液反应的离子方程式为CO+2H+===H O+CO↑
2 3 2 2
【变式探究】(2020·海南卷)某弱酸HA溶液中主要成分的分布分数随pH的变化如图所示。下列说法
错误的是( )
A.该酸-lgK ≈4.7
a
B.NaA的水解平衡常数K =
h
C.当该溶液的pH=7.0时,c(HA)