文档内容
第 23 讲 弱电解质的电离平衡
第一部分:高考真题感悟
1.(2022·湖北·高考真题)根据酸碱质子理论,给出质子 的物质是酸,给出质子的能力越强,酸性越
强。已知: , ,下列酸性强弱顺序正确的是
A. B.
C. D.
【答案】D
【解析】根据复分解反应的规律,强酸能制得弱酸,根据酸碱质子理论,给出质子 的物质是酸,则反
应 中,酸性: ,反应 中,酸
性: ,故酸性: ,答案选D。
2.(2022·全国·高考真题)常温下,一元酸 的 。在某体系中, 与 离子不能穿过
隔膜,未电离的 可自由穿过该膜(如图所示)。
设溶液中 ,当达到平衡时,下列叙述正确的是
A.溶液Ⅰ中
B.溶液Ⅱ中的HA的电离度 为
C.溶液Ⅰ和Ⅱ中的 不相等D.溶液Ⅰ和Ⅱ中的 之比为
【答案】B
【解析】A.常温下溶液I的pH=7.0,则溶液I中c(H+)=c(OH-)=1×10-7mol/L,c(H+)<c(OH-)+c(A-),A错误;
B.常温下溶液II的pH=1.0,溶液中c(H+)=0.1mol/L,K = =1.0×10-3,c (HA)=c(HA)+c(A-),
a 总
则 =1.0×10-3,解得 = ,B正确;C.根据题意,未电离的HA可自由穿过隔膜,故
溶液I和II中的c(HA)相等,C错误;D.常温下溶液I的pH=7.0,溶液I中c(H+)=1×10-7mol/L,K =
a
=1.0×10-3,c (HA)=c(HA)+c(A-), =1.0×10-3,溶液I中c
总 总
(HA)=(104+1)c(HA),溶液II的pH=1.0,溶液II中c(H+)=0.1mol/L,K = =1.0×10-3,c
a 总
(HA)=c(HA)+c(A-), =1.0×10-3,溶液II中c (HA)=1.01c(HA),未电离的HA可自由穿
总
过隔膜,故溶液I和II中的c(HA)相等,溶液I和II中c (HA)之比为
总
[(104+1)c(HA)]∶[1.01c(HA)]=(104+1)∶1.01≈104,D错误;答案选B。
3.(2022·浙江·高考真题) 时,向 浓度均为 的盐酸和醋酸的混合溶液中逐滴加入
的 溶液(醋酸的 ;用 的 溶液滴定 等浓度的盐酸,滴定终
点的 突跃范围4.3~9.7)。下列说法不正确的是
A.恰好中和时,溶液呈碱性
B.滴加 溶液至 的过程中,发生反应的离子方程式为:C.滴定过程中,
D. 时,
【答案】B
【解析】A.恰好中和时,生成氯化钠溶液和醋酸钠溶液,其中醋酸根离子会水解,溶液显碱性,A正确;
B.滴加 溶液至 的过程中,若只发生反应的离子方程式: ,则滴加NaOH溶
液的体积为20mL,则根据电离常数, 的醋酸中,c(H+)≈c(CH COO-)= =
3
= >1.0×10-4.3,故用氢氧化钠滴定的过程中,醋酸也参加了反应,则离子方程
式为:H++OH-=H O和CHCOOH+OH-=CH COO-+H O,B错误;C.滴定前盐酸和醋酸的浓度相同,故滴
2 3 3 2
定过程中,根据物料守恒可知: ,C正确;D.向 浓度均为
的盐酸和醋酸的混合溶液中逐滴加入 的 溶液,当盐酸的体积为20ml时,溶液
为氯化钠和醋酸的混合溶液,显酸性,需要再滴加适量的氢氧化钠,当加入的NaOH溶液的体积为30mL
时,溶液为NaCl和等浓度的CHCOONa、CHCOOH,根据Ka=1.8×10-5>Kh= 可知,此时溶
3 3
液仍然呈酸性,需继续滴加NaOH溶液,故有 ,D正确;故
答案为:B。
4.(2022·浙江·高考真题) 时,苯酚 的 ,下列说法正确的是
A.相同温度下,等 的 和 溶液中,
B.将浓度均为 的 和 溶液加热,两种溶液的 均变大
C. 时, 溶液与 溶液混合,测得 ,则此时溶液中D. 时, 的 溶液中加少量 固体,水的电离程度变小
【答案】C
【解析】A.醋酸的酸性大于苯酚,则醋酸根离子的水解程度较小,则相同温度下,等pH的C HONa和
6 5
CHCOONa溶液中c(C HO-)①的是
3
A.稀释到相同pH所需水的体积
B.与镁条反应生成等量H 所需时间
2
C.与镁条反应的起始速率
D.与相同浓度NaOH(aq)恰好中和时,消耗NaOH(aq)的体积
【答案】B
【解析】醋酸是弱酸,在水中部分电离,醋酸是弱酸,在水中部分电离,0.01mol•L-1的CHCOOH(aq)pH>
3
2,氢离子浓度①>②,醋酸浓度①>②。A.醋酸是弱酸,在水中部分电离,0.01mol•L-1的
CHCOOH(aq)pH>2,当①pH=2的CHCOOH(aq),②0.01mol•L-1的CHCOOH(aq)稀释到相同的pH时①
3 3 3
消耗的水的体积大,故A错误;B.②0.01mol•L-1的CHCOOH溶液中氢离子浓度小于①pH=2的
3
CHCOOH(aq),则与镁条反应生成等量H 所需时间②>①,故B正确;C.分析可知氢离子浓度①>②,
3 2
则与镁条反应的起始速率①>②,故C错误;D.由分析可知醋酸浓度①>②,则与相同浓度NaOH(aq)恰好中和时,消耗NaOH(aq)的体积①>②,故D错误;故选:B。
8.(2022·辽宁沈阳·三模)弱酸型指示剂的电离平衡可表示为: ,其分子、离子为不同颜
色。下表是酚酞在pH不同的溶液中的结构和变色规律。下列说法中错误的是
(图中环状结构为苯环)
A.pH改变时,酸碱指示剂的分子、离子相对含量变化引起溶液颜色变化
B.溶液从酸性到强碱性的过程中,酚酞中的碳原子a从 杂化转化为 杂化
C.当指示剂的 ,则 ,此时的pH为理论变色点
D.温度改变,指示剂的变色范围可能发生改变
【答案】B
【解析】A.溶液pH改变时,溶液中氢离子浓度发生变化,电离平衡会发生移动,溶液中酸碱指示剂的分
子、离子相对含量变化引起颜色变化,故A正确;B.由图可知,溶液从酸性到强碱性的过程中,酚酞中
苯环碳原子a没有发生变化,原子的杂化方式没有变化,故B错误;C.由公式可知,弱酸型指示剂的电
离常数K= ,当溶液中 时,氢离子浓度和电离常数相等,溶液 ,溶
液会发生酸碱性变化,颜色也会变化,所以此时的pH为理论变色点,故C正确;D.弱酸型指示剂的电离
为吸热过程,温度改变,电离平衡会发生移动,溶液中氢离子浓度发生变化,指示剂的变色范围可能发生
改变,故D正确;故选B。
9.(2022·湖南省新化县第一中学模拟预测)牙形石(一种微型古生物遗体)主要成分为Ca (PO ),存在于
3 4 2
灰岩(主要成分为CaCO )中。可以通过合适的酸除去灰岩显示出牙形石的形态,进而分析当时的地层环境。
3
根据以下数据,有关合适的酸分析错误的是
已知:(1)酸的电离平衡常数
弱酸 HPO CHCOOH HCO
3 4 3 2 3K =6.9×10-3
a1
K =4.5×10-7
a1
电离平衡常数(25℃) K =6.2×10-8 K=1.8×10-5
a2 a
K =4.7×10-11
a2
K =4.8×10-13
a3
(2)K [Ca (PO )]=2.07×10-33
sp 3 4 2
(3)钙的磷酸盐中只有磷酸二氢钙可溶于水,其余难溶于水A.当加入过量的盐酸时与牙形石反应为:
Ca (PO )+2H+=H PO +3Ca2+
3 4 2 2
B.过量的醋酸可以溶解灰岩:CaCO +2CH COOH=Ca2++2CH COO-+H O+CO↑
3 3 3 2 2
C.过量醋酸与牙形石:Ca (PO )+4CH COOH=3Ca2++4CH COO-+2H PO ,该反应K≈2.5×10-13
3 4 2 3 3 2
D.醋酸能溶解灰岩,不溶解牙形石,可用于除去灰岩显示出牙形石
【答案】A
【解析】A.盐酸是强酸,加入过量盐酸时与牙形石反应为:Ca (PO )+6H+=2H PO +3Ca2+,A选项错误;
3 4 2 3 4
B.据电离平衡常数的大小可判断, 酸性CHCOOH>H CO,可发生反应CaCO +2CH COOH= Ca2+
3 2 3 3 3
+2CH COO-+H O+CO↑,B选项正确;C. 据电离平衡常数的大小可判断,酸性HPO >CH COOH>H PO
3 2 2 3 4 3 2
,可写出反应式Ca (PO )+4CH COOH=3Ca2++4CH COO-+2H PO ,
3 4 2 3 3 2
,根据K [Ca (PO )] 、K(CHCOOH)、K (H PO )、K (H PO )的表达式代入上式换算化简得K=
sp 3 4 2 a 3 a2 3 4 a3 3 4
,远小于 ,因此牙形石不溶
于醋酸溶液中,C选项正确;D.醋酸能溶解灰岩,不溶解牙形石,可用于除去灰岩显示出牙形石,D选
项正确;答案选A。
10.(2022·浙江省宁波市鄞州中学模拟预测)下列说法正确的是
A.相同温度下,等pH的盐酸和醋酸加水稀释10倍后,c(Cl-)<c(CHCOO-)
3
B.0.1 mol·L-1的KA溶液pH=6.5,则HA为弱酸
C.常温下pH=3的盐酸和pH=11的氨水等体积混合:c(Cl-)+c(H+)=c(NH )+c(OH-)D.某温度下,向氨水中通入CO,随着CO 的通入, 不断增大
2 2
【答案】A
【解析】A.盐酸为强酸,醋酸为弱酸,相同pH时,醋酸物质的量浓度大于盐酸浓度,相同pH时,溶液
中c(Cl-)=c(CH COO-),加水稀释相同倍数,促进醋酸的电离,推出c(Cl-)<c(CHCOO-),故A正确;B.没
3 3
有指明温度是否是常温,因此无法判断HA是否是弱酸,故B错误;C.一水合氨为弱碱,常温下pH=3的
盐酸和pH=11的氨水等体积混合,混合后溶质为NH Cl和NH ·H O,溶液显碱性,c(OH-)>c(H+),c(NH )
4 3 2
>c(Cl-),即c(Cl-)+c(H+)<c(NH )+c(OH-),故C错误;D.
,K 只受温度影响,向氨水中通入二氧化碳气体,生成碳酸铵或碳酸氢铵,溶液c(NH )增大,该比值减
b
小,故D错误;答案为A。
11.(2022·江西·二模)25℃时,在体积均为100 mL、浓度均为0.1 mol·L-1的两种一元酸HA和HB的溶液
中,分别加入NaOH固体(温度恢复至室温,溶液体积变化忽略不计), 随加入NaOH固体的物
质的量的变化如图所示。下列有关说法不正确的是
A.酸性:HA> HB,且HA是强酸,HB是弱酸
B.由水电离出的c(H+ )的顺序:a<b<c<d
C.c点溶液中:c(H+)=c(B-)-c(HB) +c(OH-)
D.d点溶液中:c(B-)=c(Na+)>c(H+)=c(OH-)
【答案】C【解析】A.25℃时,K =1×10-14,由图可知没有加入氢氧化钠固体时,a点0.1 mol/L HA溶液中,
w
,可求得0.1 mol/L HA溶液中c(H+ )=0.1 mol/L,则HA为强酸;同理,由b点可知0.1
mol/L HB溶液中,c(H+)=0.01 mol/L,则HB为弱酸,故A项正确;B.由图和上述计算可知,a点和b点
均抑制水的电离,由于a点c(H+)更大,对水的抑制程度更大,c点和d点均为HB和NaB的混合溶液,由
于d点加入氢氧化钠的物质的量大,溶液中NaB的物质的量大,对水电离的促进大,则由水电离出的
c(H+)的顺序为a<b<c<d,故B项正确;C.c点反应后为等浓度的HB和NaB溶液,根据电荷守恒:
c(Na+)+c(H+)=c(B-)+c(OH-),根据物料守恒:2c(Na+)=c(B-)+c(HB),联立可得2c(H+)=c(B-)-c(HB)+2c(OH-),
故C项错误;D.d点c(H+)=c(OH-)=10-7 mol/L,根据电荷守恒:c(Na+)+c(H+)=c(B-)+c(OH-),则
c(Na+)=c(B-),且远大于c(H+),故对应的溶液中,c(B-)=c(Na+)>c(H+)=c(OH-),故D项正确;答案选C。
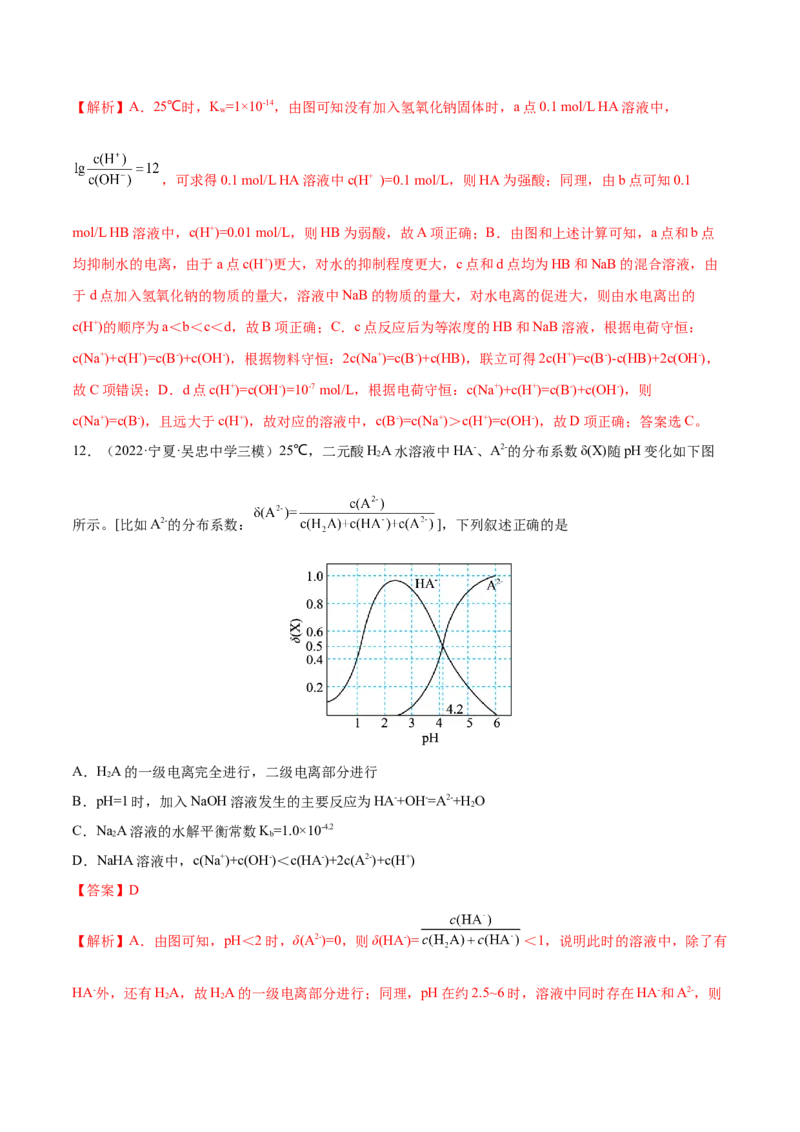
12.(2022·宁夏·吴忠中学三模)25℃,二元酸HA水溶液中HA-、A2-的分布系数δ(X)随pH变化如下图
2
所示。[比如A2-的分布系数: ],下列叙述正确的是
A.HA的一级电离完全进行,二级电离部分进行
2
B.pH=1时,加入NaOH溶液发生的主要反应为HA-+OH-=A2-+H O
2
C.NaA溶液的水解平衡常数K=1.0×10-4.2
2 b
D.NaHA溶液中,c(Na+)+c(OH-)<c(HA-)+2c(A2-)+c(H+)
【答案】D
【解析】A.由图可知,pH<2时,δ(A2-)=0,则δ(HA-)= <1,说明此时的溶液中,除了有
HA-外,还有HA,故HA的一级电离部分进行;同理,pH在约2.5~6时,溶液中同时存在HA-和A2-,则
2 2HA的二级电离也是部分进行,A错误;B.由图可知,pH=1时,δ(HA-)= =0.4,则
2
δ(H A)=1-δ(HA-)=1-0.4=0.6,故此时加入NaOH溶液,发生的主要反应为HA+OH-=HA-+H O,B错误;
2 2 2
C.pH=4.2时,δ(HA-)=δ(A2-),即c(HA-)=c(A2-),则K (H A)= = c(H+)=1.010-4.2,由于NaA
a2 2 2
溶液中的水解反应以第一步水解为主,故NaA溶液的水解平衡常数K = = =1.010-9.8,
2 b
C错误;D.在NaHA溶液中,有电荷守恒式:c(Na+)+c(H+)=c(HA-)+2c(A2-)+c(OH-);由图可知,NaHA溶
液呈酸性,即c(H+)>c(OH-),则c(Na+)<c(HA-)+2c(A2-),故可以得知c(Na+)+c(OH-)<c(HA-)+2c(A2-)
+c(H+),D正确;故选D。
二、主观题(共4小题,共40分)
13.(12分)浓度均为0.1mol·L-1的盐酸、硫酸和醋酸三种溶液,试分析:
(1)若溶液的c(H+)分别为a、b、c,则它们的大小关系是__________________________。
(2)分别用三种酸中和等物质的量的NaOH溶液,所需溶液的体积分别是a、b、c,则它们的大小关系是
________________________________。
(3)等体积的三种酸分别与足量的锌粒反应,若它们的反应速率分别为a、b、c,则反应开始时它们的大
小关系是____________。
(4)等体积的三种酸分别与足量的锌粒反应,在相同条件下,若产生气体的体积为a、b、c,则它们的关
系是____________。
【答案】(每空3分)(1)b>a>c (2)a=2b=c (3)b>a>c (4)2a=b=2c
【解析】盐酸为一元强酸,硫酸为二元强酸,醋酸为一元弱酸,强酸完全电离,弱酸部分电离。
(1)若溶液的c(H+)分别为a、b、c,浓度均为0.1mol·L-1,a=0.1mol/L,b=0.2mol/L,c<0.1mol/L,故
b>a>c;(2)酸中和等物质的量的碱,与酸的物质的量有关,V=n/c,则a=2b=c;(3)等体积的三种酸与足量
的锌粒反应,反应速率与c(H+)有关,浓度越大,反应速率越大,故b>a>c;(4)等体积的三种酸分别与足
量的锌粒反应,生成氢气的量与酸的物质的量有关,故2a=b=2c。
14.(12分)25℃时,三种酸的电离平衡常数如下:
化学式 CHCOOH HCO HClO
3 2 3
电离平衡常数 1.8×10-5 K=4.3×10-7 3.0×10-8
1K=5.6×10-11
2
回答下列问题:
(1)一般情况下,当温度升高时,Ka________(填“增大”、“减小”或“不变”)。
(2)下列四种离子结合质子能力由大到小的顺序是______________________(填字母)。
a.CO 2- b.ClO- c.CH COO- d.HCO-
3 3 3
(3)下列反应不能发生的是________(填字母)。
a. CO2-+2CHCOOH=2CHCOO-+CO↑+HO
3 3 3 2 2
b. ClO-+CHCOOH=CHCOO-+HClO
3 3
c. CO2-+2HClO=CO↑+HO+2ClO- d. 2ClO-+CO+HO=CO2-+2HClO
3 2 2 2 2 3
(4)25℃时,若测得CHCOOH与CHCOONa的混合溶液的pH=6,则溶液中c(CHCOO-)-c(Na+)=
3 3 3
___mol·L-1(填精确数值)。
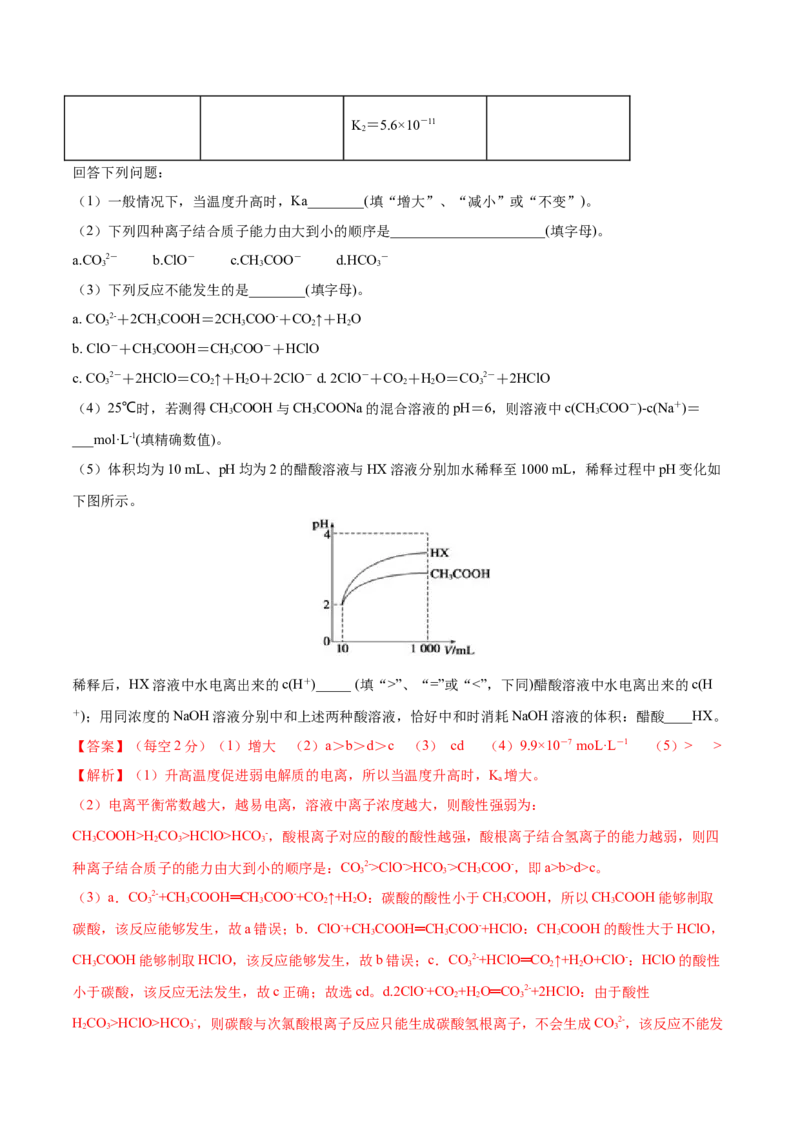
(5)体积均为10 mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000 mL,稀释过程中pH变化如
下图所示。
稀释后,HX溶液中水电离出来的c(H+)_____ (填“>”、“=”或“<”,下同)醋酸溶液中水电离出来的c(H
+);用同浓度的NaOH溶液分别中和上述两种酸溶液,恰好中和时消耗NaOH溶液的体积:醋酸____HX。
【答案】(每空2分)(1)增大 (2)a>b>d>c (3) cd (4)9.9×10-7 moL·L-1 (5)> >
【解析】(1)升高温度促进弱电解质的电离,所以当温度升高时,K 增大。
a
(2)电离平衡常数越大,越易电离,溶液中离子浓度越大,则酸性强弱为:
CHCOOH>H CO>HClO>HCO -,酸根离子对应的酸的酸性越强,酸根离子结合氢离子的能力越弱,则四
3 2 3 3
种离子结合质子的能力由大到小的顺序是:CO2->ClO->HCO->CH COO-,即a>b>d>c。
3 3 3
(3)a.CO2-+CH COOH═CH COO-+CO ↑+H O:碳酸的酸性小于CHCOOH,所以CHCOOH能够制取
3 3 3 2 2 3 3
碳酸,该反应能够发生,故a错误;b.ClO-+CH COOH═CH COO-+HClO:CHCOOH的酸性大于HClO,
3 3 3
CHCOOH能够制取HClO,该反应能够发生,故b错误;c.CO2-+HClO═CO ↑+H O+ClO-:HClO的酸性
3 3 2 2
小于碳酸,该反应无法发生,故c正确;故选cd。d.2ClO-+CO +H O═CO 2-+2HClO:由于酸性
2 2 3
HCO>HClO>HCO -,则碳酸与次氯酸根离子反应只能生成碳酸氢根离子,不会生成CO2-,该反应不能发
2 3 3 3生,故d正确;
(4)根据电荷守恒得c(CHCOO-)-c(Na+)=c(H+)-c(OH-)=(10-6-10-8)mol·L-1=
3
9.9×10-7mol·L-1。
(5)加水稀释促进弱酸电离,pH相同的不同酸稀释相同的倍数,pH变化大的酸酸性强,变化小的酸酸性
弱;酸或碱抑制水电离,酸中氢离子或碱中氢氧根离子浓度越大其抑制水电离程度越大,根据图知,pH相
同的醋酸和HX稀释相同的倍数,HX的pH变化大,则HX的酸性大于醋酸,所以HX的电离平衡常数大
于常数,稀释后醋酸中氢离子浓度大于HX,所以醋酸抑制水电离程度大于HX,则HX溶液中水电离出来
的c(H+)大于醋酸溶液水电离出来c(H+);溶液中氢离子浓度越小,对的抑制程度越小,水的电离程度
越大,稀释后HX溶液中的c(H+)小于CHCOOH溶液中的c(H+),它对水的电离的抑制能力减弱。
3
15.(16分)磷能形成多种含氧酸。
(1)次磷酸(HPO )是一种精细化工产品,向10 mL H PO 溶液中加入10 mL等物质的量浓度的NaOH
3 2 3 2
溶液后,所得的溶液中只有HPO -、OH-两种阴离子。
2 2
① 写出HPO 溶液与足量NaOH 溶液反应后形成的正盐的化学式:_______,该正盐溶液中各离子浓度由
3 2
大到小的顺序为____________。
② 若25℃时,K (HPO ) = 1×10-2,则0.01 mol · L-1的HPO 溶液的pH =________。
3 2 3 2
(2)亚磷酸(HPO )是二元中强酸,25℃时亚磷酸的电离常数为K= 1×10-2、K=2.6×10-7。
3 3 1 2
① 试从电离平衡移动的角度解释K、K 数据的差异_______________。
1 2
② NaH PO 溶液显______性(填“酸”“碱”或“中”)。
2 3
(3) 25 ℃时,HF的电离常数为K = 3.6×10-4; HPO 的电离常数为K=7.5×10-3,K=6.2×10-8,K=
3 4 1 2 3
4.4×10-13。足量NaF溶液和HPO 溶液反应的离子方程式为_________。
3 4
(4)相同温度下,等物质的量浓度的上述三种磷的含氧酸中。c(H+)由大到小的顺序为_____(用酸的分子
式表示)。
【答案】(除标注外,每空2分)(1)①NaH PO c(Na+)>c( )>c(OH-)>c(H+) (3分)
2 2
②2 (3分)
(2)①HPO 第一步电离出的H+对第二步电离起到抑制作用 ②酸
3 3
(3)F- +H PO =HF+
3 4
(4)H PO >H PO >H PO
3 3 3 2 3 4
【解析】(1)①HPO 是一元酸,HPO 溶液与足量NaOH 溶液反应后形成的正盐的化学式:NaH PO ,
3 2 3 2 2 2NaH PO 是强碱弱酸盐,溶液中各离子浓度由大到小的顺序为c(Na+)>c( )>c(OH-)>c(H+);②
2 2
,c(H+)=1×10-2 ,所以0.01 mol · L-1的HPO 溶液的pH =2;
3 2
(2)①HPO 第一步电离出的H+对第二步电离起到抑制作用,所以K>K ;
3 3 1 2
② 电离平衡常数是K=2.6×10-7, 水解平衡常数是 ,电离大于水解,所以溶
液出酸性;
(3)HF的电离常数为K = 3.6×10-4小于HPO 的第一步电离常数为K=7.5×10-3,大于HPO 的第二步电离常
3 4 1 3 4
数K=6.2×10-8,所以足量NaF溶液和HPO 溶液反应生成HF和NaH PO ,离子方程式是F- +H PO =HF+
2 3 4 2 4 3 4
;
(4)H PO 的第一步电离常数为K=7.5×10-3;亚磷酸是二元酸,第一步电离常数为K= 1×10-2;次磷酸的电
3 4 1 1
离平衡常数是K (HPO ) = 1×10-2,所以酸性亚磷酸>次磷酸>磷酸;所以相同温度下,等物质的量浓度的三
3 2
种磷的含氧酸中,c(H+)由大到小的顺序为HPO >H PO >H PO 。
3 3 3 2 3 4