文档内容
第 28 讲 原子结构与性质
1.氮、砷元素为同主族元素。下列说法正确的是
A.基态As原子的电子排布式为[Ar]4s24p3
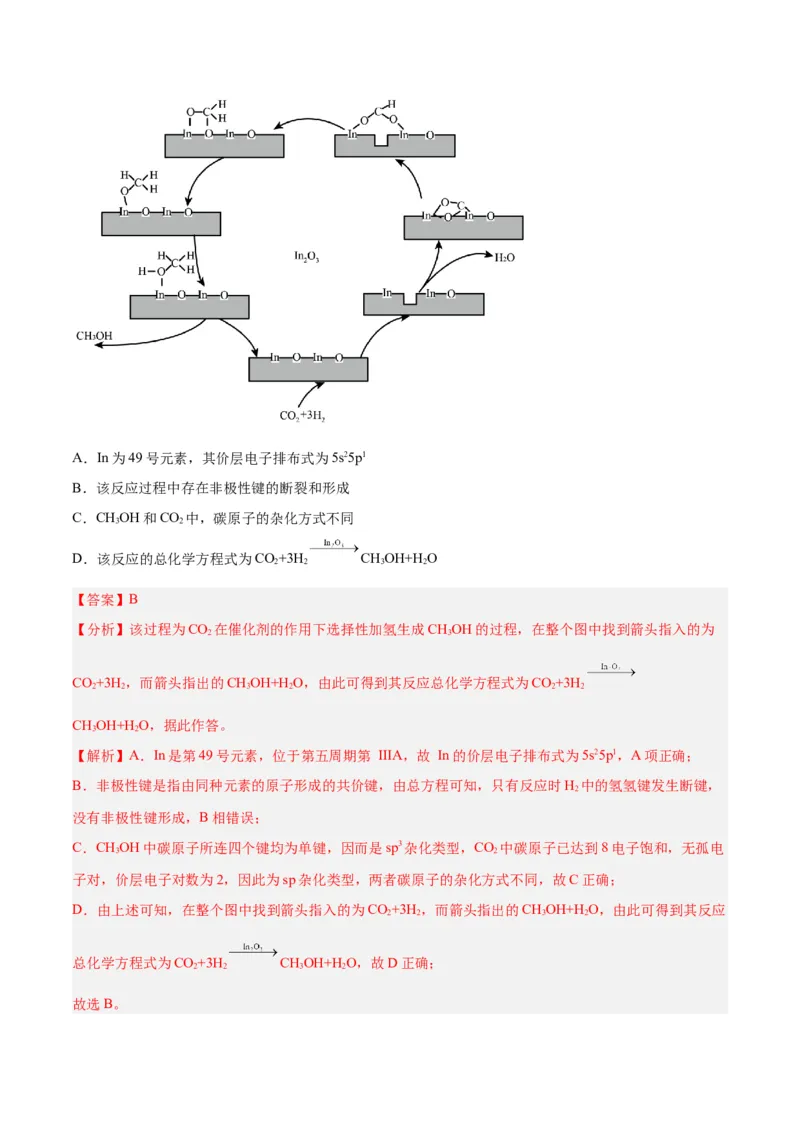
B.第一电离能:I(N)AsH
3 3
【答案】D
【解析】A.As是33号元素,处于第四周期第VA族,根据构造原理可知,基态As原子的电子排布式为
[Ar]3d104s24p3,A项错误;
B.同主族元素从上到下第一电离能逐渐减小,I(N)>I (P)>I (As),B项错误;
1 1 1
C.NH 分子间可以形成氢键,沸点最高,AsH 的沸点比NH 的低,C项错误;
3 3 3
D.AsH 中有3个σ键和1个孤电子对,价层电子对数为4,采取sp3杂化,分子空间结构为三角锥形,
3
NH 中N的电负性大于As,成键电子偏向N,成键电子对之间的排斥作用增强,NH 的键角大于AsH
3 3 3
的,D项正确;
故选D。
2.日光灯中用到的某种荧光粉的主要成分为 。已知: 、 、 和 为原子序数依次
增大的前20号元素, 为金属元素,基态 原子 轨道上的电子数和 轨道上的电子数相等,基态 、
、 原子的未成对电子数之比为 。下列说法正确的是
A.原子半径: B. 元素最高价化物对应的水化物具有强氧化性
C.电负性: D.能与水反应生成气体的单质只有 的单质
【答案】C
【分析】基态 原子 轨道上的电子数和 轨道上的电子数相等,电子排布为 ,X为O元素,基态
O原子的未成对电子数为2,Y和Z的未成对电子数分别为1和3,且原子序数为前20,则Z的价层电子排
布为 ,Z的原子序数大于O,所以Z为P,电子排布为 ,Y的原子序数在O和P之
间,基态Y原子未成对电子数为1,则Y可能为F 或者Na ,或者Al,由于 为金属元素,W和Y可形成 ,Y不可能为金属元素,所以Y只能时F,
根据化合物中正负化合价的代数和为0,W为Ca。
【解析】A.X为O元素,Y为F元素,Z为P元素,W为Ca元素,原子半径: ,A错误;
B.Z为P元素,最高价化物对应的水化物为 ,不具有强氧化性,B错误;
C.电负性: ,C正确;
D. 能与水反应生成 ,Ca能与水反应生成 ,所以能与水反应生成气体的单质有Y和W,D错误;
故选C。
3.五种短周期主族元素 X、Y、Z、M、Q 的原子序数依次增大,X 的 2p 轨道半充满,Y 的 s 能级电
子数和 p 能级电子数相等, Z 是至今发现的电负性最大的元素,M 在元素周期表中处于周期序数等于
族序数的位置,Q 的单质被广泛用作半导体材料。下列叙述中不正确的是
A.元素的第一电离能:X X >Q
C.气态氢化物分子的键角:Q>X>Y D.最高价氧化物对应的水化物的酸性:X>Q>M
【答案】A
【分析】X、Y、Z、M、Q为原子序数依次增大的短周期主族元素,X 的 2p 轨道半充满,则X的电子排
布式为1s22s22p3,则X为N;Y 的 s 能级电子数和 p 能级电子数相等,则Y的电子排布式为1s22s22p4,
则Y为O;Z 是至今发现的电负性最大的元素,则Z为F;M 在元素周期表中处于周期序数等于族序数的
位置,则M为Al;Q 的单质被广泛用作半导体材料,则Q为Si。
【解析】A.由分析知,X为N,Y为O,Z为F,元素的第一电离能为ON>Si,故B正确;
C.由分析知,X为N,Y为O,Q为Si,其气态氢化物为NH 、HO、SiH,NH 中氮原子为sp3杂化,
3 2 4 3
HO 中氧原子为sp3杂化, SiH 中硅原子为sp3杂化,但三者的孤电子对分别为2、1、0,则分子的键角为
2 4
SiH> NH > H O,故C正确;
4 3 2
D.由分析知,X为N,Q为Si,M为Al,元素非金属性越强,其最高价氧化物对应水化物的酸性越强,
则最高价氧化物对应的水化物的酸性N>Si>Al,故D正确;
答案选A。
4.一种由短周期主族元素组成的化合物(如图所示)具有良好的储氢性能,其中元素W、X、Y、Z的原子
序数依次增大,且总和为24,下列有关叙述正确的是A.同周期中第一电离能处于X和Y之间的元素有3种
B.元素X的最高价氧化物的水化物为二元弱酸
C.离子半径:
D.化合物ZW中W具有比较强的氧化性
【答案】A
【分析】Z的原子序数最大,且呈+1价,故Z为Na,根据机构图可知,W只有一个键,且原子序数最
小,故W为H,Y有三键,Y为N,原子序数总和为24,故X为B;
【解析】A.同周期中第一电离能处于B和N之间的元素有Be、C、O三种,A正确;
B.元素X的最高价氧化物的水化物为 ,在水中电离方程式为 ,属
于一元弱酸,B错误;
C.离子半径: ,C错误;
D.化合物NaH中H为-1价,易失电子,具有比较强的还原性,D错误;
故选A。
5.短周期元素W、X、Y、Z的原子序数依次递增,W、X、Z分别位于不同周期,Z的原子半径在同周期
元素中最大。科学家将这四种元素的原子“组装”成一种超分子,具有高效的催化性能,其分子结构如图
所示(实线代表共价键,其他重复单元的W、X未标注),下列说法错误的是
A.电负性:Y>X B.离子半径:Z>Y
C.W与X可组成多种共价化合物 D.简单氢化物的键角:X>Y
【答案】B
【分析】短周期元素W、X、Y、Z的原子序数依次递增,W、X、Z分别位于不同周期,Z的原子半径在
同周期元素中最大,则W为H,Z为Na。从超分子结构中可以看出,X可形成4个共价键,则其最外层有4个电子,其为C;Y可形成2个共价键,则其最外层有6个电子,其为O。从而得出W、X、Y、Z分别
为H、C、O、Na。
【解析】A.X、Y分别为C、O元素,非金属性O>N,则电负性O>N,A正确;
B.Y、Z分别为O、Na,O2-和Na+的电子层结构相同,但O的核电荷数比Na小,则离子半径:Na+<
O2-,B错误;
C.H与C可组成多种烃,包括烷烃、烯烃、炔烃、芳香烃等共价化合物,C正确;
D.C、O的简单氢化物分别为CH、HO,CH 呈正四面体结构,HO呈V形结构,则键角:CH>HO,
4 2 4 2 4 2
D正确;
故选B。
6.下列关系错误的是
A.沸点:CO>N B.第一电离能:Si<P<S
2
C.在水中的溶解度:SO >CO D.还原性:稀盐酸<浓盐酸
2 2
【答案】B
【解析】A.CO、N 的相对分子质量相同,但CO为极性分子,N 为非极性分子,所以CO分子间的作用
2 2
力比N 大,沸点:CO>N,A正确;
2 2
B.P的价电子排布式为3s23p3,3p轨道电子半充满,原子的能量低,第一电离能反常,则第一电离能:Si
<S<P,B错误;
C.SO 为极性分子,CO 为非极性分子,水为极性分子,依据相似相溶原理,在水中的溶解度:SO >
2 2 2
CO,C正确;
2
D.浓盐酸中Cl-浓度比稀盐酸中大,且浓盐酸的酸性更强,所以还原性:稀盐酸<浓盐酸,D正确;
故选B。
7.下列有关化学用语表示正确的是
A.HClO的电子式:
B.O 的分子结构空间模型:
3
C.基态As原子的电子排布式:[Ar]3d104s24p3
D.反式聚异戊二烯的结构简式:【答案】C
【解析】A.HClO的电子式: ,A错误;
B.O 的分子结构空间模型: ,B错误;
3
C.基态As原子的电子排布式:[Ar]3d104s24p3,C正确;
D.反式聚异戊二烯的结构简式: ,D错误;
故选C。
8.元素M、W、X、Y、Z分别位于3个短周期,原子序数依次增大,X原子最外层电子数是电子层数的2
倍,Y的价电子数是Z价电子数的2倍,Z基态原子的电子占据7个原子轨道,M、W可以形成的化合物
为WM。下列说法正确的是
A.离子半径:WW>Q
【答案】B
【分析】X、Y、Z、E、Q、W为原子序数依次增大的短周期主族元素,根据原子的成共价键的数量和所
带电荷数可判断X为H,Y为C,Z为N。根据原子序数大小,且Z与Q、E与W分别位于同一主族,可知Q为P,E为F,W为Cl。
【解析】A.由分析可知,Y为C,X为H,YX 为乙炔,为含有极性键的非极性分子,A正确;
2 2
B.由分析可知,Y为C,Z为N,由于C的氢化物有很多,有固态、液态和气态,而N的氢化物为NH3
和N2H4等,故无法比较它们氢化物的沸点,B错误;
C.原子序数为83的元素为铋,其位于第六周期第ⅤA族,与N位于同一主族,C正确;
D.由分析可知,E为F、W为Cl、Q为P,根据同一周期元素的第一电离从左往右增大趋势但ⅡA与
ⅢA、ⅤA与ⅥA反常,同一主族从上往下依次减小,故三种元素的第一电离能大小顺序为:F>Cl>P即
E>W>Q,D正确;
故答案为:B。
12.某食品添加剂的主要成分为WZ(RY )·12X Y。已知X、Y、Z、R、W为原子序数依次增大的前20号
4 2 2
元素,X、Z的周期序数等于主族序数,Y和R位于同主族,基态X、W原子最外层电子排布式为ns1。下
列叙述正确的是
A.原子半径:W>R>Z>Y> X
B.电负性:Y>R>X>Z> W
C.常温下,Z、W单质都能与水发生置换反应
D.R的最高价氧化物对应水化物一定有强氧化性
【答案】B
【分析】已知X、Y、Z、R、W为原子序数依次增大的前20号元素,基态X原子最外层电子排布式为
ns1,X、Z的周期序数等于主族序数,推测X为氢、Z为铝;W原子最外层电子排布式为ns1,W为钾;Y
和R位于同主族,结合物质化学式,推测Y为氧、R为硫;代入检验推理合理;
【解析】A.电子层数越多半径越大,电子层数相同时,核电荷数越大,半径越小;原子半径:W> Z>R>
Y> X,A错误;
B.同周期从左到右,金属性减弱,非金属性变强,元素的电负性变强;同主族由上而下,金属性增强,
非金属性逐渐减弱,元素电负性减弱;电负性:Y>R>X>Z> W,B正确;
C.常温下铝和水不能反应,C错误;
D.R的最高价氧化物对应水化物为硫酸,浓硫酸有强氧化性、而稀硫酸氧化性较弱,D错误;
故选B。
13.短周期元素W、X、Y、Z的原子序数依次增大,它们组成一种团簇分子,结构如图所示。W、Z的族
序数均等于周期序数,X原子核外最外层电子数是其电子总数的 ,下列说法正确的是A.电负性:XAl>Mg,即X>Z>Y,故A错误;
B.常温下,W与X形成的化合物为HO或HO,这两种物质在常温下都是液态,故B正确;
2 2 2
C.该分子中H原子周围不满足8电子的结构,故C错误;
D.Y的最高价氧化物对应的水化物是Mg(OH) ,Z的是Al(OH) ,同周期从左到右,金属性减弱,金属性
2 3
越弱,碱性越弱,所以碱性Mg(OH) >Al(OH) ,即Y>Z,故D错误;
2 3
故本题选B。
14.科学家用配位化合物氯金酸钠(NaAuCl )溶液与泪液中的葡萄糖发生反应生成纳米金单质颗粒(直径为
4
20~60nm)。下列说法错误的是
A.葡萄糖分子中6个碳均为手性碳原子
B.第一电离能:Cl>Na
C.上述反应中,氯金酸钠表现氧化性
D.生成的纳米金分散在水中所得分散系可产生丁达尔效应
【答案】A
【解析】A.连有4个不同原子或原子团的碳为手性碳,葡萄糖分子中6个碳中4个碳为手性碳原子,A项
错误;
B.同周期从左到右,元素第一电离能整体呈增大的趋势,则第一电离能;NaZ
C.Y与M形成的化合物中不可能含有非极性共价键
D.最高价氧化物对应水化物的酸性:X>Q
【答案】C
【分析】X、Y、Z、M、Q为五种短周期元素,原子序数依次增大,Q原子序数最大,s能级电子数比p能
级电子数少1,Q原子的电子排布式为1s22s22p63s23p1,Q为Al,X与Al同主族,2s轨道全充满,X为B,
Y和M为同周期元素且是纯碱中的两种元素,则Y为C,M为O,则Z为N。
【解析】A.C的最高正价为+4价,N的最高正价为+5价,最高正价CN,B正确;
C.C和O能形成C O,其结构式为O=C=C=C=O,含有非极性共价键,C错误;
3 2
D.B的非金属性强于Al,则最高价氧化物对应水化物的酸性HBO>Al(OH) ,D正确;
3 3 3
故答案选C。
16.某种化学品的结构如下图所示,已知W、X、Y、Z、M均为短周期主族元素,其中W、X、Y在同一
周期,Z、M同处另一周期,M的简单阳离子半径是同周期中最小的,则下列说法中正确的是
A.元素电负性大小的顺序:X>W>Y>Z
B.W的某种单质的分子,是极性分子且分子中含有极性键C.同一周期中,元素第一电离能处在Z和M之间的有2种
D.该分子中Y原子的杂化方式为sp2
【答案】B
【分析】W、X、Y、Z、M均为短周期主族元素,其中W、X、Y在同一周期,Z、M同处另一周期,M
的简单阳离子半径是同周期中最小的,可知M为Al元素,化合物中Z形成6个共价键,Z为S元素;X形
成1个共价键、Y形成4个共价键、W形成2个共价键,则X为F元素、Y为C元素、W为O元素,以此
来解答。
【解析】由上述分析可知,W为O元素、X为F元素、Y为C元素、Z为S元素、M为Al元素,
A.同周期,从左到右,元素的电负性逐渐增大,同主族从上到下,元素的电负性逐渐变小,则电负性
F>O>S>C,故A错误;
B.O 的空间结构为V形,分子中正电荷中心和负电荷中心不重合,O 是极性分子,分子中含有极性键,
3 3
故B正确;
C.同一周期中,随着核电荷数的增加,元素的第一电离呈现增大趋势,ⅡA族、ⅤA族反常,则元素第
一电离能处在Al和S之间的有Si共1种,故C错误;
D.Y为C原子,价层电子对数是4,杂化方式为sp3,故D错误;
故选:B。
17.我国科学家在寻找新的点击反应砌块的过程中,意外发现一种安全、高效的合成化合物,其结构简式
如图所示,其中X、Y、Z和W是原子序数依次增大的短周期元素,W的原子序数是Y的二倍。下列说法
错误的是
A.简单氢化物的稳定性:Z>Y
B.第二电离能:X>Y
C.XY为直线形结构
2
D.分子中除W外,其他元素均满足8电子结构
【答案】D
【分析】由图可知Y形成两对共用电子对形成稳定结构,结合原子序数,Y为O,W的原子序数是Y的二
倍,W为S,X形成三对共用电子对达到稳定结构,X为N,Z形成一对共用电子对形成稳定结构,结合
原子序数可知Z为F,据此分析解答。【解析】A.非金属性F>O,则氢化物的稳定性:HF>H O,故A正确;
2
B.N+最高能级为2p2,F+最高能级为2p4,F+再失去一个电子形成半满稳定结构,则F+更易失去一个电
子,即第二电离能:N> F,故B正确;
C.NO与CO 互为等电子体,等电子体的空间构型相同,CO 为直线结构,则NO为直线形结构,故C
2 2 2 2
正确;
D.由结构简式可知除S外,带负电荷的N原子不满足八电子稳定结构,故D错误;
故选:D。
18.X、Y、Z、W 是原子序数依次增大的四种短周期元素。基态X、Z原子的电子均填充了3个能级,且
均有2个未成对电子,W的核外电子数是X原子最外层电子数的3倍。下列说法正确的是
A.第一电离能:X<Y<Z B.元素X的氢化物的沸点一定比元素Y的氢化物低
C.Z与W组成的化合物可作耐高温材料 D.简单离子半径:r(W)>r(Z)>r(Y)
【答案】C
【分析】X、Y、Z、W 是原子序数依次增大的四种短周期元素。基态X、Z原子的电子均填充了3个能
级,且均有2个未成对电子,则X为碳、Z为氧,那么Y为氮;W的核外电子数是X原子最外层电子数的
3倍,W为12号元素镁;
【解析】A.同一周期随着原子序数变大,第一电离能变大,N的2p轨道为半充满稳定状态,第一电离能
大于同周期相邻元素,第一电离能:X<Z<Y,A错误;
B.碳可以形成相对分子质量很大的烃,其沸点可能很高,故元素X的氢化物的沸点不一定比元素Y的氢
化物低,B错误;
C.Z与W组成的化合物氧化镁熔点很高,可作耐高温材,C正确;
D.电子层数越多半径越大,电子层数相同时,核电荷数越大,半径越小;简单离子半径:r(Y)>r(Z)>
r(W),D错误;
故选C。
19.中国第一辆火星车“祝融号”成功登陆火星。探测发现火星上存在大量含氧橄榄石矿物
。已知前四周期元素X、Y、Z、R、W的原子序数依次增大,Y的氢化物常用于雕刻玻璃,R元素的一种
氧化物可制作光导纤维,W的合金材料是生活中用途最广泛的金属材料。其态Z原子核外s,p能级上电子
总数相等。下列叙述正确的是
A.电负性: B. 分子的键角为C.简单氢化物的稳定性: D.熔点:
【答案】B
【分析】常用于雕刻玻璃的氢化物为HF,则Y为F;R元素的一种氧化物可制作光导纤维,则该氧化物为
SiO,R为Si;W的合金材料是生活中用,途最广泛的金属材料,则W为Fe;基态Z原子核外s、p能级
2
上电子总数相等,则其电子排布式为1s22s22p4或1s22s22p63s2,又因为X、Y、Z、R、W的原子序数依次增
大,则Z的原子序数需大于F,故Z为Mg,根据含氧橄榄石矿物,可知X为O,以此解题。
【解析】A.电负性:同一周期从左往右主族元素电负性依次增强,同一主族从上往下电负性依次减小,
则电负性F>O>Si>Fe>Mg,即Y> X> R> W> Z,故A错误;
B.SiF 中Si为sp3杂化,分子为正四面体构型,键角为109°28',故B正确;
4
C.F的非金属性比O强,稳定性HF > H O,故C错误;
2
D.MgF 为离子晶体,,SiO 为原子晶体,原子晶体熔点一般高于离子晶体,MgF 熔点1261°C,SiO 熔点
2 2 2 2
1600 ~ 1700°C,故熔点MgF < SiO,故D错误;
2 2
故选B。
20.X、Y、Z、W、Q五种短周期元素,原子序数依次增大。X元素基态原子电子排布式为 ,Y
元素的第一电离能大于同周期相邻元素的第一电离能,Z元素基态原子2p轨道有一个未成对电子,W元素
基态原子s能级上的电子总数与p能级上电子总数相等,Q是地壳中含量最多的金属元素。下列说法不正
确的是
A.最高价氧化物对应水化物的碱性:
B.Y和原子序数为51的元素位于同一主族
C.同周期元素中Z的第一电离能最大
D.X、Q的氧化物、氢氧化物都有两性
【答案】C
【解析】X、Y、Z、W、Q五种短周期元素,原子序数依次增大,X元素基态原子电子排布式为
,n=2,则X为Be元素;Q是地壳中含量最多的金属元素,则Q为Al元素;Y元素的第一电离能大于同
周期相邻元素的第一电离能,Y位于IIA或VA族,且原子序数介于Be,O之间,则Y元素为N元素,W
元素基态原子s能级上的电子总数与p能级上电子总数相等,W原子核外电子排布式为 ,则
W为Mg元素;Z元素基态原子2p轨道有一个未成对电子,且原子序数介于O、Al之间,Z原子核外电子排布式为 ,则Z为F元素;
A.金属性:Be