文档内容
第 30 讲 分子结构与性质
1.下列叙述中正确的是( )
A.以非极性键结合起来的双原子分子一定是非极性分子
B.BCl 与NCl 均为三角锥形结构,均为极性分子
3 3
C.非极性分子只能是双原子单质分子
D.非极性分子中一定含有非极性键
【答案】A
【解析】B错误,BCl 为平面三角形结构,为非极性分子;C错误,某些共价化合物,如CH 、C H
3 4 2 4
等也是非极性分子;D错误,非极性分子中不一定含有非极性键,如CH、CO 等。
4 2
2.硒是人体必需的微量元素之一,价电子排布式为2nsn2np2n。下列说法错误的是( )
A.沸点:HSe>H O B.稳定性:HSeSO
2 3
【答案】A
【解析】根据s轨道上最多排2个电子可知,硒的价电子排布式为4s24p4,故其位于第四周期第ⅥA
族。HO分子间能形成氢键,故HO的沸点高于HSe,A错误。
2 2 2
3.下列事实不能用分子间作用力或氢键解释的是( )
A.HF、HO的沸点分别比HCl、HS的沸点高很多
2 2
B.正戊烷的沸点比新戊烷的沸点高
C. 的沸点比 的沸点低
D.NaO的熔点比MgO的熔点低
2
【答案】D
【解析】NaO和MgO均为离子晶体,其熔点与分子间作用力和氢键无关,D符合题意。
2
4.下列说法正确的是( )
A.甘油(CHOH—CHOH—CH OH)分子中含有1个手性碳原子
2 2
B.互为手性异构体的化合物,所含化学键的种类和数目完全相同
C.互为手性异构体的化合物,在三维空间不能重合,但物理、化学性质却几乎完全相同D.互为手性异构体的化合物,分子组成不同,所以物理、化学性质也不同
【答案】B
【解析】CHOH—CHOH—CH OH分子中不存在手性碳原子,故A错误;互为手性异构体的化合物,
2 2
物理性质不同,光学活性不同,故C错误;互为手性异构体的化合物,分子组成相同,故D错误。
5.已知几种共价键的键能如下:
化学键 H—N N≡N Cl—Cl H—Cl
键能/kJ·mol-1 390.8 946 242.7 431.8
下列说法错误的是( )
A.键能:N≡N>N===N>N—N
B.H(g)+Cl(g)===HCl(g) ΔH=-431.8 kJ·mol-1
C.H—N键能小于H—Cl键能,所以NH 的沸点高于HCl
3
D.2NH (g)+3Cl(g)===N (g)+6HCl(g) ΔH=-463.9 kJ·mol-1
3 2 2
【答案】C
【解析】C项,NH 的沸点高于HCl是由于NH 能形成分子间氢键,而HCl不能,错误。
3 3
6.徐光宪在《分子共和国》一书中介绍了许多明星分子,如HO、CO、BF、CHCOOH等。下列说
2 2 2 3 3
法正确的是( )
A.HO 分子中的O为sp2杂化 B.CO 分子中C原子为sp杂化
2 2 2
C.BF 分子中的B原子为sp3杂化 D.CHCOOH分子中C原子均为sp2杂化
3 3
【答案】B
【解析】A项,HO 分子中氧原子形成2个σ键,含有2对孤电子对,采取sp3杂化,错误;B项,
2 2
CO 分子中C原子形成2个σ键,没有孤电子对,采取sp杂化,正确;C项,BF 分子中的B原子的最外
2 3
层电子数为3,形成3个σ键,没有孤电子对,采取sp2杂化,错误;D项,CHCOOH分子中有2个碳原
3
子,其中甲基上的碳原子形成4个σ键,没有孤电子对,采取sp3杂化,错误。
7.膦又称磷化氢,化学式为PH ,在常温下是一种无色有大蒜臭味的有毒气体,它的分子呈三角锥
3
形。以下关于PH 的叙述中正确的是( )
3
A.PH 是非极性分子 B.PH 中有未成键电子对
3 3
C.PH 是一种强氧化剂 D.PH 分子中P—H键是非极性键
3 3
【答案】B
【解析】A项,正负电荷中心不重合的分子为极性分子,正负电荷中心重合的分子为非极性分子;B
项,PH 分子中有1个未成键的孤电子对;C项,根据P元素的化合价分析,错误;D项,同种非金属元素
3
之间存在非极性键,不同种非金属元素之间存在极性键。8.氨溶于水时,大部分NH 与HO以氢键(用“…”表示)结合形成NH ·H O分子。根据氨水的性质可
3 2 3 2
推知NH ·H O的结构式为( )
3 2
A. B. C. D.
【答案】B
【解析】根据NH ·H ONH+OH-可知NH ·H O的结构式为 。
3 2 3 2
9.Ⅰ.[Zn(CN) ]2-在水溶液中与HCHO发生如下反应:
4
4HCHO+[Zn(CN) ]2-+4H++4HO===[Zn(H O) ]2++4HOCH CN
4 2 2 4 2
(1)基态Zn2+核外电子排布式为________________________。
(2)1 mol HCHO分子中含有σ键为________mol。
(3)HOCHCN分子中碳原子轨道的杂化类型是__________________。
2
Ⅱ.M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素。M基态原子L层中p轨
道电子数是s轨道电子数的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起
酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满。请回答下列问题:
(1)Z位于元素周期表________族,R基态原子的电子排布式是________,X和Y中电负性较大的是
________(填元素符号)。
(2)X氢化物的沸点低于与其组成相似的M的氢化物,其原因是________________________________。
(3)X与M形成的XM 分子的空间结构是__________。
3
【答案】Ⅰ.(1)1s22s22p63s23p63d10(或[Ar]3d10)
(2)3 (3)sp3和sp
Ⅱ.(1)ⅥB [Ne]3s1(或1s22s22p63s1) Cl
(2)H O分子间存在氢键,HS分子间无氢键
2 2
(3)平面三角形
【解析】Ⅰ.(3)在HOCH CN分子中,连有羟基的碳原子的杂化类型是sp3,—CN中碳原子杂化类型是
2sp。
Ⅱ.M、R、X、Y为原子序数依次增大的短周期主族元素,M基态原子L层中p轨道电子数是s轨道电
子数的2倍,M是O;R是同周期元素中最活泼的金属元素,R是Na;X和M形成的一种化合物是引起酸
雨的主要大气污染物,X是S,则Y是Cl;Z是一种过渡元素,基态原子4s和3d轨道半充满,即价电子排
布式为3d54s1,Z是Cr。
10.已知H和O可以形成HO和HO 两种化合物,试根据有关信息完成下列问题:
2 2 2
(1)水是维持生命活动所必需的一种物质。
①1 mol冰中有________mol氢键。
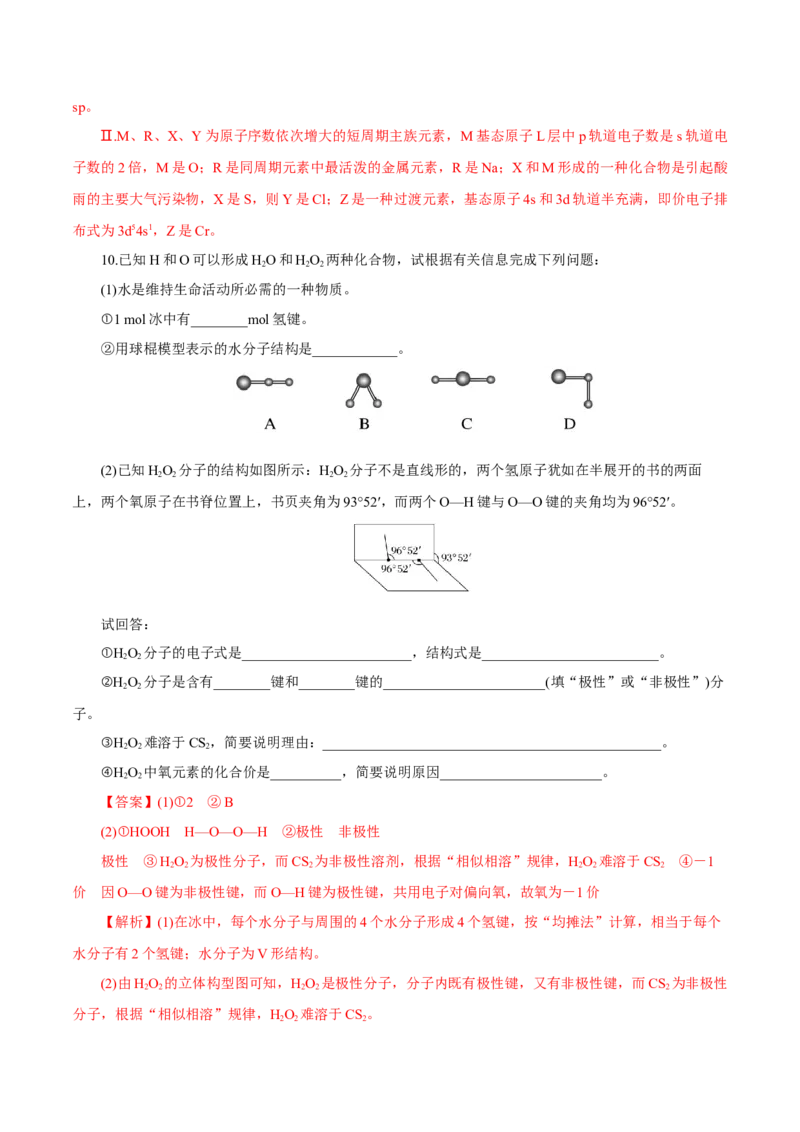
②用球棍模型表示的水分子结构是____________。
(2)已知HO 分子的结构如图所示:HO 分子不是直线形的,两个氢原子犹如在半展开的书的两面
2 2 2 2
上,两个氧原子在书脊位置上,书页夹角为93°52′,而两个O—H键与O—O键的夹角均为96°52′。
试回答:
①HO 分子的电子式是________________________,结构式是_________________________。
2 2
②H O 分子是含有________键和________键的_______________________(填“极性”或“非极性”)分
2 2
子。
③HO 难溶于CS,简要说明理由:________________________________________________。
2 2 2
④H O 中氧元素的化合价是__________,简要说明原因_______________________。
2 2
【答案】(1)①2 ②B
(2)①HOOH H—O—O—H ②极性 非极性
极性 ③HO 为极性分子,而CS 为非极性溶剂,根据“相似相溶”规律,HO 难溶于CS ④-1
2 2 2 2 2 2
价 因O—O键为非极性键,而O—H键为极性键,共用电子对偏向氧,故氧为-1价
【解析】(1)在冰中,每个水分子与周围的4个水分子形成4个氢键,按“均摊法”计算,相当于每个
水分子有2个氢键;水分子为V形结构。
(2)由HO 的立体构型图可知,HO 是极性分子,分子内既有极性键,又有非极性键,而CS 为非极性
2 2 2 2 2
分子,根据“相似相溶”规律,HO 难溶于CS。
2 2 21.根据等电子原理判断,下列说法中错误的是( )
A.B NH 分子中所有原子均在同一平面上
3 3 6
B.B NH 分子中存在双键,可发生加成反应
3 3 6
C.H O+和NH 是等电子体,均为三角锥形
3 3
D.CH 和NH是等电子体,均为正四面体形
4
【答案】B
【解析】B NH 和苯是等电子体,其结构相似;C项,HO+和NH 是等电子体,根据氨气分子的立体
3 3 6 3 3
构型判断水合氢离子的立体构型;D项,CH 和NH是等电子体,根据甲烷的立体构型判断铵根离子的立
4
体构型。
2.通常把原子总数和价电子总数相同的分子或离子称为等电子体。人们发现等电子体的空间结构相
同,则下列有关说法中正确的是( )
A.CH 和NH是等电子体,键角均为60°
4
B.NO和CO是等电子体,均为平面三角形结构
C.HO+和PCl 是等电子体,均为三角锥形结构
3 3
D.B NH 和苯是等电子体,B NH 分子中不存在“肩并肩”式重叠的轨道
3 3 6 3 3 6
【答案】B
【解析】CH 和NH是正四面体结构,键角是109°28′,A错;NO和CO是等电子体,均为平面三角形
4
结构,B对;HO+和PCl 的价电子总数不相等,不互为等电子体,C错;苯分子中存在“肩并肩”式重叠
3 3
的轨道,故其等电子体B NH 分子中也存在,D错。
3 3 6
3.短周期主族元素W、X、Y、Z的原子序数逐渐增大,四种元素形成的化合物甲的结构如图所示。
且W与X、Y、Z均可形成电子数相等的分子,WZ常温常压下为液体。下列说法正确的是( )
2
A.YW 分子中的键角为120°
3
B.WZ的稳定性大于YW
2 3
C.物质甲分子中存在6个σ键
D.Y元素的氧化物对应的水化物为强酸
【答案】B【解析】根据图示可知,X原子最外层含有4个电子,Y原子最外层含有5个电子,Z原子最外层含有
6个电子,W最外层含有1个或7个电子,结合题干信息可知,W为H元素,X为C元素,Y为N元素,
Z为O元素。YW 为NH ,NH 的结构为三角锥形,键角为107°,故A错误;非金属性:O>N,则HO的
3 3 3 2
稳定性大于NH ,故B正确;双键中含有1个σ键和1个π键,根据图示可知,物质甲分子中存在7个σ
3
键,故C错误;N的氧化物对应的水化物不一定为强酸,如亚硝酸为弱酸,故D错误。
4.下列说法中正确的是( )
A.PCl 分子空间结构是三角锥形,这是因为P原子采取sp3杂化,且含有一对孤电子对
3
B.sp3杂化轨道是由任意的1个s轨道和3个p轨道混合形成的四个sp3杂化轨道
C.凡中心原子采取sp3杂化的分子,其VSEPR模型都是四面体形
D.AB 型的分子空间结构必为平面三角形
3
【答案】AC
【解析】A项,PCl 分子的中心原子P含有3个成键电子对和1对孤电子对,为sp3杂化,空间结构为
3
三角锥形,正确;B项,能量相近的s轨道和p轨道形成杂化轨道,错误;D项,AB 型的分子空间结构与
3
中心原子的孤电子对数有关,如BF 中B原子没有孤电子对,为平面三角形,NH 中N原子有1对孤电子
3 3
对,为三角锥形,错误。
5.尿的主要成分是尿素,化学式为 CO(NH) ,结构简式可表示为 。下列有关说法正确
2 2
的是( )
A.1 mol CO(NH ) 分子中含有3 mol σ键
2 2
B.CO(NH) 分子中C原子、N原子的轨道杂化类型均为sp3
2 2
C.组成尿素的四种元素第一电离能由大到小的顺序是O、N、C、H
D.根据结构推测,尿素可能易溶于水,熔、沸点高于丙酮( )
【答案】D
【解析】单键是σ键,双键中有一个σ键,所以1 mol CO(NH ) 分子中含有7 mol σ键,故A错误;
2 2
CO(NH) 分子中C原子形成三个σ键、N原子形成三个σ键和一对孤电子对,所以C原子、N原子的轨道
2 2
杂化类型分别为sp2、sp3,故B错误;同一周期元素,其第一电离能随着原子序数增大而呈增大趋势,但
第ⅡA族、第ⅤA族第一电离能大于其相邻元素,这四种元素第一电离能由大到小的顺序是N、O、C、
H,故C错误;尿素分子与水分子间易形成氢键,所以尿素可能易溶于水,尿素分子间也可形成氢键,所以尿素的熔、沸点高于丙酮,故D正确。
6.关于化学式为[TiCl(HO)]Cl·HO的配合物,下列说法正确的是( )
2 5 2 2
A.配位体是Cl-和HO,配位数是8
2
B.中心离子是Ti4+,配离子是[TiCl(HO)]2+
2 5
C.内界和外界中的Cl-的数目比是1∶2
D.在1 mol该配合物中加入足量AgNO 溶液,可以得到3 mol AgCl沉淀
3
【答案】C
【解析】配合物[TiCl(HO)]Cl·HO中配位体是Cl-和HO,配位数是6,故A错误;中心离子是Ti3+,故
2 5 2 2 2
B错误;配合物[TiCl(HO)]Cl·HO,内配离子Cl-为1,外配离子Cl-为2,内界和外界中的Cl-的数目比是
2 5 2 2
1∶2,故C正确;加入足量AgNO 溶液,外界离子Cl-与Ag+反应,内配离子Cl-不与Ag+反应,1 mol该配合物
3
只能生成2 mol AgCl沉淀,故D错误。
7.通常情况下,NCl 是一种油状液体,其分子立体构型与NH 相似,下列对NCl 和NH 的有关叙述错误
3 3 3 3
的是( )
A.分子中N—Cl键键长与CCl 分子中C—Cl键键长不相等
4
B.NCl 分子是极性分子
3
C.NBr 比NCl 易挥发
3 3
D.在氨水中,大部分NH 与HO以氢键(用“…”表示)结合形成NH·HO分子,则NH·HO的结构式为
3 2 3 2 3 2
【答案】C
【解析】C原子的原子半径大于N原子的原子半径,所以CCl 中C—Cl键键长比NCl 中N—Cl键键长长,
4 3
故A正确;NCl 的分子立体构型与氨分子相似,都是三角锥形结构,氨分子是极性分子,所以NCl 分子也是极
3 3
性分子,故B正确;分子晶体中物质的熔、沸点与相对分子质量有关,一般来说,对于组成和结构相似的物质,
相对分子质量越大其熔、沸点越高,所以NBr 比NCl 的熔、沸点高,NCl 比NBr 易挥发,故C错误;在氨水
3 3 3 3
中, NH 与HO以氢键(用“…”表示)结合形成NH·HO分子;则NH·HO的结构式为 ,故D
3 2 3 2 3 2
正确。8.氯吡苯脲是一种常用的膨大剂,其结构简式为 ,它是经国家批准使用的植物生
长调节剂。请回答下列问题:
(1)基态氯原子核外未成对电子数为________。
(2)氯吡苯脲分子中,氮原子的杂化类型为________,碳原子的杂化类型为________,该分子
________(填“是”或“不是”)手性分子。
(3)查阅文献知,可用2氯4氨基吡啶与异氰酸苯酯反应生成氯吡苯脲。反应方程式如下:
+ ―→
反应过程中,每生成1 mol氯吡苯脲,断裂______个σ键、______个π键。
(4)膨大剂能在动物体内代谢,其产物较为复杂,其中有HO、NH 、CO 等。
2 3 2
①请用共价键知识解释HO比NH 稳定的原因:________________________________________。
2 3
②CO 的水溶液中含有 CO,则该阴离子的 VSEPR模型名称为________,中心原子的杂化类型为
2
________。
【答案】(1)1 (2)sp2、sp3 sp2 不是 (3)6.02×1023 6.02×1023
(4)①H—O键的键能大于H—N键的键能 ②平面三角形 sp2
【解析】(3)反应过程中,异氰酸苯酯分子断裂N===C中的1个π键,2氯4氨基吡啶分子断裂1个σ键
(N—H键)。
9.我国科学家借助自主研制的新型钨钴铁合金催化剂攻克了单壁碳纳米管结构的可控制备难题。海底
金属软泥是在海底覆盖着的一层红棕色沉积物,蕴藏着大量的金属资源,含有钨、铁、锰、锌、钴等金属
元素。
(1)基态钴原子的价电子排布图为________________________________。单壁碳纳米管可看作石墨烯沿
一定方向卷曲而成的空心圆柱体,其碳原子的杂化方式为________。
(2)纳米结构氧化钴可在室温下将甲硫醛(CHS)完全催化氧化,甲硫醛分子属________(填“极性”或
2
“非极性”)分子,其中心原子的VSEPR模型名称为________。
(3)多原子分子中各原子若在同一平面内,且有相互平行的 p轨道,则p电子可在多个原子间运动,形
成“离域π键”。下列物质中存在“离域π键”的是____________(填字母)。
A.苯 B.二氧化硫
C.四氯化碳 D.环己烷
【答案】(1) sp2 (2)极性 平面三角形 (3)AB【解析】(1)石墨是平面层状结构,石墨烯可看作单层石墨,单壁碳纳米管可看作石墨烯沿一定方向卷
曲而成的空心圆柱体,则碳原子均形成3个C—C键,杂化轨道数目为3,碳原子杂化方式为sp2。
(2)甲硫醛(CHS)中C原子形成3个σ键,1个π键,VSEPR模型名称为平面三角形,正负电荷中心不
2
重合,属于极性分子。
(3)苯分子中每个碳原子都采用sp2杂化,则6个碳原子均有未参与杂化的相互平行的p轨道,故苯环上
的C原子可以形成“离域π键”,其“离域π键”为Π,故选A;二氧化硫分子中S上的孤电子对数为=
1,价层电子对数为2+1=3,故中心原子为sp2杂化,立体构型为V形,中心原子S与两个O原子中有相
互平行的p轨道,可以形成“离域π键”,其“离域π键”为Π,故选B;四氯化碳分子中只存在σ键,不
存在π键,故不选C;环己烷分子中只存在σ键,不存在π键,故不选D。
10.判断含氧酸酸性强弱的一条经验规律是含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性
越强。如下表所示:
含氧酸酸性强弱与非羟基氧原子数的关系
次氯酸 磷酸 硫酸 高氯酸
含氧酸 Cl—OH
非羟基氧原子数 0 1 2 3
酸性 弱酸 中强酸 强酸 最强酸
(1)亚磷酸HPO 和亚砷酸HAsO 分子式相似,但它们的酸性差别很大,HPO 是中强酸,HAsO 既
3 3 3 3 3 3 3 3
有弱酸性又有弱碱性。由此可推出它们的结构简式分别为
①________________,②________________。
(2)H PO 和HAsO 与过量的NaOH溶液反应的化学方程式分别是
3 3 3 3
①________________________________________________________________________,
②________________________________________________________________________。
(3)在HPO 和HAsO 中分别加入浓盐酸,分析反应情况:______________________________,
3 3 3 3
写出化学方程式:________________________________________________________________。
【答案】(1)① ②
(2)①HPO +2NaOH===Na HPO +2HO
3 3 2 3 2
②H AsO +3NaOH===Na AsO +3HO
3 3 3 3 2(3)H PO 为中强酸,不与盐酸反应,HAsO 可与盐酸反应 HAsO +3HCl===AsCl +3HO
3 3 3 3 3 3 3 2
【解析】此题属于无机含氧酸的结构、性质推断题,考查同学们运用题给信息推断物质结构和性质的
能力。(1)已知HPO 为中强酸,HAsO 为弱酸,依据题给信息可知HPO 中含1个非羟基氧原子,HAsO
3 3 3 3 3 3 3 3
中不含非羟基氧原子。(2)与过量NaOH溶液反应的化学方程式的书写,需得知HPO 和HAsO 分别为几
3 3 3 3
元酸,从题给信息可知,含氧酸分子结构中含几个羟基氢,则该酸为几元酸。故HPO 为二元酸,HAsO
3 3 3 3
为三元酸。
(3)H PO 为中强酸,不与盐酸反应;HAsO 为两性物质,可与盐酸反应。
3 3 3 3
1. (1)[2018·全国卷Ⅰ·35(3)]LiAlH 是有机合成中常用的还原剂。LiAlH 中,存在________(填标号)。
4 4
A.离子键 B.σ键 C.π键 D.氢键
(2)[2018·全国卷Ⅲ·35(3)]ZnF 具有较高的熔点(872 ℃),其化学键类型是________。
2
(3)[2018·江苏高考·21(4)(5)]N 分子中σ键与π键的数目比n(σ)∶n(π)=________。
2
[Fe(H O) ]2+与NO反应生成的[Fe(NO)(H O) ]2+中,NO以N原子与Fe2+形成配位键。请在[Fe(NO)
2 6 2 5
(H O) ]2+结构示意图的相应位置补填缺少的配体。
2 5
[Fe(NO)(H O) ]2+结构示意图
2 5
【解析】(1)阴阳离子间存在离子键,Al与H之间还有共价单键,共价单键为σ键不存在双键和氢键。
(2)ZnF 具有较高的熔点(872 ℃),可以判断其为离子化合物,所以一定存在离子键。(3)N 的结构式为
2 2
N≡N,三键中含1个σ键和2个π键,N 分子中σ键与π键的数目比为n(σ)∶n(π)=1∶2。根据化学式,缺少的
2
配体是NO和HO,NO中N为配位原子,HO中O上有孤电子对,O为配位原子,故为
2 2
。
【答案】(1)AB (2)离子键
(3)1∶22.(1)(2018·江苏化学,21节选)与O 分子互为等电子体的一种阴离子为________(填化学式)。
3
(2)(2016·江苏化学,21节选)与HO分子互为等电子体的阴离子为________。
2
【解析】(1)等电子体的原子数相同,电子数相同。将臭氧分子中的一个氧原子换成电子数较少的原
子,然后增加缺少的电子将其变为阴离子即可,如NO。
【答案】(1) NO (2) NH
3.(1)(2017·全国Ⅰ卷,35节选)X-射线衍射测定等发现,IAsF 中存在I离子。I离子的几何构型为
3 6
________,中心原子的杂化形式为________。
(2)(2017·全国Ⅲ卷,35节选)CO 和CHOH分子中C原子的杂化形式分别为________和________。
2 3
(3)(2017·江苏,21节选)丙酮( )分子中碳原子轨道的杂化类型是________。
【解析】(1)I中I原子为中心原子,则其孤电子对数为1/2×(7-1-2)=2,且其形成了2个σ键,中心
原子采取sp3杂化,空间构型为V形。
(2)CO 中C原子的价层电子对数为2,故为sp杂化,CHOH分子中C的价层电子对数为4,故为sp3
2 3
杂化。
(3)甲基上的碳原子形成4个σ键,故采用sp3杂化,羰基上的碳原子形成3个σ键,故采用sp2杂化。
【答案】(1)V形 sp3 (2)sp sp3 (3)sp2、sp3
4.(1)(2019·全国Ⅱ卷,35节选)元素As与N同族。预测As的氢化物分子的立体结构为________,其沸
点比NH 的________(填“高”或“低”),其判断理由是
3
___________________________________________。
(2)(2018·全国Ⅱ卷,35节选)硫及其化合物有许多用途,相关物质的物理常数如下表所示:
HS S FeS SO SO HSO
2 8 2 2 3 2 4
熔点/ ℃ -85.5 115.2 -75.5 16.8 10.3
>600(分解)
沸点/ ℃ -60.3 444.6 -10.0 45.0 337.0
S 的结构如图,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为
8
___________________________________________。
(3)(2017·江苏,21节选)乙醇的沸点高于丙酮,这是因____________________________________。
【解析】(1)AsH 的中心原子As的价层电子对数为(5+3)/2=4,包括3对成键电子和1对孤对电子,
3
故其立体结构为三角锥形。NH 易形成分子间氢键,从而使其沸点升高。(2)S 和SO 都形成分子晶体,影
3 8 2响其熔点、沸点的主要因素是范德华力,而S 的相对分子质量大,分子间范德华力强,故S 的熔点、沸点
8 8
较高。(3)乙醇分子间存在氢键,所以沸点较高
【答案】(1)三角锥形 低 NH 分子间存在氢键
3
(2)S 相对分子质量大,分子间范德华力强
8
(3)乙醇分子间存在氢键