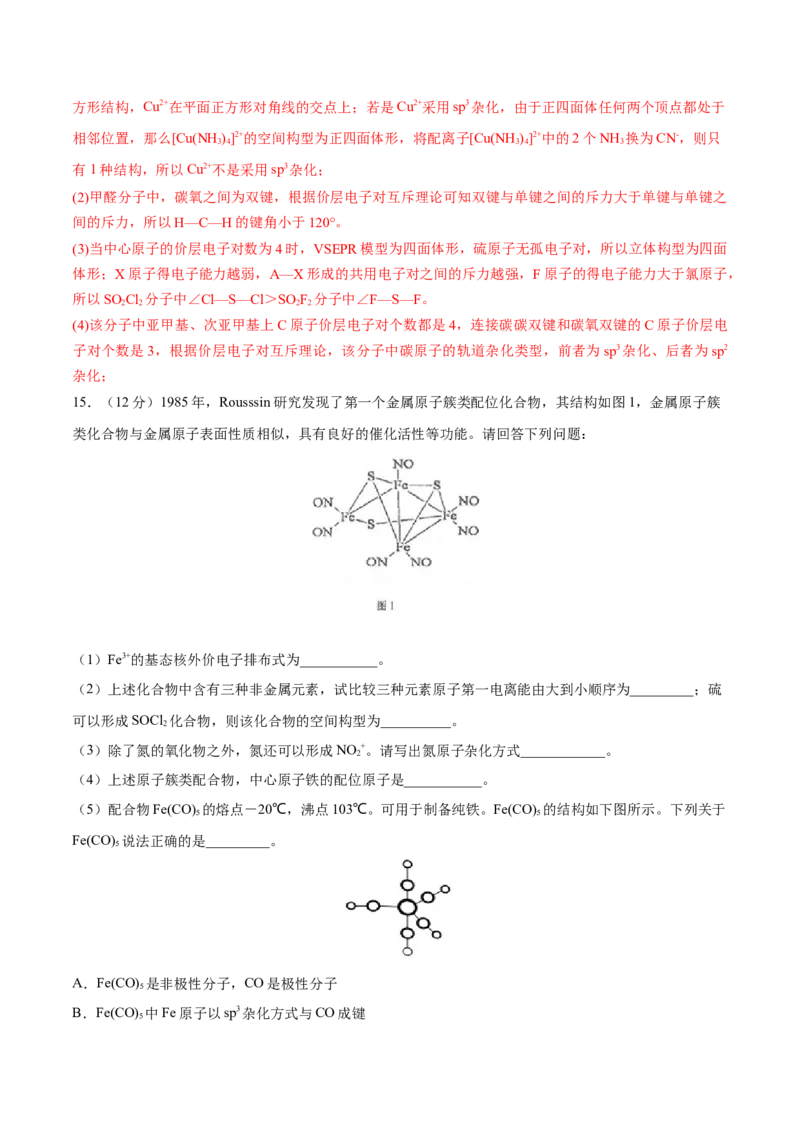
文档内容
第 37 讲 分子结构与性质
第一部分:高考真题感悟
1.(2022·江苏·高考真题)少量 与 反应生成 和 。下列说法正确的是
A. 的电子式为 B. 的空间构型为直线形
C. 中O元素的化合价为-1 D. 仅含离子键
【答案】C
【解析】A.过氧化钠是离子化合物,电子式是 ,A错误;B. 中氧原子的成
键电子对是2,孤电子对是2,根据价层电子对为4,根据价层电子对互斥理论,其空间构型为V形,B错
误;C. 中H显+1价,根据正负化合价为0,可计算出O的化合价为-1,C正确;D. 中O和
H之间是共价键,D错误;故选C。
2.(2022·辽宁·高考真题)下列符号表征或说法正确的是
A. 电离: B. 位于元素周期表p区
C. 空间结构:平面三角形 D. 电子式:
【答案】C
【解析】A. 是二元弱酸,电离分步进行,其一级电离方程式为 ,A错误;B.基态
原子的价电子排布式是 ,最后一个电子填充在s能级,位于元素周期表s区,B错误;C. 中心
碳原子的价层电子对数为 ,故其空间结构为平面三角形,C正确;D. 是
离子化合物,电子式为 ,D错误;故答案选C。
3.(2022·山东·高考真题) 、 属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存
在 键、 键。下列说法错误的是A. 的熔点高于 B.晶体中所有化学键均为极性键
C.晶体中所有原子均采取 杂化 D.晶体中所有原子的配位数均相同
【答案】A
【解析】Al和Ga均为第ⅢA元素,N属于第ⅤA元素,AlN、GaN的成键结构与金刚石相似,则其为共
价晶体,且其与金刚石互为等电子体,等电子体之间的结构和性质相似。AlN、GaN晶体中,N原子与其
相邻的原子形成3个普通共价键和1个配位键。A.因为AlN、GaN为结构相似的共价晶体,由于Al原子
的半径小于Ga,N—Al的键长小于N—Ga的,则N—Al的键能较大,键能越大则其对应的共价晶体的熔
点越高,故GaN的熔点低于AlN,A说错误;B.不同种元素的原子之间形成的共价键为极性键,故两种
晶体中所有化学键均为极性键,B说法正确;C.金刚石中每个C原子形成4个共价键(即C原子的价层
电子对数为4),C原子无孤电子对,故C原子均采取sp3杂化;由于AlN、GaN与金刚石互为等电子体,
则其晶体中所有原子均采取sp3杂化,C说法正确;D.金刚石中每个C原子与其周围4个C原子形成共价
键,即C原子的配位数是4,由于AlN、GaN与金刚石互为等电子体,则其晶体中所有原子的配位数也均
为4,D说法正确。
综上所述,本题选A。
4.(2021·江苏·高考真题)N 是合成氨工业的重要原料,NH 不仅可制造化肥,还能通过催化氧化生产
2 3
HNO;HNO 能溶解Cu、Ag等金属,也能与许多有机化合物发生反应;在高温或放电条件下,N 与O 反
3 3 2 2
应生成NO,NO进一步氧化生成NO 。2NO(g)+O (g)=2NO (g) ΔH=-116.4kJ·mol-1。大气中过量的NO
2 2 2 x
和水体中过量的NH 、NO 均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为
N,也可将水体中的NO -转化为N。下列有关NH 、NH 、NO 的说法正确的是
2 3 2 3
A.NH 能形成分子间氢键
3
B.NO 的空间构型为三角锥形
C.NH 与NH 中的键角相等
3
D.NH 与Ag+形成的[Ag(NH)]+中有6个配位键
3 3 2
【答案】A
【解析】A.NH 能形成分子间氢键,氨分子是一个极性分子,氮原子带有部分负电荷,氢原子带有部分正
3
电荷,当氨分子互相靠近时,由于取向力的作用,带有部分正电荷的氢原子与另外一个氨分子中的带有部分负电荷的氮原子发生异性电荷的吸引进一步靠拢,A正确;B.硝酸根离子的空间构型是个标准的正三
角形,N在中间,O位于三角形顶点,N和O都是sp2杂化,B错误;C.NH 和NH 都是sp3杂化,但
3
NH 中存在一个孤电子对,是三角锥结构,而NH 为标准的正四面体,所以键角是不一样的,NH 中每两
3 3
个N—H键之间夹角为107°18',正四面体为109°28',C错误;D.N-H为σ键,配位键也为σ键,则
[Ag(NH)]+中含有8个σ键,2个配位键,D错误;答案选A。
3 2
5.(2022·海南·高考真题)已知 , 的酸性比
强。下列有关说法正确的是
A.HCl的电子式为 B.Cl-Cl键的键长比I-I键短
C. 分子中只有σ键 D. 的酸性比 强
【答案】BD
【解析】A.HCl为共价化合物,H原子和Cl原子间形成共用电子对,其电子式为 ,A错误;B.
原子半径Cl<I,故键长:Cl—Cl<I—I,B正确;C.CHCOOH分子中,羧基的碳氧双键中含有π键,C
3
错误;D.电负性Cl>I,-Cl能使-COOH上的H原子具有更大的活动性,因此ClCH COOH的酸性比
2
ICHCOOH强,D正确;答案选BD。
2
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2022·江苏·模拟预测)2022年北京冬奥会首次使用CO 跨临界直冷新型环保制冰技术。下列有关说法
2
不正确的是A.CO 是由极性键构成的非极性分子
2
B.干冰中CO 分子间只存在范德华力
2
C.冰中HO分子之间的主要作用力是氢键
2
D.此技术制冰的过程中发生的是化学变化
【答案】D
【解析】A.二氧化碳中C-O键为极性键,正负电荷重心重合,是非极性分子,A正确;B.干冰为分子晶
体,分子间只存在范德华力,B正确;C.冰中水分子间存在氢键和范德华力,但氢键作用力比范德华力
强,C正确;D.该过程中无新物质生成,为物理变化,D错误;故选D。
2.(2022·湖北·襄阳五中模拟预测)金属元素钴(Co)形成的多种配合物应用广泛。下列说法错误的是
A.[Co(NH )Cl]2+中Co钴元素的化合价为+3价
3 5
B.等物质的量的[Co(H O) ]2+和[CoCl ]2-中σ键数目之比为9:2
2 6 4
C.[Co(CN) (NH )]-中配体的配位原子都是N原子
4 3 2
D.向溶有1molCoCl ·6H O(配位数为6)的溶液中滴加足量的AgNO 溶液,形成2mol沉淀。则其配离子为
3 2 3
[Co(H O) Cl]2+
2 5
【答案】C
【解析】A.已知[Co(NH )Cl]2+中的配体为NH 和Cl-,则[Co(NH )Cl]2+中Co钴元素的化合价为+3价,A
3 5 3 3 5
正确;B.已知1个[Co(H O) ]2+和[CoCl ]2-中的σ键分别为2×6+6=18,4,故等物质的量的[Co(H O) ]2+和
2 6 4 2 6
[CoCl ]2-中σ键数目之比为18:4=9:2,B正确;C.[Co(CN) (NH )]-中配体为NH 和CN-,NH 分子中的配
4 4 3 2 3 3
位原子是N,由于C的电负性小于N,对孤对电子的束缚力要更弱,由于孤对电子的能量更高,更容易形
成配位键,即配体CN-的配位原子C原子,C错误;D.向溶有1molCoCl ·6H O(配位数为6)的溶液中滴加
3 2
足量的AgNO 溶液,形成2mol沉淀,即外界有2个Cl,该配位化合物为:[Co(H O) Cl]Cl ·H O,则其配
3 2 5 2 2
离子为[Co(H O) Cl]2+,D正确;故答案为:C。
2 5
3.(2022·江苏常州·模拟预测)CO 催化加氢制甲醇有利于减少CO 的排放,实现“碳达峰”,其反应可
2 2
表示为CO (g)+3H (g) =CH OH (g)+HO (g) ΔH= -49 kJ·mol-1。今年2月我国科研团队在CO 电化学还原
2 2 3 2 2
反应机理的研究上取得新突破,明确两电子转移CO 电化学还原反应的控速步骤为CO 吸附过程。反应
2 2
CO+3H =CH OH +HO可实现二氧化碳的资源化。下列说法正确的是
2 2 3 2
A.CO 的电子式为: B.CHOH是非极性分子
2 3
C.CHOH和HO能形成分子间氢键 D.HO的球棍模型为
3 2 2
【答案】C【解析】A.CO 中C和O共用2个电子对,其电子式为 ,故A错误;B.甲醇属于极性分子,
2
故B错误;C.CHOH中的羟基与水分子间形成氢键,故C正确;D.HO的空间构型为V形,故D错误;
3 2
答案为C。
4.(2022·江苏·阜宁县东沟中学模拟预测)用氨水吸收硫酸工厂尾气中的 发生反应:
。下列说法正确的是
A. 的电子式 B. 是非极性分子
C. 的结构式为 D. 的空间构型为直线形
【答案】C
【解析】A.NH 的电子式为 ,A项错误;B.SO 中中心原子S上的孤电子对数为
3 2
=1,σ键电子对数为2,价层电子对数为3,VSEPR模型为平面三角形,略去孤电子对,SO 的空间构型为
2
V形,SO 中正、负电的中心不重合,SO 是极性分子,B项错误;C. 的结构式为 ,
2 2
C项正确;D.HO中中心原子O上的孤电子对数为 =2,σ键电子对数为2,价层电子对数为
2
4,VSEPR模型为四面体形,略去孤电子对,HO的空间构型为V形,D项错误;答案选C。
2
5.(2021·湖南株洲·一模)中科院国家纳米科学中心科研员在国际上首次“拍”到氢键的“照片”,实现
了氢键的实空间成像,为“氢键的本质”这一化学界争论了多年的问题提供了直观证据。下列有关氢键的
说法不正确的是
A.由于氢键的存在,冰能浮在水面上
B.由于氢键的存在,乙醇比二甲醚更易溶于水
C.由于氢键的存在,沸点:
D.氢键的存在影响了蛋白质分子独特的结构【答案】C
【解析】A.冰中水分子排列有序,含有氢键数目增多,使体积膨胀,密度减小,因此冰能浮在水面上,A
正确;B.乙醇与水分子间存在氢键,增大乙醇在水中的溶解度,所以乙醇比二甲醚更易溶于水,B正确;
C.卤素的氢化物中只有 分子间含有氢键,卤素的氢化物的沸点: ,C错误;
D.氢键具有方向性和饱和性,所以氢键的存在,影响了蛋白质分子独特的结构,D正确;故答案选C。
6.(2022·湖北·华中师大一附中模拟预测)关于CHCH、CH-O-CH 和CHCHO的结构与性质,下列说
3 3 3 3 3
法正确的是
A.三种有机物中碳原子的杂化方式完全相同
B.CH- O- CH 和CHCH 均为非极性分子
3 3 3 3
C.CHCHO分子中所有原子共平面
3
D.三种分子形成的晶体均为分子晶体
【答案】D
【解析】A.CHCH 中的C均为sp3杂化,CH-O-CH 中的C均为sp3杂化,CHCHO中醛基上的C为sp2
3 3 3 3 3
杂化,A错误;B.CH- O- CH 中的氧是sp3杂化的,还有两对孤对电子,所以C-O-C的键角大约是107度
3 3
左右,所以并不是直线型的分子,故为极性分子,B错误;C.CHCHO分子中含有饱和碳原子,形成四
3
面体结构,所有原子不可能共平面,C错误;D.三种分子形成的晶体均为分子晶体,D正确;答案选D。
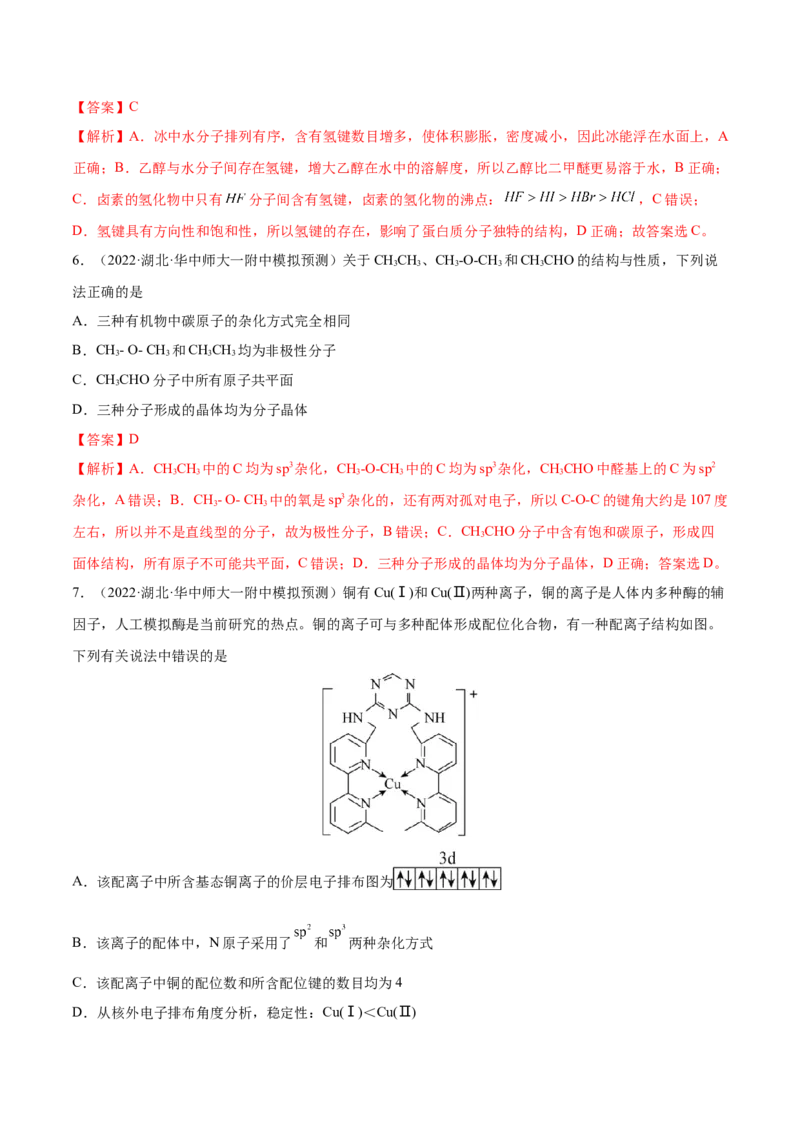
7.(2022·湖北·华中师大一附中模拟预测)铜有Cu(Ⅰ)和Cu(Ⅱ)两种离子,铜的离子是人体内多种酶的辅
因子,人工模拟酶是当前研究的热点。铜的离子可与多种配体形成配位化合物,有一种配离子结构如图。
下列有关说法中错误的是
A.该配离子中所含基态铜离子的价层电子排布图为
B.该离子的配体中,N原子采用了 和 两种杂化方式
C.该配离子中铜的配位数和所含配位键的数目均为4
D.从核外电子排布角度分析,稳定性:Cu(Ⅰ)<Cu(Ⅱ)【答案】D
【解析】A.该配离子中铜离子为 价,所以价层电子排布图为 ,A正确;B.该离子的
配体中,N原子采用了 和 两种杂化方式,B正确;C.由图可知铜离子配位数和每个离子所含配位键
数均为4,C正确;D.由于Cu(Ⅰ)的3d轨道全充满,所以更稳定,故D错误。故选D。
8.(2022·上海崇明·二模)我国科学家发现一种名为“Methanoliparia”的微生物,能以石油为食物产生甲
烷和二氧化碳。下列不属于甲烷和二氧化碳共性的是
A.非电解质 B.非极性分子 C.温室气体 D.平面型分子
【答案】D
【解析】A.甲烷溶于水不能导电,故属于非电解质,二氧化碳的水溶液能导电,是由于碳酸电离出的氢
离子和碳酸氢根离子,使水溶液导电,并非二氧化碳自身电离,故二氧化碳属于非电解质;即甲烷和二氧
化碳都是非电解质,故A不符合题意;B.甲烷为正四面体形,二氧化碳为直线形,均为对称结构,均属
于非极性分子,故B不符合题意;C.甲烷和二氧化碳均属于温室气体,故C不符合题意;D.甲烷的空
间构型为正四面体形,不是平面型分子,二氧化碳的空间构型为直线形,是平面型分子,故D符合题意;
故选D。
9.(2022·广东·梅州市梅江区梅州中学模拟预测)由徐光宪院士发起院士学子同创的《分子共和国》科普
读物生动形象地戏说了 、 、 、 、 、 等众多“分子共和国”中的明星。下
列说法正确的是
A.键角:
B.酸性:
C. 分子中只存在 键,不存在π键.
D. 、 分子的空间结构均为直线形,且均为非极性分子
【答案】A
【解析】A. 中心原子sp3杂化,有一对孤电子对,由于孤电子对的斥力,为三角锥形,键角为107.3°,而 中心原子sp2杂化,无孤电子对,为平面三角形,键角为120°,故键角: ,A项正
确;B.氟原子是吸电子基团,会使羧基中氢氧键的极性增强,易于电离出氢离子,酸性增强,则酸性:
CHCOOH<CFCOOH,B项错误;C.SOCl (结构式: )中存在硫氧双键,则分子中存在σ键,
3 3 2
也存在π键,C项错误;D.HS分子中心S原子价层电子对数为 ,有2个孤电子对,HS分
2 2
子是V形,O 分子中心O原子价层电子对数为 ,有1个孤电子对,分子呈V形,二者均为
3
极性分子,D项错误;答案选A。
10.(2022·江苏苏州·模拟预测)SO 、NO 是重要化工原料,可用于硫酸、硝酸的生产。工业制硫酸时,
2 x
接触室中主要反应为:2SO (g)+O(g) =2SO (g) ΔH=-196.6 kJ·mol-1,SO 、NO 也是大气主要污染物,NO
2 2 3 2 x x
可与NH 混合,通过选择性催化剂高温脱除,SO 可通过碱液吸收去除。下列关于SO 、SO 、NH 、NH
3 2 2 3 3
说法中正确的是
A.SO 水溶液能导电,SO 是电解质 B.NH 中含有配位键
2 2
C.SO 中硫原子轨道杂化类型为sp3 D.NH 为非极性分子
3 3
【答案】B
【解析】A. SO 水溶液能导电,但二氧化硫自身不电离产生离子,故SO 是非电解质,A错误;B.氨分
2 2
子的N上有1对孤电子对、氢离子有空轨道,则 NH 中有3根普通的N-H、有1个配位键,B正确;C.
SO 中中心原子的孤电子对数= 、价层电子对数=3+0=3,故为sp2杂化、空间构型为平面正三角
3
形,C错误;D. NH 由极性键构成、呈三角锥形,则正负电荷中心不重叠,属于极性分子,D错误;答
3
案选B。
11.(2021·山东·模拟预测)下列说法中正确的是
A.P 和CH 都是正四面体形分子,且键角都为109°28’
4 4
B.乙烯分子中,碳原子的sp2杂化轨道形成σ键,未杂化的2p轨道形成π键C.键长H-F < H-Cl < H-Br < H-I,因此稳定性HF < HCl < HBr < HI
D.PH 分子中孤电子对与成键电子对的排斥作用比成键电子对之间的排斥作用弱
3
【答案】B
【解析】A.P 和CH 都是正四面体形分子,甲烷的键角为109°28’,但P 的键角为60°,故A错误;B.
4 4 4
乙烯分子中含碳碳双键,碳原子的sp2杂化轨道形成σ键,未杂化的2p轨道形成π键,B正确;C.键长
H-F < H-Cl < H-Br < H-I,键长越长,键能越小,故稳定性HF>HCl>HBr>HI,C错误;D.PH 的键角为
3
96.3°,故PH 分子中孤电子对与成键电子对的排斥作用比成键电子对之间的排斥作用强,D错误;答案选
3
B。
12.(2022·北京·北大附中三模)在一定条件下,[Zn(CN) ]2-与甲醛发生如下反应:[Zn(CN) ]2-
4 4
+4HCHO+4H O=[Zn(OH) ]2-+4HOCH CN
2 4 2
已知:ⅰ. HCN为剧毒、易挥发的气体,其水溶液有极弱的酸性
ⅱ. Zn2++4CN- [Zn(CN) ]2- K;Zn2++4OH- [Zn(OH) ]2- K
4 1 4 2
下列说法不正确的是
A.反应前后Zn2+均提供4个空轨道容纳4对孤电子对
B.HOCH CN的氰基由CN-与甲醛发生反应而来
2
C.依据上述[Zn(CN) ]2-与甲醛的反应可以证明:K