文档内容
训练(四十九) 化学实验方案的设计及评价
1.(2020·山东烟台二模)下列实验操作能达到实验目的的是( )
实验目的 实验操作
A 制备Fe(OH) 胶体 将NaOH浓溶液滴加到饱和FeCl 溶液中
3 3
B 由MgCl 溶液制备无水MgCl 将MgCl 溶液加热蒸干
2 2 2
C 除去Cu粉中混有的CuO 加入稀硝酸溶解,过滤、洗涤、干燥
比较水与乙醇中羟基氢的活泼
D 分别将少量钠投入盛有水和乙醇的烧杯中
性
D [NaOH浓溶液滴加到饱和FeCl 溶液中生成Fe(OH) 沉淀,而Fe(OH) 胶体的制备
3 3 3
是向沸水中滴入饱和氯化铁溶液,加热至溶液出现红褐色,A错误;氯化镁是强酸弱碱盐,
MgCl 水解产生的HCl易挥发,将MgCl 溶液加热蒸干生成Mg(OH) ,故由MgCl 溶液制备
2 2 2 2
无水MgCl 要在HCl气流中加热蒸干,B错误;铜与稀硝酸反应,应该用稀盐酸或稀硫酸除
2
去Cu粉中混有的CuO,C错误;分别将少量钠投入盛有水和乙醇的烧杯中,利用反应的现象:
反应剧烈的是水,反应平缓的是乙醇,可比较水和乙醇中羟基氢的活泼性,D正确。]
2.(2021·福建南安一中检测)下列有关实验的操作正确的是( )
实验 操作
A 配制稀硫酸 先将浓硫酸加入烧杯中,后倒入蒸馏水
B 排水法收集KMnO 分解产生的O 先熄灭酒精灯,后移出导管
4 2
C 浓盐酸与MnO 反应制备纯净Cl 气体产物先通过浓硫酸,后通过饱和食盐水
2 2
先从分液漏斗下口放出有机层,后从上口倒出水
D CCl 萃取碘水中的I
4 2 层
D [配制稀硫酸时应将浓硫酸沿烧杯内壁倒入水中,并用玻璃棒不断搅拌,否则由于浓
硫酸溶解时放出大量的热,容易引起酸液飞溅伤人,A错误;应先移出导管,后熄灭酒精灯,
否则会引起倒吸而使试管炸裂,B错误;操作时应先将气体产物通过饱和食盐水除去HCl,然
后通过浓硫酸除去水,否则在通过饱和食盐水时又引入水蒸气,C错误;萃取分液时下层液
体从下口放出,上层液体从上口倒出,D正确。]
3.(2019·全国卷Ⅲ)下列实验不能达到目的的是( )
选项 目的 实验
A. 制取较高浓度的次氯酸溶液 将Cl 通入碳酸钠溶液中
2
B. 加快氧气的生成速率 在过氧化氢溶液中加入少量MnO
2
C. 除去乙酸乙酯中的少量乙酸 加入饱和碳酸钠溶液洗涤、分液
D. 制备少量二氧化硫气体 向饱和亚硫酸钠溶液中滴加浓硫酸A [A错:将Cl 通入碳酸钠溶液中发生反应:Cl+2NaCO+HO===NaCl+NaClO+
2 2 2 3 2
2NaHCO ,不能制取较高浓度的次氯酸溶液。B对:在过氧化氢溶液中加入少量二氧化锰作
3
催化剂,可加快氧气的生成速率。C对:加入饱和碳酸钠溶液可以中和乙酸,降低乙酸乙酯在
水中的溶解度,便于析出。D对:向饱和亚硫酸钠溶液中滴加浓硫酸,应用强酸制弱酸的原理,
可以制备二氧化硫气体。]
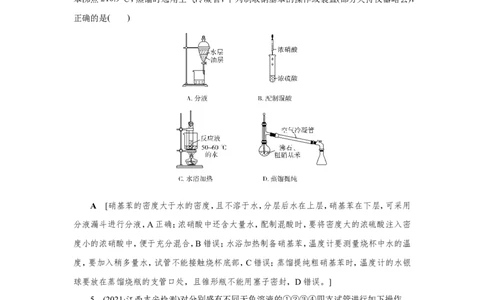
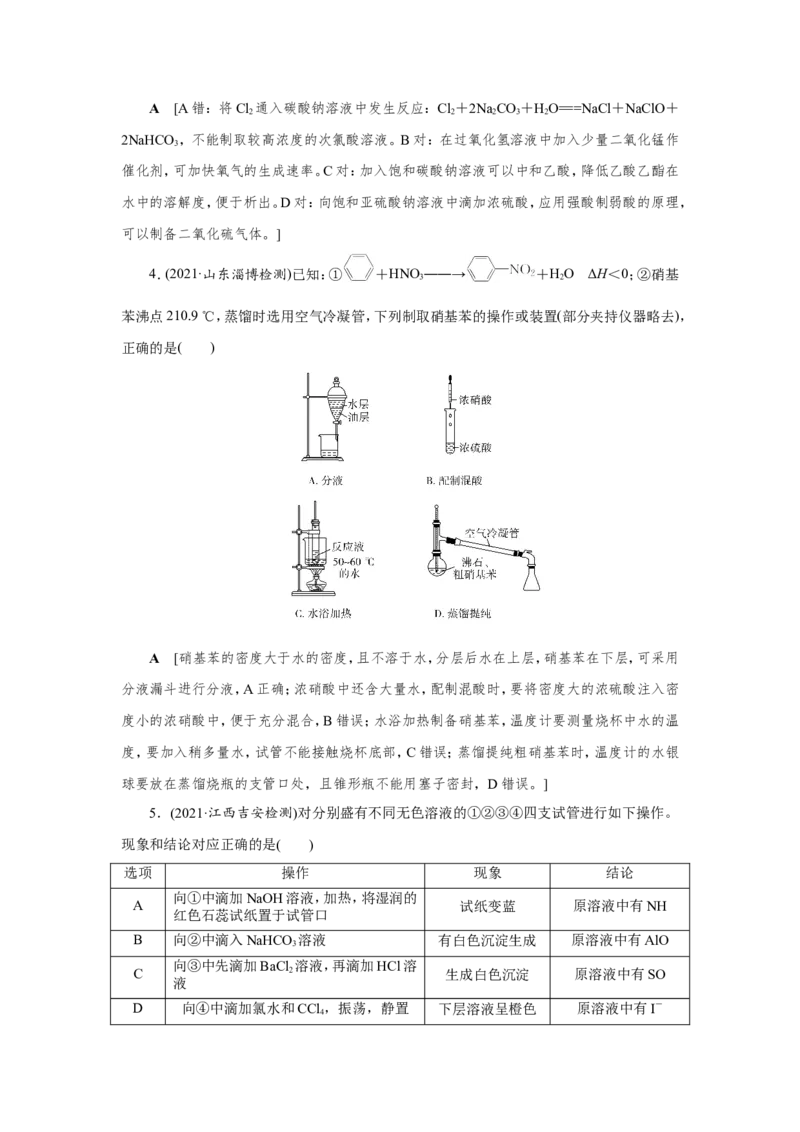
4.(2021·山东淄博检测)已知:① +HNO――→ +HO ΔH<0;②硝基
3 2
苯沸点210.9 ℃,蒸馏时选用空气冷凝管,下列制取硝基苯的操作或装置(部分夹持仪器略去),
正确的是( )
A [硝基苯的密度大于水的密度,且不溶于水,分层后水在上层,硝基苯在下层,可采用
分液漏斗进行分液,A正确;浓硝酸中还含大量水,配制混酸时,要将密度大的浓硫酸注入密
度小的浓硝酸中,便于充分混合,B错误;水浴加热制备硝基苯,温度计要测量烧杯中水的温
度,要加入稍多量水,试管不能接触烧杯底部,C错误;蒸馏提纯粗硝基苯时,温度计的水银
球要放在蒸馏烧瓶的支管口处,且锥形瓶不能用塞子密封,D错误。]
5.(2021·江西吉安检测)对分别盛有不同无色溶液的①②③④四支试管进行如下操作。
现象和结论对应正确的是( )
选项 操作 现象 结论
向①中滴加NaOH溶液,加热,将湿润的
A 试纸变蓝 原溶液中有NH
红色石蕊试纸置于试管口
B 向②中滴入NaHCO 溶液 有白色沉淀生成 原溶液中有AlO
3
向③中先滴加BaCl 溶液,再滴加HCl溶
C 2 生成白色沉淀 原溶液中有SO
液
D 向④中滴加氯水和CCl ,振荡,静置 下层溶液呈橙色 原溶液中有I-
4A [滴加NaOH溶液,加热,石蕊的红色石蕊试纸变蓝,说明反应产生NH ,则原溶液
3
中有NH,A正确;滴入NaHCO 溶液,有白色沉淀生成,该沉淀可能是Al(OH) 、BaCO 、
3 3 3
CaCO 等,不能确定原溶液中是否含AlO,B错误;先滴加BaCl 溶液,后滴加HCl溶液,生成
3 2
白色沉淀,该沉淀可能是BaSO 或AgCl,则原溶液中可能含有SO或Ag+,C错误;滴加氯水
4
和CCl ,振荡,静置,下层溶液呈橙色,则原溶液中有Br-,D错误。]
4
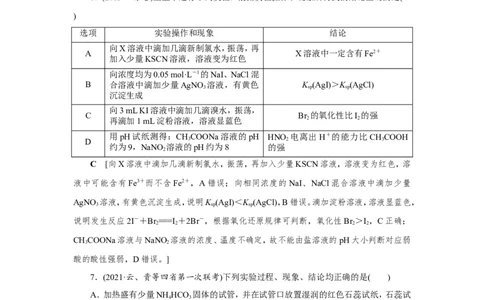
6.(2019·江苏卷)室温下进行下列实验,根据实验操作和现象所得到的结论正确的是(
)
选项 实验操作和现象 结论
向X溶液中滴加几滴新制氯水,振荡,再
A X溶液中一定含有Fe2+
加入少量KSCN溶液,溶液变为红色
向浓度均为0.05 mol·L-1的NaI、NaCl混
B 合溶液中滴加少量AgNO 溶液,有黄色 K (AgI)>K (AgCl)
3 sp sp
沉淀生成
向3 mL KI溶液中滴加几滴溴水,振荡,
C Br 的氧化性比I 的强
再滴加1 mL淀粉溶液,溶液显蓝色 2 2
用pH试纸测得:CHCOONa溶液的pH HNO 电离出H+的能力比CHCOOH
D 3 2 3
约为9,NaNO 溶液的pH约为8 的强
2
C [向X溶液中滴加几滴新制氯水,振荡,再加入少量KSCN溶液,溶液变为红色,溶
液中可能含有Fe3+而不含Fe2+,A错误;向相同浓度的NaI、NaCl混合溶液中滴加少量
AgNO 溶液,有黄色沉淀生成,说明K (AgI)<K (AgCl),B错误。滴加淀粉溶液,溶液显蓝色,
3 sp sp
说明发生反应2I-+Br ===I +2Br-,根据氧化还原规律可判断,氧化性Br >I ,C正确;
2 2 2 2
CHCOONa溶液与NaNO 溶液的浓度、温度不确定,故不能由盐溶液的pH大小判断对应弱
3 2
酸的酸性强弱,D错误。]
7.(2021·云、贵等四省第一次联考)下列实验过程、现象、结论均正确的是( )
A.加热盛有少量NH HCO 固体的试管,并在试管口放置湿润的红色石蕊试纸,石蕊试
4 3
纸变蓝,说明NH HCO 显碱性
4 3
B.用洁净的玻璃棒蘸取少量溶液进行焰色反应,火焰为黄色,说明该溶液中一定含有
Na+
C.向等物质的量浓度的FeCl 和AlCl 的混合溶液中滴加少量NaOH溶液,先出现红褐
3 3
色沉淀,说明相同温度下,K [Fe(OH) ]<K [Al(OH) ]
sp 3 sp 3
D.向蔗糖溶液中加入稀HSO ,加热几分钟,冷却后加入新制的Cu(OH) 悬浊液,加热
2 4 2
后没有砖红色沉淀生成,说明蔗糖还未水解C [碳酸氢铵受热分解:NH HCO =====NH ↑+CO↑+HO,氨气使湿润的红色石蕊
4 3 3 2 2
试纸变蓝,不能说明NH HCO 显碱性,A项错误;玻璃成分中有硅酸钠,灼烧也会使火焰变
4 3
黄色,故不能确定溶液中一定含有Na+,B项错误:Fe(OH) 和Al(OH) 的类型相同,溶度积小
3 3
的先沉淀,C项正确;向蔗糖溶液中加入稀HSO ,加热几分钟,冷却后直接加入新制的
2 4
Cu(OH) 悬浊液,加热后没有砖红色沉淀生成,是因为HSO 与Cu(OH) 发生反应,无法说明
2 2 4 2
蔗糖还未水解,D项错误。]
8.(2021·山东日照校际联考)下列由实验操作和现象所得出的结论正确的是( )
选项 实验操作 实验现象 结论
向NaSO 试样中滴入盐酸酸
A 2 3 产生白色沉淀 原NaSO 试样氧化变质
化的Ba(NO ) 溶液 2 3
3 2
将乙醇和浓硫酸混合加热至
B 170 ℃产生的气体通入酸性 紫红色褪去 使溶液褪色的是乙烯
KMnO 溶液
4
将稀硫酸与 NaHCO 混合产
C 3 溶液变浑浊 酸性:碳酸>硅酸
生的气体通入硅酸钠溶液
将炽热的木炭与浓硝酸混合
D 澄清石灰水不变浑浊 碳的氧化产物不是CO
所得气体通入澄清石灰水中 2
C [Na SO 试样中滴入盐酸酸化的Ba(NO ) 溶液,产生白色沉淀,该沉淀为BaSO,可
2 3 3 2 4
能是NO(H+)将SO氧化为SO,不能判断NaSO 是否变质,A错误;产生的气体通入酸性
2 3
KMnO 溶液,紫红色褪去,可能是乙烯或挥发出的乙醇将MnO还原为Mn2+引起,B错误;稀
4
硫酸与NaHCO 混合产生的气体是CO,通入硅酸钠溶液,溶液变浑浊,则析出HSiO 沉淀,
3 2 2 3
则酸性:碳酸>硅酸,C正确;将炽热的木炭与浓硝酸混合所得气体是NO 和CO 混合气体,
2 2
通入澄清石灰水中,NO 与HO反应生成HNO,由于HNO 的酸性强于HCO,则溶液不变
2 2 3 3 2 3
浑浊,D错误。]
9.(2021·山西运城调研)利用下列装置进行实验能达到实验目的是( )
A.利用甲装置制备少量O
2
B.利用乙装置制备无水氯化铁
C.利用丙装置提纯粗碘
D.利用丁装置在铁上镀铜
C [Na O 易溶于水,不能放在隔板上,无法控制反应速率,A错误;加热,促进了氯化
2 2铁的水解,得不到无水氯化铁,B错误;碘受热易升华,利用升华-凝华的方法可以提纯粗碘,
C正确;在铁上镀铜,铁作阴极,与电源的负极相连,铜作阳极,与电源的正极相连,D错误。]
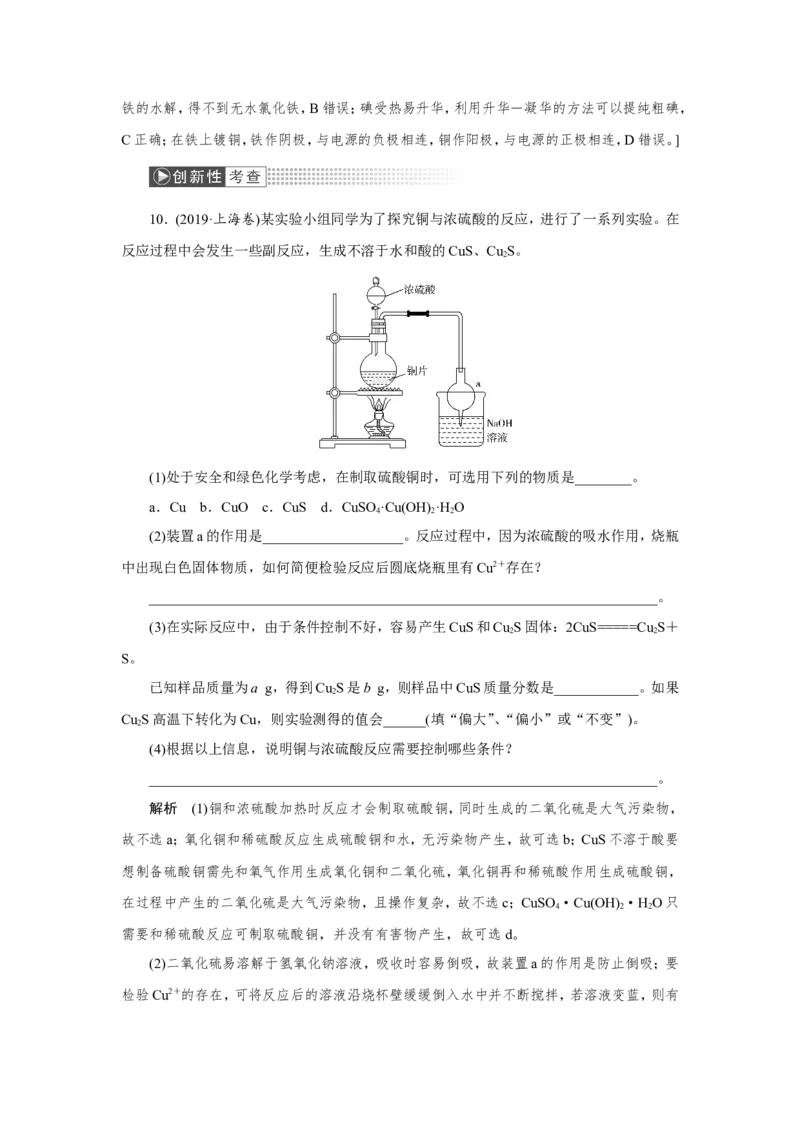
10.(2019·上海卷)某实验小组同学为了探究铜与浓硫酸的反应,进行了一系列实验。在
反应过程中会发生一些副反应,生成不溶于水和酸的CuS、Cu S。
2
(1)处于安全和绿色化学考虑,在制取硫酸铜时,可选用下列的物质是________。
a.Cu b.CuO c.CuS d.CuSO ·Cu(OH) ·H O
4 2 2
(2)装置a的作用是____________________。反应过程中,因为浓硫酸的吸水作用,烧瓶
中出现白色固体物质,如何简便检验反应后圆底烧瓶里有Cu2+存在?
________________________________________________________________________。
(3)在实际反应中,由于条件控制不好,容易产生CuS和Cu S固体:2CuS=====Cu S+
2 2
S。
已知样品质量为a g,得到Cu S是b g,则样品中CuS质量分数是____________。如果
2
Cu S高温下转化为Cu,则实验测得的值会______(填“偏大”、“偏小”或“不变”)。
2
(4)根据以上信息,说明铜与浓硫酸反应需要控制哪些条件?
________________________________________________________________________。
解析 (1)铜和浓硫酸加热时反应才会制取硫酸铜,同时生成的二氧化硫是大气污染物,
故不选a;氧化铜和稀硫酸反应生成硫酸铜和水,无污染物产生,故可选b;CuS不溶于酸要
想制备硫酸铜需先和氧气作用生成氧化铜和二氧化硫,氧化铜再和稀硫酸作用生成硫酸铜,
在过程中产生的二氧化硫是大气污染物,且操作复杂,故不选c;CuSO ·Cu(OH) ·HO只
4 2 2
需要和稀硫酸反应可制取硫酸铜,并没有有害物产生,故可选d。
(2)二氧化硫易溶解于氢氧化钠溶液,吸收时容易倒吸,故装置a的作用是防止倒吸;要
检验Cu2+的存在,可将反应后的溶液沿烧杯壁缓缓倒入水中并不断搅拌,若溶液变蓝,则有Cu2+存在。
(3)设样品中CuS为x g,Cu S为y g,根据质量守恒有x+y=a,根据铜原子守恒有(x/96
2
+2y/160)/2=b/160。两个方程联立,可解得x=6a-6b。所以样品中CuS的质量分数为(6a-
6b)/a,若Cu S在高温下会转化为Cu,则测得加热后固体的质量b偏小,故CuS的质量分数
2
偏大。
(4)根据以上分析可知,铜与浓硫酸反应需要控制温度不能过高,加热时间不宜太长。
答案 (1)bd (2)防倒吸 将反应后的溶液沿烧杯壁缓缓倒入水中,若溶液变蓝,则有
Cu2+存在
(3) (6a-6b)/a 偏大 (4)温度不宜过高,时间不宜过长
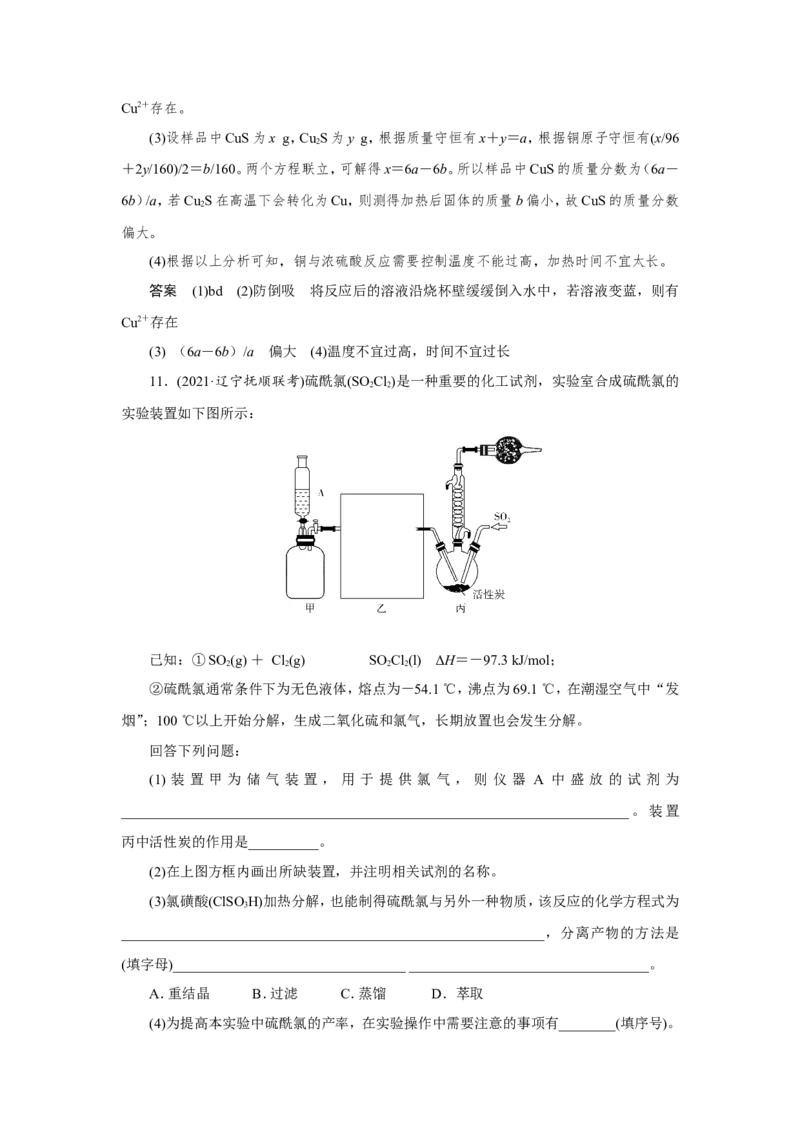
11.(2021·辽宁抚顺联考)硫酰氯(SO Cl)是一种重要的化工试剂,实验室合成硫酰氯的
2 2
实验装置如下图所示:
已知:①SO (g) + Cl(g) SO Cl(l) ΔH=-97.3 kJ/mol;
2 2 2 2
②硫酰氯通常条件下为无色液体,熔点为-54.1 ℃,沸点为69.1 ℃,在潮湿空气中“发
烟”;100 ℃以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解。
回答下列问题:
(1) 装 置 甲 为 储 气 装 置 , 用 于 提 供 氯 气 , 则 仪 器 A 中 盛 放 的 试 剂 为
________________________________________________________________________。装置
丙中活性炭的作用是__________。
(2)在上图方框内画出所缺装置,并注明相关试剂的名称。
(3)氯磺酸(ClSOH)加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为
3
____________________________________________________________,分离产物的方法是
(填字母)_________________________________ __________________________________。
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有________(填序号)。①先通冷凝水,再通气 ②控制气流速率,宜慢不宜快
③若三颈烧瓶发烫,可适当降温 ④加热三颈烧瓶
(5)在无活性炭存在的条件下SO 与Cl 也可发生反应,现将SO 、Cl 按照一定比例通入
2 2 2 2
水中,请设计一个简单实验方案验证二者是否恰好完全反应:
________________________________________________________________________
________________________________________________________________________
(简要描述实验步骤、现象和结论)。
仪器自选,供选择试剂:滴加酚酞的氢氧化钠溶液、碘化钾溶液、淀粉溶液、品红溶液。
解析 (1)根据题意,装置甲为储气装置,用于提供氯气,仪器A用于将氯气由甲装置排
入乙装置,所以氯气在仪器A中盛放的试剂中溶解度要小,以减少损失,则仪器A中盛放的
试剂为饱和食盐水;根据化学反应SO (g) + Cl(g) SO Cl(l),从实验装置丙中可以
2 2 2 2
看出,活性炭没参加反应,只能是作催化剂。
(2)因为硫酰氯在潮湿空气中“发烟”,所以制备硫酰氯的氯气必须是干燥的,则乙装置
为干燥装置,应用浓硫酸干燥氯气。
(3)根据题意,ClSOH→SO Cl,ClSOH的系数为2,根据反应前后原子个数守恒,差2个
3 2 2 3
H、1个S、4个O,即HSO ,所以反应的化学方程式为2ClSOH=====SO Cl+HSO ,SO Cl
2 4 3 2 2 2 4 2 2
为液体,沸点比较低,HSO 为液体,沸点较高,它们不分层,可以利用沸点不同进行蒸馏分
2 4
离,答案选C。
(4)Cl 具有氧化性,SO 以还原性为主,SO +Cl+2HO===H SO +2HCl,提高产率可以
2 2 2 2 2 2 4
采取措施:控制气流速率,宜慢不宜快;若三颈烧瓶发烫,可适当降温;先通冷凝水,冷凝回流
副产物和产品,再进行实验,答案选①②③。
(5)SO 和Cl 恰好反应生成硫酸和盐酸,若SO 或Cl 剩余,SO 和氯气均能使品红溶液
2 2 2 2 2
褪色,所以取少量反应后的溶液于试管中,滴加品红溶液振荡,若溶液褪色,则二者未恰好完
全反应;若不褪色,则二者恰好完全反应。
答案 (1)饱和食盐水 催化剂 (2)(浓硫酸)
(3)2ClSOH=====SO Cl + HSO C (4)①②③
3 2 2 2 4
(5)取少量反应后的溶液于试管中,滴加品红溶液振荡,若溶液褪色,则二者未恰好完全
反应;若不褪色,则二者恰好完全反应
12.(2021·安徽蚌埠第一次质检)亚硝酰氯(ClNO)是有机物合成中的重要试剂,可由NO
与Cl 在常温常压下反应得到。ClNO部分性质如下:黄色气体,熔点:-59.6 ℃,沸点:-6.4
2
℃,遇水易水解。已知:HNO 既有氧化性又有还原性;AgNO 微溶于水,能溶于硝酸:AgNO
2 2 2+HNO===AgNO +HNO。
3 3 2
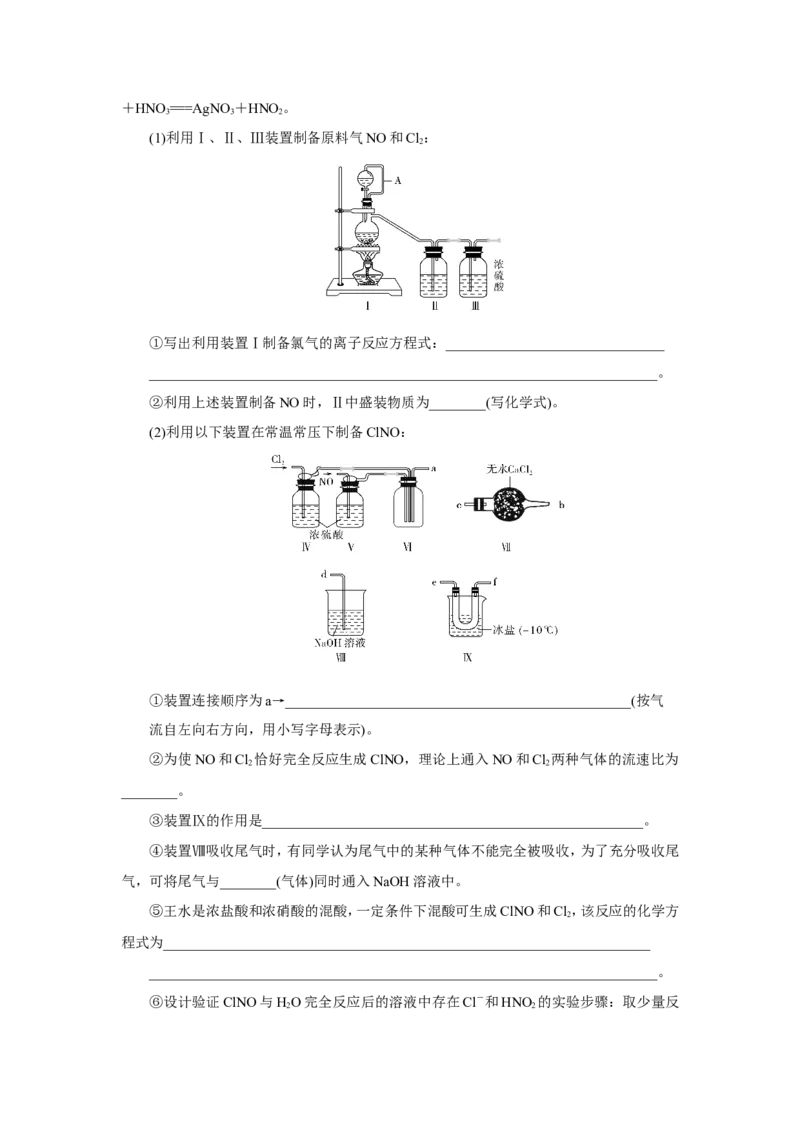
(1)利用Ⅰ、Ⅱ、Ⅲ装置制备原料气NO和Cl:
2
①写出利用装置Ⅰ制备氯气的离子反应方程式:_______________________________
________________________________________________________________________。
②利用上述装置制备NO时,Ⅱ中盛装物质为________(写化学式)。
(2)利用以下装置在常温常压下制备ClNO:
①装置连接顺序为a→_________________________________________________(按气
流自左向右方向,用小写字母表示)。
②为使NO和Cl 恰好完全反应生成ClNO,理论上通入NO和Cl 两种气体的流速比为
2 2
________。
③装置Ⅸ的作用是______________________________________________________。
④装置Ⅷ吸收尾气时,有同学认为尾气中的某种气体不能完全被吸收,为了充分吸收尾
气,可将尾气与________(气体)同时通入NaOH溶液中。
⑤王水是浓盐酸和浓硝酸的混酸,一定条件下混酸可生成ClNO和Cl,该反应的化学方
2
程式为_____________________________________________________________________
________________________________________________________________________。
⑥设计验证ClNO与HO完全反应后的溶液中存在Cl-和HNO 的实验步骤:取少量反
2 2应后的溶液于试管中,_______________________________________________________
________________________________________________________________________
________________________________________________________________________。
(限选试剂如下:AgNO 溶液,稀硝酸,KMnO 溶液)
3 4
解析 (1)①二氧化锰和浓盐酸在加热条件下反应生成氯化锰、氯气和水,其反应的离子
方程式为MnO +4H++2Cl-=====Mn2++Cl↑+2HO。
2 2 2
②用I制取NO,则反应物应该是铜和稀硝酸,因为硝酸具有挥发性,所以得到的NO中
含有硝酸蒸汽,Ⅱ中盛放物质应该能够吸收硝酸,所以Ⅱ中可以盛放HO。
2
(2)①将氯气和NO通过装置Ⅳ、V除可进一步干燥NO、Cl 外,还可以根据气泡逸出情
2
况控制气体流速,在装置Ⅵ中发生反应,在装置Ⅸ中用冰盐冷凝收集NOCl,氯气、NO以及
NOCl均不能排放到空气中,用装置Ⅷ中的氢氧化钠溶液吸收,由于NOCl遇水易水解,故在
收集装置和尾气处理装置之间需加一个干燥装置Ⅶ,所以装置连接顺序为
a→e→f→c→b→d(或a→f→e→c→b→d)。
②根据Cl 和NO反应的化学方程式Cl+2NO===2NOCl,可知为使NO和Cl 恰好完全
2 2 2
反应二者的流速之比应等于其计量数之比即可,则理论上通入NO和Cl 两种气体的流速比
2
为2∶1;
③通过①的分析可知,装置Ⅸ的作用是冷凝亚硝酰氯,便于收集。
④NO不易溶于水也不能被NaOH溶液反应,所以NO不能被完全吸收,NO应和适量的
O 同时通入NaOH溶液中。
2
⑤根据反应物、生成物和反应条件可知其反应化学方程式为 HNO(浓)+
3
3HCl(浓)=====ClNO↑+Cl↑+2HO。
2 2
⑥氯离子能和硝酸银溶液反应生成AgCl白色沉淀,所以可以用硝酸酸化的硝酸银溶液
检验氯离子,亚硝酸具有还原性,能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,
所以其检验方法为:取少量反应后的溶液于试管中,依次滴加足量的AgNO 溶液和稀硝酸,
3
充分振荡、静置,有白色沉淀生成;另取静置后上层清液少许于另一支试管中,滴加KMnO
4
溶液,溶液紫色褪去。
答案 (1)①MnO +4H++2Cl-=====Mn2++Cl↑+2HO ②HO
2 2 2 2
(2)①e→f→c→b→d(或f→e→c→b→d) ②2∶1 ③冷凝亚硝酰氯,便于收集
④ O ⑤ HNO(浓)+3HCl(浓)=====ClNO↑+Cl↑+2HO ⑥依次滴加足量的
2 3 2 2
AgNO 溶液和稀硝酸,充分振荡、静置,有白色沉淀生成;另取静置后上层清液少许于另一支
3
试管中,滴加KMnO 溶液,溶液紫色褪去
4