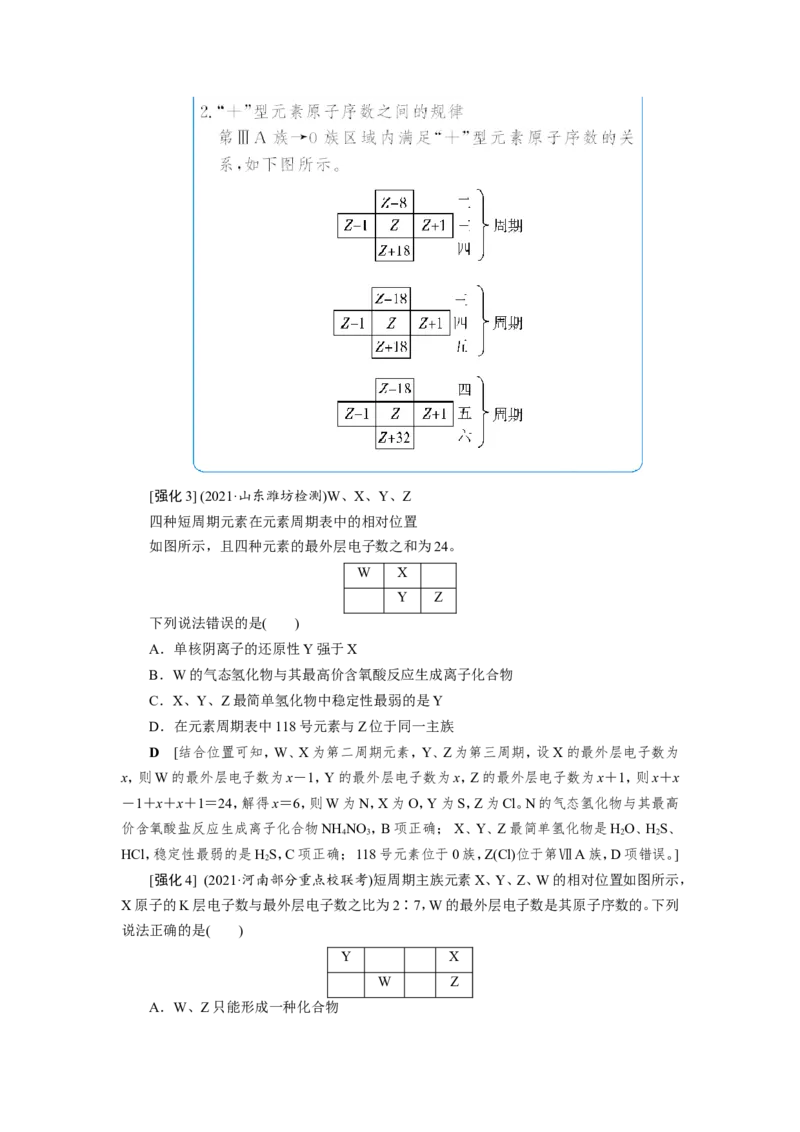
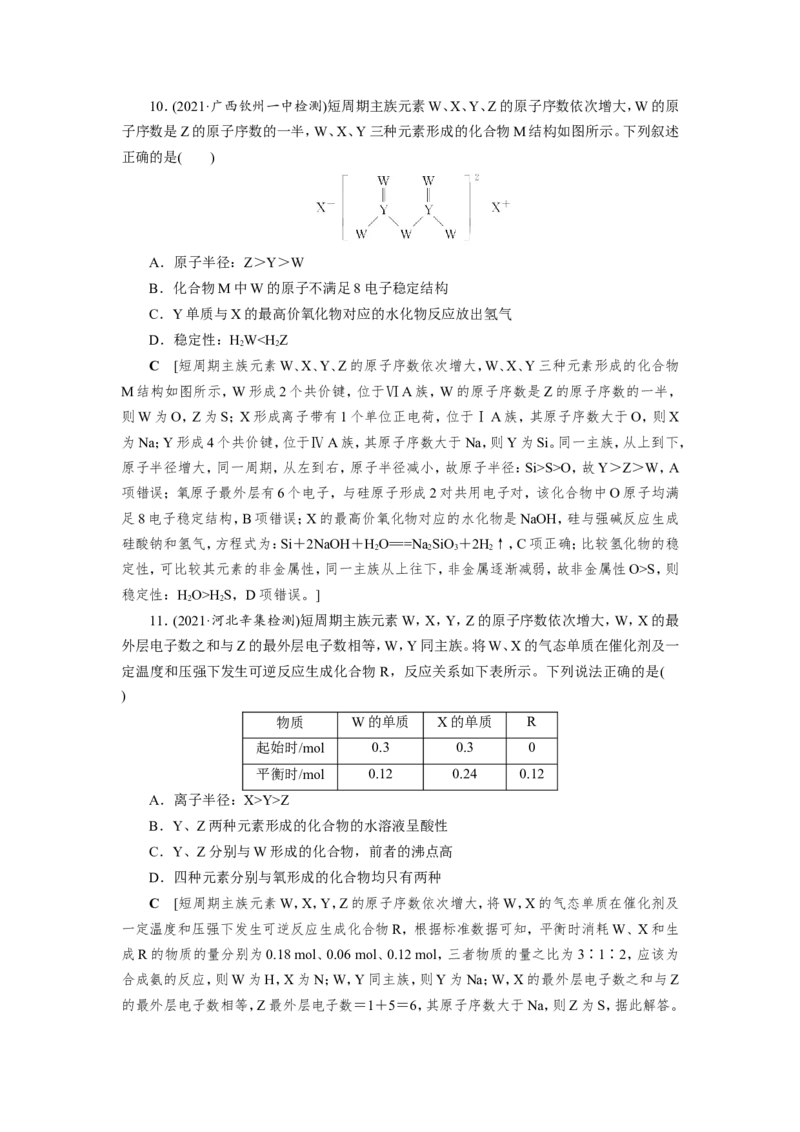
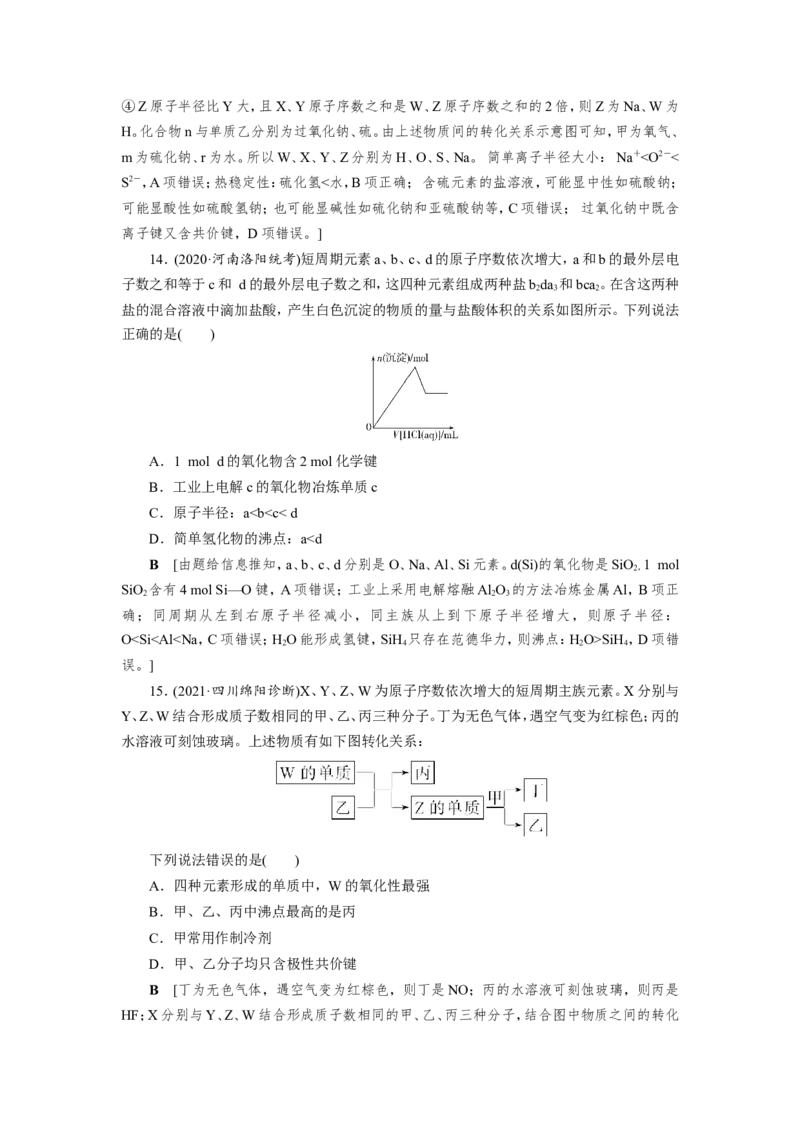
文档内容
第3课时 关键能力——元素周期表中“位-构-性”
关系及应用
元素周期律和元素周期表是高考命题的热点和重点,主要以选择题的形式考查元素在
周期表中的位置、原子结构、元素性质的关系及相互推断,同时也渗透着对元素及其化合物
知识的考查,该类题目命题形式和命题角度灵活多变,体现《中国高考评价体系》对知识获取
能力、思维认知能力的要求,考生要能够阅读和理解各种主要文本、基本符号;能够客观全面
地获取相关信息,并从情境中提取有效信息;能够准确概括和描述学科所涉及基本现象的特
征及其相互关系,并从中发现问题;能够灵活地、创造性地运用不同方法,发散地、逆向地解
决问题;能够通过敏锐的洞察能力,发现复杂、新颖情境中的关键事实特征和有价值的新问
题;能够将所学知识迁移到新情境,解决新问题,得出新结论。
考向1 文字描述型推断(演绎与推理能力)
文字叙述的角度是多方面的,大多要求考生根据元素及其化合物特殊组成、特殊性质及
应用,原子核外电子排布及原子半径的递变规律等进行演绎与推理,通过自己的逻辑思辨,
创造性地运用不同方法,确定未知元素,并结合元素周期律、化学键等知识进行分析、判断。
此类题目一般通过文字叙述提供某些数据或相关性质(如能腐蚀玻璃、黄绿色气体等),解题
时抓住这些关键特性,首先确定其为何种元素,然后以此为突破口,推知其他未知元素。
1.根据元素化合价的特征关系推断
(1)根据等式确定元素在周期表中的位置:最高正化合价数=最外层电子数=主族序数
(O、F除外)。
(2)如果已知负化合价(或简单阴离子的符号),则需用等式先求出最高正化合价:最高正
化合价=8-|负化合价|,再确定元素在周期表中的位置。
2.根据原子半径的递变规律推断
根据原子半径来推断元素的相对位置:同周期中左边元素的原子半径比右边元素的原
子半径大,同主族中下边元素的原子半径比上边元素的原子半径大。
3.根据元素的特征来推断
(1)地壳中含量最多的元素或氢化物呈液态的元素为O;地壳中含量第二的元素为Si;地
壳中含量最多的金属元素为Al。
(2)空气中含量最多的元素或气态氢化物的水溶液显碱性的元素为 N;气态氢化物与最
高价氧化物的水化物能反应生成盐的元素为N。
(3)单质硬度最大,熔沸点最高,形成化合物种类最多,正负化合价代数和为0且气态氢
化物中含氢质量分数最高的元素是C。
(4)最高价氧化物及其水化物既能与强酸反应,又能与强碱反应的元素在中学阶段为Al。
(5)两短周期金属元素的最高价氧化物对应水化物相互反应,这两种元素分别为Na和Al。
(2019·全国卷Ⅲ)X、Y、Z均为短周期主族元素,它们原子的最外层电子数之和为
10。X与Z同族,Y最外层电子数等于X次外层电子数,且Y原子半径大于Z。下列叙述正确
的是( )
A.熔点:X的氧化物比Y的氧化物高
B.热稳定性:X的氢化物大于Z的氢化物
C.X与Z可形成离子化合物ZX
D.Y的单质与Z的单质均能溶于浓硝酸
B [X、Y、Z均为短周期主族元素,X与Z同族,Y最外层电子数等于X次外层电子数,
Y的最外层电子数不可能是8,只能为2,且Y原子半径大于Z,所以Y为Mg,X、Y、Z原子
的最外层电子数之和为10,故X为C,Z为Si。A错:MgO的熔点高于CO、CO的熔点。B对:
2
元素的非金属性越强,则其气态氢化物的热稳定性越强,C的非金属性强于Si,故CH 的热
4
稳定性大于SiH。C错:X与Z形成的SiC是共价化合物。D错:Mg能溶于浓硝酸,但是Si单
4
质不能溶于浓硝酸。]
[强化1] (2018·全国卷Ⅰ)主族元素W、X、Y、Z的原子序数依次增加,且均不大于20。
W、X、Z最外层电子数之和为10;W与Y同族;W与Z形成的化合物可与浓硫酸反应,其生成物可腐蚀玻璃。下列说法正确的是( )
A.常温常压下X的单质为气态
B.Z的氢化物为离子化合物
C.Y和Z形成的化合物的水溶液呈碱性
D.W与Y具有相同的最高化合价
B [可腐蚀玻璃的物质是HF。以此为切入点,根据题意进行元素推断,可知W是F、X
是Na、Y是Cl、Z是Ca。B对:钙是活泼金属元素,氢是非金属元素,CaH 是由Ca2+和H-构
2
成的离子化合物。A错:常温常压下,钠的单质是固体。C错:CaCl 是强酸强碱盐,水溶液呈
2
中性。D错:氯有最高化合价+7,氟没有正价。]
[强化2] (2021·安徽安庆检测)五种短周期元素的某些性质如表所示,下列说法不正确的
是( )
元素 元素的相关信息
Q 最高价氧化物对应的水化物能与其气态氢化物反应生成盐
R 原子的M电子层上有3个电子
W 在短周期元素中,其原子半径最大
其最外层电子数是电子层数的2倍,且低价氧化物能与其气态氢化物反应生成X的
X
单质和HO
2
Y 元素最高正价与最低负价的代数和为6
A.Q的气态氢化物具有还原性,常温下,该氢化物水溶液的pH>7
B.W单质在氧气中燃烧后的产物中阴阳离子个数之比为1∶2
C.由R和Y所形成的化合物中存在离子键,属于离子化合物
D.R、W、X的最高价氧化物对应的水化物两两之间能发生反应
C [由题意知,Q为N;R为Al;W为Na;X为S;Y为Cl。氨气分子中N元素处于最低价,具
有还原性,其水溶液呈碱性,A项正确;钠在氧气中燃烧后的产物为过氧化钠,阴阳离子个数
之比为1∶2,B项正确;R和Y所形成的化合物为AlCl,属于共价化合物,含有共价键,C项
3
错误;硫酸为强酸,氢氧化钠为强碱,氢氧化铝为两性氢氧化物,三者两两之间能发生反应,D
项正确。]
考向2 结构片段型推断(分析与推测能力)
结构片段型元素周期表类题一般给出两种信息:一是给出局部的元素周期表,展示出几
种不同元素在元素周期表中的相对位置关系;二是给出某种元素的位置特征、原子结构特征
或由该元素形成的单质或化合物的特殊性质,要求考生运用严谨的理性思维和丰富的感性
思维,发现新线索、解决新问题、获得新结论。解答此类题目时,要先根据给出的某种元素的
特殊结构或性质,确定该元素在周期表中的位置,然后以此为“坐标原点”,根据其他元素与
该元素的相对位置关系,进而确定其他未知的元素,并结合元素周期律进行分析、判断。
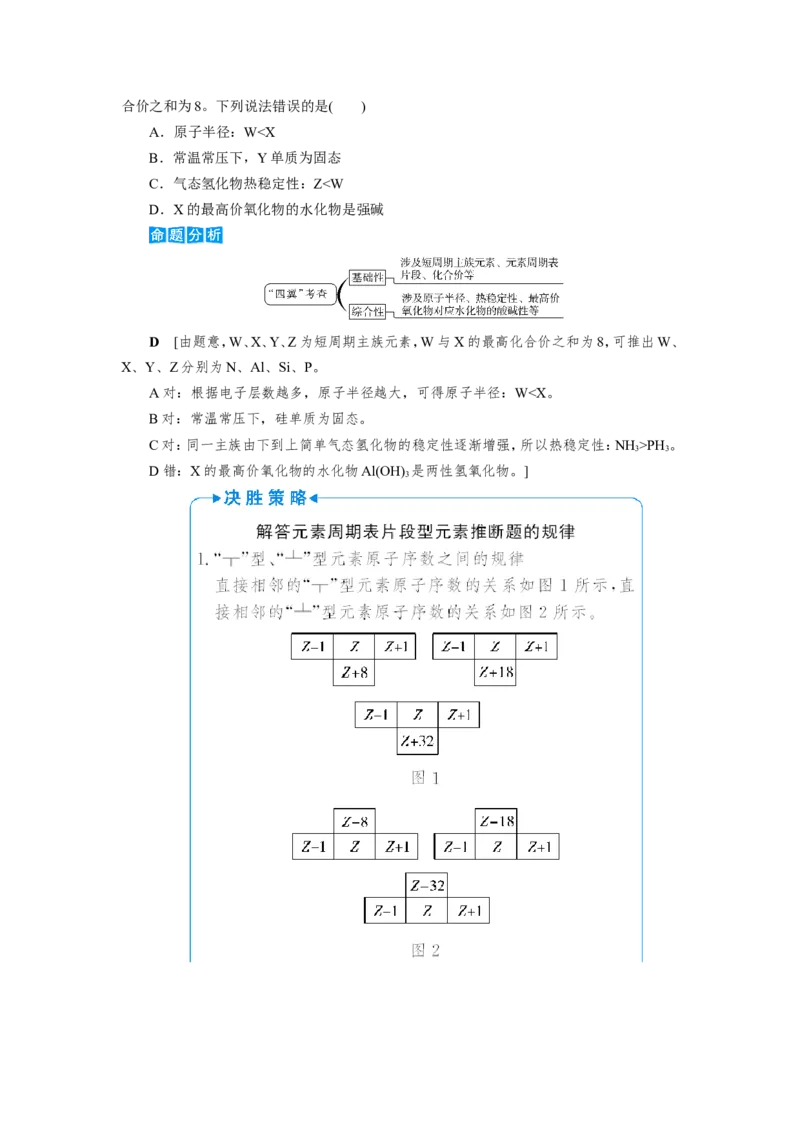
(2019·全国卷Ⅱ)今年是门捷列夫发现元素周期律150周年。下表
是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法错误的是( )
A.原子半径:WPH。
3 3
D错:X的最高价氧化物的水化物Al(OH) 是两性氢氧化物。]
3[强化3] (2021·山东潍坊检测)W、X、Y、Z
四种短周期元素在元素周期表中的相对位置
如图所示,且四种元素的最外层电子数之和为24。
W X
Y Z
下列说法错误的是( )
A.单核阴离子的还原性Y强于X
B.W的气态氢化物与其最高价含氧酸反应生成离子化合物
C.X、Y、Z最简单氢化物中稳定性最弱的是Y
D.在元素周期表中118号元素与Z位于同一主族
D [结合位置可知,W、X为第二周期元素,Y、Z为第三周期,设X的最外层电子数为
x,则W的最外层电子数为x-1,Y的最外层电子数为x,Z的最外层电子数为x+1,则x+x
-1+x+x+1=24,解得x=6,则W为N,X为O,Y为S,Z为Cl。N的气态氢化物与其最高
价含氧酸盐反应生成离子化合物NH NO ,B项正确; X、Y、Z最简单氢化物是HO、HS、
4 3 2 2
HCl,稳定性最弱的是HS,C项正确; 118号元素位于0族,Z(Cl)位于第ⅦA族,D项错误。]
2
[强化4] (2021·河南部分重点校联考)短周期主族元素X、Y、Z、W的相对位置如图所示,
X原子的K层电子数与最外层电子数之比为2∶7,W的最外层电子数是其原子序数的。下列
说法正确的是( )
Y X
W Z
A.W、Z只能形成一种化合物B.X的氢化物的水溶液常用塑料瓶保存
C.Y、Z形成的化合物不可能含有非极性共价键
D.X的最高价氧化物对应的水化物是一种强酸
B [由四种元素的相对位置关系,W处于第三周期,W的最外层电子数是其原子序数的
1/3,设W的最外层电子数为x,则有:2+8+x=3x,解得x=5,推知W是P。X原子的K层电
子数与最外层电子数之比为2∶7,则X是F,从而推知Z是Cl,Y是C。P、Cl可形成化合物
PCl 、PCl ,A项错误;X的氢化物是HF,玻璃中含SiO,可与氢氟酸反应,故常用塑料瓶保存,
3 5 2
B项正确;C、Cl元素可形成多氯代烃,如CCl ===CCl 、CCl —CCl 等,含有非极性键,C项错
2 2 3 3
误;X是F,无最高价氧化物,D项错误。]
考向3 物质转化型推断(分析与推测能力)
利用物质转化关系作为元素推断的突破口,是元素推断的新型考法之一,题目通常以框
图转化的形式给出物质的转化关系、反应现象等关键信息,要求考生结合短周期主族元素的
原子结构及元素的特殊性对元素进行合理的推断,此类试题体现《中国高考评价体系》对于
分析与推测、归纳与论证等学科关键能力的要求,要求结合物质的结构、性质、转化及反应现
象等信息,识别有效证据、科学推理论证,推断相关物质及元素,结合元素周期表、元素周期
律及化学键等知识,进行分析、判断。
(全国卷Ⅰ)短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组
成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01 mol·L
-1r溶液的pH为2,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正
确的是( )
A.原子半径的大小WX>Y
C.Y的氢化物常温常压下为液态
D.X的最高价氧化物的水化物为强酸
C [短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化
合物,n是元素Z的单质,通常为黄绿色气体,则n是氯气,Z是氯元素;0.01 mol·L-1r溶液的
pH为2,说明r是强酸,因此W是H;q的水溶液具有漂白性,s通常是难溶于水的混合物,根
据转化关系图可知m是水,r是氯化氢,q是次氯酸,p是烷烃(如甲烷),因此X是碳元素,Y
是氧元素。同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,则原子半径的大小:WX,B项错误;Y的氢化物是水或双氧水,常温常压下
为液态,C项正确;X的最高价氧化物的水化物碳酸为弱酸,D项错误。]
[强化5] (2021·四川成都检测)短周期主族元素W、X、Y、Z的原子序数依次增大,A、B、
C、D、E均由上述元素组成的中学化学常见的物质,其中A是单质,C是酸性氧化物,A的水
溶液和C均具有漂白性,B是自然界最常见的液体,E是三元化合物,物质之间存在如下图所
示的关系。下列说法不正确的是( )
A.YX 遇到蓝色石蕊试液先变红后褪色
2
B.离子半径大小关系:Y>Z>X>W
C.简单阴离子的还原性:Y>Z
D.Y与Z属于同一周期,与X属于同一主族
A [A单质的水溶液具有漂白性,说明A为Cl,C是酸性氧化物,其水溶液也具有漂白
2
性,即SO ,由此可判断B为水,D为HCl,E为HSO,则W、X、Y、Z分别为H、O、S、Cl四种
2 2 4
元素。YX 是 SO ,其水溶液呈酸性,使蓝色石蕊试液变红色,尽管SO 具有漂白性,但只能
2 2 2
选择性地漂白像品红、秸秆、毛丝等物质,而不能漂白石蕊及其变色后的物质,A项错误;四
种元素形成的简单离子中,H+半径最小,离子半径为S2->Cl->O2->H+,B项正确;由于S的
非金属性弱于Cl,则S2-的还原性强于Cl-,C项正确;S和Cl是第三周期相邻,S与O是ⅥA
相邻,D项正确。]
[强化6] (2021·北京海淀区检测)短周期元素X、Y、Z的原子序数依次增大,其中Y元素
的原子半径最大。已知A、B、C分别是X、Y、Z三种元素的单质,A和C常温下为气体。在适
宜的条件下, A、B、C可以发生如图所示的反应。下列说法正确的是( )A.化合物YX中含离子键
B.Z的含氧酸均为强酸
C.非金属性:X>Z
D.离子半径:Y>Z
A [结合题给信息推知,A是H、B是Na、Mg或Al等活泼金属,C是Cl,X、Y、Z分别
2 2
是H、Na(Mg或Al)、Cl。化合物NaH中含离子键,故A正确;HClO是弱酸,故B错误;非金
属性:Cl>H,故C错误;离子半径:Cl->Na+,故D错误。]
训练(二十六) 元素周期表中“位-构-性”关系及应用
1.(2021·江苏苏州调研)如表为元素周期
表中短周期的一部分,Y元素最高正价与
最低负价的代数和为4,
下列叙述正确的是( )
A.原子半径:WZ>Y
C.氢化物的热稳定性:WCl>S,B项正确;虽然非金属性:O>N,但没有指出是否为最简单的气态氢化物,故无法比
较氢化物的热稳定性,C项错误;根据非金属性:Cl>S,只能比较其最高价氧化物对应水化物
的酸性强弱,而D项没有说明是否为最高价氧化物对应的水化物,故无法判断,D项错误。]
2.(2020·北京顺义区二模)X、Y、Z、W是原子序数依次增大的四种短周期主族元素。X与
Z最外层电子数相同,X2-和Y+的电子层结构相同,Y的原子半径在短周期主族元素原子中
最大。下列说法正确的是( )
A.原子半径:Z>W
B.还原性:X2->Z2-
C.最高价氧化物的水化物酸性:Z>W
D.X、Y、Z形成的化合物水溶液一定显中性
A [短周期主族元素X、Y、Z、W的原子序数依次增大,Y的原子半径在短周期主族元
素原子中最大,则Y是Na;X2-和Y+的电子层结构相同,且X的原子序数小于Y,则X是O;
X和Z最外层电子数相同,且Z的原子序数大于X,则Z是S;W的原子序数大于Z(S),则W是Cl。原子半径:S>Cl,A项正确;元素的非金属性:O>S,则单质的氧化性:O>S,故阴离
2
子的还原性:O2-<S2-,B项错误;元素的非金属性:S<Cl,则最高价氧化物的水化物酸性:
HSO <HClO ,C项错误;O、Na、S元素形成的常见化合物有NaSO 、NaSO 等,其中
2 4 4 2 3 2 4
NaSO 发生水解而使水溶液呈碱性,D项错误。]
2 3
3.(2021·四川宜宾检测)W、X、Y、Z均为短周期主族元素,原子序数依次增加。W原子最
外层电子数是其所在周期数的2倍;Y+和X2-的电子层结构相同;Z的原子序数等于W和Y
的核外电子数之和。下列说法正确的是( )
A.Z的氢化物的酸性比WX 的水化物的强,说明Z的非金属性比W的强
2
B.离子半径大小:Z>Y>X
C.X和Y形成的化合物为离子化合物且阳离子和阴离子的个数之比为2∶1
D.Z元素的气态氢化物的热稳定性比X的高
C [ W、X、Y、Z均为短周期主族元素,原子序数依次增加。W原子最外层电子数是其所
在周期数的2倍,结合原子序数可知,W应位于第二周期,最外层电子数为4,W为C,若W
为S,X、Y、Z不可能均为短周期主族元素;Y+和X2-的电子层结构相同,则X为O、Y为Na;
Z的原子序数等于W和Y的核外电子数之和,Z的原子序数为6+11=17,Z为Cl,据此分析
解答。由上述分析可知,W为C、X为O、Y为Na、Z为Cl。盐酸为无氧酸,不能由盐酸与碳酸
的酸性比较C、Cl的非金属性, A项错误;电子层越多,离子半径越大,具有相同电子排布的
离子中原子序数大的离子半径小,则离子半径大小:Z>X>Y, B项错误;由Y、X两种元素组
成的常见离子化合物为NaO或NaO,其阳离子与阴离子个数比均为2∶1,C项正确;氢化
2 2 2
物稳定性与元素非金属性一致,则氢化物稳定性X>Z,D项错误。]
4.(2021·河南鹤壁一中检测)短周期主族元素A、B、C、D、E的原子序数依次增加,A和
D的质子数之和等于E的核外电子数,B和D同主族,C的原子半径是短周期主族元素中最
大的,A和E组成的化合物AE是常见强酸。下列说法错误的是( )
A.简单离子半径:B>C
B.热稳定性:AD>AE
2
C.CA为离子化合物,溶于水所得溶液呈碱性
D.实验室制备AE时可选用D的最高价含氧酸
B [短周期主族元素A、B、C、D、E的原子序数依次增加,C的原子半径是短周期主族元
素中最大的,则C为Na;A和E组成的化合物AE是常见强酸,则A为H,E为Cl;A和D的
质子数之和等于E的核外电子数,则D的质子数=17-1=16,则D为S;B和D同主族,则
B为O。氧离子和钠离子都含有2个电子层,核电荷数越大离子半径越小,则简单离子半径:
B>C,A项正确;非金属性SW>Z>X
B.元素Y与Z形成的盐在水溶液中呈碱性
C.最高价氧化物对应的水化物酸性:X>W
D.元素X与Z可以共存于同一离子化合物中
B [由信息可知,X、Y、Z、W分别为N、Al、Cl、P。元素Y与Z形成的盐AlCl 在水溶液
3
中水解呈酸性,B项错误。]
6.(2021·山东泰安检测)W、X、Y、Z是原子序数依次增大的四种短周期非金属主族元素,
q、r、s、h是这些元素形成的物质,其中h是离子化合物,q是制太阳能电池的主要原料,s常
温下呈气态且其水溶液显碱性,r为二元化合物,其浓溶液在空气中易形成白雾。下列说法正
确的是( )
A.常温常压下,W的氧化物为液态
B.单质的沸点:X>Z
C.X与Y属于同一主族,与Z属于同一周期
D.X的氧化物均能用向上排空气法收集
A [W、X、Y、Z是原子序数依次增大的四种短周期非金属主族元素,q、r、s、h 是这些元
素形成的物质,其中h 是离子化合物,应为铵盐,则含有N、H,可知W为H,q是制太阳能电
池的主要原料,应为Si,s常温下呈气态且其水溶液显碱性,s为氨气,r为二元化合物,其浓
溶液在空气中易形成白雾,应为HCl,则可知X为N,Y为Si,Z为Cl,根据上述分析可知,W
为H,X为N,Y为Si,Z为Cl。W的氧化物为水或过氧化氢。常温下,均为液体,A项正确;氮
气和氯气均为双原子分子,氯气的相对分子质量大于氮气,则氯气的范德华力大于氮气,故
沸点:氮气<氯气,B项错误;X为N,Y为Si,二者不是同主族元素, C项错误;如为NO,易
与氧气反应,则不能用排空气法收集, D项错误。]
7.(2021·河南信阳调研)主族元素W、X、Y、Z的原子序数依次增加,且均不大于20,它
们可以组成化学式为ZXY W 的硅酸盐。X3+与W2-具有相同的电子层结构,W、Z与X、Y的
3 8
质子数之和相等。下列判断正确的是( )
A.化合物ZXW 的水溶液呈碱性
2
B.简单气态氢化物稳定性:Y>W
C.最高价氧化物对应水化物酸性:X>Y
D.简单离子半径:X>Z
A [根据题给条件可以推出W、X、Y、Z依次为O、Al、Si、K,KAlO 溶液由于AlO水解
2
显碱性,故A符合题意;简单气态氢化物的稳定性SiHM>Y
B.常温下,Z和M的单质均能溶于浓硝酸
C.X+与Y结合形成的化合物是离子化合物
D.Z的最高价氧化物的水化物是中强碱
D [短周期元素X、Y、Z、M的原子序数依次增大,X、M的族序数均等于周期序数,则
X、M可能是H、Be、Al;Y原子核外最外层电子数是其电子总数的3/4,则Y是O元素;“团
簇分子”中X形成1个共价键,结合原子成键特点推知,则X是H,M是Al;“团簇分子”
的化学式为ZMY(YX) ,应为ZAl O(OH) ,则Z是化合价为+2价,Z应为Mg。电子层结
2 2 4 2 2 2 4 2
构相同的离子,核电荷数越小,离子半径越大,则离子半径:O2->Mg2+>Al3+,A项错误;常温
下,铝在浓硝酸中发生钝化,不能溶解,B项错误;H+和O形成的化合物为HO,属于共价化
2 2
合物,C项错误;Mg(OH) 是中强碱,D项正确。]
2
9.(2021·山东实验中学检测)短周期主族元素W、X、Y、Z的原子序数依次增大,W、Y同
主族,W的简单氢化物与Z的单质混合在光照下反应,气体颜色不断变浅,瓶壁上有油状液
滴,X的简单氢化物与Z的氢化物相遇会产生白烟。下列说法正确的是( )
A.“白烟”晶体中只含共价键
B.四种元素中,Z的原子半径最大
C.X的简单氢化物的热稳定性比Y的强
D.W的含氧酸的酸性一定比Z的弱
C [短周期主族元素W、X、Y、Z的原子序数依次增大,W的简单氢化物与Z的单质混
合在光照下反应,气体颜色不断变浅,瓶壁上有油状液滴,所以Z是Cl,W是C,W、Y同主族,
则Y为Si;X的简单氢化物与Z的氢化物相遇会产生白烟,X为N。根据上述分析知“白
烟”为NH Cl晶体,NH Cl属于离子化合物,既有离子键又有含共价键, A项错误;四种元
4 4
素的原子半径为Si>Cl>C>N,B项错误; X的简单氢化物为NH ,Y的简单氢化物为SiH,非
3 4
金属性:N>Si,热稳定性NH > SiH,C项正确;W的含氧酸为HCO,Z的含氧酸有HClO、
3 4 2 3
HClO 等几种,酸性HClOS>O,故Y>Z>W,A
项错误;氧原子最外层有6个电子,与硅原子形成2对共用电子对,该化合物中O原子均满
足8电子稳定结构,B项错误;X的最高价氧化物对应的水化物是NaOH,硅与强碱反应生成
硅酸钠和氢气,方程式为:Si+2NaOH+HO===Na SiO+2H↑,C项正确;比较氢化物的稳
2 2 3 2
定性,可比较其元素的非金属性,同一主族从上往下,非金属逐渐减弱,故非金属性O>S,则
稳定性:HO>HS,D项错误。]
2 2
11.(2021·河北辛集检测)短周期主族元素W,X,Y,Z的原子序数依次增大,W,X的最
外层电子数之和与Z的最外层电子数相等,W,Y同主族。将W、X的气态单质在催化剂及一
定温度和压强下发生可逆反应生成化合物 R,反应关系如下表所示。下列说法正确的是(
)
物质 W的单质 X的单质 R
起始时/mol 0.3 0.3 0
平衡时/mol 0.12 0.24 0.12
A.离子半径:X>Y>Z
B.Y、Z两种元素形成的化合物的水溶液呈酸性
C.Y、Z分别与W形成的化合物,前者的沸点高
D.四种元素分别与氧形成的化合物均只有两种
C [短周期主族元素W,X,Y,Z的原子序数依次增大,将W,X的气态单质在催化剂及
一定温度和压强下发生可逆反应生成化合物R,根据标准数据可知,平衡时消耗W、X和生
成R的物质的量分别为0.18 mol、0.06 mol、0.12 mol,三者物质的量之比为3∶1∶2,应该为
合成氨的反应,则W为H,X为N;W,Y同主族,则Y为Na;W,X的最外层电子数之和与Z
的最外层电子数相等,Z最外层电子数=1+5=6,其原子序数大于Na,则Z为S,据此解答。电子层越多离子半径越大,电子层相同时,核电荷数越大离子半径越小,则离子半径
Z>X>Y,A项错误; 硫化钠溶液中,硫离子水解溶液呈碱性,B项错误; NaH常温下为固体,
HS常温下为气体,NaH的沸点较高,C项正确; N与O形成的化合物有NO、NO 、NO 等
2 2 2 5
多种,D项错误。]
12.(2021·山东临沂模拟)短周期主族元素W、X、Y、Z、R的原子序数依次增大,其中X、
Z位于同一主族;W的气态氢化物常用作制冷剂;Y是同周期主族元素中离子半径最小的;
ZXR 能与水剧烈反应,观察到液面上有白雾生成,并有无色刺激性气味的气体逸出,该气体
2
能使品红溶液褪色。下列说法正确的是( )
A.简单气态氢化物的稳定性:W>X
B.含氧酸的酸性:ZY>Z
B.热稳定性:r>p
C.含Y元素的盐溶液可能显酸性、中性,不可能显碱性
D.二元化合物n 只含离子键,不含共价键
B [①淡黄色固体一般是单质S和二元化合物NaO,②同主族元素X、Y由半径大小
2 2
关系知分别位于二、三周期,③转化关系图中甲是O,乙是单质S,对应元素分别为X、Y,
2④Z原子半径比Y大,且X、Y原子序数之和是W、Z原子序数之和的2倍,则Z为Na、W为
H。化合物n与单质乙分别为过氧化钠、硫。由上述物质间的转化关系示意图可知,甲为氧气、
m为硫化钠、r为水。所以W、X、Y、Z分别为H、O、S、Na。 简单离子半径大小: Na+SiH,D项错
2 4 2 4
误。]
15.(2021·四川绵阳诊断)X、Y、Z、W为原子序数依次增大的短周期主族元素。X分别与
Y、Z、W结合形成质子数相同的甲、乙、丙三种分子。丁为无色气体,遇空气变为红棕色;丙的
水溶液可刻蚀玻璃。上述物质有如下图转化关系:
下列说法错误的是( )
A.四种元素形成的单质中,W的氧化性最强
B.甲、乙、丙中沸点最高的是丙
C.甲常用作制冷剂
D.甲、乙分子均只含极性共价键
B [丁为无色气体,遇空气变为红棕色,则丁是NO;丙的水溶液可刻蚀玻璃,则丙是
HF;X分别与Y、Z、W结合形成质子数相同的甲、乙、丙三种分子,结合图中物质之间的转化推知,W是F,Z是O,甲是NH ,乙是HO,则X、Y、Z、W分别是H、N、O、F元素。四种元素
2 2 3 2
中F的非金属性最强,则形成的单质中,F 的氧化性最强,A项正确;NH 、HO和HF都能形
2 3 2
成分子间氢键,但HO形成的氢键数目多余NH 和HF,故水的沸点最高,B项错误;NH 易
2 3 3
液化,气化时吸收大量的热,故NH 常用作制冷剂,C项正确;甲是NH ,乙是HO,二者都只
3 3 2
含极性共价键,D项正确。]