文档内容
训练(三十六) 化学平衡常数及平衡转化率
1.(2021·四川成都七中检测)对于反应C(s)+HO(g)CO(g)+H(g) ΔH>0,下列有
2 2
关说法正确的是( )
A.升高体系温度,平衡常数K减小
B.增大体系压强,平衡常数K不发生变化
C.平衡常数表达式为K=
D.增加C(s)的量,平衡正向移动
B [正反应为吸热反应,升高体系温度,平衡正向移动,K增大,A项错误;化学平衡常
数只受温度的影响,与体系的压强无关,B项正确;C为固体,不带入K的表达式中,因此K
=,C项错误;固体物质的浓度视为定值,因此增加C(s)的量,平衡不移动,D项错误。]
2.(2021·天津重点中学联考)一定温度下,在一个容积为1 L的密闭容器中,充入1 mol
H(g)和1 mol I (g),发生反应H(g)+I(g)2HI(g),经充分反应达到平衡后,生成的HI(g)占
2 2 2 2
气体体积的50%,该温度下,在另一个容积为2 L的密闭容器中充入1 mol HI(g)发生反应
HI(g) H(g)+I(g),则下列判断正确的是( )
2 2
A.后一反应的平衡常数为1
B.后一反应的平衡常数为0.5
C.后一反应达到平衡时,H 的平衡浓度为0.25
2
D.后一反应达到平衡时,HI(g)的平衡浓度为0.5
B [前一反应达平衡时c(H )=c(I)=0.5 mol·L-1,c(HI)=1 mol·L-1,则平衡常数K ==
2 2 1
=4,而后一反应的平衡常数K ===0.5,A项错误,B项正确;设后一反应达平衡时c(H )=
2 2
x mol·L-1,则平衡时c(I)=x mol·L-1,c(HI)=(0.5-2x) mol·L-1,K ==0.5,解得x=0.125,
2 2
故平衡时c(HI)=0.25 mol·L-1,C、D项错误。]
3.(2021·江苏苏州期初调研)羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线
虫和真菌的危害。在恒容密闭容器中,将CO和HS混合加热并达到下列平衡:CO(g)+
2
HS(g) COS(g)+H(g) K=0.1。反应前CO的物质的量为10 mol,平衡后CO的物质的量
2 2
为8 mol。下列说法正确的是( )
A.升高温度,HS浓度增大,表明该反应是吸热反应
2
B.通入CO后,正反应速率逐渐增大
C.反应前HS物质的量为5 mol
2D.CO的平衡转化率为20%
D [升高温度,HS浓度增大,说明平衡向逆反应方向移动,逆反应吸热,正反应放热,A
2
项错误;通入CO气体瞬间正反应速率增大,达到最大值,向正反应方向建立新的平衡,正反
应速率逐渐减小,B项错误;设反应前HS的物质的量为n mol,容器的容积为V L,则
2
CO(g)+HS(g)COS(g)+H(g) K=0.1
2 2
n始/mol 10 n 0 0
n转/mol 2 2 2 2
n平/mol 8 n-2 2 2
K==0.1,解得n=7,C项错误;根据上述计算可知CO的转化率为20%,D项正确。]
4.(2021·湖南长郡中学检测)将一定量的SO (g)和O(g)分别通入体积为2 L的恒容密闭
2 2
容器中,在不同温度下进行反应,得到如下表中的两组数据:
起始量/mol 平衡量/mol
达到平衡所需
实验编号 温度/℃ 平衡常数
时间/min
O SO O SO
2 2 2 2
1 T K 4 2 x 0.8 6
1 1
2 T K 4 2 0.4 y t(t>6)
2 2
下列说法中不正确的是( )
A.x=2.4
B.T、T 的关系:T>T
1 2 1 2
C.K 、K 的关系:K >K
1 2 2 1
D.实验1在前6 min的反应速率 v(SO
2
)=0.2 mol·L-1·min-1
A [根据题中信息可列“三段式”:
2SO (g)+O(g)2SO (g)
2 2 3
n(起始)/mol 4 2
n(转化)/mol 4-x 2-0.8
n(平衡)/mol x 0.8
(4-x)∶(2-0.8)=2∶1,解得:x=1.6。同理,解得y=0.2。由t>6得,2SO (g)+O(g)
2 2
2SO (g)是放热反应,温度越高,反应速率越高,反应正向进行的程度越小,根据x,y可以
3
判断出T
1
>T
2
,K
1
<K
2
。实验1在前6 min的反应速率 v(SO
2
)==0.2 mol·L-1·min-1。]5.(2021·北京顺义区检测)在一定体积的1 L密闭容器中,进行如下化学反应:CO(g)+
2
H(g)CO(g)+HO(g),其化学平衡常数K和温度t的关系如下表:
2 2
t/℃ 700 800 830 1 000
K 0.6 0.9 1.0 1.7
下列说法正确的是( )
A.上述生成CO和HO的反应为放热反应
2
B.加压、增大H 浓度和加入催化剂都能提高CO 的转化率
2 2
C.830 ℃达平衡后,再充入1.0 mol H,K值增大,平衡正向移动
2
D.830 ℃时反应CO(g)+HO(g)CO(g)+H(g)的平衡常数为1
2 2 2
D [由表格数据可知,温度越高,K越大,则生成CO和HO的反应为吸热反应,A项错
2
误;该反应为气体体积不变的反应,加压、使用催化剂,平衡均不移动,则不能提高转化率,而
增大H 浓度能提高CO 的转化率,B项错误;充入1.0 mol H,反应物浓度增大,但K只与温
2 2 2
度有关,则平衡正向移动,但K不变,C项错误;正逆反应的K互为倒数关系,由830 ℃时
CO(g)+H(g)CO(g)+HO(g) K=1.0,则830 ℃时反应CO(g)+HO(g) CO(g)+
2 2 2 2 2
H(g)的平衡常数为K==1,D项正确。]
2
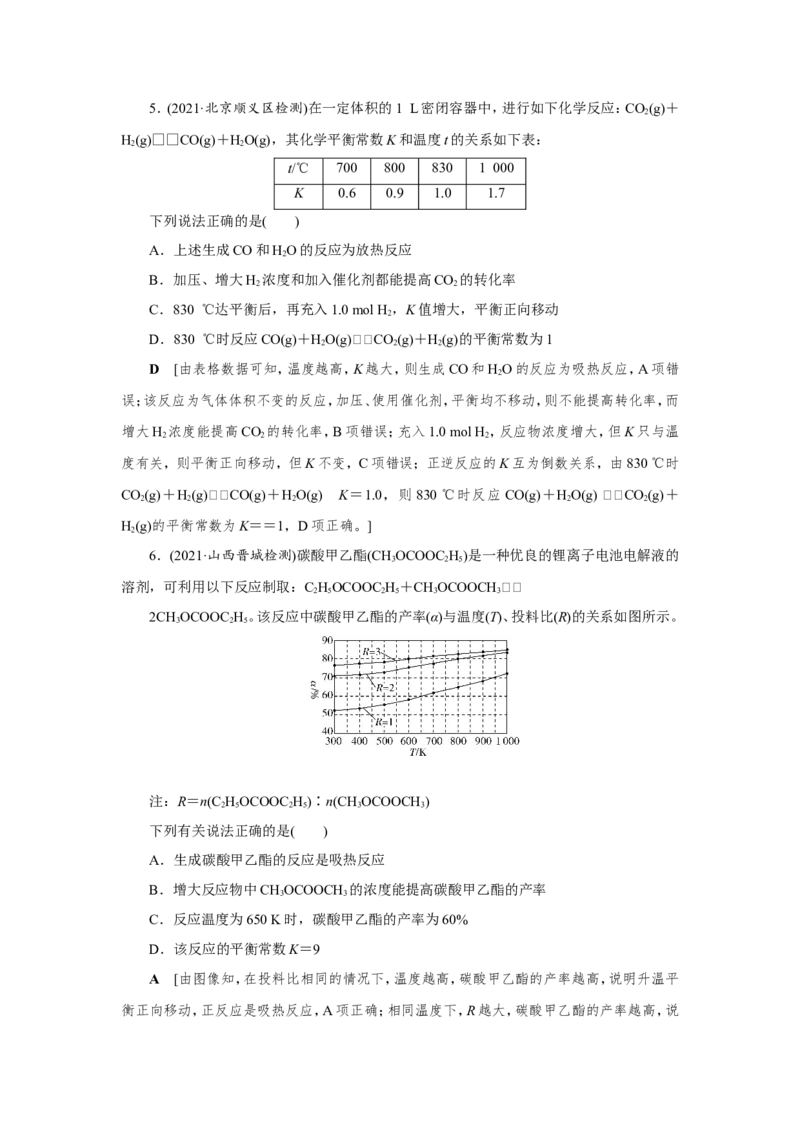
6.(2021·山西晋城检测)碳酸甲乙酯(CHOCOOC H)是一种优良的锂离子电池电解液的
3 2 5
溶剂,可利用以下反应制取:C HOCOOC H+CHOCOOCH
2 5 2 5 3 3
2CHOCOOC H。该反应中碳酸甲乙酯的产率(α)与温度(T)、投料比(R)的关系如图所示。
3 2 5
注:R=n(C HOCOOC H)∶n(CHOCOOCH )
2 5 2 5 3 3
下列有关说法正确的是( )
A.生成碳酸甲乙酯的反应是吸热反应
B.增大反应物中CHOCOOCH 的浓度能提高碳酸甲乙酯的产率
3 3
C.反应温度为650 K时,碳酸甲乙酯的产率为60%
D.该反应的平衡常数K=9
A [由图像知,在投料比相同的情况下,温度越高,碳酸甲乙酯的产率越高,说明升温平
衡正向移动,正反应是吸热反应,A项正确;相同温度下,R越大,碳酸甲乙酯的产率越高,说明C HOCOOC H 浓度越大,产物产率越高,CHOCOOCH 的浓度越大,产物产率越低,B项
2 5 2 5 3 3
错误;650 K时,只有R=1时,碳酸甲乙酯的产率为60%,C项错误;K与温度有关,温度不确
定,无法求K,D项错误。]
7.(2019·海南卷)由γ羟基丁酸生成γ丁内酯的反应如下:
在298 K下,γ羟基丁酸水溶液的初始浓度为0.180 mol·L-1,测得γ丁内酯的浓度随时
间变化的数据如表所示。回答下列问题:
t/min 21 50 80 100 120 160 220 ∞
c/mol·L-1 0.024 0.050 0.071 0.081 0.090 0.104 0.116 0.132
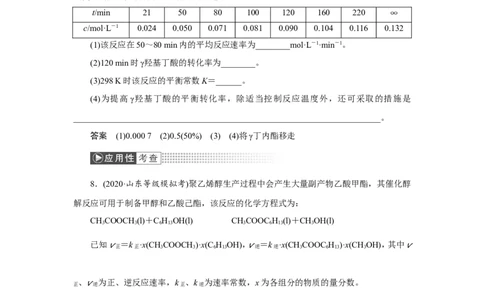
(1)该反应在50~80 min内的平均反应速率为________mol·L-1·min-1。
(2)120 min时γ羟基丁酸的转化率为________。
(3)298 K时该反应的平衡常数K=______。
(4)为提高γ羟基丁酸的平衡转化率,除适当控制反应温度外,还可采取的措施是
________________________________________________________________________。
答案 (1)0.000 7 (2)0.5(50%) (3) (4)将γ丁内酯移走
8.(2020·山东等级模拟考)聚乙烯醇生产过程中会产生大量副产物乙酸甲酯,其催化醇
解反应可用于制备甲醇和乙酸己酯,该反应的化学方程式为:
CHCOOCH (l)+C H OH(l) CHCOOC H (l)+CHOH(l)
3 3 6 13 3 6 13 3
已知 v正 =k 正 ·x(CH 3 COOCH 3 )·x(C 6 H 13 OH), v逆 =k 逆 ·x(CH 3 COOC 6 H 13 )·x(CH 3 OH),其中 v
正
、
v逆
为正、逆反应速率,k
正
、k
逆
为速率常数,x为各组分的物质的量分数。
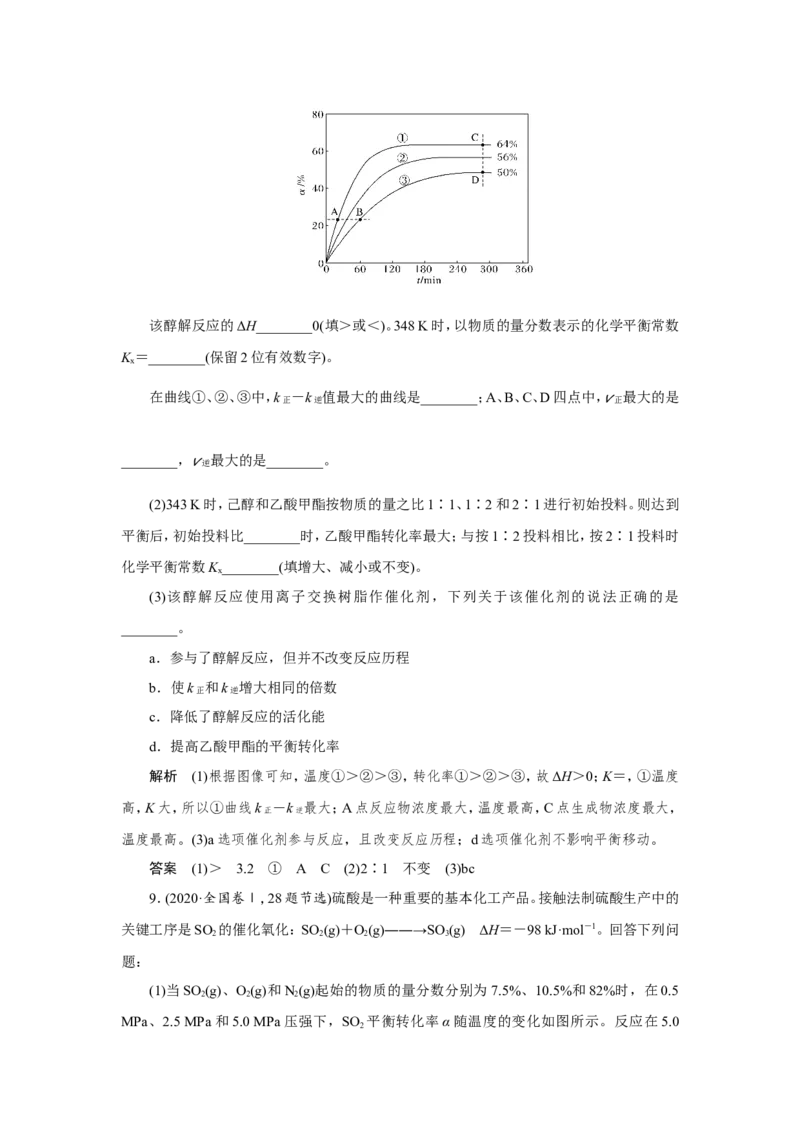
(1)反应开始时,己醇和乙酸甲酯按物质的量之比1∶1投料,测得348 K、343 K、338 K
三个温度下乙酸甲酯转化率(α)随时间(t)的变化关系如下图所示。该醇解反应的ΔH________0(填>或<)。348 K时,以物质的量分数表示的化学平衡常数
K =________(保留2位有效数字)。
x
在曲线①、②、③中,k
正
-k
逆
值最大的曲线是________;A、B、C、D四点中,
v正
最大的是
________,
v逆
最大的是________。
(2)343 K时,己醇和乙酸甲酯按物质的量之比1∶1、1∶2和2∶1进行初始投料。则达到
平衡后,初始投料比________时,乙酸甲酯转化率最大;与按1∶2投料相比,按2∶1投料时
化学平衡常数K ________(填增大、减小或不变)。
x
(3)该醇解反应使用离子交换树脂作催化剂,下列关于该催化剂的说法正确的是
________。
a.参与了醇解反应,但并不改变反应历程
b.使k 和k 增大相同的倍数
正 逆
c.降低了醇解反应的活化能
d.提高乙酸甲酯的平衡转化率
解析 (1)根据图像可知,温度①>②>③,转化率①>②>③,故ΔH>0;K=,①温度
高,K大,所以①曲线k -k 最大;A点反应物浓度最大,温度最高,C点生成物浓度最大,
正 逆
温度最高。(3)a选项催化剂参与反应,且改变反应历程;d选项催化剂不影响平衡移动。
答案 (1)> 3.2 ① A C (2)2∶1 不变 (3)bc
9.(2020·全国卷Ⅰ,28题节选)硫酸是一种重要的基本化工产品。接触法制硫酸生产中的
关键工序是SO 的催化氧化:SO (g)+O(g)――→SO (g) ΔH=-98 kJ·mol-1。回答下列问
2 2 2 3
题:
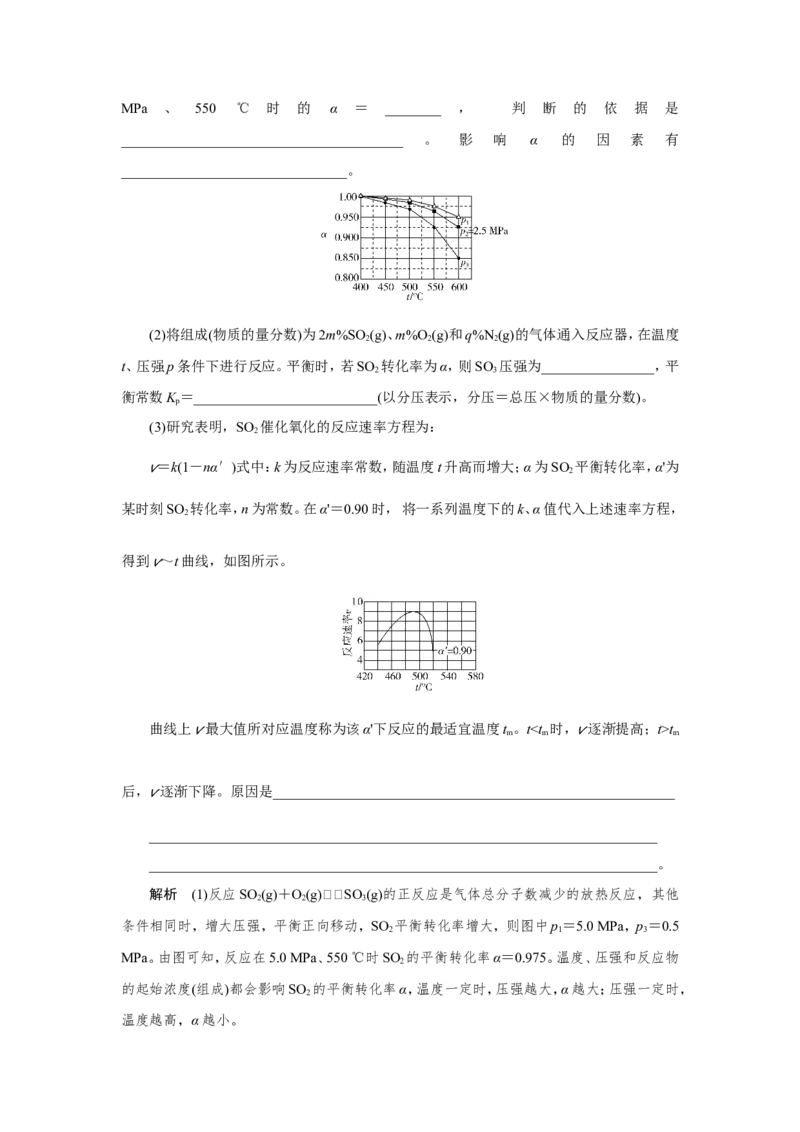
(1)当SO (g)、O(g)和N(g)起始的物质的量分数分别为7.5%、10.5%和82%时,在0.5
2 2 2
MPa、2.5 MPa和5.0 MPa压强下,SO 平衡转化率α随温度的变化如图所示。反应在5.0
2MPa 、 550 ℃ 时 的 α = ________ , 判 断 的 依 据 是
________________________________________ 。 影 响 α 的 因 素 有
________________________________。
(2)将组成(物质的量分数)为2m%SO (g)、m%O (g)和q%N (g)的气体通入反应器,在温度
2 2 2
t、压强p条件下进行反应。平衡时,若SO 转化率为α,则SO 压强为________________,平
2 3
衡常数K =__________________________(以分压表示,分压=总压×物质的量分数)。
p
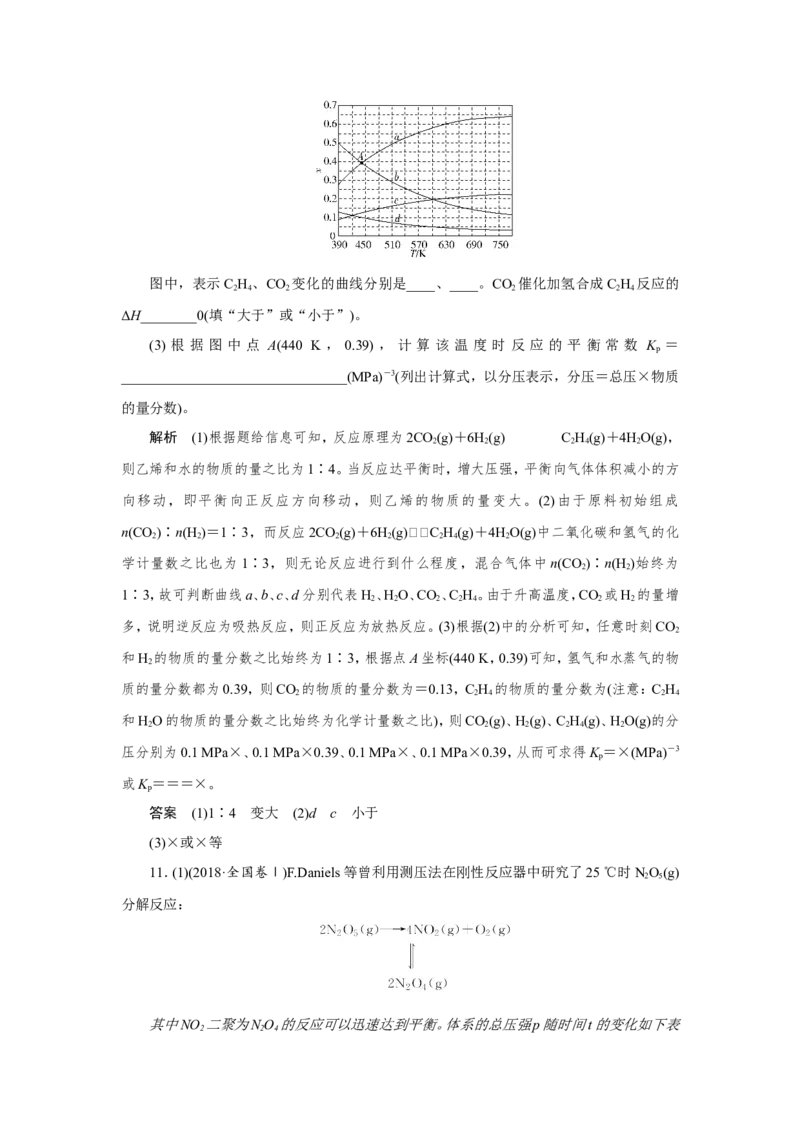
(3)研究表明,SO 催化氧化的反应速率方程为:
2
v
=k(1-nα′)式中:k为反应速率常数,随温度t升高而增大;α为SO
2
平衡转化率,α'为
某时刻SO 转化率,n为常数。在α'=0.90时, 将一系列温度下的k、α值代入上述速率方程,
2
得到
v
~t曲线,如图所示。
曲线上
v
最大值所对应温度称为该α'下反应的最适宜温度t
m
。tt
m
后,
v
逐渐下降。原因是_________________________________________________________
________________________________________________________________________
________________________________________________________________________。
解析 (1)反应SO (g)+O(g)SO (g)的正反应是气体总分子数减少的放热反应,其他
2 2 3
条件相同时,增大压强,平衡正向移动,SO 平衡转化率增大,则图中p=5.0 MPa,p=0.5
2 1 3
MPa。由图可知,反应在5.0 MPa、550 ℃时SO 的平衡转化率α=0.975。温度、压强和反应物
2
的起始浓度(组成)都会影响SO 的平衡转化率α,温度一定时,压强越大,α越大;压强一定时,
2
温度越高,α越小。(2)在温度t、压强p条件下进行反应,平衡时SO 转化率为α,由于N 对反应无影响,可
2 2
认为混合气体由SO 和O 组成,则有2m%+m%=1,2m+m=100,设SO 有2m mol,则O
2 2 2 2
有m mol,利用“三段式法”计算:
SO (g) + O(g) SO (g)
2 2 3
起始量/mol 2m m 0
转化量/mol 2mα mα 2mα
平衡量/mol 2m×(1-α) m×(1-α) 2mα
因反应恒压,故SO 的压强为p=·p=p。
3
平衡时,SO 、O 的压强分别为p、p,则平衡常数K ==。
2 2 p
(3)在α′=0.90时,SO
2
催化氧化的反应速率为
v
=k·(1-0.90n)。升高温度,k增大使
v
逐渐提高,但α降低使
v
逐渐下降。t<t
m
时,k增大对
v
的提高大于α引起的降低;t>t
m
后,k
增大对
v
的提高小于α引起的降低。
答案 (1)0.975 该反应气体分子数减小,增大压强,α提高。5.0MPa>2.5MPa=p,所以
2
p 1 =5.0MPa 温度、压强和反应物的起始浓度(组成) (2) (3)升高温度,k增大使 v 逐渐
提高,但α降低使
v
逐渐下降。t<t
m
时,k增大对
v
的提高大于α引起的降低;t>t
m
后,k增大
对
v
的提高小于α引起的降低
10.(2020·全国卷Ⅲ)二氧化碳催化加氢合成乙烯是综合利用CO 的热点研究领域。回答
2
下列问题:
(1)CO 催化加氢生成乙烯和水的反应中,产物的物质的量之比 n(C H)∶n(H O)=
2 2 4 2
________。当反应达到平衡时,若增大压强,则n(C H)________(填“变大”“变小”或“不
2 4
变”)。
(2)理论计算表明,原料初始组成n(CO)∶n(H )=1∶3,在体系压强为0.1 MPa,反应达
2 2
到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。图中,表示C H 、CO 变化的曲线分别是____、____。CO 催化加氢合成C H 反应的
2 4 2 2 2 4
ΔH________0(填“大于”或“小于”)。
(3) 根 据 图 中 点 A(440 K , 0.39) , 计 算 该 温 度 时 反 应 的 平 衡 常 数 K =
p
________________________________(MPa)-3(列出计算式,以分压表示,分压=总压×物质
的量分数)。
解析 (1)根据题给信息可知,反应原理为2CO(g)+6H(g)C H(g)+4HO(g),
2 2 2 4 2
则乙烯和水的物质的量之比为1∶4。当反应达平衡时,增大压强,平衡向气体体积减小的方
向移动,即平衡向正反应方向移动,则乙烯的物质的量变大。(2)由于原料初始组成
n(CO)∶n(H )=1∶3,而反应2CO(g)+6H(g)C H(g)+4HO(g)中二氧化碳和氢气的化
2 2 2 2 2 4 2
学计量数之比也为1∶3,则无论反应进行到什么程度,混合气体中n(CO)∶n(H )始终为
2 2
1∶3,故可判断曲线a、b、c、d分别代表H、HO、CO、C H。由于升高温度,CO 或H 的量增
2 2 2 2 4 2 2
多,说明逆反应为吸热反应,则正反应为放热反应。(3)根据(2)中的分析可知,任意时刻CO
2
和H 的物质的量分数之比始终为1∶3,根据点A坐标(440 K,0.39)可知,氢气和水蒸气的物
2
质的量分数都为0.39,则CO 的物质的量分数为=0.13,C H 的物质的量分数为(注意:C H
2 2 4 2 4
和HO的物质的量分数之比始终为化学计量数之比),则CO(g)、H(g)、C H(g)、HO(g)的分
2 2 2 2 4 2
压分别为0.1 MPa×、0.1 MPa×0.39、0.1 MPa×、0.1 MPa×0.39,从而可求得K =×(MPa)-3
p
或K ===×。
p
答案 (1)1∶4 变大 (2)d c 小于
(3)×或×等
11.(1)(2018·全国卷Ⅰ)F.Daniels等曾利用测压法在刚性反应器中研究了25 ℃时NO(g)
2 5
分解反应:
其中NO 二聚为N O 的反应可以迅速达到平衡。体系的总压强p随时间t的变化如下表
2 2 4所示[t=∞时,N O(g)完全分解]:
2 5
t/min 0 40 80 160 260 1 300 1 700 ∞
p/kPa 35.8 40.3 42.5 45.9 49.2 61.2 62.3 63.1
25 ℃时NO(g)2NO (g)反应的平衡常数K =________kPa(K 为以分压表示的平衡
2 4 2 p p
常数,计算结果保留1位小数)。
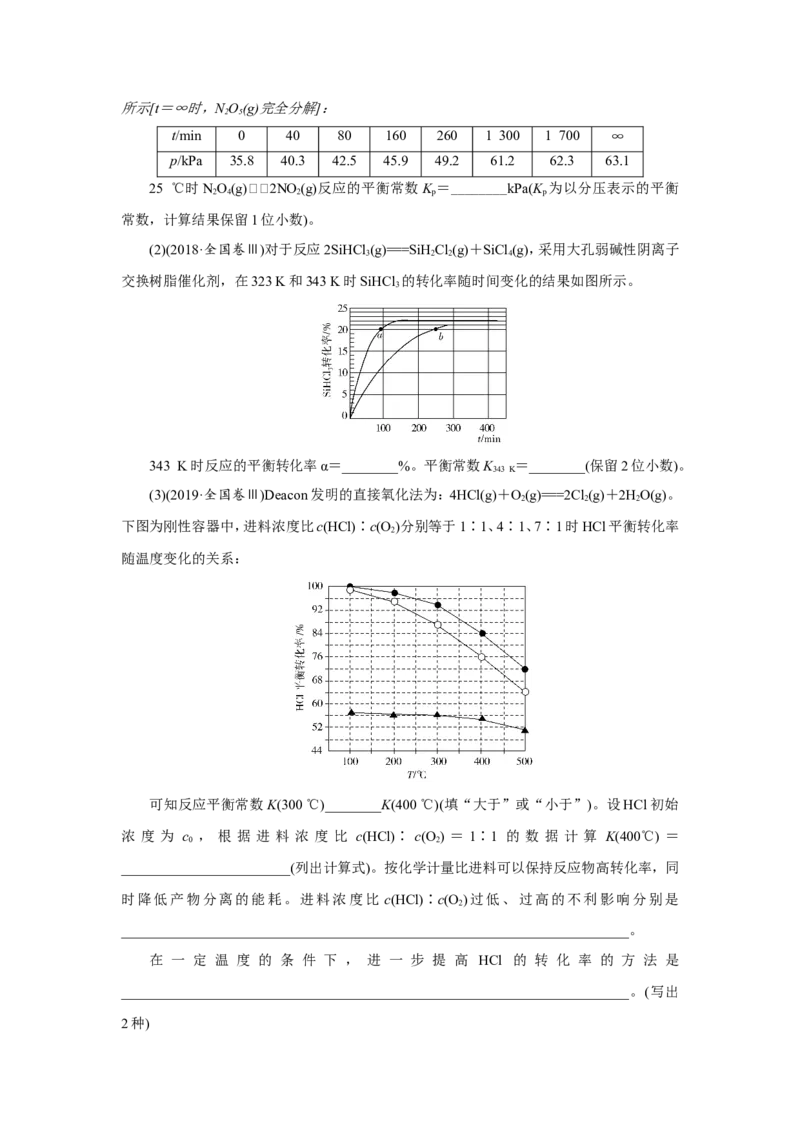
(2)(2018·全国卷Ⅲ)对于反应2SiHCl (g)===SiH Cl(g)+SiCl (g),采用大孔弱碱性阴离子
3 2 2 4
交换树脂催化剂,在323 K和343 K时SiHCl 的转化率随时间变化的结果如图所示。
3
343 K时反应的平衡转化率α=________%。平衡常数K =________(保留2位小数)。
343 K
(3)(2019·全国卷Ⅲ)Deacon发明的直接氧化法为:4HCl(g)+O(g)===2Cl(g)+2HO(g)。
2 2 2
下图为刚性容器中,进料浓度比c(HCl)∶c(O )分别等于1∶1、4∶1、7∶1时HCl平衡转化率
2
随温度变化的关系:
可知反应平衡常数K(300 ℃)________K(400 ℃)(填“大于”或“小于”)。设HCl初始
浓 度 为 c , 根 据 进 料 浓 度 比 c(HCl)∶ c(O ) = 1∶1 的 数 据 计 算 K(400℃) =
0 2
________________________(列出计算式)。按化学计量比进料可以保持反应物高转化率,同
时降低产物分离的能耗。进料浓度比 c(HCl)∶c(O )过低、过高的不利影响分别是
2
________________________________________________________________________。
在 一 定 温 度 的 条 件 下 , 进 一 步 提 高 HCl 的 转 化 率 的 方 法 是
________________________________________________________________________。(写出
2种)解析 (1)时间无限长时NO 完全分解,故由2NO(g)===4NO(g)+O(g)知,此时生成
2 5 2 5 2 2
的p(NO )===2p(N O)=2×35.8 kPa=71.6 kPa,p(O )=0.5×35.8 kPa=17.9 kPa。由题意知,
2 2 5 2
平衡时体系的总压强为63.1 kPa,则平衡体系中NO 、NO 的压强和为63.1 kPa-17.9 kPa=
2 2 4
45.2 kPa,设NO 的压强为x kPa,则
2 4
NO(g)2NO (g)
2 4 2
初始压强/kPa 0 71.6
转化压强/kPa x 2x
平衡压强/kPa x 71.6-2x
则有x+(71.6-2x)=45.2,解得x=26.4,71.6 kPa-26.4 kPa×2=18.8 kPa,K ==
p
≈13.4 kPa。
(2)温度越高,反应速率越快,达到平衡的时间越短,曲线a达到平衡的时间短,则曲线a
代表343 K时SiHCl 的转化率变化,曲线b代表323 K时SiHCl 的转化率变化。
3 3
①由题图可知,343 K时反应的平衡转化率α=22%。设起始时SiHCl (g)的浓度为1
3
mol·L-1,则有
2SiHCl (g)===SiH Cl(g)+SiCl (g)
3 2 2 4
起始浓度/mol·L-1 1 0 0
转化浓度/mol·L-1 0.22 0.11 0.11
平衡浓度/mol·L-1 0.78 0.11 0.11
则343 K时该反应的平衡常数K ==≈0.02。
343 K
(3)由图像知,随着温度的升高,HCl的平衡转化率降低,所以4HCl(g)+O(g)===2Cl(g)
2 2
+2HO(g)的ΔH<0,升高温度平衡左移,则K(300 ℃)>K(400 ℃)。在温度一定的条件下,
2
c(HCl)和c(O )的进料比越大,HCl的平衡转化率越低,所以题图中自上而下三条曲线是
2
c(HCl)∶c(O )(进料浓度比)为1∶1、4∶1、7∶1时的变化曲线。当c(HCl)∶c(O )=1∶1时,列
2 2
三段式:
4HCl(g)+O(g)===2Cl(g)+2HO(g)
2 2 2
起始浓度 c c 0 0
0 0
转化浓度 0.84c 0.21c 0.42c 0.42c
0 0 0 0
平衡浓度 (1-0.84)c (1-0.21)c 0.42c 0.42c
0 0 0 0
K(400℃)=
=。
c(HCl)∶c(CO)过高时,HCl转化率较低;当c(HCl)∶c(O )过低时,过量的O 和Cl 分离
2 2 2 2时能耗较高。
由平衡移动的条件可知,为提高HCl的转化率,在温度一定的条件下,可以增大反应体
系的压强,增加O 的量,或者及时除去产物。
2
答案 (1)13.4 (2)22 0.02
(3)大于 O 和Cl 分离能耗较高、HCl转化率较低 增加反应体系压强、及时除去产
2 2
物