文档内容
1.(2022·济南高三月考)下列说法正确的是( )
A.焓的大小受体系的温度、压强等因素的影响
B.化学反应的反应热等于反应前后焓的变化
C.浓硫酸溶于水是放热反应
D.煤的液化有利于实现碳达峰、碳中和
2.“太阳能燃料”国际会议于2019年10月在我国武汉举行,旨在交流和探讨太阳能光催
化分解水制氢、太阳能光催化二氧化碳转化为燃料等问题。下列说法错误的是( )
A.太阳能燃料属于一次能源
B.直接电催化CO 制取燃料时,燃料是阴极产物
2
C.光催化分解水产生的H 是理想的绿色能源
2
D.研发和利用太阳能燃料,有利于经济的可持续发展
3.已知化学反应A(g)+B (g)===2AB(g) ΔH=+100 kJ·mol-1的能量变化如图所示,判断
2 2
下列叙述正确的是( )
A.加入催化剂,该反应的反应热ΔH变小
B.每形成2 mol A—B,将吸收b kJ能量
C.每生成2分子AB吸收(a-b) kJ热量
D.该反应正反应的活化能大于100 kJ·mol-1
4.已知:①2H(g)+O(g)===2HO(g) ΔH=-483.6 kJ·mol-1;②H(g)+S(g)===HS(g)
2 2 2 2 2
ΔH=-20.1 kJ·mol-1,下列判断正确的是( )
A.若反应②中改用固态硫,则消耗1 mol S(s)反应放出的热量小于20.1 kJ
B.从焓变数值知,单质硫与氧气相比,更容易与氢气化合
C.由反应①②知,水的热稳定性弱于硫化氢
D.氢气的燃烧热ΔH=-241.8 kJ·mol-1
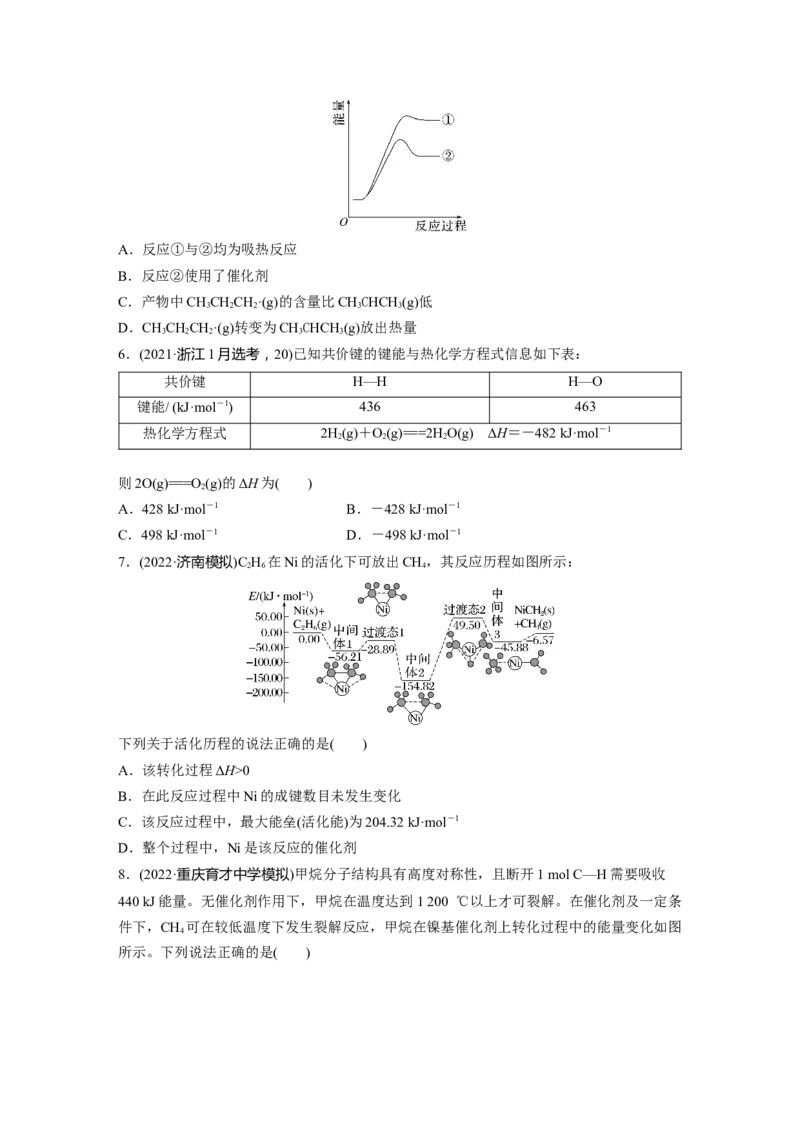
5.(2022·北京模拟)丙烷与溴原子能发生以下两种反应:
①CHCHCH(g)+Br·(g)―→CHCHCH·(g)+HBr(g)
3 2 3 3 2 2
②CHCHCH(g)+Br·(g)―→CHCHCH (g)+HBr(g)反应过程的能量变化如图所示。下列说
3 2 3 3 3
法不正确的是( )A.反应①与②均为吸热反应
B.反应②使用了催化剂
C.产物中CHCHCH·(g)的含量比CHCHCH (g)低
3 2 2 3 3
D.CHCHCH·(g)转变为CHCHCH (g)放出热量
3 2 2 3 3
6.(2021·浙江1月选考,20)已知共价键的键能与热化学方程式信息如下表:
共价键 H—H H—O
键能/ (kJ·mol-1) 436 463
热化学方程式 2H(g)+O(g)===2HO(g) ΔH=-482 kJ·mol-1
2 2 2
则2O(g)===O(g)的ΔH为( )
2
A.428 kJ·mol-1 B.-428 kJ·mol-1
C.498 kJ·mol-1 D.-498 kJ·mol-1
7.(2022·济南模拟)C H 在Ni的活化下可放出CH,其反应历程如图所示:
2 6 4
下列关于活化历程的说法正确的是( )
A.该转化过程ΔH>0
B.在此反应过程中Ni的成键数目未发生变化
C.该反应过程中,最大能垒(活化能)为204.32 kJ·mol-1
D.整个过程中,Ni是该反应的催化剂
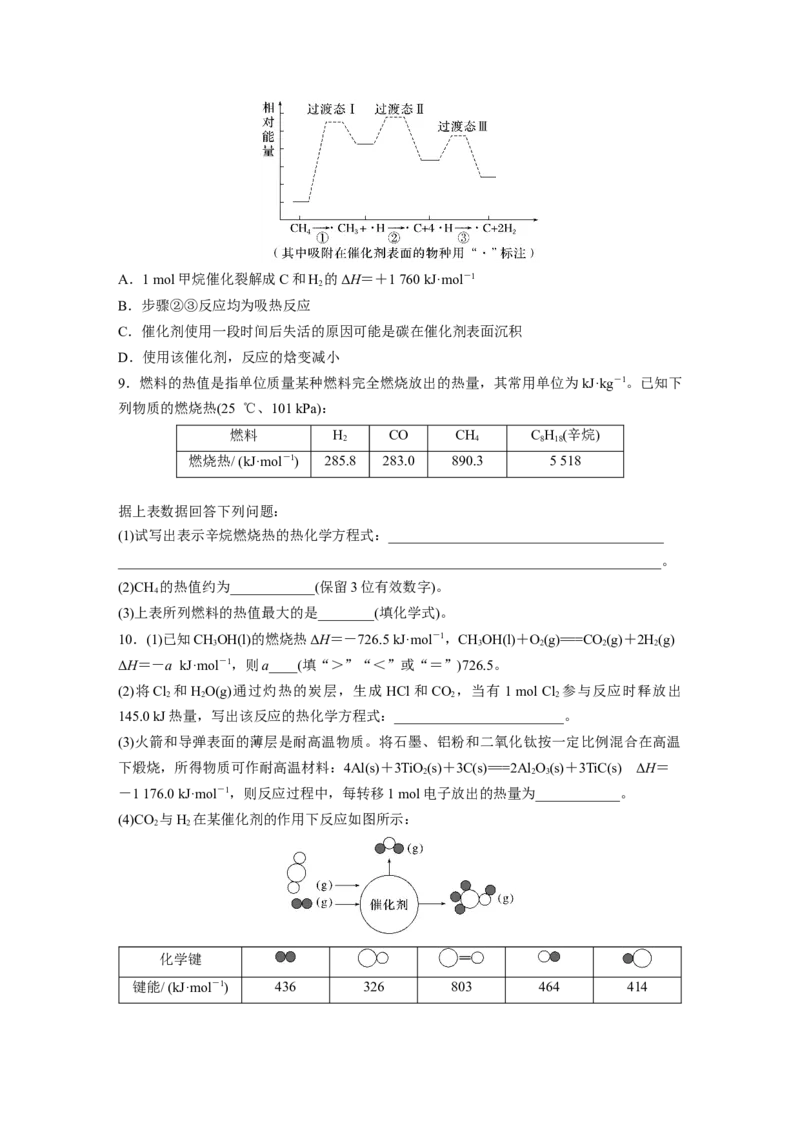
8.(2022·重庆育才中学模拟)甲烷分子结构具有高度对称性,且断开1 mol C—H需要吸收
440 kJ能量。无催化剂作用下,甲烷在温度达到1 200 ℃以上才可裂解。在催化剂及一定条
件下,CH 可在较低温度下发生裂解反应,甲烷在镍基催化剂上转化过程中的能量变化如图
4
所示。下列说法正确的是( )A.1 mol甲烷催化裂解成C和H 的ΔH=+1 760 kJ·mol-1
2
B.步骤②③反应均为吸热反应
C.催化剂使用一段时间后失活的原因可能是碳在催化剂表面沉积
D.使用该催化剂,反应的焓变减小
9.燃料的热值是指单位质量某种燃料完全燃烧放出的热量,其常用单位为kJ·kg-1。已知下
列物质的燃烧热(25 ℃、101 kPa):
燃料 H CO CH C H (辛烷)
2 4 8 18
燃烧热/ (kJ·mol-1) 285.8 283.0 890.3 5 518
据上表数据回答下列问题:
(1)试写出表示辛烷燃烧热的热化学方程式:_______________________________________
_____________________________________________________________________________。
(2)CH 的热值约为____________(保留3位有效数字)。
4
(3)上表所列燃料的热值最大的是________(填化学式)。
10.(1)已知CHOH(l)的燃烧热ΔH=-726.5 kJ·mol-1,CHOH(l)+O(g)===CO(g)+2H(g)
3 3 2 2 2
ΔH=-a kJ·mol-1,则a____(填“>”“<”或“=”)726.5。
(2)将Cl 和HO(g)通过灼热的炭层,生成 HCl和CO ,当有1 mol Cl 参与反应时释放出
2 2 2 2
145.0 kJ热量,写出该反应的热化学方程式:________________________。
(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温
下煅烧,所得物质可作耐高温材料:4Al(s)+3TiO(s)+3C(s)===2Al O(s)+3TiC(s) ΔH=
2 2 3
-1 176.0 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为____________。
(4)CO 与H 在某催化剂的作用下反应如图所示:
2 2
化学键
键能/ (kJ·mol-1) 436 326 803 464 414写出该反应的热化学方程式:_____________________________________________________
_______________________________________________________________________________
。
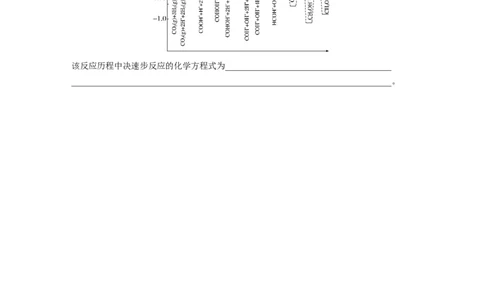
(5)CO 催化加氢制CHOH的一种反应历程如图所示(吸附在催化剂表面的物质用*标注,如
2 3
CO表示CO 吸附在催化剂表面)。
2
该反应历程中决速步反应的化学方程式为_______________________________________
___________________________________________________________________________。