文档内容
第 38 讲 反应热 热化学方程式
[复习目标] 1.知道常见的吸热反应和放热反应,了解反应热、焓变的概念以及反应热产生
的原因。2.了解热化学方程式的含义,能正确书写热化学方程式。3.了解燃烧热的含义和能
源及能源利用的意义。
考点一 反应热 焓变
1.反应热和焓变
(1)反应热:在等温条件下,化学反应体系向环境释放或从环境________的热量。
(2)焓变
①焓(H):与内能有关的物理量。
②焓变(ΔH):生成物的焓与反应物的焓之差。
③焓变与反应热的关系
等压条件下的反应热等于反应的焓变,常用____表示反应热,常用单位:______。
2.常见的吸热反应和放热反应
吸热反应(ΔH>0) 放热反应(ΔH<0)
①中和反应
①Ba(OH) ·8H O与NH Cl的反
2 2 4
②燃烧反应
应
③金属与酸或氧气的反应
②大多数的分解反应
④铝热反应
③弱电解质的电离
⑤酸性氧化物或碱性氧化物与
④盐类水解
水的反应
⑤C和HO(g)、C和CO 的反应
2 2
⑥大多数的化合反应3.吸热、放热的原因分析
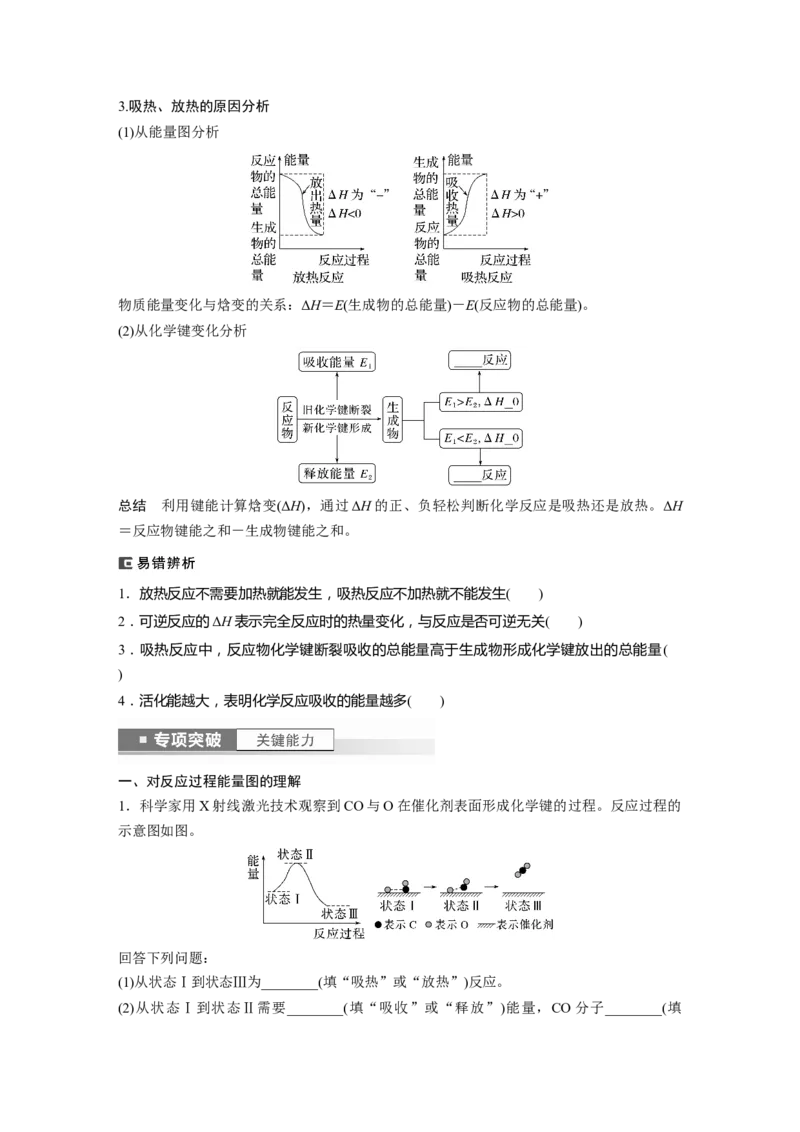
(1)从能量图分析
物质能量变化与焓变的关系:ΔH=E(生成物的总能量)-E(反应物的总能量)。
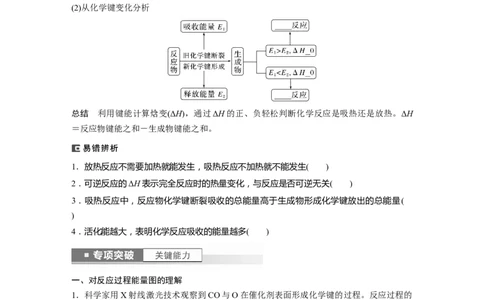
(2)从化学键变化分析
总结 利用键能计算焓变(ΔH),通过ΔH的正、负轻松判断化学反应是吸热还是放热。ΔH
=反应物键能之和-生成物键能之和。
1.放热反应不需要加热就能发生,吸热反应不加热就不能发生( )
2.可逆反应的ΔH表示完全反应时的热量变化,与反应是否可逆无关( )
3.吸热反应中,反应物化学键断裂吸收的总能量高于生成物形成化学键放出的总能量(
)
4.活化能越大,表明化学反应吸收的能量越多( )
一、对反应过程能量图的理解
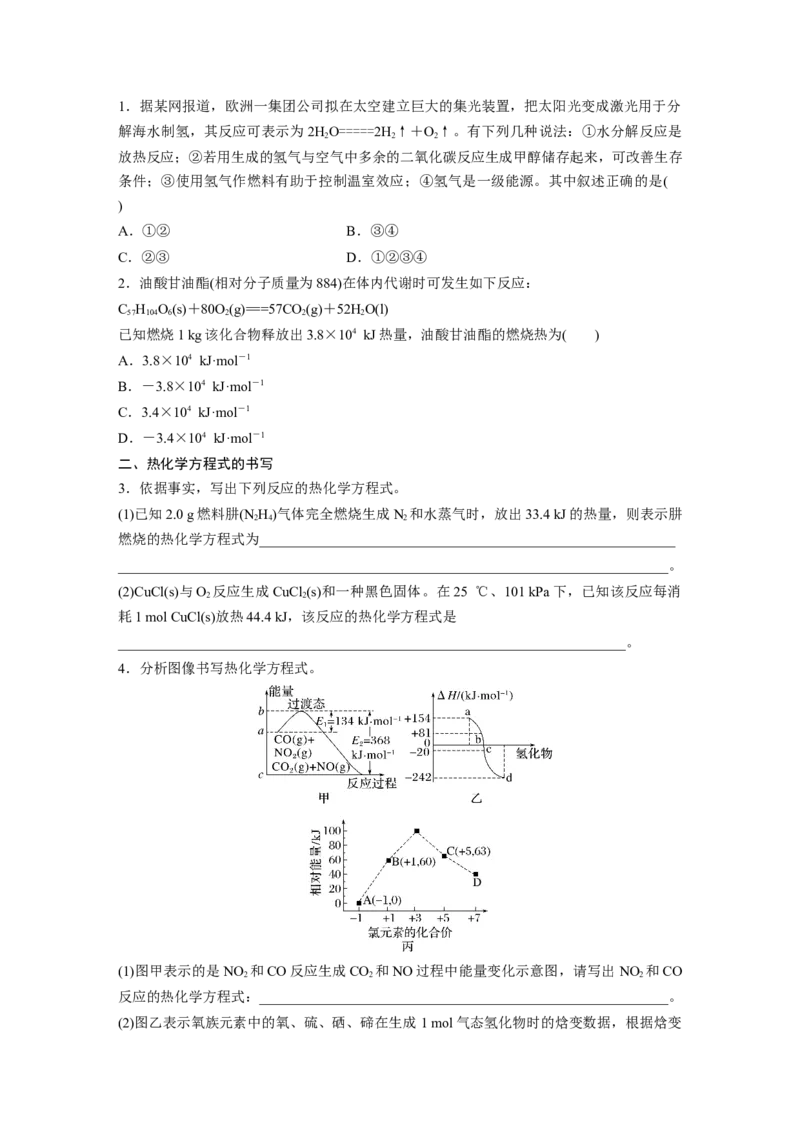
1.科学家用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的
示意图如图。
回答下列问题:
(1)从状态Ⅰ到状态Ⅲ为________(填“吸热”或“放热”)反应。
(2)从状态Ⅰ到状态Ⅱ需要________(填“吸收”或“释放”)能量,CO分子________(填“是”或“否”)需要断键形成C和O。
(3)从状态Ⅱ到状态Ⅲ形成的化学键是_____________________________________________。
(4)将相同物质的量的CO转化为CO ,CO与O比CO与O 反应放出的热量________(填
2 2
“ 多 ” 或 “ 少 ” ) , 可 能 的 原 因 是
______________________________________________________
_____________________________________________________________________________。
(5)由该反应过程可知,在化学反应中,旧化学键________(填“一定”或“不一定”)完全断
裂,但一定有新化学键的________。
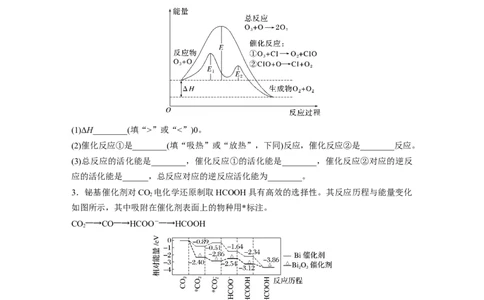
2.臭氧层中O 分解过程如图所示,回答下列问题。
3
(1)ΔH________(填“>”或“<”)0。
(2)催化反应①是________(填“吸热”或“放热”,下同)反应,催化反应②是________反应。
(3)总反应的活化能是________,催化反应①的活化能是________,催化反应②对应的逆反
应的活化能是______,总反应对应的逆反应活化能为________。
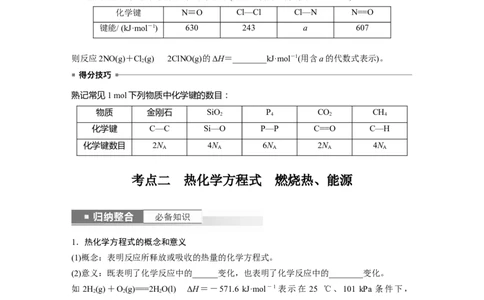
3.铋基催化剂对CO 电化学还原制取HCOOH具有高效的选择性。其反应历程与能量变化
2
如图所示,其中吸附在催化剂表面上的物种用*标注。
CO――→CO――→HCOO-――→HCOOH
2
(1)使用Bi、BiO 两种催化剂,哪个更有利于 CO 的吸附?________。简述判断依据:
2 3 2
_____________________________________________________________________________
____________________________________________________________________________。
(2)CO 电化学还原制取HCOOH反应的ΔH________(填“>”或“<”)0。
2
(3)使用 Bi 催化剂时,最大能垒是____________,使用 BiO 催化剂时,最大能垒是
2 3
________________________________________________________________________。(4)由*CO生成*HCOO-的反应为___________________________________________________
_____________________________________________________________________________。
二、根据键能计算焓变
4.CH—CH(g)―→CH==CH(g)+H(g) ΔH,有关化学键的键能如下表:
3 3 2 2 2
化学键 C—H C==C C—C H—H
键能/ (kJ·mol-1) 414 615 347 435
则该反应的反应热为____________。
5.已知几种化学键的键能数据如下表所示(亚硝酰氯的结构式为Cl—N==O):
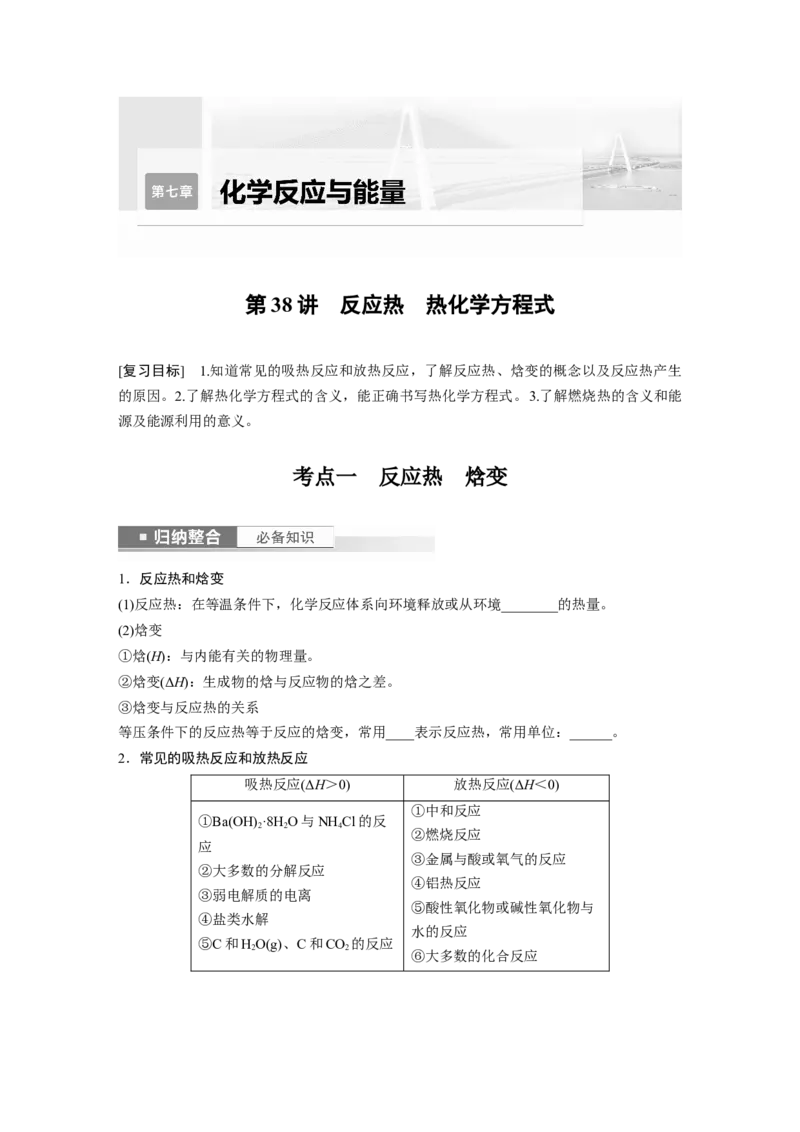
化学键 N≡O Cl—Cl Cl—N N==O
键能/ (kJ·mol-1) 630 243 a 607
则反应2NO(g)+Cl(g)2ClNO(g)的ΔH=________kJ·mol-1(用含a的代数式表示)。
2
熟记常见1 mol下列物质中化学键的数目:
物质 金刚石 SiO P CO CH
2 4 2 4
化学键 C—C Si—O P—P C==O C—H
化学键数目 2N 4N 6N 2N 4N
A A A A A
考点二 热化学方程式 燃烧热、能源
1.热化学方程式的概念和意义
(1)概念:表明反应所释放或吸收的热量的化学方程式。
(2)意义:既表明了化学反应中的______变化,也表明了化学反应中的________变化。
如 2H(g)+O(g)===2HO(l) ΔH=-571.6 kJ·mol-1表示在 25 ℃、101 kPa 条件下,
2 2 2
________________________________________________________________________。
2.书写热化学方程式的注意事项
(1)热化学方程式中必须标明反应物和生成物的____________,固体(____)、液体(____)、气
体(____)、水溶液(____),若为同素异形体,还要注明名称。
(2)热化学方程式要注明反应时的温度和压强。如不注明,即表示在25 ℃和101 kPa下测定。
(3)热化学方程式中的化学计量数为____________。故化学计量数可以是________,也可以
是________。当化学计量数改变时,其ΔH也____________的改变。
(4)要注明ΔH的符号:“+”代表________、“-”代表________,以及单位:________。
3.燃烧热(1)燃烧热的概念及意义
(2)对完全燃烧的理解
元素 C H S N
指定产物
CO(g) HO(l) SO (g) N(g)
2 2 2 2
及状态
4.燃料的选择 能源
(1)燃料的选择原则
(2)能源分类
(3)能源利用
1.开发利用各种新能源,减少对化石燃料的依赖,可以降低空气中PM 的含量( )
2.5
2.CH(g)+2O(g)===CO(g)+2HO(g) ΔH=-890.3 kJ( )
4 2 2 2
3.根据2H(g)+O(g)===2HO(l) ΔH=-571.6 kJ·mol-1可知,氢气的燃烧热为571.6 kJ·
2 2 2
mol-1( )
4.对于SO (g)+O(g)SO (g) ΔH=-Q kJ·mol-1,增大压强平衡右移,放出的热量增
2 2 3
大,ΔH减小( )
5.已知N(g)+3H(g)===2NH (g) ΔH=-92 kJ·mol-1,则NH (g)===N(g)+H(g) ΔH=
2 2 3 3 2 2
+46 kJ·mol-1( )
一、能源 燃烧热概念的理解1.据某网报道,欧洲一集团公司拟在太空建立巨大的集光装置,把太阳光变成激光用于分
解海水制氢,其反应可表示为2HO=====2H↑+O↑。有下列几种说法:①水分解反应是
2 2 2
放热反应;②若用生成的氢气与空气中多余的二氧化碳反应生成甲醇储存起来,可改善生存
条件;③使用氢气作燃料有助于控制温室效应;④氢气是一级能源。其中叙述正确的是(
)
A.①② B.③④
C.②③ D.①②③④
2.油酸甘油酯(相对分子质量为884)在体内代谢时可发生如下反应:
C H O(s)+80O(g)===57CO(g)+52HO(l)
57 104 6 2 2 2
已知燃烧1 kg该化合物释放出3.8×104 kJ热量,油酸甘油酯的燃烧热为( )
A.3.8×104 kJ·mol-1
B.-3.8×104 kJ·mol-1
C.3.4×104 kJ·mol-1
D.-3.4×104 kJ·mol-1
二、热化学方程式的书写
3.依据事实,写出下列反应的热化学方程式。
(1)已知2.0 g燃料肼(N H)气体完全燃烧生成N 和水蒸气时,放出33.4 kJ的热量,则表示肼
2 4 2
燃烧的热化学方程式为___________________________________________________________
______________________________________________________________________________。
(2)CuCl(s)与O 反应生成CuCl (s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消
2 2
耗1 mol CuCl(s)放热44.4 kJ,该反应的热化学方程式是
________________________________________________________________________。
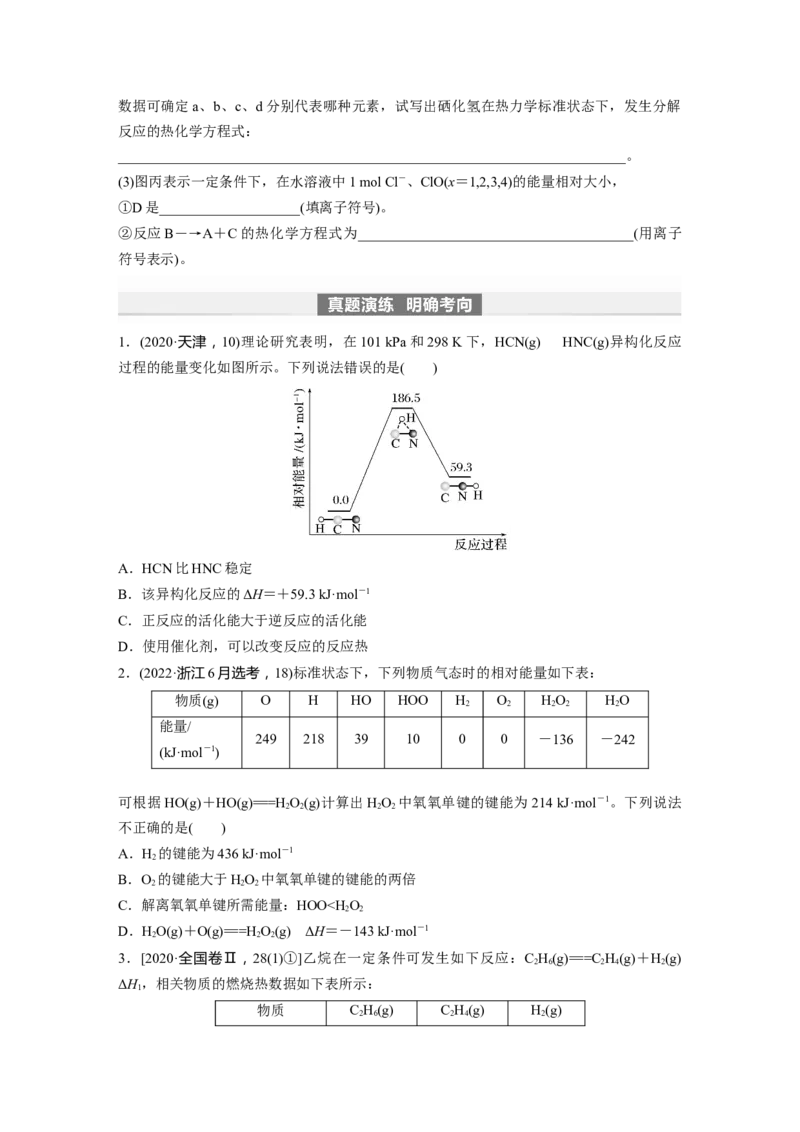
4.分析图像书写热化学方程式。
(1)图甲表示的是NO 和CO反应生成CO 和NO过程中能量变化示意图,请写出NO 和CO
2 2 2
反应的热化学方程式:__________________________________________________________。
(2)图乙表示氧族元素中的氧、硫、硒、碲在生成1 mol气态氢化物时的焓变数据,根据焓变数据可确定a、b、c、d分别代表哪种元素,试写出硒化氢在热力学标准状态下,发生分解
反应的热化学方程式:
________________________________________________________________________。
(3)图丙表示一定条件下,在水溶液中1 mol Cl-、ClO(x=1,2,3,4)的能量相对大小,
①D是____________________(填离子符号)。
②反应B―→A+C的热化学方程式为_______________________________________(用离子
符号表示)。
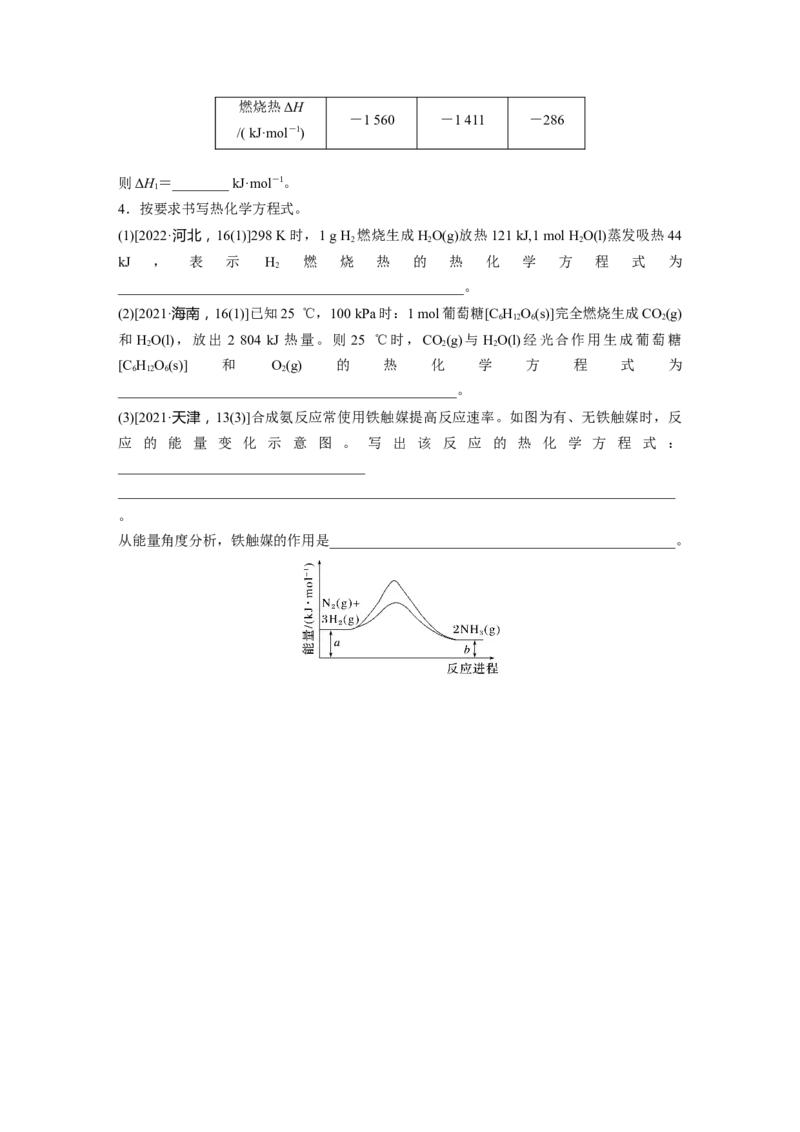
1.(2020·天津,10)理论研究表明,在101 kPa和298 K下,HCN(g)HNC(g)异构化反应
过程的能量变化如图所示。下列说法错误的是( )
A.HCN比HNC稳定
B.该异构化反应的ΔH=+59.3 kJ·mol-1
C.正反应的活化能大于逆反应的活化能
D.使用催化剂,可以改变反应的反应热
2.(2022·浙江6月选考,18)标准状态下,下列物质气态时的相对能量如下表:
物质(g) O H HO HOO H O HO HO
2 2 2 2 2
能量/
249 218 39 10 0 0 -136 -242
(kJ·mol-1)
可根据HO(g)+HO(g)===HO(g)计算出HO 中氧氧单键的键能为214 kJ·mol-1。下列说法
2 2 2 2
不正确的是( )
A.H 的键能为436 kJ·mol-1
2
B.O 的键能大于HO 中氧氧单键的键能的两倍
2 2 2
C.解离氧氧单键所需能量:HOO