文档内容
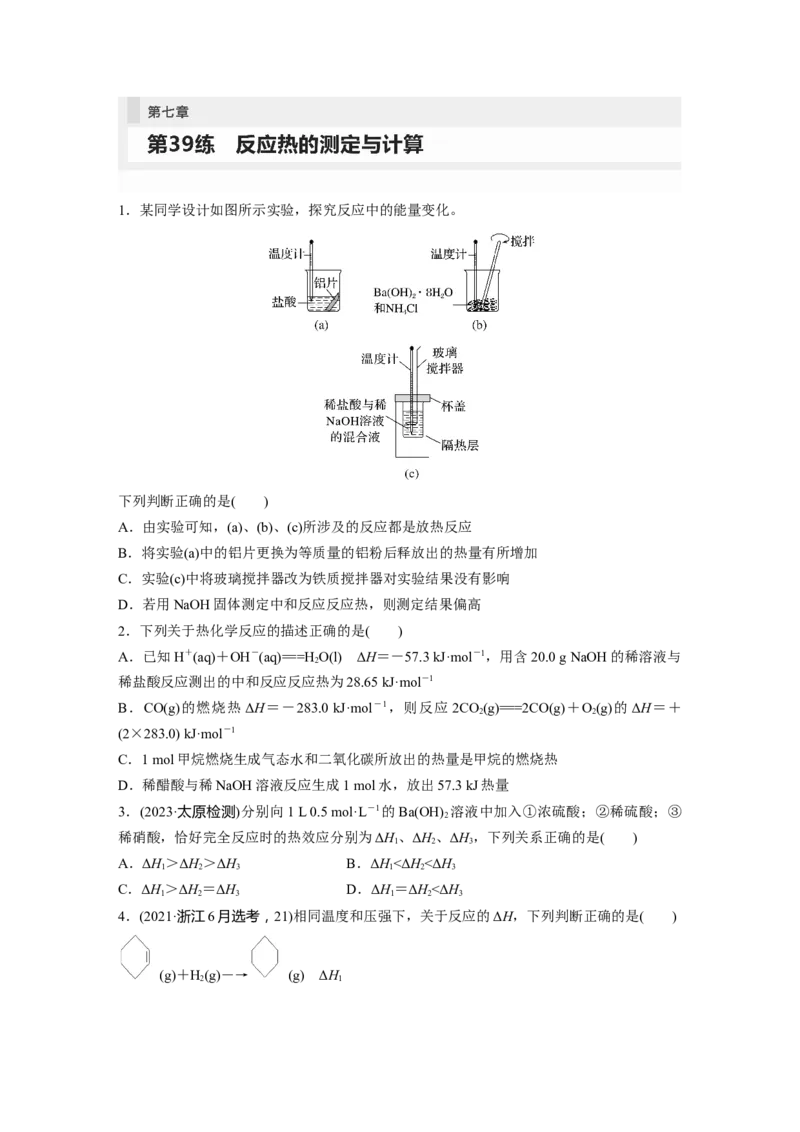
1.某同学设计如图所示实验,探究反应中的能量变化。
下列判断正确的是( )
A.由实验可知,(a)、(b)、(c)所涉及的反应都是放热反应
B.将实验(a)中的铝片更换为等质量的铝粉后释放出的热量有所增加
C.实验(c)中将玻璃搅拌器改为铁质搅拌器对实验结果没有影响
D.若用NaOH固体测定中和反应反应热,则测定结果偏高
2.下列关于热化学反应的描述正确的是( )
A.已知H+(aq)+OH-(aq)===HO(l) ΔH=-57.3 kJ·mol-1,用含20.0 g NaOH的稀溶液与
2
稀盐酸反应测出的中和反应反应热为28.65 kJ·mol-1
B.CO(g)的燃烧热 ΔH=-283.0 kJ·mol-1,则反应 2CO(g)===2CO(g)+O(g)的ΔH=+
2 2
(2×283.0) kJ·mol-1
C.1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量
3.(2023·太原检测)分别向1 L 0.5 mol·L-1的Ba(OH) 溶液中加入①浓硫酸;②稀硫酸;③
2
稀硝酸,恰好完全反应时的热效应分别为ΔH、ΔH、ΔH,下列关系正确的是( )
1 2 3
A.ΔH>ΔH>ΔH B.ΔH<ΔH<ΔH
1 2 3 1 2 3
C.ΔH>ΔH=ΔH D.ΔH=ΔH<ΔH
1 2 3 1 2 3
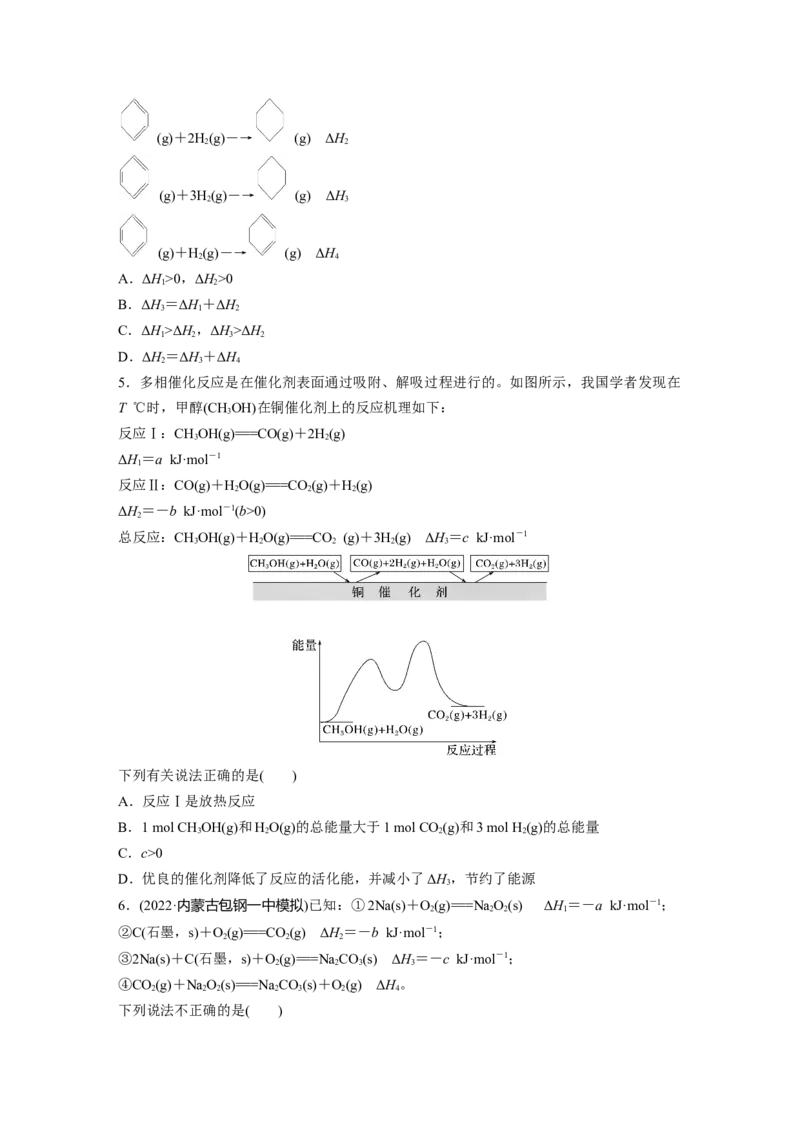
4.(2021·浙江6月选考,21)相同温度和压强下,关于反应的ΔH,下列判断正确的是( )
(g)+H(g)―→ (g) ΔH
2 1(g)+2H(g)―→ (g) ΔH
2 2
(g)+3H(g)―→ (g) ΔH
2 3
(g)+H(g)―→ (g) ΔH
2 4
A.ΔH>0,ΔH>0
1 2
B.ΔH=ΔH+ΔH
3 1 2
C.ΔH>ΔH,ΔH>ΔH
1 2 3 2
D.ΔH=ΔH+ΔH
2 3 4
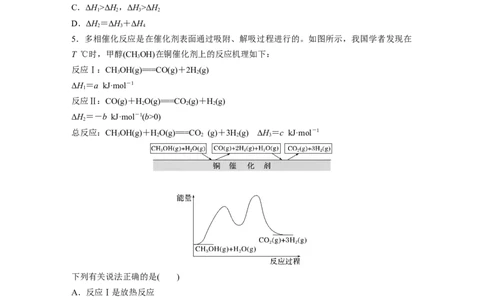
5.多相催化反应是在催化剂表面通过吸附、解吸过程进行的。如图所示,我国学者发现在
T ℃时,甲醇(CHOH)在铜催化剂上的反应机理如下:
3
反应Ⅰ:CHOH(g)===CO(g)+2H(g)
3 2
ΔH=a kJ·mol-1
1
反应Ⅱ:CO(g)+HO(g)===CO(g)+H(g)
2 2 2
ΔH=-b kJ·mol-1(b>0)
2
总反应:CHOH(g)+HO(g)===CO (g)+3H(g) ΔH=c kJ·mol-1
3 2 2 2 3
下列有关说法正确的是( )
A.反应Ⅰ是放热反应
B.1 mol CH OH(g)和HO(g)的总能量大于1 mol CO (g)和3 mol H (g)的总能量
3 2 2 2
C.c>0
D.优良的催化剂降低了反应的活化能,并减小了ΔH,节约了能源
3
6.(2022·内蒙古包钢一中模拟)已知:①2Na(s)+O(g)===NaO(s) ΔH=-a kJ·mol-1;
2 2 2 1
②C(石墨,s)+O(g)===CO(g) ΔH=-b kJ·mol-1;
2 2 2
③2Na(s)+C(石墨,s)+O(g)===NaCO(s) ΔH=-c kJ·mol-1;
2 2 3 3
④CO(g)+NaO(s)===NaCO(s)+O(g) ΔH。
2 2 2 2 3 2 4
下列说法不正确的是( )A.石墨的燃烧热ΔH=-b kJ·mol-1
B.C(石墨,s)+O(g)===CO(g) ΔH>-b kJ·mol-1
2
C.反应④中,ΔH=(c-a-b) kJ·mol-1
4
D.若将反应①设计成原电池,则32 g O 在正极反应转移2 mol电子
2
7.Li/Li O体系的能量循环如图所示。下列说法正确的是( )
2
A.ΔH<0
3
B.ΔH+ΔH+ΔH=ΔH
3 4 5 6
C.ΔH>ΔH
6 5
D.ΔH+ΔH+ΔH+ΔH+ΔH+ΔH=0
1 2 3 4 5 6
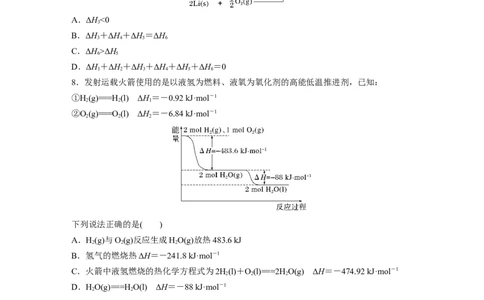
8.发射运载火箭使用的是以液氢为燃料、液氧为氧化剂的高能低温推进剂,已知:
①H(g)===H(l) ΔH=-0.92 kJ·mol-1
2 2 1
②O(g)===O(l) ΔH=-6.84 kJ·mol-1
2 2 2
下列说法正确的是( )
A.H(g)与O(g)反应生成HO(g)放热483.6 kJ
2 2 2
B.氢气的燃烧热ΔH=-241.8 kJ·mol-1
C.火箭中液氢燃烧的热化学方程式为2H(l)+O(l)===2HO(g) ΔH=-474.92 kJ·mol-1
2 2 2
D.HO(g)===HO(l) ΔH=-88 kJ·mol-1
2 2
9.下列示意图表示正确的是( )A.甲图表示反应CH(g)+HO(g)===CO(g)+3H(g) ΔH=+205.9 kJ·mo1-1的能量变化
4 2 2
B.乙图表示碳的燃烧热
C.丙图表示实验的环境温度为 20 ℃,将物质的量浓度相等、体积分别为 V 、V 的
1 2
HSO 、NaOH溶液混合,混合液的最高温度随V的变化(已知V+V=60 mL)
2 4 1 2
D.已知稳定性顺序:B